i HALAMAN JUDUL
MODIFIKASI ADSORBEN DARI ABU VULKANIK GUNUNG KELUD DENGAN HNO3 DAN UJI ADSORPTIVITASNYA TERHADAP
ION LOGAM Ni(II) DAN Zn(II) DALAM LIMBAH CAIR INDUSTRI ELEKTROPLATING
TUGAS AKHIR SKRIPSI
Diajukan kepada Fakultas Matematika dan Ilmu Pengetahuan Alam Universitas Negeri Yogyakarta untuk Memenuhi Sebagian Persyaratan guna Memperoleh
Gelar Sarjana Sains
Oleh :
Nurul Islam Miyati NIM 13307144002
PROGRAM STUDI KIMIA
FAKULTAS MATEMATIKA DAN ILMU PENGETAHUAN ALAM UNIVERSITAS NEGERI YOGYAKARTA
ii
MODIFIKASI ADSORBEN DARI ABU VULKANIK GUNUNG KELUD DENGAN HNO3 DAN UJI ADSORPTIVITASNYA TERHADAP
ION LOGAM Ni(II) DAN Zn(II) DALAM LIMBAH CAIR INDUSTRI ELEKTROPLATING
Oleh:
Nurul Islam Miyati NIM 13307144002
ABSTRAK
Tujuan penelitian ini adalah mengetahui karakter gugus fungsi, porositas, kadar air dan keasaman adsorben, daya adsorpsi dan efisiensi adsorpsi adsorben terhadap ion logam Ni(II) dan Zn(II) dalam limbah cair industri elektroplating, serta pH optimum adsorpsi.
Subjek penelitian ini adalah abu vulkanik gunung kelud. Objek penelitian ini adalah karakter adsorben hasil sintesis meliputi gugus fungsi, porositas, keasaman dan kadar air adsorben, serta efisiensi dan daya adsorpsi adsorben. Metode pembuatan adsorben adalah metode sol gel. Asam yang digunakan pada sintesis adsorben adalah asam nitrat 3M. Kondisi pH pada pengujian efisiensi dan daya adsorpsi yaitu 1, 2, 4, 6, dan 8, dengan jenis ion logam yang diadsorpsi yaitu ion logam Ni(II) dan Zn(II) dalam limbah cair industri elektroplating.
Hasil penelitian menunjukkan bahwa efisiensi produksi adsorben sebanyak 63,73%. Karakter spektra FTIR adsorben hasil sintesis memiliki kemiripan dengan kiesel gel 60G. Karakter porositas menunjukkan adsorben hasil sintesis memiliki luas permukaan 144,744 m2/g, volume total pori 0,771 cm3/g dan jari-jari ukuran pori 106,54 Å. Nilai keasaman adsorben hasil sintesis adalah 5,6859 mmol/gram dan kadar air adalah 9%. Kondisi pH optimum dalam pengujian adsorpsi adalah pH 6 dengan daya adsorpsi terhadap ion logam Ni(II) dan Zn(II) secara berurutan adalah 1,44462 mg/g dan 0,01509 mg/g, sedangkan efisiensi adsorpsi secara berurutan adalah 57,98% dan 2,73%.
iii
MODIFICATION OF ADSORBENT FROM KELUD VOLCANIC ASH USING HNO3 FOR ADSORPTION OF NICKEL(II) AND ZINC(II)
METAL IONS IN THE ELECTROPLATING WASTE
Author:
Nurul Islam Miyati NIM 13307144002
ABSTRACT
The goal of the research is to find out the functional group, the porosity, the acidity, the water content of synthesized adsorbent, the adsorption capacity, the efficiency of adsorption, and optimum pH of adsorption synthesized adsorbent on Ni(II) and Zn(II) metal ions from the electroplating wastewater.
The subject was Kelud volcanic ash. The object was the charateristic of synthesized adsorbent include the functional group in the chemical structure, the porosity, the acidity, and the water content. Furthermore, the object is to investigate the efficiency and the capacity of synthesized adsorbent in the removal of Ni(II) and Zn(II) metal ions from the electroplating wastewater. The method that used in the research was sol gel method. The acid that used for the synthesis of adsorbent was nitrate acid with 3M concentration. The effect of pH on Ni and Zn metal ions sorption were studied by varying the pH from 1, 2, 4, 6, and 8.
The result showed that the production efficiency of synthesized adsorbent was 63.73%. Based on the FTIR spectra data that showing a similar pattern to kiesel gel 60G produced by Merck. The characteristic of porosity showed that synthesized adsorbent has the surface area was 144.744 m2/g, the pore volume
was 0.771 cm3/g and the radius size pore was 106.54 Å. The acidity of synthesized adsorbent was 5.6859 mmol/gram. The water content was 9%. The optimum pH of adsorption of Ni(II) and Zn(II) was obtained at pH 6 with adsorption capacity of Ni(II) and Zn(II) ions were 1.44462 mg/g and 0.01509 mg/g respectively. The adsorption efficiency of Ni(II) and Zn(II) ions were 57.98% and 2.73% respectively.
iv
v
vi
vii
MOTTO
“...Sesungguhnya Allah tidak akan mengubah keadaan suatu kaum sebelum mereka mengubah keadaan diri mereka sendiri...” (QS. Ar-Ra‟du : 11)
“Bersemangatlah atas hal-hal yang bermanfaat bagimu. Minta tolonglah pada
Allah, jangan engkau lemah.” (HR. Muslim)
“Jika kamu tidak kuat menanggung lelahnya belajar, maka kamu akan menanggung perihnya kebodohan.” (Imam Syafi‟i)
“Bila kita bertemu dengan rintangan, Hadapi semua sebagai tantangan, Bila kita berjumpa dengan himpitan, Yakinlah Allah akan hadirkan kelapangan, Dan bila kita bersua dengan kesulitan, Niscaya Allah sudah siapkan kemudahan,
Pantang mengaku kalah meski harus berteman lelah, Pantang mengeluh meski harus berkawan peluh, Pantang mundur meski semangat mulai mengendur,
Pantang putus asa meski tubuh seakan tak kuasa,
Pantanglah menyerah hingga akhir usia.”
viii
HALAMAN PERSEMBAHAN
Alhamdulillahi rabbil „alamin. Segala puji hanya bagi Allah yang Maha
Menghukumi segala sesuatunya, Maha Berkehendak atas segala yang Dia kehendaki, tiada cela atas ketetapanNya, Dialah Allah Yang Maha Berkuasa atas hamba-hambaNya.
Karya kecil ini penulis persembahkan teruntuk:
1. Ayah dan Ibu, yang tiada henti mendoakan, mendukung dan meridhoi langkah ini.
2. Kakak terkasih, yang senantiasa membimbing dan mengingatkan agar selalu melibatkan Allah dalam perjuangan ini, karena Dialah sebenar-benarnya Eksekutor, atas ikhtiar dan doa hamba-hambaNya.
3. Ummu Sulayman, sang murabbi, dan akhwat-akhwat halaqah tarbiyah (Mbak Isti, Mbak Dede, Mbak Puji, Mbak Putu, Mbak Fitri, Mbak Ira, Mbak April, Mbak Lina, Mbak Munika, Hukma, dan Eni), jazakunnallahu khayr atas semangat dan nasihatnya.
4. Teman seperjuangan, calon bidadari Surga insyaaAllah (Asiah, Eka, Fifi, Fitri) jazakunnallahu khayr sudah banyak membantu, menemani dan menghibur selama perjalanan pencapaian ini.
5. Teman-teman Kimia E 2013, terimakasih atas dukungan, saran dan bantuannya.
ix
KATA PENGANTAR
Segala puji hanya bagi Allah atas segala Rahmat dan Karunia-Nya sehingga penyusun dapat menyelesaikan laporan Tugas Akhir Skripsi ini. Penyusunan laporan ini dapat diselesaikan berkat bantuan, bimbingan dan pengarahan dari berbagai pihak, maka dari itu pada kesempatan ini penyusun menyampaikan terima kasih kepada:
1. Bapak Dr. Hartono selaku Dekan Fakultas Matematika dan Ilmu Pengetahuan Alam Universitas Negeri Yogyakarta.
2. Bapak Drs. Jaslin Ikhsan, M.App.Sc., Ph.D selaku Ketua Jurdik Pendidikan Kimia dan Ketua Prodi Kimia Fakultas Matematika dan Ilmu Pengetahuan Alam Universitas Negeri Yogyakarta.
3. Bapak Crys Fajar Partana, M.Si. selaku Dosen Penasehat Akademik. 4. Ibu Susila Kristianingrum, M.Si selaku Dosen Pembimbing Utama
Tugas Akhir Skripsi.
5. Ibu Dra. Regina Tutik Padmaningrum, M.Si selaku Penguji Utama Sidang Tugas Akhir Skripsi.
6. Ibu Sulistyani, M.Si selaku Penguji Pendamping Sidang Tugas Akhir Skripsi.
7. Seluruh pihak yang tidak dapat penyusun sebutkan satu persatu yang telah membantu dalam penyusunan Laporan Tugas Akhir Skripsi ini. Penyusun menyadari terdapat banyak kekurangan baik dalam pelaksanaan maupun penyusunan laporan ini. Oleh karena itu, penyusun mengucapkan terimakasih kepada semua pihak yang telah membantu dan mendukung dalam menyusun laporan ini. Laporan ini diharapkan bermanfaat dan dapat menjadi referensi bagi para mahasiswa.
Yogyakarta, 26 Mei 2017 Penyusun,
x
DAFTAR ISI
HALAMAN
HALAMAN JUDUL ... i
ABSTRAK ... ii
SURAT PERNYATAAN ... iii
LEMBAR PERSETUJUAN ... iv
HALAMAN PENGESAHAN ... v
MOTTO ... vii
HALAMAN PERSEMBAHAN ... viii
KATA PENGANTAR ... ix
DAFTAR ISI ... x
DAFTAR TABEL ... xiii
DAFTAR GAMBAR ... xv
DAFTAR LAMPIRAN ... xvii
BAB I PENDAHULUAN ... 1
A. Latar Belakang ... 1
B. Identifikasi Masalah ... 3
C. Pembatasan Masalah ... 4
D. Perumusan Masalah ... 4
E. Tujuan Penelitian ... 5
F. Manfaat Penelitian ... 5
BAB II KAJIAN PUSTAKA ... 7
A. Deskripsi Teori ... 7
xi
2. Metode Sol Gel ... 8
3. Adsorben Silika Gel ... 8
4. Adsorpsi ... 10
5. Limbah Elektroplating ... 12
6. Logam Zink ... 13
7. Logam Nikel ... 13
8. Spektrofotometer FTIR ... 14
9. Spektrofotometer Serapan Atom ... 17
10. Gas Surface Analyzer ... 18
B. Penelitian Yang Relevan ... 22
C. Kerangka Berfikir ... 24
BAB III METODE PENELITIAN ... 26
A. Subjek dan Objek Penelitian ... 26
B. Teknik Pengambilan Sampel ... 26
C. Variabel Penelitian ... 26
D. Alat dan Bahan ... 27
E. Prosedur Penelitian ... 28
F. Teknik Analisis Data ... 31
BAB IV HASIL DAN PEMBAHASAN ... 33
A. Hasil Penelitian ... 33
B. Pembahasan ... 39
BAB V KESIMPULAN DAN SARAN ... 65
xii
B. Saran ... 65
xiii
DAFTAR TABEL
HALAMAN
Tabel 1. Kandungan Abu Vulkanik gunung kelud... 7
Tabel 2. Klasifikasi Lunak-Keras Asam-Basa Lewis ... 12
Tabel 3. Sifat Kimia Logam Zn ... 13
Tabel 4. Sifat Kimia Logam Ni ... 14
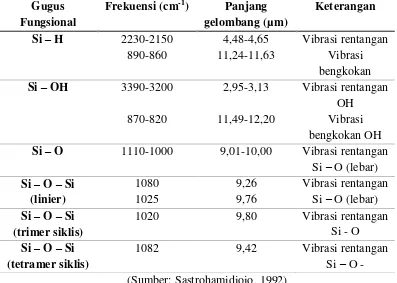
Tabel 5. Korelasi Inframerah Gugus Fungsional Senyawa Organo-Silikon ... 15
Tabel 6. Kondisi Analisis Unsur Ni dan Zn ... 18
Tabel 7. Data Keasaman dan Kadar Air Adsorben Hasil Sintesis dan Kiesel Gel 60G ... 33
Tabel 8. Interpretasi Spektra Kiesel gel 60G dan Adsorben Hasil Sintesis (ADHNO3) ... 34
Tabel 9. Porositas Adsorben Hasil Sintesis ... 35
Tabel 10. Interpretasi Spektra Adsorben Hasil Sintesis (ADHNO3) Sebelum dan Sesudah Adsorpsi pada pH optimum... 36
Tabel 11. Data Efisiensi dan Daya Adsorpsi Ion Logam Ni(II) dalam Limbah Cair Industri Elektroplating oleh Adsorben Hasil Sintesis dan kiesel Gel 60 G ... 37
Tabel 12. Data Efisiensi dan Daya Adsorpsi Ion Logam Zn(II) dalam Limbah Cair Industri Elektroplating oleh Adasorben Hasil Sintesis dan kiesel Gel 60 G ... 38
Tabel 13. Interpretasi FTIR Abu Sebelum dan Sesudah dicuci dengan HCl 0,1 M ... 46
xiv
Tabel 15. Data konsentrasi (x) dan absorbansi (y) larutan standar Ni(II) ... 89
Tabel 16. Statistik penentuan persamaan garis regresi linear larutan standar
Ni(II) ... 90
Tabel 17. Data konsentrasi (x) dan absorbansi (y) larutan standar Zn(II) ... 92
Tabel 18. Statistik penentuan persamaan garis regresi linear larutan standar
Zn(II) ... 93
Tabel 19. Daftar r nilai koefisien korelasi ... 96
xv
DAFTAR GAMBAR
HALAMAN
Gambar 1. Skema Kerja Alat Spektrofotometer FTIR ... 16
Gambar 2. Proses Serapan Atom ... 17
Gambar 3. Contoh Data Grafik yang dihasilkan dari Analisa GSA ... 20
Gambar 4. Spektra FTIR Kiesel Gel 60G dan Adsorben Hasil Sintesis (ADHNO3)... 34
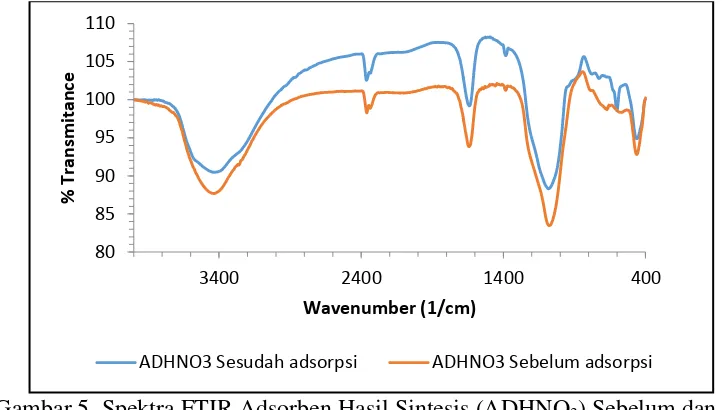
Gambar 5. Spektra FTIR Adsorben Hasil Sintesis (ADHNO3) Sebelum dan Sesudah Adsorpsi ... 35
Gambar 6. Kurva Standar Larutan Ni(II) ... 36
Gambar 7. Kurva Standar Larutan Zn(II) ... 37
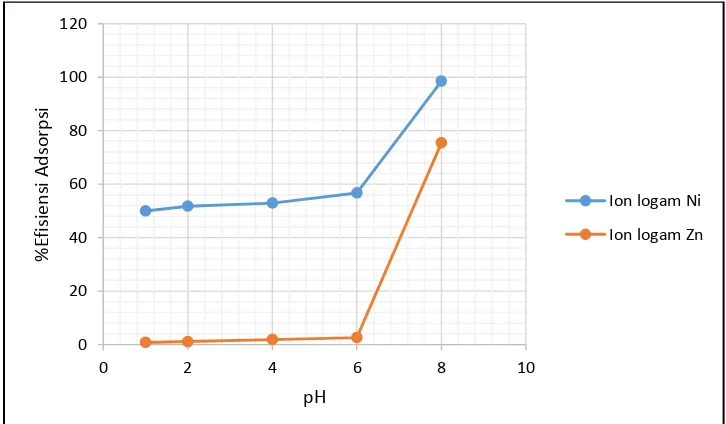
Gambar 8. Kurva % Efisiensi Adsorpsi Ion Logam Ni(II) dan Zn(II) oleh Adsorben kiesel gel 60G pada berbagai pH ... 38
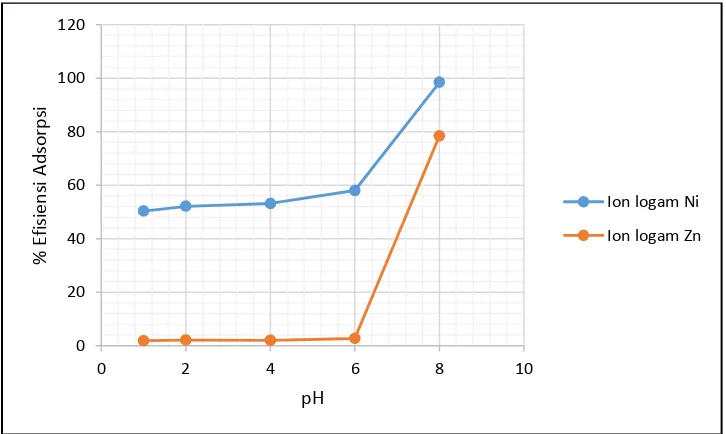
Gambar 9. Kurva % Efisiensi Adsorpsi Ion Logam Ni(II) dan Zn(II) oleh Adsorben Hasil Sintesis dengan HNO3 (ADHNO3) pada berbagai pH ... 39
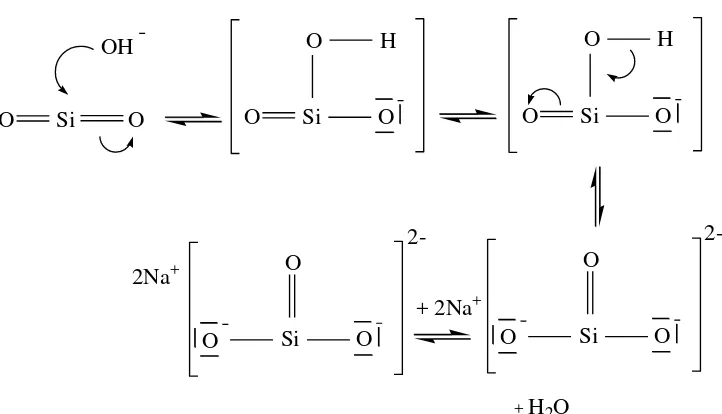
Gambar 10. Model Mekanisme Reaksi Pembentukan Natrium Silikat ... 41
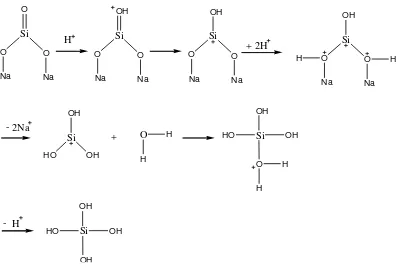
Gambar 11. Mekanisme Reaksi Pembentukan Monomer Asam Silikat ... 43
Gambar 12. Mekanisme Pembentukan Gel. ... 43
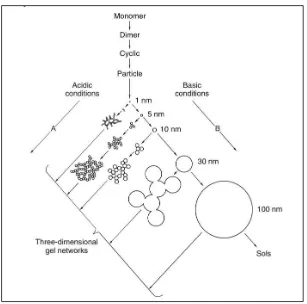
Gambar 13. Proses Pembentukan Alkogel (Brinker & Scherer, 1990: 102) ... 44
Gambar 14. Spektra FTIR Abu Vulkanik gunung kelud Sebelum dan Sesudah dicuci dengan HCl 0,1 M ... 45
Gambar 15. Reaksi Adsorben Hasil Sintesis dengan Basa NaOH ... 48
xvi
Gambar 17. Reaksi Pelepasan Air pada Silika Gel ... 51
Gambar 18. Pengikatan Ion Hidrogen oleh Gugus Fungsi pada Permukaan Adsorben ... 56
Gambar 19. Distribusi Spesies Ion Logam Ni(II) ... 57
Gambar 20. Distribusi Spesies Ion Logam Zn(II) ... 57
Gambar 21. Reaksi antara Gugus Silanol pada Permukaan Adsorben dan Ion Logam dalam Larutan dengan pH Asam ... 58
Gambar 22. Reaksi antara Gugus Siloksan pada Permukaan Adsorben dan Ion Logam dalam Larutan dengan pH Asam ... 58
Gambar 23. Pemutusan Proton pada Permukaan Silanol ... 59
Gambar 24. Reaksi antara Gugus Fungsi Silanol pada Permukaan Adsorben dengan Ion Logam pada pH 4-6 ... 60
Gambar 25. Reaksi antara Gugus Fungsi Siloksan pada Permukaan Adsorben dengan Ion Logam pada pH 4-6 ... 60
Gambar 26. Radius skematis ion yang terhidrasi dengan medan elektrostatis (a) tinggi (b) rendah ... 62
Gambar 28. Kurva Standar Larutan Ni(II) ... 89
Gambar 29. Kurva Standar Larutan Zn(II) ... 93
Gambar 30. Spektra FTIR Abu kelud ... 116
Gambar 31. Spektra FTIR Adsorben hasil sintesis ... 116
Gambar 32. Spektra FTIR Kiesel gel 60G ... 117
xvii
DAFTAR LAMPIRAN
HALAMAN
Lampiran 1. Perhitungan Efisiensi Produktivitas Silika Gel Hasil Sintesis ... 73
Lampiran 2. Pembuatan Larutan Asam Nitrat dengan Konsentrasi 3 M ... 74
Lampiran 3. Standarisasi Larutan NaOH 0,1 M dan HCl 0,1 M ... 75
Lampiran 4. Penentuan Keasaman Adsorben ... 79
Lampiran 5. Data Perhitungan Keasaman Adsorben ... 81
Lampiran 6. Penentuan Kadar Air Adsorben ... 82
Lampiran 7. Data Perhitungan Kadar Air Adsorben ... 85
Lampiran 8. Pembuatan larutan induk Ni(II) 1000 ppm dan larutan standar Ni(II) berbagai konsentrasi ... 86
Lampiran 9. Pembuatan larutan induk Zn(II) 1000 ppm dan larutan standar Zn(II) berbagai konsentrasi ... 87
Lampiran 10. Kondisi analisis ion logam dengan Spektrofotometer Serapan Atom ... 88
Lampiran 11. Penentuan Persamaan Garis Regresi Linear larutan Standar Ni(II) dan Zn(II)... 89
Lampiran 12. Penentuan Daya Adsorpsi dan Efisiensi Adsorpsi Ion Logam Ni(II) dan Zn(II) dalam Limbah Cair Industri Elektroplating oleh Adsorben Hasil Sintesis ... 98
xviii
Lampiran 14. Data Perhitungan Efisiensi Adsorpsi Ion Logam Zn(II) dalam
Limbah Cair Industri Elektroplating ... 105
Lampiran 15. Data hasil AAS Ion Logam Ni(II) dan Zn(II)... 106
Lampiran 16. Diagram Kerja ... 108
1
BAB I PENDAHULUAN
A. Latar Belakang
Limbah industri elektroplating merupakan limbah yang dihasilkan dari
proses pelapisan padatan dengan logam menggunakan arus listrik melalui larutan
elektrolit. Limbah cair elektroplating mengandung logam-logam berat, seperti
Ni(II) dan Zn(II) (Marwati, Padmaningrum & Marfuatun, 2007: 1). Kadar Ni(II)
dalam limbah elektroplating relatif cukup besar dibanding dengan logam-logam
berat lainnya, yaitu 25,955 ppm, sedangkan kadar Zn(II) sebesar 20,982 ppm
(Padmaningrum & Marwati, 2008: 87). Pada Keputusan Menteri Negara
Lingkungan Hidup No.KEP-51/MENLH/10/1995 tentang baku mutu limbah cair
bagi kegiatan industri disebutkan bahwa batas maksimum pencemaran logam
Ni(II) 1,0 mg/L dan logam Zn(II) 1,0 mg/L. Berdasarkan keputusan tersebut,
diketahui kadar Ni(II) dan Zn(II) dalam limbah cair elektroplating berada di atas
batas maksimum yang diperbolehkan.
Beberapa metode yang dapat digunakan untuk menangani limbah ion
logam berbahaya secara umum termasuk ion logam Ni(II) dan Zn(II) adalah
metode pengendapan, evaporasi, elektrokimia, dan adsorpsi (Lelifajri, 2010:
126). Metode adsorpsi merupakan salah satu metode yang paling sering
dilakukan untuk mengurangi jumlah logam beracun dalam air limbah (Priadi
dkk., 2014: 11). Adsorpsi merupakan proses fisika-kimiawi di mana adsorbat,
dalam hal ini zat pencemar, terakumulasi di permukaan padatan yang disebut
2
Adsorben adalah zat padat yang dapat menyerap komponen tertentu dari
suatu fase fluida. Adsorben memiliki struktur yang sangat berpori dengan luas
permukaan yang besar (Rahmayanti & MZ, 2013: 2). Berbagai jenis adsorben
karbon aktif telah berhasil dikembangkan dan terbukti mampu mengadsorpsi ion
logam berat, hanya saja tergolong mahal dan sulit untuk diproduksi (Nurdila,
Asri, & Suharyadi, 2015: 23).
Pemanfaatan adsorben silika gel yang relatif lebih murah dibanding
karbon aktif memiliki beberapa keunggulan, seperti stabil dalam kondisi asam,
non swelling, porositas tinggi, luas permukaan yang besar, dan tahan terhadap
temperatur tinggi (Buhani dkk., 2010: 83). Silika gel merupakan padatan organik
yang memiliki gugus aktif silanol (Si-OH) dan siloksan (Si-O-Si) pada
permukaannya. Adanya kedua gugus aktif ini, silika gel dapat digunakan untuk
adsorpsi (Kristianingrum, Siswani, & Fillaeli, 2011: 282).
Silika gel dapat dibuat dari bahan alam yang mengandung unsur silika,
seperti abu vulkanik hasil erupsi Kelud Februari 2014 silam. Berdasarkan
penelitian yang dilakukan oleh Bambang (2014), abu vulkanik yang dihasilkan
dari letusan gunung Kelud tersebut, mengandung unsur silika sebesar 70,6%.
Penelitian mengenai pemanfaatan abu vulkanik hasil erupsi Kelud pada
Februari 2014 dalam pembuatan adsorben silika gel telah dilakukan oleh
Melantika (2014). Pada penelitian ini telah berhasil dilakukan sintesis silika gel
dengan asam nitrat pada variasi konsentrasi asam 1, 2 dan 3 M menggunakan
metode sol gel dengan natrium silikat sebagai prekursornya. Hasil penelitian
3
silika gel berpengaruh pada jumlah silika gel yang dihasilkan dan efisiensi
adsorpsi terhadap ion logam. Semakin tinggi konsentrasi asam, maka semakin
banyak jumlah silika gel yang dihasilkan dan semakin meningkat harga efisiensi
adsorpsi terhadap ion logam.
Jumlah ion logam yang diserap oleh adsorben dipengaruhi oleh beberapa
faktor, seperti pH medium, konsentrasi substrat, kekuatan ion, dan pembentukan
kompleks ion (Ikhsan, Johnson, & Wells, 1999: 403). Menurut penelitian Buhani
(2009: 309), efektivitas adsorben untuk berikatan dengan logam sangat
ditentukan oleh interaksi kimia pembentukan kompleks antara ligan pada
permukaan adsorben dan ion logam. Interaksi kimia yang terjadi dipengaruhi
oleh kondisi asam-basa pada interaksi ion logam dan ligan yang terdapat pada
permukaan adsorben (Buhani dkk., 2009: 302)
Pada penelitian ini, dipelajari pengaruh pH interaksi ion logam Ni(II) dan
Zn(II) dalam limbah cair industri elektroplating pada adsorben silika gel yang
diperoleh dari sintesis silika gel dari abu Kelud melalui metode sol gel
menggunakan asam nitrat 3 M.
B. Identifikasi Masalah
Berdasarkan latar belakang masalah yang diuraikan dapat diidentifikasi
beberapa permasalahan sebagai berikut:
1. Metode yang digunakan untuk sintesis adsorben silika gel bervariasi.
2. Jenis asam yang digunakan untuk sintesis adsorben silika gel mempengaruhi
hasil sintesis.
4
4. Jenis ion logam yang diadsorpsi oleh adsorben silika gel bervariasi.
5. pH lingkungan mempengaruhi daya adsorpsi adsorben hasil sintesis terhadap
ion logam.
C. Pembatasan Masalah
Berdasarkan identifikasi masalah di atas, maka dalam penelitian ini
diberikan beberapa pembatasan masalah sebagai berikut:
1. Metode yang digunakan dalam sintesis adsorben silika gel adalah metode sol
gel.
2. Jenis asam yang digunakan dalam sintesis adsorben silika gel adalah asam
nitrat.
3. Konsentrasi asam nitrat dalam sintesis adsorben silika gel adalah 3 M.
4. Jenis ion logam yang diadsorpsi adalah logam Ni(II) dan Zn(II) dalam
cuplikan limbah cair industri elektroplating.
5. pH lingkungan dalam adsorpsi adsorben hasil sintesis terhadap ion logam
adalah 1, 2, 4, 6 dan 8.
D. Perumusan Masalah
Berdasarkan hasil identifikasi masalah dan pembatasan masalah di atas,
maka dapat dirumuskan permasalahan sebagai berikut:
1. Bagaimana karakter gugus fungsi, porositas, keasaman dan kadar air adsorben
hasil sintesis dari abu vulkanik gunung kelud?
2. Berapa daya adsorpsi dan efisiensi adsorpsi paling optimum adsorben hasil
sintesis terhadap ion logam Ni(II) dan Zn(II) dalam cuplikan limbah cair
5
3. Berapa pH optimum dalam uji daya adsorpsi adsorben hasil sintesis terhadap
ion logam Ni(II) dan Zn(II) dalam limbah cair industri elektroplating?
E. Tujuan Penelitian
Adapun tujuan dari penelitian ini adalah
1. Mengetahui karakter gugus fungsi, porositas, keasaman dan kadar air
adsorben hasil sintesis dari abu vulkanik gunung kelud.
2. Mengetahui daya adsorpsi dan efisiensi adsorpsi paling optimum adsorben
hasil sintesis terhadap ion logam Ni(II) dan Zn(II) dalam cuplikan limbah cair
industri elektroplating.
3. Mengetahui pH optimum dalam uji daya adsorpsi adsorben hasil sintesis
terhadap ion logam Ni(II) dan Zn(II) dalam limbah cair industri
elektroplating.
F. Manfaat Penelitian
1. Bagi perkembangan ilmu pengetahuan
Dapat dijadikan sebagai bahan pustaka dalam pengembangan metode
sintesis adsorben silika gel dari bahan baku murah dan mudah diperoleh sebagai
upaya penanganan limbah.
2. Bagi praktisi
Dapat dijadikan sebagai solusi untuk meminimalisir dampak buruk dari
kandungan logam berat berbahaya di dalam limbah cair elektroplating.
6
Dapat menambah pengetahuan dan wawasan, serta dijadikan sebagai
sarana untuk mengaplikasikan ilmu baik teori maupun praktik selama
7
BAB II
KAJIAN PUSTAKA
A. Deskripsi Teori
1. Deskripsi Abu Vulkanik gunung Kelud
Abu vulkanik merupakan bahan material vulkanik jatuhan yang
disemburkan ke udara pada saat terjadi letusan (Sinaga, Sembiring, & Lubis,
2015: 1160). Letusan tersebut terdiri dari batuan berukuran besar sampai
berukuran halus. Batuan yang berukuran besar akan jatuh disekitar kawah, dan
yang berukuran halus dapat jatuh pada jarak mencapai ratusan km dari kawah.
Hal tersebut terjadi karena adanya hembusan angin (Khalis, Dewi, &
Wisnumurti, 2016: 3).
Letusan Kelud yang terjadi pada 14 Februari 2014 berdampak sangat
luas. Sebaran abu vulkanik gunung kelud mencapai radius 200-300 km (Suntoro
dkk., 2014: 69). Berdasarkan hasil analisis XRF (X-Ray Fluorescence), diketahui
bahwa kandungan abu Kelud terdiri dari unsur-unsur seperti ditunjukkan dalam
Tabel 1.
Tabel 1. Kandungan Abu Vulkanik gunung kelud (Kasatriyanto, 2014)
Unsur Kadar (%)
Silika 70,60
Alumunium 9,00
Besi 5,70
Kalsium 5,00
Kalium 0,70
8
2. Metode Sol Gel
Metode sol gel merupakan proses pembentukan jaringan oksida dengan
reaksi polikondensasi yang dari molekul prekursor dalam medium air. Proses ini
meliputi transisi sistem dari fasa larutan sol menjadi fasa padat gel (Brinker &
Scherer, 1990 dalam Buhani dkk., 2012: 265). Melalui proses sol gel dapat
dilakukan pengontrolan untuk memperoleh hasil berupa bahan oksida anorganik
dengan sifat tertentu yang meliputi kekerasan, dan porositas sesuai yang
dikehendaki. Proses ini dapat dilakukan pada temperatur rendah (Brinker &
Scherer, 1990 dalam Nuryono & Narsito, 2005: 265).
Reaksi kimia yang terjadi dalam proses sol gel terdiri dari reaksi
hidrolisis dan kondensasi. Reaksi hidrolisis terjadi pada Na-silikat yang
ditambahkan asam menghasilkan asam silikat yang mengandung gugus silanol
( ) dengan reaksi berikut:
NaSiO3(aq) + 2H+(aq) + H2O(l) → Si(OH)4(aq) + 2Na+(aq)
Silanol yang terbentuk ( ) selanjutnya akan bereaksi dengan gugus
silanol dari monomer asam silikat lain membentuk siloksan ( )
dengan reaksi sebagai berikut:
Reaksi ini disebut dengan reaksi kondensasi. Reaksi kondensasi terjadi sebelum
reaksi hidrolisis selesai (Brinker & Scherer, 1990: 108).
3. Adsorben Silika Gel
Silika gel merupakan silika amorf yang terdiri dari globula-globula SiO4
9
kerangka tiga dimensi yang lebih besar (sekitar 1-25 . Rumus kimia silika
gel secara umum adalah SiO2.xH2O (Sriyanti dkk., 2005: 2). Silika gel memiliki
beberapa keunggulan, seperti stabil dalam kondisi asam, non swelling, porositas
tinggi, luas permukaan yang besar, dan tahan terhadap temperatur tinggi (Buhani
dkk., 2010: 83). Keunggulan dari silika gel ini menyebabkan silika gel banyak
digunakan sebagai adsorben.
Silika gel memiliki gugus silanol ( dan siloksan (
) yang merupakan gugus aktif pada permukaannya. Adanya kedua gugus ini
menyebabkan silika gel dapat digunakan untuk keperluan adsorpsi
(Kristianingrum, Siswani, & Fillaeli, 2011: 282). Silika gel dapat digunakan
untuk menyerap ion-ion logam. Atom O sebagai situs aktif pada permukaan
silika gel, berfungsi sebagai donor pasangan elektron, yang akan berinteraksi
dengan logam berat. Atom O mempunyai ukuran relatif kecil dan polarisabilitas
rendah atau bersifat basa keras (Atkins, 1990 dalam Mujiyanti, Nuryono, &
Kunarti, 2010: 151).
Sintesis silika gel dapat dilakukan dengan pencampuran antara natrium
silikat dan asam. Natrium silikat dibuat dengan cara ekstraksi SiO2 dengan
menggunakan NaOH (Rosmawati, Tjahjanto, & Prananto, 2013: 162). Adapun
reaksinya adalah sebagai berikut:
SiO2(s) + 2NaOH(aq) → Na2SiO3(aq) + H2O(l)
Pada SiO2, elektronegativitas atom O yang tinggi menyebabkan Si lebih
elektropositif dan terbentuk intermediet[SiO2OH]- yang tidak stabil. Lalu akan
10
hidrogen membentuk air. Dua ion Na+ akan menyeimbangkan muatan negatif
yang terbentuk dan berinteraksi dengan ion SiO32- sehingga terbentuk natrium
silikat (Na2SiO3) (Mujiyanti, Nuryono, & Kunarti, 2010: 156).
Natrium silikat yang terbentuk ditambah dengan asam maka akan
terbentuk asam silikat. Penambahan asam pada prekursor natrium silikat
menyebabkan terjadinya protonasi gugus siloksi (SiO-) menjadi silanol (SiOH).
Gugus silanol yang terbentuk kemudian diserang lanjut oleh gugus siloksi (SiO-)
dengan bantuan katalis asam membentuk ikatan siloksan ( ).
Reaksi ini akan menghasilkan alkogel yang akan mengalami sineresis apabila
didiamkan (aging) dan menjadi hidrogel. Hidrogel dicuci dan dipanaskan hingga
membentuk xerogel (Mujiyanti, Nuryono, & Kunarti, 2010: 157).
4. Adsorpsi
Molekul-molekul pada permukaan zat padat atau zat cair, mempunyai
gaya tarik ke arah dalam, karena tidak ada gaya-gaya lain yang mengimbangi.
Adanya gaya-gaya ini menyebabkan zat padat dan zat cair mempunyai gaya
adsorpsi (Sukardjo, 1997). Adsorpsi merupakan suatu fenomena fisik dimana
molekul-molekul fluida menyentuh dan melekat pada permukaan padatan.
Padatan yang berpori menyerap dan melepaskan suatu fluida disebut adsorben.
Molekul yang terserap disebut adsorbat (Jufrianto, Martin, & Nasruddin, 2014:
3). Jenis adsorpsi ada dua macam yaitu
a. Adsorpsi Fisik atau Fisisorpsi
Dalam fisisorpsi, terdapat antaraksi van der Walls antara adsorben
11
terlemah dengan energi sekitar 0,4 sampai 40 kJ/mol. Gaya ini biasanya tertutupi
oleh gaya kovalen yang lebih kuat di dalam molekul yang energinya sekitar 400
kJ/mol. Tidak seperti ikatan kovalen, yang bekerja pada jarak antar inti yang
dekat dan dihubungkan dengan tumpang tindih atau pengalihan elektron dan
mengakibatkan energi yang lebih tinggi, ikatan van der waals dapat bekerja pada
jarak yang tidak dapat menyebabkan pertumpangtindihan atau pengalihan
elektron, sehingga energinya lebih kecil (Companion, 1991).
b. Adsorpsi Kimia atau Kemisorpsi
Dalam kemisorpsi, partikel melekat pada permukaan dengan membentuk
ikatan kovalen (Atkins, 1999: 438). Gaya kovalen lebih kuat dibanding dengan
gaya van der waals. Ikatan kovalen bekerja pada jarak antarinti yang dekat dan
dihubungkan dengan tumpang tindih atau pengalihan elektron dan
mengakibatkan energi yang lebih tinggi (Companion, 1991). Adsorpsi
dikategorikan sebagai proses kimiawi jika energinya lebih dari 20,92 kJ/mol,
dan jika kurang dari itu dikategorikan sebagai adsorpsi fisik (Adamson, 1990
dalam Fahmiati, Nuryono, & Narsito, 2006: 55).
Dalam proses adsorpsi dapat digunakan prinsip asam-basa keras dan
lunak yang diusulkan oleh Pearson. Asam-basa keras merupakan asam-basa
yang tidak mempunyai elektron valensi atau yang elektron valensinya sukar
terpolarisasi. Sedangkan asam-basa lunak merupakan asam-basa yang
elektron-elektron valensinya mudah terpolarisasi atau dilepaskan. Pearson meramalkan
reaksi berbagai macam spesies, yaitu asam-asam keras memilih bersenyawa
12
basa-basa lunak (Sugiyarto dkk., 2013: 112-115). Klasifikasi asam-basa
beberapa senyawa dan ion menurut prinsip HSAB dari Pearson dapat dilihat
pada Tabel 2.
Tabel 2. Klasifikasi Lunak-Keras Asam-Basa Lewis (Sugiyarto dkk., 2013: 113)
Kelas Asam Basa
Elektroplating merupakan salah satu proses pelapisan bahan padat dengan
lapisan logam menggunakan arus listrik searah melalui suatu larutan elektrolit.
Pada proses elektroplating, larutan elektrolit yang digunakan diganti setiap dua
minggu untuk mempertahankan mutu dan kehalusan permukaan serta penampilan.
Hal ini menyebabkan limbah yang dihasilkan semakin banyak (Marwati,
Padmaningrum & Marfuatun, 2007: 1).
Limbah dari proses elektroplating merupakan limbah logam berat yang
termasuk dalam B3 (Bahan Beracun Berbahaya) (Nurhasni, Salimin, &
13
elektroplating antara lain Ag+, Hg22+, Pb2+, Hg2+, Bi3+, Cu2+, Co2+, Al3+, Cr3+,
Fe2+, Mn2+, Ni2+ dan Zn2+ (Padmaningrum & Marwati, 2008). Keberadaan ion-ion
logam tersebut menyebabkan tingkat toksisitas limbah cair elektroplating tinggi.
Karakteristik dan tingkat toksisitas dari air limbah elektroplating bervariasi
tergantung dari kondisi operasi dan proses pelapisan (Nurhasni dkk., 2013).
6. Logam Zink
Zink adalah logam yang memiliki warna biru keputihan dan berkilau.
Tekstur logam zink rapuh, namun pada temperatur 100 oC sampai 150 oC
teksturnya lunak. Logam zink merupakan penghantar panas dan listrik yang
baik. Pada umunya, zink digunakan untuk paduan dengan logam yang lain.
Sebagian besar zink digunakan dalam industri otomotif, elektronik dan
perangkat keras (Lide, 2002). Adapun sifat kimia logam Zn dapat dilihat pada
Tabel 3.
Tabel 3. Sifat Kimia Logam Zn (Cotton dan Wilkinson, 1972) Konfigurasi kulit terluar 3d10 4s2
Energi potensial 1 9,39 eV
2 17,89 eV 3 40,0 eV
Titik leleh 419 oC
Titik didih 907 oC
Eo untuk M2+ + 2e-→ M -0,762 V
Jari-jari 0,69 Å
Massa atom relatif 65,38 gram/mol
7. Logam Nikel
Nikel adalah logam yang memiliki warna putih keperakan dan
mengkilap. Teksturnya keras, mudah dibentuk, bersifat ferromagnetik, dan
14
logam besi-kobalt. Secara umum, logam nikel digunakan untuk membuat
stainless steel dan paduan logam yang tahan terhadap korosi (Lide, 2002).
Adapun sifat kimia logam Ni dapat dilihat pada Tabel 4.
Tabel 4. Sifat Kimia Logam Ni (Cotton dan Wilkinson, 1972) Konfigurasi kulit terluar 3d8 4s2
Energi potensial 1 7,63 eV
2 18,15 eV 3 35,16 eV
Titik leleh 1452 oC
Titik didih 2913 oC
Eo untuk M2+ + 2e-→ M -0,24 V
Jari-jari 1,24 Å
Massa atom relatif 58,6934 gram/mol
8. Spektrofotometer FTIR
Spektrofotometer FTIR adalah instrumen yang didasarkan pada vibrasi
atom dalam molekul (Stuart, 2004: 2). Prinsip dasar metode spektrofotometri
FTIR adalah molekul dalam sampel yang dianalisis akan menyerap radiasi
inframerah, dan mengalami eksitasi ke tingkatan energi yang lebih tinggi.
Penyerapan radiasi inframerah merupakan proses kuantisasi. Hanya frekuensi
atau energi tertentu dari radiasi inframerah yang diserap oleh molekul.
Penyerapan radiasi inframerah sesuai dengan perubahan energi yang memiliki
orde dari 2 hingga 10 kkal/mol (Sastrohamidjojo, 1992: 4).
Radiasi dalam kisaran energi ini sesuai dengan kisaran frekuensi vibrasi
rentangan dan vibrasi bengkokan dari ikatan kovalen dalam kebanyakan
molekul. Dalam proses penyerapan maka energi yang diserap akan menaikkan
15
ikatan dalam molekul dapat menyerap energi inframerah, meskipun frekuensi
radiasi tetap sesuai dengan gerakan ikatan. Hanya ikatan yang mempunyai
momen dipol dapat menyerap radiasi inframerah (Sastrohamidjojo, 1992: 6).
Kegunaan dari spektrum inframerah adalah memberikan keterangan
tentang struktur molekul. Untuk memperoleh informasi struktur dari spektra
inframerah, maka harus diketahui frekuensi atau panjang gelombang dimana
gugus fungsional menyerap (Sastrohamidjojo, 1992: 6). Korelasi inframerah
yang memuat informasi berbagai gugus fungsional senyawa organo-silikon
ditunjukkan dalam Tabel 5.
Tabel 5. Korelasi Inframerah Gugus Fungsional Senyawa Organo-Silikon
Gugus
1020 9,80 Vibrasi rentangan
Si - O
Si – O – Si (tetramer siklis)
1082 9,42 Vibrasi rentangan
Si – O - (Sumber: Sastrohamidjojo, 1992)
16
Gambar 1. Skema Kerja Alat Spektrofotometer FTIR (Stuart, 2004: 19)
Sinar yang datang dari sumber sinar akan diteruskan, kemudian dipecah
oleh pemecah sinar menjadi dua bagian sinar yang saling tegak lurus. Sinar ini
kemudian dipantulkan oleh dua cermin yaitu cermin diam dan cermin bergerak.
Sinar hasil pantulan kedua cermin akan dipantulkan kembali menuju pemecah
sinar untuk saling berinteraksi. Dari pemecah sinar, sebagian sinar akan
diarahkan menuju cuplikan dan sebagian menuju sumber. Gerakan cermin yang
maju mundur akan menyebabkan sinar yang sampai pada detektor akan
berfluktuasi. Sinar akan saling menguatkan ketika kedua cermin memiliki jarak
yang sama terhadap detektor, dan akan saling melemahkan jika kedua cermin
memiliki jarak yang berbeda. Fluktuasi sinar yang sampai pada detektor akan
menghasilkan sinyal yang disebut interferogram. Interferogram diuvah menjadi
17
9. Spektrofotometer Serapan Atom
Spektrofotometer serapan atom adalah alat yang digunakan untuk
mendeteksi logam dan ultra logam dalam berbagai variasi sampel, seperti
biologi, lingkungan, makanan, dan geologi dengan tingkat akurasi dan ketelitian
yang baik (Settle, 1997: 373). Prinsip metode spektrofotometri serapan atom
adalah absorbansi cahaya oleh atom. Pengukuran pada spektrofotometer
didasarkan pada jumlah radiasi yang diserap oleh atom-atom bebas dalam
keadaan dasar (ground state). Atom-atom menyerap cahaya pada panjang
gelombang tertentu, tergantung pada sifat unsurnya. Cahaya pada panjang
gelombang tertentu mempunyai cukup energi untuk mengubah tingkat elektronik
suatu atom. Transisi elektronik suatu unsur bersifat spesifik, dengan absorbansi
energi, berarti memperoleh lebih banyak energi, suatu atom pada keadaan dasar
dinaikkan tingkat energinya ke tingkat eksitasi (Khopkar, 2010: 288).
Gambar 2. Proses Serapan Atom (Anonim, 1996: 5)
Alat spektrofotometer serapan atom terdiri atas tiga komponen yaitu unit
atomisasi, sumber radiasi dan sistem pengukur fotometrik. Atomisasi dapat
dilakukan dengan nyala maupun tungku. Sampel yang dianalisis disedot melalui
kapiler kemudian dikeluarkan sebagai kabut halus ke dalam nyala api, maka
18
atomisasi uap sehingga terbentuk atom-atom bebas. Apabila cahaya dengan
panjang gelombang tertentu dilewatkan pada atom-atom bebas tersebut, maka
sebagian cahaya akan diserap dan intensitas penyerapan akan berbanding lurus
dengan banyaknya atom bebas logam yang berada dalam sel (Khopkar, 2010:
291). Kondisi analisis unsur Ni dan Zn dengan SSA dapat dilihat pada Tabel 6.
Tabel 6. Kondisi Analisis Unsur Ni dan Zn (Khopkar, 2010: 292-293)
Unsur Panjang
10.Gas Surface Analyzer
Gas Surface Analyzer merupakan suatu alat yang digunakan untuk
pengukuran fisik terhadap suatu material, meliputi luas permukaan, volume
pori-pori, jari-jari pori-pori, dan distribusi pori. Pengukuran tersebut bertujuan untuk
karakterisasi suatu bahan material. Prinsip kerja alat ini menggunakan
mekanisme adsorpsi gas pada permukaan suatu bahan padatan pada berbagai
tekanan dan temperatur yang konstan. Gas yang biasa digunakan adalah helium
untuk mikropori, nitrogen untuk mesopori dan argon untuk makropori (Sudarlin,
2016).
Sebelum dilakukan analisis, sampel dipreparasi terlebih dahulu untuk
menghilangkan gas atau uap atau senyawa volatil yang mungkin telah
19
penting dilakukan untuk memperoleh hasil ukuran distribusi pori pada
permukaan secara tepat (Zielinski & Kettle, 2013: 4). Proses preparasi dilakukan
pada alat degasser.
Pada alat degasser, bahan uji dipanaskan dalam sampel sel yang
dihubungkan dengan port degas menggunakan mantel pemanas. Proses ini dapat
dilakukan dengan dua cara, yaitu kondisi flow atau kondisi vakum. Pada kondisi
flow, gas dari port degas dialirkan ke dalam sampel sel sehingga mendesak
zat-zat pengotor yang ada. Sedangkan pada kondisi vakum, dilakukan dengan cara
mengurangi tekanan sehingga bahan-bahan pengotor yang ada dapat terlepas
(Sudarlin, 2016).
Proses degassing dilakukan selama 2 sampai 4 jam dengan temperatur
pemanasan berkisar 40–300 oC. Temperatur pemanasan bergantung pada
karakteristik padatan yang akan dianalisis. Temperatur yang terlalu tinggi dapat
menyebabkan melelehnya padatan atau kerusakan pada padatan, sehingga tidak
dapat dianalisis. Pada temperatur yang terlalu rendah, dimungkinkan masih
banyak zat pengotor yang tersisa pada pori atau permukaan padatan (Sudarlin,
2016). Untuk menentukan temperatur pada proses degassing dapat dilakukan
dengan analisis TGA (Thermogravimetric Analysis) pada padatan yang akan
dianalisis.
Setelah proses degassing selesai, padatan dilakukan analisis Gas Surface
Analyzer. Proses analisis dengan GSA dilakukan pada kondisi isotherm, yaitu
pada variasi tekanan dan temperatur konstan. Variasi tekanan relatif terhadap
20
Bahan uji yang akan dianalisis diletakkan pada sampel sel yang dihubungkan
dengan port gas dari alat analyzer GSA. Nitrogen cair dengan temperatur 77,035
K dimasukkan ke dalam thermostat hingga merendam sampel sel. Gas nitrogen
dialirkan oleh port gas ke dalam tabung sampel sesuai dengan tekanan yang
sudah diatur sebelumnya. Semakin tinggi tekanan maka semakin banyak gas
nitrogen yang diadsorpsi oleh bahan padatan. Hubungan volume gas yang
diadsorpsi dan tekanan tersebut akan diplot secara otomatis pada software
komputer dalam bentuk grafik hubungan V (volume gas yang diadsorpsi/
desorpsi) dengan P/Po (tekanan relatif) (Sudarlin, 2016) seperti pada Gambar 3.
Gambar 3. Contoh Data Grafik yang dihasilkan dari Analisa GSA (Sudarlin,
2016)
Pada Gambar 3 terdapat dua kurva yang sejajar. Kurva dengan garis
21
dengan garis biru menunjukkan banyaknya gas yang didesorpsi pada variasi
P/Po.
Data berupa grafik pada Gambar 3 tersebut selanjutnya akan diolah
secara otomatis dengan aplikasi dari instrument GSA untuk menghitung luas
permukaan, ukuran pori dan volume pori. Secara umum, teknik yang digunakan
dalam aplikasi GSA untuk mengukur luas permukaan dan porositas suatu
material adalah teknik Brunauer, Emmet and Teller (BET) (Brunauer, et al.,
1938 dalam Santamarina et al., 2002: 234).
Untuk menghitung luas permukaan dapat dilakukan dengan
menggunakan persamaan berikut:
s =
N adalah bilangan avogadro, M adalah berat molekul dari gas yang teradsorp,
Acs adalah cross-sectional area gas (untuk nitrogen 16,2 (Å)) dan Wm adalah
berat gas nitrogen yang membentuk lapisan monolayer pada permukaan zat
padat.
Harga Wm dapat diperoleh dengan cara membuat grafik antara P/Po
dengan 1/{W(P/Po-1)}. Berdasarkan grafik tersebut akan diperoleh persamaan
garis regresi y = b + ax yang merupakan persamaan BET. Adapun persamaan
BET adalah sebagai berikut:
=
...(2)
22
: Intersep
: Slope
W : berat gas total yang terserap pada tekanan relatif P/Po (g gas/g adsorben)
Wm : berat gas nitrogen yang membentuk lapisan monolayer pada
permukaan zat padat (g gas/g adsorben)
P : tekanan adsorbat dalam keadaan setimbang
Po : tekanan uap jenuh adsorbat pada keadaan setimbang
P/Po : tekanan relatif dan C adalah tetapan BET
Harga Wm diperoleh dari:
Wm =
B. Penelitian Yang Relevan
Yuri Melantika Azizah (2015) dalam penelitiannya yang berjudul “Sintesis
Silika Gel dari Abu Vulkanik gunung kelud dengan Asam Nitrat (HNO3) dan Uji
Adsorptivitasnya terhadap Ion Logam Kromium(VI) dan Timbal(II).” Telah
berhasil melakukan sintesis silika gel dari abu vulkanik gunung kelud melalui
ekstrasi basa dengan larutan NaOH 3 M hingga mendidih, dan menghasilkan
natrium silikat. Larutan natrium silikat yang dihasilkan di tambahkan asam nitrat
dengan variasi konsentrasi 1, 2, dan 3 M hingga terbentuk hidrogel. Gel yang
terbentuk dikeringkan dalam oven pada temperatur 110 oC selama 2 jam untuk
menghilangkan kandungan air. Hasil karakterisasi silika gel menunjukkan bahwa
silika gel hasil sintesis memiliki gugus fungsional yang hampir sama dengan
23
mempunyai daya adsorpsi serta efisiensi adsorpsi maksimal terhadap ion logam
Cr(II) dan Pb(II) dalam limbah simulasi.
Buhani, Narsito, Nuryono dan Eko Sri Kunarti (2009) dalam
penelitiannya yang berjudul “ Influence of pH Toward Interaction of Metal Ions
Cd(II) and Cu(II) by Mercapto-Silica Hybrid Adsorbent in Aquaeos Solution”
telah mempelajari pengaruh pH larutan terhadap interaksi adsorben dan logam.
Hasil penelitian menunjukkan bahwa interaksi antara adsorben dan logam yang
paling optimum di peroleh pada pH larutan 5,5.
Kesamaan antara penelitian-penelitian tersebut di atas dengan penelitian
ini adalah konsentrasi asam nitrat yang digunakan pada sintesis adsorben dari abu
vulkanik gunung kelud yaitu 3 M. Berdasarkan penelitian yang dilakukan oleh
Melantika Y dan Kristianingrum S bahwa pada sintesis silika gel dengan
penambahan asam nitrat 3M memperoleh efisiensi produksi yang lebih optimum,
daya adsorpsi dan efisiensi adsorpsi terhadap ion logam Cr(VI) dan Pb(II) yang
lebih optimum. Selain itu, kesamaan dengan penelitian yang dilakukan oleh
Buhani, Narsito, Nuryono dan Eko Sri Kunarti (2009) adalah dalam penelitian ini
kami mempelajari pengaruh variasi pH medium terhadap adsorpsi ion logam.
Perbedaan antara penelitian ini dengan penelitian sebelumnya adalah ion
logam yang digunakan dalam uji adsorpsi adsorben hasil sintesis yaitu Ni(II) dan
Zn(II). Ion logam bukan berasal dari limbah simulasi yang dibuat oleh peneliti,
namun berasal dari limbah nyata yaitu limbah cair industri elektroplating yang
24
C. Kerangka Berfikir
Silika gel merupakan salah satu jenis adsorben yang memiliki gugus
silanol ( dan siloksan ( ) yang merupakan gugus aktif
pada permukaannya. Adanya kedua gugus ini menyebabkan silika gel dapat
digunakan untuk keperluan adsorpsi (Kristianingrum, Siswani, dan Fillaeli, 2011).
Silika gel dapat dibuat dari bahan alam yang mengandung unsur silika di
dalamnya. Berdasarkan hasil analisis XRF (X-Ray Fluorescence), diketahui
bahwa kandungan silika (SiO2) dalam abu vulkanik gunung kelud hasil erupsi
pada tanggal 14 Februari 2014 sebesar 70,6% (Kasatriyanto, 2014).
Sintesis adsorben silika gel dapat dilakukan dengan pencampuran antara
natrium silikat dan asam. Natrium silikat dibuat dengan cara meleburkan SiO2
pada abu vulkanik gunung kelud yang sudah dicuci dengan menggunakan NaOH
(Rosmawati, Tjahjanto, dan Prananto, 2013). Natrium silikat yang terbentuk
ditambah dengan asam nitrat 3 M tetes demi tetes hingga terbentuk asam silikat
berupa gel berwarna putih. Penambahan asam pada prekursor natrium silikat
menyebabkan terjadinya protonasi gugus siloksi (SiO-) menjadi silanol (SiOH).
Gugus silanol yang terbentuk kemudian diserang lanjut oleh gugus siloksi (SiO-)
dengan bantuan katalis asam membentuk ikatan siloksan ( ).
Reaksi ini akan menghasilkan alkogel yang akan mengalami sinerisis apabila
didiamkan (aging) dan menjadi hidrogel. Hidrogel dicuci dengan akuades hingga
netral dan dipanaskan menggunakan oven pada temperatur 120 oC hingga
membentuk xerogel (Mujiyanti, Nuryono, dan Kunarti, 2010). Adsorben yang
25
karakter gugus fungsi silanol dan siloksan, serta analisis menggunakan Gas
sorption analyzer (GSA) untuk mengetahui karakter porositas adsorben yang
meliputi luas permukaan, ukuran pori-pori dan distrbusi volume pori.
Adsorpsi adsorben terhadap suatu logam dipengaruhi oleh beberapa faktor,
salah satunya ada kondisi pH larutan. Buhani, Narsito, Nuryono dan Eko Sri
Kunarti (2009) dalam penelitiannya yang berjudul “ Influence of pH Toward
Interaction of Metal Ions Cd(II) and Cu(II) by Mercapto-Silica Hybrid Adsorbent
in Aquaeos Solution” telah mempelajari pengaruh pH larutan terhadap interaksi
adsorben dan logam. Hasil penelitian menunjukkan bahwa interaksi antara
adsorben dan logam mencapai optimum pada pH larutan 5,5.
Pada penelitian ini, adsorpsi adsorben terhadap ion logam Ni(II) dan Zn(II)
dilakukan dalam cuplikan limbah cair elektroplating pada berbagai pH yaitu 1, 2,
4, 6 dan 8. Konsentrasi ion logam Ni(II) dan Zn(II) sebelum dan sesudah adsorpsi
26
BAB III
METODE PENELITIAN
A. Subjek dan Objek Penelitian
1. Subjek Penelitian
Subjek penelitian ini adalah abu vulkanik hasil erupsi gunung Kelud
periode Februari 2014 yang diambil di daerah Minomartani, Ngaglik, Sleman,
Yogyakarta.
2. Objek Penelitian
Objek penelitian ini adalah karakter adsorben hasil sintesis yang meliputi
spektra FTIR, porositas (luas permukaan, ukuran pori dan volume pori
adsorben), keasaman, kadar air adsorben, efisiensi adsorpsi dan daya adsorpsi
adsorben terhadap ion logam Ni dan Zn dalam limbah cair industri
elektroplating.
B. Teknik Pengambilan Sampel
Pengambilan sampel abu vulkanik gunung kelud dilakukan dengan
purpossive sampling di daerah Minomartani, Ngaglik, Sleman, Yogyakarta.
C. Variabel Penelitian
1. Variabel bebas
Variabel bebas pada penelitian ini adalah pH larutan pada pengujian
efisiensi dan daya adsorpsi ion logam dalam limbah cair industri elektroplating
yaitu 1, 2, 4, 6, dan 8, serta jenis ion logam yang diadsorpsi yaitu ion logam
Ni(II) dan Zn(II).
27
Variabel terikat pada penelitian ini adalah karakter adsorben hasil sintesis
yang meliputi spektra FTIR, keasaman, kadar air, porositas (luas permukaan,
ukuran pori dan volume pori adsorben), efisiensi adsorpsi dan daya adsorpsi
adsorben terhadap ion logam Ni dan Zn dalam limbah cair industri
elektroplating.
3. Variabel kontrol
Variabel kontrol pada penelitian ini adalah konsentrasi asam nitrat yang
ditambahkan pada proses sintesis adsorben yaitu 3M.
D. Alat dan Bahan
1. Alat yang digunakan
a. Seperangkat alat Spektrofotometer Serapan Atom
b. Seperangkat Alat Spektrofotometer FTIR
c. Seperangkat alat Gas Sorption Analyzer Nova Quantachrome
d. Ayakan 200 mesh
e. Timbangan analitik
f. Muffle Furnace
g. Oven
h. Penyaring Buchner
i. Pompa vakum
j. Magnetik stirer
k. Cawan porselen
l. Lumpang porselen
28 n. Alat-alat plastik pendukung
o. Kertas saring Whatman No.42
p. Kertas pH Universal
q. Desikator
r. Shaker
s. Sentrifuge
2. Bahan yang digunakan
a. Abu vulkanik gunung kelud (di daerah Yogyakarta)
b. Limbah cair elektroplating
c. Larutan HNO3 3 M
d. Larutan NaOH 0,1, 1, dan 3 M
e. Akuabides
f. Larutan HCl 0,1 M
g. Kristal H2C2O4.2H2O
h. Kristal Na2B4O7.10H2O
i. Kristal kiesel gel 60G buatan E Merck
j. Larutan standar Ni(II)
k. Larutan standar Zn(II)
E. Prosedur Penelitian
29
Sebanyak 500 gram abu vulkanik gunung Kelud di ayak menggunakan
ayakan lolos 200 mesh. Sebanyak 200 gram abu vulkanik hasil ayakan
ditempatkan pada krus porselin kemudian dikalsinasi dengan menggunakan muffle
furnace pada temperatur 700 0C selama 4 jam. Abu halus sebanyak 25 gram
dicuci dengan 150 mL larutan HCl 0,1 M melalui pengadukan selama 1 jam dan
didiamkan selama 24 jam, kemudin abu yang telah dicuci tersebut disaring
menggunakan kertas saring Whatman no.42 dan dibilas dengan akuabides hingga
netral. Selanjutnya abu hasil pencucian dikeringkan dalam oven pada temperatur
110oC selama 2 jam. Abu halus diambil 0,1 gram untuk dikarakterisasi
menggunakan spektrofotometer FTIR untuk mengetahui gugus fungsional silika.
2. Pembuatan Natrium Silikat
Sebanyak 6 gram abu vulkanik hasil preparasi, dimasukkan ke dalam 200
mL larutan NaOH 3M pada teflon sambil diaduk dan dipanaskan hingga
mendidih, kemudian didiamkan selama 24 jam. Larutan natrium silikat yang
terbentuk disaring dengan kertas saring Whatman no.42 untuk memisahkan filtrat
dengan endapan.
3. Sintesis Adsorben
Sintesis adsorben dilakukan dengan menggunakan metode sol gel.
Sebanyak 20 mL larutan natrium silikat ditempatkan pada wadah plastik,
kemudian ditambahkan larutan HNO3 3M tetes demi tetes hingga terbentuk gel.
Apabila sudah terbentuk gel, penambahan larutan HNO3 3M dilanjutkan hingga
mencapai pH 7 dan didiamkan selama 24 jam. Kemudian gel yang terbentuk
30
akuabides hingga pH netral. Gel tersebut dikeringkan dalam oven pada temperatur
120 oC selama 2 jam. Adsorben selanjutnya digerus dengan menggunakan mortar
dan diayak menggunakan ayakan 200 mesh. Adsorben selanjutnya dianalisis
dengan spektrofotometer FTIR dan membandingkannya dengan spektra FTIR
pada kiesel gel 60G buatan E Merck
4. Penentuan Keasaman Adsorben
Pada penelitian ini, penentuan keasaman adsorben dilakukan dengan
metode volumetri. Sebanyak 0,1 gram adsorben direndam dalam 15 mL larutan
NaOH 0,1 M (yang telah distandarisasi) selama 24 jam. Adsorben disaring dan
dipisahkan dari campurannya dengan cara didekantir. Larutan NaOH sisa dititrasi
dengan larutan standar HCl 0,1 M (yang telah distandarisasi) menggunakan
indikator fenolftalein.
5. Penentuan Kadar Air
Sebanyak 0,1 gram adsorben dipanaskan dalam oven pada temperatur
110oC selama 4 jam, kemudian didinginkan dan ditimbang, sehingga diperoleh
berat adsorben awal. Selanjutnya adsorben dipanaskan dalam muffle furnace pada
temperatur 600 oC selama 2 jam, kemudian didinginkan dan ditimbang. Proses ini
diulang hingga diperoleh berat yang konstan.
6. Adsorpsi Adsorben pada Ion Logam Ni(II) dan Zn(II)
Sebelum dilakukan variasi pH, terlebih dahulu diukur pH awal limbah cair
industri elektroplating dengan menggunakan pH meter. Selanjutnya limbah cair
elektroplating ditambahkan larutan NaOH 1 M hingga diperoleh larutan dengan
31
limbah elektroplating pada pH yang bervariasi yaitu 1, 2, 4, 6, dan 8. Campuran
tersebut diaduk dengan alat shaker selama 90 menit. Selanjutnya campuran
dimasukkan ke dalam tabung reaksi dan disentrifuge dengan kecepatan 2000 rpm
selama 30 menit. Kemudian endapan dan filtrat dipisahkan, dan filtrat yang
diperoleh dianalisis konsentrasi ion Ni(II) dan Zn(II) dengan menggunakan AAS.
Endapan dibilas dengan akuades, kemudian dikeringkan pada temperatur 60 oC
selama 6 jam untuk dianalisis menggunakan spektrofotometer inframerah.
F. Teknik Analisis Data
1. Menghitung Keasaman Adsorben
Keasaman (mmol/gram) =
=
Jumlah mmol NaOH sisa setara dengan jumlah mmol HCl yang digunakan untuk
titrasi.
2. Menentukan Kadar Air Adsorben
Kadar air =
x 100% Keterangan:
Massa awal = berat adsorben sebelum pemanasan
Massa akhir = berat adsorben setelah pemanasan
Dengan mengasumsikan kandungan yang terdapat pada adsorben hanya
H2O dan SiO2, maka rumus molekul adsorben (SiO2.xH2O) dapat ditentukan
32
3. Menghitung Daya Adsorpsi dan Efisiensi Adsorpsi Adsorben terhadap Ion
Logam Ni(II) dan Zn(II)
D =
Ep =
x 100% Keterangan:
Co = konsentrasi ion logam Ni(II) dan ion logam Zn(II) mula-mula (ppm)
Ci = konsentrasi ion logam Ni(II) dan ion logam Zn(II) setelah adsorpsi
(ppm)
Ep = efisiensi adsorpsi (%)
4. Menentukan konsentrasi ion logam Ni(II) dan Zn(II)
Penentuan konsentrasi ion logam Ni(II) dan Zn(II) didasarkan pada
persamaan garis linear yang diperoleh pada kurva larutan standar ion logam Ni(II)
dan Zn(II)
y = a + bx
Keterangan:
y = absorbansi (A)
a = konstanta
b = slope
33
BAB IV
HASIL DAN PEMBAHASAN
A. Hasil Penelitian
Produk yang dihasilkan dari penelitian ini adalah adsorben yang disintesis
dari abu vulkanik gunung kelud berupa padatan dengan tekstur yang halus dan
berwarna putih. Sebanyak 20 mL natrium silikat yang diperoleh dari sintesis per 6
gram abu Kelud dalam 200 mL NaOH direaksikan dengan asam nitrat 3 M,
diperoleh adsorben dengan efisiensi produksi sebesar 63,73%. Perhitungan
selengkapnya dapat dilihat pada Lampiran 1.
1. Hasil Karakterisasi Adsorben Hasil Sintesis
Adsorben hasil sintesis dikarakterisasi dan dibandingkan dengan kiesel gel
60G buatan E-Merck. Adapun yang dibandingkan adalah karakter yang meliputi
spektra FTIR, keasaman dan kadar air. Berdasarkan data uji kadar air, diperoleh
rumus adsorben hasil sintesis dan kiesel gel 60G, dan dari data keasaman akan
diperoleh hubungan daya adsorpsi dan efisiensi adsorpsi dengan gugus fungsi
silanol pada permukaan adsorben. Data keasaman dan kadar air adsorben hasil
sintesis ditunjukkan pada Tabel 7.
Tabel 7. Data Keasaman dan Kadar Air Adsorben Hasil Sintesis dan Kiesel Gel 60G
*) Rerata dari dua kali pengulangan (duplo)
Perhitungan selengkapnya untuk keasaman dan kadar air dapat dilihat pada
34
Karakterisasi dengan spektrofotometer FTIR dilakukan untuk mengetahui
keberadaan gugus fungsi silanol (Si–OH) dan siloksan (Si–O–Si) pada permukaan
adsorben hasil sintesis. Keberadaan kedua gugus tersebut diketahui dengan cara
menginterpretasi spektra hasil analisis FTIR dan membandingkannya dengan
spektra FTIR kiesel gel 60G. Perbandingan spektra FTIR antara kiesel gel 60G
dan adsorben hasil sintesis dapat dilihat pada Gambar 4.
Gambar 4. Spektra FTIR Kiesel Gel 60G dan Adsorben Hasil Sintesis (ADHNO3)
Hasil interpretasi spektra FTIR dari abu vulkanik gunung kelud dan
adsorben hasil sintesis dapat dilihat pada Tabel 8.
Tabel 8.Interpretasi Spektra Kiesel gel 60G dan Adsorben Hasil Sintesis (ADHNO3)
No
Bilangan Gelombang (cm-1)
35
Selain karakterisasi dengan spektrofotometer FTIR, adsorben hasil sintesis
juga dikarakterisasi dengan alat Gas Sorpstion Analyzer (GSA) untuk mengetahui
porositasnya. Karakter porositas adsorben hasil sintesis dapat dilihat pada Tabel
9.
Tabel 9. Porositas Adsorben Hasil Sintesis
Luas permukaan (m2/g) Volume total pori (cm3/g) Jari-jari pori (Å)
144,744 0,771 106,54
Karakterisasi dengan spektrofotometer FTIR dilakukan juga untuk
mengetahui pergeseran panjang gelombang yang terjadi antara adsorben hasil
sintesis sebelum adsorpsi dan sesudah adsorpsi. Perbandingan spektra FTIR
adsorben hasil sintesis sebelum adsorpsi dan sesudah adsorpsi dapat dilihat pada
Gambar 5.
Gambar 5. Spektra FTIR Adsorben Hasil Sintesis (ADHNO3) Sebelum dan
Sesudah Adsorpsi
Hasil interpretasi spektra FTIR dari abu vulkanik gunung kelud dan
adsorben hasil sintesis dapat dilihat pada Tabel 10. 80
36
Tabel 10. Interpretasi Spektra Adsorben Hasil Sintesis (ADHNO3) Sebelum dan
Sesudah Adsorpsi pada pH optimum
No
Bilangan Gelombang (cm-1)
Jenis Vibrasi
2. Hasil Daya Adsorpsi dan Efisiensi Adsorpsi Adsorben Hasil Sintesis
Pada perhitungan efisiensi adsorpsi ion logam Ni(II) dan Zn(II) dalam
limbah cair industri elektroplating oleh adsorben, diperlukan adanya kurva standar
untuk menentukan konsentrasi ion logam dari hasil analisis spektrofotometri
serapan atom. Kurva standar larutan Ni(II) dan Zn(II) ditunjukkan pada Gambar 6
dan Gambar 7.
37
Gambar 7. Kurva Standar Larutan Zn(II)
Perhitungan efisiensi adsorpsi ion logam Ni(II) dan Zn(II) dalam limbah
cair industri elektroplating oleh adsorben hasil sintesis (ADHNO3) dan kiesel gel
60G, dilakukan dengan mengukur konsentrasi ion logam dalam limbah sebelum
adsorpsi dan sesudah adsorpsi menggunakan spektrofotometri serapan atom.
Selisih konsentrasi ion logam dalam limbah antara sebelum dan sesudah adsorpsi
menunjukkan jumlah ion logam yang diserap oleh adsorben. Data efisiensi
adsorpsi dan daya adsorpsi ion logam Ni(II) dapat dilihat pada Tabel 11. Data
efisiensi adsorpsi dan daya adsorpsi ion logam Zn(II) dapat dilihat pada Tabel 12.
Perhitungan selengkapnya dapat dilihat pada Lampiran 9.
Tabel 11. Data Efisiensi dan Daya Adsorpsi Ion Logam Ni(II) dalam Limbah Cair Industri Elektroplating oleh Adsorben Hasil Sintesis dan kiesel Gel 60 G
38
Tabel 12. Data Efisiensi dan Daya Adsorpsi Ion Logam Zn(II) dalam Limbah Cair Industri Elektroplating oleh Adasorben Hasil Sintesis dan kiesel Gel 60 G
pH
Data pada Tabel 11 dan Tabel 12 mengenai efisiensi adsorpsi terhadap ion
logam Ni(II) dan Zn(II) selanjutnya diinterpretasikan dalam bentuk grafik untuk
mengetahui hubungan antara % efisiensi adsorpsi dengan perubahan pH. Grafik
hubungan antara % efisiensi adsorpsi dengan pH ditunjukkan pada Gambar 8 dan
Gambar 9.
Gambar 8. Kurva % Efisiensi Adsorpsi Ion Logam Ni(II) dan Zn(II) oleh Adsorben kiesel gel 60G pada berbagai pH
39
Gambar 9. Kurva % Efisiensi Adsorpsi Ion Logam Ni(II) dan Zn(II) oleh Adsorben Hasil Sintesis dengan HNO3 (ADHNO3) pada berbagai pH
B. Pembahasan
1. Pembuatan adsorben dari abu vulkanik gunung kelud
Pada penelitian ini, sebelum dilakukan sintesis adsorben, terlebih dahulu
dilakukan preparasi pada abu vulkanik gunung kelud. Preparasi ini penting
dilakukan dengan tujuan untuk menghilangkan substansi-substansi berupa
pengotor yang dapat memberikan interferensi pada abu. Pada tahap preparasi, abu
vulkanik gunung kelud dikalsinasi dengan menggunakan muffle furnace pada
temperatur 700 oC selama 4 jam. Pemanasan abu pada temperatur 700 oC
merupakan temperatur yang paling optimum untuk proses kalsinasi abu, karena
pada temperatur ini akan menghasilkan abu dengan silika dalam bentuk amorf
(Aina, Nuryono, & Tahir, 2007: 9). Selain itu, pada temperatur 700 oC akan
menghasilkan abu yang bebas dari pengotor berupa karbon berwarna hitam (Hadi,
40
Setelah dilakukan proses kalsinasi, selanjutnya abu dicuci dan direndam
dalam larutan HCl 0,1 M. Proses ini dilakukan dengan tujuan untuk melarutkan
kadar pengotor berupa oksida-oksida logam dan mineral selain silika yang
terdapat dalam abu yang sudah dikalsinasi, sehingga ketika dilakukan proses
penyaringan dan pencucian dengan akuades, oksida akan larut dalam filtrat dan
abu bebas dari oksida-oksida selain silika (Mujiyanti, Nuryono, & Kunarti, 2010:
154). Abu yang sudah disaring dan dipisahkan dari filtratnya, selanjutnya
dilakukan pemanasan pada temperatur 110 oC.
Proses sintesis adsorben silika gel dari abu vulkanik gunung kelud, secara
garis besar melalui beberapa tahap. Tahapan pertama adalah pembentukan
natrium silikat dengan cara mereaksikan SiO2 pada abu dengan NaOH
(Rosmawati, Tjahjanto, & Prananto, 2013: 162). Pada penelitian ini, abu yang
sudah dicuci dimasukkan ke dalam larutan NaOH 3M lalu dilakukan pemanasan
dan pengadukan hingga mendidih. Natrium silikat yang terbentuk didiamkan
selama 24 jam dan disaring untuk memisahkan filtrat dan endapan abu. Filtrat
natrium silikat ini yang akan digunakan sebagai prekursor pembuatan adsorben
silika gel. Proses pembentukan natrium silikat ditunjukkan dalam reaksi berikut:
SiO2(s) + 2NaOH(aq) → Na2SiO3(aq) + H2O(l)
Mekanisme reaksi yang diperkirakan pada pembentukan natrium silikat
tersebut ditampilkan pada Gambar 10.
Pada SiO2, elektronegativitas atom O yang tinggi menyebabkan Si lebih
elektropositif. Adanya gugus OH- dari NaOH akan menyerang Si sehingga
41
Gambar 10. Model Mekanisme Reaksi Pembentukan Natrium Silikat (Alex, 2005 dalam Mujiyanti, Nuryono, & Kunarti, 2010: 156)
Kemudian akan terjadi dehidrogenasi, di mana ion H+ dari senyawa intermediet
akan dilepaskan dan akan berikatan dengan ion hidroksil dari NaOH yang lain
membentuk H2O. Dua ion Na+ akan menyeimbangkan muatan negatif yang
terbentuk dan berinteraksi dengan ion SiO32- sehingga terbentuk natrium silikat
(Na2SiO3). Natrium silikat yang terbentuk larut dalam akuades sehingga menjadi
larutan natrium silikat Na2SiO3. Larutan natrium silikat ini akan digunakan
sebagai prekursor dalam pembuatan adsorben silika gel (Mujiyanti, Nuryono, &
Kunarti, 2010: 156).
Tahapan kedua adalah pembentukan silika gel dengan metode sol gel.
Metode sol gel merupakan proses pembentukan jaringan oksida dengan reaksi
polikondensasi dari molekul prekursor dalam medium air (Buhani dkk., 2012:
265). Pada metode sol gel, prekursor berupa natrium silikat ditambahkan dengan
asam hingga terbentuk asam ortosilikat melalui reaksi hidrolisis asam (Essien et