BAB 2
TINJAUAN PUSTAKA
2.1. Hemostasis
Menurut Bakta (2006) faal hemostasis ialah suatu fungsi tubuh yang bertujuan untuk mempertahankan keenceran darah sehingga darah tetap mengalir dalam pembuluh darah dan menutup kerusakan dinding pembuluh darah pada saat terjadinya kerusakan pembuluh darah. Faal hemostasis melibatkan berikut:
1. Sistem vaskuler 2. Sistem trombosit 3. Sistem koagulasi 4. Sistem fibrinolisis
Faal hemostasis melibatkan 2 komponen, yaitu:
1. Faal koagulasi: yang berakhir dengan pembekuan fibrin stabil 2. Faal fibrinolisis: yang berakhir dengan pembentukan plasmin. Faal koagulasi melibatkan 3 komponen, yaitu:
1. Komponen vaskuler 2. Komponen trombosit 3. Komponen koagulasi
Faal hemostasis untuk dapat berjalan normal memerlukan 3 langkah, yaitu: 1. Langkah I: hemostasis primer, yaitu pembentukan “primary platelet
plug.”
2. Langkah II: hemostasis sekunder, yaitu pembentukan stable hemostatic plug (platelet+fibrin plug).
2.1.1. Faktor Trombosit
Trombosit memegang peranan penting dalam proses awal faal koagulasi yang akan berakhir dengan pembentukan sumbat trombosit (platelet plug). Untuk itu, trombosit akan mengalami peristiwa:
1. Platelet adhesion yaitu proses perlekatan trombosit ke dinding pembuluh darah. Adhesi trombosit ke jaringan ikat subendotel terutama kolagen, terjadi dalam 1-2 menit setelah berdiam di endotel. Peningkatan adhesi trombosit menyebabkan trombosit yang beredar melekat pada kolagen. Hasilnya adalah massa trombosit kohesif yang meningkatkan dengan cepat mencapai ukuran yang cukup membentuk plug trombosit (Kiswari, 2014).
2. Platelet activation
3. Platelet aggregation yaitu penggumpalan trombosit satu sama lain. Pada proses koagulasi terdapat empat langkah utama untuk menghasilkan fibrin, yaitu:
1. Langkah pertama: proses awal yang melibatkan jalur intrinsik dan ekstrinsik yang menghasilkan tenase complex yang akan mengaktifkan faktor X menjadi faktor X aktif.
2. Langkah kedua: pembentukan prothrombin activator (prothrombinase complex) yang akan memecah prothrombin menjadi thrombin.
3. Langkah ketiga: prothrombin activator merubah prothrombin menjadi thrombin.
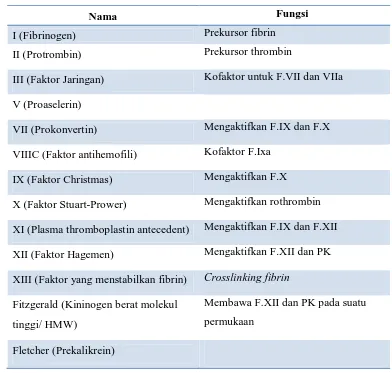
Tabel 2.1. Faktor Koagulasi
Nama Fungsi
I (Fibrinogen) Prekursor fibrin
II (Protrombin) Prekursor thrombin
III (Faktor Jaringan) Kofaktor untuk F.VII dan VIIa V (Proaselerin)
VII (Prokonvertin) Mengaktifkan F.IX dan F.X VIIIC (Faktor antihemofili) Kofaktor F.Ixa
IX (Faktor Christmas) Mengaktifkan F.X
X (Faktor Stuart-Prower) Mengaktifkan rothrombin XI (Plasma thromboplastin antecedent) Mengaktifkan F.IX dan F.XII XII (Faktor Hagemen) Mengaktifkan F.XII dan PK XIII (Faktor yang menstabilkan fibrin) Crosslinking fibrin
Fitzgerald (Kininogen berat molekul tinggi/ HMW)
Membawa F.XII dan PK pada suatu permukaan
Fletcher (Prekalikrein)
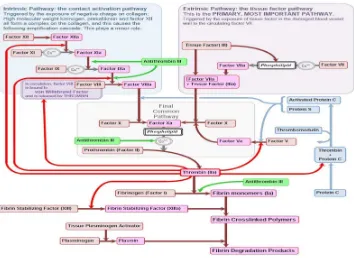
Gambar 2.1. Kaskade koagulasi. Dikutip dari:
http://www.derangedphysiology.com/php/Pathology%20tests/images/coagulation%20c ascade.JPG
2.2. Kanker
Kanker adalah istilah umum untuk pertumbuhan sel tidak normal yaitu, tumbuh sangat cepat, tidak terkontrol, dan tidak berirama yang dapat menyusup ke jaringan tubuh normal dan menekan jaringan tubuh normal sehingga memengaruhi fungsi tubuh. Kanker bukan merupakan jenis penyakit menular (Diananda, 2009).
Istilah tumor tidak sama dengan kanker. Tumor adalah istilah umum untuk setiap benjolan abnormal. Sedangkan kanker adalah tumor yang bersifat ganas. Dengan demikian, kanker itu sama dengan tumor yang ganas (Diananda, 2009). 2.2.1. Epidemiologi kanker
14,1 juta kasus tahun 2012. Sedangkan jumlah kematian meningkat dari 7,6 juta orang tahun 2008 menjadi 8,2 juta pada tahun 2012. Kanker menjadi penyebab kematian nomor 2 di dunia sebesar 13% setelah penyakit kardiovaskular. Diperkirakan pada 2030 insidens kanker dapat mencapai 26 juta orang dan 17 juta di antaranya meninggal akibat kanker, terlebih untuk negara miskin dan berkembang kejadiannya akan lebih cepat.
Di Indonesia, prevalensi penyakit kanker juga cukup tinggi. Berdasarkan data Riset Kesehatan Dasar (Riskesdas) tahun 2013, prevalensi tumor/kanker di Indonesia adalah 1,4 per 1000 penduduk, atau sekitar 330.000 orang. Kanker tertinggi di Indonesia pada perempuan adalah kanker payudara dan kanker leher rahim. Sedangkan pada laki-laki adalah kanker paru dan kanker kolorektal. Berdasarkan estimasi Globocan, International Agency for Research on Cancer (IARC) tahun 2012, insidens kanker payudara sebesar 40 per 100.000 perempuan, kanker leher rahim 17 per 100.000 perempuan, kanker paru 26 per 100.000 laki-laki, kanker kolorektal 16 per 100.000 laki-laki. Berdasarkan data Sistem Informasi Rumah Sakit 2010, kasus rawat inap kanker payudara 12.014 kasus (28,7%), kanker leher rahim 5.349 kasus (12,8%) (Depkes, 2014).
2.2.2. Faktor Risiko
Selain itu, ada juga faktor risiko yang lain yaitu zat kimia, radiasi, virus, hormon, dan iritasi kronis. Faktor lain yang tidak dapat dicegah adalah faktor genetik (Depkes, 2015).
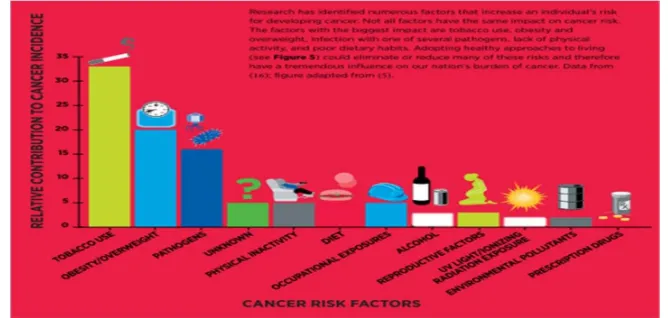
Gambar 2.2. Faktor risiko kanker
Dikutip dari: American Assoociation for Cancer Research. AACR Cancer Progress Report 2014. Clin Cancer Res 2014;20(Supplement 1):SI-S112
2.2.3. Klasifikasi Kanker
Menurut National Cancer Institute (2015) klasifikasi kanker dibagi atas dua cara antara lain, dengan tipe jaringan asal kanker tumbuh (tipe histologi) dan dengan tempat awalnya, atau lokasi pada tubuh dimana kanker pertama kali berkembang. Ada ratusan jenis kanker yang dikategorikan menjadi enam kategori utama, yaitu:
a. Karsinoma
Karsinoma merujuk pada neoplasma malignan sel asal epitel atau kanker dari lapisan internal atau eksternal tubuh. Karsinoma terbagi dua subtipe utama: adenokarsinoma, yang tumbuh pada organ atau kelenjar, dan squamos cell carcinoma, yang berasal dari epitel squamos. Sebagian
besar karsinoma mempengaruhi organ atau kelenjar sekresi, seperti payudara, yang memproduksi ASI, atau paru-paru, yang mensekresi mukus, atau kolon, prostat, dan ginjal.
b. Sarkoma
Umumnya terjadi pada remaja. Sarkoma paling umum sering berkembang sebagai massa menyakitkan pada tulang. Tumor sarkoma biasanya menyerupai jaringan di mana mereka tumbuh.
Contoh sarkomas adalah: Osteosarkoma (tulang)
Chondrosarkoma (tulang rawan) Leiomyosarkoma (otot halus) Rhabdomyosarkoma (otot rangka)
Mesothelioma (membran lapisan rongga tubuh) Fibrosarkoma (jaringan fibrosa)
Angiosarkoma atau hemangioendothelioma (pembuluh darah) Liposarkoma (jaringan adiposa)
Glioma atau pilocytic (neurogenik jaringan ikat di otak) Myxosarkoma (jaringan ikat embrio primitif)
Mesenchymous (campuran jenis jaringan ikat) c. Myeloma
Myeloma adalah kanker yang berasal dari sel-sel plasma sumsum tulang. Sel-sel plasma menghasilkan beberapa protein yang ditemukan dalam darah.
d. Leukimia
Leukemia ("kanker cair" atau "kanker darah") adalah kanker dari sumsum tulang (situs produksi sel darah). Leukemia kata berarti "darah putih" dalam bahasa Yunani. Penyakit ini sering dikaitkan dengan sel darah putih belum matang yang berlebih. Sel darah putih yang belum matang ini tidak melakukan seperti yang seharusnya, oleh karena pasien sering rentan terhadap infeksi. Leukemia juga mempengaruhi sel-sel darah merah dan dapat menyebabkan pembekuan darah tidak normal dan kelelahan akibat anemia. Contoh leukemia meliputi:
Limfatik, limfositik atau leukemia limfoblastik (keganasan limfoid dan seri sel darah limfositik)
Polisitemia vera atau erithremia (keganasan berbagai produk sel darah, tetapi dengan sel-sel darah merah yang mendominasi) e. Limfoma
Limfoma berkembang pada kelenjar atau nodus sistem limfatik, jaringan pembuluh, node, dan organ (khususnya, tonsil, limpa dan timus) yang memurnikan menghasilkan cairan tubuh dan melawan infeksi sel darah putih, atau sel-sel limfosit. Tidak seperti leukemia yang kadang-kadang disebut "kanker cair", limfoma adalah “kanker padat”. Limfoma juga bisa terjadi pada organ-organ tertentu seperti payudara, lambung atau otak. Pada limfoma ini dirujuk sebagai extranodal limfoma. Limfoma disubklasifikasikan ke dalam dua kategori: Limfoma Hodgkin dan Limfoma non-Hodgkin. Kehadiran sel-sel Reed-Sternberg di Limfoma Hodgkin membedakan diagnosa limfoma Hodgkin dari limfoma Non-Hodgkin.
f. Tipe campuran
Jenis komponen sel kanker mungkin dalam satu kategori atau dari kategori yang berbeda. Beberapa contoh, antara lain:
Sel-sel kanker dibentuk dari sel-sel normal dalam suatu proses rumit yang disebut transformasi, yang terdiri dari tahap inisiasi dan promosi. Pada tahap inisiasi, terjadi suatu perubahan bahan genetik sel yang memancing sel menjadi ganas. Perubahan dalam bahan genetik sel ini disebabkan oleh suatu agen yang disebut karsinogen (Diananda, 2009). Karsinogen dapat mempengaruhi DNA atau suatu protein yang berperan pada pengaturan siklus pembelahan sel, seperti protooncogene atau tumor supressorgene. Pada umumnya karsinogen dapat
Gambar 2.3. Cancer Stem Cell
Dikutip dari: Winslow, T., 2009. Cancer Stem Cell. U.S: National Institute of Health.
Available from:
http://www.teresewinslow.com/portshow.asp?portfolioid={FDA0DC98-2283-450D-94C5-A4FA803493B5}. [Accesed 24 April 2015].
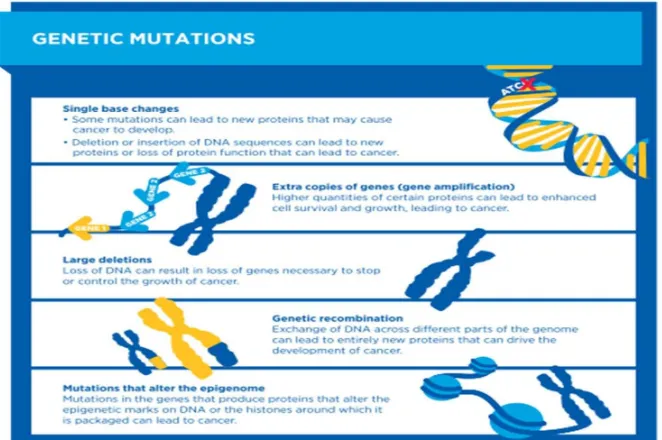
Gambar 2.4. Mutasi genetik.
Dikutip dari: American Assoociation for Cancer Research. AACR Cancer Progress Report 2014. Clin Cancer Res 2014;20(Supplement 1):SI-S112
Beberapa komponen lingkungan mikro tumor adalah bagian normal dari jaringan di mana kanker berkembang. Selebihnya adalah faktor sistemik yang mempengaruhi lingkungan mikro tumor secara perlahan karena mereka meresap melalui itu. Namun komponen lainnya secara aktif merekrut atau terbentuk sebagai hasil dari sinyal yang berasal dari sel-sel kanker sendiri. Baik komponen pasif atau aktif yang merekrut, berbagai komponen mikro sering dimanfaatkan oleh sel-sel kanker untuk memajukan pertumbuhan dan kelangsungan hidup mereka (AACR, 2014).
2.2.5. Stadium
Menurut Diananda (2009), penentuan stadium kanker biasanya diklasifikasikan terlebih dahulu menurut sistem TNM, (Tumor, Node, Metastase) sebagai berikut:
Node: penyebaran kanker ke kelenjar getah bening (N0 = tidak menyebar ke kelenjar getah bening; N1-3 = derajat penyebaran)
Metastase: ada atau tidak penyebaran ke organ jauh (M0 = tidak ada / M1= ada).
Gambar 2.5. Stadium Metastasis
Dikutip dari: American Assoociation for Cancer Research. AACR Cancer Progress Report 2014. Clin Cancer Res 2014;20(Supplement 1):SI-S112
Seiring waktu, tumor dapat membesar karena sel-sel lain menumpuk, sampai beberapa sel memperoleh kemampuan untuk menyerang jaringan lokal dan menyebar, atau bermetastasis, ke situs jauh. Munculnya metastasis kanker adalah kejadian yang mengerikan yang menyumbang lebih dari 90 persen dari kematian akibat kanker (AACR, 2014).
2.3. Trombosis Vena Dalam (DVT)
Deep Vein Thrombosis (DVT) dan Pulmonary Emboli (PE) adalah
arteri ke paru-paru, menyebabkan berpotensi Pulmonary Emboli yang mengancam kehidupan (Patel, 2014).
2.3.1. Epidemiologi
DVT dan tromboemboli tetap menjadi morbiditas dan mortalitas yang umum pada pasien rawat-inap atau terbaring di tempat tidur, serta individu yang umumnya sehat. Insiden yang tepat dari DVT tidak diketahui karena kebanyakan studi dibatasi oleh ketidaktepatan diagnosis klinis. Data insiden DVT menunjukkan bahwa sekitar 80 kasus per 100.000 penduduk terjadi setiap tahun. Kira-kira 1 dari 20 orang mengalami DVT dalam hidupnya. Rawat-inap sekitar 600.000 per tahun terjadi DVT di Amerika Serikat (Patel, 2014). Di Australia, sekitar 30.000 orang di rawat inap akibat TEV dan menyebabkan sekitar 5000 pasien meninggal setiap tahunnya (Moheimani, 2011).
Insiden TEV rendah pada anak-anak. Insiden tahunan 0,07 sampai 0,14 per 10.000 anak dan 5.3 per 10.000 penerimaan rumah sakit telah dilaporkan dalam studi Kaukasia. Insiden rendah ini mungkin disebabkan penurunan kemampuan untuk menghasilkan trombin, kemampuan yang meningkat dari alfa-2-makroglobulin untuk menghambat trombin, dan meningkatkan potensi antithrombin dinding pembuluh (Keseima, 2011).
2.3.2. Patofisiologi
Menurut Bakta (2007) Lebih dari 100 tahun yang lalu Rudolph Virchow pada tahun 1854 mengemukakan trias Virchow, yang prisipnya sampai sekarang masih dianggap valid. Berdasarkan teori trias Virchow, trombosis timbul karena tiga hal:
a. Kerusakan endotel pembuluh darah (vascular injury)
peradangan yang menyebabkan perubahan dalam fungsi endotel (Patel, 2014).
Penurunan kontraktilitas dinding pembuluh darah vena dan hilangnya fungsi katup vena berkontribusi terhadap insufisiensi vena yang kronis. Peningkatan tekanan vena ambulatori menyebabkan berbagai gejala klinis pada penderita DVT seperti edema ekstremitas bawah dan ulserasi vena (Patel, 2014).
b. Statis aliran darah vena
Aliran darah vena yang statis dapat terjadi sebagai akibat dari sesuatu yang memperlambat atau menghambat aliran darah vena. Hal ini mengakibatkan peningkatan viskositas dan pembentukan microthrombi, yang tidak dihapuskan oleh gerakan fluida. Trombus yang terbentuk kemudian dapat tumbuh dan menyebar. Aliran darah yang statis ini dapat muncul sebagai akibat dari trauma yang tidak disengaja dan juga dapat dipicu oleh pembedahan. Hiperkoagulasi dapat terjadi karena ketidakseimbangan biokimia antara faktor-faktor yang bersirkulasi. Hal ini terjadi sebagai hasil dari peningkatan faktor aktivasi jaringan yang beredar di sirkulasi sekaligus dengan penurunan antithrombin dan fibrinolisin (Patel, 2014).
c. Aktivasi koagulasi
Untuk sebagian besar, mekanisme koagulasi terdiri dari serangkaian langkah-langkah yang mengatur diri sendiri yang menghasilkan produksi fibrin untuk penggumpalan darah. Langkah-langkah ini dikendalikan oleh sejumlah kofaktor relatif tidak aktif atau zymogens, yang ketika diaktifkan akan mempromosikan atau mempercepat proses pembekuan. Reaksi ini biasanya terjadi pada permukaan fosfolipid trombosit, sel-sel endotel atau makrofag. Umumnya, inisiasi dari proses koagulasi dapat dibagi menjadi 2 jalur yang berbeda, yaitu jalur intrinsik dan ekstrinsik (Patel, 2014).
melisiskan deposit fibrin. Plasmin akan mencerna fibrin dan juga menginaktivasi faktor pembekuan V dan VIII dan fibrinogen (Patel, 2014).
Trombus paling sering terbentuk di betis. Biasanya terbentuk di belakang katup vena atau pada cabang vena poin. Venodilasi akan mengganggu barier sel endotel dan mengekspos subendothelium. Platelet melekat pada permukaan subendothelial dengan faktor von Willebrand atau fibrinogen di dinding pembuluh. Neutrofil dan platelet yang diaktivasi akan melepaskan prokoagulant dan mediator inflamasi. Neutrofil juga melekat pada dasar membran dan bermigrasi ke subendothelium. Kompleks ini membentuk permukaan platelet dan meningkatkan jumlah trombin generasi dan pembentukan fibrin. Leukosit yang dirangsang akan berikatan secara ireversibel dengan reseptor endotel dan melakukan ekstravasasi menuju dinding pembuluh darah vena dengan kemotaksis mural (Patel, 2014). 2.3.3. Tanda dan Gejala
Anamnesa dan pemeriksaan klinis tidak dapat diandalkan untuk mendiagnosa DVT. DVT ekstremitas bawah dapat asimtomatik atau menunjukkan gejala. Pasien dengan DVT ekstremitas bawah sering tidak menunjukkan gejala eritema, nyeri, rasa hangat, pembengkakan atau kelembutan. Pasien simptomatis dengan DVT proksimal mungkin menunjukkan gejala nyeri ekstremitas bawah, rasa nyeri pada betis dan pembengkakan ekstremitas bawah (Kesieme, 2011).
2.3.4. Faktor Risiko
Menurut CDC (2014) beberapa faktor yang dapat menjadi faktor risiko terkena DVT , antara lain:
a. Cedera vena, sering disebabkan oleh: Patah tulang
Cedera otot parah, atau
b. Memperlambat aliran darah, sering disebabkan oleh:
Tirah baring (misalnya karena kondisi medis atau paska operasi) Gerakan yang terbatas
Duduk untuk waktu yang lama, terutama dengan menyilangkan kaki Kelumpuhan.
c. Meningkatnya estrogen, sering disebabkan oleh: Pil
Terapi penggantian hormon, kadang-kadang digunakan setelah menopause
Kehamilan, hingga 6 minggu setelah melahirkan d. Beberapa penyakit medis kronis, seperti:
Penyakit jantung Penyakit paru-paru
Kanker dan penatalaksanaannya
Penyakit inflamasi usus (penyakit Crohn atau kolitis ulseratif) e. Faktor lainnya:
DVT sebelumnya atau PE Sejarah keluarga DVT atau PE
Usia (umur meningkat risiko meningkat) Obesitas
Kateter terletak di vena sentral Mewarisi gangguan pembekuan darah
2.4. DVT pada Kanker.
2.4.1. Epidemiologi
Pasien kanker mempunyai peningkatan risiko trombosis vena beberapa kali lipat dibandingkan dengan populasi umum atau pasien tanpa kanker, dengan nilai Risiko Relatif (RR) berkisar dari 4 sampai 7 (Timp, 2013). Kejadian trombosis merupakan penyebab kematian kedua pada pasien kanker (setelah kanker itu sendiri) (Khorana, 2012).
Berdasarkan studi yang dilakukan terhadap populasi Negara Bagian Olmsted (Minnesota), neoplasma ganas menunjukaan peningkatan risiko empat kali lipat. Sebuah penelitian meta-analisis terbaru oleh Horsted et al (2012) dalam Timp (2013) mendeskripsikan insidens trombosis vena pada pasien kanker yang dinilai berdasarkan tingkat latar belakang risiko pasien. Pada pasien kanker dengan risiko sedang, insidens trombosis vena dalam diestimasi 13 dari 1000 orang per tahun. Sedangkan insidens vena trombosis pada pasein kanker dengan risiko tinggi diestimasi 68 per 1000 orang pertahun (Timp, 2013). Di Indonesia, kejadian VTE dan pelaporannya secara nasional belum ada (Irawan, 2009). 2.4.2. Faktor Risiko
Secara keseluruhan, kanker pankreas, otak, paru-paru, dan ovarium dilaporkan mempunyai risiko yang paling tinggi. Pada literatur, risiko tinggi juga dialami oleh kanker ginjal, lambung, tulang, limfoma, dan myeloma. Selain itu, hubungan antara keganasan kanker dengan potensi terjadinya trombosis dapat diperhatikan berdasarkan stadiumnya. Pada pasien kanker dengan stadium yang lebih lanjut, terdapat risiko yang lebih besar dengan nilai RR 2,9, 2,9, 7,5, dan 17,1 diantara pasien dengan stadium I, II, III, dan IV secara berurutan (Timp, 2013).
2.4.3. Patofisiologi
Jalur biologi memiliki peran yang penting pada patofisiologi gangguan hemostasis pada kanker. Sel kanker dapat mengaktifkan sistem hemostasis melalui ekspresi protein prokoagulan, terpapar lipid prokoagulan, pelepasan sitokinin, inflamasi dan mikropartikel, serta adhesi pada sel vaskular penjamu (Kurniawan, 2013).
Menurut Suharti (2013) peran kunci mekanisme trombosis pada kanker dimainkan oleh:
(i) Faktor jaringan,
Faktor jaringan terdiri atas glikoprotein transmembran, berperan sebagai kunci inisiator koagulasi fisiologik, diekspresikan oleh berbagai jenis sel kanker, termasuk kanker padat maupun sel blas leukemia, sel makrofag yang berhubungan dengan kanker dan sel endotel. Pada pembuluh darah normal faktor jaringan tidak diekspresikan, kecuali bila diinduksi oleh sitokin proinflamasi seperti interleukin (IL)-1 dan TNF (Tumor Necrosis Factor)- atau oleh liposakarida bakteri (Suharti, 2013).
Gambar 2.6. Mekanisme aktifasi sistem hemostasis oleh sel tumor.
Dikutip dari: Falanga A. 2011. The Cancer-Thrombosis Connection. Available from:
http://www.hematology.org/Thehematologist/Mini-Review/1244.aspx. [Accesed 12 Mei
Faktor jaringan yang dilepaskan oleh permukaan sel kanker dapat menyebabkan terjadinya keadaan hiperkoagulasi lokal maupun sistemik. Aktivitas faktor jaringan pada sel kanker dapat meningkatkan ekspresi fosfolipid anionik pada bagian luar membrane sel dan sekresi heparanase. Fungsi utama heparanase adalah untuk mencerna heparin sulfat matrik ekstraseluler yang kemudian dapat menyebabkan invasi tumor dan metastasis (Kurniawan, 2013).
Faktor jaringan dapat secara aktif dilepaskan oleh sel tumor dari membran selnya dalam bentuk mikropartikel faktor jaringan. Mikropartikel adalah vesikel membran plasma dengan ukuran diameter 0,1-1 m yang dihasilkan oleh vesikulasi aktif oleh semua sel yang ada (Kurniawan, 2013). (ii) Sitokin proinflamasi
Sel tumor juga melepas sitokin proinflamasi dan kemokin, seperti TNF-, IL-1TNF-, dan VGEFTNF-, yang selanjutnya mempengaruhi leukosit dan sel endotel untuk mengekspresikan faktor jaringan dan sejumlah molekul adhesi lain yang mungkin sebagai predisposisi maupun memacu trombosis vena.
Sel tumor juga dapat berinteraksi dengan sistem fibrinolitik penjamu, melalui ekspresi aktivator plasminogen (uPA dan t-PA), inhibitornya (PAI-1 dan PAI-2), dan reseptornya seperti annexin II yang merupakan kofaktor untuk plasminogen dan aktivator plasminogen jaringan. Ketika berkontak dengan sel endotel, molekul ini mengekspresikan faktor jaringan, stimulasi produksi PAI-1, down regulation trombomodulin, dan meningkatkan up regulation molekul adhesi. Kemampuan sel tumor melekat pada endotel
vaskular menyebabkan aktivasi pembekuan darah lokal dan pembentukan thrombus (Kurniawan, 2013).
(iii) Trombosit.
tumor padat memicu angiogenesis melalui faktor proangiogenik yang berasal dari trombosit, dan dapat “menyembunyikan” pembuluh darah imatur sehingga melindungi sel tumor dari sistem imun.
Sel tumor juga mengekspresikan prokoagulan kanker, suatu protease sistein yang hanya diekspresikan oleh jaringan kanker. Prokoagulan kanker langsung mengaktifkan faktor X dalam jalur bersama, tanpa tergantung pada faktor VII. Pada periode awal diagnosis kanker kadar protease biasanya tinggi, kemudian secara menurun secara perlahan. Kondisi ini dapat menerangkan kecenderungan terjadinya tromboemboli pada 3 bulan pertama setelah didiagnosis kanker.
2.4.4. Manifestasi klinis.
Sebuah penelitian retrospective yang dilakukan oleh Amer (2013) mulai dari tahun 2005 sampai 2012 dengan 307 pasien kanker yang terkena VTE menunjukkan manifestasi sebagai berikut:
a. Orang dengan usia lanjut lebih rentan untuk mengalami trombosis.
b. Mayoritas pasien adalah overweight. Obesitas bukan merupakan faktor risiko utama untuk terjadi trombosis. Meskipun demikian, pasien yang kehilangan berat badan dan BMI rendah kurang rentan mengalami DVT. c. Dari 104 pasien dengan DVT, 59 (36,7%) mengalami trombosis vena di
tungkai bawah, 34 (32,7%) di tungkai atas, 6 (5,8%) di tungkai atas dan tungkai bawah, 5 (4,8%) tidak dapat ditentukan.
d. Pada pasien dengan trombosis pada tungkai bawah, 35 (33,7%) mengalami
antikoagulan selama menunggu hasil tes diagnostik. Tujuan yang kedua adalah menentukan pasien yang dapat dieliminasi berdasarkan hasil tes DD yang negatif. Pada pasien yang dicurigai DVT, sistem penilaian Wells Score telah diterima dengan luas (Bounameaux, 2010).
Segal (2007) melakukan ulasan terhadap 36 penelitian utama dan 22 ulasan sistematis yang berhubungan dengan penggunaan tes probabilitas risiko tromboemboli. Bukti-bukti mendukung kuat penggunaan Wells Score sebagai tes probabilitas DVT atau Emboli Paru sebelum pasien melakukan pemeriksaan diagnostik lebih lanjut.
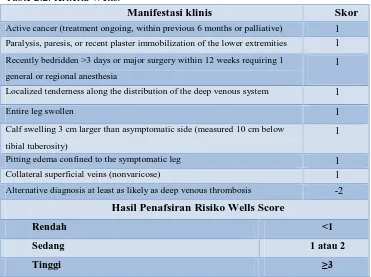
Table 2.2. Kriteria Wells.
Manifestasi klinis Skor
Active cancer (treatment ongoing, within previous 6 months or palliative) 1
Paralysis, paresis, or recent plaster immobilization of the lower extremities 1
Recently bedridden >3 days or major surgery within 12 weeks requiring 1
general or regional anesthesia
1
Localized tenderness along the distribution of the deep venous system 1
Entire leg swollen 1
Calf swelling 3 cm larger than asymptomatic side (measured 10 cm below
tibial tuberosity)
1
Pitting edema confined to the symptomatic leg 1
Collateral superficial veins (nonvaricose) 1
Alternative diagnosis at least as likely as deep venous thrombosis -2
Hasil Penafsiran Risiko Wells Score
Rendah <1
Sedang 1 atau 2
Tinggi ≥3
Menurut The Family Physicians Inquiries Network dari Priority Updates from the Research Literature dari (PURLs) (2007) terdapat beberapa sistem
penilain yang digunakan untuk memprediksi risiko DVT, namun Wells Score merupakan sistem skoring yang terbaik. Sejalan dengan PURLs, Institute for Clinical Systems Improvement (ICSI) (2006) merekomendasikan Wells Score
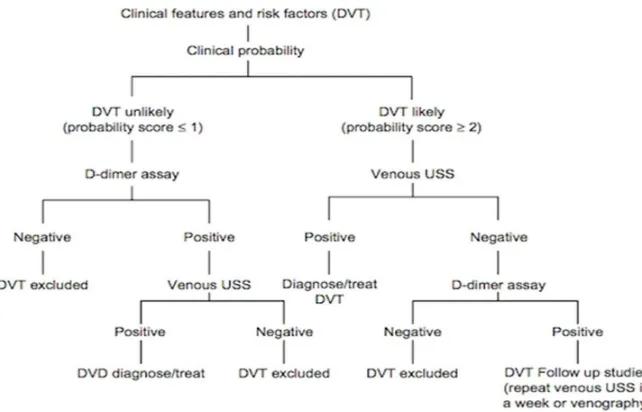
Dalam mendignosis Trombosis Vena Dalam, langkah pertama yang dilakukan adalah penilaian pretest probabilitas menggunakan model yang sudah lama dipakai dan valid seperti Wells Score. Jika skor 1 (risiko rendah), maka pemeriksaan selanjutnya adalah uji D-dimer. Jika tes negatif, sangkaan DVT disingkirkan dan pasien dapat pulang tanpa penyelidikan lebih lanjut. Jika tes positif, maka pasien diindikasikan USG vena. Jika hasil USG vena negatif, maka diagnosis DVT disingkirkan. Diagnosis DVT ditegakkan jika ultrasonografi vena positif (Kesieme, 2011).
Jika skor 2 atau lebih (risiko sedang dan tinggi), maka pemerikasaan dilanjutkan dengan ultrasonografi vena. Diagnosis DVT ditegakkan dan dirawat jika USG vena positif. Jika negatif, maka pemeriksaan D-dimer harus dilakukan. Jika hasil D-dimer negatif, maka pasien tidak termasuk diagnosis DVT, sementara hasil positif adalah indikasi untuk pemeriksaan lanjutan. Ulangi USG dalam 6-8 hari atau lakukan venografi. Algoritma ini tidak digunakan dalam kehamilan karena hasil D-dimer palsu tinggi untuk terjadi (Kesieme, 2011).
Gambar 2.7. Algoritma Diagnosis DVT