2016
Program Studi Pendidikan Kimia Universitas Sebelas Maret
ISSN 2503-4146 ISSN 2503-4154 (online)
140
BIOSORPSI ION SENG(II) OLEH SERBUK AKAR ECENG
GONDOK (
Eichhornia crassipes
) TERIMMOBILISASI PADA
KALSIUM ALGINAT
Puspita Ratri Wulandari
1*1Laboratorium Kimia Analitik, FMIPA, Universitas Gadjah Mada, Yogyakarta, Indonesia
*Keperluan korespondensi, email: puspitarw@gmail.com
Received: 17 June 2016 Accepted: December 1, 2016 Online Published: December 30, 2016
ABSTRAK
Telah dilakukan penelitian mengenai biosorpsi ion Seng(II) dengan menggunakan biosorben kalsium alginat terimmobilisasi serbuk eceng gondok. Penelitian ini diawali dengan preparasi dan karakterisasi biosorben dengan menggunakan FTIR. Parameter biosorpsi yang dipelajari meliputi massa biosorben, pH, waktu kontak dan konsentrasi awal ion Seng(II). Kadar ion Seng(II) dalam larutan diukur dengan menggunakan Spektroskopi Serapan Atom.Hasil penelitian menunjukkan bahwa biosorpsi ion Seng(II) optimum pada massa biosorben 2,01 g, pH larutan 5,5, konsentrasi awal ion Seng (II) 200 ppm dan waktu kontak 120 menit. Konstanta laju biosorpsi adalah sebesar 1,469 x 10-5 menit-1 dan mengikuti persamaan kinetika biosorpsi
pseudo orde satu. Kapasitas biosorpsi sebesar 34,88 mg/g. Biosorpsi ion Seng(II) mengikuti isoterm Langmuir dan melibatkan adsorpsi kimia (kemisorpsi) dengan energi adsorpsi sebesar 27,14 kJ.
Kata kunci: serbuk eceng gondok; kalsium alginat; Immobilisasi; Biosorpsi; Seng(II)
ABSTRACT
The research on biosorption Zinc (II) ion was done by using biosorbent calcium alginate powder immobilized hyacinth. The study started with the preparation and characterization of the biosorbent using FTIR. The parameters of biosorption were studied; mass of biosorbent, pH, contact time and initial concentration of zinc (II) ions. Concentration of zinc ion (II) in solution was measured using Atomic Absorption Spectroscopy. Results showed the ion biosorption Zinc (II) used biosorbent in the optimum mass of 2.01 g, pH 5.5, the initial concentration of zinc ions (II) of 200 ppm and a contact time of 120 minutes. Biosorption rate constant was 1.469 x 10-5 min-1 and followed the pseudo first order rate kinetics. The capacity of biosorption was found to be 34.88 mg/g. Biosorption of Zinc (II) ion also followed the Langmuir isotherm and it involved chemical adsorption (chemisorption) with the adsorption energy of 27.14 kJ
Keywords: powder hyacinth; calcium alginate; immobilization; biosorption; Zinc (II)
PENDAHULUAN
Pertumbuhan industri di Indonesia
yang melaju dengan cepat memberikan
dampak positif di bidang perekonomian. Di
sisi lain ternyata juga membawa pengaruh
negatif bagi kesehatan masyarakat. Dari
proses industri yang berlangsung dihasilkan
logam berat. Limbah logam berat antara
lain nikel, merkuri, krom, timbal, perak,
besi, seng, cadmium, dan sebagainya.
Sebagian besar logam berat
mem-bentuk garam yang terlarut dalam air dan
membentuk campuran yang sulit
dipisah-kan dengan metode pemisahan secara
fisik. Dikarenakan sulitnya membersihkan
lingkungan yang tercemar logam berat
tersebut, diperlukan kontrol pencemaran
ling-kungan dengan membatasi kandungan
maksimum logam berat sebelum dibuang
ke badan air.
Teknik adsorpsi sudah banyak di
lakukan dalam berbagai penelitian. Tren
pengembangan adsorben pada
tahun-tahun terakhir adalah pencarian adsorben
baru yang memanfaatkan bahan yang
bersifat limbah atau hasil samping suatu
produk[1]. Salah satu bahan yang
berpo-tensi sebagai adsorben adalah jaringan
tanaman. Metode adsorpsi dengan
meman-faatkan tanaman yang telah mati
(bio-massa) merupakan metode alternatif yang
tidak membutuhkan biaya besar dan efektif
untuk mengadsorp logam[2]. Dalam
pene-litian ini dilakukan eksperimen biosorpsi
pada logam Seng (II) dengan
meman-faatkan biomassa eceng gondok yag
terimmobilisasi pada Kalsium Alginat.
METODE PENELITIAN
Bahan
Bahan-bahan yang digunakan di
dalam penelitian ini adalah Natrium alginat,
CaCl2·2H2O, akar eceng gondok yang
dike-ringkan, larutan ion logam Seng(II), NaOH
penelitian ini adalah alat-alat gelas yang
umum digunakan, Spektrofotometer Infra
Merah Shimadzu FTIR 8201 PC,
Spekt-rofotometer Serapan Atom Perkin Elmer
3000, oven, pH meter, kertas saring
What-man 42, neraca digital ACIS AD 300H,
shaker, ayakan 150 mesh, dan magnetic stirer.
Prosedur Penelitian
Persiapan pembuatan biomassa serbuk eceng gondok
Tanaman eceng gondok dipisahkan
dari tanah dan dicuci. Bagian akar dan
daun dipisahkan dari batangnya dan
dikeringkan pada oven dengan suhu 90°C
hingga diperoleh berat konstan. Sampel
yang telah dikeringkan kemudian ditumbuk
sampai halus dan disaring dengan
meng-gunakan ayakan 150 mesh. Sampel dicuci
dengan menggunakan HCl 0,01 M dan
akuabides hingga netral. Sampel
dikeri-ngkan dengan oven pada suhu 50 - 60°C
sampai diperoleh berat konstan.
Immobilisasi serbuk eceng gondok pada kalsium alginat
Natrium alginat sebanyak 2 g
dila-rutkan dalam 0,1 L akuabides dan
ditam-bahkan 3 g serbuk akar eceng gondok ke
dalamnya. Akar tersebut kemudian dialirkan
ke dalam 500 mL larutan CaCl2·2H2O 0,1
M. Campuran tersebut kemudian diaduk
dengan menggunakan magnetic stirrer se-hingga gel kalsium alginat akan terbentuk
ketika larutan sudah stabil. Gel tersebut
ke-mudian dikeringkan dalam suhu kamar dan
Penyiapan larutan stok ion Seng(II) 1000 ppm dan buffer britton robinson untuk ion Seng(II)
Larutan stok ion Seng(II) 1000 ppm
dibuat dengan cara melarutkan 3,8665 g
Zn(NO3)2·3H2O ke dalam labu ukur 1000
mL, kemudian diencerkan dengan
akuab-ides sampai tanda batas.
Larutan CH3COOH sebanyak 2,3
mL, larutan H3PO4 2,7 mL dan 2,472 g
asam borat dilarutkan ke dalam akuabides
1 L. Selanjutnya ditambahkan sejumlah
la-rutan NaOH 2 M hingga diperoleh pH
dengan rentang 3 – 5,5.
Pengaruh massa biosorben terhadap biosorpsi ion Seng(II)
Larutan ion Seng(II) disiapkan
sebanyak 20 mL dengan konsentrasi 100
ppm. Ke dalam larutan tersebut
dima-sukkan biosorben dengan variasi jumlah
beads 10, 20, 20, 40, 50, 60, 70, 80, 90,
dan 100 beads. Campuran kemudian di
shaker selama 120 menit dan disaring dengan menggunakan kertas saring
What-man 42. Filtrat yang diperoleh diukur
absor-bansinya dengan menggunakan
Spektro-fotometer Serapan Atom.
Pengaruh pH larutan terhadap biosorpsi ion Seng(II)
Larutan ion Seng(II) disiapkan
de-ngan konsentrasi 100 ppm sebanyak 20
mL. Variasi pH yang digunakan untuk
ma-sing-masing larutan adalah 3; 3,5; 4; 4,5; 5;
5,5. Biosorben dengan massa opti-mum
di-masukkan ke dalam larutan terse-but.
Cam-puran kemudian dishaker selama 120 menit dan selanjutnya disaring dengan
menggu-nakan kertas saring Whatman 42. Filtrat
yang diperoleh diukur absorbansinya
de-ngan menggunakan Spektrofotometer
Se-rapan Atom.
Pengaruh waktu kontak terhadap biosorpsi ion Seng(II)
Larutan ion Seng(II) disiapkan
dengan konsentrasi 100 ppm sebanyak 20
mL pada pH optimum. Serbuk akar eceng
gondok terimmobilisasi pada kalsium
algi-nat dengan massa optimum dimasukkan ke
dalam larutan tersebut. Campuran
kemu-dian dishaker selama 30, 60, 90, 120, 150, dan 180 menit dan selanjutnya disaring
dengan menggunakan kertas saring
What-man 42. Filtrat yang diperoleh diukur
absor-bansinya dengan menggunakan
Spektro-fotometer Serapan Atom.
Pengaruh konsentrasi larutan terhadap biosorpsi ion Seng(II)
Larutan ion Seng(II) disiapkan
se-banyak 20 mL dengan variasi kon-sentrasi
50, 100, 200, 300, 400, dan 500 ppm pada
pH optimum. Serbuk akar eceng gondok
terimmobilisasi pada kalsium alginat
de-ngan massa optimum dimasukkan ke
da-lam larutan tersebut. Campuran kemudian
dishaker sesuai dengan waktu optimum
yang diperoleh sebelumnya. Campuran
tersebut disaring dengan meng-gunakan
kertas saring Whatman 42 untuk
selan-jutnya filtrat yang diperoleh diukur
absor-bansinya dengan menggunakan
Spektro-fotometer Serapan Atom.
HASIL PEMBAHASAN
Karakterisasi Gugus Fungsional Biosor-ben Serbuk akar eceng gondok
Perbandingan spektra inframerah
biosorben serbuk akar eceng gondok
bilisasi pada kalsium alginat disajikan pada
Gambar1
Gambar1. Spektra inframerah biosorben
serbuk akar eceng gondok
terimmobilisasi pada kalsium alginate
Spektra menunjukkan adanya
sera-pan di daerah 3448 cm-1, yang merupakan
vibrasi ulur gugus –OH. Serapan pada
bilangan gelombang 1635 cm-1
menun-jukkan keberadaan gugus –C=O. Selain itu, bilangan gelombang 1635 cm-1 juga dapat
diinterpretasikan sebagai keberadaan
vib-rasi tekuk N-H. Bilangan gelombang 2931
cm-1 diidentifikasi sebagai vibrasi C-H.
Pa-da spektra kalsium alginat juga ditun-jukkan
serapan di daerah 3487 cm-1, 1620 cm-1
dan 1419 cm-1 yang merupakan
kebe-radaan gugus –OH dan vibrasi ulur asi-metris COO-, vibrasi siasi-metris dari -COO
1.2 Immobilisasi Serbuk Akar Eceng Gondok pada Kalsium alginat
Teknik immobilisasi dilakukan
de-ngan mengalirkan campuran Natrium
Algi-nat dan serbuk akar eceng gondok ke
dalam larutan Kalsium Klorida. Proses
yang terjadi disebut dengan metode difusi,
dimana ion Ca2+ berdifusi dari reservoir luar
ke dalam alginat. Pengaturan difusi
dila-kukan melalui proses pembentukan gel
dengan kinetika reaksi yang cepat. Satu
tetes larutan natrium alginat akan
mem-bentuk satu bead dengan agen aktif yang terimmobilisasi di dalamnya.
.Spektra inframerah biosorben
ser-buk akar eceng gondok terimmobilisasi
pada kalsium alginat yang disajikan dalam
Gambar 1. Gambar 1 tampak mirip dengan
spektra infra merah serbuk akar eceng
gon-dok. Serapan yang melebar pada bila-ngan
gelombang 3425 cm-1 menunjukkan vibrasi
ulur gugus –OH. Keberadaan gugus COO-
ditunjukkan pada bilangan gelom-bang
1635 cm-1 dan vibrasi simetrisnya
ditu-njukkan pada serapan 1427 cm-1.Bilangan
gelom-bang ini juga dapat diinterpretasikan
sebagai keberadaan vibrasi tekuk N-H dari
serbuk eceng gondok.
Kajian Biosorpsi
Pengaruh massa biosorben
Lin dan Xing (2008) menyebutkan
bahwa permukaan akar tanaman dapat
mengadsorp ion Seng[3]. Selain berfungsi
untuk memperkuat berdirinya tubuh
tum-buhan, akar juga mampu menyerap air dan
unsur hara pada tanaman, serta juga
men-jadi tempat penyimpanan zat cadangan
makanan.
Akar tersusun oleh sel parenkim
hidup yang mengandung pati (Hartanto et al., 2005) yang mempunyai gugus –COOH
dan –OH sehingga memiliki kemampuan
yang baik untuk mengadsorp logam[4]. Hal
ini dapat dilihat dalam grafik pengujian
terhadap akar dan daun dalam mengadsorp
ion logam Seng(II) yang ditunjukkan pada
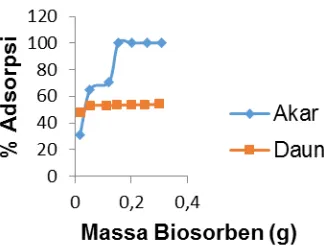
Gambar 2. Grafik pengujian terhadap akar dan daun dalam mengadsorp ion logam Seng(II)
Gambar 3. nilai persen adsorpsi dengan menggunakan serbuk akar eceng gondok
Hasil penelitian menunjukkan nilai
persen adsorpsi dengan menggunakan
ser-buk akar eceng gondok lebih baik jika
di-bandingkan dengan menggunakan daun.
Untuk komposisi kalsium alginat dengan
serbuk akar eceng gondok digunakan
per-bandingan 2 : 3. kalsium alginat yang
digu-nakan sebanyak 2 g sedangkan akar eceng
gondok yang diimmobilisasikan sebesar 3
g. Massa akar eceng gondok dibuat lebih
besar dari kalsium alginat, agar cukup
ba-nyak serbuk yang terperangkap ke dalam
beads kalsium alginat, sehingga jumlah si-tus aktif semakin banyak.
Dalam penelitian ini dilakukan
var-iasi jumlah beads biosorben terhadap
ad-sorbat. Variasi jumlah beads biosorben disajikan dalam Tabel 1. Dibawah
Tabel 1. Variasi jumlah beads biosorben
Gambar 4. Pengaruh variasi massa biosorben terhadap adsorpsi larutan ion Seng(II)
Gambar 4 menunjukkan pengaruh
variasi massa biosorben terhadap adsorpsi
larutan ion Seng(II). Pada massa 0 – 1,65 g biosorben terus terjadi peningkatan
adsor-psi ion logam Seng(II). Kenaikan massa
biosorben menyebabkan meningkatnya
gu-gus-gugus aktif dalam biosorben.
Akibat-nya, interaksi ion Seng(II) dengan gugus
aktif semakin besar, sehingga nilai persen
adsorpsi akan meningkat. Menurut Baroroh
(2008) eceng gondok mengandung
selu-losa yang kaya akan gugus –OH dan COO-
, sehingga dapat berinteraksi dengan
kom-ponen adsorbat. Selain itu ion logam
Seng(II) dapat berinteraksi dengan gugus
COO- dan –OH yang terdapat dalam algi-nat. Pada variasi massa diatas 2,01 g,
No. Jumlah Beads
Massa Biosorben(g)
1 10 0,49
2 20 0,81
3 30 1,28
4 40 1,65
5 50 2,01
6 60 2,4
7 70 2,83
8 80 3,23
9 90 3,62
kenaikan adsorpsi ion logam Seng(II) tidak
terlalu signifikan, bahkan cenderung tetap.
Hal ini disebabkan situs aktif biosorben
telah jenuh terhadap ion Seng(II).[5]
2.2 Pengaruh pH
Volesky (1990) mengemukakan
bahwa proses adsorpsi logam berat dengan
menggunakan biosorben sangat
bergan-tung dengan pH [6]. Hal ini dikarenakan pH
dapat mempengaruhi kelarutan ion logam
dalam larutan, kemampuan ion logam
untuk terikat pada permukaan biomassa
dan mempengaruhi muatan pada
permu-kaan biomassa selama reaksi berlangsung.
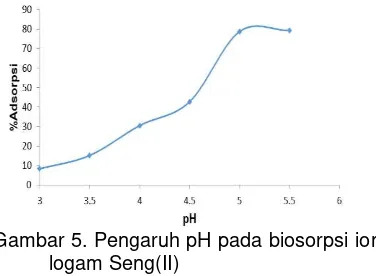
Gambar 5. Pengaruh pH pada biosorpsi ion logam Seng(II)
Pada bagian ini dipelajari pengaruh
pH larutan terhadap jumlah ion Seng(II)
yang teradsorp oleh biosorben Kalsium
alginat terimmobilisasi serbuk akar eceng
gondok. Variasi pH diambil pada rentang
3,0 – 5,5. Hal ini dikarenakan larutan ion Seng(II) dalam kondisi basa lemah akan
membentuk endapan hidroksida Zn(OH)2
(Resa, 2004)7]. Grafik pengaruh pH
disajikan dalam Gambar 5.
Pada Gambar 5 terlihat bahwa
bio-sorpsi ion logam Seng(II) mengalami
kenai-kan seiring dengan kenaikenai-kan pH. Pada pH
3 adsorpsi ion logam Seng(II) masih
ren-dah. Hal ini dikarenakan pada kondisi asam
terjadi peningkatan ion hidrogen (H+).
Aki-batnya terjadi kompetisi antara ion logam
logam Seng(II) dengan ion H+. Akibatnya
terjadi kompetisi ion logam dalam Seng(II)
dalam larutan.
Adsorpsi ion logam Seng(II) terus
meningkat seiring dengan kenaikan pH.
Pada pH yang relatif tinggi sisi aktif
bio-sorben akan bermuatan negatif, sehingga
memudahkan proses biosorpsi, namun
pada kondisi pH yang semakin tinggi akan
terjadi proses hidrolisis membentuk
kom-pleks hidrokso logam yang kemudian diikuti
dengan pengendapan hidroksida logam.
Akibatnya kenaikan adsorpsi logam pada
pH 5,5 tidak terlalu signifikan
2.3 Pengaruh waktu kontak dan kinetika biosorpsi
Pengaruh waktu kontak biosorpsi
ion logam Seng(II) dengan menggunakan
serbuk akar eceng gondok terimmobilisasi
pada kalsium alginat dilakukan pada
rentang waktu 30 – 180 menit. Hasil penga-matan disajikan pada Gambar 6
Gambar 6. Pengaruh waktu kontak bio-sorpsi ion logam Seng(II) dengan menggunakan serbuk akar eceng gondok terimmobilisasi pada kalsium alginat
Adsorpsi ion Seng(II) terus
menga-lami peningkatan pada rentang waktu 0-120
menit. Semakin lama waktu interaksi,
se-makin banyak situs aktif biosorben yang
ter-capai kesetimbangan adsorpsi, dimana
ad-sorben sudah jenuh terhadap ion logam
sehingga penambahan waktu kontak tidak
lagi menambah persen adsorpsi ion logam.
Hasil penelitian menunjukkan waktu
opti-mum penyerapan terjadi pada 120 menit.
Dalam kondisi tersebut biosorben mampu
mengadsorp ion Seng(II) sebesar 39,22
mg/g (76,92 %)
Srivastava (2006) menyebutkan
bahwa model kinetika adsorpsi yang biasa
digunakan adalah model pseudo orde
pertama atau pseudo orde kedua.[8] Untuk
mengetahui model kinetika biosorpsi ion
Seng(II) dengan menggunakan biosorben
serbuk akar eceng gondok terimmobilisasi
pada kalsium alginat, ditentukan dengan
membandingkan R2 dari orde satu, orde
dua, pseudo orde satu dan pseudo orde
dua yang ditunjukkan pada Tabel 2.
Tabel 2. model kinetika biosorpsi ion Seng(II) dengan menggunakan bio-sorben
Dari data tersebut, R2 terbesar
diperoleh untuk pseudo orde satu, dengan
nilai R2 sebesar 0,939. Hal tersebut
me-nunjukkan adanya laju pengurangan
reak-tan [H2O] dan [H+]. Namun dikarenakan
jumlahnya yang berlebih, maka laju
pengu-rangan kedua reaktan tersebut diabaikan.
2.4 Pengaruh konsentrasi awal ion Seng(II) dan isoterm biosorpsi
Pada bagian ini akan dikaji
besar-nya kapasitas biosorpsi, konstanta
kesetim-bangan dan energi biosorpsi yang diperoleh
berdasarkan model isoterm adso-rpsi
Lang-muir dan Freundlich. Pengaruh konsentrasi
awal ion Seng(II) dilakukan pada rentang
konsentrasi 0 ppm sampai 500 ppm pada
pH 5,5 dengan waktu adsorpsi 120 menit.
Gambar 6 menunjukkan bahwa
pada konsentrasi awal 0 – 200 ppm terjadi kenaikan qe. Hal tersebut menunjukkan
se-makin besar konsentrasi awal ion Seng(II),
semakin besar pula ion yang teradsorp.
Pada kondisi tersebut, situs aktif biosorben
masih mampu mengadsorp ion logam
dalam larutan. Pada konsentrasi lebih dari
200 ppm, qe mulai konstan. Besarnya
ad-sorpsi yang tidak signifikan ini disebabkan
oleh situs aktif biosorben telah jenuh
beri-katan dengan ion logam Seng(II).
Suardana (2008) menyebutkan
bahwa pengujian pola isoterm adsorpsi
Fre-undlich dilakukan dengan pembuatan kurva
log (x/m) terhadap log c.[9] Seda-ngkan
pengujian pola isoterm adsorpsi Langmuir
dilakukan dengan pembuatan kurva c/(x/m)
terhadap c. Pola adsorpsi ditentukan
de-ngan cara membandingkan tingkat
kelinier-an kurva ykelinier-ang ditunjukkkelinier-an oleh harga R2.
Model isoterm Langmuir mengacu
kepada pembentukan monolayer pada
per-mukaan biosorben, sedangkan Freun-dlich
mengasumsikan pembentukan kom-pleks
multilayer sehingga biosorpsi tidak hanya
terjadi pada satu permukaan
Biosorpsi ion Seng(II) dengan
me-nggunakan serbuk akar eceng gondok
ter-immobilisasi pada kalsium alginat,
ber-dasarkan data di Tabel 3 koefisien regresi
linier (R2) untuk model isoterm Langmuir
besarnya mendekati satu. Dengan
demi-kian dapat disimpulkan adsorpsi yang
terjadi hanya pada satu lapisan di
permu-kaan saja (monolayer). Hal tersebut sesuai
dengan penelitian Wang (2010) yang
menyebutkan bahwa biosorpsi logam berat
dengan menggunakan eceng gondok
me-ngikuti pola isoterm Langmuir[10].
Dari hasil perhitungan diperoleh
kapasitas biosorpsi ion Seng(II) dengan
menggunakan biosorben Kalsium alginat
terimmobilisasi serbuk akar eceng gondok
sebesar 38,46 mg/g. Wuyep (2007)
mela-kukan penelitian menggunakan Kalsium
alginat tanpa immobilisasi untuk
mengad-sorp logam Cr, Mn, Cu, Ni, dan Pb.
Kapa-sitas biosorpsi rata-rata yang dipe-roleh
sebesar 2,05 mg/g[11] Dibandingkan
de-ngan penelitian sebelumnya, Kalsium
algi-nat yang terimmobilisasi serbuk eceng
gon-dok mengalami peningkatan kemam-puan
mengadsorp logam berat.
Adamson (1990) mengemukakan
bahwa suatu adsorpsi dikatakan sebagai
kemisorpsi (adsorpsi kimia) jika memiliki
energi adsorpsi minimal 20,92 kJ/mol.
Energi adsorpsi dibawah 20,92kJ/mol
dise-but fisisorpsi (adsorpsi fisika)[12]. Nilai
energi adsorpsi ini menggambarkan
sebe-rapa kuat ikatan ion logam dengan situs
aktif adsorben atau dapat juga diartikan
sebagai nilai energi yang digunakan untuk
mengadsorp per mol adsorbat dengan
menggunakan adsorben.
Kemisorpsi terjadi diawali dengan
adsorpsi fisik, yaitu partikel-partikel
adso-rbat mendekat ke permukaan adsorben
melalui gaya van der Waals atau melalui
ikatan hidrogen. Kemudian diikuti oleh
ad-sorpsi kimia yang terjadi setelah adad-sorpsi
fisika.
Dari hasil penelitian diperoleh
energi biosorpsi ion Seng(II) dengan
me-nggunakan Kalsium alginat terimmobilisasi
serbuk eceng gondok sebesar 27,14
kJ/mol, sehingga energi biosorpsi dalam
penelitian ini digolongkan sebagai
kemi-sorpsi.
KESIMPULAN
Serbuk akar eceng gondok memiliki
kemampuan mengadsorp ion logam Seng
(II) lebih besar jika dibandingkan dengan
serbuk daun eceng gondok. Biosorpsi ion
logam Seng(II) dengan menggunakan
bios-orben serbuk akar eceng gondok
ter-immo-bilisasi pada kalsium alginat berlangsung
optimum pada kondisi pH 5,5, waktu kontak
120 menit, konsentrasi awal ion lo-gam 200
ppm, dan berat biosorben 2,01 g. Biosorpsi
ion logam Seng(II) dengan menggunakan
serbuk akar eceng gondok yang
diimmo-bilisasikan pada kalsium alginat mengikuti
pola laju reaksi pseudo orde satu dengan
konstanta laju reaksi sebesar 1,469 x 10-5
menit-1. Biosorpsi ion logam Seng(II)
de-ngan menggunakan serbuk akar eceng
gondok yang diimmobilisasikan pada
kal-sium alginat mengikuti pola isoterm
Lang-muir dengan kapasitas adsorpsi sebesar
34,588 mg/g. Proses adsorpsi diduga
meli-batkan adsorpsi kimia (kemisorpsi) dengan
energi adsorpsi sebesar 27,14
DAFTAR RUJUKAN
[1] Han, J.S., 1999, Stormwater
Filtration of Toxic Heavy Metal Ions
Using Lignocellulosis Material
Selection Process, Fiberization,
Chemical Modification and Mat
Inter-regional Conference on Environmental-Water.
[2] Gamez, G., Doken, K., Tieman, J
dan Herrera, I.,1999, Spectroscopy Studies of Gold (III) Binding to Alfafa Biomass, Proceeding of The 1999 Conference of Hazardous Waste Research, pp 78 -79.
[3] Lin, D.H., dan Xing, B.S., 2008, Root Uptake and Phototoxicity of ZnO Nanoparticles, J. Environ. Tech,, 42 (15), 5580-5585.
[4] Hartanto, N., Purnomo, dan
Sumardi, I., 2006, Struktur dan Perkembangan Tumbuhan, Penebar Swadaya, Jakarta
[5] Baroroh, H., 2008, Adsorpsi Biomassa Eceng Gondok, Skripsi, Universitas Islam Negeri (UIN) Malang.
[6] Volesky, B., 1990, Biosorption of Heavy Metals, CRC Boston.
[7] Shrivastava, V.C., Mall, I.D., dan Mishra, I.M., 2006, Characterization of mesoporus rice husk ash (RHA) andadsorption kinetics of metal ions
from aqueous solution onto RHA, J. Hazard, 134, 257-267.
[8] Resa, I., Carmona, E., Gutierrez-Puebla, E., and Monge,. A., 2004,
Decamethyldizincocene, a stable
compound of Zn ( II) with a Zn-Zn Bond,J.Science, 305, 1136-1138.
[9] Suardana, I.N., 2008, Optimalisasi Daya Adsorpsi Zeolit Terhadap Ion Kromium, J. Pen. & Peng Sains Humaniora, 2, 1, 17-33.
[10] Wang, G., Fuerstenau, M.C., dan Smith, R.W., 2010, Sorption of Heavy Metals onto Nonliving Water Hyacinth
Roots, Mineral Processing and
Extractive Metallurgy Review An International Journal, 19, 1, 309-322.
[11] Wuyep, P.A., Chuma, A.G., Awodi, S., dan Nok, A.J., 2007, Biosorption of Cr, Mn, Fe, Ni, Cu, and Pb metals from petroleum refinery effluent by calcium
alginate immobilized mycelia of
Polyporus Squamosus, Scientific Research and Essay, 2, 7, 217-221.
[12] Adamson. A. W., 1990, Physical
Chemistry of Surface, 5th ed. John