K
ebutuhan kedelai nasional hingga
kini belum dapat dipenuhi dari
produksi dalam negeri, sehingga impor
kedelai tidak bisa terelakkan. Untuk
produksi kedelai, terutama dengan
memanfaatkan lahan masam yang luasnya
mencapai 101.519 juta hektar di seluruh
Indonesia (Notohadiprawiro 1983).
masaman tanah rendah, keracunan Al,
kekahatan hara seperti N, P, K, Ca, Mg,
dan Mo, serta kekurangaktifan mikroba
tanah. Keracunan Al ditandai dengan
PENINGKATAN KETAHANAN TANAMAN
KEDELAI TERHADAP ALUMINIUM
MELALUI KULTUR IN VITRO
Ika Mariska
1, E. Sjamsudin
2, D. Sopandie
2, S. Hutami
1, A. Husni
1, M. Kosmiatin
1, dan A. Vivi N
11Balai Besar Penelitian dan Pengembangan Bioteknologi dan Sumberdaya Genetik Pertanian,
Jalan Tentara Pelajar No. 3A, Bogor 16111
2Jurusan Budi Daya Pertanian, Institut Pertanian Bogor, Kampus Darmaga, Bogor 16680
ABSTRAK
Salah satu upaya untuk memenuhi kebutuhan kedelai nasional adalah dengan melakukan ekstensifikasi penanaman ke lahan marginal, antara lain lahan masam yang tersedia cukup luas di Indonesia. Namun, pertanaman kedelai di lahan masam umumnya menghadapi masalah keracunan Al dan pH rendah, sehingga untuk mengatasinya diperlukan kultivar yang toleran. Sampai saat ini, sumber ketahanan terhadap Al pada kedelai masih terbatas. Metode seleksi
in vitro merupakan suatu cara yang dapat ditempuh untuk mendapatkan kultivar kedelai yang toleran terhadap Al
dan pH rendah. Sebelum dilakukan seleksi in vitro, metode regenerasi kedelai perlu dikuasai terlebih dahulu. Penelitian pada 10 varietas kedelai menunjukkan adanya perbedaan kemampuan beregenerasi melalui jalur embriogenesis somatik pada varietas tersebut. Lima varietas memperlihatkan sifat lebih embriogenik dibanding yang lain, yaitu Bromo, Wilis, Tambora, Black Manchu, dan Argomulyo. Seleksi in vitro dilakukan pada embriozigotik muda dari tiga varietas, yaitu Wilis, Sindoro, dan Slamet yang telah diradiasi untuk meningkatkan keragaman. Seleksi dilakukan pada taraf Al 0, 100, 200, 300, 400, dan 500 ppm dengan pH media 4. Dari hasil seleksi ini diperoleh 12 tanaman yang diduga toleran. Setelah dilakukan pengujian di kamar kaca, diperoleh dua genotipe yang potensial. Karena keterbatasan dana dan lahan, hanya satu genotipe yang diuji lebih lanjut, yaitu Sindoro Radiasi Al-100. Pengujian di empat lokasi pada empat generasi menunjukkan adanya potensi yang besar untuk mendapatkan galur-galur harapan kedelai yang toleran terhadap Al dan pH rendah.
Kata kunci: Kedelai, keracunan aluminium, pH tanah, kultur in vitro, embriogenesis somatik
ABSTRACT
Increasing aluminum tolerance of soybean plant through in vitro culture
One effort to increase soybean productivity is by using marginal land for soybean plantation. The marginal land that can be used is acid soil, but the problems are Al toxicity and low pH. To cope with these problems, cultivars having tolerance to Al toxicity and low pH are needed. To create this cultivar, a breeder needs a wide range of variance. Because the variance for this character is limited, in vitro selection was used. Before the selection, the regeneration method must be held. The research using 10 soybean cultivars showed that there were different abilities of regeneration through somatic embryogenesis in each cultivar. Five cultivars (Bromo, Wilis, Tambora, Black Manchu, and Argomulyo) were more embryogenic than others. In vitro selection was conducted using young embryozygotic of Wilis, Slamet, and Sindoro that have already been radiated to increase variance. Selection was conducted using Al dosage 0, 100, 200, 300, 400, and 500 ppm and pH 4. From this selection, 12 plants were obtained. After greenhouse testing, two genotypes were considered as potential ones, but because of the limited fund and land only one genotype that was further tested in the field, which was Sindoro radiated Al-100. The result of field testing in four locations and four generations showed that there is a hope to obtain potential lines that can be released as cultivar tolerant to Al and low pH.
Varietas kedelai yang digunakan petani
umumnya hanya sesuai pada pH tanah
yang cukup tinggi (± 6) dan peka terhadap
kandungan Al yang tinggi. Oleh karena
itu, untuk mengembangkan tanaman
kedelai di lahan masam diperlukan
varietas yang toleran terhadap pH rendah
dan Al tinggi.
Sumber ketahanan terhadap Al pada
kedelai sampai saat ini sangat terbatas,
sehingga perbaikan untuk karakter
tersebut dilakukan melalui metode seleksi
in vitro. Metode ini telah digunakan
untuk meningkatkan sifat resistensi
pada beberapa jenis tanaman, baik
ter-hadap cekaman biotik maupun abiotik
(Stavarek dan Rains 1984; Ahloowalia
1986). Seleksi in vitro untuk meningkatkan
ketahanan sel terhadap Al telah
di-lakukan pada tomat dan kentang (Stavarek
dan Rains 1984) serta sorgum (Smith et
al. 1983). Dalam melakukan seleksi in
vitro diperlukan metode regenerasi
dengan tingkat keberhasilan yang cukup
tinggi.
Tanaman hasil regenerasi, setelah
diseleksi secara in vitro, selanjutnya diuji
di lapangan untuk melihat penampilan
tanaman pada kondisi nyata di lapangan.
Dari beberapa metode penapisan pada
alfalfa, Dali’ Agnol et al. (1996)
menyimpulkan bahwa pengujian di lahan
masam dengan kandungan Al tinggi
merupakan metode yang paling efektif
untuk mendapatkan kultivar toleran. Oleh
karena itu, keturunan dari
tanaman-tanaman hasil seleksi in vitro perlu diuji
di lahan masam pada beberapa generasi
untuk mengetahui ketahanannya di
lapang dan juga segregasinya.
EMBRIOGENESIS SOMATIK
PADA BEBERAPA VARIETAS
KEDELAI
Metode embriogenesis somatik pada
kedelai telah dihasilkan oleh Mariska et
al. (2001a). Dari 10 varietas yang diteliti,
lima varietas (Bromo, Wilis, Tambora, Black
Manchu, dan Argomulyo) menunjukkan
sifat lebih embriogenik dibanding yang
lain. Formulasi media yang efektif dalam
menginduksi regenerasi melalui jalur
embriogenesis somatik juga telah
di-peroleh, yaitu MS + 2,4-D 40 mg/l +
beberapa asam amino.
Jumlah rata-rata embrio somatik
yang terbentuk berkisar antara 0
−
5,40
(Tabel 1). Jumlah embrio bipolar terbanyak
dihasilkan oleh varietas Wilis yang
dikulturkan pada media MS + 2,4-D 40
mg/l + 3 asam amino, diikuti oleh varietas
Bromo pada perlakuan media MS + 2,4-D
40 mg/l + sukrosa 6% (4,50). Sepuluh
minggu setelah dikulturkan pada media
yang sama, embrio somatik berproliferasi
dengan cepat.
SELEKSI MASSA SEL
EMBRIOGENIK PADA
KONDISI Al BERBEDA
DAN pH RENDAH
Masalah yang sering dihadapi dalam
seleksi in vitro adalah sulit
beregene-rasinya massa sel toleran Al dan pH
rendah. Penelitian regenerasi massa sel
embriogenik setelah diseleksi pada
kondisi Al berbeda dan pH rendah telah
dilakukan di Balai Besar Penelitian dan
Pengembangan Bioteknologi dan
Sumber-daya Genetik Pertanian, Bogor, dengan
menggunakan embriozigotik muda dari
varietas yang dapat beregenerasi melalui
jalur embriogenesis somatik, yaitu Wilis.
Dua varietas yang toleran terhadap
kemasaman tanah, yaitu Sindoro dan
Slamet, digunakan sebagai pembanding
(Sopandie et al. 1996; Jusuf et al. 1999;
Mariska et al. 1999; Mariska et al. 2001b).
Embriozigotik muda diisolasi dari polong
muda 12–20 hari setelah penyerbukan.
Sebelum ditanam, embriozigotik diradiasi
dengan sinar gamma dosis 0 dan 400 rad
untuk meningkatkan keragaman.
Setelah diradiasi, embriozigotik
muda dikulturkan pada media semisolid
MS dengan vitamin B5, dan diperkaya
dengan zat pengatur tumbuh 2,4-D
konsentrasi tinggi serta dikombinasi
dengan beberapa asam amino, sukrosa,
dan gel rite sebagai pemadat. Metode
yang digunakan untuk induksi kalus
embriogenik mengacu pada hasil
pe-nelitian Mariska et al. (1999).
Seleksi massa sel embriogenik
dilakukan dengan mengkulturkan massa
sel pada media seleksi dengan tahapan
yang berbeda. Seleksi dilakukan pada
media yang sama dengan media induksi
kalus dengan penambahan AlCl
3.6H
2O (0,
100, 300, 400, dan 500 ppm) pada pH 4.
Untuk memunculkan sifat toksisitas Al
dan mutan-mutan baru, media MS
dimodifikasi dengan menggunakan
NH
4NO
32.400 mg/l, CaCl
2.2H
2O 15 mg/l,
KH
2PO
413 mg/l, dan FeSO
4.7H
2O 28 mg/l
yang tidak dikelat oleh EDTA.
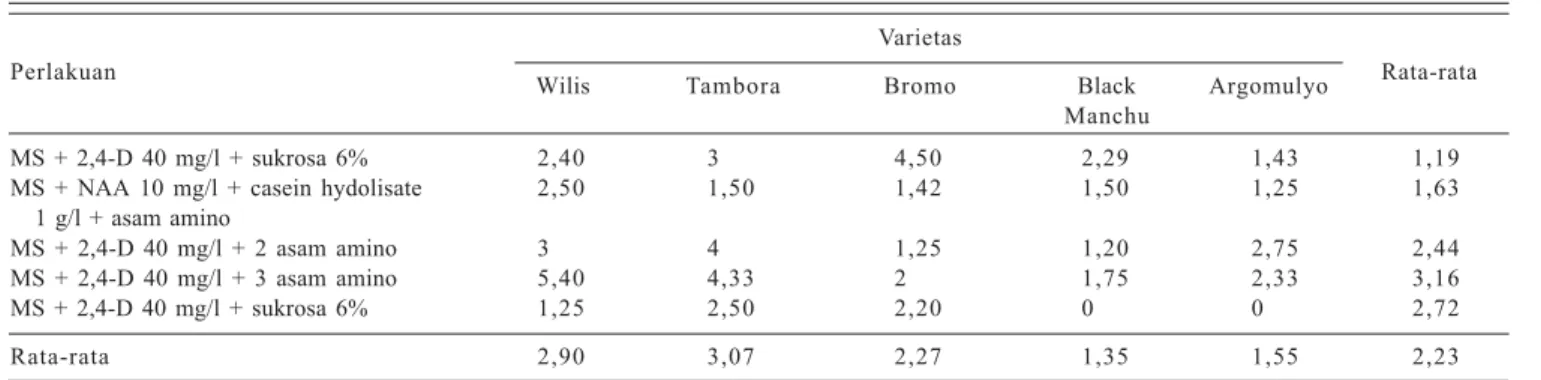
Tabel 1. Jumlah rata-rata struktur embrio somatik (globular, torpedo) pada lima varietas kedelai 10 hari setelah
dikulturkan.
Perlakuan
Varietas
Rata-rata Wilis Tambora Bromo Black Argomulyo
Manchu
MS + 2,4-D 40 mg/l + sukrosa 6% 2,40 3 4,50 2,29 1,43 1,19 MS + NAA 10 mg/l + casein hydolisate 2,50 1,50 1,42 1,50 1,25 1,63 1 g/l + asam amino
MS + 2,4-D 40 mg/l + 2 asam amino 3 4 1,25 1,20 2,75 2,44 MS + 2,4-D 40 mg/l + 3 asam amino 5,40 4,33 2 1,75 2,33 3,16 MS + 2,4-D 40 mg/l + sukrosa 6% 1,25 2,50 2,20 0 0 2,72 Rata-rata 2,90 3,07 2,27 1,35 1,55 2,23 Sumber: Mariska et al. (2001a).
Benih somatik yang berhasil
di-regenerasikan dari sel yang toleran Al dan
pH rendah kemudian diaklimatisasi atau
diperbanyak secara in vitro untuk
kegiatan selanjutnya. Tahapan seleksi
sampai pengujian benih somatik yang
berasal dari seleksi in vitro dapat dilihat
pada Gambar 1.
Jumlah benih somatik pada media
perkecambahan setelah diseleksi dengan
Al dan pH rendah berbeda untuk setiap
varietas, karena tidak semua struktur
torpedo dapat berkembang membentuk
benih somatik (Tabel 2). Meningkatnya
konsentrasi Al akan menurunkan jumlah
benih somatik. Hal ini sesuai dengan hasil
penelitian seleksi in vitro pada padi (Van
Sin Jan et al. 1997) yang menunjukkan
penurunan kemampuan beregenerasi
melalui jalur embriogenesis somatik
sejalan dengan meningkatnya konsentrasi
Al. Varietas Wilis yang diradiasi tetap
dapat menghasilkan benih somatik paling
banyak (72) dibanding varietas lainnya.
Pada varietas Sindoro dan Slamet, jumlah
embrio somatik cenderung menurun
setelah diradiasi, sedangkan pada Wilis
embrio somatik terbentuk lebih banyak
setelah diradiasi daripada kontrol.
Penampilan embrio somatik dewasa dari
ketiga varietas tersebut dapat dilihat pada
Gambar 2.
Dari hasil seleksi in vitro diperoleh
39 benih somatik yang telah diaklimatisasi
(Tabel 3). Dari penampakan visual biakan
terlihat bahwa benih somatik Slamet tidak
tumbuh secara normal, sehingga untuk
varietas Slamet belum ada benih somatik
yang dapat diaklimatisasi. Dari 39 benih
somatik tersebut, hanya 12 yang dapat
tumbuh sampai berproduksi, sedangkan
sisanya mati sebelum berbunga.
Berdasarkan hasil penelitian, masalah
yang ditemukan dalam regenerasi melalui
jalur embriogenesis somatik pada
tanam-an kedelai adalah pembentuktanam-an benih
somatik yang tidak normal dan
ke-berhasilan yang rendah dalam tahap
aklimatisasi. Semua tanaman yang tumbuh
di rumah kaca menunjukkan keragaman
yang tinggi baik pada fase vegetatif
maupun generatif. Biji yang dihasilkan
dari 12 tanaman tersebut perlu diuji kembali
pada lahan masam. Penampilan tanaman
hasil aklimatisasi dapat dilihat pada
Gambar 3.
PENGUJIAN DI LAHAN
MASAM
Biji kedelai yang dihasilkan oleh tanaman
hasil seleksi in vitro kemudian ditanam di
kamar kaca dengan menggunakan tanah
masam yang diambil dari Gajrug, Banten
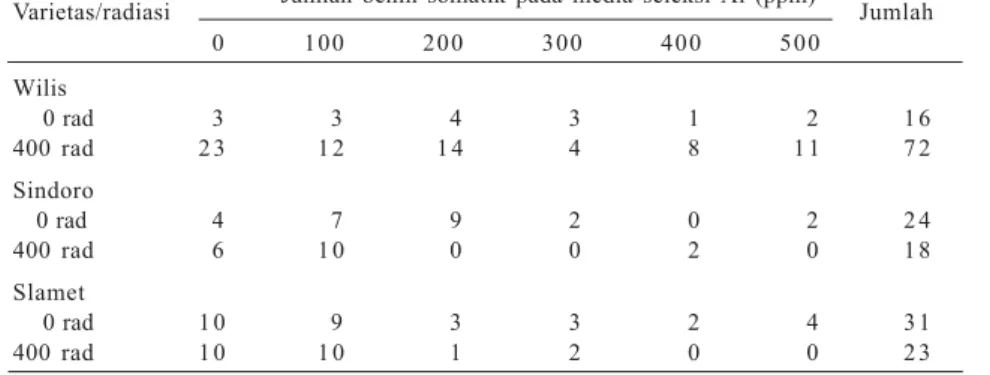
Tabel 2. Jumlah benih somatik kedelai pada media perkecambahan setelah
diseleksi dengan Al dan pH rendah.
Varietas/radiasi Jumlah benih somatik pada media seleksi Al (ppm) Jumlah 0 100 200 300 400 500 Wilis 0 rad 3 3 4 3 1 2 1 6 400 rad 2 3 1 2 1 4 4 8 1 1 7 2 Sindoro 0 rad 4 7 9 2 0 2 2 4 400 rad 6 1 0 0 0 2 0 1 8 Slamet 0 rad 1 0 9 3 3 2 4 3 1 400 rad 1 0 1 0 1 2 0 0 2 3 Sumber: Mariska et al. (2002).
Regenerasi Eksplan
Kalus
embriogenik Kalus embriosomatikhasil seleksi
Produksi kalus
Seleksi
tahap I Pendewasaan Perkecambahan Aklimatisasi tahap ISeleksi Produksibiji Tanaman
hasil seleksi Biji Benih
somatik
1 bulan
pada
media induksi kalus = MI
1,50 bulan pada media seleksi MI + A1 1 bulan pada media MI 1,50 bulan pada
media regenerasi MII 1,50 bulan
pada media seleksi 1 bulan pada media cair 2 − 3 bulan pada media tanah
Gambar 2.
Embriosomatik dewasa kedelai pada media perkecambahan setelah
diseleksi dengan Al-100 ppm (Sindoro dan Slamet) serta Al-500 ppm
(Wilis).
Gambar 3.
Penampilan tanaman kedelai hasil aklimatisasi, (A) Wilis radiasi
Al-500 dan (B) Sindoro radiasi Al-100.
(Mariska 2002a). Pengujian dibagi menjadi
dua seri karena keterbatasan biaya dan
tenaga. Pada seri pertama diuji tiga
genotipe, yaitu Wilis radiasi Al-300 (A),
Sindoro radiasi Al-100 (H), dan Sindoro
radiasi pH 4 (I). Ketiga genotipe ini dipilih
karena ketiganya memiliki jumlah polong
yang cukup banyak (< 30 buah) dan hanya
sedikit menghasilkan polong berbiji satu.
Pada percobaan seri pertama digunakan
tanah yang memiliki pH 4,80, Aldd 11,57
me, dan kejenuhan Al 57%. Pada seri kedua
ditanam sembilan genotipe yang tersisa.
Tanah yang digunakan pada seri kedua
memiliki pH 4,32, Aldd 13,32 me, dan
kejenuhan Al 81% (Mariska 2002b).
Dari hasil pengujian di rumah kaca
terpilih genotipe Sindoro radiasi Al-100 (H)
pada pengujian seri pertama dan Wilis
radiasi Al-500 (E) pada pengujian seri
kedua. Pemilihan kedua genotipe tersebut
didasarkan pada penampilan visual dan
potensi hasil yang lebih baik dibanding
varietas asalnya, yaitu Sindoro dan Wilis.
Karena keterbatasan dana dan lahan,
hanya genotipe Sindoro radiasi Al-100 (H)
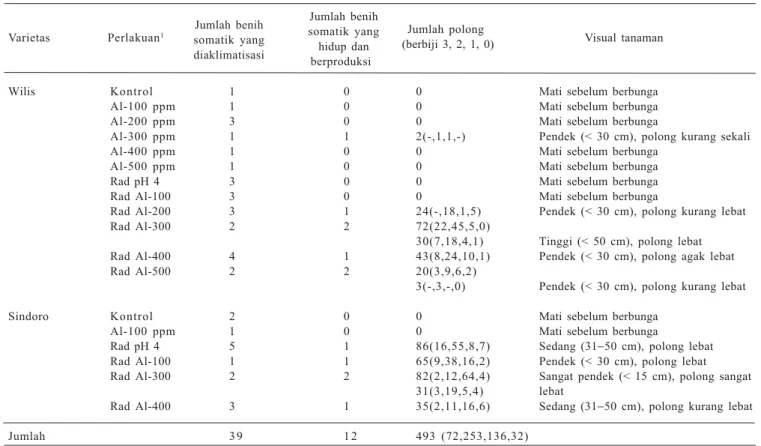
Tabel 3. Aklimatisasi benih somatik kedelai dan produksi polong dari nomor-nomor baru hasil seleksi in vitro.
Varietas Perlakuan1 Jumlah benih
Jumlah benih
Jumlah polong
Visual tanaman somatik yang somatik yang (berbiji 3, 2, 1, 0)
diaklimatisasi berproduksihidup dan
Wilis Kontrol 1 0 0 Mati sebelum berbunga Al-100 ppm 1 0 0 Mati sebelum berbunga Al-200 ppm 3 0 0 Mati sebelum berbunga
Al-300 ppm 1 1 2(-,1,1,-) Pendek (< 30 cm), polong kurang sekali Al-400 ppm 1 0 0 Mati sebelum berbunga
Al-500 ppm 1 0 0 Mati sebelum berbunga Rad pH 4 3 0 0 Mati sebelum berbunga Rad Al-100 3 0 0 Mati sebelum berbunga
Rad Al-200 3 1 24(-,18,1,5) Pendek (< 30 cm), polong kurang lebat Rad Al-300 2 2 72(22,45,5,0)
30(7,18,4,1) Tinggi (< 50 cm), polong lebat Rad Al-400 4 1 43(8,24,10,1) Pendek (< 30 cm), polong agak lebat Rad Al-500 2 2 20(3,9,6,2)
3(-,3,-,0) Pendek (< 30 cm), polong kurang lebat Sindoro Kontrol 2 0 0 Mati sebelum berbunga
Al-100 ppm 1 0 0 Mati sebelum berbunga
Rad pH 4 5 1 86(16,55,8,7) Sedang (31−50 cm), polong lebat Rad Al-100 1 1 65(9,38,16,2) Pendek (< 30 cm), polong lebat Rad Al-300 2 2 82(2,12,64,4) Sangat pendek (< 15 cm), polong sangat
31(3,19,5,4) lebat
Rad Al-400 3 1 35(2,11,16,6) Sedang (31−50 cm), polong kurang lebat Jumlah 3 9 1 2 493 (72,253,136,32)
1Al = diseleksi dengan AlCl
3.6H2O; Rad pH 4 = radiasi 400 rad dengan media seleksi pH 4; Rad = radiasi sinar gamma 400 rad; Rad Al = radiasi 400 rad dengan media seleksi pH 4 dan AlCl3.6H2O.
yang diuji kembali di lapang. Genotipe
ini lebih berpotensi dibanding Wilis
radiasi Al-500 (E) karena jumlah
polong-nya relatif bapolong-nyak sejak generasi pertama.
Pengujian dilakukan di Gajrug, Banten
pada tanah dengan pH 4,60, Aldd 12,60
me, dan kejenuhan Al 45,90%. Dari
pertanaman ini terdapat lima nomor yang
tidak ditanam kembali karena jumlah
polongnya jauh di bawah Sindoro sebagai
pembanding.
Kondisi pertanaman di lahan masam
ini sangat beragam karena kondisi tanah
yang tidak homogen. Pada tanah yang
berwarna hitam, kondisi tanaman relatif
baik karena pH tanah lebih tinggi (4,93)
dan kejenuhan Al rendah (16,19).
Keragaman pertanaman di Gajrug terlihat
dari nilai ragam Sindoro yang cukup besar
(1,70 ± 1,20). Mengingat keragaman yang
besar di lahan masam Gajrug, penanaman
generasi keempat dilakukan di dua lokasi,
yaitu di Gajrug dan di Bogor. Lahan di
Bogor memiliki pH 4,78, Aldd 1,49 me, dan
kejenuhan Al 7,69%.
Penampilan tanaman di Bogor
ter-lihat lebih baik dibandingkan di Gajrug
(Gambar 4). Dari hasil pengujian di empat
lokasi pada tiga generasi terlihat ada
beberapa nomor yang memiliki
ketahan-an dketahan-an daya hasil yketahan-ang lebih tinggi
dibanding Sindoro sebagai kontrol
(Tabel 4). Hal ini berarti terdapat potensi
yang cukup besar untuk mendapatkan
galur-galur harapan kedelai yang toleran
terhadap Al dan pH rendah.
Pada pertanaman generasi keempat
di Gajrug diperoleh tiga tanaman yang
lebih tinggi dibanding Sindoro (Tabel
5). Ketiga tanaman ini berasal dari satu
nomor dan diduga merupakan hasil
Gambar 4. Penampilan tanaman kedelai toleran Al di dua lokasi, (A) Gajrug
generasi ke-3; (B) Gajrug generasi ke-4; dan (C) Bogor generasi ke-4.
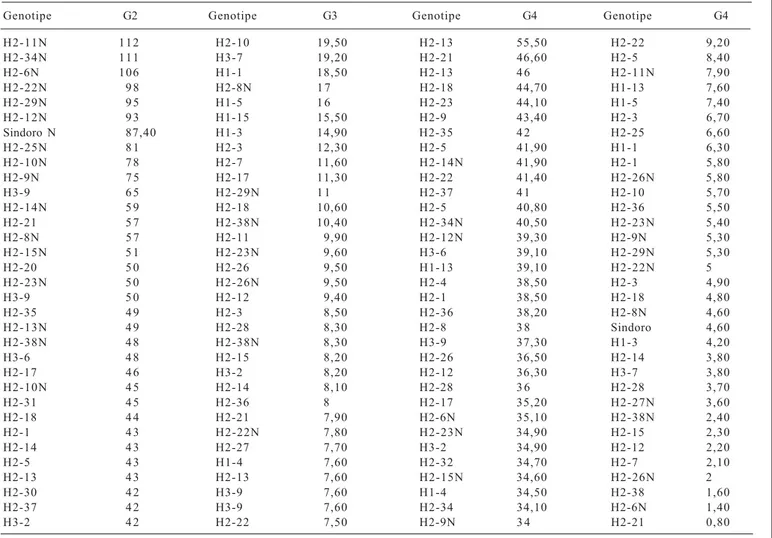
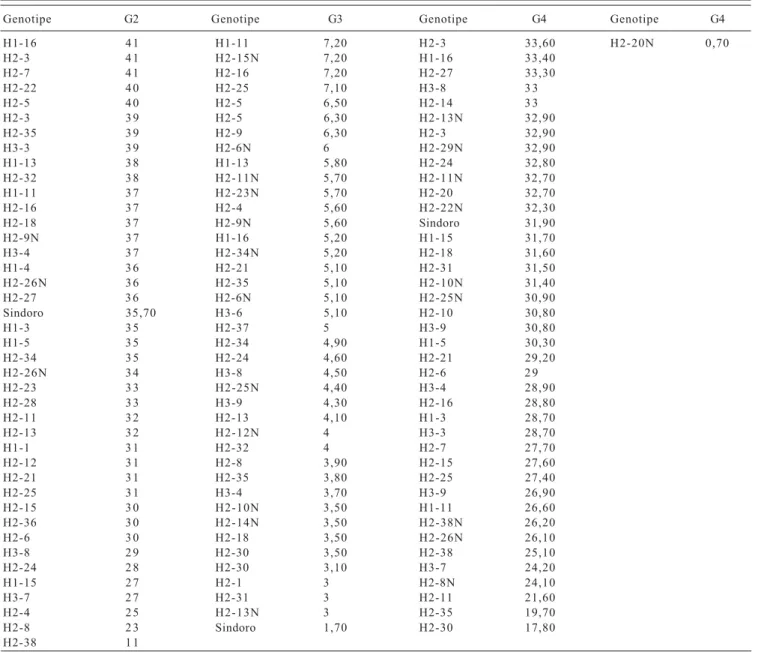
Tabel 4. Pengurutan jumlah polong kedelai di tiga lokasi penanaman pada tiga generasi.
Genotipe G2 Genotipe G3 Genotipe G4 Genotipe G4 H2-11N 112 H2-10 19,50 H2-13 55,50 H2-22 9,20 H2-34N 111 H3-7 19,20 H2-21 46,60 H2-5 8,40 H2-6N 106 H1-1 18,50 H2-13 4 6 H2-11N 7,90 H2-22N 9 8 H2-8N 1 7 H2-18 44,70 H1-13 7,60 H2-29N 9 5 H1-5 1 6 H2-23 44,10 H1-5 7,40 H2-12N 9 3 H1-15 15,50 H2-9 43,40 H2-3 6,70 Sindoro N 87,40 H1-3 14,90 H2-35 4 2 H2-25 6,60 H2-25N 8 1 H2-3 12,30 H2-5 41,90 H1-1 6,30 H2-10N 7 8 H2-7 11,60 H2-14N 41,90 H2-1 5,80 H2-9N 7 5 H2-17 11,30 H2-22 41,40 H2-26N 5,80 H3-9 6 5 H2-29N 1 1 H2-37 4 1 H2-10 5,70 H2-14N 5 9 H2-18 10,60 H2-5 40,80 H2-36 5,50 H2-21 5 7 H2-38N 10,40 H2-34N 40,50 H2-23N 5,40 H2-8N 5 7 H2-11 9,90 H2-12N 39,30 H2-9N 5,30 H2-15N 5 1 H2-23N 9,60 H3-6 39,10 H2-29N 5,30 H2-20 5 0 H2-26 9,50 H1-13 39,10 H2-22N 5 H2-23N 5 0 H2-26N 9,50 H2-4 38,50 H2-3 4,90 H3-9 5 0 H2-12 9,40 H2-1 38,50 H2-18 4,80 H2-35 4 9 H2-3 8,50 H2-36 38,20 H2-8N 4,60 H2-13N 4 9 H2-28 8,30 H2-8 3 8 Sindoro 4,60 H2-38N 4 8 H2-38N 8,30 H3-9 37,30 H1-3 4,20 H3-6 4 8 H2-15 8,20 H2-26 36,50 H2-14 3,80 H2-17 4 6 H3-2 8,20 H2-12 36,30 H3-7 3,80 H2-10N 4 5 H2-14 8,10 H2-28 3 6 H2-28 3,70 H2-31 4 5 H2-36 8 H2-17 35,20 H2-27N 3,60 H2-18 4 4 H2-21 7,90 H2-6N 35,10 H2-38N 2,40 H2-1 4 3 H2-22N 7,80 H2-23N 34,90 H2-15 2,30 H2-14 4 3 H2-27 7,70 H3-2 34,90 H2-12 2,20 H2-5 4 3 H1-4 7,60 H2-32 34,70 H2-7 2,10 H2-13 4 3 H2-13 7,60 H2-15N 34,60 H2-26N 2 H2-30 4 2 H3-9 7,60 H1-4 34,50 H2-38 1,60 H2-37 4 2 H3-9 7,60 H2-34 34,10 H2-6N 1,40
segregasi. Oleh karena itu, ketiga tanaman
tersebut digalurkan dan dijadikan nomor
tersendiri. Penampilan polong tanaman
terpilih dibandingkan dengan Sindoro
dapat dilihat pada Gambar 5.
KESIMPULAN
Metode regenerasi beberapa varietas
kedelai telah dapat dikuasai. Terdapat
perbedaan kemampuan beregenerasi
melalui jalur embriogenesis somatik pada
Tabel 4. lanjutan
Genotipe G2 Genotipe G3 Genotipe G4 Genotipe G4 H1-16 4 1 H1-11 7,20 H2-3 33,60 H2-20N 0,70 H2-3 4 1 H2-15N 7,20 H1-16 33,40 H2-7 4 1 H2-16 7,20 H2-27 33,30 H2-22 4 0 H2-25 7,10 H3-8 3 3 H2-5 4 0 H2-5 6,50 H2-14 3 3 H2-3 3 9 H2-5 6,30 H2-13N 32,90 H2-35 3 9 H2-9 6,30 H2-3 32,90 H3-3 3 9 H2-6N 6 H2-29N 32,90 H1-13 3 8 H1-13 5,80 H2-24 32,80 H2-32 3 8 H2-11N 5,70 H2-11N 32,70 H1-11 3 7 H2-23N 5,70 H2-20 32,70 H2-16 3 7 H2-4 5,60 H2-22N 32,30 H2-18 3 7 H2-9N 5,60 Sindoro 31,90 H2-9N 3 7 H1-16 5,20 H1-15 31,70 H3-4 3 7 H2-34N 5,20 H2-18 31,60 H1-4 3 6 H2-21 5,10 H2-31 31,50 H2-26N 3 6 H2-35 5,10 H2-10N 31,40 H2-27 3 6 H2-6N 5,10 H2-25N 30,90 Sindoro 35,70 H3-6 5,10 H2-10 30,80 H1-3 3 5 H2-37 5 H3-9 30,80 H1-5 3 5 H2-34 4,90 H1-5 30,30 H2-34 3 5 H2-24 4,60 H2-21 29,20 H2-26N 3 4 H3-8 4,50 H2-6 2 9 H2-23 3 3 H2-25N 4,40 H3-4 28,90 H2-28 3 3 H3-9 4,30 H2-16 28,80 H2-11 3 2 H2-13 4,10 H1-3 28,70 H2-13 3 2 H2-12N 4 H3-3 28,70 H1-1 3 1 H2-32 4 H2-7 27,70 H2-12 3 1 H2-8 3,90 H2-15 27,60 H2-21 3 1 H2-35 3,80 H2-25 27,40 H2-25 3 1 H3-4 3,70 H3-9 26,90 H2-15 3 0 H2-10N 3,50 H1-11 26,60 H2-36 3 0 H2-14N 3,50 H2-38N 26,20 H2-6 3 0 H2-18 3,50 H2-26N 26,10 H3-8 2 9 H2-30 3,50 H2-38 25,10 H2-24 2 8 H2-30 3,10 H3-7 24,20 H1-15 2 7 H2-1 3 H2-8N 24,10 H3-7 2 7 H2-31 3 H2-11 21,60 H2-4 2 5 H2-13N 3 H2-35 19,70 H2-8 2 3 Sindoro 1,70 H2-30 17,80 H2-38 1 1
G2 = kamar kaca (pH 4,80; Aldd 11,57 me; kejenuhan Al 57%); G3 = Gajrug 1 (pH 4,67; Aldd 16,02 me; kejenuhan Al 45,98%); G4 = Bogor (pH 4,78; Aldd 1,49 me; kejenuhan Al 7,69%); G4 = Gajrug 2 (pH 4,67; Aldd 16,02 me; kejenuhan Al 45,98%).
Untuk G2, kode N menunjukkan bahwa nomor tersebut ditanam di tanah normal (Aldd = 0).
Data G2 merupakan data jumlah polong individu, sedangkan data G3 dan G4 merupakan data jumlah polong rata-rata. Sumber: Mariska (2002c).
Tabel 5. Parameter pertumbuhan tanaman kedelai pilihan generasi keempat
di Gajrug (Aldd 16,02 me, kejenuhan Al 45,98%, pH 4,67), Banten.
Tanaman pilihan Parameter I II III Sindoro 1 Tinggi tanaman (cm) 1 8 1 6 2 2 23/15,60 Polong total 3 7 2 8 5 4 30/6,60 Polong isi 3 5 2 2 5 4 19/4,60 Polong hampa 2 4 0 30/2,70 Keempat tanaman ini berasal dari H2-18.
1Data Sindoro merupakan nilai maksimum/nilai rata-rata dari 190 tanaman contoh. Sumber: Mariska (2002c).
10 varietas yang diuji. Dari 10 varietas
tersebut, lima varietas bersifat lebih
embriogenik dibanding yang lain, yaitu
Bromo, Wilis, Tambora, Black Manchu,
dan Argomulyo.
Seleksi in vitro dapat digunakan
untuk meningkatkan ketahanan tanaman
kedelai terhadap cekaman Al dan pH
rendah. Pengujian di lapang
menghasil-kan beberapa nomor yang memiliki
ketahanan yang lebih baik terhadap Al
dan pH rendah dibandingkan varietas
yang toleran. Diharapkan nomor-nomor
harapan baru kedelai toleran Al dapat
diperoleh sehingga dapat meningkatkan
produksi kedelai nasional.
Gambar 5.
Polong tanaman kedelai toleran Al generasi keempat (A dan B)
dibandingkan dengan Sindoro sebagai kontrol (C).
DAFTAR PUSTAKA
Ahloowalia, B.S. 1986. Limitation to the use of somaclonal variation in crop improvement. p. 15−27. In J. Semal (Ed.). Somaclonal Variation and Crop Improvement. Martinus Nijhoff Publ., Dordrecht.
Dali’Agnol, M., J.H. Bouston, and W.A. Parrot. 1996. Screening methods develop alfalfa germplasm tolerant of acid, aluminium toxic soils. Crop Sci. 44(4): 64−70.
Jusuf, M., D. Sopandie, and Suharsono. 1999. Molecular biology of soybean tolerance to aluminium stress. Graduate Team Research, URGE. DHGE.
Mariska, I., S. Hutami, M. Kosmiatin, A. Husni, W.H. Adil, dan Y. Supriyati. 1999. Regenerasi dan seleksi in vitro untuk mendapatkan sifat ketahanan terhadap aluminium pada ta-naman kedelai. Laporan Hasil Penelitian Tahun 2000. Balai Penelitian Bioteknologi dan Sumberdaya Genetik Pertanian, Bogor. Mariska, I., S. Hutami, M. Kosmiatin, A. Husni,
W.H. Adil, and Y. Supriati. 2001a. Somatic embryogenesis in different soybean varie-ties. In N. Sunarlim, M. Machmud, W.H. Adil, F. Salim, and I.A. Orbani (Eds.). Proceedings of Workshop on Soybean Biotechnology for Aluminum Tolerance on Acid Soils and Disease Resistance. Central Research Institute for Food Crops, Bogor.
Mariska, I., S. Hutami, M. Kosmiatin, dan W.H. Adil. 2001b. Regenerasi massa sel embrio-genik kedelai setelah diseleksi pada kondisi Al berbeda dan pH rendah. Berita Pusat Penelitian dan Pengembangan Tanaman Pangan 20: 1−3.
Mariska, I., S. Hutami, dan M. Kosmiatin. 2002. Peningkatan toleransi terhadap aluminium dan pH rendah pada tanaman kedelai melalui kultur in vitro. Dalam N. Hilmy, M. Ismachin, F. Suhadi, E.L. Pattiradjawane, S. Sutrisno, M. Utama, Wandowo, M. Sumatra, Mugiono, E. Suwadji, S. Yatim, Ishak, N.D. Leswara, dan K. Idris (Ed.) Risalah Per-temuan Ilmiah Penelitian dan Pengembangan Aplikasi Isotop dan Radiasi. BATAN, Jakarta.
Mariska, I. 2002a. Peningkatan ketahanan terhadap aluminium pada pertanaman kedelai melalui kultur in vitro. Laporan Kemajuan RUT VIII.1. Tahap I. Kementeri-an Riset dKementeri-an Teknologi dKementeri-an LIPI, Jakarta. Mariska, I. 2002b. Peningkatan ketahanan
terhadap aluminium pada pertanaman kedelai melalui kultur in vitro. Laporan Kemajuan RUT VIII.1. Tahap II. Ke-menterian Riset dan Teknologi dan LIPI, Jakarta.
Mariska, I. 2002c. Peningkatan ketahanan terhadap aluminium pada pertanaman
kedelai melalui kultur in vitro. Laporan Riset Unggulan Terpadu RUT VIII.1. Kementerian Riset dan Teknologi dan LIPI, Jakarta. Notohadiprawiro, T. 1983. Persoalan tanah
masam dalam pembangunan pertanian di Indonesia. Buletin Fakultas Pertanian Universitas Gadjah Mada 18: 44−47. Smith, R.H., S. Bhaskaran, and K. Scherz. 1983.
Sorghum plant regeneration from aluminum selection media. Plant Cell Rep. 2: 129−
132.
Sopandie, D., M. Jusuf, Supriyatno, dan Hanum. 1996. Fisiologi dan genetik daya adaptasi kedelai terhadap cekaman kekeringan, pH rendah dan aluminium tinggi. Laporan Akhir RUT. Dewan Riset Nasional, Kementerian Riset dan Teknologi, Jakarta.
Stavarek, S.J. and D.W. Rains. 1984. The development of tolerance cells to mineral stress. Hort. Sci. 19: 377−382.
Van Sin Jan, V., C.C. de Macedo, J.M. Kinet, and J. Bouharmont. 1997. Selection of Al-resistant plants from a sensitive rice cultivar, using somaclonal variation, in vitro and hydroponic culture. Euphytica 97: 303−