BAB 2
TINJAUAN PUSTAKA
2.1Plak Dental
Plak dental didefinisikan sebagai lapisan biofilm bakteri yang merupakan
gabungan kompleks dari berbagai macam bakteri yang berbeda di dalam satu
lingkungan yang sama. Biofilm plak terbentuk melalui interaksi bakteri dengan
permukaan gigi yang dilapisi oleh pelikel, kemudian dilanjutkan melalui interaksi
fisik dan fisiologis antara spesies-spesies berbeda di dalam massa mikroba. Bakteri
yang terdapat pada plak dipengaruhi oleh faktor lingkungan yang dimediasi oleh
pejamu. Kesehatan periodonsium dianggap sebagai suatu keseimbangan di mana
populasi bakteri hidup berdampingan dengan pejamu, dan dalam kondisi ini tidak
terjadi kerusakan pada keduanya. Namun adanya gangguan keseimbangan
mengakibatkan perubahan baik pada pejamu maupun biofilm bakteri sehingga terjadi
kerusakan pada jaringan periodontal.17
Secara klinis, plak digambarkan sebagai substansi berwarna kuning keabuan
yang melekat secara kuat ke permukaan jaringan keras rongga mulut, yaitu
permukaan gigi, restorasi, maupun gigi tiruan.5,18 Matriks ekstraseluler yang melekat
erat tersebut menyebabkan penyingkiran plak tidak dapat dilakukan hanya dengan
berkumur ataupun menggunakan semprotan air. Oleh karena itu, plak dental dapat
dibedakan dari deposit rongga mulut lainnya, seperti material alba dan kalkulus.
Material alba merupakan akumulasi lunak yang terdiri dari bakteri, debris sisa
makanan, dan sel-sel jaringan epitel yang strukturnya tidak terorganisir, dan oleh
karenanya tidak bersifat kompleks seperti pada plak dental. Akumulasi berwarna
putih seperti keju ini dapat dengan mudah disingkirkan dengan menggunakan
semprotan air. Sementara itu, kalkulus diartikan sebagai deposit keras yang terbentuk
dari mineralisasi plak dental dan diselubungi oleh lapisan plak yang tidak
2.1.1 Komposisi Plak Dental
Plak dental terdiri dari 70-80% mikroba dan sisanya berupa matriks
interseluler. Satu gram plak mengandung sekitar 2 x 1011 bakteri dan diperkirakan
terdapat lebih dari 325 spesies bakteri berbeda pada plak dental. Mikroorganisme
non-bakteri yang dapat dijumpai pada plak yaitu spesies Mycoplasma, fungi,
protozoa, dan virus. Mikroorganisme tersebut berada di dalam matriks interseluler
yang juga mengandung beberapa sel pejamu seperti sel epitel dan leukosit.17
Matriks interseluler sebanyak 20-30% dari masa plak tersebut terdiri dari
material organik dan anorganik yang berasal dari saliva, cairan krevikular gingiva,
dan produk bakteri. Unsur organik utama dari matriks tersebut meliputi polisakarida,
protein, glikoprotein, dan lipid. Karbohidrat yang paling umum dihasilkan oleh
bakteri yaitu dekstran, selain itu terdapat juga beberapa levan dan galaktosa.
Sementara itu, komponen anorganik yang utama yaitu kalsium, fosfor, magnesium,
sodium, potasium, dan fluorida. Seiring dengan meningkatnya kandungan mineral,
massa plak akan terkalsifikasi membentuk kalkulus.17
2.1.2 Klasifikasi Plak Dental
Berdasarkan posisinya dari permukaan gigi menuju margin gingiva, plak
dental diklasifikasikan menjadi plak supragingiva dan plak subgingiva. Plak
supragingiva terletak pada atau di atas margin gingiva dan jika berkontak langsung
dengan margin gingiva disebut dengan plak marginal.18,19 Umumnya, plak
supragingiva ditemukan pada sepertiga gingiva mahkota gigi, area interproksimal,
dan pit-fisur, serta permukaan-permukaan yang abnormal lainnya.20 Jumlah plak
supragingiva yang sedikit akan sulit dideteksi tanpa penggunaan disclosing solution
atau menggoreskan permukaan gigi menggunakan instrumen. Namun, seiring dengan
perkembangan plak, deposit ini akan terlihat sebagai masa berwarna putih
kekuningan.19
Plak supragingiva pada permukaan gigi didominasi oleh bakteri kokus positif
Gram dan bakteri batang pendek, sedangkan bakteri batang negatif Gram dan filamen
Pada gingiva yang sehat, jumlah bakteri relatif rendah sekitar 102-103 organisme yang
didominasi oleh bakteri kokus positif Gram, seperti Streptococcus mutans,
Streptococcus mitis, Streptococcus sanguis, Streptococcus oralis, Rothia
dentocariosa, Staphilococcus epidermidis, diikuti oleh beberapa bakteri batang positif
Gram dan filamen, seperti Actinomyces viscosus, Actinomyces israeli, Actinomyces
gerencseriae, Corinebacterium sp., dan bakteri kokus negatif Gram dalam jumlah
yang kecil, seperti Veillonella parvula dan Neisseria sp. Plak supragingiva yang
matang pada jaringan gingiva sehat tanpa adanya riwayat gingivitis didominasi oleh
spesies negatif Gram, mencakup Fusobacterium nucleatum, Porphyromonas
gingivalis, Prevotella intermedia, Campylobacter rectus, Eikenella corrodens,
Leptotrichia, dan Selenomonas sp. Pada gingivitis, terdapat peningkatan jumlah
bakteri menjadi sekitar 104-106 organisme yang terdiri dari bakteri positif Gram dan
negatif Gram dengan jumlah yang seimbang. Selanjutnya, bakteri kokus dan batang
positif Gram serta bakteri kokus negatif Gram menjadi lebih kompleks. Pada
awalnya, terjadi peningkatan jumlah bakteri filamen, seperti Actinomyces. Kemudian,
jumlah spesies anaerob dan kokus negatif Gram, seperti Veillonella, dan bakteri
batang anaerob negatif Gram, seperti Fusobacterium dan Prevotella intermedia
mengalami peningkatan, serta munculnya bakteri batang motile dan Spirocheta.5,21
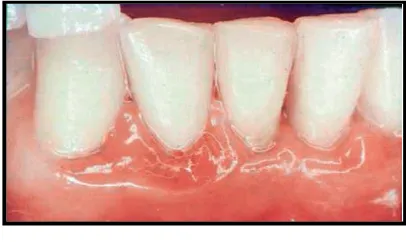
Gambar 1. Plak supragingiva marginal dan gingivitis22
Plak subgingiva terletak di bawah margin gingiva di antara gigi dan jaringan
3, yaitu plak subgingiva yang melekat pada permukaan gigi, jaringan epitel, dan plak
subgingiva yang tidak melekat pada permukaan gigi maupun jaringan epitel.20,23 Plak
subgingiva dapat dilihat melalui penyingkiran massa biofilm dari sulkus gingiva
dengan menggunakan instrumen.19
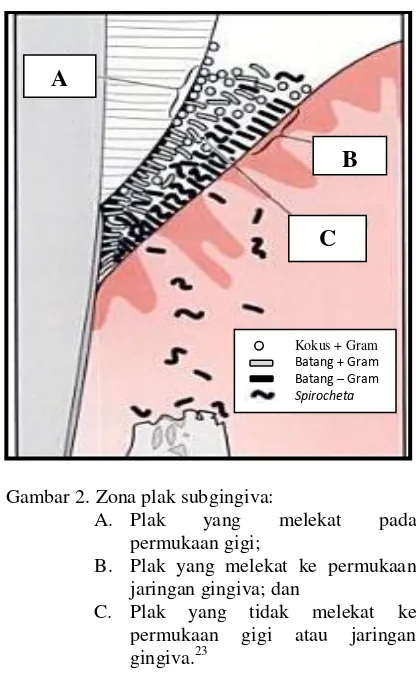
Gambar 2. Zona plak subgingiva:
A. Plak yang melekat pada
permukaan gigi;
B. Plak yang melekat ke permukaan
jaringan gingiva; dan
C. Plak yang tidak melekat ke
permukaan gigi atau jaringan gingiva.23
Secara umum, komposisi mikroba plak subgingiva berbeda dengan mikroba
plak supragingiva. Hal ini dikarenakan lingkungan pada plak subgingiva bersifat
anaerob. Komposisi plak subgingiva tergantung pada kedalaman sulkus gingiva atau
poket periodontal. Plak subgingiva yang mengarah ke apikal lebih didominasi oleh
bakteri Spirocheta, kokus, dan batang, sedangkan plak subgingiva yang mengarah ke
koronal lebih didominasi oleh bakteri filamen. Beberapa bakteri kokus dan batang
positif Gram yang terdapat pada plak subgingiva diantaranya termasuk Streptococcus
mitis, Streptococcus sanguinis, Actinomyces oris, Actinomyces naeslundii, dan
Kokus + Gram
Batang + Gram Batang – Gram
Spirocheta
A
B
Eubacterium sp.18 Selain itu, terjadi peningkatan jumlah bakteri kokus, batang, dan
filamen negatif Gram, serta munculnya bakteri anaerob, seperti Fusobacterium
nucleatum, Campylobacter gracilis, Tannerella forsthia, dan Capnocytphaga sp.21
Plak subgingiva yang berhubungan dengan permukaan gigi mengandung bakteri
kokus dan batang positif Gram maupun negatif Gram. Namun, bakteri filamen positif
Gram merupakan mikroorganisme yang paling mendominasi. Pada bagian apikal,
jumlah bakteri filamen akan mengalami penurunan, dan lebih didominasi oleh bakteri
batang negatif Gram.18,19 Plak subgingiva yang berhubungan dengan jaringan epitel
sulkus gingiva atau poket periodontal mengandung bakteri kokus dan batang negatif
Gram, serta sejumlah besar bakteri filamen, bakteri batang berflagel, dan
Spirocheta.18 Plak subgingiva yang tidak melekat ke permukaan gigi maupun jaringan
epitel didominasi oleh bakteri batang negatif Gram dan Spirocheta.23
Lokasi spesifik dari plak secara signifikan dihubungkan dengan penyakit
periodontal. Plak marginal memiliki peranan penting dalam inisiasi dan
perkembangan gingivitis. Plak supragingiva dan plak subgingiva yang berhubungan
dengan permukaan gigi berperan dalam pembentukan kalkulus dan karies pada akar
gigi. Sementara itu, plak subgingiva yang berhubungan dengan jaringan pada sulkus
gingiva atau poket periodontal berperan dalam menyebabkan kerusakan jaringan yang
parah sehingga menyebabkan terjadinya periodontitis.5,18
2.1.3 Proses Pembentukan Plak Dental
Proses pembentukan plak terdiri dari 3 fase, yaitu pembentukan pelikel pada
permukaan gigi, kolonisasi awal bakteri pada pelikel, dan kolonisasi sekunder serta
maturasi plak.18,19
2.1.3.1Pembentukan Pelikel pada Permukaan Gigi
Pelikel berasal dari protein saliva yang sebagian besar berupa glikoprotein dan
melekat ke permukaan jaringan keras rongga mulut, seperti gigi, restorasi, maupun
gigi tiruan beberapa saat setelah tindakan pembersihan gigi. Secara klinis, pelikel
terlihat sebagai lapisan tipis dengan ketebalan 0,5 µm, licin, tidak berwarna, dan
permukaan enamel dari aktivitas asam dengan cara membatasi difusi atau penyebaran
produk asam dari pemecahan gula. Selain itu, pelikel dapat mengikat ion anorganik
seperti fluorida yang akan mendorong terjadinya proses remineralisasi. Pelikel juga
mengandung faktor antibakteri seperti IgG, IgA, IgM, komplemen, dan lisozim.5,17,19
Pada awalnya, pelikel merupakan lapisan yang tidak mengandung bakteri.17
Sebaliknya, pelikel berperan sebagai bahan perekat dua sisi, di mana satu sisi melekat
ke permukaan gigi dan sisi lainnya menyediakan permukaan lengket yang
memfasilitasi perlekatan bakteri pada permukaan gigi melalui
komponen-komponennya.5 Pelikel pada permukaan gigi mengandung lebih dari 180 peptida,
protein, dan glikoprotein, termasuk keratin, mucin, protein kaya proline, fosfoprotein,
protein kaya histidine, dan molekul-molekul lainnya yang berfungsi sebagai reseptor
atau sisi perlekatan bagi bakteri. Oleh karena itu, bakteri yang melekat ke permukaan
gigi tidak bersentuhan langsung dengan enamel, melainkan melalui interaksi dengan
pelikel pada enamel.18
2.1.3.2Kolonisasi Awal Bakteri pada Pelikel
Beberapa jam setelah pembentukan pelikel, bakteri mulai melekat pada
permukaan luar pelikel.17 Bakteri melekat ke pelikel melalui struktur seperti rambut
yang dinamakan fimbriae atau pili, di mana pada struktur tersebut terdapat molekul
adhesin yang akan berikatan dengan reseptor pada pelikel. Protein lektin dapat
berikatan dengan struktur karbohidrat spesifik pada glikoprotein pelikel. Interaksi
seperti lektin tersebut juga dilibatkan pada tahap koagregasi bakteri.5,19 Namun,
komponen saliva yang terdapat pada pelikel juga berperan menghambat perlekatan
bakteri melalui penghambatan reseptor bakteri untuk berikatan dengan permukaan
pelikel. Selain itu, IgA yang disekresikan oleh kelenjar saliva merupakan antibodi
yang paling dominan pada saliva. Oleh karenanya, komposisi saliva dapat berperan
sebagai fasilitator maupun inhibitor perlekatan bakteri pada pelikel. Laju alir saliva,
tekanan pengunyahan, dan prosedur higene oral juga dapat menyingkirkan bakteri
permukaan gigi yang abnormal dan daerah lainnya yang tidak terkena mekanisme
pembersihan gigi.19
Selama 4 sampai 8 jam pertama, sekitar 60%-80% bakteri yang ada
merupakan genus Streptococcus. Bakteri lain bersifat aerob yang ada yaitu
Haemophillus sp. dan Neisseria sp. Selain itu, terdapat pula bakteri fakultatif anaerob
yaitu Actinomyces sp. dan Veilonella sp. Bakteri tersebut dikenal dengan koloni
primer yang menyediakan sisi perlekatan baru untuk bakteri rongga mulut lainnya.
Ketika bakteri melekat ke permukaan pelikel, koloni primer ini akan memulai
aktivitas metabolismenya dan memproduksi substansi-substansi yang akan merubah
kondisi lingkungan sehingga memengaruhi kemampuan bakteri lainnya untuk
bertahan hidup pada biofilm plak dental. Misalnya dengan merubah kondisi
lingkungan aerob menjadi anaerob.5,18 Bakteri baru melekat ke bakteri plak yang
sudah ada melalui mekanisme molekular kunci dan gembok spesifik, di mana proses
ini disebut dengan koagregasi. Pembentukan plak supragingiva dipelopori oleh
bakteri yang memiliki kemampuan membentuk polisakarida ekstraseluler yang
memungkinkan bakteri-bakteri tersebut melekat ke permukaan gigi dan bakteri
lainnya. Bakteri tersebut yaitu Streptococcus sanguis, Actinomyces viscosus, dan
Actinomyces naeslundii. Kedua fase pada tahap pembentukan plak awal ini terjadi
dalam 2 hari.17
2.1.3.3Kolonisasi Sekunder dan Maturasi Plak
Bakteri pengkoloni sekunder melekat di atas bakteri pengkoloni primer dan
memanfaatkan perubahan lingkungan yang terjadi sebagai akibat dari pertumbuhan
dan metabolisme plak. Pada awalnya, bakteri kokus negatif Gram seperti Neisseria
sp. dan Veillonella sp. berada pada ruang interstitial yang terbentuk dari interaksi
bakteri pada tahap sebelumnya. Selanjutnya, setelah 4-7 hari pembentukan plak,
jaringan gingiva akan mengalami inflamasi dan perlahan-perlahan terjadi perubahan
lingkungan yang menyebabkan perubahan selektif lebih lanjut. Perubahan tersebut
mencakup pembukaan krevikular gingiva sebagai jalur pertumbuhan plak dan
dari serum yang memungkinkan bakteri lain dengan kebutuhan metabolisme berbeda
memasuki plak. Bakteri tersebut yaitu jenis batang negatif Gram, seperti Prevotella
sp., Porphyromonas sp., Capnocytophaga sp., Fusobacterium sp., dan Bakteriodes
sp. Interaksi bakteri lebih lanjut terjadi antara jenis bakteri berbeda. Bakteri
pengkoloni sekunder ini juga membentuk kelompok bakteri utama dari plak
subgingiva.17 Selama pematangan plak, terjadi peningkatan massa dan ketebalan plak
sebagai hasil dari proliferasi bakteri pada plak. Proses pematangan plak
membutuhkan kohesi dari sel-sel bakteri yang dihasilkan dari pembentukan matriks
intermikroba yang tersusun dari material saliva, eksudat gingiva, dan substansi
mikroba seperti polisakarida.19
2.2Gingiva
Gingiva merupakan bagian dari jaringan pendukung gigi atau periodonsium
yang menutupi prosesus alveolaris dari rahang dan mengelilingi leher gigi, serta
memiliki fungsi utama melindungi jaringan dibawahnya. Secara klinis, gingiva dapat
terlihat di dalam rongga mulut, sedangkan struktur periodontal pendukung lainnya
yaitu ligamen periodontal, sementum, dan tulang alveolar tidak terlihat, kecuali
sementum jika terjadi resesi gingiva.24
2.2.1 Gambaran Klinis Gingiva
Gingiva normal dikarakteristikkan oleh beberapa gambaran klinis, antara lain:
2.2.1.1Warna Gingiva
Margin gingiva dan gingiva cekat secara umum berwarna koral pink. Hal ini
diakibatkan oleh karena adanya suplai vaskular, ketebalan dan derajat keratinisasi
epitel, serta sel-sel yang mengandung pigmen. Warna ini bervariasi pada setiap
individu dan berhubungan dengan pigmentasi kulit. Warna gingiva lebih terang pada
orang berambut pirang dengan kulit kuning langsat daripada orang berambut gelap
Gambar 3. Warna gingiva:
A. Gingiva normal pada dewasa muda
B. Gingiva dengan pigmentasi berat pada dewasa paruh baya24
Gingiva cekat dibatasi dari batas mukosa alveolar pada sisi bukal dengan garis
mukogingival berbatas jelas. Mukosa alveolar lebih berwarna merah, halus, dan
berkilat. Hal ini dikarenakan perbedaan struktur mikroskopis dari gingiva cekat
dengan mukosa alveolar, di mana epitelium mukosa alveolar lebih tipis, tidak
terkeratinisasi, dan tidak terdiri dari rete pegs. Selain itu jaringan ikat mukosa
alveolar tersusun longgar dan mengandung lebih banyak pembuluh darah.24
2.2.1.2Konsistensi Gingiva
Gingiva memiliki konsistensi kaku (firm) dan lenting (resilient). Hal ini
disebabkan oleh kandungan kolagen pada lamina propria dan perlekatan gingiva ke
mukoperiosteum tulang alveolar. Gingiva bebas memiliki konsistensi yang kaku
karena mengandung serabut gingiva meskipun tidak melekat ke mukoperiosteum
tulang alveolar.5,24
2.2.1.3Kontur Gingiva
Kontur atau bentuk gingiva sangat bervariasi, tergantung pada bentuk dan
susunan gigi geligi pada lengkung rahang, lokasi dan besar area kontak proksimal,
dan dimensi embrasur gingiva oral maupun vestibular. Margin gingiva mengelilingi
gigi seperti kerah baju dan mengikuti pola seperti busur pada permukaan vestibular
dan oral. Pola tersebut berbentuk garis lurus sepanjang gigi dengan permukaan relatif
datar. Pada gigi yang sangat konveks dalam arah mesio distal, seperti kaninus
gingiva akan berada lebih ke apikal. Sementara itu, gingiva akan lebih datar dan
menebal pada gigi lingoversi.5,24
Gambar 4. Kontur gingiva yang menebal
pada gigi linguoversi24
2.2.1.4Tekstur Permukaan Gingiva
Tekstur permukaan gingiva cekat yaitu seperti kulit jeruk disebut dengan
stippled atau stippling, sedangkan tekstur permukaan gingiva bebas yaitu licin. Pola
dan perluasan stippling bervariasi antar individu dan antar sisi pada satu individu.
Stippling kurang terlihat pada permukaan oral daripada vestibular dan pada beberapa
orang mungkin tidak dijumpai. Stippling muncul sebagai akibat dari protuberansia
dan depresi pada permukaan gingiva.5,24
2.2.1.5Posisi Margin Gingiva
Posisi gingiva menunjukkan level di mana margin gingiva melekat ke
permukaan gigi. Ketika gigi erupsi ke rongga mulut, margin gingiva dan sulkus
gingiva berada pada puncak mahkota, seiring dengan erupsi gigi posisi margin
gingiva dan sulkus gingiva mengarah semakin dekat ke akar gigi. Pada kondisi
normal, margin gingiva berada pada atau sedikit ke arah koronal dari batas sementum
2.3Gingivitis
Gingivitis merupakan salah satu jenis penyakit periodontal berupa respon
inflamasi yang menyebabkan kerusakan bersifat reversible pada jaringan gingiva.5
Inflamasi gingiva cenderung terjadi pada daerah papila interdental. Hal ini
dikarenakan daerah interdental terlindung dari aktivitas pembersihan rongga mulut,
akibatnya plak lebih banyak berakumulasi pada daerah tersebut. Inflamasi gingiva
bermula pada daerah papila interdental dan berlanjut menyebar ke sekitar leher gigi.17
The American Academy of Periodontology mengklasifikasikan penyakit
gingiva secara garis besar berdasarkan penyebabnya menjadi dua, yaitu penyakit
gingiva yang disebabkan oleh plak dental dan lesi gingiva yang bukan disebabkan
oleh plak dental. Pengklasifikasian ini telah didiskusikan dalam the 1999
International Workshop for the Classification of the Periodontal Disease. Penyakit
gingiva yang disebabkan oleh plak dental dapat dipengaruhi oleh beberapa faktor
predisposisi, seperti faktor lokal, faktor sistemik, pengobatan penyakit, dan kondisi
malnutrisi. Sementara itu, lesi gingiva yang bukan disebabkan oleh plak dental terjadi
dikarenakan adanya respon inflamasi terhadap beberapa bakteri spesifik, virus, dan
jamur, manifestasi penyakit sistemik, reaksi alergi, lesi traumatik, dan reaksi terhadap
benda asing.4,25
Gingivitis yang diinduksi plak dental merupakan hasil interaksi antara
mikroorganisme yang terdapat pada biofilm plak, jaringan gingiva, dan sel-sel
inflamatori.25 Berdasarkan lokasi dan luasnya daerah yang terkena, gingivitis
diklasifikasikan menjadi dua, yaitu gingivitis yang terlokalisir pada beberapa gigi dan
gingivitis yang tergeneralisasi pada seluruh rongga mulut. Selain itu, gingivitis dapat
terjadi hanya terbatas pada papila interdental ataupun menyebar ke seluruh margin
gingiva sampai melibatkan seluruh gingiva bebas.4 Beberapa faktor lokal dapat
memengaruhi terjadinya gingivitis, diantaranya pembentukan kalkulus pada mahkota
dan akar gigi, kondisi gigi yang berjejal, dan alat ortodontik. Faktor-faktor tersebut
berperan dalam mempertahankan plak dental dan mempersulit prosedur higiene oral
2.3.1 Patogenesis Gingivitis
Perkembangan gingiva yang sehat menjadi gingivitis terbagi menjadi 3 fase,
yaitu fase initial lesion, fase early lesion, dan fase established lesion, namun antara
satu fase dengan fase selanjutnya tidak terdapat batasan yang terlalu jelas.4,22
2.3.1.1Initial Lesion
Perubahan yang terjadi pada fase initial lesion hanya dapat dideteksi melalui
pemeriksaan mikroskopik. Oleh sebab itu, tahap ini disebut juga dengan gingivitis
subklinis. Perubahan jaringan terjadi pada epitel penyatu dan jaringan ikat dari
margin gingiva bebas dalam 2-4 hari setelah akumulasi plak pada sulkus gingiva.
Respon inflamasi akut pada fase ini ditandai dengan dilatasi pembuluh darah
sehingga meningkatkan aliran darah ke area inflamasi.Selanjutnya, leukosit terutama
neutrofil (polymorphonuclear neutrophil/PMN) meninggalkan pembuluh darah
dengan cara migrasi melalui dinding pembuluh darah. Leukosit dan protein plasma
yang keluar dari pembuluh kapiler menuju jaringan ikat disekitarnya menyebabkan
edema pada jaringan. Selain itu, peningkatan migrasi leukosit ke epitel penyatu
menyebabkan peningkatan cairan sulkular pada sulkus gingiva.4,5,22
Limfosit T berperan mempertahankan keseimbangan respon terhadap infeksi
bakteri. Namun, aktivasi sistem imun menyebabkan degenerasi kolagen dan
perubahan pada sel epitel.4 Degenerasi kolagen menyebabkan berkurangnya
kandungan kolagen di dalam jaringan ikat gingiva yang terinflamasi dan hilangnya
kolagen yang mendukung epitel penyatu bagian koronal.5
2.3.1.2Early Lesion
Berbeda dengan fase sebelumnya, pada fase ini perubahan jaringan sudah
dapat dideteksi secara klinis dalam 4-14 hari setelah akumulasi plak pada sulkus
gingiva. Akumulasi plak pada sulkus gingiva menyebabkan gangguan perlekatan
epitel penyatu bagian koronal pada gigi. Akibatnya, epitel tersebut akan kehilangan
Pada fase ini, respon yang terjadi masih berupa respon inflamasi akut. Aliran
darah terus mengalami peningkatan. Selain itu, protein plasma dan leukosit tetap
bermigrasi menuju jaringan ikat.4,5 Begitu juga halnya dengan jumlah limfosit T yang
meningkat dan terlokalisir pada jaringan ikat di bawah epitel sulkus gingiva.
Peningkatan eksudat tersebut menyebabkan edema pada jaringan gingiva dan warna
gingiva menjadi merah. Selanjutnya, serabut kolagen perivaskular pada jaringan ikat
mengalami kerusakan akibat inflamasi dan digantikan oleh plasma darah dan sel
inflamatori. Hal ini yang menyebabkan perubahan konsistensi jaringan gingiva
menjadi lebih lunak dan spongius. Kerusakan serabut kolagen yang melekat pada
jaringan ikat gingiva dan hilangnya stippling mengakibatkan tampilan gingiva
menjadi kilat. Selain itu, perdarahan gingiva mungkin terjadi saat dilakukan
probing.4,5,22
2.3.1.3Established Lesion
Jika prosedur higiene oral yang memadai tidak juga dilakukan, fase early
lesion akan berkembang menjadi fase established lesion dalam 15-21 hari.Pada fase
ini, perbedaan yang jelas terlihat pada jenis sel darah putih melalui pemeriksaan
histopatologis, di mana limfosit B dan T berada pada jumlah yang seimbang. Hal ini
mengindikasikan terjadinya kerusakan jaringan akibat reaksi inflamasi. Limfosit B
dapat melepaskan limfokinase yang menambah kerusakan jaringan. Selain itu,
kerusakan pada jaringan ikat kolagen juga semakin meningkat.4 Sel basal epitel
penyatu mulai melakukan replikasi dan epithelial ridge meluas ke jaringan ikat. Hal
ini dikarenakan terjadinya kerusakan pada serabut gingiva yang menghasilkan
ruangan untuk pertumbuhan jaringan epitel.4,5
Pada fase inflamasi kronis, tubuh berusaha untuk memperbaiki kerusakan
jaringan dengan membentuk serabut kolagen baru. Peningkatan deposisi serabut
kolagen ini menyebabkan jaringan gingiva mengalami pembesaran dan perubahan
konsistensi menjadi fibrous. Jumlah serabut kolagen yang meningkat akan
menyamarkan warna gingiva yang merah menjadi kurang merah. Selain itu,
darah mengalami penurunan, sehingga warna gingiva dapat menjadi kebiruan.5 Pada
fase ini terjadi peningkatan kedalaman probing yang dapat disebabkan edema pada
jaringan menyebabkan bergesernya margin gingiva ke arah koronal sehingga
menambah kedalaman probing.Pada ketiga fase gingivitis, tidak terjadi migrasi epitel
penyatu ke arah apikal, tidak terdapat kerusakan serabut ligamen periodontal, dan
tulang alveolar tidak mengalami kerusakan.4,5
2.3.2 Gambaran Klinis
Respon inflamasi sebagai mekanisme perlawanan terhadap bakteri pada
biofilm plak menghasilkan perubahan pada gingiva bebas, gingiva cekat, maupun
papila interdental.5 Perubahan-perubahan tersebut diantaranya:
2.3.2.1Perubahan Warna Gingiva
Peningkatan vaskularisasi dan penurunan derajat keratinisasi epitel
menyebabkan warna gingiva pada fase inflamasi akut menjadi lebih merah.
Perubahan warna ini tersebar pada daerah margin gingiva dengan tampilan seperti
bintik-bintik. Sementara itu, pada fase inflamasi kronis warna gingiva menjadi merah
kebiruan atau merah keunguan dikarenakan jumlah sel darah yang terlalu banyak
pada pembuluh darah sehingga menyebabkan terjadinya venous stasis atau aliran
darah yang melambat. Perubahan warna ini terjadi dimulai dari papila interdental dan
margin gingiva kemudian menyebar ke gingiva cekat.5,26
2.3.2.2Perdarahan Saat Probing
Perdarahan gingiva saat probing dapat dengan mudah dideteksi secara klinis
dan merupakan tanda yang lebih dahulu muncul daripada perubahan warna gingiva.
Oleh karena itu, perdarahan saat probing merupakan tanda yang penting untuk
mendiagnosis dan mencegah fase gingivitis berikutnya. Gingiva yang terinflamasi
menghasilkan perubahan histopatologis, yaitu kapiler yang mengalami dilatasi, epitel
sulkular yang menipis dan disertai ulserasi, serta posisinya yang mendekati
permukaan sehingga stimulus ringan yang sebenarnya tidak berbahaya
mengakibatkan pecahnya kapiler dan terjadi perdarahan pada gingiva.5,26
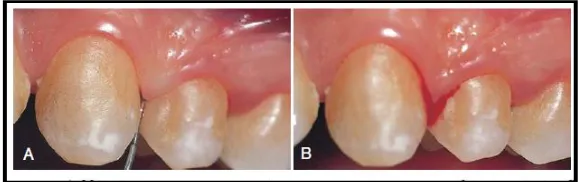
Gambar 6. Perdarahan saat probing:
A.Gingivitis oedematous ringan, prob dimasukkan ke dasar sulkus gingiva.
B.Perdarahan terjadi setelah beberapa detik.26
2.3.2.3Perubahan Konsistensi Gingiva
Pada fase inflamasi akut, jaringan ditandai dengan konsistensi yang lunak atau
spongius dikarenakan serabut kolagen perivaskular pada jaringan ikat mengalami
kerusakan akibat inflamasi dan digantikan oleh plasma darah dan sel inflamatori.
Ketika jaringan gingiva tersebut diberikan tekanan menggunakan prob, jaringan ini
akan mudah tertekan dan meninggalkan bekas selama beberapa detik.5 Pada fase
inflamasi kronis, perubahan destruktif menghasilkan jaringan edema dan perubahan
reparatif ditandai dengan terbentuknya jaringan fibrotik terjadi secara berdampingan.
Konsistensi gingiva pada fase ini ditentukan oleh jumlah jaringan edema atau
2.3.2.4Perubahan Kontur Gingiva
Pada jaringan yang terinflamasi, gingiva bebas yang awalnya datar mengalami
pembengkakan dikarenakan edema jaringan pada leher gigi. Selain itu, papila
interdental dapat berubah bentuk menjadi bulbous atau blunted. Papila yang
berbentuk bulbous mengalami pembengkakan dan memiliki tampilan yang menonjol
keluar dari ruangan interproksimal, sedangkan papila yang berbentuk blunted
memiliki bentuk yang datar, namun tidak mengisi ruangan interproksimal.5
2.3.2.5Perubahan Tekstur Permukaan Gingiva
Hilangnya stippling pada permukaan gingiva merupakan tanda awal
gingivitis. Pada fase inflamasi kronis, permukaan gingiva dapat menjadi halus dan
kilat atau keras dan bernodul-nodul, tergantung perubahan cairan eksudat atau
jaringan fibrotik yang paling dominan.26 Peningkatan cairan yang berasal dari respon
inflamasi tubuh menyebabkan jaringan gingiva berpenampilan halus dan sangat
kilat.5
Gambar 7. Gingivitis kronis disertai dengan pembengkakan, hilangnya stippling, dan diskolorisasi26
2.3.2.6Perubahan Posisi Margin Gingiva
Perubahan posisi margin gingiva ke arah koronal dapat menjadi salah satu
tanda klinis gingivitis. Perubahan posisi ini dapat disebabkan oleh pembesaran
jaringan gingiva. Posisi margin gingiva dapat dikaitkan dengan kedalaman probing.
perlekatan epitel penyatu, sehingga perubahan posisi gingiva ke arah koronal akan
menambah kedalaman probing.5
2.4Oil Pulling
Oil pulling atau oil swishing merupakan salah satu bentuk pengobatan
Ayurveda yang dilakukan dengan berkumur menggunakan minyak nabati.10 Oil
pulling telah digunakan secara luas sebagai pengobatan tradisional yang berasal dari
India untuk mencegah berbagai penyakit sistemik dan rongga mulut. Selain itu, oil
pulling dibicarakan di buku pengobatan Ayurveda, yaitu Charaka Samhita dan
Susrutha Arthashastra, serta dikenal dengan sebutan Kavala Gandoosha atau Kavala
Graha. Pengobatan Ayurveda sangat tergantung pada tumbuhan, tanaman, minyak,
dan rempah-rempah yang digunakan sebagai obat-obatan.9,13,27 Beberapa metode
untuk mempertahankan kebersihan mulut yang terdapat di dalam pengobatan
Ayurveda diantaranya menyikat gigi (Danta Dhavana), membersihkan lidah
(Jihwanirlekhana), berkumur (Gandusha dan Kavala), mengunyah sirih (Tambula
Sevana), dan membersihkan muka (Mukha Prakshalana).Meskipun oil pulling telah
dikenal sejak tahun 3000 SM, konsep ini baru diperkenalkan kembali oleh Dr. F.
Karach pada tahun 1990 di Rusia.27-29
2.4.1 Prosedur Berkumur dengan Metode Oil Pulling
Prosedur melakukan terapi oil pulling secara umum hampir sama seperti
layaknya menggunakan obat kumur. Sebanyak satu sendok makan atau kurang lebih
10-15ml minyak sayuran dimasukkan ke dalam mulut sampai mulut terisi setengah
penuh. Minyak tersebut kemudian dihisap, ditarik, dan didorong melalui gigi-gigi
dari kiri ke kanan, dari depan ke belakang, dan sebaliknya. Terapi oil pulling
umumnya dilakukan selama 8-10 menit atau sampai mulut terasa penuh. Ketika
berada di dalam mulut, minyak akan bercampur dengan saliva, berubah dari minyak
yang kental menjadi cair, berwarna putih seperti susu, dan berbusa. Selanjutnya,
dengan tindakan menyikat gigi dan membilas mulut dengan air selama beberapa
kali.10,11,13
Ada beberapa instruksi yang harus diikuti selama melakukan terapi oil
pulling. Oil pulling sebaiknya dilakukan pada pagi hari. Selain itu, terapi ini
dilakukan dalam posisi duduk dengan dagu tegak. Terapi ini dapat dilakukan
maksimal tiga kali sehari pada kasus adanya penyakit akut. Tidak terdapat kontra
indikasi untuk melakukan oil pulling kecuali untuk anak-anak dibawah umur 5 tahun
karena ditakutkan cairan tersebut teraspirasi atau tertelan. Terapi oil pulling juga
dapat dilakukan oleh wanita hamil dan menstruasi.6,11
2.4.2 Manfaat Oil Pulling
Berkumur dengan metode oil pulling dipercaya memiliki manfaat bagi
kesehatan sistemik maupun rongga mulut. Di dalam kesehatan sistemik, terapi oil
pulling dipercaya dapat mencegah dan menyembuhkan kurang lebih 30 penyakit
sistemik mulai dari sakit kepala, migrain, hipertensi, diabetes, asma, bronkitis,
trombosis pada arteri, kelainan darah yang bersifat kronis seperti leukemia, artritis,
paralisis neurofisiologi, eksema, gastroentritis, peritonitis, meningitis, penyakit
jantung iskemik, penyakit liver, gangguan pernafasan dan ginjal, gangguan hormonal
pada wanita, dan memperlambat proses penuaan.6,8,11 Sementara itu, di dalam
kesehatan rongga mulut terapi oil pulling dianggap sebagai salah satu cara untuk
menghambat bakteri, jamur, dan organisme lainnya yang berbahaya bagi mulut, gigi,
gusi, dan tenggorokan. Oleh karena itu, terapi oil pulling dipercaya berpotensi
mengurangi pembentukan plak dan terjadinya gingivitis serta karies. Manfaat lain
dari terapi oil pulling yaitu mencegah bau mulut, tenggorokan kering, bibir
pecah-pecah, dan xerostomia.9,27,29
Penelitian yang dilakukan oleh Amith dkk selama 45 hari, menunjukkan
bahwa terapi oil pulling menggunakan minyak bunga matahari signifikan
menurunkan skor plak dan gingivitis. Asokan dkk melakukan penelitian klinis dan
mikrobiologi. Hasil penelitian tersebut menunjukkan bahwa terapi oil pulling
plak.6,9 Penelitian lain yang dilakukan oleh Saravanan menunjukkan bahwa terapi oil
pulling mengurangi skor plak dan gingiva serta jumlah koloni bakteri secara
signifikan.13
Berkumur dengan metode oil pulling tidak hanya berperan dalam mencegah
dan menyembuhkan berbagai penyakit tetapi juga memiliki kelebihan dibandingkan
berkumur dengan obat kumur komersial yang ada. Minyak nabati yang digunakan
tidak mengandung bahan kimia dan alkohol, tidak menyebabkan stein pada
permukaan gigi, tidak menimbulkan sisa rasa yang menetap lama, tidak menimbulkan
reaksi alergi, meskipun keefektifan dan mekanisme aksinya belum jelas. Selain itu,
terapi ini dianggap menarik dan inovatif karena pemakaiannya yang sederhana,
harganya yang murah, mudah didapatkan, tidak perlu membeli produk yang beraneka
ragam, tidak perlu mencampurkan berbagai produk, ataupun menggunakan banyak
suplemen. 6,10,11
2.4.3 Jenis Minyak yang dapat Digunakan dalam Oil Pulling
Beberapa jenis minyak yang dapat digunakan dalam terapi oil pulling di
antaranya minyak bunga matahari, minyak wijen, minyak zaitun, minyak kelapa, dan
minyak kacang.9-12 Minyak wijen mengandung konsentrasi asam lemak tak jenuh
ganda yang tinggi dan merupakan sumber vitamin E yang baik. Selain itu, tanaman
wijen mengandung komponen lignan, yaitu sesamol, sesamin, dan sesamolin. Minyak
bunga matahari juga diketahui efektif digunakan dalam terapi oil pulling. Bunga
matahari kaya akan kandungan vitamin E dan rendah akan kandungan lemak jenuh.
Minyak kelapa dapat digunakan dalam terapi oil pulling karena mengandung asam
laurat yang terbukti bersifat antimikroba.12
2.5Minyak Kelapa
Minyak kelapa berdasarkan cara ekstraksinya digolongkan menjadi 2 jenis
yaitu, minyak kelapa murni atau VCO (Virgin Coconut Oil) dan minyak kelapa
komersil atau RBD (Refined, Bleached and Deodorized) coconut oil. Minyak kelapa
terlebih dahulu menjadi kopra. Kopra kemudian dilakukan proses pengepresan untuk
mendapatkan ekstrak minyak kelapa. Selanjutnya, ekstrak minyak kelapa ini perlu
dilakukan proses penyulingan (refining), pemutihan (bleaching) dan penghilangan
bau (deodorizing) agar dapat dikonsumsi.16,30
2.5.1 Taksonomi Tanaman Kelapa
Secara taksonomi, tanaman kelapa diklasifikasikan sebagai berikut:31
Kingdom : Plantae (Tumbuhan)
Subkingdom : Viridaeplantae (Tumbuhan hijau)
Infrakingdom : Streptophyta (Tanaman darat)
Divisi : Tracheophyta (Tumbuhan berpembuluh)
Subdivisi : Spermatophyta (Tumbuhan berbiji)
Infradivisi : Angiosperma (Tumbuhan berbunga)
Kelas : Magnoliopsida (Tumbuhan berkeping dua/dikotil)
Superordo : Lilianae
Ordo : Arecales
Famili : Arecaceae
Genus : Cocos L.
Spesies : Cocos nucifera L.
2.5.2 Mekanisme Aksi Berkumur dengan Metode Oil Pulling Menggunakan Minyak Kelapa
Kemampuan menghambat pembentukan plak melalui berkumur dengan
metode oil pulling dikarenakan sifat kekentalan dari minyak kelapa, di mana melalui
sifat kekentalan tersebut dapat menghambat adhesi bakteri dan koagregasi plak.
Mekanisme lainnya yang mungkin yaitu proses saponifikasi atau proses pembentukan
lapisan seperti sabun. Sabun merupakan agen emulsifikasi yang berperan sebagai
agen pembersih yang baik sehingga akan menyingkirkan plak dan sel skuamosa
superfisial yang rusak.6,9,12
Minyak kelapa mengandung substansi bioaktif yaitu tocopherols, tocotrienols,
phytosterols, phytostanols, phospholipids, flavonoids dan polyphenols lainnya.
Tocopherols dan tocotrienols merupakan agen antioksidan yang berperan dalam
mengurangi injuri radikal bebas. Tocotrienols memiliki kemampuan antioksidan yang
lebih baik dari pada daripada tocopherols dan oleh karenanya merupakan inhibitor
yang lebih efektif dalam mengurangi peroksidasi lemak dan oksidasi protein.
Phytosterols diketahui dapat menurunkan kadar kolesterol dalam darah terutama Low
Density Lipid (LDL), mengurangi gejala pembesaran prostat, memperbaiki kontrol
gula darah pada penderita diabetes, mengurangi inflamasi pada pasien penderita
penyakit autoimun, seperti rhematoid arthritis dan lupus. Phytostanols merupakan
bentuk phytosterols jenuh yang juga berperan dalam menurunkan kadar kolesterol.
Phenols dapat mempengaruhi proses karsinogenesis melalui beberapa mekanisme,
salah satunya dengan mencari bahan karsinogen atau radikal bebas. Flavonoids
berperan sebagai antivirus, anti-alergi, antiplatelet, anti-inflamasi, antitumor, dan
antioksidan.16
Sekitar 92,92 ± 0,56 % dari kandungan asam lemak pada minyak kelapa
berupa asam lemak jenuh (Saturated Fatty Acid/SFAs), terdiri dari asam kaprilat6,21
± 0,34 %; asam kaprat 6,15 ± 0,21 %; asam laurat 51,02 ± 0,71 %; asam miristat
18,94 ± 0,63%; asam palmitat 8,62 ± 0,50 %; asam stearat 1,94 ± 0,17 %. Sisanya
berupa asam lemak tak jenuh (Unsaturated Fatty Acids/UFAs) sebesar 7,12 ± 0,51 %
kaprilat, kaprat, dan laurat tergolong asam lemak rantai sedang (Medium Chain Fatty
Acid/MCFAs) yang memiliki aktivitas antivirus, antifungi, antibakteri, dan
antiprotozoa.33 Asam linoleat merupakan salah satu asam lemak tak jenuh ganda yang
paling penting pada makanan manusia karena dapat mencegah penyakit
kardiovaskular.34 Kandungan asam lemak tak jenuh tersebut dipercaya menurunkan
peroksidasi lemak dan memiliki sifat anti-inflamasi. Kemampuan menurunkan
peroksidasi lemak dan sifat antioksidan pada minyak kelapa mampu mengurangi
injuri radikal bebas yang dihasilkan dari proses fagositosis bakteri oleh neutrofil.
Sifat anti-inflamasi dan kemampuan mengurangi injuri radikal bebas tersebut akan
2.6Kerangka Teori
Berkumur dengan Metode OilPulling Menggunakan Minyak Kelapa
2.7Kerangka Konsep
Variabel Bebas:
Minyak kelapa yang
dikumur dengan metode oil
pulling
Variabel Terikat:
Skor indeks plak
Skor indeks gingiva
Variabel Terkendali:
Volume minyak kelapa
Lama berkumur dengan
metode oil pulling
Frekuensi berkumur dengan
metode oil pulling
Frekuensi dan waktu
menyikat gigi
Metode menyikat gigi
Variabel Tak Terkendali: