LAMPIRAN 1
DATA HASIL PERCOBAAN
L1.1 DATA HASIL PERCOBAAN
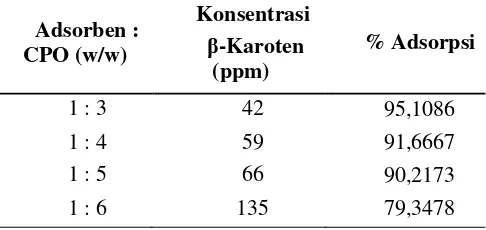
Berikut merupakan hasil analisa β-karoten dengan konsentrasi awal β-karoten
sebesar 552 ppm menggunakan spektrofotometer UV-Vis (Ultraviolet-Visible).
L1.2 DATA HASIL PERHITUNGAN
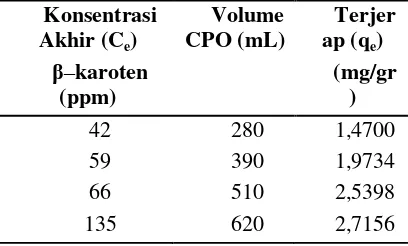
Berikut merupakan data hasil perhitungan untuk mencari jumlah β – karoten yang
terjerap oleh karbon aktif dengan konsentrasi awal (Co) β – karoten sebesar 552 ppm.
L1.2.4 Data Untuk Isoterm Adsorpsi Langmuir Pada T = 40 oC, 50 oC dan 60 oC
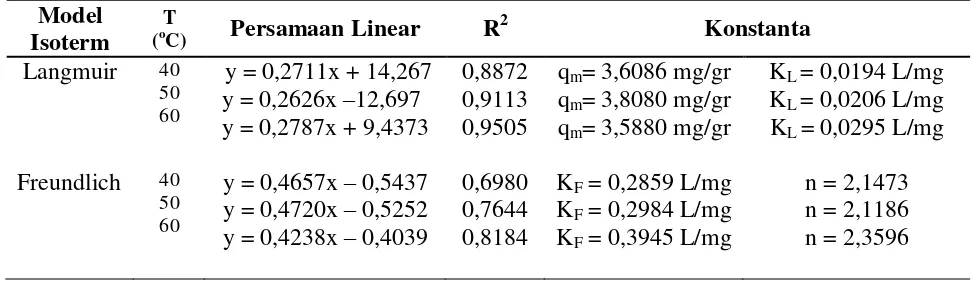
L1.2.6 Data Hasil Isoterm Adsorpsi β-Karoten
Tabel L1.9 Data Hasil Isoterm Adsorpsi β-Karoten
Model
L1.2.7 Data Untuk Penentuan Model Kinetika Adsorpsi Pada T = 60 ⁰C
Tabel L1.10 Data Untuk Penentuan Model Kinetika Adsorpsi Pada T = 60 ⁰C
Adsorben :
L1.2.8 Data Model Kinetika Adsorpsi β-Karoten
Tabel L1.11 Data Model Kinetika Adsorpsi β-Karoten
Model Kinetika
Persamaan
R
2Konstanta
Orde Satu Lagergen
y = -0,0125x - 0,0676 0,9869
-0,0287
Orde Dua
Difusi Intra Partikel
y = 0,3232x + 1,0142
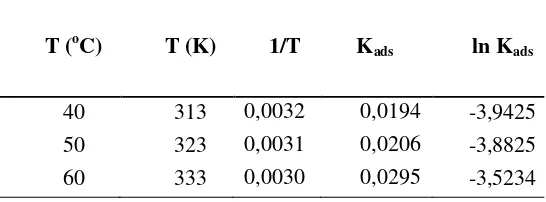
L1.2.9 Data Untuk Termodinamika Adsorpsi β-Karoten
Tabel L1.12 Data Untuk Termodinamika Adsorpsi β-Karoten
T (oC) T (K) 1/T Kads ln Kads
40 313 0,0032 0,0194 -3,9425 50 323 0,0031 0,0206 -3,8825
L1.2.10 Data Hasil Termodinamika Adsorpsi β-Karoten
Tabel L1.13 Data Hasil Termodinamika Adsorpsi β-Karoten
T (oC)
T
(K) ΔG (J/mol)
ΔS
(J/mol K)
ΔH (J/mol)
40 313 -24.482,4845
22,5575 -17.421,9870 50 323 -24.708,0595
LAMPIRAN 2
CONTOH HASIL PERHITUNGAN
L2.1 PERHITUNGAN PERSENTASE ADSORPSI
Dalam perhitungan persentase adsorpsi digunakan Persamaan L2.1 Maka untuk
contoh perhitungan persentase adsorpsi β-karoten diambil adsorben : CPO (1:3) pada
waktu 120 menit dan jumlah adsorben 100 gram.
% Adsorpsi = x100%) (L2.1)
Diketahui: Co = 552 mg/L
Ce = 27 mg/L
Maka :
% Adsorpsi = x100%)
= 95,1086 %
L2.2 PERHITUNGAN JUMLAH β-KAROTEN YANG DIJERAP
Dari Persamaan L2.2 dapat dihitung β-karoten yang dijerap oleh adsorben. Maka
untuk contoh perhitungan jumlah β-karoten yang dijerap diambil adsorben : CPO (1:3),
jumlah adsorben sebesar 100 gram, volume CPO sebesar 280 mL, pada konsentrasi awal β-karoten sebesar 552 ppm, konsentrasi akhir β-karoten sebesar 27 ppm.
W = xV)
(L2.2)
Diketahui : Co = 552 mg/L 1 ppm = 1 mg/L
Ce = 27 mg/L
V = 280 mL = 0,280 L
m = 100 gram
Maka :
W = x 0,280 L)
L2.3 PERHITUNGAN KINETIKA ADSORPSI
Untuk perhitungan kinetika adsorpsi maka digunakan data dari hasil kinetika β
-karoten. Diplot hasil yang diperoleh sehingga akan didapatkan persamaan kinetika adsorpsi yang sesuai untuk penjerapan β-karoten dengan adsorben karbon aktif. Data untuk penentuan kinetika adsorpsi penjerapan β-karoten dapat dilihat pada Tabel L2.1.
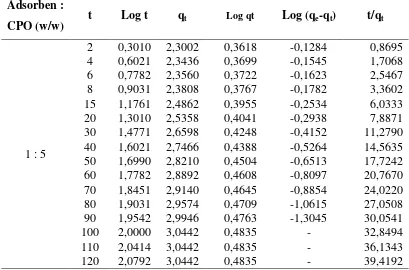
Tabel L2.1 Data Penentuan Kinetika Adsorpsi β-Karoten T = 60 oC
Adsorben :
CPO (w/w)
t
Log t
q
t Log qtLog (q
e-q
t)
t/q
t1 : 5
2
0,3010
2,3002
0,3618
-0,1284
0,8695
4
0,6021
2,3436
0,3699
-0,1545
1,7068
6
0,7782
2,3560
0,3722
-0,1623
2,5467
8
0,9031
2,3808
0,3767
-0,1782
3,3602
15
1,1761
2,4862
0,3955
-0,2534
6,0333
20
1,3010
2,5358
0,4041
-0,2938
7,8871
30
1,4771
2,6598
0,4248
-0,4152
11,2790
40
1,6021
2,7466
0,4388
-0,5264
14,5635
50
1,6990
2,8210
0,4504
-0,6513
17,7242
60
1,7782
2,8892
0,4608
-0,8097
20,7670
70
1,8451
2,9140
0,4645
-0,8854
24,0220
80
1,9031
2,9574
0,4709
-1,0615
27,0508
90
1,9542
2,9946
0,4763
-1,3045
30,0541
100
2,0000
3,0442
0,4835
-
32,8494
110
2,0414
3,0442
0,4835
-
36,1343
120
2,0792
3,0442
0,4835
-
39,4192
Persamaan Orde Satu Semu Lagergen
Diplot kurva t vs log (qe-qt) dengan slope adalah k1 dan instersep adalah
Gambar L2.1 Kinetika Orde Satu Semu Lagergen
Dari Gambar L2.1 diperoleh persamaan kinetika orde satu semu
Lagergen adalah y = -0,0125x - 0,0676 dengan R² = 0,9869. Maka untuk
mencari nilai dari k1 dapatdilihat pada cara berikut :
Persamaan Orde Dua
Diplot kurva vs
dengan slope adalah dan intersep adalah .
Kurva vs
dapat dilihat pada gambar L2.2
y = -0,0125x - 0,0676
R² = 0,9869
-1,40
-1,20
-1,00
-0,80
-0,60
-0,40
-0,20
0,00
0 10 20 30 40 50 60 70 80 90 100 110 120
t
log
(
q
e-q
tGambar L2.2 Kinetika Orde Dua
Dari Gambar L2.2 diperoleh persamaan kinetika orde dua adalah y =
0,323x + 1,0142 dengan R² = 0,9987. Maka untuk mencari nilai dari k2
dapat dilihat pada cara berikut :
Persamaan Difusi Intra Partikel
Diplot kurva log t vs log qt dengan slope adalah ndan instersep adalah
log k3 . Kurva log t vs log qt dapat dilihat pada Gambar L2.3
y = 0,323x + 1,0142
R² = 0,9987
0
5
10
15
20
25
30
35
40
45
0 10 20 30 40 50 60 70 80 90 100 110 120 130
t
t/q
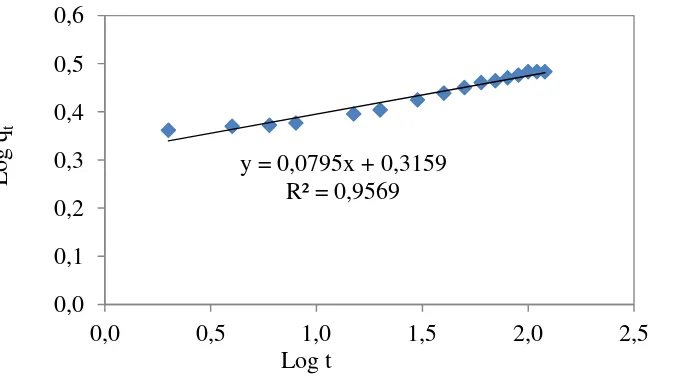
Gambar L2.3 Kinetika Difusi Intra Partikel
Dari Gambar L2.3 diperoleh persamaan kinetika difusi intra partikel
adalah y = 0,0795x + 0,3159 dengan R² = 0,9569. Maka untuk mencari
nilai k3 apat dilihat pada cara berikut :
L2.4 PERHITUNGAN ISOTERM ADSORPSI
Untuk contoh perhitungan isoterm adsorpsi digunakan data dari β-karoten yang
sudah terjerap. Dari hasil yang diperoleh dapat ditabelkan pada tabel dibawah :
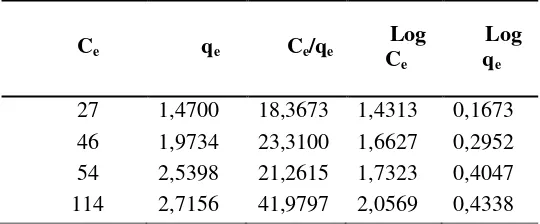
Tabel L2.2 Data Perhitngan Isoterm Adsorpsi T = 40 oC
Ce qe Ce/qe
Log Ce
Log qe
42 1,4280 29,4117 1,6232 0,1547 59 1,9227 30,6860 1,7709 0,2839 66 2,4786 26,6279 1,8195 0,3942 135 2,5854 52,2163 2,1303 0,4125
y = 0,0795x + 0,3159
R² = 0,9569
0,0
0,1
0,2
0,3
0,4
0,5
0,6
0,0
0,5
1,0
1,5
2,0
2,5
Log t
L
og
Tabel L2.3 Data Perhitngan Isoterm Adsorpsi T = 50 oC
Tabel L2.4 Data Perhitungan Isoterm Adsorpsi T = 60 oC
Ce qe Ce/qe
Diplot kurva isoterm yang dapat mewakili penjerapan β-Karoten.
Trial I (Isoterm Langmuir)
Gambar L2.4 Kurva Isoterm Langmuir Pada T = 40 oC, 50 oC dan 60 oC
Dari Gambar L2.4 untuk T = 40 oC diperoleh persamaan isoterm Langmuir adalah
y = 0,2711x + 14,267. Maka dapat dihitung nilai bqm dan qm seperti cara berikut :
0,2711=
qm=
qm= 3,6086
14,267 =
KL.qm =
KL. 3,6086 = 0,0701
KL=0,0194
Dari Gambar L2.4 untuk T = 50 oC diperoleh persamaan isoterm Langmuir adalah
y = 0,2626x + 12,697. Maka dapat dihitung nilai bqm dan qm seperti cara berikut :
0,2626 =
qm=
qm= 3,8080
12,697 =
KL.qm =
KL. 3,8080 = 0,0787
KL=0,0206
Dari Gambar L2.4 untuk T = 60 oC diperoleh persamaan isoterm Langmuir adalah
0,2787=
Trial II (Isoterm Freundlich)
Untuk isoterm adsorpsi Freundlich akan diplot kurva log Ce Vs loq qe. Kurva
tersebut akan memberikan nilai slope adalah 1/n dan intersep adalah log KF. Kurva
isoterm Freundlich dapat dilihat pada Gambar L2.5.
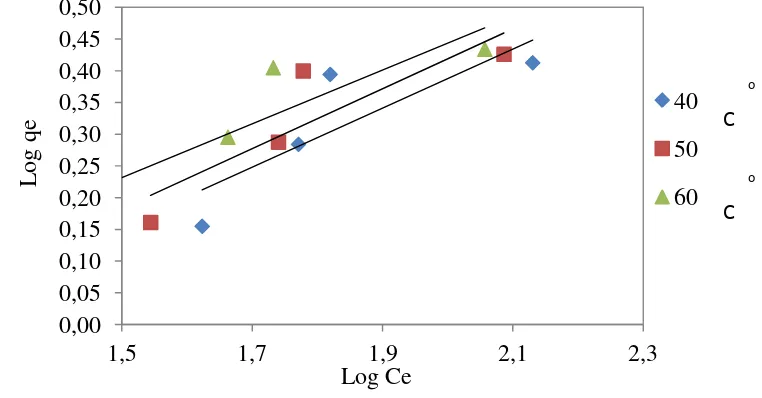
Gambar L2.5 Kurva Isoterm Freundlich Pada T = 40 oC, 50 oC dan 60 oC
Dari Gambar L2.2 untuk T = 40 oC diperoleh persamaan isoterm Freundlich adalah
y = 0,4657x - 0,5437. Maka dapat dihitung nilai n dan k seperti cara berikut :
KF = 10 -0,5437
.
KF = 0,2859
0,4657 =
n =
n = 2,1473
Dari Gambar L2.2 untuk T = 50 oC diperoleh persamaan isoterm Freundlich adalah
y = 0,472x - 0,5252. Maka dapat dihitung nilai n dan k seperti cara berikut :
-0,5252 = log KF
KF = 10 -0,5252
KF = 0,2984
0,472 =
n =
n = 2,1186
Dari Gambar L2.2 untuk T = 60 oC diperoleh persamaan isoterm Freundlich adalah
y = 0,4238x - 0,4039. Maka dapat dihitung nilai n dan k seperti cara berikut :
- 0,4039= log KF
KF = 10 - 0,4039
KF = 0,3945
0,4238=
n =
Parameter Kesetimbangan (RL)
Karakteristik dari adsorpsi isoterm Langmuir dapat dinyatakan dengan
parameter kesetimbangan (RL). Persamaan untuk parameter kesetimbangan dapat
dihitunga dengan cara :
L2.5 PERHITUNGAN TERMODINAMIKA ADSORPSI
Perhitungan termodinamika adsorpsi dapat dihitung dengan memplot kurva 1/T vs
ln Kads. Data yang digunakan dapat dilihat pada Tabel L2.5.
Tabel L2.5 Data Perhitungan Untuk Termodinamika Adsorpsi β-Karoten
T (oC) T (K) 1/T Kads ln Kads
40 313 0,0032 0,0194 -3,9425
50 323 0,0031 0,0206 -3,8825
60 333 0,0030 0,0295 -3,5234
Gambar L2.6 Kurva Temodinamika Adsorpsi β-Karoten
y = -2095,5x + 2,7133
R² = 0,8549
-4,1
-4
-3,9
-3,8
-3,7
-3,6
-3,5
-3,4
0,00295 0,003 0,00305 0,0031 0,00315 0,0032 0,00325
1/T
ln
K
adY = -2095x + 2,7132
Ln Kads =
Perhitungan Energi Bebas Gibbs.
-24.482,4845 J/mol
-24.708,0595 J/mol
- 24.933,6345 J/mol
Tabel L2.6 Data Hasil Perhitungan Termodinamika Adsorpsi β-Karoten
T (oC)
T
(K) ΔG (J/mol)
ΔS
(J/mol K)
ΔH (J/mol)
40 313 -24.482,4845
22,5575 -17.421,9870 50 323 -24.708,0595