BAB 2
TINJAUAN PUSTAKA
2.1 Jeruk Lemon (Citrus limon burm f.)
Lemon (Citrus limon) merupakan tanaman asli Asia Tenggara (Manner et al, 2006). Lemon pertama kali tumbuh di India, Burma utara dan Cina. Pada tahun 1493, Christopher Colombus membawa biji Citrus limon ke Hispaniola. Budidaya Citrus limon pertama kali di Genoa pada pertengahan abad ke 15. Pada abad ke 18 dan abad 19, Citrus limon ditanam di Florida dan California. Bagian dari tanaman Citrus limon yang sering dimanfaatkan adalah kulit buah, bunga, daun, air perasan (Sauls, 1998).
Jeruk lemon (Citrus limon (L.) Burm. f.) termasuk salah satu jenis tumbuhan perdu yang banyak memiliki dahan dan ranting dengan tinggi maksimal mencapai 10 sampai 15 kaki (3-6 m). Citrus limon memiliki batang berduri, daun hijau dan lonjong, bunga berbentuk oval dan berwarna putih dengan garis-garis ungu didalamnya. Buah Citrus limon berukuran 7-12 cm dan berbentuk bulat telur dengan ujung yang runcing pada salah satu ujungnya. Kulit Citrus limon berwarna kuning terang, kadang terdapat garis berwarna hijau atau putih dan mempunyai tebal sekitar 6-10 mm. Daging buah Citrus limon berbulir, berwarna kuning pucat, terdapat sekitar 8-10 segmen, bersifat juicy dan mempunyai rasa asam (Morton, 1987, p.160).
Gambar 2.1 Jeruk lemon (Citrus limon burm f.) (Morton, 1987, p.160)
2.1.1 Klasifikasi Jeruk lemon (Citrus limon burm f.)
Klasifikasi botani tanaman Citrus limon menurut Manner et al, (2006, p.2) : Kingdom : Plantae
Sub Kingdom : Tracheobionta Super Divisi : Spermatophyta Divisi : Magnoliophyta
Kelas : Magnoliopsida-Dicotyledons Sub Kelas : Rosidae
Ordo : Sapindales Famili : Rutaceae Genus : Citrus
2.1.2 Kandungan Kimia dan Manfaat
Citrus limon mengandung sejumlah asam sitrat (3,7%), minyak atsiri (2,5%), 70% limoneme penine. Citrus limon juga mengandung potassium 145 mg per 100 g lemon, bioflavonoids, dan vitamin C 40-50 mg per 100 g (Chevallier, 1996, p.81).
Senyawa kimia dalam buah Citrus limon (Stanway, 2011, p.8) terdiri dari: a. Asam sitrat
Rumus kimia asam sitrat adalah C6H8O7. Asam sitrat termasuk salah satu asam organik dengan nama kimia 2-hydroxy-1,2,3-propanetricarboxylic acid (Lewis, 2001, p.1205.). Kandungan asam sitrat dalam air perasan Citrus limon dapat membantu memindahkan cairan yang berlebih dari dalam jaringan ke dalam pembuluh darah, sehingga mengurangi kemampatan jaringan dan darah mengalir dengan bebas. Asam sitrat lebih cepat mengerosi enamel gigi terutama pada pH rendah, 1,5 dan 2,5. Asam ini dua kali lebih destruktif terhadap enamel gigi dari pada asam klorida ataupun asam nitrat karena afinitasnya yang tinggi terhadap kalsium.
b. Asam Askorbat (vitamin C)
Citrus limon juga kaya akan vitamin C. Bentuk utama vitamin C adalah asam askorbat (ascorbic acid) dengan rumus C6H8O6 (Molina et al, 2010, p.329).
Kadar vitamin C yang dibutuhkan tubuh hanya berkisar 90 mg (US) dan 75 mg (UK), sedangkan dalam satu buah Citrus limon mengandung vitamin C 60-100 mg. Jadi satu buah Citrus limon dapat melengkapi kebutuhan tubuh.
c. Glucaric acid
Glucaric acid dapat menurunkan kadar kolesterol dalam darah, mencegah kanker usus dan radang usus dengan mengeluarkan butyric acid dalam usus besar, mencegah kanker payudara, kanker prostat, kanker ovarium, mencegah pre menstruasi sindrom dengan mendorong glucoronidation dan mengurangi kadar polusi dalam tubuh.
d. Polifenol
Citrus limon mengandung polifenol sebagai antioksidan dan antibakteri terhadap Staphylococcus aureus, Bacillus subtillis, Salmonella typhi, Klebsiella pneumonia, dan E. coli (Kumar et al, 2011, p.5421) dan memiliki efek anti fungi Candida albicans (Kirbaslar et al, 2009, p.3212).
Polifenol pada Citrus limon (Grohmann & Manthey 2001, p.3268) meliputi:
1. Flavonoid
Flavonoid dalam Citrus limon menyebabkan warna kuning terang yang berguna untuk melindungi kekuatan vitamin C dengan meningkatkan absorpsi dan melindungi dari oksidasi, mengurangi kadar kolesterol sampai 40% dengan mengurangi produksi kolesterol pada liver, dapat mengurangi resiko penyakit jantung, mencegah kanker, menguatkan dinding pembuluh darah. Flavonoid yang water-soluble antara lain citrin, bioflavonoid. Kadar flavonoid paling tinggi terdapat pada kulit Citrus limon.
2. Coumarins
Coumarins paling banyak terdapat pada kulit Citrus limon dan berminyak. Kadar coumarins pada kulit Citrus limon lebih tinggi daripada bulir Citrus limon. Coumarins bersifat sebagai antioksidan.
3. Limonene
Limonene ditemukan pada seluruh bagian Citrus limon, namun paling banyak terdapat pada pith dan pips. Limonene menyebabkan rasa pahit pada Citrus limon. Penelitian telah membuktikan bahwa limonene dapat membantu mencegah multiplikasi sel kanker pada mulut, payudara, kulit, paru-paru, kolon. Limonene juga dapat mengurangi kadar kolesterol pada liver.
4. Tanin
Tanin ditemukan pada kulit dan daun Citrus limon. Tanin berfungsi sebagai anti bakteri dan antioksidan. Tanin menyebabkan rasa Citrus limon menjadi agak pahit dan asam.
5. Fenol
Fenol terdapat pada kulit, daun dan air perasan Citrus limon. Fenol berfungsi sebagai anti bakteri, antifungi dan antioksidan. Fenol pada Citrus limon dapat mengurangi kolesterol dalam darah sehingga dapat mengurangi resiko penyakit jantung.
2.2 Jaringan Keras Gigi
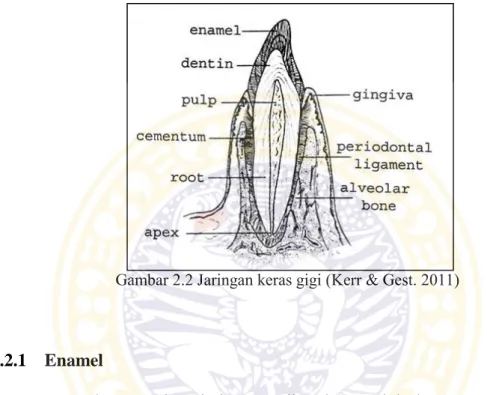
Struktur gigi terdiri dari jaringan keras dan jaringan lunak. Jaringan keras gigi adalah jaringan yang melindungi jaringan lunak gigi, yaitu pulpa. Struktur jaringan keras terdiri dari enamel, dentin, dan sementum (Gambar 2.2). Dentin
merupakan lapisan terbesar gigi yang mengelilingi rongga pulpa, paling tebal di bagian mahkota dan menipis ke arah apeks akar gigi. Enamel melapisi mahkota gigi dan paling tipis di daerah leher. Pada akar gigi, dentin dilapisi sementum tipis yang meluas dari leher ke foramen apikal (Fawcett, 2002, p.516).
Gambar 2.2 Jaringan keras gigi (Kerr & Gest. 2011)
2.2.1 Enamel
Enamel merupakan jaringan paling keras gigi dan merupakan sistem biologis kompleks yang dibentuk oleh sel-sel ameloblast dari lapisan embrional ectoderm. Satu ameloblas membentuk tiap enamel rods berdiameter 6 µm. Struktur dasar enamel terdiri dari berjuta-juta batang enamel atau enamel rods, sekitar 5 juta pada gigi insisif rahang bawah sampai 12 juta pada gigi molar rahang atas (Roberson et al, 2002, p.16). Enamel melapisi mahkota gigi dan memiliki ketebalan yang bervariasi. Ketebalan enamel semakin menipis dari insisal edge atau oklusal ke cementoenamel junction (batas antara sementum dan enamel). Ketebalan enamel sekitar 1-2 mm pada gigi permanen dan 0,5-1mm pada gigi sulung, sedangkan ketebalan enamel pada insisal ridge gigi insisif dan
kaninus 2,3-2,5 mm, dan 2-3 mm pada cusp gigi molar. Kepadatan enamel adalah sekitar 2,9 g/cm3 (Roberson et al, 2002, p.17).
Enamel memiliki komposisi struktur kristal mineral yang tinggi, terdiri dari 99% bahan anorganik yaitu hidroksi apatit (Ca10(PO4)6(OH)2), dan 1% bahan
organik (Roberson et al, 2002, p.17). Williams & Elliot (1979, p.311) menyusun komposisi mineral enamel normal secara rinici mulai dari jumlah terbesar yaitu Ca, P, CO2 , Na, Mg, Cl dan K, hingga jumlah kecil yaitu F, Fe, Zn, Sr, Cu, Mn,
Ag. Garam-garam mineral organik enamel tersusun dalam bentuk jaringan-jaringan kecil yaitu terdiri dari :
a. Keratin (pseudokeratin) : C4H9N3O2
b. Protein : enamelins, amelogenins dan albumin) c. Kolagen : Hydroxyproline, C5H9O3N
d. Lemak : CH3(CH2)2CO2H
e. Asam-asam amino lainnya : Aspartic acid, Threonine, Serine, Glutamic acid, Proline, Glycine, Alanine, Valine, Methionine, Isoleucine, Leucine, Tyrosine, Phenylalanine, Lysine, Histidine, Arginine.
Fase mineral enamel terdiri dari kristal halus hidroksi apatit berbentuk heksagonal yang membentuk prisma berbentuk rod-like kristal bersama dengan organik material. Susunan batang enamel dimulai dari pertautan dentin-enamel/dentinoenamel junction dan berakhir pada permukaan enamel. Batang enamel tersusun tegak lurus terhadap permukaan dentin dan mengikuti pola spiral menuju permukaan, yang berakhir dengan sudut hampir tegak lurus pada permukaan (Roberson et al, 2002, p.17).
Enamel gigi (Roberson et al, 2002, p.18-19) terdiri dari : 1. Gnarled enamel
Gnarled enamel adalah enamel rods yang berjalan mengikuti pola spiral dan berbentuk kurva yang tidak teratur menuju ke permukaan gigi, terletak pada insisal atau oklusal dan servikal gigi.
2. Enamel tufts
Enamel tufts adalah enamel rods yang hipomineralisasi, berjalan dari dentin ke enamel sepanjang mahkota gigi. Penyebaran karies terjadi pada bagian ini.
3. Enamel lamellae
Bagian ini sangat lemah, terletak dari enamel menuju ke dentinoenamel junction kadang-kadang sampai ke dentin. Bagian ini mengandung bahan organik lemah, tempat masuknya bakteri, sehingga dapat menyebabkan karies gigi.
4. Enamel spindles
Enamel spindles adalah proses odontoblastik dari dentinoenamel junction ke enamel. Enamel spindles sebagai reseptor rasa sakit dari enamel yang sensitif selama proses preparasi kavitas.
5. Incremental striae of Retzius
Enamel rods yang tersusun linier dan menghasilkan struktur dan mineralisasi yang bervariasi. Pada potongan transversal terlihat concentric circles. Pada potongan longitudinal tampak garis melintang pada daerah cusp dan insisal, terus menurun membentuk garis miring ke servikal gigi yang berakhir pada dentinoenamel junction.
6. Dentinoenamel junction (DEJ)
Dentinoenamel junction adalah pertautan antara enamel dan dentin, hipermineralisasi dengan ketebalan 30 µm.
7. Nasmyth membrane/primary enamel cuticle
Nasmyth membrane/primary enamel cuticle adalah membran inti yang melapisi gigi yang baru erupsi dan selama proses pengunyahan dan pembersihan gigi, membran diganti dengan deposit bahan organik yang disebut pelikel yang berasal dari endapan protein saliva.
Enamel merupakan struktur yang memiliki modulus elastisitas tinggi dan kekuatan tarik rendah, tetapi enamel masih dapat ditembus oleh ion-ion dan molekul melalui struktur yang hipomineralisasi. Enamel dapat terlarut atau terbuka oleh karena asam, kelarutan ini meningkat pada dentinoenamel junction. Kekerasan enamel terbesar pada permukaan dan semakin berkurang pada dentinoenamel junction. Densitas enamel juga semakin berkurang pada dentinoenamel junction (Roberson et al, 2002, p.19).
2.2.1.1 Sifat-sifat Enamel
Enamel gigi merupakan jaringan paling stabil dalam tubuh manusia. Jaringan ini tidak mengandung persarafan, sehingga tidak terasa sakit bila terjadi kerusakan pada enamel. Bahan kimia dan faktor lingkungan dapat mengubah struktur enamel, antara lain keasaman makanan dan minuman yang akan menyebabkan keausan enamel yang disebut demineralisasi gigi. Enamel tidak mempunyai kemampuan untuk menggantikan bagian-bagiannya yang rusak. Enamel merupakan suatu unsur bradytrophes yaitu jaringan yang paling sedikit
sekali mendapat makanan, melalui mikroskop elektron tidak ditemukan saluran makanan pada enamel. Secara mikroskopis struktur enamel berpori sehingga enamel mampu dilewati oleh ion dan molekul tertentu. Ion-ion saliva dapat berdifusi masuk ke dalam enamel, sehingga semakin bertambah umur pasien, maka semakin keras enamel. Kekerasan dan ketahanan kimia enamel berbeda dari dentin, tulang dan sementum. Walaupun empat jaringan ini termineralisasi oleh hidroksiapatit, tetapi terdapat dua perbedaan penting antara enamel dan jaringan lain. Pertama, tulang, dentin, dan sementum terdiri dari 20% kolagen sedangkan enamel hanya 0.6%. Kedua, kandungan kristal apatit enamel sepuluh kali lebih besar dan lebih tebal daripada yang dikalsifikasi kolagen sehingga volume kristal enamel 1000 kali lebih besar (Lussi & Jaeggi, 2008, p.55).
2.2.1.2 Kekerasan Enamel
Kekerasan permukaan luar gigi berbeda-beda tergantung pada lokasinya, dan kekerasannya akan berkurang menuju ke arah dentin. Kekerasan enamel makin ke arah dentin makin berkurang. Hal ini disebabkan kandungan mineral anorganik pada dentin dan sementum lebih rendah dari enamel (Roberson et al (2002, p.17). Enamel merupakan struktur yang sangat keras dan padat, namun enamel bersifat permeabel terhadap ion-ion dan molekul yang dapat berpenetrasi sebagian atau kompleks. Enamel dapat larut ketika berkontak dengan asam, sehingga larutnya sebagian atau keseluruhan mineral enamel akan menurunkan kekerasannya (Roberson et al, 2002, p.21).
Kekerasan enamel diukur dengan menggunakan alat Knoop (KHN) atau Vickers (VHN). Variasi kekerasan enamel disebabkan oleh gambaran histologi
gigi, komposisi kimiawi gigi, pembuatan sampel, beban yang digunakan pada pengukuran dan kesalahan membaca (reading error) pada intentional length (IL). Micro Vickers Hardness Tester adalah pengukuran kekerasan suatu material dengan nilai kekerasan yang kecil dengan indenasi yang lebih kecil. Rerata kekerasan enamel yang diukur berkisar 294-408 VHN (O’Brien, 2002, p.308).
2.2.1.3 Demineralisasi Enamel
Demineralisasi adalah hilangnya sebagian atau seluruh mineral enamel karena larut dalam asam. Semakin rendah pH asam maka meningkatkan ion hidrogen yang merusak hidroksiapatit enamel. pH kritis bagi hidroksiapatit adalah dibawah 5,5. Menurut Dawes, (2003, p.723) larutnya hidroksiapatit akan meningkat sepuluh kali lipat dengan setiap penurunan unit pH. Pada pH 7 larutnya hidroksiapatit sekitar 30 mg/L, sedangkan pada pH 4 sekitar 30 g/L. Demineralisasi enamel dapat disebabkan karies dan non karies. Demineralisasi non karies terdiri dari atrisi, abrasi dan erosi. Erosi dan karies gigi memiliki kesamaan dalam jenis kerusakan, yaitu demineralisasi jaringan keras gigi yang disebabkan asam, tetapi sumber asam penyebab erosi berbeda dengan karies. Erosi gigi terjadi akibat asam dari makanan-minuman, uap asam yang berasal dari industri serta asam lambung yang secara langsung berkontak dengan gigi tanpa adanya aktivitas bakteri. Karies berasal dari asam yang merupakan hasil fermentasi karbohidrat sisa-sisa makanan oleh bakteri. Perbedaan lainnya juga dapat dilihat dari morfologi dan proses terjadinya erosi dan karies. Erosi terjadi secara merata di permukaan gigi sedangkan karies lebih terlokalisasi, dengan arah kerusakan ke dalam dan memerlukan waktu yang lebih lama. Pada tahap awal,
erosi kurang disadari oleh penderita sebab tidak terjadi perubahan warna dan bukan berbentuk lubang.Gejala awal erosi adalah suatu bercak putih yang secara mikroanatomi terlihat bulat, licin, dan mengkilap. Pada tahap lanjut, semakin banyak enamel hilang, permukaan gigi semakin licin dan mengkilap serta permukaan yang membulat pada elemen gigi menjadi rata (Pintauli dan Hamada, 2008, p.22).
Pada saat asam berkontak dengan enamel maka ion hidrogen pada larutan asam mulai melarutkan kristal enamel. Mula-mula, daerah selubung prisma (prisma sheath) melarut dan berlanjut ke inti prisma, membentuk permukaan yang dikenal dengan sarang lebah. Kemudian asam yang tidak berionisasi (anion) berdifusi ke dalam daerah interprismatik pada enamel gigi dan melarutkan lebih lanjut mineral pada daerah bagian bawah permukaan enamel. Struktur prisma enamel menjadi irreguler diikuti dengan derajat hilangnya enamel yang bervariasi dari satu tempat ketempat lain (Lussi & Jaeggi, 2008, p.55). Menurut Dawes (2003, p.722), apabila hidroksiapatit berkontak dengan minuman asam, reaksi yang terjadi sebagai berikut (Gambar 2.3):
Presipitation ↔ Demineralisasi Ca10(PO4)6(OH)2 ↔ 10 Ca2+ + 6PO43-+2OH Solid ↔ Solution
Sejumlah kecil hidroksiapatit terurai melepaskan kalsium, fosfat, dan ion hidroksil. Pada proseus acidification (berkontak dengan asam) OH- akan diubah
oleh H+ menjadi H
20 dan PO43- akan diubah menjadi HPO42-, yang apabila kontak
dengan asam lebih lama maka akan berubah menjadi H2PO4-. Ini akan
menyebabkan berkurangnya OH- dan PO
43- pada persamaan di sebelah kanan.
Apabila mencapai tahap akhir, bahan yang solid akan masuk ke dalam larutan (Fathilah dan Rahim, 2008, p.2).
Kalsium merupakan unsur utama dalam struktur gigi dan demineralisasi terjadi karena lepasnya ion kalsium dari enamel gigi, maka pengaruh asam pada enamel gigi merupakan reaksi penguraian. Beberapa faktor yang mempengaruhi proses demineralisasi, yaitu jenis dan konsentrasi asam minuman yang tidak berdisosiasi, kandungan karbohidrat dalam minuman, pH dan kapasitas buffer minuman serta kandungan fosfat dan f1uor yang ada dalam minuman. Demineralisasi yang terus menerus akan membentuk pori-pori kecil pada enamel yang disebut juga porositas pada permukaan enamel yang sebelumnya tidak ada, yang dapat menyebabkan kekerasan enamel menurun (Edhie, 2005, p.61).
2.3 Uji kekerasan permukaan
Kekerasan permukaan secara umum dapat didefinisikan sebagai ketahanan suatu benda terhadap daya penetrasi oleh suatu beban yang telah dispesifikasikan. Untuk mengetahui nilai kekerasan permukaan suatu benda, digunakan alat pengukur kekerasan. Secara umum, angka uji kekerasan didapatkan dengan cara membagi beban yang dijatuhkan pada spesimen dengan luas atau kedalaman area yang didapatkan, sehingga semakin kecil area, maka semakin besar angka
kekerasan dan semakin keras bahan tersebut. Semakin rendah angka kekerasan, mengindikasikan suatu bahan yang lunak. Nilai kekerasan berhubungan dengan derajat deformitas permanen suatu permukaan bahan yang di beri beban tertentu (Mc Cabe & Walls, 2008, p.145).
Penggunaan jenis uji kekerasan ditentukan berdasarkan bahan yang akan diuji. Uji kekerasan dilakukan berdasarkan kemampuan permukaan bahan untuk menahan penetrasi dari bahan tertentu. Prinsip pengujian Vickers Hardness Test adalah dengan menekankan ujung penguji ke permukaan benda dengan beban dan waktu tertentu. Beban penguji berupa intan berbentuk piramida dengan sudut permukaan piramida 136˚, yang menunjukkan tekanan yang tinggi saat kontak dengan bahan yang diuji (Anusavice, 2003, p.97). Beban berhenti saat tekanan yang diberikan ekuivalen dengan batas elastisitas bahan uji (Mc Cabe & Walls, 2008, p.170). Setelah dilakukan uji, dilakukan perhitungan untuk mendapatkan nilai Vickers Hardness Number (VHN) dengan rumus (ADA, 1974) :
HV = 1,8544 x L/d2
Keterangan :
HV : Hardness Vickers (nilai kekerasan Vickers) (kg/mm2)
L : Beban yang digunakan (kg)
d : Panjang diagonal (mm) = (D1 + D2)/2
1,8544 : 2 sin a/2
a : sudut yang dibentuk ujung penguji (136˚)
Micro Vickers Hardness Tester merupakan pengukuran kekerasan suatu material dengan nilai kekerasan yang kecil dan indentasi yang lebih kecil. Beban yang digunakan adalah antara 1-1.000 gram (Anusavice, 2003, p.98).