BAB II
TINJAUAN PUSTAKA
2.1 BIJI PEPAYAPepaya merupakan tanaman monodioecious (berumah tunggal sekaligus berumah dua) dengan 3 kelamin yaitu tumbuhan jantan, betina dan hermafrodit. Biasanya bunga jantan dan bunga betina susah dibedakan, namun sekitar 6 bulan setelah perkecambahan baru terlihat perbedaannya. Bunga jantan lebih tipis dan menempel pada tangkai yang pendek, sedangkan bunga betina lebih lebar dan menempel langsung pada batang.
Tata nama tanaman pepaya (Carica papaya) sebagai berikut: Kingdom : Plantae Subkingdom : Tracheophyta Divisio : Spermatophyta Subdivisio : Angiospermae Kelas : Magnoliopsida Subkelas : Dicotyledoneae Ordo : Brassicales Famili : Caricaceae Genus : Carica
Jenis : Carica papaya Linn [13]
Salah satu tanaman yang dapat dimanfaatkan sebagai obat tradisional adalah tanaman pepaya (Carica papaya L). Seluruh bagian pepaya dari akar sampai ujung daunnya, termasuk bunga dan buahnya memiliki nilai medis yang tinggi [14]. Pepaya disebut multiguna karena memiliki banyak manfaat antara lain sebagai bahan makanan dan minuman, pakan ternak, bahan kosmetik, industri, serta bahan obat tradisional. Meskipun bagian-bagian pepaya banyak dimanfaatkan dalam berbagai bidang, tetapi manfaat biji pepaya masih belum banyak diketahui masyarakat [15].
Kandungan biji pepaya merupakan hal yang sangat penting dalam pembuatan biosorben. Hal ini merupakan salah satu karakteristik yang dijadikan acuan dalam pembuatan biosorben, karena kandungan tersebut sangat menentukan dalam pemanfaatan biji pepaya sebagai pembuatan biosorben yang digunakan untuk penyerapan zat warna. Berikut kandungan biji pepaya dapat di lihat pada Tabel 2.1:
Tabel 2.1 Kandungan Senyawa Kimia Biji Pepaya
No. komposisi Jumlah (%)
1. Lemak majemuk 25 2. Lemak 26 3. Protein 24,3 4. Serat 17 5. Karbohidrat 15,5 6. Abu 8,8 7. Air 8,2
Apabila dikaitkan dengan senyawa aktif dari tanaman ini ternyata banyak di antaranya mengandung alkaloid, steroid, tanin dan minyak atsiri. Dalam biji papaya mengandung senyawa-senyawa steroid. Kandungan biji dalam buah papaya kira-kira 14,3 % dari keseluruhan buah papaya. Kandungannya berupa asam lemak tak jenuh yang tinggi, yaitu asam oleat dan palmitat. Selain mengandung asam-asam lemak, biji pepaya diketahui mengandung senyawa kimia lain seperti golongan fenol, alkaloid, terpenoid dan saponin. Zat-zat aktif yang terkandung dalam biji pepaya tersebut bisa berefek sitotoksik, anti androgen atau berefek estrogenic. Alkaloid salah satunya yang terkandung dalam biji pepaya dapat berefek sitotoksik. Efek sitotoksik tersebut akan menyebabkan gangguan metabolisme sel spermatogenik [17].
2.2 BIOSORBEN
Adsorben banyak digunakan di industri – industri untuk kepentingan pemurnian suatu campuran. Keefektifan adsorben tergantung pada performa adsorben dilihat dari keseimbangan dan kinetika penyerapan suatu adsorbat di dalam adsorben tersebut [18]. Adsorben yang menjanjikan adalah adsorben yang berasal dari limbah organik seperti limbah tanaman jagung, padi, pisang dan lain-lain. Kelemahan dari adsorben organik adalah kapasitas penyerapannya yang rendah [19].
Adsorben mempunyai banyak jenis diantaranya, karbon aktif merupakan yang paling banyak digunakan untuk menghilangkan kromium dari larutan encer karena mempuyai poros, adsorp yang tinggi dan murah [20].
Karbon aktif didefinisikan sebagai bahan yang mengandung karbon dengan luas permukaan internal yang besar dan struktur berpori kompleks yang dihasilkan dari pengolahan bahan baku pada reaksi suhu tinggi. Karbon aktif terdiri dari 87 sampai 97% karbon tetapi juga mengandung unsur-unsur lain tergantung pada bahan baku dan metode pengolahan yang digunakan. Struktur berpori karbon aktif memungkinkan karbon aktif tersebut untuk menyerap bahan-bahan berfasa cair dan gas [21]. Ketika pemanasan berlangsung, diusahakan tidak terjadi kebocoran udara didalam ruangan pemanasan sehingga bahan yang mengandung karbon tersebut hanya terkarbonisasi dan tidak teroksidasi [22].
Arang aktif merupakan senyawa karbon amorf yang dapat dihasilkan dari bahan – bahan yang mengandung karbon atau dari arang yang diperlakukan dari cara khusus untuk mendapatkan permukaan yang lebih luas. Luas permukaan arang aktif berkisar antara 300 – 3500 m2/gram dan ini berhubungan dengan struktur pori internal yang menyebabkan arang aktif mempunyai sifat sebagai adsorben. Arang aktif dapat mengadsorpsi gas dan senyawa – senyawa kimia tertentu atau sifat adsorpsinya selektif, tergantung pada besar atau volume pori – pori dan luas permukaan. Daya serap arang aktif sangat besar yaitu 25 – 100% terhadap berat arang aktif [23].
Karbon aktif dibuat dengan mengaktifasi arang dengan tujuan untuk memperbesar luas permukaan arang dengan membuka pori-pori yang tertutup, sehingga memperbesar kapasitas adsorpsi terhadap zat warna. Karbon aktif sebagai bahan pemucat lebih efektif untuk menyerap warna dibandingkan dengan bleaching
clay. Penggunaan karbon aktif sebaiknya menggunakan yang berbentuk serbuk
karena memiliki daya serap yang lebih bagus dibandingkan dengan karbon aktif yang berbentuk granula [24].
Karbo aktif mengandung elemen – elemen terikat secara kimia, seperti oksigen dan hidrogen. Elemen – elemen ini dapat berasal dari bahan baku yang tertinggal akibat tidak sempurnanya proses karbonisasi, atau pula dapat terikat secara kimia pada proses aktivasi. Demikian pula adanya kandungan abu yang bukan bagian organik dari produk. Untuk tiap – tiap jenis karbon aktif kandungan abu dan komposisinya ada bermacam – macam. Adsorpsi dari elektrolit dan non elektrolit dari larutan karbon aktif, juga dipengaruhi oleh adanya sejumlah kecil abu. Adanya oksigen dan hidrogen mempunyai pengaruh besar pada sifat – sifat karbon aktif. Elemen – elemen ini berkombinasi dengan atom – atom karbon membentuk gugus – gugus fungsional tertentu. Pengujian mutu arang aktif sangat diperlukan untuk mengetahui kemampuan arang aktif agar dapat berfungsi sebagaimana mestinya. Pengujian mutu arang aktif meliputi: penentuan bagian yang hilang pada pemanasan 950 °C, penentuan kadar air, penentuan kadar abu dan daya serap terhadap larutan I2 [25]. Menurut SNI karbon aktif yang baik mempunyai persyaratan seperti pada tabel 2.1 berikut:
Tabel 2.2 Persyaratan Karbon Aktif
No. Jenis Persyaratan
1. Bagian yang hilang pada pemanasan 950 °C Maksimum 15 %
2. Kadar air Maksimum 15 %
3. Kadar abu Maksimum 10 %
4. Bagian yang tidak diperarang Tidak nyata
5. Daya serap terhadap larutan I2 Maksimum 20 %
Ukuran partikel dan luas permukaan merupakan hal yang paling penting dalam karbon aktif. Ukuran partikel karbon aktif mempengaruhi proses kecepatan adsorpsi, tetapi tidak mempengaruhi adsorpsi yang berhubungan dengan luas permukaan karbon [2]. Porositas adsorben juga mempengaruhi daya adsorbsi dari suatu adsorben. Adsorben dengan porositas yang besar mempunyai kemampuan menyerap yang lebih tinggi dibandingkan dengan adsorben yang memiliki porositas kecil. Untuk meningkatkan porositas dapat dilakukan dengan mengaktivasi secara (SNI 06 – 3730 – 95)
fisika seperti mengalirkan uap air panas ke dalam pori-pori adsorben atau mengaktivasi secara kimia [26].
Volume pori karbon aktif biasanya berukuran antara 0,2 sampai 0,6 cm3/g. Sedangkan luas permukaannya berukuran antara 800 sampai 1500 m2/g (Beguin and E. Frackowiak). Secara umum, ukuran diameter pori dalam suatu karbon aktif biasanya dikelompokkan sebagai berikut:
1. Mikropori memiliki dimensi < 2,0 nm
2. Mesopori memiliki dimensi antara 2 sampai 50 nm 3. Makropori memiliki dimensi > 50 nm
[27]
Saat ini, karbon aktif telah digunakan secara luas dalam industri kimia makanan atau minuman, dan farmasi. Pada umumnya karbon aktif digunakan sebagai bahan penyerap dan penjernih serta sebagai katalisator dalam jumlah kecil [23].
Biosorben banyak digunakan dalam kehidupan sehari – hari . Beberapa manfaat dari biosorben dalam berbagai bidang dapat dilihat pada tabel 2.2 berikut:
Tabel 2.3 Beberapa manfaat biosorben dalam berbagai bidang
No. Pemakaian Kegunaan
1. Industri obat dan makanan Menyaring dan menghilangkan warna, bau, rasa yang tidak enak pada makanan
2. Minuman ringan, minuman keras
Menghilangkan warna, bau pada arak/minuman keras dan minuman ringan 3. Kimia perminyakan Penyulingan bahan mentah, zat perantara 4. Pembersih air Menyaring atau menghilangkan bau, warna,
zat pencemar dalam air, sebagai pelindung, dan penukaran resin dalam alat atau penyulingan air
5. Pembersih air buangan Mengatur dan membersihkan air buangan dan pencemar, warna, bau, dan logam berat 6. Penambakan udan dan benur Pemurnian, menghilangkan bau dan warna 7. Pelarut yang digunakan
kembali
Penarikan kembali berbagai pelarut, sisa methanol, etil, asetat dan lain – lain
8. Pemurnian gas Menghilangkan sulfur, gas beracun, dan bau busuk asap
9. Katalisator Reaksi katalisator pengangkut vinil klorida, vinil asetat
10. Pengolahan pupuk Pemurnian, penghilangan bau
2.3 ADSORPSI
Adsorpsi (penyerapan) adalah suatu proses pemisahan dimana komponen dari suatu fase fluida berpindah ke permukaan zat padat yang menyerap (biosorben). Biasanya partikel – partikel kecil zat penyerap dilepaskan pada adsorpsi kimia yang merupakan ikatan kuat antara penyerap dan zat yang diserap sehingga tidak mungkin terjadi proses yang bolak – balik [2].
Adsorpsi merupakan proses difusi suatu komponen pada suatu permukaan atau antar partikel. Adsorspsi dapat terjadi secara fisika maupun kimia. Adsorpsi fisika sering disebut fisiosorpsi, terjadi akibat adanya gaya tarik – menarik (interaksi elektrolisis antar dipol) antara permukaan adsorben dengan molekul-molekul adsorben yang disebabkan oleh ikatan Van der Walls. Sedangkan jika partikel adsorben yang melekat pada permukaan adsorben dengan membentuk ikatan kimia disebut adsorpsi kimia. Adsorben yang digunakan dapat bersifat polar (silika dan alumina) ataupun non polar (arang aktif, lempung bentonite). Ada beberapa faktor yang mempengaruhi adsoprsi antara lain:
1. Sifat-sifat kimia dan fisika dari adsorben (ukuran pori, luas permukaan, dan komposisi kimia).
2. Sifat-sifat kimia dan fisika dari adsorbat, (ukuran dan molaritas molekul, komposisi kimia).
3. pH, tekanan dan temperatur. 4. Konsentrasi adsorben.
5. Waktu kontak antara adsorbat dengan adsorben. [28].
Proses adsorpsi dapat terjadi karena adanya gaya tarik atom atau molekul pada permukaan padatan yang tidak seimbang. Adanya gaya ini, padatan cenderung menarik molekul – molekul lain yang bersentuhan dengan permukaan padatan, baik fasa gas atau fasa larutan ke dalam permukaannya. Akibatnya, konsentrasi molekul pada permukaan menjadi lebih besar daripada dalam fasa gas atau zat terlarut dalam larutan. Adsorpsi dapat terjadi pada antarfasa padat – cair, padat – gas, atau gas – cair [29].
Beberapa faktor yang mempengaruhi proses penyerapan dalam adsorpsi adalah :
1. Bahan penyerap
Bahan yang digunakan untuk menyerap mempunyai kemampuan berbeda – beda, tergantung dari bahan asal dann juga metode aktivasi yang digunakan.
2. Ukuran partikel
Semakin kecil ukuran butir, maka semakin besar permukaan sehingga dapat menyerap kontaminan makin banyak. Secara umum kecepatan adsorpsi ditujukan oleh kecepatan difusi zat terlarut ke dalam pori – pori partikel adsorben. Ukuran partikel yang baik untuk proses penyerapan antara 100 – 200 mesh.
3. Derajat keasaman (pH)
Pada pH rendah, ion H+ akan berkompetisi dengan kontaminan yang akan diserap. Sehingga efisien penyerapan turun. Proses penyerapan akan berjalan baik bila pH larutan tinggi. Derajat keasaman mempengaruhi adsorpsi karena pH menentukan tingkat ionisasi laritan, pH yang baik berkisar antara 8 – 9. Senyawa asam organik dapat diadsorpsi pada pH rendah dan sebaliknya basa organik diadsorpsi pada pH tinggi.
4. Waktu penyerapan
Waktu penyerapan yang lama akan memungkinkan proses difusi dan penempelan molekul zat terlarut yang terserap berlangsung dengan baik.
5. Konsentrasi
Pada konsentrasi larutan rendah, jumlah bahan diserap sedikit, sedangkan pada konsentrasi tinggi jumlah bahan yang diserap semakin banyak. Hal ini disebabkan karena kemungkinan frekuensi tumbukan antara partikel semakin besar.
2.4 ZAT WARNA
Zat warna merupakan senyawa organik atau anorganik berwarna yang digunakan untuk memberi warna tekstil atau suatu makanan, minuman, obat - obatan, kosmetika, dan lain-lain [30]. Sebagian zat warna adalah racun bagi tubuh manusia, tetapi ada zat warna yang relatif aman bagi manusia, yaitu zat warna yang digunakan dalam industry pangan, minuman dan farmasi. Penggolongan zat warna [25]
berdasarkan pada sifat-sifat dan penggunaannya yaitu zat warna asam, basa, direct, mordan, komplek logam, azoat, belerang, bejana, dispersi dan reaktif [31].
Zat warna yang umumnya digunakan terdiri dari dua macam, yaitu zat warna alami dan zat warna buatan atau sintetik. Zat warna alami yang sering digunakan sejak dahulu berasal dari sumber alam, baik berasal dari tanaman maupun mineral seperti kunyit untuk warna kuning, daun pandan untuk warna hijau, caramel, dan lain-lain. Zat warna alami umumnya mempunyai keterbatasan memberi warna, sehingga kurang sesuai dengan yang diinginkan. Zat warna alami mulai banyak ditinggalkan sejak zat warna sintetik ditemukan. Hal ini disebabkan karena biaya produksi zat warna sintetik lebih murah, umumnya mempunyai jenis warna yang lebih banyak, serta kemampuan pewarnaan yang lebih baik [30]. Zat warna sintetik merupakan zat warna yang berasal dari batubara atau zat warna yang dihasilkan dari reaksi dua atau lebih senyawa kimia. Zat warna sintetik dalam perdagangan biasanya berupa serbuk yang larut dalam air dan dapat mewarnai bahan untuk tekstil, makanan, minuman dan dapat juga digunakan dalam percetakan dan lain-lain. Contoh zat warna sintetik antara lain Rhodamin B, ponceau 3R, ponceau 4R, tartazine, magenta, carmine, carmoisine dan lain-lain [32].
2.4.1 Methyl Orange
Methyl orange merupakan molekul zat warna dengan rumus molekul
C14H14N3NaO3S dan mempunyai berat molekul 327,33 g/mol. Panjang gelombang maksimum larutan methyl orange adalah sekitar 465 nm Methyl orange termasuk jenis zat warna azo. Zat warna azo mempunyai system kromofor dari gugus azo (-N=N) yang berikatan dengan gugus aromatik [10].
Methyl orange digunakan sebagai pewarna tekstil, dalam industri gelas, dan
cat Sedangkan di laboratorium digunakan sebagai indikator titrasi. Trayek pH methyl
orange berkisar 3,0 hingga 4,4 [10]
Molekul zat warna merupakan gabungan dari zat organik tidak jenuh dengan kromofor sebagai pembawa warna. Zat organik tidak jenuh yang dijumpai dalam pembentukan zat warna adalah senyawa aromatik antara lain senyawa hidrokarbon aromatik dan turunannya, fenol dan turunannya serta senyawa - senyawa hidrokarbon yang mengandung nitrogen. Gugus kromofor adalah gugus yang menyebabkan molekul menjadi berwarna. Kromofor zat warna reaktif biasanya merupakan sistem azo dan antrakuinon dengan berat molekul relatif kecil. Daya serap terhadap serat tidak besar. Sehingga zat warna yang tidak bereaksi dengan serat mudah dihilangkan. Gugus-gugus penghubung dapat mempengaruhi daya serap dan ketahanan zat warna terhadap asam atau basa. Gugus-gugus reaktif merupakan bagian-bagian dari zat warna yang mudah lepas. Dengan lepasnya gugus reaktif ini, zat warna menjadi mudah bereaksi dengan serat kain. Pada umumnya agar reaksi dapat berjalan dengan baik maka diperlukan penambahan alkali atau asam sehingga mencapai pH tertentu [33].
2.4.2 Methyl Violet
Methyl violet termasuk zat warna golongan trifenilmetana yang digunakan
secara intensif untuk mewarnai nilon, nilon yang dimodifikasi poliakrilonitril, wol, sutera dan kapas. Beberapa diantaranya dimanfaatkan untuk kegunaan medis dan biologis. Methyl violet bersifat persisten dan sulit dibiodegradasi. Bahan kimia ini dapat memicu tumor pada beberapa spesies ikan yang hidup di dasar perairan sehingga diperlukan penanganan yang serius untuk mengatasi masalah tersebut [12].
Methyl violet merupakan salah satu contoh zat pewarna tekstil. Zat warna methyl violet tergolong dalam zat warna karbon-nitrogen yang terdapat pada gugus
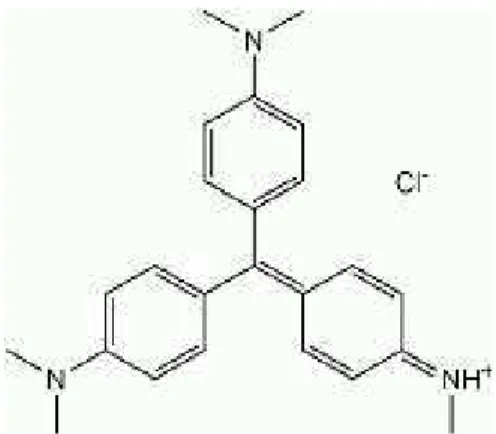
benzennya. Gugus benzena sangat sulit didegradasi, kalaupun dapat didegradasi membutuhkan waktu yang lama. Methyl violet termasuk dalam golongan zat warna kation dengan rumus kimia C24H28N3Cl dan mempunyai berat molekul 393,96 gram/mol. Methyl violet larut dalam air, etanol glikol, dietilena glikol dan dipropilen [12]. Struktur molekul methyl violet dapat dilihat pada gambar 2.3 berikut:
Gambar 2.3 Struktur Methyl Violet
Kegunaan methyl violet adalah sebagai pewarna ungu untuk tekstil dan memberikan warna ungu pada cat dan tinta. Nama kimia dari methyl violet adalah pentametil p-rosanilia hidroklorida. Selain digunakan sebagai pewarna pada pencelupan, methyl violet dapat digunakan sebagai indikator untuk menentukan pH suatu zat. Methyl violet dalam larutan asam berwarna kuning yang berubah menjadi hijau-biru pada pH 0-1,8 dan diatas pH 1,8 akan berwarna ungu [12]
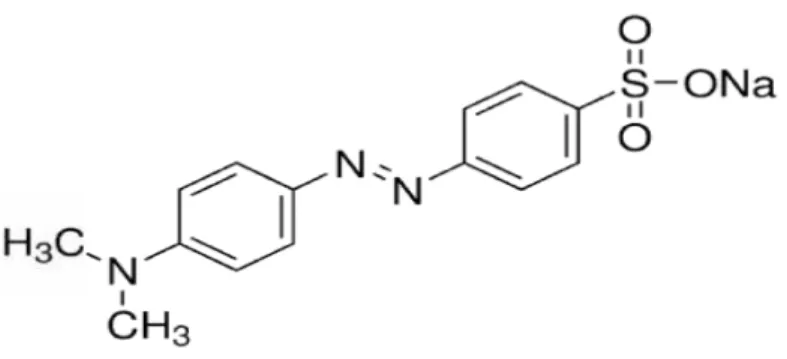
2.4.3 Methyl Red
Methyl red biasa digunakan sebagai zat warna monoazo di laboratorium dan
industri tekstil, serta industri-industri lainnya. Penggunaan methyl red dapat menyebabkan gangguan/iritasi pada mata dan kulit iritasi pada saluran pencernaan, faringeal bila terhirup atau tertelan, terlebih methyl red bersifat mutagenik pada kondisi aerobik, mengalami biotransformasi menjadi asam 2-aminobenzoat dan N-N’ dimetil-p-fenilen diamin [9]. Struktur molekul methyl red seperti gambar 2.4 berikut:
Gambar 2.4 Struktur Molekul Methyl Red
Methyl red merupakan salah satu zat warna azo yang digunakan dalam
2.5 SPEKTROFOTOMETRI UV-VIS
Spektrofotometri UV-Vis merupakan suatu metode pengukuran secara analisis analit yang didasarkan pada fenomena hasil interaksi antara materi dengan sinar (radiasi elektromagnetik = REM) dengan menggunakan instrument spektrofotometer. Daerah pengukuran spektrofotometri UV-Vis adalah pada panjang gelombang 180-380 nm untuk daerah ultra violet (UV) dan 380-780 nm untuk visibel (tampak). Hampir semua molekul organik dan anorganik dapat dianalisis [30].
Spektrofotometer UV – Vis menggunakan cahaya tampak alam rentang ultraviolet (UV) dan infrared (IR). Sifat optik Spektrofotometer UV – Vis digunakan untuk mengetahui tingkat adsorpsi dan dispersi bahan. Spektrofotometer UV – Vis mempunyai rentang panjang gelombang 10-6 – 10-7 nm dengan peristiwa adsorpsi yang mengakibatkan adanya transisi elektron. [25]. Serapan cahaya oleh molekul dalam daerah spektrum ultraviolet dan sinar tampak tergantung pada struktur elektronik dari senyawa-senyawa berkaitan erat dengan transisi-transisi diantara tingkatan-tingkatan tenaga elektronik [35].
Spektrofotometer UV – Vis terdiri atas: 1. Sumber radiasi (cahaya)
Sumber cahaya yang digunakan adalah sebuah lampu pijar dengan kawat rambut terdiri dari wolfram. Wolfram dapat merupakan sumber cahaya yang dapat menyediakan seluruh spektrum tampak dan ultra – ungu dekat sehingga didapat spektrum pada daerah 200 nm – 800 nm.
2. Monokromator
Monokromator adalah suatu alat optik yang digunakan untuk memunculkan suatu berkas radiasi dari suatu sumber secara berkesinambungan, dimana berkas yang ditampilkan mempunyai spektral yang tinggi dengan panjang gelombang yang akan diteliti. Komponen dari monokromator yang utama adalah suatu sistem celah dan suatu unsur dispersif. Radisi dari sumber difokuskan masuk ke celah, kemudian disejajarkan oleh sebuah lensa atau cermin sehingga suatu berkas sejajar jatuh prisma atau kisi tersebut secara mekanis, macam – macam tampilan spektrum yang dihasilkan oleh unsur pendispersi dipusatkan pada celah keluar kemudian diteruskan ke sampel.
3. Tempat sampel (kuvet)
Kuvet adalah wadah gelas yang terbuat dari kaca atau silika yang dibuat sedemikian rupa dengan jarak yang dilalui berkas sinar adalah 1 cm. Sel sampel berisi larutan yang akan diuji yang biasanya berupa larutan yang sangat encer. 4. Detektor dan komputer
Detektor mengubah sinar yang menjadi arus listrik. Arus lebih tinggi jika sinarnya lebih tinggi. Untuk tiap panjang gelombang sinar yang melewati spektrofotometer, intensitas yang melewati sel sampel dihitung. Biasanya disimbolkan I0 untuk intensitas yang masuk dan I untuk intensitas yang keluar. Jika I lebih kecil dari I0 berarti sampel menyerap sejumlah sinar.
Gambar 2.5 Cara Kerja Spektrofotometer UV – Vis [25]
Secara umum cara kerja Spektrofotometer UV – Vis adalah sinar dari sumber radiasi diteruskan menuju monokromator. Cahaya dari monokromator diarahkan terpisah melalui blangko dan sampel dengan sebuah cermin berotasi. Kedua cahaya lalu bergantian berubah arah karena pemantulan dari cermin yang berotasi secara kontinyu. Detektor menerima cahaya dari blangko dan sampel secara bergantian secara berulang – ulang. Sinyal listrik dari detektor diproses, diubah ke digital dan dibandingkan anatara sampel dan blangko. Perhitungan dilakukan dengan komputer yang sudah terprogram [25].

![Gambar 2.5 Cara Kerja Spektrofotometer UV – Vis [25]](https://thumb-ap.123doks.com/thumbv2/123dok/4127285.2817995/12.892.223.760.470.636/gambar-cara-kerja-spektrofotometer-uv-vis.webp)