SINDROMA KARDIORENAL AKIBAT GAGAL JANTUNG
Naomi N. Dalimunthe, Sari Harahap, Rahmad Isnanta,
Zainal Safri, Refli Hasan, Jamaluddin
Divisi Kardiologi – Departemen Ilmu Penyakit Dalam
Fakultas Kedokteran Universitas Sumatera Utara
RSUP. H. Adam Malik Medan
PENDAHULUAN
Jantung bertanggung jawab untuk menyuplai darah ke jaringan tubuh dan
organ-organ, termasuk ginjal, yang berfungsi dalam menjaga keseimbangan cairan dan homeostasis
garam dalam tubuh. Oleh karena itu, gangguan pada ginjal sering disertai gagal jantung dan
gangguan pada jantung sering disertai gagal ginjal. Hubungan saling bergantungan ini dikenal
sebagai "sindrom kardiorenal". Frase ini telah digunakan sejak tahun 2004, telah
menghasilkan sejumlah berbagai macam teori mengenai ini dan terus diteliti dan
dikembangkan dalam berbagai penelitian. Sindroma kardiorenal (CRS) pertama kali secara
resmi didefinisikan pada konferensi konsensus acute dialysis quality Initiative (ADQI) pada
tahun 2009. Definisi ini dibuat dalam usaha untuk mengelompokkan berbagai hubungan
antara kondisi akut dan kronis pada penyakit jantung dan ginjal.1 Diperkirakan bahwa
tumpang tindih antara penyakit kardio vaskuler dan disfungsi ginjal mewakili proses
patofisiologi umum yang berinteraksi dalam memacu siklus disfungsinya suatu organ.2
Prevalensi gagal jantung diestimasi sekitar 1-2% dari populasi dewasa pada
Negara-negara berkembang, dan angkanya meningkat 10% pada individu dengan usia 70 tahun.3
Gagal jantung itu sendiri dapat disertai oleh beberapa kornorbid utama yang memiliki
dampak pada pengobatan dan prognosis penyakit yaitu salah satunya insufisiensi ginjal
ataupun gagal ginjal.4 Fungsi ginjal yang direfleksikan melalui kadar kreatinin serum ataupun
yang lebih akurat melalui estimasi laju filtrasi glomerulus (eGFR) dipengaruhi pada
kebanyakan pasien dengan gagal jantung terutama bila tingkat keparahannya berat dan hal ini
merupakan prediktor penting dalarn menentukan prognosis pasien.5
Interaksi antar organ tidak hanya terjadi pada kasus-kasus kronis. Suatu penelitian
kohort prospektif yaitu: The Cardiovascular Health Study dilakukan oleh Mittalhenkle dkk
yang dikenal sebagai penderita Penyakit Kardio Vaskuler (PKV=CVD).6 Chittineni dkk
(2007) melaporkan angka kejadian yang lebih tinggi yaitu 21% kasus GgGA pada penderita
yang dirawat karena gagal jantung. Sebaliknya penelitian United States Renal Data System
(USRDS) melaporkan bahwa sepanjang tahun 2001 dan 2003 terjadi kematian mendadak
akibat henti jantung (cardiac arrest) sebesar 32 % pada pasien hemodialisis baik diluar
rumah sakit atau selama menjalani dialisis (81%).6 Forman dkk (2004) melaporkan terjadinya
perburukan fungsi ginjal pada pasien yang dirawat oleh karena gagal jantung. Yang menjadi
kriteria perburukan fungsi ginjal adalah kenaikan kadar kreatinin serum ≥ 0.3 mg/dl bila
dibandingkan dengan kadar awal. Perburukan fungsi ginjal terjadi pada 27% dari pasien yang
dirawat dan berhubungan dengan prognosis yang lebih buruk pula.6
Smith dkk (2006) mengadakan meta-analisis dan review kepustakaan, mereka
melaporkan bahwa dari 80.098 pasien dirawat karena gagal jantung didapatkan 63%
diantaranya mengalami perburukan fungsi ginjal, Tingkat perburukan fungsi ginjal sebanding
dengan peningkatan angka kematian. Untuk setiap kenaikan kadar kreatinin serum sebesar
0,5 mg/dl terjadi peningkatan angka kematian sebesar 15%.6 Fried dkk menentukan kadar
kreatinin serum < 1.5 mg/dl sebagai batas normal. Interaksi antar organ tidak hanya terjadi
pada angka kematian, tetapi juga pada angka kejadian stroke, transient ischemic attact (TIA),
hipertrofi bilik kiri (LVH), gagal jantung kongestif, infark miokard dan berbagai penyakit
kardiovaskuler lain.6 Patrick dan Foley (2008) melaporkan bahwa peningkatan angka
kejadian LVH berkorelasi dengan penurunan LFG (laju filtrasi glomeruli), yaitu 27 % pada
LFG ≥ 50 cc/menit, 31% pada LFG 25-49 cc/menit, dan 45% pada LFG < 25 cc/menit.6
Telah menjadi jelas bahwa disfungsi ginjal dihubungkan dengan prognosis yang buruk pada
pasien gagal jantung dengan tingginya angka masuk rawatan rumah sakit dan mortalitas
jangka pendek maupun panjang, serta memanjangnya durasi rawatan di rumah sakit.6
DEFINISI SINDROMA KARDIORENAL (CRS)
The National Heart, Lung, and Blood Institute (NHLBI), di Amerika, membentuk grup kerja ”Cardio-Renal Connections”, mengajukan definisi sederhana tentang sindrom kardiorenal (CRS/Cardiorenal syndrome) pada tahun 2004, CRS adalah penurunan fungsi
ginjal yang disebabkan oleh penurunan fungsi jantung. Mengingat fungsi ginjal antara lain
mengatur garam dan cairan maka penurunan fungsinya akan menyebabkan pengobatan
antar organ ginjal-jantung. Defenisi yang disepakati, diperlukan untuk menjelaskan
koeksistensi gangguan jantung dan ginjal dan untuk mengidentifikasi perjalanan waktu
interaksi jantung-ginjal.6
Bila ditinjau dari sudut ahli ginjal (nefrologis) kondisi ini adalah bila terjadi penyakit
kardiovaskular atau gagal jantung yang berhubungan dengan penurunan fungsi ginjal
sebelumnya. Bila ditinjau dari ahli jantung (kardiologis) kondisi ini adalah penurunan fungsi
ginjal yang terjadi akibat penyakit kardiovaskular atau gagal jantung sebelumnya. Atas dasar
itu, Schrier (2007) membedakan istilah antalra “cardiorenal syndrome “, yaitu : penurunan
fungsi ginjal yang terjadi pada pasien gagal jantung dan menimbulkan perburukan prognosis,
sedangkan penurunan fungsi jantung akibat gagal ginjal, disebutnya sebagai “renocardiac
syndrome“.7
Pada tahun 2008, di Venesia, sebuah konferensi konsesus Acute Dialysis Quality
Initiative (ADQI), membahas epidemiologi, kriteria diagnostik, termasuk defenisi dari
sindrom kardiorenal. Berdasarkan konferensi ini, istilah CRS digunakan untuk
mengidentifikasi penyakit jantung dan ginjal baik itu akut maupun kronis, disfungsi salah
satu organ dapat meyebabkan disfungsi akut atau kronik organ lainnya.Tujuan dari definisi
ini akan memfasilitasi penelitian epidemiologi, mengidentifikasi sasaran populasi untuk
intervensi, mengembangkan alat diagnostik, mencegah dan mengelola sindrom yang berbeda.
Konferensi konsesus memilih istilah yang luas, menggunakan bentuk jamak (sindroma
kardiorenal, CRS), untuk menunjukkan adanya sindrom ganda. Istilah ini dipilih untuk
mengenali disfungsi organ utama (jantung vs ginjal) dan akut vs kronis dan
mempertimbangkan struktur dan / atau kelainan fungsional dari kedua organ yang
diperlukan.8 Namun, sampai saat ini definisi sindrom kardiorenal belum sepenuhnya
disepakati, diantaranya adalah9 :
“Suatu kondisi patofisiologik yang merupakan kombinasi antara disfungsi ginjal dan jantung yang mempercepat kegagalan masing-masing organ dan berakibat pada peningkatan morbiditas dan mortalitas”
“Suatu sindrom yang ditandai dengan kegagalan ginjal atau jantung dalam mengkompensasi gangguan fungsi masing-masing organ tersebut, menyebabkan lingkaran setan yang berakhir dengan kegagalan seluruh sistem sirkulasi”
Secara praktis Liang dkk, mendefinisikan sindrom kardiorenal sebagai disregulasi
kardiorenal tahap lanjut yang ditandai oleh setidaknya salah satu dari tiga kondisi yaitu9 :
2. Perburukan fungsi ginjal yang terjadi selama pengobatan pada acute decompensated
heart failure (ADHF), dan
3. Resistensi terhadap terapi diuretik akibat penurunan fungsi ginjal. Dalam konteks gagal
jantung kronik, sindrom kardiorenal seringkali merupakan masa transisi menuju gagal
jantung tahap lanjut (advanced heart failure).
KLASIFIKASI SINDROMA KARDIORENAL (CRS)
Ronco dkk, membuat klasifikasi sindrom kardiorenal berdasarkan mekanisme
patofisiologi yang mendasari kegagalan fungsi jantung dan ginjal. Klasifikasi tersebut
menitikberatkan pada dua aspek yaitu durasi (onset akut atau kronik), dan urutan kejadian
(didahului gagal ginjal atau didahului gagal jantung, atau terjadi simultan akibat penyakit
sistemik).6,10
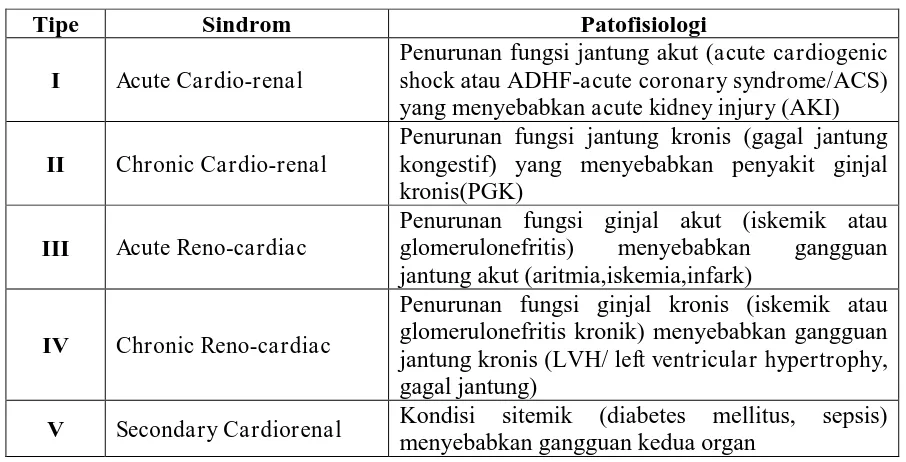
Tabel 1. Klasifikasi sindroma kardiorenal (CRS) menurut Ranco dkk berdasarkan
konferensi konsesus Acute Dialysis Quality Initiative (ADQI)6,10
Tipe Sindrom Patofisiologi
I Acute Cardio-renal
Penurunan fungsi jantung akut (acute cardiogenic shock atau ADHF-acute coronary syndrome/ACS) yang menyebabkan acute kidney injury (AKI)
II Chronic Cardio-renal
Penurunan fungsi jantung kronis (gagal jantung kongestif) yang menyebabkan penyakit ginjal kronis(PGK)
III Acute Reno-cardiac
Penurunan fungsi ginjal akut (iskemik atau glomerulonefritis) menyebabkan gangguan jantung akut (aritmia,iskemia,infark)
IV Chronic Reno-cardiac
Penurunan fungsi ginjal kronis (iskemik atau glomerulonefritis kronik) menyebabkan gangguan jantung kronis (LVH/ left ventricular hypertrophy, gagal jantung)
V Secondary Cardiorenal Kondisi sitemik (diabetes mellitus, sepsis)
menyebabkan gangguan kedua organ
Dalam suatu World Congress of Nephrology tahun 2008 Ronco dkk. mengajukan
definisi dari sindroma kardiorenal yaitu suatu gangguan patofisiologi dari jantung dan ginjal
dimana disfungsi akut atau kronik pada satu organ tersebut dapat mencetuskan disfungsi akut
atau kronik pada organ yang lain tersebut. Berdasarkan definisi tersebut mereka
Tipe 1 : Acute Cardiorenal Syndrome
Didefinisikan sebagai suatu perburukan akut fungsi jantung dijumpai pada syok
kardiogenik, gagal jantung kongestif dekompensata, dan sindroma koroner akut yang
mencetuskan secara mendadak perburukan fungsi ginjal ataupun gagal ginjal akut yang
dideskripsikan sebagai peningkatan kadar kreatinin serum sebesar 0,3-0,5 mg/dl, ataupun
penurunan laju filtrasi glomerulus sebesar 9-15 ml/menit saat awal masuk rawatan dengan
gagal jantung akut. Sekitar 27-40% pasien yang dirawat dengan acute decompensated heart
failure (ADHF) tampaknya berkembang menjadi acute kidney injury (AKI). Kebanyakan
pasien dengan kondisi ini mengalami mortalitas dan morbiditas yang tinggi dan meningkatkan
lamanya rawat inap.
Tipe 2 : Chronic Cardiorenal Syndrome
Didefinisikan sebagai gagal jantung kronik yang rnengarah menjadi penyakit ginjal
kronik akibat dari kerusakan mikrovaskular dan makrovaskular ginjal yang semakin
dirumitkan dengan gangguan hemodinamik. Sindroma tipe ini cukup sering terjadi dan telah
dilaporkan pada 63% pasien gagal jantung kongestif rawat inap.
Tipe 3 : Acute Renocardiac Syndrome
Didefinisikan sebagai penurunan fungsi ginjal akut seperti dapat dijumpai pada
keadaan kekurangan volume cairan, glomerulonefritis akut ataupun pada stenosis arteri renal
bilateral yang menyebabkan gangguan ataupun penurunan fungsi jantung yang akut
dimanifestasikan dengan gagal jantung akut, aritmia, ataupun iskemia. Subtipe ini mengacu
pada kelainan pada fungsi jantung sekunder terhadap AKI.
Tipe 4 : Chronic Renocardiac Syndrome
Didefinisikan sebagai penyakit ginjal kronik yang berkontribusi pada penurunan
berkelanjutan terhadap fungsi jantung atau gagal jantung, hipertrofi jatung, dan predisposisi
terhadap kejadian kardiovaskular lainnya yang merugikan. Berbagai efek disfungsi ginjal
kronik menyebabkan gangguan fungsi jantung meliputi ketidakseimbangan hemodinamik,
inflamasi kronik, dan proses aterosklerosis yang progresif. Subtipe ini mengacu pada penyakit
atau disfungsi jantung yang terjadi sekunder akibat penyakit ginjal kronis.
Tipe 5 : Secondary Cardiorenal Syndrome
maupun ginjal yang dipengaruhi atau disebabkan oleh obat-obatan maupun gangguan
sistemik seperti diabetes melitus, hipertensi, penyakit autoimun, sepsis, amiloidosis, ataupun
disseminated intravascular coagulation (DIC). Gangguan ini dapat bersifat akut (seperti pada
kondisi toksisitas obat ataupun keadaan sepsis) maupun kronik (contohnya bila diakibatkan
oleh diabetes melitus).
Liang dkk (2008) membuat definisi CRS berdasarkan gambaran kliniknya. Menurut
mereka apakah penyebab awalnya organ ginjal atau jantung, gambaran kliniknya dapat
berupa gagal jantung yang disertai dengan penurunan fungsi ginjal, memburuknya fungsi
ginjal saat dilakukan pengobatan pada acute decompensated heart failure (ADHF) atau
resistensi terhadap terapi diuretik akibat penurunan fungsi ginjal. Mereka membuat
klasifikasi definisi seperti tercantum pada tabel berikut6,9 :
Tabel. 2 Defenisi dan klasifikasi sindroma kardio renal (CRS menurut Liang dkk)
tahun 2008.6
Cardiorenal Failure (ADHF) Ringan : Gagal jantung + eGFR 30-59 cc/menit/ 1.73 m2 Sedang : Gagal jantung + eGFR 15-29 cc/menit/ 1.73 m2 Berat : Gagal jantung + eGFR <15 cc/menit/ 1.73 m2 Perburukan fungsi ginjal
saat pengobatan untuk ADHF
Kenaikan kadar kreatinin serum > 0,3 mg/dl atau> 25 % dari kadar asalnya
Resistensi Diuretik Resistensi terhadap terapi diuretik, walaupun telah diberikan :
- > 80 mg furosemid / 6 jam - > 240 mg furosemid / hari - Infus furosemid secara kontinu - Kombinasi terapi diuretik
(loop diuretic + tiazide + aldosterone antagonist)
INSIDENSI
Belum ada laporan yang khusus yang mempelajari insidensi CRS, tetapi dari hasil
penelitian Candesartan in Heart Failure Assessment in Mortality and Morbidity (CHARM)
yang dilaporkan oleh Hillege dkk terbukti bahwa penurunan laju filtrasi glomeruli terhitung
(eGFR) merupakan penanda meningkatnya angka kejadian dan kematian akibat gagal jantung
(heart failure). The Acute Decompensated Heart Failure National Registry (ADHERE) suatu
penelitian populasi besar yang menyangkut 105.388 pasien gagal jantung yang dirawat di
Amerika, melaporkan terdapat 30% kasus diantaranya menderita juga PGK. Dari hasil review
kepustakaan yang dilakukan oleh Liang dkk dilaporkan bahwa lebih dari 70% kasus
Tingkat penurunan fungsi ginjal selama perawatan gagal jantung berkorelasi dengan angka
kematian, komplikasi dan lamanya perawatan. Penelitian VALIANT (Valsartan in Acute
Myocardial Infarction Trial) yang dilaporkan oleh Anavekar dkk membuktikan bahwa
penurunan LFG merupakan faktor risiko bebas untuk terjadinya infark miokard akut atau
PKV lainnya. Setiap penurunan LFG sebesar 10 cc/menit berasosiasi dengan hazard ratio
sebesar 1.10 untuk angka kematian dan komplikasi lainnya.6
Pada pasien dengan ADHF selalu terjadi kelebihan volume tubuh (volume overload)
dan biasanya diberikan pengobatan diuretik. Penurunan fungsi ginjal mengganggu efektifitas
diuretik atau disebut sebagai diuretic resistant. Belum ada suatu penelitianpun dilakukan
terhadap insidensi diuretic resistant pada ADHF walaupun kejadian ini jelas meningkatkan
angka kematian (Golikorsky).6
PATOFISIOLOGI SINDROMA KARDIORENAL PADA TIPE 1 & 2
Mekanisme dasar penyebab sindroma kardiorenal bersifat multifaktorial yang
meliputi kerusakan struktur oleh karena proses aterosclerosis, perubahan hemodinamik, efek
neurohormonal, dan peranan komponen inflamasi 12
Pada kondisi fisiologis GFR dipertahankan tetap konstan dalam rentang tekanan darah
yang tinggi oleh mekanisme autoregulasi yang terutama berada dalam pembuluh darah
afferent dan efferent glumerulus. Bila terjadi penurunan cardiac output, tekanan darah dapat
turun dibawah rentang yang dapat dikompensasi oleh mekanisme autoregulasi tersebut.
Kondisi ini akan diikuti oleh hipoperfusi, hipofiltrasi dan kemudian iskemia ginjal.
Menurunnya perfusi ginjal akan mengaktivasi sistem renin-angiotensin-aldosteron (RAA)
dengan dilepaskannya renin yang akan meningkatkan perubahan angiotensin I oleh
angiotensin converting enzyme (ACE) menjadi angiotensin II yang kemudian akan
menyebabkan vasokonstriksi sistemik dan retensi natrium di ginjal, sehingga terjadi
peningkatan volume sirkulasi efektif.13,14
Pada gagal jantung, respons fisiologik tersebut tidak hanya mengaktivasi sistem RAA,
tetapi juga meyebabkan efek spiral negatif berupa aktivasi sistem saraf simpatik, disfungsi
endotel, inflamasi, dan gangguan keseimbangan reactive oxygen/nitric oxide. Berbagai sistem
yang teraktivasi tersebut akan berinteraksi membentuk lingkaran setan yang akan
Mekanisme disfungsi ginjal pada penderita gagal jantung sangat kompleks dan sangat
mungkin beberapa faktor bekerja pada penderita yang sama. Mengenal faktor-faktor yang
terlibat pada masing-masing penderita dan mengeliminasinya bila mungkin merupakan
komponen yang penting dalam tatalaksana sindrom kardiorenal.13
1. Sindroma Kardiorenal Akut (Tipe I)
Sindrom kardiorenal tipe I ditandai oleh perburukan akut fungsi jantung yang
menyebabkan jejas ginjal akut (acute kidney injury=AKI). Sindrom kardiorenal tipe I
sering terjadi. Sebagian besar penderita gagal jantung yang dirawat di rumah sakit akibat
gagal jantung akut de novo atau dekompensasi akut gagal jantung kronik seringkali
mempunyai kondisi pre-morbid disfungsi ginjal yang menjadi predisposisi terjadinya
AKI.13
Kepentingan klinik dari masing-masing mekanisme tampaknya berbeda untuk
masing-masing penderita (misalnya pada penderita syok kardiogenik dan edema paru
akut), dan berbeda pula untuk masing-masing keadaan (misalnya pada gagal jantung akut
akibat regurgitasi mitral akut dan dekompensasi akut akibat ketidakpatuhan berobat).10,13
AKI yang terjadi pada gagal jantung akut tampak lebih berat pada penderita
dengan fraksi ejeksi ventrikel kiri yang terganggu, dan penurunan fungsi ginjal tersebut
secara konsisten menjadi faktor risiko independen mortalitas penderita gagal jantung
akut. Pengaruh independen tersebut menunjukkan bahwa penurunan akut fungsi ginjal
pada gagal jantung akut bukan semata-mata karena dari beratnya penyakit tetapi juga
berhubungan dengan percepatan jejas kardiovaskular melalui aktivasi jaras-jaras
neurohormonal, imunologis, dan inflamasi.13
Pada sindrom kardiorenal tipe I terjadinya AKI berhubungan dengan penurunan
perfusi ginjal. Disamping itu terjadi pula penurunan respons terhadap diuretik akibat
fenomena fisiologik yang disebut diuretic braking (semakin menghilangnya efek diuretik
yang terjadi sekunder akibat retensi natrium pasca pemberian diuretik).10,13
Diagnosis dini AKI pada sindrom kardiorenal tipe I maupun tipe III sangatlah
penting. Pada kedua kondisi tersebut penanda klasik seperti peningkatan kadar kreatinin
sudah menunjukkan kondisi yang terlambat, dan hanya sedikit yang bisa dilakukan untuk
mencegah dan melindungi ginjal dari kerusakan lebih lanjut. Penemuan berbagai
2. Sindroma Kardiorenal Kronik (Tipe II)
Sindroma kardiorenal tipe II ditandai oleh abnormalitas kronik fungsi jantung
(misalnya pada gagal jantung kronik) yang menyebabkan penyakit ginjal kronik
progresif. Perburukan fungsi ginjal pada penderita gagal jantung kronik berhubungan
dengan outcome yang buruk dan bertambahnya lama perawatan di rumah sakit.13
Mekanisme yang mendasari perburukan fungsi ginjal pada gagal jantung kronik
berbeda dibandingkan pada gagal jantung akut. Pada gagal jantung kronik telah terjadi
penurunan perfusi ginjal dalam jangka panjang, dan seringkali disertai predisposisi
penyakit mikrovaskular dan makrovaskular. Walaupun sebagian besar penderita dengan
GFR yang rendah juga berada pada kelas fungsional NYHA yang rendah, tidak terdapat
bukti konsisten yang menghubungkan fraksi ejeksi ventrikel kiri dengan GFR. Estimasi
GFR pada penderita gagal jantung kronik dengan fungsi ventrikel kiri yang baik dapat
tidak berbeda dibanding penderita dengan fraksi ejeksi ventrikel kiri yang terganggu.13
Patofisiologi disfungsi ginjal pada gagal jantung kronik belum sepenuhnya
dipahami. Kondisi tersebut tidak dapat diterangkan semata-mata akibat hipoperfusi.
Sebuah penelitian hemodinamik invasif pada gagal jantung kronik tidak menemukan
hubungan antara berbagai variabel hemodinamik pada pemeriksaan kateter arteri
pulmonal dengan kadar kreatinin serum. Satu-satunya variabel yang berhubungan adalah
peningkatan tekanan atrium kanan, menunjukkan kemungkinan peran kongesti ginjal
dalam perburukan fungsi ginjal pada gagal jantung kronik.13
Pada sindrom kardiorenal kronik terdapat abnormalitas neurohormonal dengan
produksi berlebih mediator-mediator vasokonstriktif (epinefrin, angiotensin, endotelin)
dan perubahan sensitivitas dan/atau pelepasan faktor-faktor vasodilator endogen (peptida
natriuretik, oksida nitrat). Farmakoterapi yang digunakan dalam pengelolaan gagal
jantung dapat turut memperburuk fungsi ginjal.10,13
Peran patogenik defisiensi absolut atau relatif eritropoietin terhadap terjadinya
anemia pada penderita gagal jantung tahap lanjut mungkin bukan semata-mata
disebabkan oleh gagal ginjal. Terdapat bukti bahwa aktivasi reseptor eritropoietin di
jantung dapat mencegah terjadinya apoptosis, fibrosis, dan inflamasi.13
Low-Flow State Hypotesis15
Pemikiran konvensional selama beberapa dekade menempatkan perburukan fungsi
ginjal yang progresif bersumber dari penurunan aliran darah atau hipoperfusi ginjal yang
disebabkan oleh penurunan curah jantung / cardiac output. Hipoperfusi yang persisten
kemungkinan akan menyebabkan proses iskemia pada parenkim ginjal yang pada akhirnya
menjadi infark.
Peningkatan Tekanan Vena Central Intra abdomen 15,16
Hubungan antara tekanan darah, cardiac output, dan resistensi pembuluh darah
sistemik diringkas oleh Hukum Poiseuille: aliran jantung tergantung pada tekanan yang
cukup gradien melalui jaringan kapiler tubuh. Gagal jantung ditandai oleh tingginya tekanan
vena sentral, yang melemahkan gradien seluruh jaringan kapiler glomerulus. Memang, ada
peningkatan bukti yang mendukung peran untuk tingginya tekanan vena renal dan tekanan
intra abdomen (IAP) dalam pengembangan disfungsi ginjal progresif pada pasien dengan HF.
Peningkatan tekanan vena ginjal mengakibatkan pembentukan urin terbatas dan aliran darah
ginjal berkurang pada tekanan arteri. Peningkatan tekanan vena ginjal dari kompresi
ekstrinsik dari pembuluh darah akan merusak fungsi ginjal. Lebih dari 60 tahun yang lalu,
Bradley dan Bradley menunjukkan bahwa kompresi abdomen yang menghasilkan tekanan
intraabdomen (IAP) 20 mmHg pada orang normal, nyata mengurangi GFR dan aliran plasma
ginjal. Hubungan ini didukung oleh penelitian in vivo model hewan modern. Dalam beberapa
menyertai sindrom kompartemen abdomen pada pasien bedah dan trauma. Perubahan ini
segera diatasi dengan dekompresi abdomen dan dapat dihubungkan dengan poliuria
berikutnya.
Gagal jantung ditandai dengan peningkatan central venous pressure (CVP) yang
mengakibatkan penurunan aliran perfusi yang melintasi kapiler ginjal. Studi-studi
menunjukkan peningkatan tekanan vena ginjal dapat menurunkan ataupun meniadakan
produksi urin, dan peningkatan tekanan vena ginjal ini lebih penting dibandingkan penurunan
tekanan arteri / perfusi pada kondisi ini. Sebelumnya telah dipaparkan bahwa kompresi
sementara terhadap vena ginjal menghasilkan penurunan ekskresi sodium, peningkatan
tekanan intertisial ginjal, dan akhimya mengakibatkan penurunan laju filtrasi glomerulus.
IAP dikatakan meningkat bila IAP > 8 mmHg, dan hipertensi intarabdominal
didefinisikan sebagai IAP > 12 mmHg. Studi yang dilakukan terhadap pasien ADHF yang
memiliki IAP > 8 mmHg didapati derajat penurunan IAP dengan pengobatan diuretik
berkorelasi dengan perbaikan fungsi ginjal. Pada studi-studi lain juga didapati disfungsi ginjal
ataupun perburukan fungsi ginjal sesudah awal ravvatan pada pasien-pasien dengan
peningkatan CVP yang signifikan, dan sebagai tambahan peningkatan tekanan vena jugularis
(JVP) pada pemeriksaan fisik berhubungan dengan tingginya kadar serum kreatinin awal
masuk rawatan.
Aktifasi Renin - Angiotensin - Aldosterone System (RAAS) 15,17,18
Aliran perfusi ginjal yang inadekuat menimbulkan mekanisme protektif tubuh dengan
mengaktifasi RAAS. Namun, bila kondisi ini terstimulasi secara kronis maka konsekuensi
patofisiologinya cukup berat dan memiliki pengaruh yang merusak pada sistem organ jantung
maupun ginjal.
Proses ini dimulai dengan renin yang diproduksi oleh juxtaglomerular apparatus
ginjal dan mengkatalisasi konversi angiotensinogen menjadi angiotensin I, dan akhirnya
menjadi angiotensin II oleh angiotensin-coverting enzyme (ACE). Angiotensin II (Ang II)
memiliki beberapa efek negatif terhadap sistem kardiovaskular pada pasien gagal jantung
yaitu menyebabkan peningkatan preload dan afterload, serta peningkatan myocard oxygen
demand.
Ang II juga dapat mengaktifasi enzim NADPH oksidase pada sel endotelial, otot
polos pembuluh darah, sel tubular ginjal, dan otot jantung; hal ini mengarah kepada
berkembang banyak bukti menyatakan bahwa ROS bertanggung jawab terhadap proses
aging, inflamasi, dan disfungsi organ yang progresif. Pada kondisi lain telah diketahui bahwa
Nitric Oxide (NO) bertanggung jawab terhadap proses vasodilatasi dan natriuresis, serta
inembantu ginjal dalam mengatur volume cairan ekstraseluler (ECF). Dalam hal ini
superoksida melawan efek NO tersebut dan mengurangi bioavailabilitas NO tersebut.
Keadaan stress oksidatif itu sendiri dapat merusak DNA, protein, karbohidrat, dan lemak,
juga mengakibatkan produksi sitokin menjadi mediator-mediator proinflamasi seperti : IL-1,
IL-6, dan TNF-a. Produksi sitokin-sitokin proinflamasi tersebut dapat menstimulasi proses
fibroblas yang akhirnya menyebabkan peningkatan fibrosis organ jantung dan ginjal.
Cardiorenal Anemia Syndrome (CRAS) 15
Anemia sering terjadi pada individu dengan penyakit ginjal kronis dan gagal jantung
dan dapat berkontribusi untuk keadaan abnormal oksidatif ginjal ; hemoglobin adalah
antioksidan. Anemia akan menginduksi peningkatan erythropoietin, ada bukti bahwa
penurunan konsentrasi pada pasien dengan kardiorenal mungkin langsung memperburuk
kelainan ginjal. Oleh karena itu, kombinasi dari anemia dan penurunan erythropoietin dapat
memperburuk faktor yang mendasari menyebabkan sindroma kardiorenal. Tingginya
frekuensi anemia pada sindroma kardiorenal telah berulang kali dibuktikan. Dalam the
Organized Program to Initiate Lifesaving Treatment in Hospitalized Patients With Heart
Failure (OPTIMIZE-HF), 51% dari hampir 50.000 pasien dengan gagal jantung memiliki
hemoglobin ≤12g/dL dan 25% memiliki hemoglobin antara 5 dan 10,7g/dL. Pasien dengan
gagal jantung dengan anemia meningkatkan kematian, lamanya tinggal di rumah sakit, dan
biaya pengobatan yang tinggi dibandingkan dengan pasien non anemia dengan gagal jantung.
Baik pasien dengan gagal jantung dan penyakit ginjal, bagaimanapun, memiliki konsentrasi
erythropoietin yang rendah.
Hipotesa ini pertama sekali dideskripsikan hampir beberapa dekade yang lalu oleh
Silverberg dkk. sebagai suatu siklus perburukan penyakit yang mengarah pada prognosis
yang kurang baik meliputi progresi yang cepat menjadi end-stage renal failure (ESRF)
ataupun progresi yang lebih jauh pada gagal jantung kongestif.27 Mereka memaparkan bahwa
anemia tidak hanya sebagai kondisi yang memicu disfungsi salah satu organ tapi juga dapat
mengeksaserbasi disfungsi salah satu organ. Studi The Candesartan inHeart Failure :
Assessment of Reduction in Morbidity and Mortality (CHARM) menyatakan bahwa anemia
DIAGNOSIS SINDROMA KARDIORENAL PADA TIPE 1 & 2
Terdapat banyak indikator diagnostik yang dapat menentukan kerusakan akut maupun
kronik pada sindroma kardiorenal yang meliputi analisa fungsi dan struktur kedua organ
dengan cara pemeriksaan biomarker kerusakan jantung, biomarker kerusakan ginjal, dan
pemeriksaan imejing. Kelompok konsensus IQDI membahas tentang peran biomarker dalam
diagnosis dari CRS. Tujuannya adalah untuk mengintegrasikan biomarker ke dalam diagnosis
berbagai tipe CRS, terutama yang berhubungan dengan AKI daripada penyakit jantung akut.
Berikut biomarker jantung dan ginjal serta pemeriksaan yang menunjang CRS8 :
1. Peptida natriuretik dan gagal jantung
Brain-type natriaretic peptide (BNP) dan N - terminal pro BNP (NT-pro BNP) disekresi dari miokard ventrikular sebagai respon jantung terhadap peningkatan tekanan
dan volume. ditetapkan sebagai alat diagnostik dalam ADHF dan merupakan prediktor
independen terhadap kejadian kardiovaskular dan mortalitas secara keseluruhan dalam
penyakit kritis, ACS, dan HF stabil. Peptida natriuretik (NP) meningkat pada pasien
dengan CRS (tipe I) di mana AKI terjadi sebagai konsekuensi dari ADHF. Selain itu,
mereka telah menunjukkan utilitas prognostik pada pasien dengan berbagai tahap
insufisiensi ginjal, menunjukkan aplikasi potensial dalam jenis CRS tipe II dan IV.
Menurut kebanyakan pedoman gagal jantung saat ini, pada keadaan akut kadar BNP >
100pg/ml atau kadar NT-pro BNP 300 pg/ml konsisten mengarah pada gagal jantung,
sedangkan pada keadaan kronik kadar yang direkomendasikan adalah BNP >35 pg/ml
atau kadar NT-pro BNP >125 pg/m1.3,8
2. Biomarker cedera ginjal
Kemampuan filtrasi ginjal diekspresikan sebagai laju filtrasi glomerulus (GFR)
yang secara klasik diestimasi menggunakan parameter kreatinin serum. Namun, GFR
tidak secara keseluruhan mewakili fungsi ginjal yang juga meliputi permeabilitas
glomerulus dan fungsi tubular, serta sebagai tambahan termasuk metabolisme vitamin D
dan produksi eritropoetin. Oleh sebab itu, beberapa biomarker selain kadar kreatinin
a. Neutrophil gelatinase-associated lipocalin (NGAL)
NGAL merupakan salah satu penanda awal iskemik ginjal ataupun kerusakan
karena nefrotoksik dan dapat dideteksi kadarnya melalui darah dan urin sesaat sesudah
terjadi acute kidney injury (AKI). Dalam penelitian terbaru, pengukuran tunggal dari
NGAL dari urin bisa mendeteksi AKI, dengan sensitivitas dan spesifisitas 90% dan 99%.
NGAL dapat digunakan sebagai penanda awal ARF selama pengobatan ADHF.8,19
b. Cystatin C
Kadar Cystatin C dalam sirkulasi telah muncul menjadi prediktor yang superior dibandingkan kadar kreatinin serum dalam mengestimasi laju filtrasi glomerulus.
Biomarker ini memiliki dampak yang kuat terhadap prognosis sindroma kardiorenal dan
berpotensi dalam menilai efek disfungsi ginjal yang ringan pada prognosis penyakit
kardiovaskular, serta menunjukkan sebagai prediktor progresi penyakit gagal jantung dan
insufisiensi ginjal pada pasien usia tua.8,19
c. Pemeriksaan kadar albuminuria
Selain sebagai target terapi yang penting pada pasien insufisiensi ginjal kronik,
juga awalnya telah dipaparkan sebagai penanda kerusakan permeabilitas glomerulus.
Pada pasien-pasien dengan diabetes, hipertensi, dan disfungsi ginjal kronik pemeriksaan
kadar albuminuria hams selalu diperiksa karena parameter ini dapat menjadi penanda
ataupun prediktor progresi penyakit kardiovaskular. Hasil perneriksaan
mikroalbuminuria didefinisikan dengan kadar albumin dalam urin 30-300 mg/24 jam,
sedangkan makroalbuminuria bila kadarnya dalam urin > 300 mg/24 jam.
d. Kidney injury molecule-1 (KIM-1)
KIM-1 merupakan protein yang dapat dideteksi dalam urin sesudah terjadi proses
urin tampaknya sangat spesifik untuk AKI iskemik dan bukan untuk pra-ginjal azotemia,
CKD, atau nefropati.8,19
e. N-asetil-β-(D) glucosaminidase
N-asetil-β-(D) glucosaminidase adalah enzim lisosomal ditemukan di sel-sel tubulus proksimal. N-asetil-β-(D) glucosaminidase telah terbukti berfungsi sebagai
penanda cedera ginjal, mencerminkan khususnya kerusakan tubular. Hal ini tidak hanya
ditemukan dalam konsentrasi kemih yang meningkat pada AKI dan CKD, tetapi juga
pada pasien diabetes, pasien dengan hipertensi esensial, dan gagal jantung.8,19
f. Interleukin-18
Interleukin-18 (IL-18) merupakan sitokin proinflamasi yang dapat dideteksi pada
urin setelah proses kerusakan iskemik akut pada tubulus proksimal dengan tingkat
sensitifitas dan spesifitas > 90%, dan juga kadarnya dapat meningkat 48 jam sebelum
didapati peningkatan kadar kreatinin serum.8,19
g. Bioimpedance vector analysis
Ada suatu kesepakatan bahwa Bioimpedance vector analysis (BIVA) dapat
berkontribusi untuk menjelaskan definisi yang lebih baik dari status hidrasi pasien.
Kombinasi NGAL dan BNP dapat digunakan untuk merencanakan strategi pemberian
cairan. Dengan cara ini, pasien dapat dijaga dengan ketat hidrasi yang adekuat dalam
pencegahan perburukan fungsi ginjal dan jantung. 8
Dari biomarker yang disajikan di atas, NGAL (urin dan plasma) dan C Cystatin
yang paling mungkin untuk diintegrasikan ke dalam praktek klinis dalam waktu dekat.
Uji klinis akan diperlukan untuk melihat apakah identifikasi awal AKI dan penggunaan
algoritma pengobatan khusus berdasarkan tanda tersebut akan memperbaiki prognosis.8
3. Pencitraan
Teknik pencitraan memiliki peran tambahan sehubungan dengan biomarker
laboratorium pada CRS. Pencitraan mungkin meningkatkan, memperluas, dan memperbaiki
kemampuan kita untuk menghitung kerusakan ginjal dan menilai fungsinya. Pada pasien
yang dicurigai CRS, sebaiknya menghindari penggunaan media kontras iodinasi jika tidak
benar-benar diperlukan. Kedepannya, diharapkan penelitian harus diarahkan studi
eksperimental yang menerapkan teknik pencitraan molekular (seperti MRI/magnetic
resonance imaging, MRS/magnetic resonance spectroscopy, PET/positron emission
keparahan berbagai jenis CRS. Juga di masa depan, teknik non-invasif pencitraan perlu
diperbaiki untuk mengukur aliran darah ginjal. Data tersebut kemudian dapat dikorelasikan
dengan biomarker jantung dan ginjal dan yang paling penting untuk merencanakan terapi
berkelanjutan yang dirancang dalam pengoptimalan aliran darah ginjal dan akhirnya menjaga
fungsi ginjal. Adapun tipe 1 CRS, kongesti vena dan CVP (central vein pressure) yang tinggi
tampaknya dikaitkan dengan gangguan fungsi ginjal dan independen terkait dengan semua
penyebab kematian dalam spektrum yang luas dari pasien dengan penyakit kardiovaskular.
Pemeriksaan ekokardiografi dapat menyediakan informasi mengenai anatomi dan
fungsi jantung. Penilaian terhadap fungsi sistolik dan diastolik ventrikel kiri danai juga
dilakukan dan pasien dapat dikategorikan ke dalam gagal jantung dengan ejection
fraction yang rendah ataupun dengan ejection fraction yang normal.12
Ultrasonografi yang meliputi ultrasound ginjal dan ultrasoncgrafi vena cava
inferior dapat sangat membantu dalam menentukan diagnosis dan secara tepat
mengklasifikasikan sindroma kardiorenal. Ultrasound ginjal itu sendiri dapat membantu
klinisi dalam membedakan antara gagal ginjal akut maupun kronik, serta mampu
mengeksklusi adanya tidaknya obstruksi pada saluran kemih, menilai arteri ginjal dengan
menggunakan doppler, dan juga mampu memberikan informasi mengenai ukuran ginjal
ataupun ekogenisitas parenkim ginja1.12
TATALAKSANA SINDROMA KARDIORENAL PADA TIPE 1 & 2
Penderita dengan gangguan fungsi ginjal tidak secara adekuat terwakili dalam
penelitian-penelitian klinik acak berskala besar pada gagal jantung, sehingga sebagian besar
rekomendasi terapi lebih bersifat empirik.13
Pengelolaan penderita gagal jantung dengan gangguan fungsi ginjal dapat menjadi
sulit disebabkan fungsi kedua organ tersebut sangat bergantung pada volume sirkulasi. Secara
garis besar sasaran pengobatan adalah mencapai status volume yang normal tanpa
memperberat disfungsi ginjal, dan menerapkan seoptimal mungkin terapi yang secara
evidence-based bermanfaat pada gagal jantung maupun disfungsi ginjal. Sampai saat ini tidak
ada strategi yang secara konsisten efektif. Langkah-langkah berikut dapat digunakan dalam
Sindroma Kardiorenal Tipe 1
Abnormalitas fungsi renal dan juga perburukan pada awal rencana pengobatan ADHF
meningkatkan mortalitas. Oleh sebab itu, pengobatan terhadap gagal jantung seharusnya
memiliki efek yang diharapkan untuk memperbaiki fungsi ginjal dan menghindari pemakaian
zat ataupun obat yang bersifat nefrotoksik yang justru akan semakin memperburuk fungsi
ginja1.3
Manajemen gagal jantung akut seperti yang telah dipaparkan dalam pedoman yang
disusun oleh European Society of Cardiology (ESC) bahwa penggunaan obat vasodilator dan
loop diuretik sangat direkomendasikan pada kasus gagal jantung akut dan sindroma
kardiorenal tipe 1 selain pemberian oksigenasi yang adekuat dan opiat sebagai penenang serta
pereda kesulitan dalam bernafas.3
Penggunaan loop diuretik secara infus kontinu dengan estimasi total dosis harian
dapat memberikan efek diuresis yang lebih efektif dan aman bila dibandingkan dengan
pemberian injeksi bolus. Kombinasi diuretik dapat diberikan untuk lebih memberikan efek
diuresis yang efektif terutama dalam mengatasi kondisi resistensi diuretik.5
Obat vasodilator seperti nitrogliserin intravena ataupun nesiritide (recombinant
human B-type atrial natriuretic peptide) telah menunjukkan dapat secara cepat rnenurunkan
tekanan pengisian ventrikel dan CVP, serta mengurangi konsumsi oksigen miokard. Obat ini
juga dapat menurunkan resistensi vaskular sistemik, mengurangi beban kerja ventrikular,
meningkatkan stroke volume dan memperbaiki cardiac output. Nitrogliserin intravena
merupakan vasodilator yang sering digunakan untuk mengurangi kongesti pulmonal pada
pasien pasien dengan gagal jantung dekompensata. Penurunan tekanan vena dapat
memberikan keuntungan dalam menurunkan tekanan perfusi ginjal.5
Pada kasus syok kardiogenik maka terapi yang diberikan bertujuan untuk
meningkatkan cardiac output dan mengembalikan aliran darah ginjal melalui optimalisasi
tekanan darah sistolik. Untuk tujuan tersebut dapat diberikan dopamin dosis rendah (renal
dose), dobutamin, atupun milrinone. Bila kondisi hipotensi sistemik masih menetap ataupun
refrakter maka dapat dipertimbangkan pemberian vasopresor seperti norepinefrin, dan
tindakan ventilasi elektif ataupun intraaortic balloon pump dengan target yang ingin dicapai
yaitu cardiac index>2 L/menit/m2 dan mean arterial pressure (MAP) > 60 mmHg.3,5
Pada pasien dengan perburukan fungsi ginjal yang menetap, tindakan continous
venovenous ultrafiltration telah dipaparkan sebagai alternatif untuk mengurangi volume
diindikasikan pada kondisi resistensi diuretik pada pasien gagal jantung berat.5
Sindroma Kardiorenal Tipe 2
Pendekatan terapeutik pada pasien-pasien dengan gagal jantung kronik (CHF) sangat
kompleks dan berbasis pada skor NYHA, restriksi cairan dan garam, perubahan pola hidup
(aktifitas fisik, berhenti merokok), juga meliputi pengobatan dan penyebab dasar dan / atau
penyakit yang menyebabkan kerusakan pada sistem kardiovaskular dan progresi terhadap
gagal jantung kronik (yang utamanya seperti : hipertensi, diabetes melitus, hiperlipidemia,
aritmia).3
Seperti dalam pedoman penanganan gagal jantung oleh ESC, penggunaan angiotensin
converting enzyme inhibitor (ACE-I) / angiotensin receptor blocker (ARB), beta blocker,
antagonis aldosteron secara signifikan menurunkan tingkat morbiditas (perburukan fungsi
ginjal) dan mortalitas pada CHF. Pendekatan yang optimal yaitu mengkombinasi ACE-I /
ARB dan beta blocker dengan dosis dititrasi, kemudian ditambahkan antagonis aldosteron
tergantung pada kondisi klinis dan karakteristik pasien. Digoxin dan diuretik juga dapat
diberikan untuk membantu memperbaiki gejala pada CHF. Secara tipikal pasien-pasien CHF
dalam kondisi hipervolemik sehingga pemberian terapi diuretik intensif diperlukan terutama
loop diuretik infus kontinu yang lebih poten. Pada kasus overload refrakter ataupun resistensi
KESIMPULAN
Sindroma kardiorenal memiliki patofisiologi yang unik dan kompleks. Diagnosis
lebih awal pada kondisi ini (dengan pemeriksaan biomarker dan/ ataupun pemeriksaan
pencitraan) serta manajemen yang efektif (optimalisasi pengobatan gagal jantung seperti :
penggunaan vasodilator, diuretik, inotropik, ACE-I / ARB, beta blocker, antagonis
aldosteron, digoksin, maupun tindakan ultrafiltrasi), serta menghindari pemakaian zat
ataupun obat-obatan yang bersifat nefrotoksik dapat menurunkan insidensi perburukan fungsi
ginjal pada pasien-pasien gagal jantung dekompensata sehingga dapat memperbaiki
prognosis pasien.
Sampai saat ini tidak ada panduan tatalaksana gagal jantung pada penderita dengan
disfungsi ginjal yang berdasarkan bukti-bukti kuat (evidence-based). Langkah-langkah berikut
dapat digunakan dalam pendekatan pengelolaan penderita yaitu identifikasi dan antisipasi
gangguan dan perburukan fungsi ginjal, optimalisasi terapi gagal jantung, evaluasi struktur ginjal,
optimalisasi terapi diuretik, dan terapi lain. Walaupun demikian penderita tampaknya akan
memperoleh manfaat yang sama bila dikelola dengan panduan tatalaksana gagal jantung untuk
populasi umum, asalkan dengan pemantauan lebih ketat. Tatalaksana sindrom kardiorenal
menjadi sulit disebabkan terbatasnya pengetahuan tentang mekanisme yang mendasarinya, dan
terbatasnya pilihan terapi yang tersedia. Sampai saat ini tidak ada terapi efektif yang telah
DAFTAR PUSTAKA
1. Shah BN, Greaves K. The Cardiorenal Syndrome: A Review. International Journal of
Nephrology. 2011; 920195: 1-11.
2. Rosner MH, Rastogi A, Ronco C. The Cardiorenal Syndrome. International Journal of
Nephrology.2011; 982092:1-2.
3. McMurray JJV, Adamopoulos S, Anker SD, et al. ESC Guidelines for the diagnosis and
treatment of acute and chronic heart failure 2012. Eur Heart J2012; 33:1787-1847
4. Owan TE, Hodge DO, Herges RM, Jacobsen SJ, Roger VL, Redfield MM. Secular
trends in renal dysfunction and outcomes in hospitalized heart failure patients. J Card
Fail 2006;12:257-62
5. PP Liu. Cardiorenal syndrome in heart failure: A cardiologist's perspective. Can J
Cardiol 2008;24(Suppl B):25B-29B
6. Roesli RM, Martakusumah AH. Sindroma Kardio Renal. FK UNPAD/ RS dr Hasan
Sadikin Bandung : Subbag Ginjal Hipertensi, Bag. Ilmu Penyakit Dalam. Available
from: http://pustaka.unpad.ac.id/wp-content/uploads/2009/10/sindroma_kardio_renal.pdf
7. Schrier W R. Cardiorenal versus renocardiac syndrome: is there a difference? Nat Clin
Prac Nephrol 2007; 3; 12; 637
8. Ronco C, et al. Cardio-renal syndromes: report from the consensus conference of the
Acute Dialysis Quality Initiative. European Heart Journal. 2010;31, 703-7011.
9. Liang KV, Williams AW, Greene EL, Redfield MM. Acute decompensated heart failure
and the cardiorenal syndrome. Crit Care Med 2008;36(Suppl 1):S75-88.
10. Ronco C, Haapio M, House AA, Anavekar N, Bellomo R. Cardiorenal syndrome. J Am
Coll Cardiol 2008;52:1527-39.
11. Ronco C, House AA, Haapio M. Cardiorenal syndrome: refining the definition of a
complex symbiosis gone wrong. Intensive Care Med 2008; 34 (5): 957-62
12. Manolis AS, Papadimitriou P, Manolis TA, Apostolou T. Cardiorenal Syndrome: A
13. Hidayat S. Interaksi Kardiorenal : Implikasi Terapi. Dep Cardiology & Vascular
Medicine. Fakultas Kedokteran Universitas Indonesia. 2010. Available from:
http://www.kardiologi-ui.com/newsread.php?id=354.
14.Bongartz LG, Cramer MJ, Doevendans PA, Joles JA, Braam B. The severe cardiorenal
syndrome: Guyton revisited. Eur Heart J 2005;26:1115-40
15. Jeremy S. Bock, Stephen S. Gottlieb. Contemporary Reviews in Cardiovascular
Medicine. Cardiorenal Syndrome. 2010. Available from:
http://circ.ahajournals.org/content/121/23/2592.full.pdf
16. Malbrain ML, Cheatham ML, Kirkpatrick, Sugrue M, Parr M, De Waele J, Balogh Z,
Leppäniemi A, Olvera C, Ivatury R, D'Amours S, Wendon J, Hillman K, Johansson K,
Kolkman K, Wilmer A. Results from the International Conference of Experts on
Intra-abdominal Hypertension and Abdominal Compartment Syndrome. Intensive Care Med.
2006; 32: 1722–1732
17. Remuzzi G, Perico N, Macia M, Ruggenenti P. The role of the
renin-angiotensin-aldosterone system in the progression of chronic kidney disease. Kidney Int. 2005; suppl:
S57–S65.
18. Vaziri ND, Dicus M, Ho ND, Boroujerdi-Rad L, Sindhu RK. Oxidative stress and
dysregulation of superoxide dismutase and NADPH oxidase in renal insufficiency.
Kidney Int. 2003; 63: 179–185.
19. Pam R Taub; Kelly C Borden; Arrash Fard; Alan Maisel. Role of Biomarkers in the
Diagnosis and Prognosis of Acute Kidney Injury in Patients With Cardiorenal Syndrome.
Expert Rev Cardiovasc.Ther. 2012;10(5):657-667. Available from:
Sampai saat ini tidak ada strategi yang secara konsisten efektif. Langkah-langkah berikut
dapat digunakan dalam pendekatan pengelolaan penderita. Pendekatan pengelolaan sindroma
kardiorenal8 :
1. Identifikasi dan antisipasi gangguan dan perburukan fungsi ginjal
2. Optimalisasi terapi gagal jantung
3. Evaluasi struktur ginjal
4. Optimalisasi terapi diuretik
5. Terapi lain
1. Identifikasi dan antisipasi gangguan dan perburukan fungsi ginjal
Gangguan fungsi ginjal yang ditandai oleh penurunan GFR kurang dari 60
mL/menit merupakan prediktor yang kuat untuk terjadinya dampak yang buruk pada
penderita gagal jantung, bahkan nilai prognosis tersebut relatif lebih kuat dibanding
penurunan fraksi ejeksi ventrikel kiri. Penurunan GFR tidak selalu disertai peningkatan
kadar kreatinin serum, bahkan sebagian besar penderita dengan gangguan fungsi ginjal
mempunyai kadar kreatinin serum dalam rentang relatif normal. Penilaian fungsi ginjal
yang didasarkan pada pemeriksaan kadar kreatinin serum menyebabkan sebagian besar
gangguan fungsi ginjal pada penderita gagal jantung tidak terdeteksi secara klinis.
Mengingat perannya yang penting, penilaian GFR sebaiknya secara rutin dilakukan
sebagai bagian dalam evaluasi dan tatalaksana penderita gagal jantung.13
Secara akurat GFR dapat ditentukan dengan pemeriksaan klirens inulin atau
marka radionuklida, tetapi mengingat pemeriksaan tersebut tidak praktis, nilai GFR dapat
diperkirakan dengan menggunakan formula Cockfoft-Gault atau Modified Diet in Renal
Disease (MDRD). Berlainan dengan penilaian disfungsi ginjal yang lebih akurat
ditentukan dengan pemeriksaan GFR, terjadinya perburukan fungsi ginjal pada penderita
gagal jantung yang dirawat di rumah sakit ditandai oleh peningkatan kadar kreatinin
serum lebih dari 0,3 mg/dl atau lebih dari 25% kadar awal. Walaupun setiap peningkatan
tersebut baru bermakna pada peningkatan lebih dari 0,3 mg/dl. Faktor-faktor risiko yang
secara konsisten mempengaruhi terjadinya perburukan fungsi ginjal pada penderita gagal
jantung adalah usia lanjut, hipertensi, diabetes dan terdapat gangguan fungsi ginjal
sebelumnya. Faktor-faktor lain yang potensial adalah penggunaan dosis besar diuretik
loop, dan penggunaan diuretik thiazide. Perburukan fungsi ginjal tidak berhubungan
bermakna dengan fraksi ejeksi ventrikel kiri, cardiac index, resistensi vaskular sistemik,
dan kondisi low-output (hipotensi). Perburukan fungsi ginjal lebih sering ditemukan pada
penderita-penderita dengan presentasi klinik retensi cairan (edema paru, peningkatan
tekanan vena jugular). Dalam menghadapi penderita dengan disfungsi kardiorenal adalah
penting untuk mengidentifikasi faktor-faktor yang potensial reversibel seperti hipotensi,
dehidrasi, penggunaan inhibitor ACE atau penyekat reseptor angiotensin (angiotensin
receptor blocker/ARB), penggunaan non-steroid anti inflamasi drugs (NSAID), dan
stenosis arteri renalis. Langkah-langkah yang harus dilakukan adalah penilaian status
volume, cardiac output dan kemungkinan terdapatnya penyakit ginjal intrinsik. Kondisi
hipovolemia harus diatasi sebelum terjadi kerusakan ginjal lebih lanjut. Perfusi ginjal
harus dijaga dengan mempertahankan tekanan darah sistolik > 80 mmHg dan tekanan
arterial rata-rata > 50 mmHg. Fungsi ginjal akan membaik sejalan dengan perbaikan
cardiac output dan perfusi ginjal. Bila disfungsi ginjal menetap walaupun telah
dilakukan perbaikan status volume, cardiac output dan resistensi vaskular sistemik, perlu
dipertimbangkan adanya penyakit ginjal intrinsik yang mendasari. Terapi yang dipandu
dengan pemantauan tekanan pembuluh darah kapiler pulmonal tidak terbukti lebih
unggul dibanding pemantauan secara klinis dalam memperbaiki outcome penderita gagal
jantung tahap lanjut. Penggunaan kateter arteri pulmonal mungkin diperlukan pada
penderita sindrom kardiorenal yang berat untuk mengoptimalkan hemodinamik,
memandu terapi gagal jantung lebih agresif, memfasilitasi keputusan untuk memulai
terapi ginjal pengganti, atau dalam membuat keputusan untuk memulai terapi paliatif
gagal jantung kronik.13
Penelitian akhir-akhir ini menunjukkan bahwa perburukan fungsi ginjal pada
penderita gagal jantung lebih banyak dipengaruhi oleh kondisi hipervolemik dibanding
hipoperfusi ginjal akibat penurunan cardiac output atau penurunan volume intravaskuler
akibat penggunaan diuretik berlebih. Bendungan vena yang ditandai oleh peningkatan
tekanan vena sentral merupakan penyebab yang paling kuat untuk terjadinya perburukan
dengan terapi medik intensif selama perawatan hanya sedikit berpengaruh terhadap
fungsi ginjal. Sampai saat ini masih terlalu dini untuk menyimpulkan bahwa terapi yang
spesifik bertujuan menurunkan tekanan vena sentral akan memperbaiki disfungsi ginjal
dan outcome penderita gagal jantung, walaupun demikian hal tersebut perlu
dipertimbangkan dalam strategi tatalaksana gagal jantung.13
2. Optimalisasi terapi gagal jantung
Inhibisi pada sistem renin-angiotensin-aldosteron telah diketahui merupakan
bagian penting dalam tatalaksana gagal jantung. Berbagai penelitian acak terkontrol
berskala besar menunjukkan bahwa obat-obat tersebut secara bermakna meningkatkan
harapan hidup penderita. Akan tetapi evidence-based manfaatnya pada penderita gagal
jantung dengan gangguan fungsi ginjal sangat terbatas. Penggunaan inhibitor ACE atau
ARB biasanya berhubungan dengan penurunan ringan fungsi ginjal yang ditandai oleh
peningkatan kadar kreatinin dan penurunan GFR. Penurunan fungsi ginjal tersebut
semakin nyata pada penderita disfungsi ginjal. Kekhawatiran akan semakin
memburuknya fungsi ginjal disertai risiko hipotensi dan hiperkalemia menyebabkan
banyak klinisi menghindari atau menghentikan penggunaan inhibitor ACE atau ARB
pada penderita disfungsi ginjal. Akan tetapi sebuah meta-analisis tentang penggunaan
inhibitor ACE dalam hubungannya dengan peningkatan kadar kreatinin menunjukkan
bahwa penderita yang mengalami peningkatan kadar kreatinin setelah pemberian
inhibitor ACE adalah kelompok penderita yang justru mendapat manfaat paling besar
dari penggunaan obat tersebut.13
Untuk mengurangi risiko perburukan fungsi ginjal, penggunaan inhibitor ACE
sebaiknya dimulai dengan dosis rendah. Bila terjadi perburukan fungsi ginjal perlu
dinilai kemungkinan penyebab lain seperti diuresis yang berlebihan, hipotensi persisten,
atau penggunaan obat lain yang nefrotoksik termasuk NSAID. Bila kadar kreatinin
meningkat tajam dan penderita menunjukkan intoleransi ekstrim terhadap inhibitor ACE,
perlu dipertimbangkan kemungkinan stenosis arteri renalis bilateral. Pada kondisi ini
penggunaan inhibitor ACE atau ARB harus dihentikan. Beberapa penelitian
menunjukkan penggunaan inhibitor ACE pada penderita disfungsi ginjal dapat
menghambat perburukan fungsi ginjal dan memperbaiki outcome kardiovaskular. Oleh
karena itu obat ini sebaiknya tetap diberikan walaupun terjadi peningkatan kadar
kreatinin, asalkan fungsi ginjal tidak terus memburuk dan tidak terjadi hiperkalemia.
dengan efek renoprotektif jangka panjang. Perburukan fungsi ginjal pada penderita gagal
jantung yang terjadi selama perawatan di rumah sakit sebagian besar tidak disebabkan
oleh inhibitor ACE. Pada penderita yang mengalami vasodilatasi berlebih, mungkin
diperlukan penurunan dosis atau penghentian sementara penggunaannya, tetapi
mengingat efek jangka panjang yang menguntungkan baik pada gagal jantung maupun
disfungsi ginjal, penggunaan inhibitor ACE atau ARB sebaiknya tidak dihentikan atau
segera diberikan kembali.13
Tidak ada patokan kadar kretinin yang mutlak untuk menghentikan penggunaan
inhibitor ACE atau ARB, tetapi pada kadar kreatinin diatas 2,5 mg/dl penggunaannya
harus dengan pemantauan ketat. Pada penderita dengan kadar kreatinin diatas 5 mg/dl
mungkin dibutuhkan hemofiltrasi atau dialisis untuk mengontrol retensi cairan dan
mengatasi uremia. Proporsi penderita disfungsi ginjal yang mendapat terapi modifikasi
risiko kardiovaskular yang memadai jauh lebih rendah dibanding populasi umum.
Kurang dari 50% penderita disfungsi ginjal mendapat kombinasi aspirin, penyekat beta,
inhibitor ACE, dan statin setelah suatu serangan infark miokard. Sebuah penelitian
kohort prospektif menunjukkan penggunaan inhibitor ACE dan penyekat beta pada
penderita gagal jantung yang disertai disfungsi ginjal berhubungan dengan penurunan
mortalitas yang sebanding dengan penderita tanpa gangguan fungsi ginjal. Penggunaan
antagonis aldosteron pada penderita gagal jantung dengan disfungsi ginjal harus
dilakukan dengan hati-hati. Bila indikasinya telah terpenuhi, yaitu pada penderita gagal
jantung simptomatik berat dengan fraksi ejeksi yang rendah, penambahan antagonis
aldosteron pada regimen inhibitor ACE/ARB dan penyekat beta berhubungan dengan
peningkatan kesintasan penderita gagal jantung. Untuk menghindari kejadian
hiperkalemia yang mengancam jiwa, obat ini sebaiknya tidak diberikan bila kadar
kreatinin > 2,5 mg/dl atau kadar kalium > 5,0 mmol/l. Walaupun sampai saat ini tidak
ada panduan dengan evidence-based yang kuat untuk terapi gagal jantung pada penderita
disfungsi ginjal, tampaknya penderita dalam populasi tersebut akan memperoleh manfaat
yang sama bila dikelola dengan panduan tatalaksana gagal jantung untuk populasi umum,
walaupun diperlukan pemantauan yang lebih ketat.13
3. Evaluasi struktur ginjal
Pemeriksaan ultrasonografi ginjal dapat digunakan untuk mengevaluasi ukuran
ginjal, adanya obstruksi atau penyakit ginjal struktural. Pemeriksaan ini bermanfaat
reversibel. Pencitraan Doppler digunakan bila terdapat kecurigaan stenosis arteri renalis.
Bila diperlukan pemeriksaan angiografi atau pencitraan resonansi magnetik yang
menggunakan kontras, rasio risiko–manfaatnya harus dipertimbangkan dengan seksama
mengingat kemungkinan perburukan fungsi ginjal.13
4. Optimalisasi terapi diuretik
Diuretik memegang peran penting dalam tatalaksana gagal jantung yang disertai
disfungsi ginjal. Manfaatnya dalam memperbaiki simptom telah disepakati secara luas,
walaupun tidak pernah dievaluasi melalui penelitian-penelitian acak klinik berskala
besar. Pada kondisi gagal jantung dan disfungsi ginjal kurva respons-dosis diuretik akan
terpengaruh. Selain diperlukan penambahan dosis untuk menghasilkan respons diuresis
yang memadai, juga akan terjadi penurunan respons maksimum yang dapat dicapai, menciptakan keadaan resistensi diuretik relatif yang dikenal sebagai “braking phenomenon”, yaitu kondisi toleransi jangka pendek terhadap pemberian diuretik.13
Peningkatan dosis dan penurunan respons diuretik akan bertambah sejalan
dengan progresifitas gagal jantung. Sesuai beratnya penyakit, dosis maksimum diuretik
untuk masing-masing penderita berbeda, dan penambahan dosis diatas dosis maksimum
tidak akan menambah respons diuresis lebih lanjut. Penggunaan diuretik memerlukan
kecermatan. Dosis yang digunakan harus memadai untuk mengatasi kelebihan cairan dan
memperbaiki simptom tanpa menyebabkan efek yang kurang menguntungkan.
Penggunaan diuretik, terutama dosis besar diuretik loop diketahui berhubungan dengan
perburukan fungsi ginjal, meningkatkan risiko perawatan di rumah sakit dan mortalitas
penderita gagal jantung. Hal ini diantaranya disebabkan efek diuretik dalam
menstimulasi sistem RAA. Stimulasi sistem RAA tersebut merupakan salah satu faktor
utama penyebab terjadinya resistensi diuretik. Resistensi diuretik merupakan salah satu
ciri sindrom kardiorenal, dan menjadi indikator prognosis yang buruk penderita gagal
jantung kronik. Kombinasi antara perburukan fungsi ginjal, volume overload, dan
resistensi diuretik, menyebabkan tatalaksana sindrom kardiorenal menjadi sulit, dan
sampai saat ini terapi yang efektif sangat terbatas. Definisi resistensi diuretik telah
disebutkan sebelumnya. Banyak faktor yang mempengaruhi terjadinya resistensi diuretik
diantaranya adalah dosis yang tidak adekuat, asupan garam berlebih, gangguan absorbsi
intestinal, menurunnya ekskresi diuretik dalam urine, peningkatan reabsorbsi natrium
respons-dosis diuretik tidak linier, sehingga natriuresis tidak akan terjadi sampai ambang
ekskresi obat tercapai. Dengan demikian bila respons diuresis tidak terjadi dengan
pemberian furosemide 20 mg, menaikkan dosisnya menjadi 40 mg akan lebih efektif
dibanding meningkatkan frekuensinya.13
Diuretik thiazide akan menghambat reabsorbsi natrium di tubulus distal, sehingga
bila dikombinasi dengan diuretik loop diharapkan akan memberi respons diuresis lebih
baik. Kombinasi ini perlu pemantauan ketat karena dapat menyebabkan hiponatremia
dan hipokalemia berat. Diuretik thiazide tidak efektif bila klirens kreatinin < 30
ml/menit. Pada penderita gagal jantung yang berat sering terjadi gangguan perfusi
intestinal, penurunan motilitas intestinal, dan edema mukosa yang akan menyebabkan
absorbsi obat terganggu. Absorbsi furosemid oral pada keadaan edema hanya sekitar
50%. Untuk menghasilkan respons diuresis yang adekuat mungkin diperlukan
penambahan dosis atau menggantinya dengan obat yang diabsorbsi lebih baik yaitu
bumetanide atau torsemide. Untuk memperbaiki respons diuresis dapat pula diberikan
diuretik intravena dalam jangka pendek. Respons inadekuat dengan pemberian diuretik
oral seringkali reversibel setelah kelebihan cairan diatasi.13
Pemberian diuretik loop dengan infus intravena kontinyu dapat mempertahankan
kecepatan penghantaran obat ke tubulus renal dan mencegah reabsorbsi natrium lebih
konsisten. Pemberian diuretik loop dengan infus kontinyu pada penderita gagal jantung
menghasilkan respons diuresis lebih adekuat dengan efek samping yang lebih rendah
dibanding pemberian bolus intravena. Apabila berbagai upaya tersebut tidak berhasil
mengatasi resistensi diuretik, perlu dipertimbangkan untuk melakukan ultrafiltrasi. 12
5. Terapi lain
Terdapat berbagai terapi lain untuk mengatasi sindrom kardiorenal, beberapa
diantaranya telah ditinggalkan dan beberapa masih dalam penelitian.13 Dopamin dosis rendah13
Dopamin dosis rendah pernah digunakan secara luas di seluruh dunia untuk
mencegah atau mengobati AKI dan dipakai untuk meningkatkan produksi urine pada
penderita gagal jantung yang refrakter terhadap diuretik loop. Dopamin terutama akan
menstimulasi reseptor-reseptor dopaminergik yang menyebabkan vasodilatasi renal dan
peningkatan aliran darah ginjal. Dopamin juga menyebabkan natriuresis melalui efek
Terdapat 2 meta-analisis, tinjauan sistematik dan penelitian klinik acak yang
mengevaluasi peran dopamin dosis rendah dalam mencegah perburukan fungsi ginjal.
Semua penelitian tersebut sampai pada kesimpulan yang sama yaitu dopamin dosis
rendah tidak mencegah terjadinya AKI, kebutuhan untuk dialisis, atau kematian. Efek
protektif dopamin pada ginjal tidak terbukti, bahkan dapat menginduksi AKI pada
penderita normo dan hipovolemik. Dopamin juga dapat menurunkan aliran darah mukosa
gaster, menekan sekresi dan fungsi hormon-hormon pituitari anterior termasuk
menginduksi hipotiroid, dan dapat menumpulkan ventilatory drive.
Dengan berbagai bukti yang kuat tersebut, penggunaan dopamin dosis rendah
untuk proteksi ginjal pada berbagai keadaan termasuk pada gagal jantung tidak lagi
dianjurkan.
Kombinasi furosemide – manitol13
Manitol bila diberikan secara intravena akan segera difiltrasi oleh glomerulus
kedalam cairan tubulus menyebabkan efek diuresis osmotik. Manitol dapat
meningkatkan aliran darah intrarenal melalui efeknya terhadap produksi prostaglandin
dan bertindak sebagai penangkap radikal bebas selama reperfusi ginjal. Sebuah
penelitian terhadap 100 penderita AKI pasca operasi jantung menunjukkan pemberian
larutan mengandung 500 cc manitol 20% dan 1000 mg furosemide yang diberikan dalam
waktu 30 – 60 menit, dengan disertai pemberian dopamin dosis rendah dapat mendorong
terjadinya diuresis pada AKI fase oligurik atau anurik pasca operasi. Bila diberikan dini
yaitu dalam 6 jam setelah onset AKI, kombinasi ini dapat memperbaiki fungsi ginjal dan
menurunkan kebutuhan dialisis. Beberapa penelitian berskala kecil yang mengevaluasi
pemberian manitol untuk mencegah atau mengatasi AKI menunjukkan hasil yang
bertentangan. Dapat terjadi efek samping berupa gangguan elektrolit, hipovolemia, dan
perburukan fungsi ginjal. Sampai saat ini tidak ada bukti kuat tentang manfaat manitol
dalam tatalaksana AKI sehingga penggunaannya harus dibatasi. Kombinasi furosemide – albumin13
Penderita dengan kadar albumin yang rendah dapat resisten terhadap pemberian
diuretik. Pemberian kombinasi albumin dan furosemide pada kondisi tersebut diharapkan
dapat meningkatkan konsentrasi diuretik yang mencapai nefron proksimal dan
memperbaiki diuresis. Penelitian pada penderita sindrom nefrotik maupun pada sirosis
respons diuresis, sehingga penggunaannya untuk tujuan memperbaiki resistensi diuretik
pada kondisi hipoalbuminemik tidak dianjurkan. Kombinasi furosemide – natrium hipertonik13
Pemberian infus larutan natrium hipertonik (hypertonic saline solution=HSS)
akan menyebabkan kenaikan konsentrasi NaCl ekstraseluler dengan cepat sehingga
terjadi kenaikan tekanan osmotik, ekspansi volume plasma, mobilisasi cairan
ekstravaskular ke intravaskular, dan bertambahnya aliran darah ginjal. Pemberian secara
simultan furosemide dosis tinggi akan mengoptimalkan efek diuresis dan mengatasi
resistensi diuretik. Penelitian acak tersamar ganda pada 94 penderita gagal jantung tahap
lanjut mendapatkan bahwa pemberian dua kali per hari infus furosemide 500–1000 mg
yang dilarutkan dalam 150 cc NaCl hipertonik (1,4% – 4,6%) dan diberikan dalam 30
menit selama 4 – 6 hari, disertai diet normosodium (2,8 gr natrium/hari), secara
signifikan berhubungan dengan pencapaian berat kering yang lebih cepat, penurunan
konsentrasi plasma B-type natriuretic peptide (BNP) lebih cepat, perawatan di rumah
sakit yang lebih singkat, dan menurunkan insiden perawatan kembali dalam 30 hari. Pada
follow-up selama hampir 3 tahun, insiden perawatan kembali penderita yang mendapat
HSS sebesar 47% (25 dari 53 penderita), sedangkan penderita yang mendapat perawatan
biasa sebesar 80% (43 dari 54 penderita). Mortalitas penderita yang mendapat HSS juga
lebih rendah. Efek langsung intratubuler pemberian natrium hipertonik akan melampaui
pengaruh retensi natrium pasca diuretik sehingga akan mengurangi “braking
phenomenon”. Disamping itu peningkatan volume intravaskular dan kadar natrium yang
lebih tinggi pada tubulus distal akan menghambat sistem RAA. Walaupun tampaknya
memberi harapan, pemberian natrium hipertonik atau asupan garam yang lebih bebas
pada penderita gagal jantung masih memerlukan penelitian lebih lanjut. Terapi ini dapat
dipertimbangkan pada penderita sindrom kardiorenal yang tidak berhasil diatasi dengan
terapi lain. Nesiritide12 Nesiritide adalah rekombinan peptida natriuretik tipe B manusia.
Mekanisme kerjanya terutama sebagai vasodilator sistemik dan pulmonal yang kuat.
Obat ini dengan cepat dan konsisten menurunkan tekanan pengisian jantung dan
mengurangi tekanan kapiler pulmonal. Disamping itu obat ini mempunyai efek
natriuresis dan diuresis, serta menghambat norepinefrin, endotelin-1, dan aldosteron.
Sebuah meta-analisis dari 5 penelitian acak terkontrol berskala besar menunjukkan
penggunaan nesiritide pada dekompensasi akut gagal jantung secara signifikan