HASIL DAN PEMBAHASAN Penapisan Sampel
Tanaman daun dewa yang digunakan pada penelitian ini berasal dari Balitro dan PSB. Hasil Identifikasi yang dilakukan oleh Pusat Penelitian Biologi Lembaga Ilmu Pengetahuan Indonesia di Bogor, menunjukkan tanaman daun dewa yang digunakan pada penelitian ini termasuk ke dalam suku Asteraceae, dengan spesies Gynura pseudochina (L.) DC.
Tanaman yang digunakan dalam penelitian ini adalah tanaman daun dewa yang telah cukup umur, yaitu 6-8 bulan, sehingga diharapkan zat-zat yang terkandung dalam umbi dan daun telah terbentuk sempurna. Daun yang digunakan adalah daun yang berwarna hijau tua dan ukuran daun cukup besar serta berkualitas baik. Kualitas daun yang baik adalah bentuk daun utuh, tidak rusak dimakan hama dan tidak terserang penyakit, yaitu yang tidak terkena infeksi virus, bakteri atau jamur. Umbi yang digunakan pada penelitian ini adalah umbi yang telah berusia 8 bulan. Untuk menghindari pencemaran yang diakibatkan oleh zat pengotor seperti debu dan tanah, maka daun dan umbi sebelum dianalisa ataupun dikeringkan, terlebih dahulu dicuci. Pencucian daun dan umbi dilakukan dalam waktu singkat dan tidak diulang untuk mencegah berkurangnya rendemen pigmen antosianin terlalu banyak karena sebagian kecil antosianin akan larut bersama air pencuci.
Daun dewa yang telah dicuci siap digunakan untuk keperluan berbagai analisis. Untuk mencegah terjadinya perubahan kimia, daun yang sudah dicuci langsung dikeringkan dalam oven bersuhu rendah (40-60 oC) dan memiliki aliran udara yang baik. Sedangkan umbinya selesai dicuci, diris tipis-tipis terlebih dahulu baru dikeringkan dalam oven. Pengeringan yang dilakukan selama 48 jam terus menerus pada suhu 40-60 oC menghasilkan daun yang tetap berwarna hijau dengan rendemen kurang lebih 12% untuk sampel daun dewa dari Balitro, 5% untuk sampel dari Pusat Studi Biofarmaka (PSB). Untuk umbi tanaman tersebut diperoleh umbi kering yang berwarna tetap putih dengan rendemen kurang lebih 29% untuk sampel umbi dewa dari Balitro dan PSB.
Penapisan fitokimia umum dan golongan flavonoid dilakukan terhadap sampel daun dan umbi tanaman daun dewa, baik yang masih segar maupun yang telah dikeringkan menjadi serbuk, untuk menelusuri golongan senyawa metabolit sekunder yang dikandungnya. Hasil uji fitokimia dapat dilihat pada Tabel 1.
Tabel 1 Hasil Uji Fitokimia Umum dan Golongan Flavonoid Sampel
Asal dan Jenis Sampel
Balitro PSB Keberadaan Golongan Senyawa
DDS SDD UDS SUD DDS SDD UDS SUD
Meyer - + - + - + - + Wagner - ++ + ++ + - ++ - ++ Alkaloid Dragendorf - ++ + +++ - ++ + ++ Flavonoid H2SO4/p + + + + + + + + CH3COONa + FeCl3 - + - - - - - - Sianidin Na2CO3 - - - CH3COONa + FeCl3 - - - - - - - - Malvidin Na2CO3 - - - Pelargonidin Na2CO3 - - - Mg + HCl/p - - + + - - - - (CH3COO)2Pb + + - - - - NaOH - - - + + + Flavon H2SO4/p + + - - + + + + Mg + HCl/p - + - - - + + - (CH3COO)2Pb - - - - - - - - NaOH - - - + - - Flavonol H2SO4/p + + - - - + + - Mg + HCl/p - - - - (CH3COO)2Pb - - - + - - - - NaOH + + + + - - - - Kalkon H2SO4/p - - + + - - - - Mg + HCl/p - - - - (CH3COO)2Pb - - + - - - - - NaOH + + + + - - - - F l a v o n o i d Auron H2SO4/p - - - Fenolhidrokuinon - + - - - + Triterpenoid - - + + - - + + Steroid + +++ - + + + - + Tanin + + - + + + + + Saponin + + ++ + + + + +
Keterangan : DDS = Daun Dewa Segar SDD = Serbuk Daun Dewa UDS = Umbi Dewa Segar SUD = Serbuk Umbi Dewa
- = hasil uji negatif
Data pada Tabel 1 menunjukkan bahwa beberapa golongan senyawa metabolit sekunder yang ada dalam tanaman daun dewa tidak teridentifikasi pada keadaan segar, tetapi hampir semuanya dapat teridentifikasi pada keadaan kering/serbuk. Hal ini juga menunjukkan bahwa proses pengeringan oven dengan suhu 40-60 oC tidak merusak kandungan metabolit sekunder tanaman. Senyawa flavonoid yang terdapat dalam daun dan umbi tanaman daun dewa termasuk golongan senyawa flavon, flavonol, kalkon dan auron. Sedangkan untuk senyawa flavonoid yang termasuk kelas antosianin yaitu sianidin, malvidin dan pelargonidin tidak teridentifikasi pada daun dan umbi baik dalam keadaan segar maupun serbuknya, kecuali sianidin teridentifikasi hanya pada serbuk daun dewa untuk sampel yang berasal dari Balitro. Dari hasil pengeringan sampel tanaman daun dewa segar, sampel yang berasal dari Balitro menghasilkan rendemen yang lebih tinggi, selain itu hasil uji fitokimia juga menunjukkan sampel dari Balitro memiliki kandungan jenis metabolit sekunder yang lebih banyak, sehingga dalam penelitian ini digunakan sampel yang berasal dari Balitro.
Ekstraksi Senyawa Flavonoid
Proses ekstraksi senyawa flavonoid dilakukan menggunakan pelarut metanol. Hasil penapisan fitokimia daun dewa segar menunjukkan hasil negatif untuk kelas senyawa antosianin, namun isolasi senyawa antosianin dari daun dewa tetap dilakukan, karena hasil penapisan terhadap serbuk daunnya ada yang menunjukkan hasil positif (Tabel 1) dan dari penampakan daun yang permukaan bagian belakangnya berwarna ungu, sehingga diduga kemungkinan ada senyawa antosianin di dalam daun dewa.
Proses ekstraksi untuk mendapatkan kelompok senyawa antosianin dilakukan dengan mengekstraksi daun dewa segar dengan pelarut metanol yang mengandung asam klorida. Menurut Markham (1988), untuk antosianin daun segar atau daun bunga jangan dikeringkan, tetapi harus digerus dengan MeOH yang mengandung 1% HCl pekat. Sedangkan untuk mendapatkan senyawa flavonoid lain yang bukan kelompok antosianin dilakukan isolasi dengan mengekstrak serbuk daun dan umbi sampel tanaman daun dewa.
Ekstraksi Antosianin dari Daun Dewa
Isolasi dilakukan terhadap sampel tanaman daun dewa yang berasal dari Balitro. Jumlah total rendemen yang diperoleh dari hasil ekstraksi adalah 4,6692 % dengan nilai total fenol adalah 0,6587 mg/g.
Pengamatan secara visual terhadap filtrat hasil ekstraksi daun dewa segar menunjukkan warna kuning kemerahan. Pemeriksaan secara kualitatif sederhana menggunakan larutan HCl 2M dan NaOH 2M, menunjukkan bahwa pemanasan filtrat hasil ekstraksi daun dewa segar dalam larutan HCl 2M selama 5 menit (100 oC) menghasilkan warna yang tetap tidak berubah yaitu warna kuning kemerahan. Penambahan larutan NaOH 2 M ke dalam filtrat hasil ekstraksi merubah warna menjadi lebih pekat. Jika filtrat mengandung antosianin, filtrat akan berubah warna menjadi hijau biru dan memudar perlahan-lahan. Ekstraksi filtrat dengan amilalkohol, memberikan warna jingga dengan penambahan CH3COONa dan FeCl3, dan bening dengan penambahan Na2CO3. Hal ini tidak sesuai dengan ciri-ciri warna jika ekstrak mengandung antosianin.
Penapisan fitokimia flavonoid yang dilakukan untuk mengetahui keberadaan senyawa flavonoid dalam ekstrak kasar antosianin (EAD) memberikan hasil (Tabel 2) golongan antosianin dalam ekstrak EAD sampel tidak terdeteksi, tetapi senyawa flavonoid golongan lainnya, yaitu flavon, dan flavonol serta kalkon dan auron menunjukkan hasil uji positif.
Tabel 2 Hasil Uji Fitokimia Flavonoid Ekstrak Hasil Isolasi Antosianin No. Golongan Flavonoid Keberadaan Senyawa
1 Sianidin - 2 Malvidin - 3 Pelargonidin - 4 Flavon + 5 Flavonol + 6 Kalkon + 7 Auron +
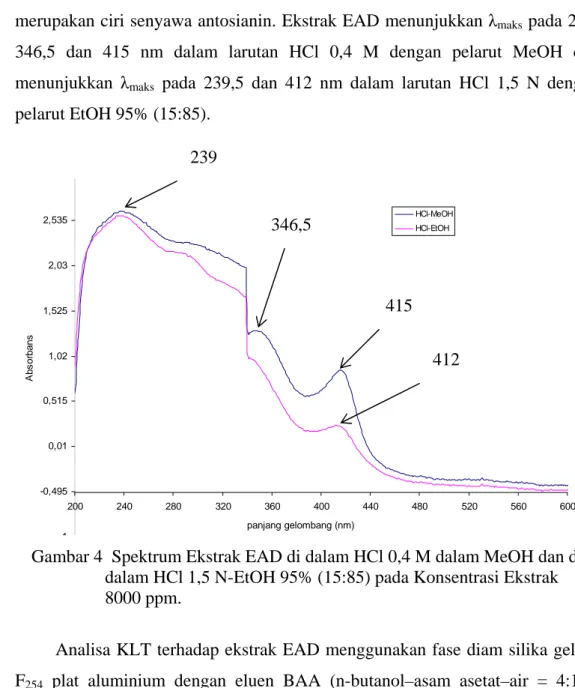
Spektrum tampak ekstrak EAD di dalam larutan HCl 0,4 M dalam metanol dan di dalam larutan HCl 1,5N-EtOH 95% (15:85) memberikan spektrum seperti terlihat pada gambar 4. Spektrum ekstrak EAD tidak menunjukkan panjang gelombang maksimum (λmaks) pada kisaran 505-535 nm yang
merupakan ciri senyawa antosianin. Ekstrak EAD menunjukkan λmaks pada 239, 346,5 dan 415 nm dalam larutan HCl 0,4 M dengan pelarut MeOH dan menunjukkan λmaks pada 239,5 dan 412 nm dalam larutan HCl 1,5 N dengan pelarut EtOH 95% (15:85). 1 -0,495 0,01 0,515 1,02 1,525 2,03 2,535 200 240 280 320 360 400 440 480 520 560 600 panjang gelombang (nm) A b s or b ans HCl-MeOH HCl-EtOH
Gambar 4 Spektrum Ekstrak EAD di dalam HCl 0,4 M dalam MeOH dan di dalam HCl 1,5 N-EtOH 95% (15:85) pada Konsentrasi Ekstrak 8000 ppm.
Analisa KLT terhadap ekstrak EAD menggunakan fase diam silika gel 60 F254 plat aluminium dengan eluen BAA (n-butanol–asam asetat–air = 4:1:5) penampak bercak uap amonia (Harborne 1988) menghasilkan kromatogram dengan perhitungan nilai Rf seperti pada Tabel 3. Hasil analisa menunjukkan bahwa ekstrak EAD menghasilkan spot lebih dari satu. Hal ini berarti terdapat keragaman senyawa metabolit yang terkandung di dalam ekstrak tersebut. Di samping itu, adanya spot yang berwarna kuning, jika diuapi dengan amoniak dapat menunjukkan adanya senyawa flavon atau flavonol di dalam ekstrak.
239
346,5
412 415
Tabel 3 Hasil KLT Analitik Ekstrak EAD dengan Eluen BAA Warna
Kromatogram Jumlah Spot
UV-365 NH3 Rf 6 violet violet violet violet violet violet coklat coklat kuning (samar) - kuning kuning (samar) 0,10 0,29 0,40 0,53 0,62 0,74
Hasil uji toksisitas ekstrak terhadap larva A. salina Leach menunjukkan ekstrak memiliki potensi bioaktivitas (Tabel 4). Karena berdasarkan hasil uji tersebut diperoleh nilai LC50 <1000 ppm.
Tabel 4 Data Uji Toksisitas Ekstrak EAD dengan Larva A. salina Leach. Jumlah larva yang mati
Jenis Konsentrasi (ppm) 1 2 3 4 Rata-rata LC50 (ppm) Kontrol 0 0 0 0 0 0 - 10 2 5 1 2 2,5 100 12 12 10 12 11,5 Ekstrak EAD 1000 15 15 15 15 15
61,35737
Dilihat dari nilai LC50 yang lebih kecil dari 1000 ppm menunjukkan ekstrak memiliki potensi bioaktivitas. Namun dari hasil uji antikhamir ekstrak terhadap khamir S. cerevisiae ternyata ekstrak EAD dengan konsentrasi 1000 ppm tidak menunjukkan aktivitas antikhamir, karena dari hasil uji tidak terbentuk zona bening pada media uji, berarti ekstrak tidak menghambat pertumbuhan khamir S.
cerevisiae. Hasil uji ditunjukkan pada gambar 5.
Berdasarkan hasil uji fitokimia pada Tabel 2 dan hasil pembacaan spektrum ekstrak yang tidak menunjukkan terdeteksinya senyawa antosianin, maka tahapan lanjutan untuk isolasi antosianin tidak diteruskan.
Ekstraksi Flavonoid
Serbuk daun dan umbi yang digunakan sebagai sampel pada penelitian ini adalah hasil pengeringan daun dan umbi tanaman daun dewa yang berasal dari Balitro. Kadar air serbuk daun 10,25% dan umbi 12,35%. Sampel serbuk daun dan umbi masing-masing direndam dalam pelarut metanol-air (9:1) selama 12 jam dan dilakukan penyaringan. Selanjutnya ampas dimaserasi kembali dengan pelarut metanol-air (1:1) selama 12 jam dan dilakukan penyaringan. Ekstrak yang diperoleh dikumpulkan dan dirotavapor, lalu dipartisi berturut-turut dengan n-heksan, kloroform, dietil eter, etil asetat dan n-butanol. Hasil uji flavonoid, perhitungan total rendemen dan nilai total fenol serta nilai LC50 yang diperoleh dari hasil uji bioassay menggunakan larva A. salina terhadap hasil ekstraksi dan partisi dapat dilihat pada Tabel 5.
Data Tabel 5 menunjukkan fraksi yang memiliki nilai total fenol tertinggi dari keseluruhan ekstrak uji adalah fraksi metanol, tetapi nilai LC50 jauh di atas 1000 ppm. Fraksi yang memiliki nilai LC50 lebih kecil dari 1000 ppm untuk ekstrak ESD adalah fraksi D-FK dan D-FB. Dari hasil uji kualitatif D-FK tidak mengandung senyawa golongan flavonoid, sehingga untuk ekstrak ini, fraksi yang mungkin diteruskan untuk pemurnian lebih lanjut adalah fraksi D-FB. Sedangkan untuk ekstrak ESU, fraksi yang memiliki nilai LC50 lebih kecil dari 1000 ppm adalah fraksi U-FE dan positif mengandung senyawa flavonoid, sehingga untuk ekstrak ini, fraksi yang mungkin diteruskan untuk pemurnian lebih lanjut adalah fraksi U-FE.
Tabel 5 Keberadaan Golongan Flavonoid dalam Fraksi Hasil Partisi Ekstrak Sampel, Jumlah Rendemen, Nilai Total Fenol dan Nilai LC50
Ekstrak Sampel Fraksi Uji Flavonoid Total Rendemen (%) Total Fenol (mg/g) LC50 (ppm) ESD kasar + 22,0456 0,02467 D-FH - 1,2995 D-FK - 0,4664 0,0077 972,69909 D-FD + 0,0520 0,0059 1586,61372 D-FE + 0,0964 0,0028 2209,79950 D-FB + 0,7947 0,0101 832,12297 D-FA + 5,0472 0,0109 1082,68283 ESD D-FM + 0,6727 0,0682 3041,63585 ESU kasar + 8,6645 0,0589 U-FH - 0,1982 0,0293 - U-FK + 0,1044 0,0142 - U-FD - 0,0492 0,0036 1306,5619 U-FE + 0,0742 0,0282 723,44205 U-FB + 0.1341 0,0166 - U-FA + 0,8542 0,0246 - ESU U-FM + 0,9031 0,3863 -
Keterangan: ESD = ekstrak serbuk daun ESU = ekstrak serbuk umbi D-FH = fraksi n-heksan U-FH = fraksi n-heksan D-FK = fraksi kloroform U-FK = fraksi kloroform D-FD = fraksi dietil eter U-FD = fraksi dietil eter D-FE = fraksi etil asetat U-FE = fraksi etil asetat D-FB = fraksi n-butanol U-FB = fraksi n-butanol D-FA = fraksi air U-FA = fraksi air D-FM = fraksi metanol U-FM = fraksi metanol
Penapisan Fraksi Terpilih
Analisa KLT menggunakan fase diam silika gel 60 F254 plat aluminium dengan eluen BAA (4:1:5), penampak bercak uap amonia (Harborne 1988) terhadap Fraksi D-FB dan U-FE merupakan fraksi terpilih yang menunjukkan fraksi D-FB menghasilkan spot yang lebih banyak dibandingkan fraksi U-FE. Kromatogram hasil analisa dan perhitungan nilai Rf fraksi ini ditunjukkan pada Tabel 6.
Tabel 6 Hasil KLT Analitik Ekstrak D-FB dan U-FE dengan Eluen BAA Warna Kromatogram Fraksi UV-254 UV-365 NH3 Rf D-FB (7 spot) coklat (samar) coklat (samar) coklat (samar) coklat gelap coklat (samar) coklat (samar) coklat gelap berpendar putih tidak tampak berpendar putih coklat gelap berpendar ungu tidak tampak berpendar merah kuning (samar) kuning kuning (samar) hijau 0,28 0,36 0,46 0,53 0,67 0,81 0,95 U-FE (3 spot) kuning coklat (samar) coklat gelap violet violet gelap violet gelap Kuning Hijau hijau 0,59 0,75 0,89
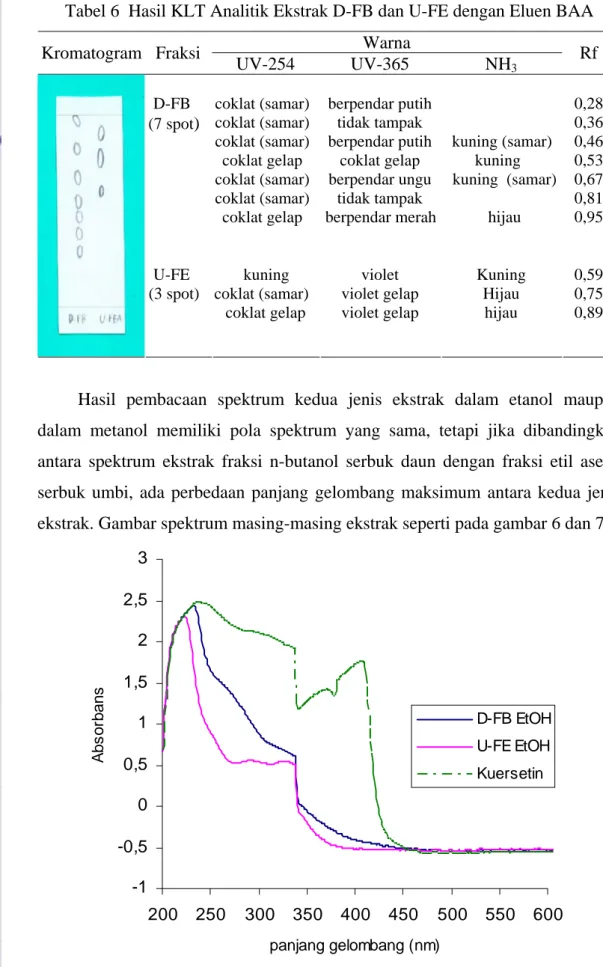
Hasil pembacaan spektrum kedua jenis ekstrak dalam etanol maupun dalam metanol memiliki pola spektrum yang sama, tetapi jika dibandingkan antara spektrum ekstrak fraksi n-butanol serbuk daun dengan fraksi etil asetat serbuk umbi, ada perbedaan panjang gelombang maksimum antara kedua jenis ekstrak. Gambar spektrum masing-masing ekstrak seperti pada gambar 6 dan 7.
-1 -0,5 0 0,5 1 1,5 2 2,5 3 200 250 300 350 400 450 500 550 600 panjang gelombang (nm) Ab s o rb a n s D-FB EtOH U-FE EtOH Kuersetin
0 0,5 1 1,5 2 2,5 3 3,5 4 200 250 300 350 400 450 500 550 600 650 700 panjang gelombang (nm) Ab s F4-DB F7-DB Kuersetin
Gambar 7 Spektrum Ekstrak D-FB, U-FE dan Kuersetin dalam metanol. Berdasarkan spektrum UV, fraksi D-FB menunjukkan panjang gelombang maksimum pada 234 (dalam metanol) dan 232,5 nm (dalam etanol). Fraksi U-FE menunjukkan panjang gelombang maksimum 240,5 (dalam metanol) dan 223 nm (dalam etanol).
Dari hasil analisa KLT, fraksi D-FB menunjukkan kandungan senyawa metabolit yang lebih beragam dibanding fraksi U-FE. Jika ditinjau dari hubungan jumlah total rendemen dengan nilai total fenol (Tabel 5), fraksi U-FE memiliki nilai total fenol yang lebih tinggi, sehingga kemungkinan kandungan flavonoid-nya lebih tinggi. Nilai LC50 fraksi U-FE lebih tinggi daripada fraksi D-FB, namun hasil uji antikhamir kedua fraksi tersebut memberikan hasil negatif, tidak terbentuk zona bening di sekitar kertas cakram. Hal ini berarti kedua fraksi tidak bersifat menghambat pertumbuhan khamir S. cerevisiae (Gambar 8).
Gambar 8 Hasil Uji Antikhamir Fraksi D-FB dan U-FE terhadap khamir S. cerevisiae.
Hasil analisa KCKT terhadap fraksi D-FB dan fraksi U-FE dengan pembanding standar kuersetin menunjukkan hasil (Gambar 9) bahwa, di dalam fraksi D-FB terdapat senyawa flavonid kuersetin. Hal ini diyakini berdasarkan adanya puncak yang muncul pada rentang waktu retensi 8-9 menit, meskipun tinggi puncak lebih rendah dari tinggi rerata noise. Oleh karena rendahnya rendemen dari fraksi U-FE, maka yang ditelusuri lebih lanjut adalah fraksi D-FB.
Minutes 0 5 10 15 20 25 30 Vo lt s 0.0 2.5 5.0 Vo lt s 0.0 2.5 5.0 0. 920 1. 337 1.5601. 833 1.890 2.193 2.3102.380 2.557 3.450 4.113 4.287 4.543 4.807 8.460 UV-VIS Retention Time ( a) (b) (c)
Gambar 9 Kromatogram KCKT, (a) standar kuersetin [5 ppm] (b) Fraksi D-FB [0,25 ppm] (c) Fraksi U-FE [1,25 ppm].
Ditinjau dari perolehan total rendemen yang lebih tinggi, dan analisa KCKT menggunakan larutan standar kuersetin sebagai pembanding, mem-perlihatkan fraksi D-FB menunjukkan adanya puncak pada rentang waktu retensi 8,0 – 9,0 seperti halnya yang ditunjukkan pada analisa KCKT standar kuersetin. Untuk itu, yang ditelusuri lebih lanjut adalah fraksi D-FB.
Karakterisasi Komponen
Pemisahan fraksi D-FB dilakukan dengan KLT preparatif menggunakan fase diam silika gel 60 F254 (ukuran 5x10 cm) eluen pengembang n-butanol-asam asetat- air (4:1:5), dan diperoleh 7 pita. Masing-masing pita yang dihasilkan dilarutkan kembali dalam pelarut n-Butanol untuk selanjutnya dikeringkan menggunakan rotavapor. Persentase rendemen fraksi (pita 1 sampai 7) yang didapat berturut-turut 0,0584; 9,8920; 16,3700; 23,3754; 20,7762; 0,8170 dan 24,5112%.
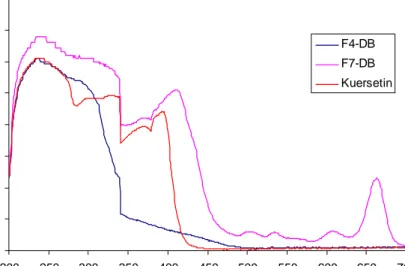
Dari tujuh pita yang dihasilkan diambil 2 pita dengan rendemen tertinggi, yaitu fraksi pita ketujuh (F7-DB) yang dibawah sinar UV 365 nm berpendar merah dan fraksi pita keempat (F4-DB) yang berwarna coklat gelap di bawah sinar UV 365 nm dan berwarna kuning dengan uap amoniak.
Karakterisasi dengan Spektrometer UV-Vis
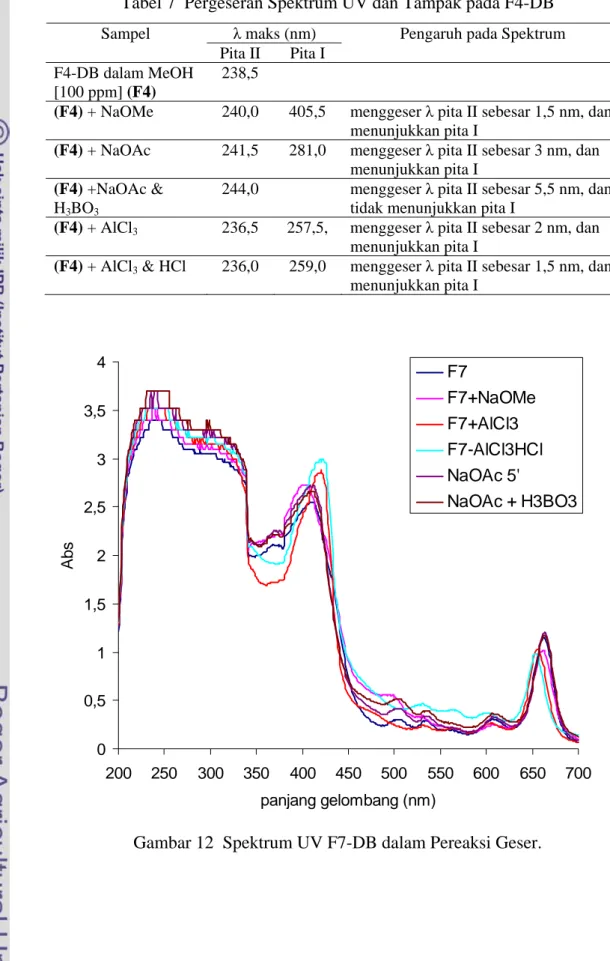
Karakterisasi F4-DB dan F7-DB secara spektrometri UV-Vis dilakukan dalam metanol dan metanol dengan penambahan pereaksi geser yaitu NaOMe, AlCl3, AlCl3 + HCl, NaOAc dan NaOAc + H3BO3. Spektum UV F4-DB, F7-DB dan kuersetin dalam metanol menunjukkan spektrum seperti pada gambar . Hasil karakterisasi F4-DB, F7-DB dan kuersetin dalam metanol dengan penambahan pereaksi geser menghasilkan spektrum seperti pada Gambar 10, 11, 12 dan 13 serta Tabel 7, 8 dan 9.
0 0,5 1 1,5 2 2,5 3 3,5 4 200 250 300 350 400 450 500 550 600 650 700 panjang gelombang (nm) Ab s F4-DB F7-DB Kuersetin
Gambar 10 Spektrum UV F4-DB, F7-DB dan Kuersetin dalam MeOH.
0 0,5 1 1,5 2 2,5 3 3,5 200 250 300 350 400 450 500 550 600 650 700 panjang gelombang (nm) Ab s F4 F4-NaOMe 5' F4-NaOAc 5' F4+NaOAc+H3BO3 F4+AlCl3 F4+AlCl3/HCl
Gambar 11 Spektrum UV F4-DB dalam Pereaksi Geser.
246,5 244,5 238,5 411,5 395 371
Tabel 7 Pergeseran Spektrum UV dan Tampak pada F4-DB
λ maks (nm) Sampel
Pita II Pita I
Pengaruh pada Spektrum
F4-DB dalam MeOH [100 ppm] (F4)
238,5
(F4) + NaOMe 240,0 405,5 menggeser λ pita II sebesar 1,5 nm, dan menunjukkan pita I
(F4) + NaOAc 241,5 281,0 menggeser λ pita II sebesar 3 nm, dan menunjukkan pita I
(F4) +NaOAc &
H3BO3
244,0 menggeser λ pita II sebesar 5,5 nm, dan tidak menunjukkan pita I
(F4) + AlCl3 236,5 257,5, menggeser λ pita II sebesar 2 nm, dan
menunjukkan pita I
(F4) + AlCl3 & HCl 236,0 259,0 menggeser λ pita II sebesar 1,5 nm, dan
menunjukkan pita I 0 0,5 1 1,5 2 2,5 3 3,5 4 200 250 300 350 400 450 500 550 600 650 700 panjang gelombang (nm) Ab s F7 F7+NaOMe F7+AlCl3 F7-AlCl3HCl NaOAc 5' NaOAc + H3BO3
Tabel 8 Pergeseran Spektrum UV dan Spektrum Tampak pada F7-DB
λ maksimum (nm) Sampel
Pita II Pita I
Pengaruh pada Spektrum
Fraksi 7 dalam MeOH [110 ppm] (F7)
246,5 411,5
(F7) + NaOMe 242 405,5 menggeser λ pita I sebesar 6 nm, pita II sebesar 4,5 nm
(F7) + NaOAc 242,5 412 menggeser λ pita I sebesar 0,5 nm, pita II sebesar 4 nm
(F7) +NaOAc &
H3BO3
254,5 412 menggeser λ pita I sebesar 0,5 nm, pita II sebesar 8 nm
(F7) + AlCl3 250,5 420,5 menggeser λ pita I sebesar 9 nm, pita II
sebesar 4 nm
(F7) + AlCl3 & HCl 253 423 menggeser λ pita I sebesar 11,5 nm,
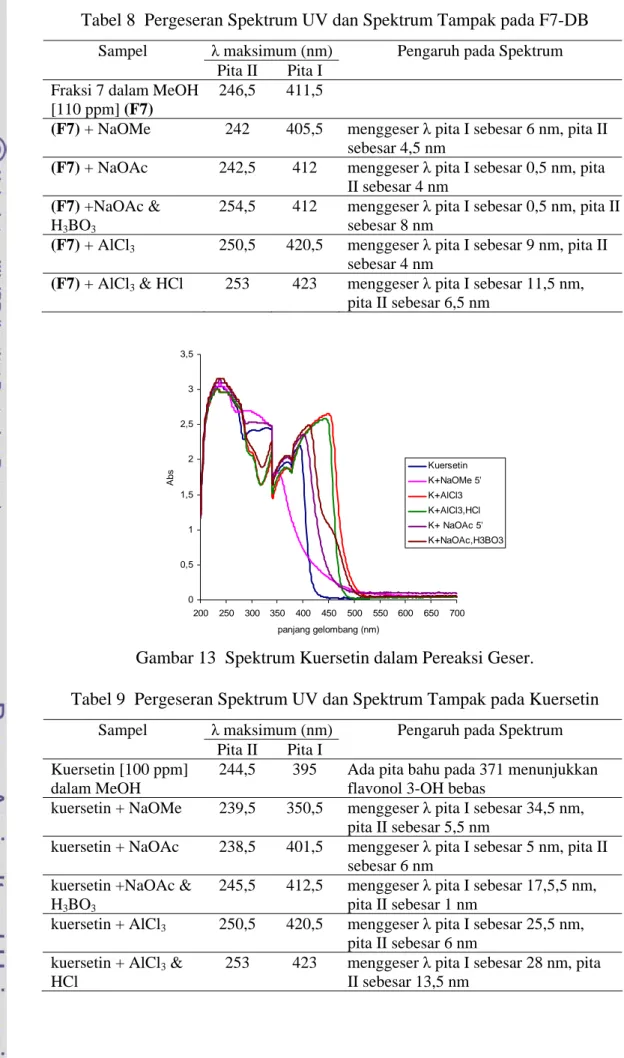
pita II sebesar 6,5 nm 0 0,5 1 1,5 2 2,5 3 3,5 200 250 300 350 400 450 500 550 600 650 700 panjang gelombang (nm) Ab s Kuersetin K+NaOMe 5' K+AlCl3 K+AlCl3,HCl K+ NaOAc 5' K+NaOAc,H3BO3
Gambar 13 Spektrum Kuersetin dalam Pereaksi Geser.
Tabel 9 Pergeseran Spektrum UV dan Spektrum Tampak pada Kuersetin
λ maksimum (nm) Sampel
Pita II Pita I
Pengaruh pada Spektrum
Kuersetin [100 ppm] dalam MeOH
244,5 395 Ada pita bahu pada 371 menunjukkan flavonol 3-OH bebas
kuersetin + NaOMe 239,5 350,5 menggeser λ pita I sebesar 34,5 nm, pita II sebesar 5,5 nm
kuersetin + NaOAc 238,5 401,5 menggeser λ pita I sebesar 5 nm, pita II sebesar 6 nm
kuersetin +NaOAc & H3BO3
245,5 412,5 menggeser λ pita I sebesar 17,5,5 nm, pita II sebesar 1 nm
kuersetin + AlCl3 250,5 420,5 menggeser λ pita I sebesar 25,5 nm,
pita II sebesar 6 nm kuersetin + AlCl3 &
HCl
253 423 menggeser λ pita I sebesar 28 nm, pita II sebesar 13,5 nm
Hasil karakterisasi dengan spektrometer UV-Vis dalam metanol dan dalam metanol dengan penambahan pereaksi geser yaitu NaOMe, AlCl3, AlCl3 + HCl, NaOAc dan NaOAc + H3BO3 menunjukkan tidak ada pergeseran λ yang berarti pada λ maksimum untuk F4-DB dan F7-DB jika dibandingkan dengan kuersetin. Hal ini menunjukkan bahwa ikatan rangkap (=) dalam F4-DB dan F7-DB tidak dalam keadaan terkonjugasi. F4-DB dan F7-DB memiliki satu puncak serapan maksimum di daerah UV, yaitu 238,5 nm untuk F4 dan 246,5 nm untuk F7 (satu puncak serapan pada daerah tampak, yaitu 411,5 nm). Serapan-serapan senyawa flavonoid berhubungan dengan resonansi gugus sinamoil yang melibatkan cincin B (serapan sekitar 300-550 nm, pita I) dan gugus benzoil yang melibatkan cincin A (serapan sekitar 230-295 nm, pita II). F4-DB dan F7-DB memiliki satu puncak serapan di daerah UV (pita II) yang menunjukkan rentang serapan gugus benzoil. Sehingga diduga F4-DB dan F7-DB mengandung senyawa golongan flavonoid.
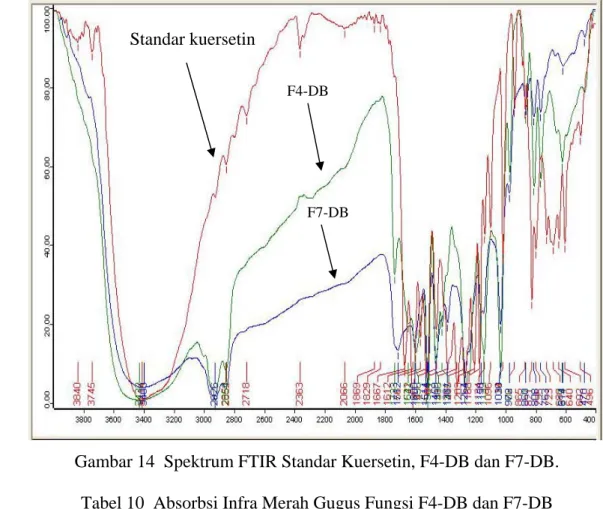
Karakterisasi dengan spektometer FTIR
Karakterisasi F4-DB, F7-DB dan kuersetin dengan FTIR menunjukkan spektrum dengan puncak serapan pada rentangan yang sama (seperti dalam gambar 14 dan Tabel 10), diduga F4-DB dan F7-DB mempunyai gugus fungsi O--H yang dapat berikatan hidrogen antar molekul, karena adanya serapan lebar pada 3200 - 3600 cm-1 tetapi tidak adanya pergeseran serapan ke daerah 3000 cm-1 menunjukkan senyawa tidak mempunyai gugus karboksilat, karena tidak ada korelasi gugus C=O dengan gugus O-H. Adanya serapan pada daerah 1690-1760 cm-1 menunjukkan senyawa mempunyai gugus C=O. Serapan di daerah 1100-1300 cm-1 menunjukkan adanya uluran C-C-C dan tekukan C
C C O
yang berarti senyawa mengandung gugus C=O keton. Adanya serapan di daerah 1200-1275 cm-1 menunjukkan adanya uluran C-O-C tak simetrik dari aril alkil eter. Serapan di daerah 1500-1600 cm-1 menunjukkan adanya regang C=C aromatik.
Gambar 14 Spektrum FTIR Standar Kuersetin, F4-DB dan F7-DB. Tabel 10 Absorbsi Infra Merah Gugus Fungsi F4-DB dan F7-DB Bilangan gelombang Kuersetin Bilangan gelombang F4-DB Bilangan gelombang F7-DB Bilangan gelombang Tabel Korelasi (*) (cm-1) Perkiraan Gugus Fungsi 3409 3433 3428 3200-3600 regang O-H, berikatan hidrogen 2854 2926 ; 2854 2926 ; 2855 2850-2970 regang C-H 1668 1734 1712 1690-1760 regang C=O 1523 1594; 1514 1601 ;1514 1500-1600 regang C=C aromatik 1351 1461 ; 1417 ; 1387 1461 ; 1420 ; 1382 1340-1470 lentur C-H 1168 ; 1096 1265 1264 1050-1300 C-O
Keterangan: (*) Bilangan gelombang rujukan dari tabel korelasi Skoog (1992)
Dari Gambar 14 dan data Tabel 10 menunjukkan F4-DB dan F7-DB memiliki gugus fungsi yang juga dimiliki oleh standar kuersetin. Dengan demikian F4-DB dan F7-DB memiliki gugus fungsi yang dimiliki oleh senyawa flavonoid.
F4-DB
F7-DB
Karakterisasi dengan KLT Analitik 2 Arah
Analisa secara KLT analitik 2 arah dengan pengembang butanol-asam asetat-air (BAA) (4:1:5) dan asam asetat (HOAc) 5% terhadap kedua fraksi tersebut memberikan hasil seperti pada gambar 15.
Gambar 15 Kromatogram KLT 2 Arah F4-DB dan F7-DB.
Hasil KLT F4-DB dengan eluen BAA menghasilkan spot tunggal, tetapi elusi dengan HOAc 5% menghasilkan pemisahan spot, berarti menunjukkan F4-DB belum merupakan senyawa tunggal. F7-F4-DB dengan eluen BAA menghasilkan spot tunggal. Spot yang didapat tidak bergeser ketika dielusi kembali dengan eluen HOAc 5%, berarti komponen memiliki kepolaran yang berbeda dengan HOAc 5%, sehingga komponen tersebut tidak terelusi.
Karakterisasi dengan KCKT
Karakterisasi KCKT F4-DB dan F7-DB dilakukan dengan kondisi kolom chrospher(R)100 RP-18, laju alir 0,8 mL/menit, detektor UV 370 nm, isokratik dengan eluen MeOH-buffer KH2PO4 0,025 M pH 2,4. Hasil analisa menunjukkan MeOH dan bufer KH2PO4 sebagai eluen hanya tampak sebagai
noise. Analisa terhadap standar kuersetin, F7-DB dan F4-DB menunjukkan
kromatogram seperti pada gambar 15 (Kromatogram standar kuersetin pada Lampiran 11). Data konsentrasi dan luas puncak kromatogram ditampilkan pada Tabel 11 . B A A HOAc 5% F4-DB F7-DB
Minutes 0 5 10 15 20 25 30 Vol ts 0 5 10 Vol ts 0 5 10 0.827 1.340 1.557 1.810 2.3972.457 2.803 3.3 3 3 3.950 4.400 5.0 2 3 6.280 6.743 8.9 8 3 14.603 UV-VIS Retention Time Minutes 0 5 10 15 20 25 30 Vo lts 0.0 0.2 0.4 Vo lts 0.0 0.2 0.4 0.0 5 7 0.12 3 0.327 0.6 6 3 0 .817 0.883 1.3 6 3 1 .750 1.937 2.253 2.55 0 2.627 2.7632.840 3.3 0 0 3.653 3.833 4.130 4.91 3 5.4 7 3 5.7506.10 7 6.227 6.393 6.587 6.713 6.83 7 6.953 7.0 5 0 7.1 0 7 7.42 3 7.4 6 3 7.593 7.7 1 3 7.850 8.06 0 8.163 8.233 8.387 8.5308.643 8.737 8.8838.95 3 9.300 9.4779.5 3 0 9.783 9.8939.963 10.067 10.440 10.61 7 10 .910 1 1 .060 11.207 11 .383 11.617 11.84711 .893 1 2 .063 12 .230 12.3 9 7 12.5 6 3 12.820 12 .933 13.1 0 3 13.2 0 7 13.40 7 13.557 13 .7 23 13.973 14.203 14.340 14 .4 63 14.807 14.93 0 15.057 15 .273 15 .400 15.55 7 15.650 15.900 16.070 16.18016.31 3 16.423 16 .680 16.90716.973 17.19 3 17 .303 17.5 2 7 17.6 0 7 17.90 3 18.060 18.213 18 .357 18.64 7 18.780 18.92 3 1 9 .123 1 9 .217 19.357 19 .7 83 19.97 3 20 .173 20.3 3 7 2 0 .513 20.7 1 0 20.827 21.1 9 7 21.4 0 0 21 .497 21.543 21 .657 21 .893 2 2 .213 22 .290 2 2 .373 22.57 0 22.727 22.8 2 0 22 .947 23.103 23 .243 23 .310 23.560 23.653 23.927 24 .040 24 .183 24.3 4 3 2 4 .493 2 4 .803 24.987 25 .227 25.2 7 0 25.4 3 0 25.590 25.717 25.8 0 7 25.883 26.12026.2 6 7 26.44 3 26 .623 26 .793 26.8 8 0 27.01027 .060 27.2 6 3 27 .353 2 7 .497 27.603 27.7 3 0 27.84 0 27.947 28 .140 28.21 7 28.420 28.6 2 0 28.7 3 0 28 .853 29.0 5 7 2 9 .147 2 9 .340 29.427 29 .723 29.8 2 0 2 9 .937 UV-VIS Retention Time
Gambar 16 Kromatogram KCKT F4-DB dan F7-DB.
Tabel 11 Konsentrasi Kuersetin dan Luas Puncak Kromatogram Hasil Analisa KCKT
Larutan Konsentrasi Kuersetin (ppm)
Luas Puncak Tinggi Puncak Standar F7-DB F4-DB 0,50 2,50 5,00 7,50 10,00 - 1,9454 29,2913 746624 2337656 4434117 6141223 2350 764692 1844 5829 22787 53514 71918 211 5096
Tinggi puncak rerata noise pada pengukuran KCKT 236,6. Untuk konsentrasi standar terendah 0,5 ppm yang digunakan pada analisa ini tinggi puncak yang muncul adalah 1844, maka dapat digunakan untuk menghitung kadar kuersetin. Menurut Chow et al. (2004) perbandingan sinyal dan noise adalah sebesar 10:1 untuk limit kuantifikasi dan 1:3 untuk limit deteksinya. Menurut Levin (2002) limit kuantifikasi mempunyai tinggi puncak tiga kali tinggi rerata noise. Limit kuantifikasi adalah batas minimum suatu sinyal dapat
Puncak kuersetin
Puncak kuersetin
F4-DB
dikuantifikasi (Linda et al. 1994). Kromatogram standar yang digunakan memenuhi limit kuantifikasi dan limit deteksi. Untuk F7-DB kromatogram KCKT menunjukkan tinggi dibawah rerata noise, maka puncak yang muncul pada waktu retensi pada rentang 8-9 tidak dapat diyakini sebagai puncak senyawa kuersetin.
F4-DB dari pembacaan kromatogram KCKT menunjukkan adanya senyawa kuersetin dengan rentang waktu retensi 8,0-9,0 menit. Hasil penambahan larutan standar kuersetin ke dalam fraksi F4-DB dengan perbandingan volume 1:1 menunjukkan penambahan luas area puncak, sehingga memperkuat dugaan dalam F4-DB terdapat senyawa kuersetin (Gambar 18). Hasil perhitungan berdasarkan kurva standar kuersetin, kadar kuersetin dalam F4-DB adalah 1,9454 ppm atau 2,7458 mg/g. Minutes 0 5 10 15 20 25 30 V o lt s 0 5 10 Vol ts 0 5 10 0 .827 1 .340 1.55 7 1.81 0 2.39 7 2 .457 2.80 3 3 .333 3.9 5 0 4.40 0 5.0 2 3 6 .280 6.74 3 8.98 3 14 .6 03 UV-VIS Retention Time Gambar 17 Kromatogram KCKT F4-DB. Minutes 0 5 10 15 20 25 30 Volt s 0 1 2 3 Volt s 0 1 2 3 1. 3 4 7 1.740 2.27 3 2. 723 3. 3 5 3 3. 743 4. 3 1 7 4.863 6.087 6. 4 8 0 6.550 6.6 4 3 8. 883 UV-VIS Retention Time
Gambar 18 Kromatogram KCKT F4-DB + Standar Kuersetin [7,5ppm], Perbandingan Volume (1:1).
Puncak kuersetin F4-DB
Kromatogram KCKT F4-DB dan F7-DB menghasilkan puncak lebih dari satu pada waktu retensi yang berbeda, dibandingkan dengan kromatogram standar kuersetin yang hanya menghasilkan satu puncak (Gambar 20), hal ini menunjukkan bahwa F4-DB dan F7-DB bukan merupakan senyawa tunggal tetapi terdapat beberapa senyawa.
Minutes 0 5 10 15 20 25 30 Vo lts 0 10 20 Vo lts 0 10 20 0.8 40 1.1 77 1.333 1.55 7 1.81 3 1.89 7 2.19 3 2.26 3 2.49 7 2 .777 2 .927 3.45 3 4.10 3 4.27 7 4.5 20 4.860 5.020 5.45 7 8.367 UV-VIS Retention Time
Gambar 19 Kromatogram KCKT Standar Kuersetin [10 ppm].
Karakterisasi dengan GC-MS
Karakterisasi F4-DB dan F7-DB dengan GC-MS menghasilkan kromatogram dengan beberapa puncak pada waktu retensi yang berbeda, seperti ditampilkan pada Gambar 20 dan 21. Hasil ini menunjukkan bahwa F4-DB dan F7-DB belum merupakan senyawa tunggal. Adanya puncak dengan waktu retensi yang hampir sama antara F4-DB dan F7-DB menunjukkan senyawa yang terdapat dalam F4-DB dan F7-DB ada yang sama atau dalam banyak hal memiliki sifat yang sama.
Gambar 20 Kromatogram GC F4-DB.
Gambar 21 Kromatogram GC F7-DB.
Kromatogram hasil analisa GC terhadap F4-DB dan F7-DB menunjukkan ada beberapa senyawa yang diduga merupakan senyawa yang sama, karena beberapa puncak yang muncul memiliki waktu retensi yang hampir sama seperti tercantum pada Tabel 12.
Tabel 12 Waktu Retensi Puncak Hasil GC dari F4-DB dan F7-DB
Ekstrak Waktu Retensi (menit)
F4-DB 25,55 ; 26,33 ; 30,55 ; 31,68 ; 32,59 ; 33,88 ; 40,79 ; 43,75 ; 49,28 ; 49,78 ; 56,95 F7-DB 25,41 ; 26,32 ; 30,42 ; 30,83 ; 31,59 ; 33,90 ; 49,27 ; 49,77 49.77 33.90 26.32 30.83 49,27 31.60 30,42 25,41 49.28 49,78 40.79 43.75 33.88 26.33 31.68 56.95 32.59 25.55 30.55 F7-DB F4-DB
Puncak dengan waktu retensi hampir sama pada kromatogram GC F4-DB dan F7-DB memiliki pola fragmentasi m/z yang hampir sama (Tabel 13), sehingga diduga merupakan senyawa yang sama.
Tabel 13 Pola Fragmentasi Massa Hasil GC-MS Waktu
Retensi (menit)
Sampel Karakteristik Spektrum Massa Data m/z Dugaan Senyawa Berdasarkan Data Base (Wiley 275.L) 26.33 F4-DB M+ = 219; 190 (100); 175; 159; 144; 128; 115; 104; 97; 91; 77; 69; 63; 51; 41 2-dimetil amino indene 26.32 F7-DB M+ = 190; 175 (100); 159; 144; 128; 120; 115; 103; 91; 77; 69; 63; 51; 45 2-dimetil amino indene 31.68 F4-DB M+ = 219; 208; 192; 177 (100); 162; 146; 131; 119; 105; 91; 77; 69; 63; 55; 43 (E)-4-(3`,4`- dimetoksifenil)But-3-en-1-ol 31.59 F7-DB M+ = 208; 193; 177 (100); 162; 153; 146; 137; 131; 121; 115; 103; 91; 77; 65; 57; 51; 41 (E)-4-(3`,4`- dimetoksifenil)But-3-en-1-ol 33.88 F4-DB M+ = 264; 250; 206; 190; 175; 159 (100); 146; 131; 115; 103; 91; 77; 65; 51; 43 1,2-dihidro-3,5-dimetoksinaftalena 33.90 F7-DB M+ = 250; 190 (100); 175; 146; 131; 115; 103; 91; 77; 65; 51; 43 1,2-dihidro-3,5-dimetoksinaftalena 49.28 F4-DB M+ = 380; 190 (100); 175; 159; 144; 128; 115; 103; 91; 77; 65; 53; 41 (E dan Z)-1-(3,4-dimetoksifenil) butadiena 49.27 F7-DB M+ = 380; 190 (100); 175; 159; 144; 128; 115; 104; 91; 77; 65; 51 (E dan Z)-1-(3,4-dimetoksifenil) butadiena 49.78 F4-DB M+ = 380; 190 (100); 175; 159; 144; 127; 115; 104; 91; 78; 65; 43 2-oksatetrasiklo[6.5.0.0 (3,7).0(5,13)]trideka-9,11-d 49.77 F7-DB M+ = 380; 190 (100); 175; 159; 144; 128; 115; 104; 91; 77; 65; 51; 40 2-oksatetrasiklo[6.5.0.0 (3,7).0(5,13)]trideka-9,11-d
Adanya golongan flavonoid yang merupakan salah satu golongan senyawa fenol dalam F4-DB dan F7-DB diduga dari hasil analisa dengan spektometer UV-Vis menunjukkan serapan dengan λmaks berada pada rentang λmaks untuk senyawa golongan flavonoid (300-350 dan 230-295), hasil analisa dengan
spektrometer FTIR menunjukkan serapan pada rentangan yang sama dengan rentangan serapan senyawa kuersetin yang digunakan sebagai pembanding dan hasil analisa dengan KCKT yang menunjukkan adanya kandungan senyawa kuersetin di dalam F4-DB. Hasil analisa GC-MS, adanya golongan flavonoid diduga dari adanya puncak pada waktu retensi 31,68 menit untuk F4-DB dan 31,59 menit untuk F7-DB. Berdasarkan data base yang ada pada alat GC-MS puncak yang muncul pada waktu retensi 31,68 dan 31,59 menit merupakan fragmen bagian dari F4-DB dan F7-DB adalah (E)-4-(3`,4`-dimetoksifenil)but-3-en-1-ol (Rumus Struktur, Gambar 22) dengan pola fragmentasi mengikuti harga m/z 208, 177 (100), 146 dan 91 (Gambar 23).
O
CH3
O
H3C OH
Gambar 22 Rumus struktur (E)-4-(3`,4`dimetoksifenil)But-3-en-1-ol.
Pengujian Bioaktivitas
Uji bioaktivitas terhadap kematian larva A. salina menunjukkan F4-DB memiliki potensi bioaktif yang lebih tinggi dibanding F7-DB, tetapi keduanya dapat dikatakan memiliki potensi bioaktivitas, karena memiliki nilai LC50 kurang dari 1000 ppm (Tabel 14).
Tabel 14 Data Uji Toksisitas Kuersetin, Ekstrak F4-DB dan F7-DB dengan Larva A. salina Leach.
Jumlah larva yang mati Jenis Konsentrasi (ppm) 1 2 3 4 Rata-rata LC50 (ppm) Kontrol 0 0 0 0 0 0 - 10 9 9 10 10 9,5 100 10 10 10 10 10 500 10 10 10 10 10 Kuersetin dihidrat 1000 10 10 10 10 10 6,48384 10 9 8 9 8 8,5 100 10 10 10 10 10 500 10 10 10 10 10 F4-DB 1000 10 10 10 10 10 7,80408 10 7 8 2 4 6,25 100 5 5 4 10 6,00 500 6 6 6 7 6,25 F7-DB 1000 10 10 10 10 10 208,51563
Gambar 23 Dugaan Pola Fragmentasi Fragmen (E)-4-(3`,4`dimetoksifenil)but-3-en-1-ol. +e -
![Gambar 9 Kromatogram KCKT, (a) standar kuersetin [5 ppm]](https://thumb-ap.123doks.com/thumbv2/123dok/4781132.3439008/11.892.129.761.406.1065/gambar-kromatogram-kckt-a-standar-kuersetin-ppm.webp)