5 2.1 Tanaman Daun Sirih
2.1.1 Klasifikasi Kingdom : Plantae Division : Magnoliophyta Class : Magnoliopsida Ordo : Piperales Family : Piperaceae Genus : Piper
Species : Piper betle Linn
(Inayatullah, 2012)
Gambar 2.1 Daun Sirih Hijau (Inayatullah, 2012) 2.1.2 Deskripsi Tanaman
Sirih termasuk dalam family piperaceae, merupakan jenis tumbuhan merambat dan bersandar pada batang pohon lain, yang tingginya 5-15 meter. Sirih
memiliki daun tunggal letaknya berseling dengan bentuk bervariasi mulai dari bundar telur atau bundar telur lonjong, pangkal berbentuk jantung atau agak bundar berlekuk sedikit, ujung daun runcing, pinggir daun rata agak menggulung ke bawah, panjang 5-18 cm, lebar 3-12 cm. Batang sirih berwarna cokelat kehijauan, berbentuk bulat, berkerut, dan beruas yang merupakan tempat keluarnya akar. Morfologi daun sirih berbentuk jantung, berujung runcing, tumbuh berselang-seling, bertangkai, teksturnya agak kasar jika diraba, dan mengeluarkan bau khas aromatis jika diremas. Panjang daun 6-17,5 cm dan lebar 3,5-10 cm. Sirih memiliki bunga majemuk yang berbentuk bulir dan merunduk. Bunga sirih dilindungi oleh daun pelindung yang berbentuk bulat panjang dengan diameter 1 mm. Buah terletak tersembunyi atau buni, berbentuk bulat, berdaging dan berwarna kuning kehijauan hingga hijau keabu-abuan. Tanaman sirih memiliki akar tunggang yang bentuknya bulat dan berwarna cokelat kekuningan (Koensoemardiyah, 2010).
Daun berwarna hijau, permukaan atas rata, licin agak mengkilat, tulang daun agak tenggelam permukaan bawah agak kasar, kusam, tulang daun menonjol, bau aromatiknya khas dan rasanya pedas. Batang tanaman berbentuk bulat dan lunak berwarna hijau agak kecoklatan dan permukaan kulitnya kasar serta berkerut-kerut (Inayatullah, 2012). Tanaman sirih merupakan tanaman yang perdu, merambat, batang berkayu, berbuku buku dan bersalur (Kharisma et al., 2010). Daun sirih mempunyai bau aromatik khas dan rasa pedas. Daun sirih
merupakan daun tunggal. Tangkai daun bulat, warna coklat kehijauan panjang 1,5–8 cm (Kristio, 2007).
2.1.3 Kandungan Kimia
Komponen utama minyak astsiri terdiri dari betlephenol dan beberapa derivatnya diantaranya euganol allypyrocatechine 26,8-42,5%, cineol 2,4-4,8%, methyl euganol 4,2-15,8%, caryophyllen 3-9,8%, hidroksikavikol, kavikol 7,2-16,7%, Kabivetol 2,7-6,2%, estragol, ilypryrokatekol 9,6%, karvakol 2,2-5,6%, alkaloid, flavonoid, triterpenoid atau steroid, saponin, terpen, fenilpropan, terpinen, diastase 0,8-1,8%, dan tannin 1-1,3%. Pada konsentrasi 0,1-1% fenol bersifat bakteriostatik, sedangkan pada konsentrasi 1-2% phenol bersifat bakteriosida (Inayatullah, 2012).
2.1.4 Bioaktivitas
Alam (2013) melaporkan aktivitas antioksidan dan aktivitas antiinflamasi dari ekstrak metanol daun sirih hijau. Potensi aktivitas antibakteri dari daun sirih hijau juga sudah pernah dibuktikan dalam penelitian Paramita et al., (2016) bahwa ekstrak terpurifikasi (fraksi bioaktif) daun sirih hijau pada konsentrasi 640 mg/mL menunjukkan efek antibakteri terhadap P. acnes dengan kategori intermediate. Jesonbabu et al., (2011) hidroksikavikol yang diisolasi dari ekstrak kloroform sirih hijau (Piper betle L.) mampu menghambat pertumbuhan bakteri Staphylococcus aureus dan Staphylococcus pyogenes. Menurut Putri (2010) bahwa flavonoid merupakan senyawa yang memiliki aktivitas antibakteri terhadap bakteri P. acnes yang ditunjukan dengan adanya zona hambat pada Rf 0,77 saat
dilakukan pengujian dengan KLT-Bioautografi. Menurut (Suppakul et al., 2006) aktivitas antibakteri minyak atsiri daun sirih hijau (Piper betle L.) telah terbukti mampu menghambat pertumbuhan bakteri Gram positif. Pada penelitian tersebut diperoleh hasil bahwa minyak atsiri daun sirih hijau mampu menghambat pertumbuhan bakteri Bacillus cereus, Enterococcus faecalis, Listeria monocytogenes, Micrococcus luteus dan Staphylococcus aureus dengan MIC berturut-turut yaitu: 50 μL/mL, 25 μL/mL, 12,5 μL/mL, 25 μL/mL dan 100 μL/mL. Bakteri yang digunakan dalam penelitian tersebut termasuk bakteri Gram positif yang memiliki persamaan terhadap struktur dinding sel dengan bakteri P. acnes.
2.2 Ekstrak
2.2.1 Definisi Ekstrak
Ekstrak adalah sediaan pekat yang diperoleh dengan mengekstraksi zat aktif dari simplisia nabati atau hewani menggunakan pelarut yang sesuai. Kemudian semua atau hampir semua pelarut diuapkan dan massa atau serbuk yang tersisa diperlakukan sedemikian rupa hingga memenuhi baku yang telah ditetapkan (Inayatullah, 2012).
2.2.2 Metode Ekstraksi
Ekstraksi adalah teknik pemisahan suatu senyawa berdasarkan perbedaan distribusi zat terlarut diantara dua pelarut yang saling bercampur. Pada umumnya zat terlarut yang diekstrak bersifat tidak larut atau larut sedikit dalam suatu pelarut tetapi mudah larut dengan pelarut lain (Inayatullah, 2012). Proses ekstraksi
menggunakan pelarut dapat dilakukan dengan beberapa metode yaitu maserasi, perkolasi, refluks, sokletasi dan digesti (Depkes RI, 2000).
Maserasi adalah proses pengekstrakan simplisia dengan menggunakan pelarut dengan beberapa kali pengocokan atau pengadukan pada temperatur ruangan (kamar) (Inayatullah, 2012). Maserasi dilakukan dengan cara merendam serbuk simplisia dalam cairan penyari. Cairan penyari akan menembus dinding sel atau masuk ke dalam rongga sel yang mengandung zat aktif, zat aktif tersebut akan larut karena adanya perbedaan konsentrasi antara larutan zat aktif di dalam sel dengan yang di luar sel. Larutan yang lebih pekat (di dalam sel) didesak keluar sel, masuk ke dalam larutan di luar sel. Peristiwa tersebut berulang sehingga terjadi kesetimbangan konsentrasi antara larutan di luar sel dan di dalam sel. Keuntungan cara penyarian dengan maserasi adalah cara pengerjaan dan peralatan yang digunakan sederhana dan mudah diusahakan (Depkes RI, 2000). Berdasarkan Farmakope Indonesia edisi IV bahwa pelarut yang digunakan sebagai cairan penyari adalah air, etanol, etanol-air, atau eter. Umumnya digunakan campuran etanol dan air untuk meningkatkan keefektifan penyarian (Depkes RI, 1995).
2.2.3 Purifikasi
Purifikasi ekstrak diharapkan akan meningkatkan khasiat ekstrak disamping memperkecil jumlah dosis pemberian kepada pengguna. Berbagai teknik purifikasi ekstrak dapat dilakukan di antaranya adalah teknik ekstraksi cair-cair (Srijanto dkk., 2012).
Ekstraksi cair-cair digunakan sebagai cara untuk perlakuan sampel atau clean up sampel untuk memisahkan analit-analit dari komponen matriks yang akan mengganggu pada saat kuantifikasi atau deteksi. Selain itu juga digunakan untuk memekatkan analit yang ada pada sampel sehingga konsentrasi analit menjadi lebih tinggi sehingga menurunkan jumlah dosis terapi (Gandjar dan Rohman, 2007). Ekstraksi cair-cair merupakan pemisahan komponen kimia di antara dua fase pelarut yang tidak saling bercampur di mana sebagian komponen larut pada fase pertama dan sebagian larut pada fase kedua, lalu kedua fase yang mengandung zat terdispersi dikocok, lalu didiamkan sampai terjadi pemisahan sempurna dan terbentuk dua lapisan fase cair dan komponen kimia akan terpisah ke dalam kedua fase tersebut sesuai dengan tingkat kepolarannya dengan perbandingan konsentrasi yang tetap (Sudjadi, 1986). Pada ekstraksi cair-cair, distribusi analit pada kedua fase pelarut yang digunakan mengikuti konsep like dissolve like dimana senyawa polar akan cenderung larut pada fase yang berair atau pelarut polar dan senyawa non-polar akan cenderung larut pada fase organik atau pelarut non-polar (Setlle, 1997; Cairns, 2009).
Menurut Cowan et al., (1999) penggunaan variasi pelarut dapat menarik senyawa tertentu berdasarkan kelarutan senyawa yang ingin dipisahkan dan polaritas dari pelarut yang digunakan seperti contohnya dalam penggunaan pelarut etanol dapat menarik senyawa golongan polifenol, tannin, alkaloid, terpenoid dan flavonol, untuk pelarut kloroform hanya dapat menarik senyawa dari golongan terpenoid dan flavonoid sedangkan pelarut eter dapat menarik senyawa dari
golongan alkaloid, terpenoid dan coumarin. Pada penelitian Singburaudom (2015) diperoleh bahwa fraksi kloroform dan fraksi dietileter memiliki aktivitas antifungi yang sangat besar (nilai zona hambat) dengan nilai zona hambat sebesar 28.2 mm, 8.7 mm dan 2 mm untuk fraksi kloroform sedangkan untuk fraksi dietileter memiliki zona hambat sebesar 12.4 mm, 5 mm dan 2.2 mm dimana pada penelitian tersebut senyawa yang paling banyak didapatkan atau persentase terbesar adalah hidroksikavikol. Penelitian lainnya juga menyebutkan bahwa kloroform mampu menarik 80% hidroksikavikol (Sharma et al., 2009).
2.3 Acne Vulgaris
Acne vulgaris adalah suatu penyakit peradangan kronik dari unit pilosebaseus disertai penyumbatan dari penimbunan bahan keratin duktus kelenjar yang ditandai dengan adanya komedo, papula, pustula, nodul, kista sering ditemukan pada daerah predileksi seperti muka, bahu bagian atas dari ekstremitas superior, dada dan punggung (Afriyanti, 2015). Menurut catatan studi dermatologi kosmetika Indonesia menunjukan yaitu 60% penderita acne vulgaris pada tahun 2006, 80% terjadi pada tahun 2007 dan 90% pada tahun 2009. Prevelansi tertinggi yaitu pada umur 14-17 tahun, dimana pada wanita berkisar 83-85% dan pada pria yaitu pada umur 16-19 tahun berkisar 95-100%. Penyebab Acne vulgaris sangat banyak (multifaktorial) antara lain faktor genetik, faktor bangsa ras, faktor makanan, faktor iklim, faktor jenis kulit, faktor kebersihan, faktor penggunaan kosmetik, faktor stres, faktor infeksi dan faktor pekerjaan.
2.4 Propionibacterium acnes
Salah satu bakteri yang mengakibatkan timbulnya jerawat pada permukaan kulit yaitu P. acnes. Berikut ini klasifikasi dari bakteri P. acnes
Kingdom : Bacteria Phylum : Actinobacteria Class : Actinobacteridae Ordo : Actinomycetales Famili : Propionibacteriaceae Genus : Propionibacterium Spesies : Propionibacterium acnes
(Bruggemann, 2010)
P. acnes tergolong kedalam kelompok bakteri berbentuk batang atau benang Gram positif yang tidak membentuk spora. Bakteri ini tergolong bakteri anaerob hingga aerotolerant. Pertumbuhan optimum pada suhu 30-37°C. Koloni bakteri pada media agar berwarna kuning muda sampai merah muda dan memiliki bentuk yang khas (Bojar, 2004). P. acnes ikut serta dalam patogenesis jerawat dengan menghasilkan lipase yang memecahkan asam lemak bebas dari lipid kulit. Asam lemak ini dapat menimbulkan radang jaringan akut menyebabkan jerawat. P. acnes kadang kadang menyebabkan infeksi katup jantung prostetik prostetik dan pintas cairan serebrospinal (Jawetz et al., 2005). Mekanisme terjadinya jerawat adalah bakteri P. acnes yang merusak stratum corneum dan srtatum germinat dengan cara mensekresikan bahan kimia yang menghancurkan dinding
pori. Kondisi ini dapat menyebabkan inflamasi. Asam lemak dan minyak pada kulit tersumbat dan mengeras. Jika jerawat disentuh maka inflamasi meluas sehingga padatan asam lemak dan minak kulit yang mengeras akan membesar (Athikomkulchai et al., 2008).
2.5 Minyak Atsiri
Minyak atsiri adalah zat berbau yang terkandung dalam tanaman. Minyak ini disebut juga minyak menguap, minyak eteris, atau minyak essensial karena pada suhu biasa (suhu kamar) mudah menguap di udara terbuka. Istilah essensial dipakai karena minyak atsiri mewakili bau dari tanaman asalnya. Secara kimia, minyak atsiri bukan merupakan senyawa tunggal, tetapi tersusun dari berbagai macam komponen yang secara garis besar terdiri dari kelompok terpenoid dan fenil propana. Adapun sifat dari minyak atsiri yaitu mudah menguap apabila dibiarkan pada udara terbuka, tidak larut dalam air, larut dalam pelarut organik, tidak berwarna, tetapi semakin lama menjadi gelap karena mengalami oksidasi dan pendamaran, memiliki bau khas seperti tumbuhan aslinya (Gunawan dan Mulyani, 2004).
Minyak atsiri larut dalam kloroform, eter, alkohol dan petroleum eter. Bobot jenis minyak atsiri daun sirih hijau 0,9313 gram/mL, indek bias 1,4526 dan putaran optik 4,259. Bersifat tidak stabil terhadap pengaruh lingkungan, baik pengaruh oksigen udara maupun sinar matahari karena terdiri dari berbagai macam komponen penyusun (Novalny, 2006).
2.6 Uji Aktivitas Antibakteri dengan Metode Difusi Disk
Pada metode ini, penentuan aktivitas didasarkan pada kemampuan difusi dari zat antibakteri dalam lempeng agar yang telah diinokulasikan dengan bakteri uji. Pada metode cakram kertas (Cara Kirby Bauer) digunakan suatu kertas cakram saring (paper disc) yang befungsi sebagai tempat menampung zat antibakteri. Kertas saring yang mengandung zat antibakteri tersebut diletakkan pada lempeng agar yang telah diinokulasi dengan bakteri uji, kemudian diinkubasi pada waktu dan suhu tertentu, sesuai dengan kondisi optimum dari bakteri uji yaitu pada suhu 37°C selama 18-24 jam. Ada dua macam zona hambat yang terbentuk dari cara Kirby Bauer :
1. Zona radikal yaitu suatu daerah di sekitar disk dimana sama sekali tidak ditemukan adanya pertumbuhan bakteri. Potensi antibakteri diukur dengan mengukur diameter dari zona radikal.
2. Zona irradikal yaitu suatu daerah di sekitar disk dimana pertumbuhan bakteri dihambat oleh antibakteri tetapi tidak dimatikan (Inayatullah, 2012).
Disc diffusion test atau uji difusi disk dilakukan dengan mengukur diameter clear zone (zona bening yang tidak memperlihatkan adanya pertumbuhan bakteri yang terbentuk di sekeliling zat antimikroba pada masa inkubasi bakteri) yang merupakan petunjuk adanya respon penghambatan pertumbuhan bakteri oleh suatu senyawa antibakteri dalam ekstrak. Semakin besar zona hambatan yang terbentuk maka semakin besar pula kemampuan aktivitas zat
antibakteri (Inayatullah, 2012). Zona hambatan diukur dengan mistar dengan cara mengurangi diameter keseluruhan (sumuran + zona hambatan) dengan diameter sumuran. Pengujian dilakukan 3 kali pengulangan (Lathifah, 2008). Syarat jumlah bakteri untuk uji kepekaan/sensitivitas yaitu 105-108CFU/mL (Inayatullah, 2012).
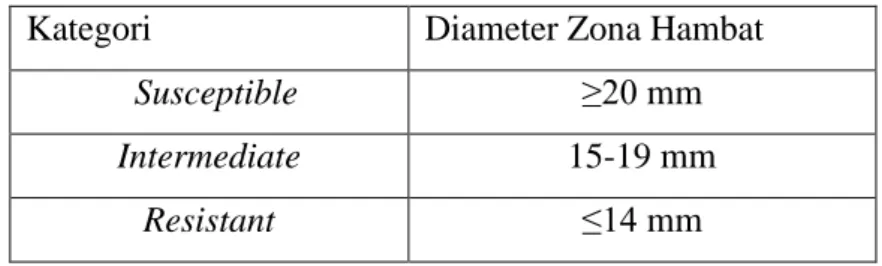
Tabel 2.1 Berikut Klasifikasi Daya Hambat Pertumbuhan Bakteri
Kategori Diameter Zona Hambat
Susceptible ≥20 mm
Intermediate 15-19 mm
Resistant ≤14 mm