BAB II
TINJAUAN PUSTAKA
2.1 Simvastatin 2.1.1 Uraian Bahan
Menurut Moffat, et al., (2004), sifat fisiko kimia simvastatin adalah sebagai berikut:
Rumus struktur:
Gambar 1. Struktur Simvastatin Rumus Molekul : C25H38O5
Berat Molekul : 418,6
Titik Lebur : 135o sampai 138oC
Pemerian : Serbuk kristal putih
Kelarutan : Tidak larut dalam air, n-heksana, dan asam klorida; larut dalam kloroform, dimetil sulfoksida, metanol, etanol, polietilen glikol, NaOH, dan propilen glikol.
2.1.2 Farmakologi
Statin merupakan kelompok dari 3-hydroxy-3-methylglutaroyl-coenzyme A (HMG-CoA) inhibitor reduktase yang digunakan untuk hiperkolesteramia dan hiperlipidemia. Simvastatin, lovastatin dan atorvastatin adalah yang paling sering digunakan, namun hanya yang pertama yang merupakan prodrug. Bentuk prodrug lebih baik di absorbsi dibandingkan dengan bentuk non-modifikasi (Guzik, et al., 2010).
Simvastatin berdaya menurunkan kadar LDL (Low Density
Lipoprotein) dan kolesterol total dalam 2-4 minggu. Kadar VLDL (Very Low Density Lipoprotein) dan TG juga dapat diturunkan, sedangkan HDL (High Density Lipoprotein) dinaikkan sedikit. Digunakan tersendiri atau dikombinasi
dengan damar. Khasiat menurunkan LDL-nya kuat, tetapi lebih lemah daripada atorvastatin (Tan dan Rahardja, 2007).
2.1.3 Efek Samping
Pada umumnya ringan, antara lain nyeri otot reversibel, yang adakalanya menjadi gangguan otot parah yang disebut rhabdomyolysis. Wanita hamil tidak boleh menggunakannya karena statin berdaya teratogen (mengakibatkan cacat pada bayi), lagipula kolesterol mutlak dibutuhkan bagi pengembangan janin (Tan dan Rahardja, 2007).
2.1.4 Dosis
Permulaan 10 mg pada malam hari, bila perlu dinaikkan dengan interval 4 minggu sampai maksimal 40 mg (Tan dan Rahardja, 2007).
2.2 Kromatografi
Kromatografi merupakan suatu proses pemisahan yang mana analit-analit dalam sampel terdistribusi antara 2 fase, yaitu fase diam dan fase gerak. Fase diam dapat berupa bahan padat atau porus dalam bentuk molekul kecil, atau dalam bentuk cairan yang dilapiskan pada pendukung padat atau dilapiskan pada dinding kolom. Fase gerak dapat berupa gas atau cairan. Jika gas digunakan sebagai fase gerak, maka prosesnya dikenal sebagai kromatografi gas. Dalam kromatografi cair dan kromatografi lapis tipis, fase gerak yang digunakan selalu cair (Rohman, 2009).
Saat ini kromatografi merupakan teknik pemisahan yang paling umum dan paling sering digunakan dalam bidang kimia analisis kualitatif, kuantitatif, atau preparatif dalam bidang farmasi, lingkungan, industri, dan sebagainya. Kromatografi merupakan suatu teknik pemisahan yang menggunakan fase diam (stationary phase) dan fase gerak (mobile phase) (Gandjar dan Rohman, 2009).
2.2.1 Klasifikasi Kromatografi
Kromatografi dapat dibedakan atas berbagai macam, tergantung pada pengelompokannya. Berdasarkan pada mekanisme pemisahannya, kromatografi dibedakan menjadi : (a) kromatografi adsorbsi; (b) kromatografi partisi; (c) kromatografi pasangan ion; (d) kromatografi penukar ion (e) kromatografi eksklusi ukuran dan (f) kromatografi afinitas. Berdasarkan pada alat yang digunakan, kromatografi dapat dibagi atas: (a) kromatografi kertas; (b) kromatografi lapis tipis, yang kedua sering disebut kromatografi planar; (c)
kromatografi cair kinerja tinggi (KCKT) dan (d) kromatografi gas (KG) (Rohman, 2009).
2.3 Kromatografi Cair Kinerja Tinggi
Kromatografi Cair Kinerja Tinggi memisahkan komponen campuran senyawa kimia terlarut dengan sistem adsorpsi pada fase diam padat atau sistem partisi di antara fase diam cair yang terikat pada penyangga padat, dan fase gerak cair. Kromatografi Cair Kinerja Tinggi dapat memisahkan makromolekul, ion, bahan alam yang tidak stabil, polimer dan berbagai gugus polifungsi dengan berat molekul tinggi. Berbeda dengan kromatografi gas, pemisahan pada KCKT adalah hasil antaraksi spesifik antara molekul senyawa dengan fase diam dan fase gerak (Satiadarma, dkk., 2004).
Kromatografi cair kinerja tinggi (KCKT) merupakan sistem pemisahan dengan kecepatan dan efisiensi yang tinggi. Hal ini karena didukung oleh kemajuan dalam teknologi kolom, sistem pompa tekanan tinggi, dan detektor yang sangat sensitif dan beragam. KCKT mampu menganalisa berbagai cuplikan secara kualitatif maupun kuantitatif, baik dalam komponen tunggal maupun campuran (Ditjen POM, 1995).
KCKT merupakan teknik pemisahan yang diterima secara luas untuk analisis dan pemurnian senyawa tertentu dalam suatu sampel pada sejumlah bidang antara lain: farmasi, lingkungan dan industri-industri makanan (Munson, 1984).
2.4 Cara Kerja KCKT
Kromatografi merupakan teknik yang mana solut atau zat-zat terlarut terpisah oleh perbedaan kecepatan elusi, dikarenakan solut-solut ini melewati suatu kolom kromatografi. Pemisahan solut-solut ini diatur oleh distribusi dalam fase gerak dan fase diam. Penggunaan kromatografi cair membutuhkan penggabungan secara tepat dari berbagai macam kondisi operasional seperti jenis kolom, fase gerak, panjang dan diameter kolom, kecepatan alir fase gerak, suhu kolom, dan ukuran sampel (Gandjar dan Rohman, 2009).
Pemisahan analit dalam kolom kromatografi berdasarkan pada aliran fase gerak yang membawa campuran analit melalui fase diam dan perbedaan interaksi analit dengan permukaan fase diam sehingga terjadi perbedaan waktu perpindahan setiap komponen dalam campuran (Meyer, 2010).
2.5 Jenis Pemisahan KCKT
Dari kedua fase, yaitu fase diam dan fase gerak, salah satu di antaranya selalu harus lebih polar daripada yang lainnya. Misalnya, heksana yang dipakai pada kolom silika kepolarannya jauh lebih rendah daripada permukaan silika. Jika fase yang lebih polar itu fase diam, ini disebut kromatografi normal. Jika fase yang kepolarannya lebih rendah ialah fase diam, ini dikenal sebagai kromatografi fase balik (Gritter, dkk., 1991).
Kromatografi fase balik menggunakan fase diam dari silika yang dimodifikasi secara kimiawi. Fase diam yang paling popular digunakan adalah oktadesilsilan (ODS atau C18) yang relatif non polar sedangkan fase geraknya
relatif lebih polar daripada fase diam. Kondisi kepolaran kedua fase ini merupakan kebalikan dari kromatografi fase normal sehingga disebut kromatografi fase balik (Meyer, 2010).
2.6 Komponen KCKT
Instrumentasi KCKT terdiri atas wadah fase gerak, pompa, injektor, kolom, detektor, dan pengolah data. Diagram skematik alat KCKT ditunjukkan oleh Gambar 2.
Gambar 2. Diagram Skematik Alat KCKT (Rohman, 2009). 2.6.1 Wadah Fase Gerak
Wadah fase gerak harus bersih dan lembam (inert). Wadah pelarut kosong ataupun labu laboratorium dapat digunakan sebagai wadah gerak. Wadah ini biasanya dapat menampung fase gerak antara 1 sampai 2 liter pelarut. Fase gerak sebelum digunakan harus dilakukan degassing (penghilangan gas) yang ada pada fase gerak, sebab dengan adanya gas akan berkumpul dengan komponen lain terutama di pompa dan detektor sehingga akan mengacaukan analisis. Pada saat membuat pelarut untuk fase gerak, maka akan sangat dianjurkan untuk menggunakan pelarut, buffer, dan reagen dengan
kemurnian yang sangat tinggi, dan lebih terpilih lagi jika pelarut-pelarut yang akan digunakan berderajat KCKT (HPLC grade). Adanya pengotor dalam reagen dapat menyebabkan gangguan pada sistem kromatografi. Adanya partikel yang kecil dapat berkumpul dalam kolom atau dalam tabung sempit, sehingga dapat mengakibatkan suatu kekosongan pada kolom atau tabung tersebut (Gandjar dan Rohman, 2009).
2.6.2 Pompa
Ada dua jenis pompa yang digunakan: tekanan-tetap dan pendesakan-tetap. Pompa pendesakan tetap dapat dibagi lagi menjadi pompa torak dan pompa semprit. Pompa torak menghasilkan aliran yang berdenyut, jadi memerlukan peredam denyut atau peredam elektronik untuk menghasilkan garis alas detektor yang stabil jika detektor peka terhadap aliran. Kelebihan utamanya ialah tandonnya tidak terbatas. Pompa semprit menghasilkan aliran yang tak berdenyut, tetapi tandonnya terbatas (Jhonson dan Stevenson, 1978). 2.6.3 Injektor
Menurut Jhonson dan Stevenson (1978), ada tiga tipe dasar injektor yang dapat digunakan, yaitu:
a. Aliran henti: Aliran dihentikan, penyuntikan dilakukan pada tekanan atmosfir; sistem ditutup, dan aliran dilanjutkan lagi (biasanya sistem aliran utama tetap berada dalam tekanan kerja). Cara ini dapat dipakai karena difusi di dalam zat cair kecil, jadi umumnya daya pisah tidak dipengaruhi;
b. Septum: Ini adalah injektor langsung pada aliran, yang sama dengan injektor yang lazim dipakai pada kromtografi gas. Injektor tersebut dapat
dipakai pada tekanan sampai sekitar 60 - 70 atmosfer. Sayang sekali, septum tidak dapat dipakai untuk semua pelarut KC. Selain itu, partikel kecil terlepas dari septum dan cenderung menyumbat;
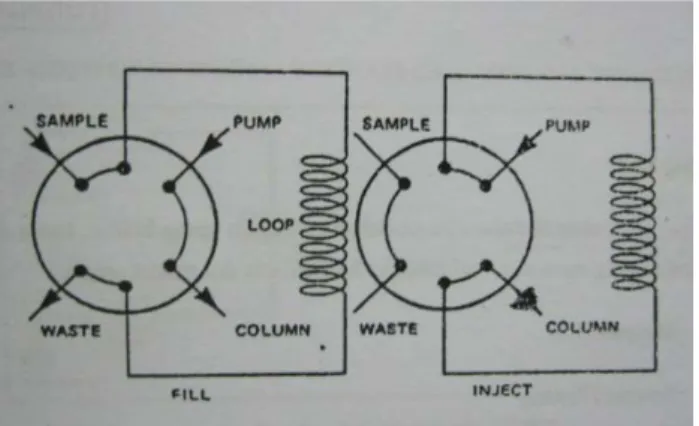
c. Katup jalan-kitar: jenis injektor ini, biasanya dipakai untuk menyuntikkan volum lebih besar dari pada 10 µl dan sekarang dipakai dalam sistem yang diotomatkan. (volume yang lebih kecil dapat disuntikkan secara manual memakai adaptor khusus). Pada kedudukan mengisi, jalan-kitar cuplikan diisi pada tekanan atmosfir. Jika katup dijalankan (dibuka), cuplikan di dalam jalan-kitar teralirkan ke dalam kolom. Katup jalan-kitar secara skematik ditunjukkan oleh Gambar 3.
Gambar 3. Tipe Injektor Katup Putaran (De Lux Putra, 2007). 2.6.4 Kolom
Kolom merupakan jantung kromatografi. Keberhasilan atau kegagalan analisis bergantung pada pemilihan kolom dan kondisi kerja yang tepat. Menurut Johnson dan Stevenson (1978), kolom dapat dibagi menjadi dua kelompok:
a. Kolom analitik: garis tengah dalam 2 – 6 nm. Panjang bergantung pada jenis kemasan,untuk kemasan pelikel biasanya panjang kolom 50 – 100 cm. Untuk kemasan mikropartikel berpori, biasanya 10 – 30 cm;
b. Kolom preparatif: umumnya bergaris tengah 6 mm atau lebih besar dan panjang kolom 25 – 100 cm.
Kolom hampir selalu terbuat dari baja nirkarat. Kolom biasanya dipakai pada suhu kamar, tetapi suhu yang lebih tinggi dapat juga dipakai, terutama dalam kromatografi penukar ion dan kromatografi eksklusi. Kemasan bergantung pada ragam KCKT yang dilakukan.
2.6.5 Fase Diam
Fase diam dapat berupa permukaan zat padat yang berfungsi sebagai medium yang menjerap, atau permukaan zat cair yang terdapat pada sejenis zat padat. Banyak sistem fase diam baru telah dikembangkan untuk KCKT, dan pemakaian bahan tersebut sangat meningkatkan keefisienan dan kemampuan metode itu. Sebagian besar bahan itu didasarkan pada silika (Gritter, dkk., 1991).
Kebanyakan fase diam pada KCKT berupa silika yang dimodifikasi secara kimiawi, silika yang tidak dimodifikasi, atau polimer-polimer stiren dan divinil benzen. Permukaan silika adalah polar dan sedikit asam karena adanya residu gugus silanol (Si-OH). Oktadesil silika (ODS atau C18) merupakan fase diam yang paling banyak digunakan karena mampu memisahkan senyawa-senyawa dengan kepolaran yang rendah, sedang maupun tinggi (Gandjar dan Rohman, 2009).
Sekarang ini, gel silika ODS atau fase-fase sejenis seperti gel silika oktil digunakan untuk >80% analisis farmasi namun fase-fase lain hanya digunakan jika diperlukan selektivitas khusus, misalnya untuk senyawa-senyawa yang sangat mudah larut dalam air atau untuk pemisahan bioanalisis yang menjadi penting karena matriks sampel tersebut menghasilkan banyak puncak yang mengganggu (Watson, 2005).
2.6.6 Detektor
Detektor pada KCKT dikelompokkan menjadi 2 golongan yaitu: detektor universal (yang mampu mendeteksi zat secara umum, tidak bersifat selektif) seperti detektor indeks bias dan detektor spektrofotometri massa; dan golongan detektor yang spesifik yang hanya akan mendeteksi analit secara spesifik dan selektif, seperti detektor UV-Vis, detektor fluoresensi, elektrokimia. Idealnya, suatu detektor mempunyai karakteristik sebagai berikut: (1) mempunyai respon terhadap solut yang cepat dan reprodusible; (2) mempunyai sensitifitas yang tinggi, yakni mampu mendeteksi solut pada kadar yang sangat kecil; (3) stabil dalam pengoperasiannya, dan sebagainya (Gandjar dan Rohman, 2009).
2.6.7 Pengolah Data
Alat pengumpul data seperti komputer, integrator, dan rekorder dihubungkan ke detektor. Alat ini akan mengukur sinyal elektronik yang dihasilkan oleh detektor dan memplotkannya sebagai suatu kromatogram yang selanjutnya dievaluasi oleh seorang analis (Gandjar dan Rohman, 2009).
2.6.8 Fase Gerak
Fase gerak atau eluen biasanya terdiri atas campuran pelarut yang dapat bercampur yang secara keseluruhan berperan dalam daya elusi dan resolusi. Daya elusi dan resolusi ini ditentukan oleh polaritas keseluruhan pelarut, polaritas fase diam, dan sifat komponen-komponen sampel (Gandjar dan Rohman, 2009).
Pada KCKT, susunan pelarut atau fase gerak merupakan salah satu hal penting yang mempengaruhi proses pemisahan. Berbagai macam pelarut dipakai dalam semua jenis KCKT, tetapi ada beberapa syarat fase gerak yang digunakan dalam KCKT. Menurut Jhonson dan Stevenson (1978), kriteria fase gerak yang ideal adalah sebagai berikut:
(a) Murni, tanpa cemaran;
(b) Tidak bereaksi dengan kemasan; (c) Sesuai dengan detektor;
(d) Dapat melarutkan cuplikan; (e) Mempunyai viskositas rendah;
(f) Memungkinkan memperoleh kembali cuplikan dengan mudah, jika diperlukan;
(g) Harganya wajar.
Pada umumnya, pelarut dibuang setelah digunakan karena tata kerja pemurniannya memakan waktu dan mahal. Dari semua persyaratan di atas, 4 persyaratan pertama merupakan yang paling penting (Jhonson dan Stevenson (1978).
2.6.9 Elusi Gradien dan Isokratik
Menurut Gritter, dkk., (1991), elusi pada kromatografi cair kinerja tinggi dapat dibagi menjadi dua sistem yaitu:
1. Sistem elusi isokratik
Pada sistem ini, elusi dilakukan dengan satu macam atau lebih fase gerak dengan perbandingan tetap (komposisi fase gerak tetap selama elusi). 2. Sistem elusi gradien
Pada sistem ini, elusi dilakukan dengan campuran fase gerak yang perbandingannya berubah-ubah dalam waktu tertentu (komposisi fase gerak berubah-ubah selama elusi).
Elusi gradien digunakan pada situasi yang membutuhkan pemprograman temperatur dalam GC, dan ini dibutuhkan ketika range dari waktu retensi dari pelarut dalam kolom besar sehingga tidak dapat terlarut dan elusi dalam waktu tertentu menggunakan saju jenis atau campuran pelarut (Lindsay, 1987).
2.7 Validasi Metode
Validasi metode analisis adalah suatu tindakan penilaian terhadap parameter tertentu, berdasarkan percobaan laboratorium, untuk membuktikan bahwa parameter tersebut memenuhi persyaratan untuk penggunaannya (Harmita, 2004).
Validasi metode menurut United States Pharmacopeia (USP) tahun 2012 dilakukan untuk menjamin bahwa metode analisis akurat, spesifik,
reprodusibel dan tahan pada kisaran analit yang akan dianalisis. Suatu metode analisis harus divalidasi untuk verifikasi bahwa parameter-parameter kinerjanya cukup mampu untuk mengatasi masalah dalam analisis. Parameter analisis yang ditentukan pada validasi adalah akurasi, presisi, batas deteksi, batas kuantitasi, spesifikasi, linieritas dan rentang, kekasaran (Ruggedness) dan ketahanan (Robutness).
Akurasi/kecermatan adalah ukuran yang menunjukkan derajat kedekatan hasil analisis dengan kadar analit yang sebenarnya. Kecermatan dinyatakan sebagai persen perolehan kembali (recovery). Presisi/keseksamaan adalah ukuran kedekatan antar serangkaian hasil analisis yang diperoleh dari beberapa kali pengukuran pada sampel yang sama. Presisi dinyatakan dengan Relatif Standar Deviasi (RSD) (Harmita, 2004).
Batas deteksi adalah jumlah terkecil analit dalam sampel yang dapat dideteksi yang masih memberikan respon signifikan dibandingkan dengan blanko. Batas deteksi merupakan parameter uji batas. Batas kuantitasi merupakan parameter pada analisis renik dan diartikan sebagai kuantitas terkecil analit dalam sampel yang masih dapat memenuhi kriteria cermat dan seksama. Limit Of Detection (LOD) dan Limit Of Quantitation (LOQ) dapat dihitung secara statistik melaljui garis regresi linier dari kurva kalibrasi (Harmita, 2004).
Batas deteksi (limit of detection, LOD) didefinisikan sebagai konsentrasi analit terendah dalam sampel yang masih dapat terdeteksi, meskipun tidak selalu dapat dikuantitasi. Batas kuantitasi (limit of quantitation,
LOQ) didefinisikan sebagai konsentrasi analit terendah dalam sampel yang dapat ditentukan dengan kecermatan dan keseksamaan yang dapat diterima pada kondisi operasional metode yang digunakan (Gandjar dan Rohman, 2009).