Pengolahan Limbah Cair Pabrik Pupuk Urea dengan Menggunakan Proses
Gabungan Nitrifikasi-denitrifikasi dan Microalgae
Dian K. Wardhany, Fitria Ayuningtyas
J urusan T eknik K imia F akultas T eknik, Universitas D iponegoro
J l. Prof. S oedarto, S H, K ampus T embalang, S emarang 50239
T elp/F ax. (024)7460058, E -mail : cheundip@ usa.net
2008
Abstrak
Selama ini limbah dari pabrik urea di Indonesia diolah menggunakan proses nitrifikasi -denitrifikasi
heterotrofik dengan menggunakan bantuan lumpur aktif nitrifying. Sayangn ya proses ini memiliki kelemahan. K adar
C OD limbah urea yang rendah, menyebabkan perlu-nya penambahan asupan sumber karbon. Alternatif pengolahan
yang diteliti adalah proses yang menggabungkan microalgae dengan lumpur aktif nitrifying. D engan proses ini
penambahan asupan karbon bisa dihindari karena microalgae-nya mampu memanfaatkan (NH)2C O dan NH3-N
sebagai sumber nitrogen untuk kemudian difotosinteis dengan bantuan C O2. Sedangkan microalgae yang terbentuk
bisa dimanfaatkan oleh lumpur aktif sebagai sumber karbon. L imbah dengan variasi kadar ammonia yang berbeda
dialirkan menuju bak microalgae kemudian dialrkan lagi ke bak lumpur aktif. Respon yang diamati adalah
penurunan kadar NH3-N yang terjadi serta kadar NO2-NO3 yang terbentuk dari penguraian ammonia. D ari
penelitian ini dapat disimpulkan konsentrasi NH3-N dalam influent berbanding terbalik dengan persentase
penurunan NH3-N dimana semakin besar konsentrasi NH3-N influent mengakibatkan persentase penurunan
konsentrasi NH3-N dalam limbah cenderung semakin turun. Persentase penurunan NH3-N paling tinggi yaitu
dalam effluent cenderung semakin turun seiring dengan semakin besarnya
konsentrasi NH3-N influent. K onsentrasi NO2
diperoleh saat konsentrasi influent NH3-N paling rendah yaitu 2747,95 mg/L .
K ata kunci : (NH)2C O, NH3-N,, microalgae, L umpur aktif nitrifying.
Abstract
F or all this time, waste that come from urea manufacturer in Indonesia was treated by using the nitrifying sludge
with nitrification-denitrification process. Nevertheless this process still has a flaw. L ow C OD content in urea waste
makes it needs some additional carbon source to be treated.T his research study about alternative treatment for the
urea waste by mixed-up nitrifying sludge with microalgae. With this kind of process we can avoid adding carbon
source because microalgae could exploit (NH)2C O and NH3-N as nitrogen source so that with adding C O2
photosynthesis process could be done. Microalgae which have been produced by the process than could be feed to
the nitrifying sludge as the carbon source. F rom the research we conclude that influent with more NH3-N content in
it will cause percentage of NH3-N degradation depressed. T he highest percentage of NH3-N depreesed, 67,33 %
caused by the influent with lowest content of NH3-N, 2747,05 mg/L . Meanwhile lowest percentage of NH3-N
depressed, 57,17 % caused by influent with hig hest content of NH3-N 4690,02 mg/L F rom analysis result we see that
mainly NO2
content, 2,03 mg/L caused by influent with highest content of NH3-N, 4690,02 mg/L . Meanwhilethe highest
NO2
and NO3
content 60,87 mg/L obtained when influent contain of lowest NH3-N ocntent, 2747,95 mg/L .
1. P endahuluan
Meskipun (NH2)2C O dan NH3-N tidak termasuk senyawa B 3, limbah cair pabrik pupuk urea dapat menimbulkan
kerusakan ekosistem badan air yang sangat serius. S ampai saat ini, pengolahan limbah cair pabrik pupuk urea dilakukan dengan proses nitrifikasi-denitrifikasi heterotrofik dalam kolam-kolam terbuka. K arena kadar C OD limbah cair ini rendah, proses nitrifikasi-denitrifikasi heterotrofik tersebut memerlukan banyak masukan sumber karbon, dalam hal ini adalah metanol. S elain itu, kinerja proses tidak terkendali ketika terjadi fluktuasi karakteristik limbah yang ekstrim.
T eknologi yang diterapkan berbasis pada penggabungan activated microalgae dan nitrifikasi -denitrifikasi autotrofik untuk menguraikan limbah cair urea kadar tinggi dan ammonia kadar tinggi. Microalgae merupakan mikroba autotrof yang mampu memanfaatkan (NH2)2C O dan NH3-N sebagai sumber nitrogen (sumber N) dan gas
karbon dioksida (C O2) sebagai sumber karbon (sumber C ) .
D alam skala besar mikroalgae selalu berasosiasi dengan bakteria/mikroba lain.Pada dasarnya, interaksi bakteri -algae mampu memurnikan air sungai. A ktivitas metabolisme bakteri heterotropik-aerobik menghasilkan C O2, NH4
+
dan sebagainya. Mikroalgae menyerap senyawa-senyawa tersebut dan menghasilkan bahan organik, O2,
dan H2O. Oksigen yang diproduksi mikroalgae digunakan oleh bakteri aerobik-heterotrofik diantaranya untuk reaksi
nitrifikasi dan bakteri anaerobik-denitrifikasi. D alam penelitian ini, akan dicoba menggunakan microalgae yang telah di-activated yang digabungkan dengan bakteri alam dalam lumpur aktif yang telah dipra-kondisikan, untuk mengolah air limbah yang mengandung urea dan amonia konsentrasi tinggi.
Melalui proses fotosintesis, microalgae menggunakan C O2 dari bakteri aerob dan amonia untuk membentuk
protoplasma sel dan melepaskan molekul oksigen [S tein, 1973; C oombs dan Hall, 1992; D anks et al, 1983; Polle et al, 1999]:
C ahaya
NH3 + 8 C O2 + 4,5 H2O C5H14O3N + 8,75 O2
F aktor lingkungan yang mempengaruhi pertumbuhan (fotosintesis) microalgae adalah intensitas cahaya, suhu air, pH, makro dan mikronutrien, 5 konsentrasi C O2 [S urk-K ey & T oshiuki, 2002].
W alaupun mengandung unsur karbon, karbon pada urea tidak bisa digunakan sebagai sumber hara [S tein, 1973; Polle et al, 1999], karena karbon dalam bentuk teroksidasi dan selama hidrolisis terlepas sebagai C O2 dalam reaksi
sebagai berikut:
(NH2)2C O + 2 H2O (NH)2 C O3 2NH3 + C O2 + H2O
S umber nitrogen utama yang dapat digunakan oleh microalgae adalah nitrat dan amonia-N, sedangkan penggunaan nitrit dibatasi oleh toksisitasnya. B ila nitrat dan amonia-N terdapat bersama, maka nitrat tidak akan diabsorpsi sampai semua amonia-N habis terserap.
Hampir semua microalgae memiliki enzim urease sebagaimana halnya tumbuhan tingkat tinggi [B arr, 2002]. Urea digunakan sebagai sumber N dalam pertumbuhan berbagai jenis microalgae, bahkan juga oleh microalgae yang tidak mempunyai urease [S yrett, 1962 dalam Morris, 1974].
B akteri memanfaatkan bahan organik yang dihasilkan oleh microalgae atau berasal dari microalgae mati sebagai sumber karbon untuk mensintesa sel baru dan untuk kebutuhan energi membentuk produk akhir seperti C O2, NH4
+
pada proses respirasi dan sintesis, Microalgae memanfaatkan C O2 sebagai sumber karbon untuk fotosintesis. R espirasi sparger, yang sekaligus berfungsi sebagai pengaduk.
Proses konvensional untuk menghilangkan ammonium pada umumnya melalui 2 tahap, nitrifikasi aerobik dan denitrifikasi anaerobik. K ajian yang dilangsungkan pada dekade terakhir menemukan bahwa konversi NH4
+
menjadi gas N2 secara autotrofik meliputi 2 tahap: (i) nitrifikasi aerobik NH4
+
penerima electron dan (ii ) denitrifikasi anoksik NO2 atau NO3 menjadi gas N2 dengan NH4 +
sebagai donor elektron [ A nderson & L evine, 1986].
Pada dasarnya pembuatan lumpur aktif nitrifying relatif mudah [Gernaey et al, 1997]. T etapi bila lumpur itu kemudian dapat diinduksi untuk mengkonversi NH4
+
menjadi N2 tanpa bantuan sumber karbon organik, maka sebuah
langkah penting dalam pengolahan limbah akan mugkin dilakukan.
T ujuan dari penelitian ini adalah mengembangkan proses gabungan activated microalgae dan nitrifikasi-denitrifikasi autotrofik untuk pengolahan limbah cair pabrik pupuk urea. S erta mengetahui efisiensi penurunan konsentrasi NH3-N dalam limbah cair urea menggunakan proses gabungan activated microalgae dan nitrifikasi-denitrifikasi autotrofik.
2. Bahan dan Metode Penelitian
A lat yang digunakan antara lain bak Nitrifikasi 160 liter, bak S edimentasi, tandon F eed 200 liter, constant feed tank, submersible water pump, timbangan R eagen, kompressor dan A ir D iffuser. B ahan yang digunakan adalah urea sintesis, microalgae dan lumpur aktif yang telah diaklimatisasi.
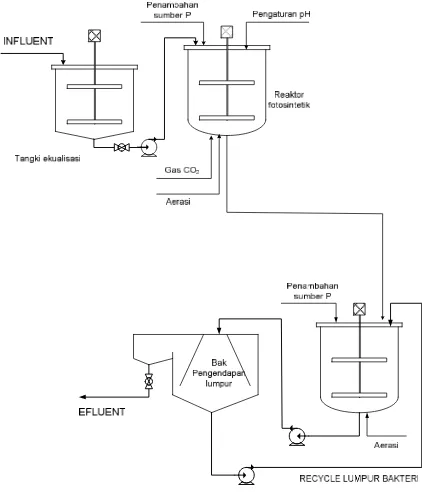
Prosedur percobaan diawali dengan pembuatan larutan urea sintesis sebanyak 200 L , larutan urea sintesis ini kemudian dialirkan ke dalam reaktor fotosintesis yang berisi microalgae, setelah itu dialirkan lagi ke bak nitrifikasi yang berisi lumpur aktif, dari bak nitrifikasi effluent ditampung di bak sedimentasi sehingga lumpur yang terbawa pada aliran umpan bisa diendapkan untuk direcycle kembali ke bak nitrifikasi.
Gambar 3.1 R angkaian A lat Penelitian
D ari effluent respon yang akan diamati adalah persen penurunan kadar NH3-N dan kadar NO2-NO3 yang
terbentuk. A nalisa NH3-N dilakukan dengan metode kjeldahl. S edangkan untuk analisa kadar NO2-NO3 hal yang
3. Hasil dan Pembahasan
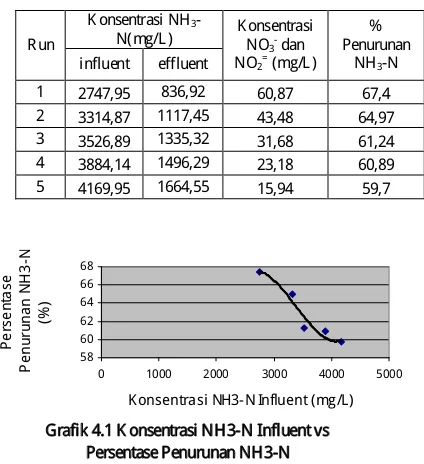
T abel 4.1 K adar ammonia awal dan akhir serta konsentrasi nitrat-nitrit pada sample
K onsentrasi NH3
-Grafik 4.1 K onsentrasi NH 3-N Influent vs Persentase Penurunan NH 3-N
influent semakin tidak efektif. Hal ini dikarenakan konsentrasi NH3-N influent terlalu pekat sehingga mikroba
(lumpur aktif) mencapai kondisi jenuhnya, dan tidak dapat lagi menguraikan. NH3-N yang merupakan nutrient bagi
mikroba jumlahnya tidak boleh terlalu banyak karena jika terlalu banyak akan mengganggu aktivitas mikroba dalam menguraikan ammonia.
Grafi k 4.2 K onsentrasi NH3-N Infl uent vs
K onsentrasi NO3 & NO2
K onversi ammonia menjadi N2 melalui 2 tahap, yaitu : 1. nitrifikasi aerobik dimana NH4
dengan O2 sebagai penerima elektron
2. denitrifikasi anoksik dimana NO2 S emakin sedikitnya konsentrasi NO2
dan NO3 -
yag terdapat dalam effluent berarti semakin banyak yang terkonversi menjadi N2. NO2
K onsentrasi NH3-N dalam influent berbanding terbalik dengan persentase penurunan NH3-N dimana semakin
semakin turun. Persentase penurunan NH3-N paling tinggi yaitu 67,33 % diperoleh pada konsentrasi NH3-N influent
paling rendah yaitu 2747,95 mg/L . S edang persentase penurunan NH3-N paling rendah yaitu 57,17 % diperoleh pada
konsentrasi NH3-N influent paling tinggi yaitu 4690,02 mg/L .
K onsentrasi NO2
-dan NO3 -
dalam effluent cenderung semakin turun seiring dengan semakin besarnya konsentrasi NH3-N influent. K onsentrasi NO2 diperoleh saat konsentrasi influent NH3-N paling rendah yaitu 2747,95 mg/L .
K ami menyarankan penelitian ini perlu ditindaklanjuti dengan menaikkan konsentrasi microalga-lumpur aktif yang digunakan di dalam pengolahan limbah untuk mendapatkan kondisi optimumnya dan mendapatkan persentase penurunan NH3-N yang lebih baik.
Ucapan T erima K asih
1. B apak Ir. A bdullah, MS , selaku ketua J urusan T eknik K imia Universitas D iponegoro. 2. B apak Ir. Indro S umantri, ME ng., selaku dosen Pembimbing.
3. B apak Ir. Herry S antosa selaku K oordinator penelitian.
4. B apak Untung selaku L aboran L aboratorium Pengolahan L imbah. 5. B apak Murdiono selaku L aboran L aboraturium Penelitian. 6. T eman – teman angkatan 2005.
7. S emua pihak yang telah membantu hingga penelitian ini dapat terselesaikan sampai dengan tersusunnya laporan penelitian ini.
D aftar Pustaka
A nonimus, 1988, B iotechnology and D evelopment, UNE S C O, T echnical C entre for A gricultural and R ural C ooperation (C T A ), Netherland.
A nderson, I, C ,, and J , S , L evine, 1986, R elative rates of nitric oxide and nitrous oxide production by nitrifiers, denitrifiers, and nitrate respirers, A ppl, E nviron, Microbiol, 51 :938-945.
B agchi, T ,P, 1993, T aguchi Methods E xplained, Practical Steps to R obust D esign, Prentice-Hall of India Private L td,, New D elhi-110001.
B lackmer, A , M,, J , M, B remner, and E , L , S chmidt, 1980, Production of nitrous oxide by ammonia-oxidizing chemoautotrophic micro- organisms in soil, A ppl, E nviron, Microbiol, 40:1060-1066.
B ock, E ,, I, S chmidt, R , S tüven, and D , Z art, 1995, Nitrogen loss caused by denitrifying Nitrosomonas cells using ammonium or hydrogen as electron donors and nitrite as electron acceptor, A rch, Microbiol, 163 :16-20. C oombs, J , and Hall, D ,O, 1982, T echniques in B ioproductivity and Photo-synthesis, Pergamon Press L td, Oxford. D anks, S ,M,, E vans, E ,H, and W hittaker, P,A , 1983, Photosynthetic S ystems, S tructure, F unction and A ssembly,
J ohn W iley and S ons L td, C hicester.
Gernaey, K ,, L , V erschuere, L , L uyten, and W , V erstraete, 1997, F ast and sensitive acute toxicity detection with an enrichment nitrifying culture, W ater E nviron, R es, 69:1163-1169.
Goreau, T , J ,, W , A , K aplan, S , C , W ofsy, M, B , McE lroy, F , W , V alois, and S , W , W atson, 1980, Production of NO2 and N2O by nitrifying bacteria at reduced concentrations of oxygen, A ppl, E nviron, Microbiol,
40:526-532. discovered in a denitrifying fluidized bed reactor, F E MS Microbiol, E col, 16:177-184.
Muller, E , B ,, A , H, S touthamer, and H, W , van V erseveld, 1995, S imultaneous NH3 oxidation and N2 production at
reduced O2 tensions by sewage sludge subcultured with chemolithotrophic medium, B iodegradation
Polle, J ,, S , K anakagiri, J ,R , B enemann, A , Melis, 1999, Maximizing Photosynthetic E ficiencies and Hydrogen Production by microalgal cultures, Proceedings of the 1999 U,S D OE Hydrogen Prog, Review NRE L /C P -570-26938.
Poth, M, 1986, D initrogen production from nitrite by a Nitrosomonas isolate, A ppl, E nviron, Microbiol, 51:957-959. S chmidt, I,, 2002, A naerobic Metabolism of Nitrosomonas and New A pplication in W astewater.
i,schmidt@ T NW ,T UD elft,NL
S chmidt, I,, and E , B ock, 1997, A naerobic ammonia oxidation with nitrogen dioxide by Nitrosomonas eutropha, A rch, Microbiol, 167:106-111.
S trous, M,, E , van Gerven, J , G, K uenen, and M, J etten, 1997, E ffects of aerobic and microaerobic conditions on anaerobic ammonium-oxidizing ( A nammox) sludge, A ppl, E nviron, Microbiol, 63:2446-2448.
S trous, M,, E , van Gerven, P, Z heng, J , G, K uenen, and M, S , M, J etten, 1997, A mmonium removal from concentrated waste streams with the anaerobic ammonium oxidation (A nammox) process in different reactor configurations, W ater R es, 31:1955-1962.
S tein, J ,R ,, 1973, Handbook of Phycological Methods, C ulture Methods and Growth Measurement, C ambridge Univ, Press.
S urk-K ey, Y ,& N, T oshiuki, 2002, A ctivity of C hlorella vulgaris associated by E scherichia coli W 3110 on removal of T otal Organic C arbon in C ontinuous R iver W ater F low S ystem, Algae vol, 17(3): 195-199.
V an D ongen, U, 2002, T he C ombined S haron A nammox Process, udo,vandongen @ S T M,T UD elft,NL .