1
SINTESIS DAN UJI TOKSISITAS SENYAWA ANALOG KALKON TURUNAN 3’,4’- DIMETOKSI ASETOFENON
D.W.P.Sari1, A.Zamri, Yuharmen2
1Mahasiswa Program Studi S1 Kimia
2Bidang Kimia Organik Jurusan Kimia Fakultas Matematika dan Ilmu Pengetahuan Alam
Binawidya Pekanbaru, 28293, Indonesia Mitha2392@gmail.com
ABSTRACT
Chalcone is one of secondary metabolites included into the class of flavonoids that are known to have biological activities. Chalcone can be used as an intermediate for synthesizing heterocyclic compounds, such as flavones, flavanols, flavanones, and others that also have biological activities. Chalcone generally can be synthesis by Claisen-Schmidth condensation from aldehide and ketone aromatic using acid or base catalyst. Chalcone compound 3,4’- dimetoxy acetophenone derivative was synthesis using the microwave with a base catalyst (KOH). The yield obtained from each of chalcone analogs are (E)-1-(3,4-dimetoxy phenil)-3-(4-hidroxy phenil)prop-2-en-1-one (M1) with value 36,5%, (E)-1-(3,4-dimetoxy phenil)-3-(3-hidroxy phenil)prop-2-en-1- one (M2) with value 93,3% and (E)-1-(3,4-dimetoxy phenil)-3-(2-hidroxy phenil)prop- 2-en-1-one (M3) with value 57,3%. The characterization of all compounds have been tested using UV-Vis. IR, 1H NMR and MS. The toxicity test was done by Brine Shrimp Lethality Test (BSLT) method using Artemia salina Leach. The compound of M1, M2
and M3 showed that value LC50 in sequence are 41,687 µg/mL; 253,513 µg/mL and 29,512 µg/mL. Two analogs of chalcone compounds are positive as anticancer proved by LC50 values <200 µg/mL and one compound is negative as anticancer proved by LC50 value > 200 µg/mL.
Keywords : chalcone , Brine Shrimp Lethality Test (BSLT) ABSTRAK
Kalkon merupakan salah satu metabolit sekunder yang termasuk ke dalam golongan flavonoid yang dikenal memiliki aktivitas biologis. Kalkon dapat digunakan sebagai senyawa antara untuk mensintesis senyawa-senyawa heterosiklik, seperti flavon, flavanol, flavanon dan lain sebagainya yang juga memiliki aktivitas biologis. Kalkon umumnya dapat disintesis melalui kondensasi Claisen-Schmidt dari suatu aldehid dan keton aromatik menggunakan katalis asam atau basa. Senyawa kalkon turunan 3,4’- dimetoksiasetofenon disintesis menggunakan microwave dengan katalis basa (KOH).
Rendemen dari masing-masing senyawa kalkon (E)-1-(3,4-dimetoksi fenil)-3-(4- hidroksi fenil)prop-2-en-1-on (M1) sebesar 36,5%, (E)-1-(3,4-dimetoksi fenil)-3-(3-
2
hidroksi fenil)prop-2-en-1-on (M2) sebesar 93,3% dan (E)-1-(3,4-dimetoksi fenil)-3-(2- hidroksi fenil)prop-2-en-1-on (M3) sebesar 57,3%. Karakterisasi senyawa dianalisis menggunakan spektroskopi UV-Vis, IR, 1H NMR dan MS. Uji toksisitas senyawa kalkon menggunakan metode Brine Shrimp Lethality Test (BSLT) terhadap larva Artemia salina Leach. Senyawa M1, M2 dan M3 menunjukkan nilai LC50 secara berturut- turut yaitu, 41,687 µg/mL; 253,513 µg/mL dan 29,512 µg/mL. Dua senyawa analog kalkon positif berpotensi sebagai antikanker terbukti dengan nilai LC50 < 200 µg/mL dan satu senyawa tidak berpotensi sebagai antikanker karena nilai LC50 > 200 µg/mL.
Keywords : kalkon, Brine Shrimp Lethality Test (BSLT) PENDAHULUAN
Kalkon merupakan salah satu hasil metabolit sekunder golongan flavonoid yang mempunyai berbagai aktivitas biologis seperti antibakteri (Usman et al.,), antidiabetes (Enoki, 2007), antitumor, sitotoksik, analgesik, antidemam dan anti-inflamasi (Kim et al., 2007). Selain itu, senyawa kalkon juga dikenal sebagai senyawa antara untuk mensintesis senyawa-senyawa heterosiklik, seperti flavon, flavanol, flavanon dan lain sebagainya yang juga mempunyai aktivitas biologis (Tiwari et al., 2010). Senyawa kalkon terdapat pada berbagai jenis tumbuhan di alam yang berperan sebagai senyawa prekursor untuk biosintesis flavonoid dan isoflavonoid (Patil et al., 2009).
Meskipun kalkon tersebar di berbagai famili tanaman, namun jumlahnya terbatas dibanding dengan senyawa flavonoid lain karena senyawa ini termasuk dalam kategori minor flavonoid dan presentasenya dalam tumbuhan juga kecil serta variasi strukturnya relatif sedikit (Harborne, 1994). Kondisi ini tentu sulit diperoleh melalui isolasi dari tumbuhan, disamping kurang menguntungkan dari segi biaya juga membutuhkan banyak bahan kimia yang mungkin berbahaya bagi lingkungan. Karena itu, sintesis merupakan jalan keluar dari pemecahan masalah tersebut.
Secara umum senyawa turunan kalkon dapat disintesis melalui kondensasi aldol atau lebih spesifik melalui kondensasi Claisen-Schmidt dari suatu keton aromatik dengan aldehid aromatik. Kondensasi aldol merupakan salah satu metoda untuk pembentukan ikatan karbon-karbon dan dikenal ramah lingkungan karena tidak banyak menggunakan bahan kimia yang berbahaya. Sintesis kalkon telah banyak dikembangkan dan diteliti saat ini. Oleh karena itu, dilakukan penelitian turunan kalkon dengan metode iradiasi microwave. Iradiasi microwave lebih efisien sebagai suatu teknik non- konvensional untuk sintesis organik. Karena, iradiasi microwave tahan terhadap suhu sangat tinggi, memiliki kontrol yang baik terhadap energi dalam suatu reaksi, hasil yang didapat lebih tinggi dan sintesisnya cepat terhadap senyawa organik (Ahmed, 2011).
Aktivitas biologis kalkon dipengaruhi oleh gugus karbonil α, β-tak jenuh dan subtituen yang terikat pada kedua cincin aromatik (Kamble et al, 2011). Oleh karena itu, variasi subtituen pada kedua cincin aromatik akan menghasilkan kalkon dengan struktur yang beragam. Kalkon dengan variasi struktur yang luas hanya dapat diperoleh melalui sintesis secara kombinatorial. Untuk maksud tersebut, grup riset organik sintesis telah mencanangkan program sintesis 100 molekul kalkon.
Pada penelitian ini hanya dilakukan sintesis tiga molekul kalkon dengan
menggunakan bahan baku aldehid aromatik yaitu senyawa 2-hidroksibenzaldehid,
3
3-hidroksibenzaldehid dan 4-hidroksibenzaldehid dengan suatu turunan keton aromatik yaitu 3,4’-dimetoksiasetofenon.
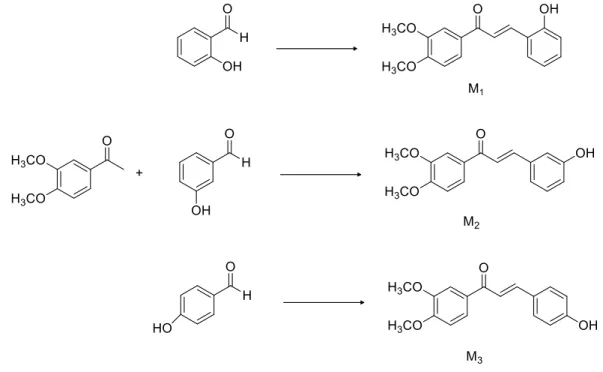
M1 : (E)-1-(3,4-dimetoksi fenil)-3-(2-hidroksi fenil)prop-2-en-1-on M2 : (E)-1-(3,4-dimetoksi fenil)-3-(3-hidroksi fenil)prop-2-en-1-on M3 : (E)-1-(3,4-dimetoksi fenil)-3-(4-hidroksi fenil)prop-2-en- 1-on
Gambar 1. Sintesis Analog Kalkon Senyawa M1, M2 Dan M3
METODE PENELITIAN
Sintesis senyawa analog kalkon dilakukan dalam satu tahap reaksi melalui kondensasi Claisen-Schimdt dengan menggunakan senyawa awal turunan benzaldehida dan turunan asetofenon yakni 3,4-dimetoksiasetofenon dengan menggunakan katalis basa (KOH).
a. Sintesis senyawa analog kalkon (M1, M2 dan M3)
Dicampurkan senyawa 3,4-dimetoksiasetofenon (5 mmol), turunan benzaldehid (5 mmol), 3 ml etanol absolut, dan 5 ml kalium hidroksida (KOH) 6N ke dalam labu bulat yang telah dilengkapi magnet stirer. Campuran tersebut diiradiasi microwave selama 3-12 menit. Produk ditambahkan aquades dingin sebanyak 15-20 mL dan setetes demi setetes larutan HCl 3N hingga produk menjadi netral. Endapan yang dihasilkan selanjutnya disaring dan dicuci dengan n-heksana dan akuades dingin, kemudian senyawa yang didapat diuji kemurniannya dengan uji KLT, jika senyawa yang didapat belum murni maka dilakukan rekristalisasi dengan pelarut yang sesuai.
4 b. Uji aktivitas toksisitas
Sampel sebanyak 20 mg dilarutkan dalam 2 mL metanol, kemudian dari larutan induk dibuat konsentrasi yang berbeda 1000 µg/mL, 100 µg/mL, 10 µg/mL, 1 µg/mL, 0,1 µg/mL, 0,01 µg/Ml. Sampel dipipet ke dalam masing-masing vial sebanyak 0,5 mL, lalu pelarut diuapkan hingga mengering. Selanjutnya, ke dalam masing-masing vial ditambahkan 50 µL DMSO dan air laut. Sebanyak 10 ekor larva udang yang sudah disiapkan dimasukkan ke dalam vial tersebut dan ditambah air laut hingga batas kalibrasi 5 mL. Tingkat toksisitas diukur dengan cara menghitung jumlah larva udang yang masih hidup dalam selang waktu 24 jam. Pengujian dilakukan sebanyak tiga kali pengulangan dengan perlakuan yang sama untuk masing-masing konsentrasi. Data yang diperoleh dianalisis untuk menentukan nilai LC50 dengan metoda kurva menggunakan Tabel analisis probit (Harefa, 1987).
HASIL DAN PEMBAHASAN
a. (E)-1-(3,4-dimetoksi fenil)-3-(2-hidroksi fenil)prop-2-en-1-on.
Senyawa M1 (0,5182 g; 36,5 %), Orange, titik leleh 153-1550C, Rf = 0,5 (heksana/EtOAc = 2:1); IR (cm-1) : 3040 (OH); 1598 (C=O); 1356 (C=C); 1150 (Ar- OH); 1240 (C-O pada OCH3); 1H NMR (500 MHz) (δ) : 6,87 ppm (d, 1H, J = 8 Hz), 6,97 ppm (t, 1H, J = 7 Hz), 6,97 ppm (t, 1H, J = 7 Hz), 7,60 ppm (d, 1H, J = 7,5 Hz), 7,69 ppm (d, 1H, J = 16 Hz), 8,12 ppm (d, 1H, J = 16 Hz), 7,63 ppm (s, 1H), 3,97 ppm (s, 3H, -OCH3), 3,977 ppm (s, 3H, -OCH3), 6,93 ppm (d, 1H) J = 8 Hz), 7,68 ppm (d, 1H, J = 9,5 Hz); Massa molekul dihitung sebagai C17H16O4 [M+H]- : 284,0963 m/z; UV (MeOH) : λmaks (nm) : 205, 302, 358; HPLC λ1 205 nm, tR : 11,5 menit, λ2 305 nm, tR : 11,5 menit; LC50 41,687 µg/mL.
b. M2 : (E)-1-(3,4-dimetoksi fenil)-3-(3-hidroksi fenil)prop-2-en-1-on
Senyawa M2 (2,7145 g; 95,54 %), kuning, titik leleh 166-1680C, Rf = 0,4 heksana/EtOAc = 2:1); IR (cm-1) : 2985 (OH); 1601 (C=O); 1356 (C=C); 1120 (Ar- OH); 1246 (C-O pada OCH3); 1H NMR (500 MHz) (δ) : 7,28 ppm (s, 1H), 6,89 ppm (dd, 1H, J = 8 Hz), 7,14 ppm (t, 1H, J = 8 Hz), 7,05 ppm (d, 1H, J = 8,5 Hz), 7,65 ppm (d, 1H, J = 16 Hz), 7,70 ppm (d, 1H, J = 15,5 Hz), 7,63 ppm (d, 1H, J = 1,5 Hz), 3,90 ppm (s, 3H, -OCH3), 3,88 ppm (s, 3H, -OCH3), 6,98 ppm (td, 1H, J = 5,5 Hz), 7,78 (dd, 1H, Ja = 8,5 Hz, Jb = 2 Hz); Massa molekul dihitung sebagai C17H16O4 [M+H]+ : 284,1131m/z; UV (MeOH) : λmaks (nm) : 219, 308, 341; HPLC λ1 280 nm, tR : 7,8 menit λ2 337 nm, tR : 7,8 menit; LC50 253,513 µg/mL.
c. (E)-1-(3,4-dimetoksi fenil)-3-(4-hidroksi fenil)prop-2-en- 1-on
Senyawa M3 (0,4125 g; 57,3 %), kuning, titik leleh 171-173 0C, Rf = 0,4 heksana/EtOAc = 2:1); IR (cm-1) : 3090 (O-H); 1631 (C=O); 1513 (C=C); 1022 (Ar- OH); 1248 (C-O pada OCH3); 1H NMR (500 MHz) (δ) : 7,68 ppm (d, 1H, J = 9 Hz), 6,91 ppm (d, 1H, J = 8,5 Hz), 6,91 ppm (d, 1H, J = 8,5 Hz), 7,68 ppm (d, 1H, J = 9 Hz), 7,69 ppm (d, 1H, J = 16 Hz), 7,72 ppm (d, 1H, J = 16 Hz), 7,65 ppm (d, 1H, J = 2 Hz), 3,90 ppm (s, 3H, -OCH3), 3,89 ppm (s, 3H, -OCH3), 7,06 ppm (d, 1H, J = 8,5 Hz), 7,82 ppm (dd, 1H, Ja = 8,25 Hz, Jb = 2 Hz); Massa molekul dihitung sebagai C17H16O4
5
[M+H]+ : 284,1140 m/z; UV (MeOH) : λmaks (nm) : 205, 238, 356; λ1 205 nm, tR : 10,5 menit λ2 305 nm, tR : 10,5 menit; LC50 29,512 µg/mL.
d. Sintesis senyawa M1, M2 dan M3
Senyawa murni ketiga senyawa yang dihasilkan dianalisis menggunakan HPLC.
Kromatogram yang diperoleh menunjukkan satu puncak pada tR = 11,5 menit senyawa M1, tR = 7,8 menit senyawa M2 dan tR = 10,5 menit senyawa M3 (λ 205 nm, 305nm, 280 nm dan 337nm ). Hal ini menunjukkan ketiga senyawa hasil sintesis murni.
Spektrum UV senyawa M1, M2 dan M3 masing-masing memperlihatkan adanya serapan maksimum pada λ 205-219 nm yang merupakan ikatan rangkap pada cincin benzene, λ238-308 nm merupakan ikatan rangkap pada cincin aromatik A yang terkonjugasi dengan gugus karbonil dan λ 341-358 nm yang merupakan ikatan rangkap pada cincin aromatic B.
Spektrum IR senyawa M1 memperlihatkan adanya serapan pada bilangan gelombang 3040 cm-1 yang menunjukkan adanya gugus OH ; 1598 cm-1 menunjukkan adanya gugus C=O; 1356,98 cm-1 menunjukkan adanya gugus C=C aromatik; 1150,59 cm-1 menunjukkan adanya gugus C-O pada OH; dan 1240,28 cm-1 menunjukkan adanya gugus metoksi (Ar-OCH3). Spektrum IR senyawa M2 memperlihatkan adanya serapan pada bilangan gelombang 2985,94 cm-1 yang menunjukkan adanya gugus OH ; 1601,95 cm-1 menunjukkan adanya gugus C=O; 1356,98 cm-1 menunjukkan adanya gugus C=C aromatik; 1120,69 cm-1 menunjukkan adanya gugus C-O pada OH; dan 1246,07 cm-1 menunjukkan adanya gugus metoksi (Ar-OCH3). Spektrum IR senyawa M3
memperlihatkan adanya serapan pada bilangan gelombang 3090,10 cm-1 yang menunjukkan adanya gugus OH ; 1631,85 cm-1 menunjukkan adanya gugus C=O; 1464 cm-1 menunjukkan adanya gugus C=C aromatik; 1022,32 cm-1 menunjukkan adanya gugus C-O pada OH; dan 1248 cm-1 menunjukkan adanya gugus metoksi (Ar-OCH3).
Spektrum 1H NMR senyawa M1 menunjukkan adanya pergeseran kimia pada δ 7,69 ppm (d, 1H, J= 16 Hz), 8,12 ppm (d, 1H, J= 16 Hz) berturut-turut memperlihatkan proton H pada C-α dan C-β. Dari harga tetapan kopling (J) pada C-α dan C-β dapat diperkirakan bahwa proton pada ikatan rangkap ini mempunyai konfigurasi trans.
Proton pada gugus metoksi ditunjukkan pada pergeseran kimia δ 3,97 ppm (s, 3H) posisi atom C-3’ dan C-4’. Pergeseran kimia pada δ 6,97 ppm (t, 1H, J= 7Hz) menunjukkan proton H pada atom C-4 dan C-5. Spektrum 1H NMR senyawa M2
menunjukkan adanya pergeseran kimia pada δ 7,65 ppm (d, 1H, J= 16 Hz), 7,70 ppm (d, 1H, J= 15,5 Hz) berturut-turut memperlihatkan proton H pada C-α dan C-β. Dari harga tetapan kopling (J) pada C-α dan C-β dapat diperkirakan bahwa proton pada ikatan rangkap ini mempunyai konfigurasi trans. Pergeseran kimia pada δ 6,89 ppm menunjukkan proton H pada posisi C-4 dengan puncak doublet of doublet. Puncak ini karena adanya interaksi antara proton H pada C-4 dengan proton h pada C-2. Proton pada gugus metoksi ditunjukkan pada pergeseran kimia δ 3,90 ppm (s, 3H) dan δ 3,88 ppm (s, 3H) posisi atom C-3’ dan C-4’. Pergeseran kimia pada δ 7,78 ppm (dd, 1H) Ja
= 8,5 Hz merupakan interaksi proton C-6’ dengan C-5’, Jb= 2 Hz merupakan interaksi proton C-6’ dengan C-2’. Spektrum 1H NMR senyawa M3 menunjukkan adanya pergeseran kimia pada δ 7,69 ppm (d, 1H, J= 16 Hz), 7,72 ppm (d, 1H, J= 15,5 Hz) berturut-turut memperlihatkan proton H pada C-α dan C-β. Dari harga tetapan kopling (J) pada C-α dan C-β dapat diperkirakan bahwa proton pada ikatan rangkap ini
6
mempunyai konfigurasi trans. Proton pada gugus metoksi ditunjukkan pada pergeseran kimia δ 3,90 ppm (s, 3H) dan δ 3,89 ppm (s, 3H) posisi atom C-3’ dan C-4’.
Pergeseran kimia pada δ 7,82 ppm (dd, 1H) Ja = 8,5 Hz merupakan interaksi proton C- 6’ dengan C-5’, Jb= 2 Hz merupakan interaksi proton C-6’ dengan C-2’. Pergeseran kimia pada δ 6,91 ppm dan 7,68 ppm merupakan proton H yang saling simetris pada atom C-3/C-5 dan C-2/C-6 dengan puncak masing-masing doublet.
Berat molekul M1 ditunjukkan oleh spektrum massa yang dihitung sebagai C17H16O4 dengan puncak molekul m/z 284,0963 [M+H]- dan berat molekul M1 yang dihitung secara teoritis adalah 284,0970, selisih massa molekul tersebut 0,0007. Berat molekul M2 ditunjukkan oleh spektrum massa yang dihitung sebagai C17H16O4 dengan puncak molekul m/z 284,1131 [M+H]+ dan berat molekul M1 yang dihitung secara teoritis adalah 284,1127, selisih massa molekul tersebut 0,0004. Berat molekul M3
ditunjukkan oleh spektrum massa yang dihitung sebagai C17H16O4 dengan puncak molekul m/z 284,1140 [M+H]+ dan berat molekul M1 yang dihitung secara teoritis adalah 284,1127, selisih massa molekul tersebut 0,0013. Selisih massa ketiga senyawa kalkon dari spektrum massa dengan perhitungan menunjukkan perbedaan yang kecil dan dapat dikatakan bahwaketiga senyawa kalkon tersebut murni.
e. Uji toksisitas senyawa M1, M2 dan M3
Uji toksisitas dilakukan terhadap ketiga senyawa analog kalkon (M1, M2 dan M3) dengan konsentrasi 10, 100 dan 1000 µg/mL. Perbedaan konsentrasi ini dimaksudkan untuk mengetahui tingkat aktivitas masing-masing senyawa terhadap kematian larva Artemia Salina Leach dan angka tersebut memiliki range yang cukup luas sehingga memudahkan untuk memperkirakan konsentrasi LC50.
Hasil uji yang diperoleh senyawa M1 memiliki nilai LC50 sebesar 41,68 µg/mL;
senyawa M2 253,51 µg/mL dan senyawa M3 29,512 µg/mL. Senyawa M1 dan M3
menunjukkan tingkat toksisitas yang lebih tinggi dari pada senyawa M2, hal ini dikarenakan adanya gugus hidroksi yang terletak pada posisi orto (M1) dan para (M2).
Efek mesomeri positif gugus hidroksi pada posisi orto dan para akan bergerak cepat ke sistem karbonil sehingga meningkatkan aktivitas toksisitas senyawa dibandingkan dengan efek mesomeri gugus hidroksi pada posisi meta.. Sementara senyawa M2 tidak menunjukkan aktif terhadap aktivitas toksisitas karena memiliki nilai LC50 >200 µg/mL.
Hal ini disebabkan oleh gugus hidroksi terletak pada posisi meta sehingga efek mesomeri positif gugus hidroksi tidak berpengaruh pada gugus karbonil.
KESIMPULAN
Berdasarkan hasil penelitian yag telah dilakukan, maka dapat diambil kesimpulan bahwa senyawa analog kalkon M1, M2 dan M3 diperoleh melalui reaksi kondensasi aldol Claisen-Schmidt menggunakan katalis basa (KOH) dengan metode microwave.
Rendemen yang dihasilkan yaitu 36,5% untuk senyawa M1, 93,3% untuk senyawa M2
dan 57,3% untuk senyawa M3. Hasil karakterisasi menggunakan spektroskopi UV, IR, 1H NMR dan MS menunjukkan bahwa senyawa yang diperoleh dari hasil penelitian adalah murni dan merupakan senyawa kalkon dengan struktur sesuai dengan yang diharapkan. Ketiga senyawa memiliki toksisitas dengan nilai LC50 pada senyawa M1, M2 dan M3 berturut-turut adalah 41,68; 253,51 dan 29,512 µg/ml.
7
UCAPAN TERIMA KASIH
Penulis mengucapkan terima kasih kepada pembimbing penelitian Bapak Prof.Dr.Adel Zamri MS. DEA dan Drs.Yuharmen M.Si beserta seluruh pihak yang telah mambantu sehingga penelitian ini dapat diselesaikan.
DAFTAR PUSTAKA
Ahmed, R.M., Sastry, G.V., Bano, N., Ravichandra, S., and Raghavendra, M. 2011.
Synthesis and Cytotoxic, Antioxidant Activities of New Chalcone Derivatives.
Rasayan Journal Chem. 4(2): 289-294.
Enoki, T, Antidiabetic Activities of Chalcones Isolated From a Japanese Herb Angelica Keiskei. http://pubs.acs.org/doi/pdf/10.1021/jf0707209 (accesed date: 10 Mei 2007).
Harborne, J.B. 1987. Metoda Fitokimia: Penentuan Cara Modern Menganalisis Tumbuhan. Terjemahan Kosasih Padmawinata dan Iwang Sudiro. ITB, Bandung.
Harborne, J.B. 1994. The Flavonoids Advances In Research Since 1986. Chapman &
Hall: London.
Harefa, F. 1997. Pembudidayaan Artemia salina untuk Pakan Udang dan Ikan. Penerbit Swadaya, Jakarta.
Kamble, S., Torane, R., Mundhe, K dan Salvekar, V. 2011. Evolution Of Free Radical Scavenging Potential Of Embelia Basal. J. Chem Pharm. Res., 3(2): 465-471 Kim, Y.H., Kim, J., Park, H., dan Kim, H.P. 2007. Anti-inflammatory Activity of the
Synthetic Chalcone Derivatives: Inhibition of Inducible Nitric Oxide Synthase- Catalyzed Nitric Oxide Production from Lipopolysaccharide-Treated RAW 264.7 Cells. Biological and Pharmaceutical Bulletin. 30(8): 1450-1455.
Patil, C.B., Mahajan, S.K., dan Katti, S.A. 2009. Chalcone: A Versatile Molecule.
Journal of Pharmaceutical Science and Research. 1(3): 11-12.
Tiwari, B., Pratapwwar, A.S., Tapas, A.R., Butle, S.R., dan Vatkar, B.S. 2010.
Synthesis and Antimicrobial activity of some chalcone derivates. International Journal of ChemTech Research. 1(2): 499-503.
Usman, H., Hakim, E.H., Achmad, S.A., Harlim, T., Jalaluddin, M.N., Syah, Y.M., Juliawati, L.D., Makmur, L., dan Katajima, M. 2005. 2’,4’-dihidroksi-3’,5’,6’- Trimetoksi Calkon suatu Senyawa Antitumor dari Kulit Batang Tumbuhan Cryptocarya costata (Lauraceae). Jurnal Matematika dan Sains.10. 97-100.