Jurnal Ilmiah Farmako Bahari
Journal Homepage : https://journal.uniga.ac.id/index.php/JFB
ANTIOXIDANT ACTIVITY OF PINING (
Hornstedtia alliacea
)
BY USING DPPH METHOD
Firman Gustaman, Winda Trisna Wulandari, Vera Nurviana,
Keni Idacahyati
STIKes Bakti Tunas Husada, Jl. Cilolohan No. 36 Tasikmalaya
Korespondensi: Firman Gustaman (firmangustaman@stikes-bth.ac.id)
ARTICLE HISTORY
Received: 19 December 2019 Revised: 27 January 2020 Accepted: 31 January 2020
Abstract
Indonesia is an archipelagic country located in the equatorial zone and famous for having a diversity of plant species, but not all of this potential can be utilized as industrial materials, especially medicinal plants. Pining (Hornstedtia alliacea) is a plant that is still underutilized in the health sector due to the lack of information about the phytochemicals of the plant. In this study, phytochemical screening of pining was done to determine the content of alkaloids, triterpenoids/steroids, flavonoids, tannins, and saponins as well as testing the antioxidant activity by using DPPH method. The result of phytochemical screening shows that pining has flavonoids, quinones, monoterpenes, and sesquiterpenes in ethanol, ethyl acetate and n-hexane extracts. In antioxidant testing, ethyl acetate extract has the most powerful antioxidant potential with an IC50 value of 23.43 ppm which is classified as a strong antioxidant.
Key words: antioxidant, flavonoids, Pining (Hornstedtia alliacea)
AKTIVITAS ANTIOKSIDAN BUAH PINING (
Hornstedtia alliacea
)
DENGAN MENGGUNAKAN METODE DPPH
Abstrak
Indonesia merupakan negara kepulauan yang berada pada zona khatulistiwa dan terkenal memiliki keanekaragaman jenis tanaman, tetapi potensi ini belum semuanya dapat dimanfaatkan sebagai bahan industri khususnya tanaman berkhasiat obat. Buah pining (Hornstedtia alliacea) merupakan tanaman yang masih sedikit dimanfaatkan dalam bidang kesehatan dikarenakan masih minimnya informasi mengenai fitokimia dari tanaman tersebut. Skrining fitokimia tanaman buah pining (Hornstedtia alliacea) dilakukan untuk mengetahui kandungan senyawa alkaloid, triterpenoid/steroid, flavonoid, tanin, dan saponin, serta pengujian aktivitas antioksidan menggunakan metode DPPH. Hasil skrining fitokimia yang diperoleh menunjukkan hasil positif untuk flavonoid, kuinon, monoterpen dan seskuiterpen pada ekstrak etanol, etil asetat dan n-heksana. Pada pengujian antioksidan, ekstrak etil asetat memiliki potensi antioksidan yang paling kuat dengan nilai IC50 sebesar 23,43 ppm yang tergolong antioksidan kuat.
Jurnal Ilmiah Farmako Bahari Firman Gustaman Vol. 11; No. 1; Januari 2020
Halaman 67-74
Pendahuluan
Radikal bebas merupakan molekul yang sangat reaktif yang memiliki elektron tidak berpasangan dalam orbital terluarnya.1 Radikal bebas dapat terbentuk di dalam tubuh akibat proses produk samping metabolisme. Penyakit degeneratif seperti diabetes mellitus, hipertensi, stoke, peyakit autoimun hingga kanker dapat disebabkan oleh radikal bebas.1
Senyawa yang dapat memperlambat terjadinya oksidasi sehingga memperlambat terjadinya penyakit kronik dan melindungi tubuh dari serangan radikal bebas adalah antioksidan. Antioksidan juga mampu memperlambat terjadinya penyakit kronik yang disebabkan penurunan spesies oksigen reaktif (ROS) terutama radikal hidroksil dan radikal superoksida.2,3 Indonesia mempunyai kekayaan alam yang memiliki berbagai jenis tumbuhan yang berkhasiat bagai obat, tetapi potensi ini belum semuanya dapat dimanfaatkan.4 Secara turun-temurun masyarakat Indonesia telah memanfaatkan berbagai jenis tanaman sebagai bahan obat tradisional untuk pencegahan maupun pengobatan terhadap berbagai macam penyakit.5 Buah pining
(Hornstedtia alliacea) mengandung senyawa bahan alam golongan Flavonoid seperti Flavones, Flavonones, Flavonol, Flavanonols, anidins Anthocy, Aurones, Flavanoid, Chromones Furan, Biflavones, Isofavones, Isoflavanones, Chaocones, Xanthone dan Dihydrocalcones yang dapat bertindak sebagai Antioksidan.6 (Hornstedtia alliacea) adalah sejenis tumbuhan penghasil buah anggota suku jahe-jahean (Zingiberaceae).7
Rimpang Zingiberaceae merupakan aromatik kuat dan pada umumnya mengandung minyak atsiri yang telah dilaporkan mempunyai sifat antioksidan, antiinflamasi dan antimicrobial.8 Zingiberaceae juga dapat digunakan pada penyakit kronis seperti osteoarthritis, rheumatoid artritis, dan depresi.9
Metode DPPH (1,1-difenil-2-pikrilhidrazil) dipilih sebagai pengujian antioksdian . Metode ini merupakan metode yang konvensional, sederhana, cepat mudah, reliabel dan praktis untuk melakukan skrinning aktivitas penangkap radikal beberapa senyawa.1
Metode
Alat
Alat yang digunakan dalam penelitian ini adalah rotary evaporator timbangan analitik, mesh, oven, gelas ukur, , vortex mixer, , rotary evaporator, dan spektrofotometer UV-Vis, , blender, desikator, gelas kimia, mikropipet, labu Erlenmeyer, magnetik stirrer.
Bahan
Bahan yang digunakan dalam peneltian ini adalah etanol, etil asetat, n-heksana reagen mayer, reagen wagner dan (DPPH) 1,1-difenil-2-pikrilhidrazil. Sampel yang digunakan yaitu buah pining yang diambil dari kecamatan Cikatomas kabupaten Tasikmalaya, reagen dragendorff.
Prosedur
Ekstraksi Sampel
Ekstraksi yang dilakukan menggunakan metode maserasi bertingkat dengan 7 sampel serbuk simplisia buah pining. pelarut yang digunakan adalah pelarut dengan kepolaran makin meningkat yaitu n-heksana, etil asetat, dan etanol 70% masing-masing pelarut yang digunakan sebanyak 100mL (1:10). Serbuk simplisia ditimbang 10 g, dimasukkan ke dalam erlenmeyer 250 mL. Maserasi pertama simplisia direndam dengan 100 mL n-heksan selama 24 jam sambil sesekali diaduk
Jurnal Ilmiah Farmako Bahari Firman Gustaman Vol. 11; No. 1; Januari 2020
Halaman 67-74
(setiap 6 jam), setelah 24 jam, residu dipisahkan dari filtrat dan ampas simplisia dikeringkan dengan oven pada suhu 50 ̊C. Setelah residu kering dilakukan dimaserasi kembali selama 24 jam dengan etil asetat 100 mL sambil sesekali diaduk (setiap 6 jam), setelah 24 jam residu dipisahkan dari filtrat, setelah maserasi dengan etil asetat selesai, residu dikeringkan kemudian dimaserasi dengan pelarut etanol 70% dengan prosedur yang sama. Ekstrak yang diperoleh dari etanol 70% dimasukkan ke dalam labu 100 mL dan digenapkan sampai batas ditambahkan dengan etanol 70% lalu ekstrak dituangkan selama 24 jam. Filtrat selanjutnya dilakukan pengujian.
Skrining Fitokimia 1. Pembuatan Pereaksi
a) Pereaksi Mayer
Sebanyak 1,36 g HgCl2 dilarutkan dalam 60 mL akuades. Pada bagian yang lain larutkan pula 5 g KI dalam 10 mL akuades. Kedua larutan ini kemudian dicampur dan diencerkan dengan akuades sampai 100 mL. Reagen ini harus disimpan dalam botol yang berwarna coklat, agar tidak terjadi kontak langsung dengan cahaya.
b) Pereaksi Dragendorff
Sebanyak 8 g KI dilarutkan dalam 20 mL akuades, sedangkan pada bagian yang lain dilarutkan 0,85 g bismut subnitrat dalam 10 mL asam asetat glasial dan 40 mL akuades. Kedua larutan ini kemudian dicampurkan. Larutan disimpan dalam botol berwarna coklat. Dalam penggunaannya, larutan ini diencerkan dengan 2/3 bagian larutan 20 mL asam asetat glasial dalam 100 mL akuades.
c) Pereaksi Wagner
Sebanyak 1,27 g I2 dan 2 g KI dilarutkan dalam 5 mL akuades. Larutan ini kemudian diencerkan dengan akuades hingga 100 mL. Endapan yang terbentuk disaring dan disimpan dalam botol berwarna coklat.
2. Uji Alkaloid
Beberapa mL ekstrak buah pining, ditambahkan dengan 2 mL kloroform dan 2 mL amonia lalu disaring. Filtrat kemudian ditambahkan 3-5 tetes H2SO4 pekat lalu dikocok hingga terbentuk dua lapisan. Lapisan atas dipindahkan ke dalam tiga tabung reaksi masing-masing 2,5 mL. Ketiga larutan ini dianalisis dengan pereaksi Mayer, Dragendorff dan Wagner sebanyak 4-5 tetes. Terbentuknya endapan menunjukkan bahwa sampel tersebut mengandung alkaloid. Reaksi dengan pereaksi Mayer akan terbentuk endapan putih, dengan pereaksi Dragendorff terbentuk endapan merah jingga dan dengan pereaksi wagner terbentuk endapan coklat.10
3. Uji Flavonoid
Beberapa mL ekstrak buah pining, ditambahkan dengan 100 mL air panas, didihkan selama 5 menit, kemudian disaring. Filtrat sebanyak 5 mL ditambahkan 0,05 g serbuk Mg dan 1 mL HCl pekat, kemudian dikocok kuat-kuat. Uji positif ditunjukkan dengan terbentuknya warna merah, kuning atau jingga.10
4. Uji Steroid dan Triterpenoid
Beberapa mL ekstrak buah pining ditambahkan dengan CH3COOH glasial sebanyak 10 tetes dan H2SO4 pekat sebanyak 2 tetes. Larutan dikocok perlahan
Jurnal Ilmiah Farmako Bahari Firman Gustaman Vol. 11; No. 1; Januari 2020
Halaman 67-74
dan dibiarkan selama beberapa menit. Uji positif Steroid jika menghasilkan warna biru atau hijau, sedangkan triterpenoid menghasilkan warna merah atau ungu.10
5. Uji Saponin
Beberapa mL ekstrak buah pining, ditambahkan dengan 10 mL air sambil dikocok selama 1 menit, lalu ditambahkan 2 tetes HCl 1 N. Bila busa yang terbentuk tetap stabil selama kurang lebih 7 menit, maka ekstrak positif mengandung saponin. 10
6. Uji Tanin
Beberapa mL ekstrak buah pining, ditambahkan dengan 10 tetes FeCl3 10%. Ekstrak positif mengandung tanin apabila menghasilkan warna hijau kehitaman atau biru kehitaman. 10
Uji Aktivitas Antioksidan
Ekstrak buah pining dengan variasi konsentrasi 1, 0,5 dan 0,2 mg/L sebanyak 5 mL ditambahkan larutan DPPH sebanyak 2 mL dan divortex selama 2 menit. Perubahan warna dari larutan DPPH menunjukkan aktivitas antioksidan. Absorbansi DPPH diukur dengan menggunakan spektrofotometer UV-Vis pada λ = 517 nm. Aktivitas antioksidan sebagai persentase berkurangnya warna DPPH atau dikenal dengan %Inhibisi:
% Inhibisi = (1- absorbansi sampel
absorbansi kontrol )x 100%
Pembahasan
Hasil Ekstraksi Buah Pining
Ekstraksi yang dilakukan terhadap buah pining dengan menggunakan etanol diperoleh ekstrak kental sebanyak 41,77 gram dengan persentase rendemen 4,1%. Ektraksi buah pining menggunakan etil asetat diperoleh ektrak kental sebanyak 52,023 gram dengan presentase rendemen 5,2%. Ektraksi buah pining menggunakan
n-heksan 23,125 g dengan presentase rendemen sebanyak 2,3%.
Hasil Skrining Fitokimia
Berdasarkan Tabel 1 pada ekstrak buah pining menunjukan adanya metabolit sekunder yang terkandung yaitu flavonoid, saponin, kuinon, monoterpenoid dan seskuiterpenoid, serta senyawa albumin dari identifikasi albumin.
Jurnal Ilmiah Farmako Bahari Firman Gustaman Vol. 11; No. 1; Januari 2020
Halaman 67-74
Tabel 1. Hasil Penafisan Fitokimia Simplisia dan Ekstrak Etanol, ektrak etil asetat dan ekstrak N-Hexan buah pining
No Metabolit Sekunder Reagen Hasil Simplisia Ekstrak Etanol Ekstrak Etil asetat Ekstrak n-Heksana 1. Flavonoid HCl Pekat, Logam Mg + + + + 2. Saponin HCl pekat + + - + 3. Kuinon NaOH 1N + + + + 4. Steroid Pereaksi Lieberman-Buchard - - + - 5. Tanin dan polifenol Lar. Gelatin 1%, FeCl3 +/- + +/- +/- 6. Alkaloid Peraksi Mayer, Wagner, Dragendorff + + + -
7. Monoterpenoid Lar. Vanilin 10% + + + +
8. Seksuiterpenoid Asam Sulfat
pekat + + + + 9. Triterpenoid CH3COOH glasial dan larutan H2SO4 pekat + + + -
Keterangan: (+) Positif = Terdapat senyawa metabolit sekunder.
(-) Negatif = Tidak terdapat senyawa metabolit sekunder.
Berdasarkan hasil penafisan fitokimia bahwa simplisia dan esktrak etanol, ektrak etil asetat dan ekstrak n-heksan buah pining mengandung senyawa metabolit sekunder seperti flavonoid, kuinon, monoterpenoid, seskuiterpenoid. Flavonoid bersifat antimikroba yang dapat membentuk kompleks dengan protein ekstraseluler terlarut serta dinding sel mikroba flavonoid bersifat antiinflamasi sehingga dapat mengurangi peradangan serta membantu mengurangi rasa sakit, bila terjadi perdarahan atau pembengkakan pada luka.11,12 Selain sebagai antimikroba, golongan flavonoid juga memiliki aktivitas sebagai antioksidan, antivirus, antiinflamasi.13 kardioprotektif, antidiabetes, antikanker. Flavonoid yang memiliki aktivitas antioksidan meliputi flavon, flavonol, isoflavon, kateksin, flavonol dan kalkon. Aktivitas antioksidan dari senyawa alamiah yang berasal dari tanaman seperti flavonoid disebabkan adanya gugus hidroksil pada struktur molekulnya.14
Seskuiterpen dan moniterpen berfungsi sebagai antibakteri. Mekanisme aksi dari senyawa tersebut dalam menghambat pertumbuhan bakteri, belum banyak dilaporkan, beberapa penelitian menyebutkan bahwa lipofilitas senyawa tersebut menyebabkan terpenoid bekerja dengan cara mengganggu fungsi membran sel bakteri.12,11
Uji Antioksidan
Metode yang digunakan untuk menentukan aktivitas antioksidan dari biji buah pining adalah metode DPPH. Absorbansi DPPH diukur dengan menggunakan spektrofotometri UV-VIS pada panjang gelombang maksimal DPPH yaitu pada 516 nm. Vitamin C digunakan sebagai pembanding pada pengukuran ini. Berikut adalah hasil dari pengujian aktivitas antioksidan vitamin C, ekstrak etanol, etil asetat dan n -heksana dari biji buah pining.
Jurnal Ilmiah Farmako Bahari Firman Gustaman Vol. 11; No. 1; Januari 2020
Halaman 67-74
Pengujian Aktivitas Antioksidan dari Vitamin C sebagai Standar
Hasil pengujian aktivitas antioksidan vitamin C dapat dilihat pada grafik dibawah ini:
Gambar 1. Grafik Aktivitas Antioksidan Vitamin C
Parameter kekuatan senyawa sebagai antioksidan dapat dilihat dari nilai IC50 nya. Apabila nilai IC50 kurang dari 50 ppm dikategorekan sangat kuat, apabila antara 50-100 ppm termasuk kategori kuat, apabila antara 101-150 ppm termasuk sedang dan lemah apabila antara 150-200 ppm.15 Nilai IC50 untuk vitamin C adalah sebesar 4,19 ppm yang tergolong antioksidan yang sangat kuat
Aktivitas Antioksidan Biji Buah Pining
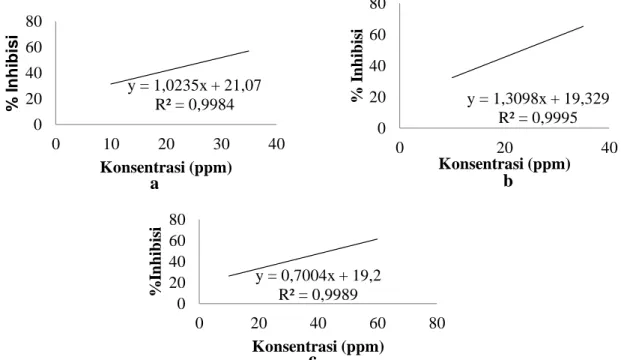
Biji buah pining diekstraksi dengan tiga pelarut yang memilik perbedaan kepolaran yaitu etanol, etil asetat dan n-heksana. Ketiga ekstrak tersebut diuji aktivitas antioksidannya. Hasil pengujiannya dapat dilihat pada Gambar 2.
Gambar 2. Grafik Pengujian Aktivitas Antioksidan Biji Buah Pining Ekstrak Etanol (a); etil asetat (b); n-heksana (c)
Berdasarkan hasil pengujian antioksidan diperoleh nilai IC50 untuk ekstrak etanol adalah sebesar 28,27 ppm, etil asetat sebesar 23,43 ppm dan n-heksana adalah 44 ppm. Ketiga ekstrak biji buah pining memiliki aktivitas antioksidan yang tergolong
y = 7,0723x + 20,342 R² = 0,9991 0 20 40 60 80 0 2 4 6 8 % In h ib is i Konsentrasi (ppm) y = 1,0235x + 21,07 R² = 0,9984 0 20 40 60 80 0 10 20 30 40 % I n h ib is i Konsentrasi (ppm)
a
y = 1,3098x + 19,329 R² = 0,9995 0 20 40 60 80 0 20 40 % I n h ib is i Konsentrasi (ppm)b
y = 0,7004x + 19,2 R² = 0,9989 0 20 40 60 80 0 20 40 60 80 % In h ib is i Konsentrasi (ppm)c
Jurnal Ilmiah Farmako Bahari Firman Gustaman Vol. 11; No. 1; Januari 2020
Halaman 67-74
sangat kuat.14 Diantara ketiga ekstrak biji buah pining, ekstrak yang memiliki aktivitas antioksidan yang paling tinggi atau yang memiliki nilai IC50 terendah adalah ekstrak etil asetat. Hasil pengujian aktivitas antioksidan ini sesuai dengan hasil skrining fitokimia yang menunjukkan adanya senyawa flavonoid pada ekstrak etil asetat yang dapat berperan sebagai antioksidan.
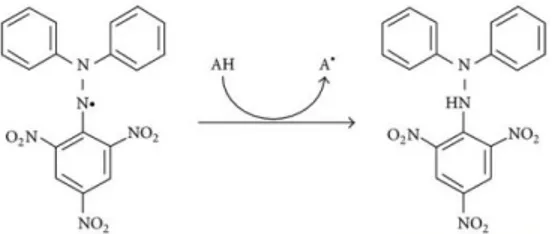
Mekanisme peredaman radikal bebas DPPH oleh antioksidan adalah dengan adanya donor atom H dari senyawa antioksidan yang menyebabkan radikal bebas menjadi stabil. Hal ini ditandai dengan perubahan warna ungu menjadi warna kuning (terbentuknya pikrilhidrazil).
Gambar 3. Reaksi Radikal Bebas DPPH dengan Antioksidan.16
Kesimpulan
Hasil penelitian menunjukkan bahwa buah pining mengandung senyawa metabolit sekunder diantaranya flavonoid, kuinon, monoterpenoid dan seskuiterpenoid. Buah pining memiliki aktivitas antioksidan tertinggi pada ekstrak etil asetat dengan nilai IC50 sebesar 23,43 ppm yang tergolong sangat kuat.
Daftar Pustaka
1. Salamah N, Widyaningsih W, Izati I, Susanti H. Aktivitas penangkap radikal bebas ekstrak etanol ganggang hijau Spirogyra sp. dan Ulva lactuca dengan metode DPPH. J Ilmu Kefarmasian Indones. 2015;13(2):145–50.
2. Wahdaningsih S, Erna Prawita Setyowati Subagus Wahyuono. Aktivitas penangkap radikal bebas dari batang pakis (Alsophila glauca J. Sm). Maj Obat Tradisional. 2011;16(3):156 – 160.
3. Handayani V, Ahmad AR, Sudir M. Uji aktivitas antioksidan ekstrak metanol bunga dan daun patikala (Etlingera elatior (Jack) R.M.Sm) menggunakan metode DPPH. Pharm Sci Res. 2014;1(2):86–93.
4. Rahman N, Bahriul P, Diah A. Uji aktivitas antioksidan ekstrak daun salam (Syzygium Polyanthum) dengan menggunanakan 1,1-Difenil-2-Pikrilhidrazil. J Akad Kim. 2014;3(3):143–9.
5. Agus S, Agustin W. Kemampuan air rebusan daun salam ( Eugenia polyantha W ) dalam menurunkan jumlah koloni bakteri Streptococcus sp . Capability of boiling water of bay leaf ( Eugenia polyantha W ) for reducing Streptococcus sp. colony. Maj Farm Indones. 2009;20(3):112–7.
6. Elim HI, L. Mapanawang A. Electronics physical system of large antioxidant structure in herbal medicine based zingiberaceae fruit: understanding and application. Nanotechnol Appl. 2018;1(1):1–4.
7. Seaver FJ. A preliminary study of the genus lamprospora. Mycologia. 1914;6(1):5.
Jurnal Ilmiah Farmako Bahari Firman Gustaman Vol. 11; No. 1; Januari 2020
Halaman 67-74
8. Praptiwi, Jamal Y, Wulansari D, Fathoni A, Palupi K, Nurainas, et al. Skrining aktivitas antioksidan beberapa tumbuhan suku zingiberaceae. Pros SEMNAS Biodiversitas. 2015;4(MAY):188–92.
9. Lakhan SE, Ford CT, Tepper D. Zingiberaceae extracts for pain: A systematic review and meta-analysis. Nutr J. 2015;14(1):1–10.
10. Harborne JB. Metode fitokimia: Penuntun cara modern menganalisis tumbuhan. Bandung: Penerbit ITB;1987.
11. Simões M, Bennett RN, Rosa EAS. Understanding antimicrobial activities of phytochemicals against multidrug resistant bacteria and biofilms. Nat Prod Rep. 2009;26(6):746–57.
12. Saleem M, Nazir M, Ali MS, Hussain H, Lee YS, Riaz N, et al. Antimicrobial natural products: An update on future antibiotic drug candidates. Nat Prod Rep. 2010;27(2):238–54.
13. Wang Q, Jin J, Dai N, Han N, Han J, Bao B. Anti-inflammatory effects, nuclear magnetic resonance identification, and high-performance liquid chromatography isolation of the total flavonoids from Artemisia frigida. J Food Drug Anal [Online]. 2016;24(2):385–91. Available from: http://dx.doi.org/10.1016/j.jfda.2015.11.004 14. Pokorny J, Yanishlieva N, Gordon M. Antioxidants in food. Cambridge:
Woodhead Publishing Limited; 2001.
15. Molyneux P. The Use of the stable free radical diphenylpicryl-hydrazyl (DPPH) for Estimating Antioxidant Activity. Songklanakarin J Sci Technol. 2004;26(December 2003):211–9.
16. Teixeira J, Gaspar A, Garrido EM, Garrido J, Borges F. Hydroxycinnamic acid antioxidants: An electrochemical overview. Biomed Res Int. 2013;1-11.