PENGARUH PEMBERIAN DAUN LAMTORO MERAH (Acacia villosa) DIKUKUS DAN TIDAK DIKUKUS TERHADAP
GAMBARAN HISTOPATOLOGI HATI TIKUS
DJUHARTI
FAKULTAS KEDOKTERAN HEWAN INSTITUT PERTANIAN BOGOR
PENGARUH PEMBERIAN DAUN LAMTORO MERAH (Acacia villosa) DIKUKUS DAN TIDAK DIKUKUS TERHADAP
GAMBARAN HISTOPATOLOGI HATI TIKUS
DJUHARTI
SKRIPSI
sebagai salah satu syarat untuk memperoleh gelar Sarjana Kedokteran Hewan
pada
Fakultas Kedokteran Hewan Institut Pertanian Bogor
FAKULTAS KEDOKTERAN HEWAN INSTITUT PERTANIAN BOGOR
Judul skripsi : Pengaruh Pemberian Daun Lamtoro Merah (A.villosa) Dikukus dan Tidak Dikukus Terhadap Gambaran Histopatologi Hati Tikus Nama : Djuharti
NRP : B04102171
Disetujui,
Dr. drh. Eva Harlina, MSi. drh. HernomoadiHuminto,MVS Dosen Pembimbing I DosenPembimbingII
Diketahui,
Dr. drh. I Wayan Teguh Wibawan, MS
Wakil Dekan FKH IPB
ABSTRAK
DJUHARTI. Pengaruh Pemberian Daun Lamtoro Merah (A.villosa) Dikukus dan Tidak Dikukus Terhadap Gambaran Histopatologi Hati Tikus. Dibimbing oleh EVA HARLINA dan HERNOMOADI HUMINTO.
A.villosa adalah leguminosa yang potensial sebagai pakan ternak karena mengandung protein tinggi (22-28%). Namun pemanfaatan A.villosa terkendala karena mengandung senyawa sekunder yang bersifat toksik. Penelitian ini bertujuan untuk mengetahui pengaruh pengukusan terhadap senyawa sekunder daun A.villosa yang diamati melalui performa, nilai fungsi dan gambaran histopatologi hati serta gambaran darah tikus setelah percobaan selama 4 minggu. Sebanyak 18 ekor tikus (Rattus rattus) dibagi menjadi 3 kelompok, yaitu kelompok kontrol yang diberi pakan kontrol, kelompok KS yang diberi pakan yang dicampur dengan tepung daun A.villosa dikukus, dan kelompok TKS yang diberi pakan yang mengandung daun A.villosa tidak dikukus.
ABSTRACT
Acacia villosa is a leguminous tree that potential as ruminant feedstuff caused it’s highly protein content (22-28%). However, the usage is hindered by its content of toxic secondary compounds. The aim of this research is to find out the effect of steaming of A. villosa leaf on its toxic secondary compounds by evaluation of performance, liver serum profile and histopathological changes, and hematological profile of rats (Rattus rattus) after treated for 4 weeks. Eighteen rats were divided into 3 groups; K group was control that given control feed, KS group was given feed which mixed with steamed A. villosa leaf and TKS group which was given un-steamed Acacia villosa leaf.
RIWAYAT HIDUP
Penulis dilahirkan di Jakarta, 16 Mei 1982 dari Ayah Alm. E. Djumanta dan Ibu Warnati. Penulis merupakan putri ke-9 dari sembilan bersaudara. Penulis menyelesaikan sekolah dasar di SDN Cipayung Depok pada tahun 1994, kemudian melanjutkan pendidikan di SLTPN 3 Depok, dan lulus pada tahun 1997.
Pada tahun 2000 penulis menyelesaikan pendidikan di SMUN 2 Depok, dan melanjutkan pendidikan ke Universitas Muhamadiyah PROF.DR.HAMKA Jakarta pada tahun yang sama. Pada tahun 2002, penulis diterima di Fakultas Kedokteran Hewan Institut Pertanian Bogor melalui jalur Seleksi Penerimaan Mahasiswa Baru (SPMB).
KATA PENGANTAR
Syukur Allhamdulillah penulis sampaikan kepada ALLAH SWT atas segala karunia dan kasih sayangNya sehingga penulis dapat menyelesaikan penulisan skripsi ini.
Penulis mengucapkan terima kasih kepada Ibu Dr. drh. Eva Harlina, MSi., selaku dosen pembimbing pertama dan Bapak drh. Hernomoadi Huminto, MVS., selaku dosen pembimbing kedua yang telah meluangkan waktunya untuk memberikan bimbingan dan nasihat kepada penulis dalam pelaksanaan penelitian hingga penyusunan skripsi.
Penulis menyampaikan terimakasih yang sebesar-besarnya kepada Dr. drh. Wiwin Winarsih MSi., selaku dosen penguji yang sudah memberikan banyak saran dan masukan untuk kesempurnaan dalam penulisan skripsi ini. Penulis juga menyampaikan rasa terimakasih yang tulus kepada Dr. drh. Tuty L. Yusuf, MS., selaku dosen pembimbing akademik atas bimbingan dan nasihat selama ini.
Ucapan terima kasih juga penulis sampaikan kepada seluruh staf dan pegawai Bagian Patologi Departemen Klinik Reproduksi dan Patologi FKH IPB, terutama Pak Kasnadi, Pak Endang dan Pak Soleh atas bantuannya selama penelitian.
Kepada Diyah Kuswarini sebagai rekan sepenelitian, Villosa Team (Kak jaka, Kak Ato, Au, Rahma, Lona, Asri, Nita, Putri, Erda dan Efal), Angga, Isti, Afrida, Budi, Teguh, Insa, Nila, Wayan, Mela, Dina, Joana, Ferdi, Jimmy, Dinda, Nalia, Dely, Kris dan Karen, terima kasih atas bantuan dan keceriaan yang telah merubah dan memberikan warna dalam hidup penulis.
bantuan, dukungan, semangat, kerja sama, dan kebersamaan yang telah terjalin selama ini.
Kepada Ayah dan Ibu tercinta yang selalu memanjatkan doa dan memberikan kepercayaan, serta seluruh Kakak-kakak yang selalu memberikan semangat dan dukungan materil hingga saat ini, penulis menyampaikan rasa terimakasih dan penghargaan yang tak terhingga.
Penulis menyadari bahwa karya ilmiah ini belum sempurna, semoga karya ilmiah ini bermanfaat bagi kemajuan ilmu pengetahuan dan semua pihak yang memerlukan.
Bogor, Februari 2007
DAFTAR ISI
Halaman
ABSTRAK ... i
RIWAYAT HIDUP ... ii
KATA PENGANTAR ... iii
DAFTAR ISI ... iv
DAFTAR TABEL ... v
DAFTAR GAMBAR ... vi
DAFTAR LAMPIRAN ... vii
PENDAHULUAN Latar Belakang ... 1
Tujuan ... 2
Manfaat ... 2
TINJAUAN PUSTAKA A.villosa ... 3
Tanin ... 4
Asam Amino Non-Protein ... 6
Hati ... 8
Detoksifikasi Senyawa Sekunder ... 11
BAHAN DAN METODE Waktu dan Tempat ... 13
Bahan dan Alat ... 13
Metode ... 13
Evaluasi Histopatologi ... 14
Analisis Data ... 14
Pengaruh Pemberian Daun A.villosa Dikukus dan
Tidak Dikukus Terhadap Gambaran Histopatologi Hati Tikus... 17
Pengaruh Pemberian Daun A.villosa Dikukus dan Tidak Dikukus Terhadap Fungsi Hati Tikus ... 23
Pengaruh Pemberian Daun A.villosa Dikukus dan Tidak Dikukus Terhadap Gambaran Darah Tikus ... 25
Pengaruh Pengukusan dan Pengeringan Terhadap Senyawa Sekunder A.villosa ... 28
KESIMPULAN DAN SARAN Kesimpulan ... 29
Saran ... 29
DAFTAR PUSTAKA ... 30
PENGARUH PEMBERIAN DAUN LAMTORO MERAH (Acacia villosa) DIKUKUS DAN TIDAK DIKUKUS TERHADAP
GAMBARAN HISTOPATOLOGI HATI TIKUS
DJUHARTI
FAKULTAS KEDOKTERAN HEWAN INSTITUT PERTANIAN BOGOR
PENGARUH PEMBERIAN DAUN LAMTORO MERAH (Acacia villosa) DIKUKUS DAN TIDAK DIKUKUS TERHADAP
GAMBARAN HISTOPATOLOGI HATI TIKUS
DJUHARTI
SKRIPSI
sebagai salah satu syarat untuk memperoleh gelar Sarjana Kedokteran Hewan
pada
Fakultas Kedokteran Hewan Institut Pertanian Bogor
FAKULTAS KEDOKTERAN HEWAN INSTITUT PERTANIAN BOGOR
Judul skripsi : Pengaruh Pemberian Daun Lamtoro Merah (A.villosa) Dikukus dan Tidak Dikukus Terhadap Gambaran Histopatologi Hati Tikus Nama : Djuharti
NRP : B04102171
Disetujui,
Dr. drh. Eva Harlina, MSi. drh. HernomoadiHuminto,MVS Dosen Pembimbing I DosenPembimbingII
Diketahui,
Dr. drh. I Wayan Teguh Wibawan, MS
Wakil Dekan FKH IPB
ABSTRAK
DJUHARTI. Pengaruh Pemberian Daun Lamtoro Merah (A.villosa) Dikukus dan Tidak Dikukus Terhadap Gambaran Histopatologi Hati Tikus. Dibimbing oleh EVA HARLINA dan HERNOMOADI HUMINTO.
A.villosa adalah leguminosa yang potensial sebagai pakan ternak karena mengandung protein tinggi (22-28%). Namun pemanfaatan A.villosa terkendala karena mengandung senyawa sekunder yang bersifat toksik. Penelitian ini bertujuan untuk mengetahui pengaruh pengukusan terhadap senyawa sekunder daun A.villosa yang diamati melalui performa, nilai fungsi dan gambaran histopatologi hati serta gambaran darah tikus setelah percobaan selama 4 minggu. Sebanyak 18 ekor tikus (Rattus rattus) dibagi menjadi 3 kelompok, yaitu kelompok kontrol yang diberi pakan kontrol, kelompok KS yang diberi pakan yang dicampur dengan tepung daun A.villosa dikukus, dan kelompok TKS yang diberi pakan yang mengandung daun A.villosa tidak dikukus.
ABSTRACT
Acacia villosa is a leguminous tree that potential as ruminant feedstuff caused it’s highly protein content (22-28%). However, the usage is hindered by its content of toxic secondary compounds. The aim of this research is to find out the effect of steaming of A. villosa leaf on its toxic secondary compounds by evaluation of performance, liver serum profile and histopathological changes, and hematological profile of rats (Rattus rattus) after treated for 4 weeks. Eighteen rats were divided into 3 groups; K group was control that given control feed, KS group was given feed which mixed with steamed A. villosa leaf and TKS group which was given un-steamed Acacia villosa leaf.
RIWAYAT HIDUP
Penulis dilahirkan di Jakarta, 16 Mei 1982 dari Ayah Alm. E. Djumanta dan Ibu Warnati. Penulis merupakan putri ke-9 dari sembilan bersaudara. Penulis menyelesaikan sekolah dasar di SDN Cipayung Depok pada tahun 1994, kemudian melanjutkan pendidikan di SLTPN 3 Depok, dan lulus pada tahun 1997.
Pada tahun 2000 penulis menyelesaikan pendidikan di SMUN 2 Depok, dan melanjutkan pendidikan ke Universitas Muhamadiyah PROF.DR.HAMKA Jakarta pada tahun yang sama. Pada tahun 2002, penulis diterima di Fakultas Kedokteran Hewan Institut Pertanian Bogor melalui jalur Seleksi Penerimaan Mahasiswa Baru (SPMB).
KATA PENGANTAR
Syukur Allhamdulillah penulis sampaikan kepada ALLAH SWT atas segala karunia dan kasih sayangNya sehingga penulis dapat menyelesaikan penulisan skripsi ini.
Penulis mengucapkan terima kasih kepada Ibu Dr. drh. Eva Harlina, MSi., selaku dosen pembimbing pertama dan Bapak drh. Hernomoadi Huminto, MVS., selaku dosen pembimbing kedua yang telah meluangkan waktunya untuk memberikan bimbingan dan nasihat kepada penulis dalam pelaksanaan penelitian hingga penyusunan skripsi.
Penulis menyampaikan terimakasih yang sebesar-besarnya kepada Dr. drh. Wiwin Winarsih MSi., selaku dosen penguji yang sudah memberikan banyak saran dan masukan untuk kesempurnaan dalam penulisan skripsi ini. Penulis juga menyampaikan rasa terimakasih yang tulus kepada Dr. drh. Tuty L. Yusuf, MS., selaku dosen pembimbing akademik atas bimbingan dan nasihat selama ini.
Ucapan terima kasih juga penulis sampaikan kepada seluruh staf dan pegawai Bagian Patologi Departemen Klinik Reproduksi dan Patologi FKH IPB, terutama Pak Kasnadi, Pak Endang dan Pak Soleh atas bantuannya selama penelitian.
Kepada Diyah Kuswarini sebagai rekan sepenelitian, Villosa Team (Kak jaka, Kak Ato, Au, Rahma, Lona, Asri, Nita, Putri, Erda dan Efal), Angga, Isti, Afrida, Budi, Teguh, Insa, Nila, Wayan, Mela, Dina, Joana, Ferdi, Jimmy, Dinda, Nalia, Dely, Kris dan Karen, terima kasih atas bantuan dan keceriaan yang telah merubah dan memberikan warna dalam hidup penulis.
bantuan, dukungan, semangat, kerja sama, dan kebersamaan yang telah terjalin selama ini.
Kepada Ayah dan Ibu tercinta yang selalu memanjatkan doa dan memberikan kepercayaan, serta seluruh Kakak-kakak yang selalu memberikan semangat dan dukungan materil hingga saat ini, penulis menyampaikan rasa terimakasih dan penghargaan yang tak terhingga.
Penulis menyadari bahwa karya ilmiah ini belum sempurna, semoga karya ilmiah ini bermanfaat bagi kemajuan ilmu pengetahuan dan semua pihak yang memerlukan.
Bogor, Februari 2007
DAFTAR ISI
Halaman
ABSTRAK ... i
RIWAYAT HIDUP ... ii
KATA PENGANTAR ... iii
DAFTAR ISI ... iv
DAFTAR TABEL ... v
DAFTAR GAMBAR ... vi
DAFTAR LAMPIRAN ... vii
PENDAHULUAN Latar Belakang ... 1
Tujuan ... 2
Manfaat ... 2
TINJAUAN PUSTAKA A.villosa ... 3
Tanin ... 4
Asam Amino Non-Protein ... 6
Hati ... 8
Detoksifikasi Senyawa Sekunder ... 11
BAHAN DAN METODE Waktu dan Tempat ... 13
Bahan dan Alat ... 13
Metode ... 13
Evaluasi Histopatologi ... 14
Analisis Data ... 14
Pengaruh Pemberian Daun A.villosa Dikukus dan
Tidak Dikukus Terhadap Gambaran Histopatologi Hati Tikus... 17
Pengaruh Pemberian Daun A.villosa Dikukus dan Tidak Dikukus Terhadap Fungsi Hati Tikus ... 23
Pengaruh Pemberian Daun A.villosa Dikukus dan Tidak Dikukus Terhadap Gambaran Darah Tikus ... 25
Pengaruh Pengukusan dan Pengeringan Terhadap Senyawa Sekunder A.villosa ... 28
KESIMPULAN DAN SARAN Kesimpulan ... 29
Saran ... 29
DAFTAR PUSTAKA ... 30
DAFTAR TABEL
Halaman 1. Komposisi kimia A.villosa ... 4 2. Distribusi dan efek merugikan dari beberapa AANP ... 7 3. Pengaruh pemberian daun A.villosa dikukus dan tidak dikukus
selama 4 minggu terhadap konsumsi pakan, bobot badan dan nilai konversi pakan tikus ... 15
4. Pengaruh pemberian daun A.villosa dikukus dan tidak dikukus selama 4 minggu terhadap persentase perubahan histpatologi hati tikus ... 18
5. Pengaruh pemberian daun A. villosa dikukus dan tidak dikukus selama 4 minggu terhadap fungsi hati tikus... 23
6. Pengaruh pemberian daun A. villosa dikukus dan tidak dikukus selama 4 minggu terhadap gambaran darah tikus... 26
DAFTAR GAMBAR
Halaman 1. Gafik rata-rata konsumsi pakan tikus yang diberi daun
A.villosa dikukus dan tidak dikukus selama
4 minggu ... 16
2. Grafik rata-rata bobot badan tikus yang diberi daun A. villosa
dikukus dan tidak dikukus selama 4 minggu... 16
3. Grafik perubahan histopatologi hati tikus berdasarkan jenis kerusakan hepatosit yang diberi daun A. villosa dikukus dan
tidak dikukus selama 4 minggu... 19
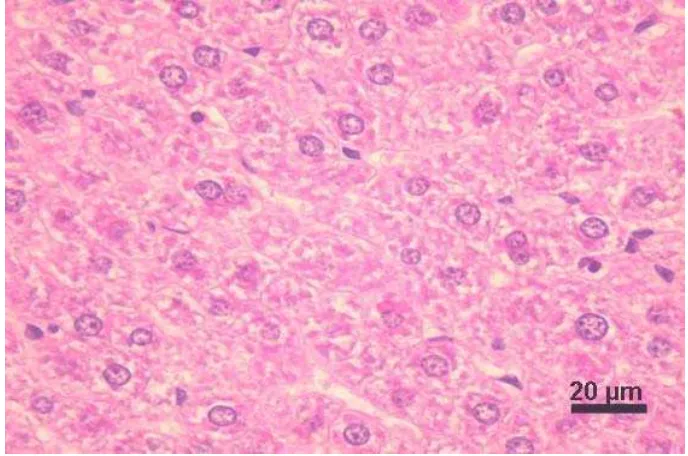
4. Hati tikus yang mengalami degenerasi berbutir pada
kelompok kontrol... 22
5. Hati tikus yang mengalami degenerasi hidropis pasca pemberian daun A. villosa dikukus selama 4 minggu... ... 22
DAFTAR LAMPIRAN
Halaman 1. Tabel komposisi pakan tikus ... 34 2. Uji ANOVA terhadap konsumsi pakan tikus pasca pemberian
daun A. villosa dikukus dan tidak dikukus ... 35
3. Uji ANOVA terhadap bobot badan tikus pasca pemberian daun A. villosa dikukus dan tidak dikukus ... 37
4. a. Kerusakan hepatosit pasca pemberian daun A. villosa dikukus dan tidak dikukus ... 39 b. Kerusakan hepatosit daerah sentrolobuler
dan segitiga Kiernan ... 39
5. Uji ANOVA terhadap gambaran kerusakan hati tikus
pasca pemberiandaun A. villosa dikukus dan tidak dikukus ... 40
6. Uji ANOVA terhadap fungsi hati tikus pasca pemberian daun
A. villosa dikukus dan tidak dikukus ... 41
7. Uji ANOVA terhadap gambaran darah tikus pasca pemberian
daun A. villosa dikukus dan tidak dikukus ... 43
1
PENDAHULUAN
Latar Belakang
Makanan pokok ruminansia adalah rumput yang mengandung bahan kering
15-20%, protein 2% dan energi 4.300 kal/g bahan kering. Disamping kadar
proteinnya yang rendah, rumput juga mengandung lignin dan silika yang tinggi.
Tingginya lignin dan silika mengakibatkan rendahnya tingkat konsumsi ternak dan
kualitas hasil ternak (Wiradarya 1991).
Dalam usaha peternakan sebagian besar biaya produksi ditentukan oleh biaya
pakan. Oleh karena itu, faktor keuntungan yang besar dapat diperoleh apabila ransum
dapat dimanipulasi secara efektif dan efisien, terutama dalam hal penggunaan bahan
pakan yang kaya akan protein. Hijauan leguminosa adalah salah satu contoh tanaman
yang mengandung protein tinggi karena kaya akan nitrogen dan tidak tergantung pada
kondisi nitrogen dalam tanah. Penggunaan hijauan leguminosa sebagai sumber
protein ransum mempunyai beberapa keuntungan, antara lain : 1) dapat menyediakan
protein yang cukup tinggi, murah, mudah didapat dan pasokan terjamin sepanjang
tahun; 2) mengandung sejumlah tanin sehingga dapat mencegah kembung dan
melindungi degradasi protein yang berlebihan oleh mikroba rumen; 3) beradaptasi
baik pada berbagai jenis lahan (Manurung 1995).
Acacia villosa merupakan jenis leguminosa yang sangat potensial digunakan
sebagai pakan karena mengandung protein yang tinggi. Tumbuhan ini mudah
diperoleh karena banyak ditemukan di daerah penyangga hutan. Pemanfaatan
A.villosa mempunyai banyak kendala karena adanya senyawa sekunder yaitu tanin
dan asam amino non-protein (AANP) (Wina dan Tangendjaja 2000).
Pengaruh negatif dari senyawa sekunder yang terkandung pada tanaman
leguminosa dapat dikurangi dengan perlakuan fisik atau kimia (Odenyo et al. 2003),
diantaranya adalah dengan perendaman dan pencucian daun, penambahan
polyethilenaglycol (PEG) untuk mengurangi efek tanin (Wina et al. 1994),
pengeringan yang berpengaruh terhadap penurunan kecernaan tanin (Hove et al.
2
amino non-protein (Widiyastuti 2001). Pada tanaman Leucaena leucephala, asam
amino non-protein mimosin yang bersifat toksik dapat berubah menjadi
3-hydroxi-4(1H)-pyridone (DHP) yang kurang toksik melalui proses pemanasan pada suhu 70oC
selama 10 menit. Pada ruminansia, pemberian A.villosa dalam dosis tinggi dan tanpa
masa adaptasi menyebabkan kematian, sedangkan dengan masa adaptasi tidak
menyebabkan kematian. Hal ini dikarenakan mikroflora rumen mampu mendegradasi
senyawa toksin (Widiyastuti 2001).
Penelitian dilakukan pada hewan coba tikus putih (Rattus rattus). Tikus putih
digunakan sebagai hewan model karena selain dapat menghemat waktu, juga lebih
sensitif terhadap toksin tanaman daripada ruminansia (Smith et al. 2001).
Tujuan
Tujuan penelitian ini adalah untuk mengetahui perubahan histopatologi hati
tikus putih (Rattus rattus) yang diberi daun A.villosa dikukus dan tidak dikukus
melalui penghitungan jumlah kerusakan hepatosit.
Manfaat
Penelitian ini diharapkan dapat memberikan informasi mengenai pengaruh
3
TINJAUAN PUSTAKA
Acacia villosa
Acacia merupakan salah satu jenis leguminosa yang dapat tumbuh di daerah
tropis dan subtropis, mempunyai nilai nutrisi tinggi, tahan terhadap kekeringan,
mudah tumbuh dan ekonomis (Subagyo 2002).
A.villosa atau lamtoro merah termasuk leguminosa pohon atau semak dari
keluarga Mimosoidea. Tanaman ini masuk ke Indonesia tahun 1920 dari Curacao
(West Indies) dan sekarang secara luas dapat ditemukan di hutan-hutan di Pulau Jawa
dan Sumatra. Lamtoro merah sangat cocok digunakan untuk reboisasi karena
pertumbuhannya yang cepat. Selain itu semak ini juga sebagai tanaman penghasil
kayu yang berguna bagi masyarakat sekitar hutan (Wina dan Tangendjaja 2000).
Tumbuhan ini merupakan perdu atau tanaman kecil, tegak dengan tinggi 1-3
m bahkan mencapai 5 m dengan batang dan cabang berwarna merah tua. Mempunyai
cabang yang banyak dan sistem perakaran yang dangkal serta kuat. Daun dicirikan
dengan bentuk majemuk dan bersirip ganda yang terdiri atas 2-10 pasang, panjang
4-9 cm, perbungaan pendek, terdiri atas 20-40 butir bunga. Bunga berkelamin dua,
berwarna putih, yang kemudian menjadi kekuningan. Buah A.villosa berbentuk
polong, pipih, dan berwarna cokelat mengkilap. Tiap polong berisi 1-8 buah biji yang
berbentuk bulat telur dan berwarna cokelat (Jukema dan Danimihardja 1997).
A.villosa tersebar dari dataran rendah hingga ± 1200 m di atas permukaan
laut, dan tumbuh cepat pada curah hujan 200-520 mm/tahun dengan kelembaban
55-70% (Bansi 2001). Di Kupang, A.villosa dikenal dengan nama lamtoro merah karena
tangkai dan batangnya berwarna merah, tetapi bentuk dan rupanya mirip dengan
lamtoro (Wina dan Tangendjaja 2000). Di daerah Timor Barat tanaman ini digunakan
sebagai pakan ternak, sedangkan di daerah Karibia, A.villosa digunakan sebagai
bahan obat untuk menyembuhkan radang mulut dan tenggorokan serta sebagai bahan
4
Salah satu jenis acacia yang menyerupai A.villosa adalah Acacia
angustissima. Keduanya mempunyai ciri fisik yang hampir sama, hanya saja jika
diperhatikan dengan seksama batang A.angustissima mempunyai warna lebih gelap
dibanding dengan batang A.villosa (ILCA 1991 dalam Bansi 2001). Komposisi kimia
A.villosa disajikan pada Tabel 1.
Tabel 1 Komposisi kimia A.villosa
Komposisi %
Protein Kasar Ekstrak Eter
Serat Detergen Netral Serat Detergen Asam Selulosa
Seperti tanaman leguminosa lainnya, A.villosa mempunyai kandungan protein
yang tinggi (Tabel 1) sehingga sangat berpotensi menjadi sumber protein bagi
ruminansia. Namun demikian, ada keterbatasan dalam penggunannya, karena
tanaman ini mengandung beberapa senyawa sekunder seperti tanin, AANP, oksalat,
cyanoglikosid, selenium, fluoroacetat, dan saponin (ILCA 1991 dalam Bansi 2001).
Wina dan Tangendjaja (2000) juga memaparkan zat antinutrisi yang sama, tetapi
tidak mendeteksi adanya asam sianida (HCN).
Tanin
Tanin adalah senyawa organik yang termasuk kedalam kelompok polifenol
kompleks dengan bobot molekul lebih besar dari 2.000 (Aryetti 2003). Sifat utama
5
hemiselulosa, dan pektin untuk membentuk suatu kompleks yang stabil. Hal ini
dikarenakan tanin mempunyai sejumlah besar senyawa bebas hydroxylphenol yang
membentuk ikatan hidrogen kuat dengan protein dan karbohidrat (Reed 1995).
Kemampuan tanin untuk membentuk senyawa kompleks dengan protein
merupakan aspek penting pada nilai gizi dan efek toksikologinya. Kekuatan senyawa
kompleks ini tergantung pada karakteristik tanin dan protein seperti berat molekul,
struktur tersier, nilai isoelektrik, dan kemampuan sisi perlekatan (Reed 1995). Tanin
dapat diikat oleh polyvinylpyrollidone (PVP) dan polyethilenaglycol (PEG) serta oleh
senyawa pendenaturasi protein seperti fenol (Makkar 2003).
Tanin dengan konsentrasi tinggi dapat mengurangi asupan pakan, kecernaan
protein dan karbohidrat, sehingga mempengaruhi penampilan fisik hewan. Tanin
mengurangi asupan pakan dengan menurunkan palatabilitas (selera makan), tetapi
tanin dalam konsentrasi sedang sampai rendah dapat mencegah kembung, dan
mempunyai efek anthelmintik (Makkar 2003). Selain itu tanin juga dapat membentuk
ikatan kompleks dengan protein pada pH rumen serta melindungi protein dari enzim
mikroba rumen. Kompleks protein tersebut tidak stabil, tetapi pada pH abomasum
menjadi stabil sehingga dapat dicerna (Reed 1995).
Berdasarkan sifat dan struktur kimianya, tanin diklasifikasikan kedalam tanin
terhidrolisis dan tanin terkondensasi. Tanin terhidrolisis merupakan asam gallat dan
asam ester ellagat yang terdiri dari rantai panjang senyawa gula dan fenol. Senyawa
ini sangat mudah dihidrolisis oleh asam, basa, atau enzim dan lebih mudah larut
dalam air (Reed 1995). Tanin terhidrolisis sangat toksik bagi ruminansia karena asam
gallat dapat dimetabolisme oleh mikroba menjadi pyrogallol dan senyawa fenol lain
dengan berat molekul rendah, sehingga mudah diabsorbsi. Senyawa fenol
dimetabolisme menjadi asam glukuronat setelah diabsorbsi (Murdiati et al. 1992
dalam Reed 1995). Kerusakan terbanyak yang disebabkan tanin terhidrolisis adalah
hemoragi gastrointestinal, nekrosa sel-sel hati dan kerusakan ginjal pada tubulus
proksimal (Dollahite et al. 1962 dalam Reed 1995).
Tanin terkondensasi adalah polimer yang terdiri atas unit-unit monomer
6
ikatan karbon yang tidak mudah untuk dihidrolisis (Reed 1995). Tanin terkondensasi
sering juga disebut proanthocyanidin. Tanin ini tidak dapat diabsorbsi tetapi
memberikan efek negatif pada mukosa saluran pencernaan dan menurunkan absorbsi
nutrisi. Proanthocyanidin dapat menurunkan absorbsi asam amino esensial metionin
dan lisin jika terdapat dalam konsentrasi tinggi. Menurunnya ketersediaan metionin
dapat meningkatkan toksisitas dari senyawa tumbuhan lain seperti glikosida
cyanogenik, sebab metionin terlibat dalam detoksifikasi cyanida (Reed 1995). Tanin
A.villosa termasuk dalam kelompok tanin terkondensasi (Odenyo et al. 2003).
Asam Amino Non-Protein
Asam amino non-protein (AANP) merupakan asam amino yang bukan
pembangun protein. Hampir 300 jenis asam amino non-protein telah diisolasi dari
tumbuhan dan umumnya terakumulasi pada biji dan daun. Asam amino non-protein
mempunyai struktur kimia yang analog dengan asam amino pembentuk protein
(Cheeke 1989).
Asam amino non-protein yang terkandung dalam A.angustissima antara lain
ADAB (2-amino-4-acetylaminobutyric acid), DABA (2,4-diamynobutyric acid) dan
oxalylabizine. Diantara ketiga asam amino non-protein tersebut jumlah yang paling
mendominasi adalah ADAB, yang diduga diperoleh dari degradasi β
-(isoxazolin-5-on-2-yl)-homoalanine (BIHA) menjadi DABA lalu melalui asetilasi oleh enzim
sintesis acetyl-coA diubah menjadi ADAB (Evans et al. 1993).
Odenyo et al. (1997) melaporkan bahwa domba yang mengkonsumsi
A.angustissima mengalami gejala keracunan yang mirip akibat pemberian Lathyrus
spp, diantaranya sindrom sistem saraf pusat akut yang diikuti oleh kematian lebih dari
50%. Gejala fisik lain yang bisa ditemukan antara lain kolaps, mabuk, mulut berbusa,
gigi gemeretak, dan kejang. Perubahan histopatologi yang ditemui antara lain
kerusakan hati berupa degenerasi lemak di daerah sentrolobuler, kongesti dan edema
7
Penelitian yang dilakukan oleh McSweeney et al. (2001) menemukan adanya
asam amino non-protein lain yaitu oxalyl diaminopropionic (ODAP) dan oxalyl
diaminobutyric (ODAB) yang diketahui berefek neurotoksin dalam konsentrasi
sangat rendah. Juga ditemukan asam beta acetyl diaminopropionic (ADAP) dan dua
asam amino non-protein yang belum teridentifikasi pada daun A.angustissima dengan
konsentrasi antara 1-4.4 g/kg berat kering.
DABA (2,4-diamynobutyric acid) merupakan asam amino non-protein yang
homolog dengan ornitin dan bersifat neurotoksik. Cara kerja AANP ini adalah dengan
menghambat ornithine-carbamoyl transferase di hati, sehingga mengganggu siklus
pembentukan urea yang dapat menginduksi toksisitas amonia. Pemberian DABA
(2,4-diamynobutyric acid) pada tikus menimbulkan gejala kelemahan, tremor, dan
kejang-kejang (Cheeke 1989).
Beberapa asam amino non-protein tanaman leguminosa yang bersifat
merugikan hewan disajikan pada Tabel 2.
Tabel 2 Distribusi dan efek merugikan dari beberapa asam amino non-protein
AANP Spesies tumbuhan Efek merugikan
Mimosin Leucaena leucephala Efek teratogenik, kerusakan organ, bulu
rontok, kematian.
Canavanine Canavalia ensiformis
Gliricidia sepium Robinia pseudoacacia
Mengurangi pertumbuhan dan retensi nitrogen
Indospicine Indigofera spicata Efek teratogenik dan kerusakan hati.
Homoarginine Lathyrus cicera Menghambat pertumbuhan dan
mengurangi asupan pakan
Sumber : D’Mello (2003)
Mimosin adalah asam amino aromatik yang mempunyai kontribusi sebagai
racun pada hewan. Mimosin mempunyai struktur yang analog dengan tirosin dan
8
menyebabkan gangguan fungsi reproduksi, teratogenik, kebotakan bahkan kematian
(D’Mello 2003).
Toksisitas mimosin dipengaruhi oleh mikroba rumen dan keberadaan bakteri
pemecah mimosin. Mimosin didegradasi menjadi 3,4-dihydroxypyridone (3,4-DHP)
oleh enzim ketika daun dikunyah dalam mulut ternak. Mimosin atau DHP
mempengaruhi kehilangan citarasa (apetite), penurunan kadar tiroksin dalam darah,
kondisi goitrogenik, berat badan menurun, kelemahan bahkan kematian (Rosenthal
1982). Selain itu, 3,4-DHP diketahui ada pada daun legum sebagai aktivitas enzim
pasca panen atau pasca pemotongan (Widiyastuti 2001).
Rosenthal (1982) menyatakan bahwa ruminansia lebih tahan terhadap
mimosin dibanding ternak berlambung tunggal, sebab bakteri rumen mampu
mengubah mimosin menjadi 3-hydroksi-4(1H)-pyridone (DHP) yang kurang beracun.
Hati
Hati merupakan organ yang mempunyai peranan penting dalam metabolisme
dan memiliki beberapa fungsi dalam tubuh termasuk penyimpanan glikogen, sintesis
protein plasma dan penetralan racun.
Struktur histologi dan komponen sel hati tikus pada dasarnya sama dengan
semua spesies mamalia. Hati terdiri dari beberapa hepatosit (sel parenkim), sel-sel
sinusoid (sel endotel, sel Kuppfer), sel hematopoietik, sel saraf, sel pembuluh darah,
dan limfatik (Harada et al.1999).
Permukaan hati ditutupi oleh kapsula fibrosa yang padat, yang sebagian
berhubungan langsung dengan diafragma dan dinding abdominal sebelah posterior,
lalu dilapisi lagi dengan peritoneum. Unit fungsional hati adalah lobulus hati, yang
merupakan struktur silindris di sekeliling vena sentralis, terdiri dari banyak
lempengan sel hepatika yang tersebar secara sentrifugal dari vena sentralis. Tiap
lempengan hepatika mempunyai tebal dua sel dan antara sel yang berdekatan terletak
9
Menurut struktur dan fungsinya, lobulus hati dibagi menjadi tiga zona atau
daerah yaitu daerah sentrolobuler, daerah tengah (midzonal) dan daerah periportal.
Daerah sentrolobuler merupakan akhir dari mikrosirkulasi yang menerima darah dari
pertukaran gas dan metabolit dengan sel-sel dari daerah tengah dan periportal. Hal ini
menyebabkan daerah sentrolobuler lebih sensitif terhadap gangguan sirkulasi
(iskemia, anoksia, kongesti) dan defisiensi nutrisi. Sebaliknya, daerah periportal dekat
dengan pembuluh darah, menerima darah yang kaya O2 dan nutrisi. Akan tetapi,
apabila ada senyawa yang bersifat toksik dalam darah, maka daerah ini akan terpapar
terlebih dahulu. Hepatosit di daerah periportal mempunyai lebih banyak mitokondria
sedangkan di daerah sentrolobuler mempunyai jumlah sitokrom P450 yang lebih
banyak (Harada et al. 1999).
Hati mempunyai suplai darah ganda yaitu dari arteri hepatika dan vena porta.
Arteri hepatika mempunyai fungsi utama sebagai pembawa nutrisi, sedangkan vena
porta membawa darah dari traktus gastrointestinalis, limpa, dan pankreas. Arteri
hepatika dan vena porta memasuki hati pada porta hepatika, akhirnya membentuk
cabang arteri dan vena yang terlihat dalam segitiga porta (portal triad), yang
bergabung dengan pembuluh limfatik. Cabang-cabang arteri hepatika membentuk
kapiler-kapiler yang berpenetrasi di tepi-tepi sinusoid, atau ke arah lebih dalam ke
daerah parenkim. Sejumlah kecil darah masuk ke sinusoid secara langsung dari
cabang-cabang arteri hepatika. Sebagian besar sinusoid mengosongkan isinya ke
dalam vena sentralis. Semua vena sentralis dalam lobulus bergabung menjadi vena
hepatika besar yang mengalirkan darahnya ke vena kava (Harada et al. 1999).
Beberapa fungsi hati antara lain merupakan tempat sekresikan empedu,
metabolisme protein, lemak dan karbohidrat, detoksifikasi berbagai senyawa dan
pembentukan protein. Hati merupakan organ yang sering terpapar oleh bahan toksik.
Perjalanan toksikan di dalam tubuh mengalami beberapa tahap yang dimulai dari
proses absorbsi, distribusi, biotransformasi atau metabolisme (aktivasi dan
detoksifikasi) dan eliminasi. Penyerapan toksikan merupakan proses masuknya bahan
10
difusi sederhana, filtrasi, melalui media pembawa dan endositosis (pencaplokan oleh
sel) (Lu 1995).
Setelah toksikan mengalami penyerapan maka akan diedarkan melalui
peredaran darah ke seluruh jaringan atau organ tubuh sesuai dengan organ sasaran
masing-masing, misalnya otot, tulang, sistem saraf pusat, hati dan ginjal. Hati dan
ginjal dapat menyimpan lebih dari satu zat toksikan. Toksikan akan mengalami
proses metabolisme atau biotransformasi di dalam hati. Proses biotransformasi
toksikan terjadi dalam dua fase, yakni fase I yang melibatkan reaksi oksidasi, reduksi
dan hidrolisis, dan fase II yang melibatkan reaksi konjugasi atau reaksi sintetik.
Biotransformasi melibatkan banyak enzim seperti sitokrom P450, glutathione
transferase, epoksida hidrolase dan flavin terikat monoksidase (Harada et al. 1999).
Toksikan setelah diserap akan dibawa vena porta ke hati, oleh karena itu kadar
enzim (terutama sitokrom P450) akan meningkat. Oksidasi toksikan oleh sitokrom
P450 menghasilkan senyawa yang sangat reaktif, yang dalam keadaan normal segera
dirubah menjadi metabolit yang lebih stabil. Metabolit yang diperoleh dari fase
oksidasi tersebut akan dikonjugasi dengan substrat endogen yang akan menghasilkan
senyawa yang lebih polar dan mudah terionisasi sehingga mudah diekskresikan. Bila
kadar toksikan sangat tinggi, maka metabolit antara yang terbentuk juga tinggi.
Apabila inaktivasi tidak cukup cepat, maka senyawa metabolit tersebut akan bereaksi
dengan komponen sel dan menyebabkan kerusakan jaringan (Ganiswara et al. 1995).
Berbagai macam kerusakan yang terjadi di hati dapat diakibatkan oleh
berbagai sebab, salah satunya adalah racun tanaman. Selain merusak hati, racun
tanaman juga dapat merusak ginjal dan epitel saluran pencernaan (Reed 1995).
Kerusakan yang terjadi pada hati akan meningkatkan kadar enzim-enzim
transaminase karena enzim ini akan dilepaskan ke dalam serum ketika sel hati
mengalami kerusakan. Enzim-enzim transaminase tersebut adalah Serum Glutamat
Pyruvat Transaminase (SGPT) dan Serum Glutamat Oxaloacetat Transaminase
(SGOT). SGPT terdapat dalam jumlah besar pada sel hati manusia, primata, anjing
dan tikus, tetapi terdapat dalam jumlah kecil pada sel hati babi, domba, sapi dan kuda.
11
jantung, pankreas, ginjal, tulang dan otot sehingga tidak bisa dijadikan sebagai
ukuran kerusakan hati (Girindra 1988).
Detoksifikasi Senyawa Sekunder
Berbagai usaha yang dilakukan untuk mengurangi kadar senyawa sekunder
daun A.villosa adalah dengan perendaman, pencucian daun, penambahan
polyethilenaglycol (PEG) (Wina et al. 1994), pengeringan dan pemanasan untuk
menurunkan kecernaan tanin (Hove et al. 2003).
Pengukusan adalah proses pemanasan yang sering diterapkan dalam sistem
jaringan sebelum dilakukan pembekuan dan pengeringan. Adapun tujuannya adalah
untuk menonaktifkan enzim yang akan merubah warna, cita rasa maupun nilai gizi.
Pada proses pengukusan terjadi pengurangan zat gizi namun tidak sebesar pada
perebusan. Pengukusan dilakukan dengan suhu air lebih tinggi dari 66oC tetapi
kurang dari 82oC. Pada pengukusan tradisional, partikel pada bagian tepi mengalami
pengukusan lebih banyak sedangkan di bagian tengah lebih sedikit (Khotimah 2002).
Pengukusan juga dipakai sebagai perlakuan pendahuluan untuk mempercepat
pengeringan (Krisdianto 2004).
Pembekuan adalah suatu upaya agar bahan perlakuan melewati kisaran suhu
pembentukan kristal es maksimum (0-4oC) dalam waktu sependek mungkin (30 menit
atau kurang), karena pembentukan kristal es yang besar menyebabkan perubahan
yang tidak diinginkan terhadap tekstur jaringan. Pada proses pembekuan terjadi
penghilangan air yang menyebabkan naiknya konsentrasi garam. Salah satu metode
utama pembekuan adalah immersion freezing, yaitu dengan meletakkan bahan
langsung ke dalam cairan pembeku. Salah satu cairan pembeku adalah nitrogen cair,
yang digunakan pada proses pembekuan modern (Gardjito et al. 1992).
Pengeringan secara tradisional dilakukan hanya dengan meletakkan bahan
perlakuan di bawah sinar matahari. Cara ini dipakai untuk mengendalikan
pertumbuhan mikroorganisme maupun untuk menghilangkan air. Salah satu contoh
proses pengeringan adalah proses dehidrasi, yaitu proses penghilangan air
12
suhu yang dipergunakan jangan terlalu tinggi, karena dapat menyebabkan
perubahan-perubahan yang tidak dikehendaki pada bahan perlakuan. Salah satu metode yang
dipakai untuk pengeringan adalah freeze drying (pengeringan beku) (Gardjito et al.
1992).
Pada freeze drying (pengeringan beku), semua bahan pada awalnya dibekukan
kemudian dilakukan suatu proses pemanasan ringan dalam suatu lemari hampa udara.
Kristal-kristal es yang terbentuk selama tahapan pembekuan, menyublim jika
dipanaskan pada tekanan hampa, yaitu berubah secara langsung dari es menjadi uap
air tanpa melewati fase cair. Hal ini menghasilkan produk yang bersifat porous
(keropos) dengan perubahan yang sangat kecil terhadap ukuran dan bentuk bahan
aslinya. Karena panas yang dipergunakan sangat rendah, maka kerusakan akibat
panas juga kecil (Gardjito et al. 1992). Lowry et al. (1982) dalam Widiyastuti (2001)
menyatakan bahwa aktivitas enzim mimosinase yang merombak mimosin menjadi
13
BAHAN DAN METODE
Waktu dan Tempat
Penelitian dilakukan di Bagian Patologi, Departemen Klinik, Reproduksi dan
Patologi, Fakultas Kedokteran Hewan Institut Pertanian Bogor dan Balai Penelitian
Ternak Ciawi, dimulai dari bulan Februari 2005 hingga Juli 2006.
Bahan dan Alat
Bahan yang digunakan adalah daun A.villosa, nitrogen cair, aquades steril,
bahan-bahan untuk pakan tikus dengan formula khusus, bahan-bahan untuk
pembuatan sediaan histopatologi (buffer neutral formaline 10%, alkohol bertingkat
70-100%, xylol, paraffin, alkohol absolut, pewarna Haematoxylin-Eosin, perekat
untuk mounting), serta diethyl eter untuk anastesi hewan coba.
Hewan percobaan yang digunakan adalah tikus putih (Rattus rattus) betina
dari jenis Sprague Dawley (SD) berumur empat minggu, dengan bobot badan berkisar
antara 50-80 g.
Alat-alat yang digunakan dalam penelitian ini adalah kandang individu dari
bak plastik, timbangan elektronik Precisa 3000D, freeze dryer, panci untuk
mengukus, alat-alat nekropsi, tissue cassette, tissue processor, rotary microtome,
lemari es, gelas objek, serta mikroskop cahaya dan video micrometer.
Metode
Daun A.villosa segar dikukus selama sepuluh menit, kemudian direndam
dalam nitrogen cair, lalu dikeringkan dalam tabung freeze dryer selama satu minggu.
Sebagai pembanding, daun A.villosa segar langsung direndam dalam nitrogen cair
dan dikeringkan dalam freeze dryer. Daun yang telah kering kemudian digiling
menjadi tepung daun, dan sebanyak 21% dicampurkan dengan bahan pakan lain
14
Sebanyak 18 ekor tikus dibagi menjadi 3 kelompok, satu kelompok kontrol
yang hanya diberi pakan kontrol, sisanya adalah kelompok perlakuan, yaitu kelompok
yang diberi pakan mengandung 21% A.villosa dikukus (kelompok KS), dan
kelompok yang diberi pakan mengandung 21% A.villosa tanpa dikukus (kelompok
TKS).
Sebelum perlakuan, hewan coba diadaptasikan terlebih dahulu terhadap pakan
dan lingkungan selama dua minggu. Pakan dan minum diberikan ad libitum.
Percobaan dilaksanakan selama satu bulan dan selama penelitian berlangsung diukur
konsumsi pakan dan bobot badan perminggu untuk mengetahui jumlah konsumsi
pakan, pertambahan bobot badan dan konversi pakan.
Pada tahap akhir penelitian, hewan coba dianastesi terlebih dahulu
menggunakan eter untuk pengambilan darah jantung guna pemeriksaan darah (benda
darah merah, hemoglobin, benda darah putih dan hematokrit) dan fungsi hati (SGPT,
SGOT, total protein, albumin dan globulin). Selanjutnya dilakukan nekropsi pada
semua hewan coba untuk pengambilan organ hati.
Organ hati difiksasi dengan BNF (Buffer Neutral Formaline) 10%, dibuat
sediaan histopatologi dan diwarnai dengan Haematoxylin-Eosin.
Evaluasi Histopatologi
Evaluasi histopatologi dilakukan pada hepatosit yang mengalami degenerasi
berbutir (cloudy swelling), degenerasi hidropis, dan nekrosa pada 20 lapang pandang,
10 buah di sekitar vena sentralis dan 10 buah di sekitar vena porta. Persentase
kerusakan hepatosit diperoleh dengan cara menghitung jumlah yang mengalami
perubahan dalam satu lapang pandang dengan luas 176 µm2 (lensa objektif 40 X).
Analisis Data
Nilai konsumsi pakan, bobot badan, nilai konversi pakan dan evaluasi
histopatologi diolah menggunakan analisis sidik ragam (ANOVA). Jika berbeda
15
HASIL DAN PEMBAHASAN
Pengaruh Pemberian Daun A.villosa Dikukus dan Tidak Dikukus Terhadap Konsumsi Pakan, Bobot Badan dan Nilai Konversi Pakan Tikus
Pengamatan yang dilakukan terhadap kondisi fisik tikus selama percobaan
tidak memperlihatkan tanda-tanda keracunan. Konsumsi pakan, bobot badan dan nilai
konversi pakan tikus pada pemberian daun A.villosa dikukus dan tidak dikukus
disajikan pada Tabel 3 serta Gambar 1 dan 2.
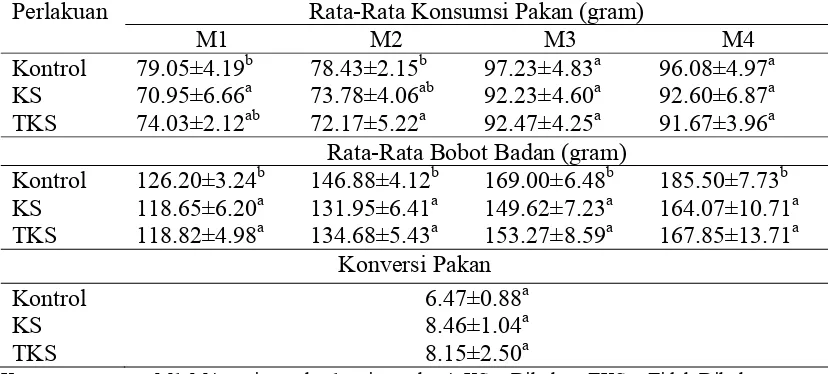
Pada Tabel 3 terlihat bahwa hasil pemberian pakan yang dicampur dengan
daun A.villosa hanya mempengaruhi konsumsi pakan di minggu pertama dan kedua
saja. Pada minggu pertama dan kedua, konsumsi pakan kelompok dikukus (KS) dan
tidak dikukus (TKS) cenderung lebih rendah dari kelompok kontrol. Hal ini
disebabkan adanya proses adaptasi hewan coba terhadap pakan baru yang
mengandung daun.
Tabel 3 Pengaruh pemberian daun A.villosa dikukus dan tidak dikukus selama 4 minggu terhadap konsumsi pakan, bobot badan dan konversi pakan tikus
Perlakuan Rata-Rata Konsumsi Pakan (gram)
M1 M2 M3 M4 Rata-Rata Bobot Badan (gram)
Kontrol
16
Berbeda dengan minggu sebelumnya, pada minggu ke-3 dan ke-4 terlihat ada
peningkatan konsumsi pakan kelompok KS dan TKS sehingga tidak berbeda nyata
dengan kelompok kontrol (p>0.05) (Gambar 1). Konsumsi pakan yang baik pada
kelompok perlakuan disebabkan oleh hewan coba telah beradaptasi dengan jenis
pakan yang diberikan yaitu pakan yang mengandung daun A.villosa.
Gambar 1 Pengaruh pemberian daun A.villosa dikukus dan tidak dikukus terhadap konsumsi pakan tikus selama 4 minggu.
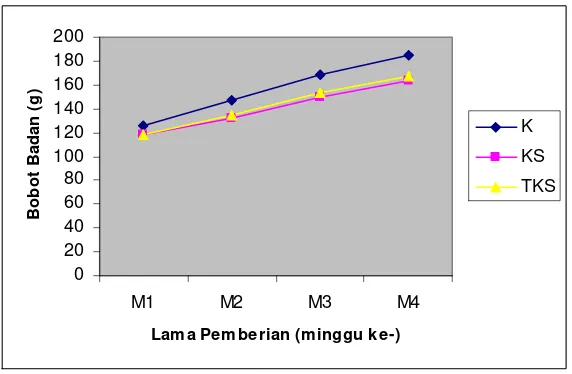
Gambar 2 Pengaruh pemberian daun A.villosa dikukus dan tidak dikukus terhadap bobot badan tikus selama 4 minggu.
17
Pada Tabel 3 tampak bahwa bobot badan hewan coba memperlihatkan
peningkatan setiap minggunya (Gambar 2). Bobot badan kelompok KS tidak berbeda
nyata dengan kelompok TKS, namun bobot badan kelompok perlakuan lebih rendah
dan berbeda nyata dengan kelompok kontrol (p<0.05). Hal ini dikarenakan daun
A.villosa pada kelompok KS dan TKS mengandung serat kasar yang tinggi sehingga
menurunkan kecernaan nutrisi pakan. Adanya kemampuan tanin yang dapat mengikat
karbohidrat, protein dan enzim-enzim pencernaan (Reed 1995 dan Makkar 2003)
menyebabkan kecernaan pakan rendah sehingga mengurangi sumber energi untuk
pertumbuhan.
Konversi pakan adalah hasil pembagian total konsumsi pakan dengan
perolehan pertambahan bobot badan. Semakin kecil nilai konversi pakan
memperlihatkan semakin efisien penggunaan pakan. Pada Tabel 3 terlihat nilai
konversi pakan kelompok KS tidak berbeda nyata dengan kelompok TKS maupun
kontrol (p>0.05). Hal ini mengindikasikan pakan yang dikonsumsi dapat
dikonversikan menjadi pertambahan bobot badan.
Pengaruh Pemberian Daun A.villosa Dikukus dan Tidak Dikukus Terhadap Gambaran Histopatologi Hati Tikus
Hasil pemeriksaan histopatologi hati kelompok kontrol maupun perlakuan
ditemukan adanya perubahan-perubahan pada parenkim dan interstisium. Kongesti
dan dilatasi sinusoid merupakan perubahan yang ditemukan pada interstisium hati,
dan terjadi pada semua kelompok tikus. Kongesti yang terjadi pada vena sentralis dan
sinusoid disebabkan penggunaan eter pada saat euthanasia. Menurut Ganiswara
(1995), eter adalah anaestetikum yang sangat kuat yang dapat menyebabkan
vasodilatasi pembuluh darah di berbagai organ. Oleh sebab itu kongesti dan dilatasi
sinusoid tidak dijadikan parameter kerusakan hati pada penelitian ini. Pada parenkim
hati ditemukan degenerasi berbutir, degenerasi hidropis dan nekrosa sel-sel hati.
Persentase berbagai perubahan pada sel-sel hati disajikan pada Tabel 4 serta Gambar
18
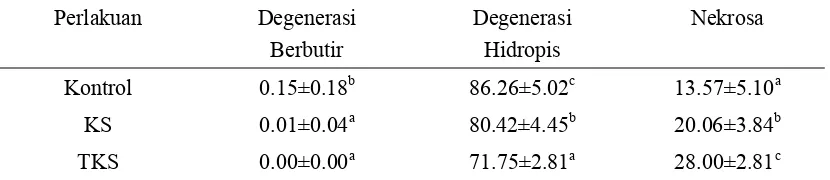
Tabel 4 Pengaruh pemberian daun A.villosa dikukus dan tidak dikukus selama 4 minggu terhadap persentase perubahan histopatologi hati tikus
Perlakuan Degenerasi Berbutir
Degenerasi Hidropis
Nekrosa
Kontrol 0.15±0.18b 86.26±5.02c 13.57±5.10a
KS 0.01±0.04a 80.42±4.45b 20.06±3.84b
TKS 0.00±0.00a 71.75±2.81a 28.00±2.81c
Keterangan : KS = Dikukus, TKS = Tidak Dikukus
Huruf yang berbeda pada kolom yang sama menunjukkan perbedaan yang nyata (p<0.05)
Hasil pengamatan histopatologi menunjukkan bahwa degenerasi berbutir
kelompok KS tidak berbeda nyata dengan kelompok TKS, namun kelompok
perlakuan berbeda nyata dengan kontrol (p<0.05). Degenerasi berbutir adalah
langkah pertama perubahan sel yang dapat mengarah pada nekrosa. Hal ini dapat
terjadi apabila sel-sel terpapar oleh senyawa yang bersifat toksik dalam konsentrasi
besar dan jangka waktu yang lama.
Degenerasi merupakan perubahan morfologi dan penurunan fungsi sel yang
bersifat sementara yang disebabkan oleh adanya gangguan metabolisme, anoksia,
iskemia dan senyawa-senyawa toksik. Berbagai kondisi tersebut menyebabkan
berkurangnya energi sel sehingga merusak sel secara tidak langsung (Jubb et al.
1993). Degenerasi dapat meluas sampai ke inti dan menyebabkan kehilangan
kromatin sehingga berlanjut menjadi nekrosa sel.
Degenerasi berbutir pada sel hati tampak sebagai sitoplasma yang berisi
butiran keruh atau bergranulasi yang tersusun mengitari inti (Jubb et al. 1993).
Keadaan tersebut disebabkan oleh terjadinya kebengkakan mitokondria, penambahan
jumlah protein tertentu dalam sitoplasma, imbibisi cairan ekstraseluler dan hidrasi ion
natrium akibat permeabilitas dinding sel hati terganggu sehingga sel hati
membengkak dan berbutir keruh (Harada et al.1999). Hepatosit yang mengalami
19
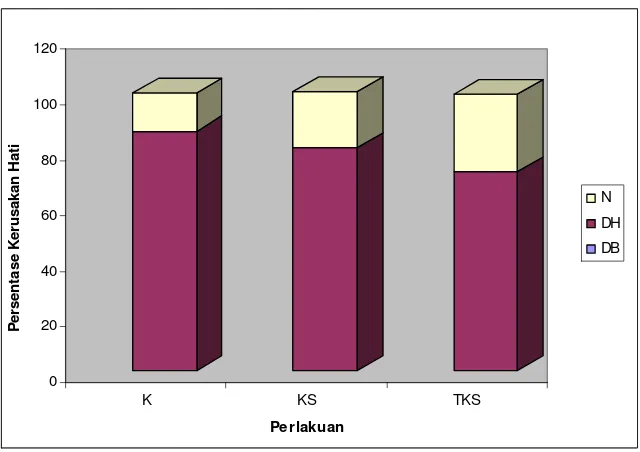
Gambar 3 Pengaruh pemberian daun A.villosa dikukus dan tidak dikukus terhadap persentase perubahan histopatologi hati tikus.
Persentase degenerasi hidropis kelompok KS berbeda nyata (p<0.05) dengan
kelompok TKS, dan persentase kelompok perlakuan berbeda nyata dengan kontrol
(p<0.05). Tingginya persentase hepatosit yang mengalami degenerasi hidropis pada
kelompok perlakuan disebabkan oleh adanya gangguan metabolisme hati yang
diakibatkan oleh pakan atau lingkungan. Daun A.villosa yang ditambahkan ke dalam
pakan mengandung senyawa sekunder yang bersifat hepatotoksik, sehingga
menyebabkan kerusakan hepatosit. Odenyo et al. (1997) melaporkan bahwa domba
yang mengkonsumsi A.angustissima mengalami kerusakan hati berupa degenerasi
lemak di daerah sentrolobuler.
Degenerasi hidropis merupakan kelanjutan dari degenerasi berbutir yang
masih bersifat reversible. Sitoplasma sel hati bervakuol dengan inti di tengah dan
batas sel yang jelas. Setelah membran sel mengalami kerusakan, maka kerusakan
akan menyebar ke organel-organel sel. Cheville (1999) menjelaskan bahwa salah satu
penyebab terjadinya degenerasi hidropis adalah karena anoksia, dimana oksigen
dalam sel digunakan untuk mengatur pemasukan ion natrium dan air. Apabila
20
ketersediaan oksigen dalam jaringan rendah, maka terjadi imbibisi cairan interstisium
yang memasuki sel menyertai ion natrium. Akibatnya, ion kalium banyak keluar dari
sel sehingga sel membengkak dan mengalami edema intraseluler.
Dalam kondisi normal, 2 molekul ion K+ dipompa keluar sel untuk setiap 3
molekul ion Na+ yang dipompa ke dalam sel. Pompa ion natrium tersebut
mempertahankan keseimbangan jumlah cairan sel dan interstisium. Kerusakan
membran dan pompa natrium dapat menyebabkan ion Na+ banyak tinggal dalam sel.
Kondisi ini menyebabkan cairan disekitar sel akan merembes masuk ke dalam sel dan
menyebabkan kebengkakan pada organel-organel sel (Cheville 1999). Hepatosit yang
mengalami degenerasi hidropis disajikan pada Gambar 5.
Kerusakan sel berupa degenerasi hidropis banyak ditemukan di daerah
sentrolobuler, sedangkan di daerah periportal banyak ditemukan sel nekrosa. Hal ini
disebabkan daerah periportal dekat dengan pembuluh darah, menerima darah yang
kaya O2 dan nutrisi, akan tetapi apabila ada toksikan dalam darah, maka daerah ini
akan terpapar terlebih dahulu. Di daerah sentrolobuler banyak terdapat enzim
sitokrom P450 yang dapat membuat sebagian besar zat toksik menjadi kurang toksik,
sehingga lebih mudah larut dalam air dan mudah diekskresikan.
Akumulasi metabolit yang kurang toksik dapat merusak sel hati dalam bentuk
yang lebih ringan seperti degenerasi berbutir atau hidropis. Apabila kadar toksikan
tersebut melebihi kemampuan detoksifikasi hati, maka toksikan tersebut akan sampai
ke daerah sentrolobuler dan menyebabkan kerusakan hepatosit.
Persentase kematian sel (nekrosa) kelompok TKS lebih tinggi dan berbeda
nyata (p<0.05) dibandingkan dengan kelompok KS maupun kontrol. Hal ini
menunjukkan bahwa pengukusan daun dapat mengurangi jumlah hepatosit yang
mengalami nekrosa. Nekrosa merupakan kerusakan sel yang permanen atau
irreversible. Apabila sejumlah besar hepatosit mengalami nekrosa dan penggantian
atau regenerasi tidak mencukupi, maka sebagian fokus nekrosa akan diisi oleh
jaringan ikat.
Kematian sel atau nekrosa merupakan kerusakan sel yang bersifat irreversible
21
terlihat lebih asidofilik (merah). Perubahan warna ini disebabkan oleh denaturasi
protein sitoplasma dan kerusakan ribosom. Pada kondisi normal, ribosom
bertanggung jawab terhadap warna basofil sitoplasma. Kromatin inti sel yang nekrosa
menggumpal, inti mengecil dan berwarna biru (piknosis). Inti piknosis dapat pecah
menjadi bagian-bagian kecil (karyorhexis) atau menghilang (karyolisis) (Harada et al.
1999). Hepatosit yang mengalami nekrosa disajikan pada Gambar 6.
Nekrosa pada penelitian ini banyak ditemukan di daerah perilobuler
(Kelompok KS= 20.34%, TKS= 28.78%) dan sentrolobuler (Kelompok KS= 19.47%,
TKS= 27.71%), tetapi jumlah terbanyak adalah di daerah perilobuler. Mekanisme
terjadinya nekrosa perilobuler berkaitan dengan vaskularisasi hati. Seperti diketahui
bahwa hati mendapat suplai darah yang berasal dari saluran pencernaan melalui vena
porta. Perjalanan darah yang mengandung toksin yang berasal dari usus, masuk ke
hati melalui vena porta, melewati sinusoid-sinusoid yang akhirnya sampai di vena
sentralis. Hepatosit yang terletak di bagian perifer lobulus adalah hepatosit yang
bersinggungan terlebih dahulu dengan bahan-bahan bersifat toksik dibandingkan
dengan hepatosit yang berada di tengah lobulus atau yang di sekitar vena sentralis,
sehingga hepatosit di daerah perilobuler terlebih dahulu mengalami degenerasi.
Apabila daerah tersebut terus menerus terpapar bahan-bahan toksik, maka degenerasi
akan meluas menjadi nekrosa.
Tingginya persentase kerusakan hepatosit kelompok perlakuan kemungkinan
disebabkan oleh adanya senyawa AANP di daun, terutama DABA (
2,4-diamynobutyric acid). DABA adalah AANP yang homolog dengan ornitin, bekerja
dengan menghambat ornitine-carbamoyl transferase di hati, sehingga mengganggu
siklus pembentukan urea. Hal ini mengakibatkan kadar amonia dalam darah
meningkat sehingga memicu terjadinya toksisitas amonia. Hal ini mempengaruhi
22
Gambar 4 Hati tikus yang mengalami degenerasi berbutir (panah) pada kelompok kontrol. Pewarnaan HE, bar 20 µm.
23
Gambar 6 Hati tikus yang mengalami nekrosa pasca pemberian daun A.villosa tidak dikukus selama 4 minggu. Pewarnaan HE, bar 20 µm.
Pengaruh Pemberian Daun A.villosa Dikukus dan Tidak Dikukus terhadap Fungsi Hati Tikus
Hasil pemeriksaan fungsi hati yang meliputi kadar SGPT, SGOT, total
protein, albumin, dan globulin pasca pemberian daun A.villosa dikukus dan tidak
dikukus selama 4 minggu disajikan pada Tabel 5.
Tabel 5 Pengaruh pemberian daun A.villosa dikukus dan tidak dikukus selama 4 minggu terhadap fungsi hati tikus
Perlakuan SGPT (IU/L)
SGOT (IU/L)
Total Protein (g/dl)
Albumin (g/dl)
Globulin (g/dl)
Kontrol 49.50±8.09a 173.33±49.54a 8.10±0.36b 4.13±0.37b 4.07±0.45a
KS 80.50±6.44b 152.00±30.44a 7.18±0.44a 3.33±0.46ab 3.85±0.55a
TKS 75.67±12.09b 291.17±18.86a 6.98±0.31a 2.80±0.35a 3.68±0.48a
Keterangan : KS = Dikukus, TKS = Tidak Dikukus
24
Tabel 5 menunjukkan perbedaan nilai SGPT dan total protein yang nyata
antara kelompok perlakuan dengan kontrol (p<0.05), namun tidak berbeda nyata
antara kelompok KS dengan TKS (p>0.05). Nilai SGOT tidak berbeda nyata antara
kelompok perlakuan dengan kontrol maupun antara perlakuan (p>0.05).
SGPT merupakan enzim yang spesifik dihasilkan oleh sitoplasma hepatosit.
Oleh karena itu kadar SGPT yang lebih tinggi pada kelompok perlakuan
menunjukkan jumlah kerusakan hepatosit yang lebih banyak dibandingkan kelompok
kontrol. Hal ini sesuai dengan presentase degenerasi dan nekrosa hepatosit kelompok
perlakuan yang lebih besar dibandingkan kelompok kontrol. Kerusakan hepatosit
diduga disebabkan oleh senyawa sekunder tanin dan AANP A.villosa. Penyebab
lainnya adalah kemungkinan adanya senyawa lain yang bersifat toksik dalam
A.villosa yang tahan oleh pengukusan sehingga merusak hepatosit.
Apabila terjadi kerusakan sel, maka enzim SGPT akan dilepaskan ke dalam
cairan ekstraseluler karena terjadi perubahan permeabilitas membran plasma.
Perubahan permeabilitas membran plasma tersebut disebabkan oleh perbedaan
konsentrasi antara lingkungan dalam dan luar sel (Girindra 1988). Dengan demikian
pengukusan daun tidak mengurangi aktivitas senyawa yang bersifat hepatotoksik
pada A.villosa.
Kadar albumin kelompok TKS cenderung lebih rendah dari kelompok KS dan
berbeda nyata (p<0.05) dengan kelompok kontrol. Hasil ini sesuai dengan presentase
nekrosa hepatosit kelompok TKS yang lebih besar dibandingkan dengan kelompok
KS. Meningkatnya jumlah sel hati yang mengalami nekrosa menyebabkan penurunan
kemampuan hati untuk mensintesis albumin. Girindra (1988) menyatakan bahwa,
kasus hipoalbuminemia banyak ditemui pada hewan yang menderita
glomerulonefritis amiloidosis, diare karena parasit, nekrosa hati, fibrosa hati dan
hepatitis.
Albumin dan globulin darah disintesis di hati, kecuali beberapa jenis globulin.
Apabila terjadi kerusakan pada sel-sel hati, maka sintesis albumin dan globulin
terganggu. Gangguan sintesis albumin juga ditemui bila persediaan asam amino
25
dimana ketersediaan asam amino berkurang karena protein banyak terikat oleh tanin.
Pengukuran kadar globulin seluruh hewan coba tidak memperlihatkan perbedaan
yang nyata. Hal ini terjadi karena tidak semua jenis globulin disintesis oleh sel-sel
hati, sehingga kerusakan sel-sel hati hanya sedikit mempengaruhi nilai globulin
darah.
Kadar SGOT seluruh hewan coba tidak berbeda nyata, namun kelompok TKS
mempunyai nilai paling tinggi dibandingkan dengan kelompok lain, walaupun secara
statistik tidak berbeda nyata. Tingginya kadar SGOT tidak hanya berasal dari
kerusakan hepatosit, tetapi dapat diperoleh dari sumber lain yaitu jantung, ginjal,
pankreas, tulang dan otot (Girindra 1988). Oleh karena itu pengukuran kadar SGOT
tidak spesifik untuk mengetahui keadaan fungsi hati, walaupun tetap dapat digunakan
untuk menilai keadaan hati dan organ lainnya. Pada penelitian ini, tingginya kadar
SGOT kelompok TKS selain disebabkan oleh kerusakan hati kemungkinan
disebabkan adanya kerusakan di organ lain.
Pengaruh Pemberian Daun A.villosa Dikukus dan Tidak Dikukus Terhadap Gambaran Darah Tikus
Hasil pemeriksaan darah seluruh hewan coba disajikan pada Tabel 6. Pada
tabel tersebut dapat diketahui bahwa jumlah BDM dan BDP kelompok kontrol tidak
memperlihatkan perbedaan yang nyata dengan kelompok perlakuan. Pada
pemeriksaan hematokrit terlihat bahwa kelompok TKS lebih rendah dan berbeda
nyata (p<0.05) dengan kelompok KS dan kontrol. Begitu pula dengan pemeriksaan
kadar hemoglobin (Hb), kelompok TKS cenderung lebih rendah dibandingkan
dengan kelompok KS, namun sangat berbeda nyata dengan kontrol (p<0.05).
Fungsi utama BDM adalah pembawa hemoglobin yang selanjutnya membawa
oksigen dari paru-paru ke seluruh jaringan. Penurunan jumlah BDM menyebabkan
penurunan jumlah hemoglobin, dan salah satu penyebabnya adalah keadaan anemia
26
Tabel 6 Pengaruh pemberian daun A.villosa dikukus dan tidak dikukus selama 4 minggu terhadap gambaran darah tikus
Perlakuan BDM PCV Hb BDP
Keterangan : KS= Dikukus, TKS= Tidak Dikukus, BDM= Benda Darah Merah, BDP= Benda Darah Putih, PCV= Packed Cell Volume (Hematokrit), Hb= Hemoglobin
Huruf yang berbeda pada kolom yang sama menunjukkan perbedaan yang nyata (p<0.05)
Hemoglobin merupakan pigmen eritrosit (pemberi warna merah pada eritrosit)
yang terdiri dari protein kompleks terkonjugasi yang mengandung besi. Sintesis
hemoglobin, sebagian besar terjadi di dalam mitokondria sel hati. Apabila terjadi
defisiensi dari salah satu materi penyusunnya seperti ion Fe, maka hemoglobin tidak
akan terbentuk sempurna sehingga menyebabkan terbentuknya sel darah merah yang
lebih kecil dengan kandungan hemoglobin yang rendah. Apabila kejadian tersebut
berlangsung lama dapat menyebabkan anemia mikrositik hipokromik (Guyton 1992).
Anemia dapat ditentukan dengan melihat morfologi eritrosit seperti ukuran dan
intensitas warna eritrosit, atau dengan menghitung indeks eritrosit. Hasil perhitungan
indeks eritrosit disajikan pada Tabel 7.
Tabel 7 Hasil Perhitungan Indeks Eritrosit
Perlakuan MCV (fl) MCHC (g/dl)
Keterangan : KS = Dikukus, TKS = Tidak Dikukus, MCV = Mean Corpuscular Volume, MCHC = Mean Corpuscular Hemoglobin Concentration
Tabel 7 menunjukkan bahwa nilai MCV maupun MCHC kelompok KS dan
27
menunjukkan bahwa kelompok perlakuan mengalami anemia mikrositik hipokromik
yang disebabkan oleh defisiensi besi sehingga sintesis hemoglobin terganggu (Doxey
1983).
Menurut Makkar (2003), rendahnya kadar hemoglobin pada seluruh
kelompok perlakuan disebabkan adanya tanin yang memiliki kemampuan mengikat
zat besi. Hal yang sama juga disampaikan oleh Robbins dan Kumar (1995), bahwa
tanin yang terkandung dalam teh dapat menurunkan absorbsi zat besi. Kadar
hemoglobin kelompok TKS cenderung lebih rendah dibandingkan dengan kelompok
KS juga lebih rendah dan berbeda nyata dibandingkan dengan kelompok kontrol
(p<0.05). Hal ini disebabkan efek negatif tanin yang dapat mengikat zat besi.
Peningkatan nilai PCV dalam darah dapat ditemukan pada hewan bunting,
keadaan splenomegali, polisitemia primer dan sekunder dan pada individu yang
berada di daerah ketinggian. Sedangkan pada kondisi anemia, kongesti akibat
kegagalan jantung, dan kejadian retensi cairan ekstravaskuler terjadi penurunan nilai
PCV (Eastham 1984).
Kadar PCV pada kelompok TKS lebih rendah dan berbeda nyata (p<0.05)
dibandingkan kelompok KS maupun kontrol. Hal ini kemungkinan disebabkan oleh
adanya retensi cairan ekstravaskuler pada tubuh hewan coba kelompok TKS karena
ditemukan juga kerusakan pada ginjal (Kuswarini, komunikasi personal).
Benda darah putih merupakan salah satu sistem khusus dalam tubuh untuk
melawan agen infeksius. Jenis-jenis sel darah putih adalah netrofil, limfosit, monosit,
basofil dan eosinofil. Sel-sel tersebut bekerja dengan cara menghancurkan agen
penyerang dengan proses fagositosis dan membentuk antibodi (Guyton 1992).
Peningkatan jumlah sel darah putih (lekositosis) dihubungkan dengan
tingginya aktivitas pertahanan tubuh dalam melawan agen infeksius. Lekositosis
terutama netrofil akan terlihat meningkat pada infeksi bakteri. Jumlah limfosit yang
tinggi ditemui pada kasus limfosarkoma sedangkan jumlah monosit yang tinggi
ditemukan pada kasus brucellosis. Jumlah eosinofil ditemukan sangat tinggi pada
28
ditemukan pada kasus sirosis hati, anemia hemolitik kronis, splenomegali dan
polisitemia (Eastham 1984).
Penurunan lekosit (lekopenia) dapat ditemukan apabila terjadi apoplasia atau
hipoplasia sum-sum tulang dan stress, sehingga menurunkan jumlah limfosit dan
eosinofil, infeksi virus seperti feline enteritis (panleukopenia), swine fever, rinderpest
dan infeksi parvovirus yang menyebabkan neutropenia (Eastham 1984). Kadar BDP
pada seluruh hewan coba tidak memperlihatkan perbedaan yang nyata antar
masing-masing kelompok (p>0.05). Hal ini menunjukkan bahwa tidak ada proses peradangan
akibat pemberian daun A.villosa yang telah dikukus maupun tidak dikukus.
Pengaruh Pengukusan terhadap Senyawa Sekunder A.villosa
Berdasarkan pengamatan pada konsumsi pakan, bobot badan dan konversi
pakan yang tidak berbeda antara pemberian daun dikukus maupun tidak dikukus
menunjukkan bahwa pengukusan tidak mempengaruhi senyawa sekunder A.villosa
kecuali kelompok polifenol. Pengukusan tidak mengurangi aktivitas maupun
konsentrasi senyawa sekunder A.villosa yang bersifat hepatotoksik.
Bila dianalogkan dengan adanya perubahan mimosin menjadi DHP akibat
pemanasan, maka pada A.villosa kemungkinan terjadi perubahan senyawaan ADAB
menjadi DABA yang bersifat toksik. Hal ini ditunjukkan dengan meningkatnya
degenerasi hidropis hepatosit dan kadar SGPT kelompok KS. Peningkatan jumlah
nekrosa hepatosit pada kelompok TKS disebabkan hepatosit yang tidak bertahan
akibat pengaruh hepatotoksik senyawa sekunder A.villosa. Dilain pihak, pengukusan
dapat menurunkan kadar tanin, sehingga meningkatkan kadar hemoglobin kelompok
29
KESIMPULAN DAN SARAN
Kesimpulan
1. Pemberian daun A.villosa yang dikukus dan tidak dikukus tidak mempengaruhi
performa hewan coba.
2. Pengukusan daun A.villosa tidak mengurangi sifat hepatotoksisitas senyawa
sekunder A.villosa.
3. Pengukusan daun kemungkinan mengurangi daya ikat tanin terhadap zat besi.
4. Pemberian daun A.villosa tidak dikukus mengganggu fungsi hati dengan
menurunkan kadar albumin serum.
5. Pengukusan daun A.villosa mempengaruhi senyawa sekundernya.
Saran
1. Perlu dilakukan pengukuran kandungan senyawa AANP A.villosa pada daun
sebelum dikukus dan setelah dikukus.
2. Perlu dilakukan uji lanjut untuk mengetahui metabolisme senyawa AANP
30
DAFTAR PUSTAKA
Aryetti. 2003. Senyawa-senyawa Halogen Organik. Di dalam : Anwar NHM et al.,editor. Diktat Kuliah Kimia Organik. Bogor : IPB.
Bansi H. 2001. Potensi lamtoro merah (Acacia villosa) dan kaliandra putih (Caliandra tetragona) sebagai sumber protein baru bagi ternak ruminansia [skripsi]. Bogor : Fakultas Peternakan, Institut Pertanian Bogor.
Cheeke PR. 1989. Toxicants of Plant Origin. Volume ke-3, Protein and Amino Acid. Boca Raton, Florida : CRC Press.
Cheville NF. 1999. Introduction Veterinary Pathology. Edisi ke-2. USA : Lowa State University Press.
Corwin EJ. 2001. Buku Saku Patofisiologi. Pendit BU, Penerjemah; Prakaryaningsih E, editor. Terjemahan dari : Handbook Of Pathophysiology New Mexico Albuquerque.
D’Mello JPF. 2003. Food Safety Contaminations and Toxin. UK : CABI Publishing.
Doxey DL. 1983. Clinical Pathology and Diagnostic Procedures. London : Bailliere Tindall.
Eastham RD. 1984. Clinical Haematology. Edisi ke-6. Bristol : Wright.
Evans CS, Shah AJ, Adlard MW and Arce MLR. 1993. Non-protein amino acid in seed of neotropical species of acacia. Phytochemistry 32: 123-126.
Finco DR. 1980. Clinical Biochemistry of Domestic Animal. Edisi ke-3. New York : Academic Press.
Ganiswara SG, Setiabudy R, Suyatna FD, Nafrialdi, editor. 1995. Farmakologi dan Terapi. Edisi ke-4. Jakarta : Gaya Baru.
31
Girindra A. 1988. Biokimia Patologi Hewan. Bogor : Pusat Antar Universitas IPB.
Guyton AC. 1992. Fisiologi Manusia dan Mekanisme Penyakit. Edisi ke-3. Petrus Andrianto, penerjemah. Jakarta : Penerbit Buku Kedokteran EGC. Terjemahan dari : Human Physiology and Mechanism of Disease.
Harada T, Enomoto A, Boorman GA, and Maronpot RR. 1999. Liver and Gallblader. Di dalam : Maronpot RR. Pathology of The Mouse. Edisi ke-1. Vienna, USA : Cache River Press.
Hove L, Ndlovu LR, Sibanda S. 2003. The effects of drying temperature on chemical compotition and nutritive value of some tropical fooder shrubs. Animal Feed Science and Technology 59 : 231-241.
Jubb KVP, Kennedy PC, Palmer N. 1993. Pathology of Domestic Animals. Edisi ke-4. New York : Academic Press.
Jukema J dan Danimihardja S. 1997. Acacia. In: Hanum IF dan LJG Van der Maeser, (eds). Auxiliary Plants. Plant resources of south east asia. Prosea Bogor PP : 58-60.
Khotimah K. 2002. Pengaruh ekstrak jeruk nipis (Citrus aurantifolia) dan metode pengolahan pada kualitas daging broiler. http://digilib.itb.ac.id. [22 September 2006].
Krisdianto. 2004. Pengaruh perlakuan pendahuluan terhadap kecepatan pengeringan kayu mangium. http://www.dephut.go.id/informasi/ LITBANG/penelitian_ 04htm [22 September 2006].
Lowry JB, Petheram RJ, Tangendjaya B. 1992. Plants feed in village ruminant in Indonesia. ACIAR. Techincal Reports no. 22. Canberra.
Lu FC. 1995. Toksikologi Dasar. Asas, Organ Sasaran dan Penilaian Resiko. Edisi ke-2. Jakarta : UI Press.