CaO DAN MgO SEBAGAI KATALISATOR TERHADAP
REAKSI TRANSESTERIFIKASI MINYAK JARAK (RICINUS
COMMUNIS) MENJADI METIL ESTER ASAM LEMAK
SKRIPSI
MANGISI R.E TOBING
040802038
DEPARTEMEN KIMIA
FAKULTAS MATEMATIKA DAN ILMU PENGETAHUAN ALAM
UNIVERSITAS SUMATERA UTARA
MEDAN
2009
PERSETUJUAN
Judul : CaO DAN MgO SEBAGAI KATALISATOR
TERHADAP REAKSI TRANSESTERIFIKASI
MINYAK JARAK (RICINUS COMMUNIS)
MENJADI METIL ESTER ASAM LEMAK
Kategori : SKRIPSI
Nama : MANGISI R.E TOBING
Nomor Induk Mahasiswa : 040802038
Program Studi : SARJANA (S1) KIMIA
Departemen : KIMIA
Fakultas : MATEMATIKA DAN ILMU
PENGETAHUAN ALAM (FMIPA)
UNIVERSITAS SUMATERA UTARA
Disetujui di
Medan, Mei 2009
Komisi Pembimbing :
Pembimbing II, Pembimbing I,
Prof. Dr.Seri Bima Sembiring, MSc Drs. Nimpan Bangun, MSc
NIP. 130 535 842 NIP. 130 872 295
Disetujui oleh
Departemen Kimia FMIPA USU
Ketua,
Dr.Rumondang Bulan, MS
PERNYATAAN
CaO DAN MgO SEBAGAI KATALISATOR TERHADAP REAKSI TRANSESTERIFIKASI MINYAK JARAK (RECINUS COMMUNIS)
MENJADI METIL ESTER ASAM LEMAK
SKRIPSI
Saya mengakui bahwa skripsi ini adalah hasil kerja saya sendiri, kecuali beberapa kutipan dan ringkasan yang masing-masing disebutkan sumbernya.
Medan, Juni 2009
PENGHARGAAN
Pujian dan syukur penulis ucapkan kepada Tuhan Yesus Kristus atas berkat dan kasih setia-Nya, sehingga penulis dapat menyelesaikan penelitian dan penyusunan skripsi ini sesuai dengan Recana Dan waktu-Nya. Banyak pembelajaran yang didapatkan sehingga dalam setiap waktu Penulis semakin melihat Kebesaran-Nya
ABSTRAK
TRANSESTERIFICATION CASTOR OIL (RICINUS COMMUNIS) TO FATTY ACID METHYL ESTER WITH CaO AND MgO AS A CATALYSTATOR
ABSTRACT
DAFTAR ISI
Halaman
Persetujuan iii
Pernyataan iv
Penghargaan v
Abstrak vi
Abstrac vii
Daftar isi viii
Daftar gambar x
Daftar tabel xi
Daftar Grafik xii
Daftar Lampiran xiii
Bab 1 : Pendahuluan
1.1 Latar Belakang 1
1.2 Permasalahan 3
1.3 Tujuan Penelitian 3
1.4 Manfaat Penelitian 3
1.5 Lokasi Penelitian 4
1.6 Metodologi Percobaan 4
Bab 2 : Tinjauan Pustaka 5
2.1 Minyak jarak 5
2.2 Asam Lemak 8
2.2.1 Asam Ricinoleat 9
2.3 Metil ricinoleat 9
2.4 Reaksi Transesterifikasi 10
2.5 Sifat Unsur Golongan II A 13
2.6 Sifat unsur Periode III 14
2.7 Katalis 15
2.5.1 Katalis CaO 16
2.5.2 Katalis MgO 18
Bab 3 : Bahan Dan Metodologi Penelitian
3.1 Alat-alat 17
3.2 Bahan 18
3.3 Prosedur Penelitian 19
3.4 Bagan Penelitian 20
Bab 4 Hasil dan Pembahasan
4.1 Hasil 22
4.2 Pembahasan 25
Bab 5 Kesimpulan Dan Saran
5.1 Kesimpulan 32
5.2 Saran 32
Daftar Pustaka 33
DAFTAR GAMBAR
Halaman
Gambar 1 Analisa Kromatografi gas komponen asam lemak 37 minyak jarak castor oil
Gambar 2 Analisa Kromatografi gas hasil reaksi 38
transesterifikasi dengan perbandingan metanol dan minyak castor oil 12 : 1, waktu reaksi 4 jam, suhu 650C, katalis CaO dan co-solvent dietil eter
Gambar 3 Analisa Kromatografi gas hasil reaksi 40
transesterifikasi dengan perbandingan metanol dan minyak castor oil 12 : 1, waktu reaksi 4 jam, suhu 650C dan katalis CaO
Gambar 4 Analisa Kromatografi gas hasil reaksi 42
DAFTAR TABEL
Halaman
Tabel 1 Kandungan asam lemak castor oil 5
Tabel 2 Sifat fisik dan kimia minyak jarak castor oil 6 Tabel 4.1 Komponen pada asam lemak pada casor oil 26
Dari data Analisa kromatografi gas
DAFTAR GRAFIK
Halaman
Grafik 4.1 Grafik pengaruh perbandingan mol metanol dan 27 Minyak jarak pada reaksi transesterifikasi
Menggunakan katalis CaO terhadap Yield metil ester Pada suhu 650C dan waktu reaksi 6 jam
Grafik 4.2 Grafik pengaruh perbandingan mol metanol dan 28 Minyak jarak pada reaksi transesterifikasi
Menggunakan katalis MgO terhadap Yield metil ester Pada suhu 650C dan waktu reaksi 6 jam
Grafik 4.3 Grafik pengaruh perbandingan mol metanol dan 28 Minyak jarak pada reaksi transesterifikasi
Menggunakan katalis CaO dan MgO terhadap Yield metil ester pada suhu 650C dan waktu reaksi 6 jam
Grafik 4.4 Grafik pengaruh waktu reaksi pada reaksi transesterifikasi 29 Menggunakan katalis CaO terhadap Yield metil ester
Pada suhu 650C dan perbandingan mol methanol dan minyak jarak (12 : 1)
Grafik 4.5 Grafik pengaruh waktu reaksi pada reaksi transesterifikasi 29 Menggunakan katalis MgO terhadap Yield metil ester
Pada suhu 650C dan perbandingan mol methanol dan minyak jarak (12 : 1)
Grafik 4.6 Grafik pengaruh waktu reaksi pada reaksi transesterifikasi 30 Menggunakan katalis CaO dan MgO terhadap Yield
ABSTRAK
TRANSESTERIFICATION CASTOR OIL (RICINUS COMMUNIS) TO FATTY ACID METHYL ESTER WITH CaO AND MgO AS A CATALYSTATOR
ABSTRACT
BAB 1
PENDAHULUAN
1.1 Latar Belakang
Indonesia banyak tumbuh tanaman jarak (ricinus communis) secara sporadis.Tanaman
jarak (Ricinus communis L) termasuk dalam famili Euphorbiaceae, merupakan
tanaman tahunan yang hidup didaerah tropik dan subtropik yang dapat menghasilkan
minyak jarak (castor oil). Tumbuhan ini belum dibudidayakan karena dianggap belum
bernilai jual.
Minyak jarak (castor oil) mengandung asam lemak yaitu asam ricinoleat
(Asam 12-hidroksi) (89,5%) dan komponen asam lemak yang lain adalah asam
linoleat (4,2%), asam oleat (3 %), asam stearat (1 %), asam palmitat (1%), asam
dihidroxy stearat (0,7%) (Naughton, 1973)
Saat ini dunia banyak mengkaji tentang sumber energi yang terbaharui yaitu
lemak atau minyak nabati ataupun hewani . Bahan ini ditransformasikan menjadi alkil
metil ester asam lemak atau yang disebut juga FAME menggunakan katalis NaOH dan
KOH. Secara umum telah banyak dikaji metode pembuatan metil ester asam lemak
dari kelapa sawit dengan proses transesterifikasi dengan katalis NaOH dan KOH.
Reaksi memakai KOH dan NaOH sebagai katalis dapat digambarkan seperti dibawah
ini
NaOCH3 dengan adanya metanol dan trigliserida membentuk reaksi dibawah ini
O
H2C C
CH O
O
R'
H2C
C O O R'' C O R'''
+ CH3OH 3 R C
O
OCH3 +
OH H2C
HC OH
H2C OH katalis
Penggunaan katalis ini mempunyai kekurangan seperti sifat korosif yang tinggi
dan katalis ini tidak mungkin digunakan kembali sehingga dalam proses pembuatan
metil ester ini NaOH dibuang dalam bentuk larutan dan mengganggu lingkungan.
(Edgar, L, 2006)
Sebagaimana basa alkali dengan metanol membentuk metoksida secara insitu,
maka sifat ini juga dapat terjadi pada golongan II A. Misalnya MgO dan CaO dapat
juga menghasilkan Mg(OCH3)2 dan Ca(OCH3)2. Pemakaian oksida ini sebagai katalis
memberi keuntungan dimana MgO dan CaO memiliki kelarutan yang kecil dalam air.
Jika dipakai CaO sebagai katalis maka akan terbentuk reaksi seperti dibawah ini,
dimana reaksi ini tidak menghasilkan air.
CaO + CH3OH Ca O
OCH3 H
Keuntungan ini mendorong peneliti untuk menggunakan oksida golongan II A sebagai
katalis dalam reaksi transesterifikasi.
Penggunaan CaO sebagai katalis telah banyak dilaporkan. Suppes telah
menggunakan CaO sebagai katalis heterogen dalam reaksi alkoholisis untuk
menghasilkan monogliserida pada temperatur 200 – 220 0 C dengan lama reaksi 1 – 4 jam. (Suppes, 2001)
Zhu meneliti reaksi transesterifikasi minyak jarak curcas jatropha
katalis ini harus dicampurkan kedalam larutan karbonat terlebih dahulu kemudian
dikalsinasi pada temperatur yang tingi. (Liu. H, 2007)
Meneghetti telah melakukan etanolisis minyak jarak castor oil dengan katalis
NaOH dan katalis KOH menghasilkan yield metil ester asam lemak 50 – 60 %.
(Meneghetti,P, 2006)
Dalam kaitan ini akan dicoba memakai CaO dan MgO sebagai katalis dalam
reaksi transestrifikasi minyak jarak Ricinus Communis yang akan meningkatkan yield
metil ester
1.2 Permasalahan
Apakah CaO dan MgO dapat berfungsi sebagai katalis dalam reaksi
transesterifikasi minyak jarak (ricinus communis) menjadi metil ester
1.3 Tujuan Penelitian
Untuk memakai CaO dan MgO pada reaksi tranesterifikasi minyak jarak
(ricinus communis) menjadi metil ester asam lemak serta mendapatkan kondisi
optimum reaksi
1.4 Manfaat penelitian
- Hasil penelitian dapat memberikan informasi ilmiah terhadap industri metil ester dari
minyak Castor oil
- Pembentukan metil ester asam lemak dengan katalis CaO dan MgO yang tidak
1.5 Lokasi penelitian
Penelitian ini dilakukan di laborotarium kimia Anorganik FMIPA-USU
Medan, dan Analisa GC dilakukan di PPKS
1.6 Metodologi penelitian
Kalsium oksida didispersi dengan metanol menggunakan magnetik stirer.
Kemudian ditambahkan minyak jarak (recinus communis) dengan perbandingan
metanol dan trigliserida ( 12 : 1). Direfluks selama 2 jam pada suhu 65 0 C sambil diaduk dengan megnetik stirer. Disaring, filtrat diekstraksi dengan n-heksana. Lalu
dicuci dengan aquadest sebanyak 3 kali. Fase n-heksana ditambahkan dengan Natrium
Sulfat anhidrat. Disaring lalu diuapkan pelarutnya. Dihasilkan metil ester asam lemak
selanjutnya dianalisa dengan gas kromatografi.
Perlakuan yang sama dilakukan dalam reaksi tranesterifikasi minyak jarak
BAB 2
TINJAUAN PUSTAKA
2.1 Minyak Jarak (Castor Oil)
Castor oil atau minyak jarak dihasilkan dari biji tanaman jarak (ricinus communis),
termasuk dalam famili Euphorbiaceae yang banyak tumbuh didaerah tropik dan
subtropik. Castor oil mengandung trigliserida asam-asam lemak terutama asam
ricinolet dengan konsentrasi 85% sehingga sering disebut trigliserida asam ricinoleat.
Minyak jarak mempunyai kandungan asam lemak dengan komposisi sebagai
berikut:
Tabel 1. Kandungan asam lemak
Asam Lemak Jumlah ( % )
Asam Risinoleat 86
Asam Oleat 8,5
Asam Linoleat 3,5
Asam Stearat 0,5 – 2,0
Asam dihidroksi Stearat 1 – 2
Minyak jarak mempunyai rasa asam dan dapat dibedakan dengan trigliserida
lainnya karena bobot jenis, kekentalan (viskositas) dan bilangan asetil serta
kelarutannya dalam alcohol nilainya relative tinggi. Castor alkohol larut dalam
etil-alkohol 95 persen pada suhu kamar serta pelarut organik yang polar, dan sedikit larut
dalam golongan hidrokarbon alifatis. Kandungan tokoferol relative kecil (0,05%),
serta kandungan asam lemak esensial yang sangat rendah menyebabkan mnyak jarak
tersebut berbeda dengan minyak nabati lainnya. (Ketaren, 1986)
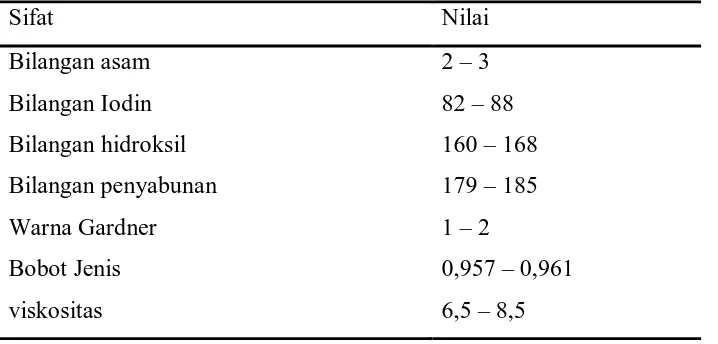
Tabel 2. Sifat Fisik Dan Kimia Minyak Jarak
Sifat Nilai
Bilangan asam 2 – 3
Bilangan Iodin 82 – 88
Bilangan hidroksil 160 – 168
Bilangan penyabunan 179 – 185
Warna Gardner 1 – 2
Bobot Jenis 0,957 – 0,961
viskositas 6,5 – 8,5
(Naughton, 1973)
Penggunaan produk-produk turunan castor oil yang banyak diproduksi didunia
berdasarkan urutan nilai produksinya adalah minyak pelumas, kosmetik, pengobatan,
detergen, sabun, pelapis, serat nylon dan Textil
Berikut ini disajikan beberapa contoh produk yang dapat dihasilkan dari castor oil.
1. Minyak pelumas
Castor oil memiliki viskositas pada temperatur yang tinggi dan cair pada
temperatur yang rendah sehingga dapat dijadikan sebagai minyak pelumas yang cukup
bagus. Perkembangan pasar dan teknologi telah mengarahkan penggunaan castor oil
untuk dijadikan bahan baku minyak pelumas karena kualitasnya yang lebih baik
daripada pelumas berbasis meineral dan lebih ramah lingkungan karena pelumas ini
2. Bahan Pencelupan Textil
Castor oil digunakan sebagai bahan pencelup textil umumnya dalam bentuk
castor oil yang disulfasi (sulfated castor oil) seperti minyak merah turki.
3. Sabun
Castor oil dapat memberikan sifat transparan terhadap sabun sehingga banyak
digunakan dalam industri sabun transparan. Sodium ricinoelat dan sulfo ricinoleat
dalam sabun castor oil dapat menghilangkan bakteri sehingga banyak digunakan
dalam industri sabun desinfektan.
4. Cat dan Permis
Penemuan dan proses dehidrasi castor oil telah meningkatkan perkembangan
penggunaan castor oil sebagai salah satu bahan penunjang industri cat dengan
kemampuan castor oil yang memberikan sifat berpendar terhadap cahaya dan anti
kuning pada cat sehingga dapat menghasilkan cat yang berwarna putih bersih. Castor
oil juga banyak dimanfaatkan dalam industri percetakan dan resin.
5. Isolator
Turunan castor oil dalam bentuk urethane banyak untuk memproduksi basa
yang dapat digunakan sebagai bahan isolasi dan penguat. Selain untuk isolator
urethane juga dapat digunakan untuk memproduksi karet elastis.
6. Serat Nylon
Serat Nylon-11 banyak diproduksi dengan bahan baku castor oil polyamide
karena dapat menghasilkan sifat-sifat tahan abrasi, sangat elastis dan sifat peregangan.
2.2 Asam Lemak
Asam lemak bersama-sama dengan gliserol, merupakan penyusun utama minyak
nabati atau lemak dan merupakan bahan baku untuk semua lipida pada makhluk
hidup. Asam ini mudah dijumpai dalam minyak masak (goreng), margarin, atau lemak
hewan dan menentukan nilai gizinya. Secara alami, asam lemak bisa berbentuk bebas
(karena lemak yang terhidrolisis) maupun terikat sebagai gliserida. Asam lemak
merupakan salah satu basic oleochemical.
Asam lemak tidak lain adalah asam alkanoat atau asam karboksilat berderajat
tinggi (rantai C lebih dari 6). Rumus molekulnya adalah : CnH2n O2. Asam lemak
merupakan asam lemah, dan dalam air terdisosiasi sebagian.
Umumnya berfase cair atau padat pada suhu ruang (27 °C). Semakin panjang rantai C
penyusunnya, semakin mudah membeku dan juga semakin sukar larut.
Keberadaan ikatan ganda pada asam lemak tak jenuh menjadikannya memiliki
dua bentuk: cis dan trans. Semua asam lemak nabati alami hanya memiliki bentuk cis
(dilambangkan dengan "Z"). Asam lemak bentuk trans (trans fatty acid,
dilambangkan dengan "E") hanya diproduksi oleh sisa metabolisme hewan atau dibuat
secara sintetis.
Akibat polarisasi atom H, asam lemak cis memiliki rantai yang melengkung.
Asam lemak trans karena atom H-nya berseberangan tidak mengalami efek polarisasi
yang kuat dan rantainya tetap relatif lurus. (Tambun , 2006)
2.2.1 Asam Risinoleat
Asam risinoleat (Asam 12-hidroksi-9-Oktadekanoat)
CH3 (CH2)5 C CH2 CH CH (CH2)7 COOH
Memiliki 18 atom karbon dengan 1 gugus hidroksi pada atom karbon ke 12
dan ikatan rangkap Cis antara atom karbon 9 dan 10. Berat molekul asam risinoleat
298,46. Adanya asam lemak ricinoleat pada castor oil membuat castor oil memiliki
sifat yang khusus. Castor oil memilki bilangan hidroksi dan asetil yang tinggi,
bilangan Iodin yang sebanding dengan minyak lain. Viskositas dan berat jenis yang
tinggi.
Tidak seperti minyak yang lain, castor oil bercampur dengan alkohol dan
sedikit larut dalam petroleum eter pada temperatur kamar. (Naughton, 1973)
2.3 Metil Risinoleat dari Minyak Jarak (Ricinus Communis)
Metil risinoleat dapat dengan mudah diisolasi dari ester minyak jarak dengan
adsorbsi menggunakan Kromatografi kolom lapis Tipis. Gugus hidroksi yang lebih
polar lebih kuat diadsorbsi dibandingkan pengotor yang kurang polar. Pelarut yang
digunakan untuk mengisolasi adalah Petroleum ether dengan dietil ether dengan
perbandingan (4 : 1) tetapi untuk menghasilkan hasil yang lebih bagus digunakan
petroleum ether dengan propana-2-ol dengan perbandingan (99 : 1). Penggunaan
pelarut ini memiliki keuntungan yaitu ketika pelarut itu telah digunakan maka dapat
diperoleh kembali dengan mudah. (Emanuele, 1984)
2.4 Reaksi Transesterifikasi
Pembentukan ester merupakan salah satu reaksi yang penting dalam pemberian nilai
tambah dari lemak hewan dan minyak tumbuhan.
Reaksi pembentukan ester diklasifikasikan kedalam dua reaksi yaitu
1. Esterifikasi yaitu reaksi antara Asam karboksilat dengan Alkohol
RCOOH .+ MeOH RCOOMe + H2O
2. Transesterifikasi dibagi kedalam tiga jenis reaksi yaitu:
1. Interesterifikasi yaitu pembentukan ester dari ester dengan ester
2. Alkoholisis yaitu pembentukan ester dari reaksi suatu ester dengan alkohol
3. Asidolisis yaitu reaksi antara ester dengan asam karboksilat.
Reaksi transesterifikasi menggunakan katalis heterogen memilki parameter penting
untuk diperhatikan seperti temperatur, luas dari muatan katalis, perbandingan mol
antara metanol dengan minyak dan waktu reaksi. ( Viswanathan, 2005)
Transesterifikasi dari miyak nabati menjadi biodiesel [metil ester asam lemak,
MEAL] dapat dikatalisis dengan basa dan asam .Katalis basa termasuk katalis basa
homogen dan katalis basa heterogen. Secara umum menggunakan katalis homogen
seperti NaOH, KOH dan alkosidanya. Transesterifikasi dengan menggunakan katalis
alkali homogen lebih cepat daripada menggunakan transesterifikasi katalis asam. Dan
harus dipertimbangkan untuk memisahkan katalis dari larutan produk.
Katalis basa heterogen mempunyai banyak keuntungan: yaitu tidak korosif,
ramah lingkungan dan menghasilkan sedikit masalah pembuangan. Sementara itu,
lebih mudah memisahkanya dari larutan produk dan dapat dirancang untuk
memberikan aktivitas tertinggi, selektivitas dan katalis dengan daya tahan yang lebih
lama .Sekarang ini, banyak tipe katalis heterogen yang telah ditemukan untuk
transesterifikasi dari minyak sayuran menjadi biodiesel, seperti logam oksida alkali
tanah, berbagai senyawa logam alkali seperti alumina atau zeolit .Bagaimanapun,
untuk kebanyakan pendukung katalis-katalis alkali, komposisi aktifnya mudah
berkarat oleh metanol dan mempunyai waktu hidup yang singkat. CaO merupakan
basa yang lebih kuat dan CaO telah dipelajari sebagai katalis basa kuat padat oleh
banyak peneliti.
2.5 Sifat-sifat unsur Golongan II A
Unsur alkali tanah merupakan logam golongan II A dalam sistem periodik. Unsur ini
mempunyai elektron valensi 2, Yang cenderung melepas elektron , sehingga
bermuatan +2. Karena elektron valensinya mudah terlepas, unsur alkali tanah bersifat
mudah teroksidasi, walaupun tidak semudah golongan alkali. Jadi, unsur golongan
Golongan ini dikatakan alkali ”tanah” karena unsur ini agak sukar larut dalam
air dan tetap stabil pada temperatur tinggi. Unsur alkali pada kulit terluarnya
mempunyai 1 elektron. Unsur alkali tanah pada kulit terluarnya mempunyai 2 elektron
sehingga pada unsur alkali tanah gaya tarik inti dengan elektron pada kulit terluarnya
akan lebih kuat daripada golongan alkali, yang mengakibatkan sebagai berikut:
- Unsur alkali tanah memiliki jari-jari yang lebih kecil dan energi ionisasi
lebih besar dibandingkan dengan unsur alkali
- Unsur alkali tanah merupakan logam keras yang mempunyai titik leleh
tinggi.
Kecuali Be semua unsur golongan alkali tanah jika bereaksi dengan air, akan
membentuk basa kuat dengan H2.
Senyawa yang terbentuk dengan unsur alkali tanah akan membentuk ikatan sebagai
berikut:
- Ca, Sr dan Ba akan membentuk ikatan ionik
- Mg akan membentuk ikatan ion, tetapi dalam senyawa organik akan
membentuk ikatan kovalen, seperti CH3MgBr dan Mg(C2H5)2
- Be sebagian besar membentuk ikatan kovalen. (Lestari S, 2006)
Konfigurasi elektron secara langsung mempengaruhi sifat unsur-unsur. Konfigurasi
elektron terluar secara langsung mempengaruhi sifat-sifat atom unsur-unsur golongan
utama. Keragaman periodik dari sifat-safat fisika dari unsur mencerminkan perbedaan
dalam struktur. Karakter logam unsur-unsur menurun dalam satu periode melalui
metaloid ke nonlogam dan meningkat dari atas kebawah dalam golongan tertentu
unsur-unsur golongan utama. Ukuran atom yang didefenisikan melalui jari-jari atom
juga beragam secara periodik, berkurang dari kiri kekanan dan bertambah dari atas
kebawah.
Energi ionisasi adalah kecenderungan suatu atom untuk menahan lepasnya
satu elektron. Makin besar energi ionisasi, makin kuat inti menahan elektron. Afinitas
elektron adalah ukuran kecenderungan suatu atom untuk memperoleh sebuah elektron.
Secara umum logam memilik energi ionisasi yang rendah dan nonlogam memiliki
2.6 Sifat-sifat Unsur Periode III
Salah satu cara untuk membandingkan sifat-sifat unsur golongan utama dalam
satu periode adalah dengan mengkaji dari deretan senyawa yang serupa. Karena
oksigen bergabung dengan hampir semua unsur, maka akan dibandingkan sifat-sifat
oksida unsur-unsur periode ketiga untuk melihat logam berbeda dari metaloid dan
non-logam.
Kecenderungan oksigen untuk membentuk oksida dengan semua unsur
disebabkan oleh logam yang memiliki energi ionisasi yang rendah yaitu Golongan I
A, II A dan aluminium. Jadi Na2O, MgO dan Al2O3 adalah senyawa-senyawa ionik
seperti yang terlihat dari titik leleh dan titik didihnya yang tinggi. Kebanyakan oksida
dapat digolongkan sebagai asam atau basa, bergantung pada apakah oksida ini
menghasilkan asam atau basa ketika dilarutkan dalam air atau bereaksi pada asam atau
basa dalam proses tertentu. Beberapa oksida bersifat amfoter yang berarti
oksida-oksida tersebut bersifat asam atau basa. Dua oksida-oksida pertama dalam periode ketiga
Na2O dan MgO adalah oksida basa. Misalnya Na2O bereaksi dengan air membentuk
natrium oksida (yang bersifat basa).
Magnesium oksida agak sulit larut, oksida ini tidak bereaksi dengan air dalam
tingkat yang teramati. Tetapi oksida tersebut bereaksi dengan asam dengan cara yang
menyerupai reaksi asam-basa:
MgO + 2 HCl(aq) MgCl2(aq) + H2O(l)
Aluminium oksida bahkan lebih sulit larut bila dibandingkan dengan magnesium
oksida: oksida ini juga tidak larut dengan air. Tetapi zat ini menunjukkan sifat-sifat
basa jika bereaksi dengan asam dan bersifat asam jika bereaksi dengan basa. Jadi
Al2O3 digolongkan sebagai oksida amfoter. Oksida amfoter yang lain adalah ZnO,
BeO dan Bi2O3.
Kajian singkat mengenai oksida unsur-unsur periode ketiga ini menunjukkan
bahwa dengan menurunnya karakter logam dari unsur-unsur dari kekanan dalam satu
asam. Karena karekter logam unsur-unsur golongan utama meningkat dari atas
kebawah kita mengharapkan oksida unsur-unsur dengan nomor atom yang lebih tinggi
akan bersifat lebih basa dibandingkan dengan unsur-unsur yang lebih ringan.
(Chang,R. 2005)
2.7 Katalis
Katalis adalah zat yang meningkatkan laju reaksi kimia tanpa ikut terpakai. Katalis
dapat bereaksi membentuk zat antara, tetapi akan diperoleh kembali dalam tahap
reaksi berikutnya. Katalis mempercepat reaksi dengan menyediakan serangkaian
tahapan elementer dengan kinetika yang lebih baik dibandingkan jika tanpa katalis.
Dalam banyak kasus, katalis meningkatkan laju dengan cara menurunkan energi
aktivasi reaksinya.
Ada dua jenis katalis yang digunakan
1.Katalis heterogen
Dalam katalis heterogen, reaktan dan katalis berbeda fasa. Biasanya katalis berupa
padatan dan reaktan berwujud gas atau cairan. Katalis heterogen sejauh ini adalah
jenis katalis yang paling penting dalam kimia industri, terutama dalam sintesis
berbagai bahan kimia penting
2. Katalis homogen
Dalam katalis homogen, reaktan dan katalis terdispersi dalam satu fasa biasanya fasa
cair. Katalis asam dan basa adalah jenis katalis homogen yang paling penting dalam
larutan cairan. (Raymond Chang, 2005)
Keuntungan dari katalis homogen adalah kespesifikannya dan tidak
homogen ini adalah sulitnya katalis ini untuk dipisahkan dari produknya. Katalis dapat
terdegradasi dan harganya relatif tinggi.
Katalis heterogen memiliki keuntungan dibandingkan katalis homogen
khususnya dalam pemisahannya karena produk yang terlarut dalam medium reaksi
dapat dipisahkan dari katalisnya dengan menyaringnya.(Leach.B.E,1983)
Katalis heterogen bereaksi pada permukaan bahan. Reaksi fase gas dan fase
cair dikatalisa oleh katalis heterogen biasanya lebih mungkin terjadi di permukaan
katalis dari pada di fase gas atau fase cair. Untuk alasan ini maka kadangkala katalis
heterogen disebut katalis kontak.
Proses katalis heterogen sedikitnya dapat melalui 4 tahap:
1. Difusi produk dari permukaan katalis
2. Reaksi reaktan yang diserap
3. Aktivasi penyerapan reaktan
4. Adsorpsi reaktan pada permukaan katalis
(Holzchaw,1988)
2.7.1 Katalis CaO
Oksida dari semua unsur logam telah dikenal dan oksida-oksida ini menunjukkan
beragam struktur, asam basa, dan hantaran. Oksida dapat membentuk rantai satu
dimensi, lapisan dua dimensi atau struktur 3-dimensi.
Oksida logam dapat bersifat basa, amfoter atau asam bergantung identitas
logamnya. Lebih lanjut, tentang sifat fisik yang ditunjukkan juga sangat luas, dari
isolator, semikonduktor, konduktor bahkan superkonduktor. Komposisi oksida logam
dapat stoikiometrik sederhana, stoikiometrik tetapi tidak sederhana, atau kadang
Gamping dapat digunakan untuk pengobatan, insektisida pakan ternak dan
tanaman, absorbsi gas, presipitasi, dehidrasi dan kaustisasi. Gamping juga dapat
digunakan sebagai pereaksi dalam proses sulfit, dalam pembuatan kertas, pembersihan
bulu dalam pengolahan kulit, pembuatan semen dan baja bermutu tinggi, pelunakan
air, pemulihan amonia sebagai hasil samping serta pembuatan sabun, karet dan bata
pasir gamping.
Kalsium oksida diperoleh dari pemanasan kalsium karbonat (CaCO3) dan
kalsium sulfat (CaSO4).
Kalsinasi
CaCO3 900
0 C
CaO + CO2
CaSO4 1149
0 C
CaO + SO3
Hidrasi
CaO + H2O Ca(OH)2
Pada proses kalsinasi volumenya menciut dan pada waktu hidrasi volumenya
berkembang. (Austin, 1996)
Sekarang ini banyak tipe katalis heterogen yang digunakan dalam proses
transesterifikasi minyak nabati untuk menghasilkan biodiesel seperti oksida logam
alkali tanah, logam alkali yang didukung oleh alumina dan Zeolit.
Katalis basa heterogen mempunyai banyak keuntungan dalam
penggunaannya. Katalis ini tidak korosif, ramah lingkungan dan katalis tidak akan
menimbulkan masalah yang baru.
Penggunaan CaO sebagai katalis basa heterogen dalam proses transesterifikasi
memiliki banyak keuntungan seperti
- Aktivitas katalisnya yang tinggi
- Kondisi reaksi yang sederhana
- Waktu penggunaan katalis yang lama
2.7.2 Katalis MgO
Magnesium adalah salah satu unsur yang paling luas penyebarannya dan merupakan
1,9 % dari kerak bumi. Biasanya magnesium terdapat dalam bentuk klorida, silikat,
hidrat, oksida, sulfat atau karbonat.
Semua unsur golongan II A jika dibakar dengan oksigen membentuk oksida
(MO). Salah satu contohnya adalah MgO. MgO diperoleh dari pemanasan MgSO4 dan
MgCO3.
MgSO4 895
0 C
MgO + SO3
MgCO3 540
0 C
MgO + CO2
Bila magnesium karbonat atau hidroksida dipanaskan terbentuklah magnesium
oksid. Oksida ini dapat digunakan untuk bermacam tujuan misalnya vulkanasi karet,
sebagai bahan untuk membuat berbagai senyawa magnesium lainnya, sebagai bahan
refraktori dan sebagai abrasif. Magnesium oksida juga banyak dipakai dalam sistem
pengendalian pencemaran untuk menyingkirkan sulfur dioksida dari gas cerobong
BAB 3
METODOLOGI PENELITIAN
3.1 Alat- Alat Penelitian
Nama Alat Ukuran Mereck
Erlenmeyer 500 mL Pyrex
Gelas Ukur 50 mL Pyrex
Neraca Analitis
Labu leher tiga 250 mL Pyrex
Statif dan klem
Pengaduk magnetik
Kondensor
Pendingin liebig Quickfit
Corong Pyrex
Hot plate Stirer Gallenkamp
Termometer 2000C Fisher
Autoclave
3.2. Bahan – bahan
Nama bahan Mereck
Castor Oil Bratachem
Dietil eter p.aE’Mereck
N-heksana p.a E’Mereck
Methanol p.a E’Mereck
CaO p.a E’Mereck
MgO p.a E’Mereck
Natrium Sulfat Anhidrat p.a E’Mereck
3.3 Bagan Penelitian
3.3.1 Proses Transesterifikasi antara Metanol dan Minyak Jarak Menggunakan Katalis CaO
Kalsium Oksida
dimasukkan kedalam labu leher tiga
metanol kering
didispersikan
minyak jarak (Resinus Communis)
direfluks selama 2 jam
disaring
Filtrat Residu
dietil eter
HCl 5 N
terbentuk 2 lapisan
lapisan atas lapisan bawah
dicuci dengan akuadest
Na2SO4 anhidrat
disaring
filtrat
diuapkan pelarutnya
Metil Ester Asam Lemak
Analisa Kromatografi gas
3.4 Prosedur Penelitian
Kedalam labu leher tiga dimasukkan 0,6 mol metanol kering (19,2 g) untuk
mensuspensikan 0,06 mol CaO (3,7 g) sambil diaduk dengan magnetik stirer.
Kedalam campuran ditambahkan 0,05 mol castor oil (46,6 g) kemudian dipanaskan
pada suhu 650C selama 2 jam dengan kecepatan pengadukan konstan. Campuran hasil reaksi disentrifuse selama 30 menit, maka terbentuk 2 fase yaitu fase padat dan fase
cair. Fase cair dicampur dengan dietil eter kemudian ditambahkan 5 mL HCl 5 N
sebanyak 3 kali, dipisahkan. Lapisan atas dicuci dengan 10 mL aquadest sebanyak 3
kali. Lalu fase dietil eter ditambahkan Na2SO4 anhidrat, didiamkan, disaring
kemudian didestilasi. Metil ester murni dianalisa dengan kromatografi gas. (Suppes,
2001)
Perlakuan yang sama dibuat dengan variasi perbandingan mol metanol dan
castor oil ( 9 : 1, 12 : 1 dan 15 : 1), variasi waktu ( 4 dan 6 jam) dan katalis (MgO).
Hasil analisa kromatografi gas dilihat pada lampiran 8 dan 9.
3.4.1 Proses Transesterifikasi Minyak Jarak (Ricinus Communis) Menjadi Metil Ester Asam Lemak dengan Katalis CaO Dalam Media Pelarut dietil eter
Kedalam autoclave dimasukkan 1,2 mol metanol kering (38,4 g) untuk
mensuspensikan 0,12 mol CaO (7,4 g) sambil diaduk dengan magnetik stirer.
Kedalam campuran ditambahkan 0,1 mol castor oil (93,2 g) kemudian dipanaskan
pada suhu 650C selama 4 jam dengan kecepatan pengadukan konstan. Kemudian didiamkan maka terbentuk 2 fase yaitu fase padat dan fase cair. Fase cair dicampur
dengan dietil eter kemudian ditambahkan 10 mL HCl 5 N sebanyak 3 kali, dipisahkan.
Lapisan atas dicuci dengan 20 mL aquadest sebanyak 3 kali. Lalu fase dietil eter
ditambahkan Na2SO4 anhidrat, didiamkan, disaring kemudian didestilasi. Metil ester
murni dianalisa dengan kromatografi gas. (Suppes, 2001)
3.5 Karekterisasi Produk
3.5.1 Penentuan Komposisi Asam Lemak
Penentuan Kadar Produk metil ester menggunakan instrumen Kromatografi
Gas Agilent Technologies yang didukung dengan perangkat lunak Agilent
Technologies Coorporation. Volume sebanyak 2 μliter, kolom yang digunakan adalah
J&W DB-624 dengan panjang kolom 30 m. Fase diam adalah silika dan mengunakan
detektor Flame Ionization Detector (FID).
3.5.2 Perhitungan Yield Metil Ester
Yield dihitung dengan cara membandingkan berat produk hasil transesterifikasi
dengan berat castor oil yang digunakan berdasarkan persamaan :
Yield=
CastorOil produk m
m
BAB 4
HASIL DAN PEMBAHASAN
4.1 HASIL
4.1.1 Analisis Komposisi Asam Lemak Pada Minyak jarak (Ricinus Communis)
Minyak jarak (ricinus communis) yang digunakan dalam penelitian ini adalah minyak
jarak yang dijual di Bratachem. Selanjutnya minyak jarak ini ditransesterifikasi
dengan metanol menggunakan katalis Oksida alkali tanah ( CaO dan MgO) diperoleh
metil ester minyak jarak Castor Oil.
Berdasarkan hasil analisis kromatografi gas(GC) yang dilakukan terhadap
metil ester castor oil, maka komponen asam lemak yang diperoleh dari minyak jarak
[image:35.595.100.533.569.676.2]castor oil sebagai berikut
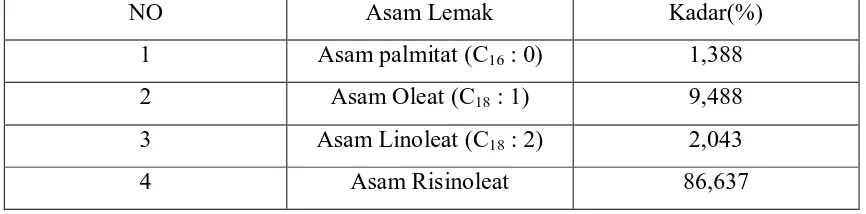
Tabel 4.1 Komponen Asam Lemak pada Castor Oil dari data analisa Kromatografi gas (lampiran 6)
NO Asam Lemak Kadar(%)
1 Asam palmitat (C16 : 0) 1,388
2 Asam Oleat (C18 : 1) 9,488
3 Asam Linoleat (C18 : 2) 2,043
Data hasil pengaruh perbandingan mol, waktu reaksi dan jenis katalis terhadap reaksi
transesterifikasi minyak jarak (Ricinus Communis) adalah sebagai berikut
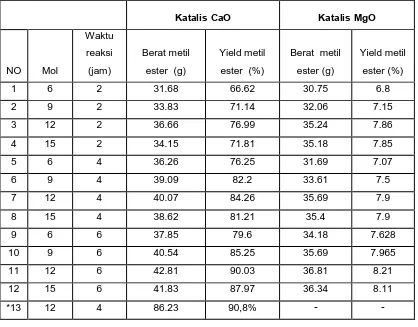
Tabel 4.2 Data hasil reaksi transesterifikasi Minyak Jarak (Ricinus Communis) Dengan Katalis CaO dan MgO
Katalis CaO Katalis MgO
NO Mol
Waktu reaksi (jam)
Berat metil ester (g)
Yield metil ester (%)
Berat metil ester (g)
Yield metil ester (%) 1 6 2 31.68 66.62 30.75 6.8 2 9 2 33.83 71.14 32.06 7.15 3 12 2 36.66 76.99 35.24 7.86 4 15 2 34.15 71.81 35.18 7.85 5 6 4 36.26 76.25 31.69 7.07 6 9 4 39.09 82.2 33.61 7.5 7 12 4 40.07 84.26 35.69 7.9 8 15 4 38.62 81.21 35.4 7.9 9 6 6 37.85 79.6 34.18 7.628 10 9 6 40.54 85.25 35.69 7.965 11 12 6 42.81 90.03 36.81 8.21 12 15 6 41.83 87.97 36.34 8.11
*13 12 4 86.23 90,8% - -
Catatan
(*) Reaksi transesterifikasi minyak jarak castor oil dengan perbandingan mol metanol
dan minyak jarak (12 : 1), waktu reaksi 4 jam, katalis CaO dengan co-solvent dietil
[image:36.595.107.525.209.536.2]4.1.2 Produk Hasil Reaksi Transesterifikasi Minyak jarak (Ricinus Communis)
Reaksi transesterifikasi minyak jarak( ricinus communis) menggunakan katalis oksida
logam alkali tanah ( CaO dan MgO) menghasilkan senyawa campuran yang terdiri
dari metil ester, monogliserida, digliserida dan trigliserida.
1. Dengan Katalis MgO
Reaksi transesterifikasi minyak jarak (ricinus communis) menjadi metil ester
dengan perbandingan metanol : minyak jarak(mol/mol) 12 : 1 dan waktu reaksi 6 jam
diperoleh data sebagai berikut
Monogliserida : 0,0759 %
Digliserida : 13,6519%
Metil ester : 10,4169%
Trigliserida : 75,8553%
2. Dengan Katalis CaO
Reaksi transesterifikasi minyak jarak (ricinus communis) menjadi metil ester
dengan perbandingan metanol : minyak jarak(mol/mol) 12 : 1 dan waktu reaksi 6 jam
diperoleh data sebagai berikut
Monogliserida : 0,195 %
Digliserida : 1,6741 %
Metil ester : 98,0019%
Trigliserida : 0,1325 %
3. Dengan Katalis CaO dan Co-solvent dietil eter
Reaksi transesterifikasi minyak jarak (ricinus communis) menjadi metil ester
dengan perbandingan metanol : minyak jarak(mol/mol) 12 : 1 dan waktu reaksi 4 jam
diperoleh data sebagai berikut
Monogliserida : 0,5844 %
Digliserida : 1,2079%
Metil ester : 98,175%
4.2 PEMBAHASAN
4.2.1 Pembuatan Metil Ester dengan Katalis CaO
Minyak jarak (recinus communis) ditransesterifikasi dengan metanol
menggunakan katalis CaO sehingga menghasilkan metil ester asam lemak campuran
minyak jarak dengan mekanisme reaksi sebagai berikut:
R' C
O
O CH2
CH O C O "R
CH2 O C R"'
+
O
R' C O
O CH2
CH O C O "R
CH2 O C R"' OCH3
O
-R' C
O
O CH2
CH O C O "R
CH2 O C R"' OCH3
O
-R' C
O
O CH2
CH O C O "R
CH2 O
-+ R C O
OCH3
R' C
O
O CH2
CH O C O "R
CH2 O -+
R' C O
O CH2
CH O C O "R
CH2 OH
+ CaO CaO + CH3OH
Ca O OCH3 H
Ca O H
Ca O OCH3 H
R' C
O
O CH2
CH O C O "R CH2 O C O R
+ 3 CH3OH 3 R C O
OCH3 + HC OH
CH2
CH2
OH
4.2.2 Pembuatan Metil Ester dengan Katalis MgO
R' C
O
O CH2
CH O C O "R
CH2 O C R"'
+
O
R' C O
O CH2
CH O C O "R
CH2 O C R"' OCH3
O
-R' C
O
O CH2
CH O C O "R
CH2 O C R"' OCH3
O
-R' C
O
O CH2
CH O C O "R
CH2 O
-+ R C O
OCH3
R' C
O
O CH2
CH O C O "R
CH2 O
-+
R' C O
O CH2
CH O C O "R
CH2 OH
+ MgO MgO + CH3OH
Mg O OCH3 H
Mg O H
Mg O OCH3 H
R' C
O
O CH2
CH O C O "R CH2 O C O R
+ 3 CH3OH 3 R C O
OCH3 + HC OH
CH2
CH2
OH
Mekanisme dari transesterifikasi gliserida menjadi biodiesel diikuti dengan hadirnya
anion metoksida. Pada langkah pertama, anion metoksida menyerang atom karbon
karbonil dari molekul trigliserida untuk membentuk intemediate tetrahedral. Pada
langkah kedua, intermediate tetrahedral meneruskan atom H+ dari permukaan CaO .Intemediate tetrahedral juga dapat bereaksi dengan metanol untuk membentuk anion
metoksida. Pada langkah terakhir, penataan ulang dari intermediate tetrahedral
menghasilkan pembentukan biodiesel dan gliserol. Keseluruhan reaksi dapat
diperlihatkan pada ,dimana R1, R2 dan R3 mewakili gugus alkil rantai panjang.
60
70
80
90
100
3
6
9
12
15
18
Mol Methanol
Y
iel
d M
et
il
E
s
ter
Dari hasil perbandingan mol metanol dan minyak jarak pada reaksi transesterifikasi
dengan katalis CaO dan MgO antara metanol dengan minyak jarak (ricinus communis)
terhadap yield metil ester dapat dilihat melalui kurva berikut
Perbandingan mol
metanol
yield meti ester
(%)
6 79.6
9 85.25
12 90.03
[image:41.595.136.520.156.534.2]15 87.97
Gambar 4.1 Grafik pengaruh perbandingan mol metanol dan minyak jarak pada
reaksi transesterifikasi menggunakan katalis CaO terhadap yield metil ester
7.5
7.6
7.7
7.8
7.9
8
8.1
8.2
8.3
3
6
9
12
15
18
Mol Methanol
Y
ie
ld
M
e
til E
s
te
r (
%)
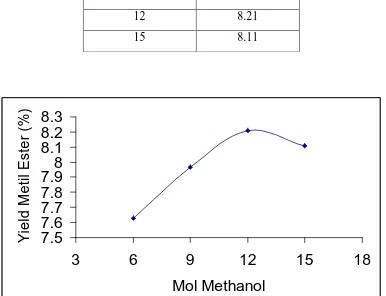
perbandingan mol yield metil ester (%)
6 7.628
9 7.965
12 8.21
[image:42.595.136.522.181.477.2]15 8.11
Gambar 4.2 Grafik pengaruh perbandingan mol metanol dan minyak jarak pada
reaksi transesterifikasi menggunakan katalis MgO terhadap yield metil ester pada suhu
-10
10
30
50
70
90
3
6
9
12
15
18
Mol Methanol
Y
ie
ld
M
e
til E
s
te
r(
%)
CaO
MgO
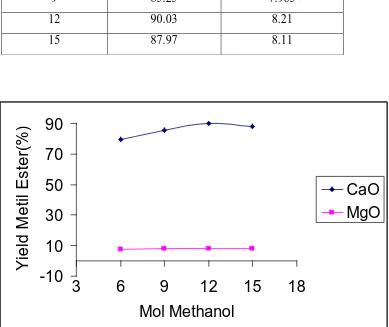
Perbandingan mol metanolYield metil ester (%)
dengan katalis CaO
Yield metil ester (%)
dengan katalis MgO
6 79.6 7.628
9 85.25 7.965
12 90.03 8.21
[image:43.595.120.509.178.505.2]15 87.97 8.11
Gambar 4.3 Grafik pengaruh perbandingan mol metanol dan minyak jarak pada
reaksi transesterifikasi menggunakan katalis CaO dan MgO terhadap yield
60
70
80
90
100
0
2
4
6
8
Waktu Reaksi (jam)
Y
ie
ld
M
e
til E
s
te
r (
%)
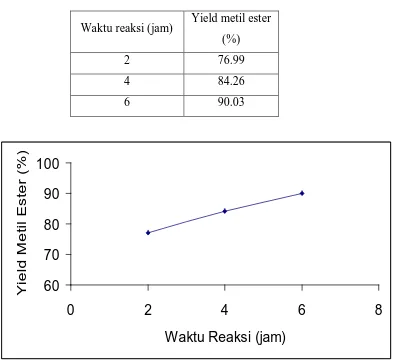
Waktu reaksi (jam) Yield metil ester (%)
2 76.99
4 84.26
[image:44.595.118.512.95.456.2]6 90.03
Gambar 4.4 Grafik pengaruh waktu reaksi pada reaksi transesterifikasi menggunakan
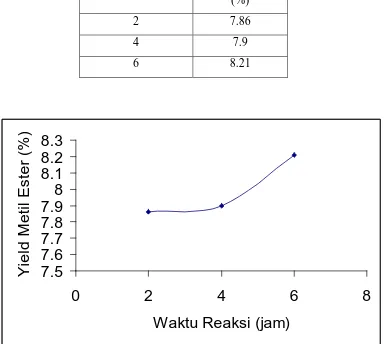
Waktu reaksi (jam) Yield Metil Ester (%)
2 7.86
4 7.9
[image:45.595.109.493.134.478.2]6 8.21
Gambar 4.5 Grafik pengaruh waktu reaksi pada reaksi transesterifikasi menggunakan
katalis MgO terhadap yield metil ester pada suhu 650C dan perbandingan mol methanol dan minyak jarak yaitu 12 : 1
7.5
7.6
7.7
7.8
7.9
8
8.1
8.2
8.3
0
2
4
6
8
Waktu Reaksi (jam)
Y
ie
ld
M
e
til E
s
te
r (
0
20
40
60
80
100
0
2
4
6
8
Waktu Reaksi (Jam)
Y
ie
ld
M
e
til E
s
te
r (
%)
CaO
MgO
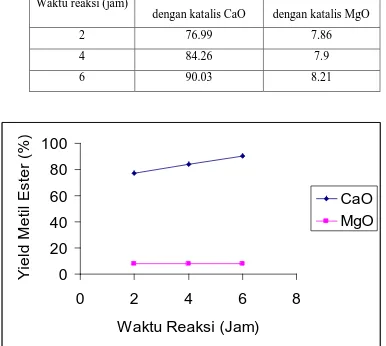
Waktu reaksi (jam) Yield Metil Ester (%) dengan katalis CaO
Yield Metil Ester (%)
dengan katalis MgO
2 76.99 7.86
4 84.26 7.9
[image:46.595.109.495.120.466.2]6 90.03 8.21
Gambar 4.6 Grafik pengaruh waktu reaksi pada reaksi transesterifikasi menggunakan
Reaksi transesterifikasi antara metanol dan minyak jarak menggunakan katalis
CaO dan MgO adalah reaksi kesetimbangan yang bersifat reversibel (bolak- balik).
Secara koefisien reaksi maka perbandingan mol antara metanol dengan minyak jarak
adalah 6 : 1 (mol/mol), sehingga untuk menggeser kesetimbangan kearah produk
sesuai dengan Azas Le Chatelier ( Jika konsentrasi pereaksi diperbesar maka
kesetimbangan akan bergeser kearah produk).
Penggunaan perbandingan mol ( 9 : 1 ) antara metanol dan minyak jarak
menghasilkan yield metil ester sebesar CaO yaitu 79,6 % dan MgO yaitu 7,69 %
menghasilkan konversi metil ester yang tidak sempurna disebabkan oleh tidak
tercapainya konsentrasi metanol berlebih untuk menggeser reaksi kesetimbangan ke
arah pembentukan produk metil ester sesuai dengan azas Le Chatelier. Sedangkan
penggunaan perbandingan mol (15 : 1) antara metanol dengan minyak jarak
menghailkan yield sebesar CaO yaitu 87,97 % dan MgO yaitu 8,11 %, menghasilkan
konversi metil ester yang tidak maksimum dan semakin menurun disebabkan oleh
pengggunaan perbandingan mol yang cukup besar sehingga mengakibatkan sukarnya
proses pemisahan anatar gliserol dengan metil ester.
Dalam penelitian ini yield yang diperoleh pada waktu reaksi 2 jam sebesar
CaO yaitu 76,99 % dan MgO yaitu 7,86 %. Dalama hal ini belum terjadi
kesetimbangan antara reaktan dan produk. Kemudian meningkat pada waktu reaksi 4
jam dan mendapatkan yield metil ester yang maksimum pada waktu reaksi 6 jam
sebesar CaO yaitu 90,03 % dan MgO yaitu 8,21 % Hal ini terutama disebakan karena
CaO dan MgO didespersikan terlebih dahulu dengan metanol sehingga membutuhkan
waktu lebih lama dibandingkan dengan katalis homogen.
Dari yield yang dihasilkan dengan menggunakan terdapat perbedaan yang
besar antara yield metil ester yang dihasilkan dengan katalis CaO dan MgO. Dimana
dengan katalis CaO dengan kondisi reaksi perbandingan mol metanol dan minyak
jarak (12 : 1) dan waktu reaksi dihasilkan yield metil ester 90,03 dan dengan katalis
MgO dengan kondisi reaksi yang sama dihasilkan yield metil ester 8,21% hal in
terbentuk CaO memiliki ikatan ionik dan MgO ikatan yang terbentuk adalah kovalen,
sehingga kondisi reaksi pada perbandingan mol metanol dan minyak jarak (12 : 1) dan
waktu reaksi 6 jam dengan katalis MgO tidak sesuai dan tidak bisa menghasilkan
yield metil ester yang tinggi.
Maka dalam reaksi transesterifikasi Minyak jarak (ricinus communis) menjadi
metil ester asam lemak, kondisi optimum diperoleh pada kondisi reaksi yaitu
Perbandingan mol antara metanol dengan minyak jarak 12 : 1 (mol/mol), waktu reaksi
BAB 5
KESIMPULAN DAN SARAN
5.1 Kesimpulan
Reaksi transesterifikasi minyak jarak (Ricinus communis) menjadi metil ester
asam lemak menghasilkan yield yang maksimum pada perbandingan mol methanol :
minyak jarak ( 12 : 1) , suhu 650C, dan waktu reaksi 6 jam
Yield metil ester yang dihasilkan pada reaksi transesterifikasi dengan
menggunakan katalis CaO yaitu 90,03 % dan katalis MgO yaitu 8,21 %
5.2. Saran
Diharapkan untuk peneliti selanjutnya untuk mencari kondisi reaksi yang tepat dengan
DAFTAR PUSTAKA
Austin, G., 1985. Shreve’s Chemical Process Industries. New York : Mc- Graw-Hill, Co
Bascetta,E., Frank,D.G., and Charles,M.S. 1984. Purification of Fatty Acid Methyl
Ester By High Pressure Liquid Chromatography. Departement Of Chemistry.
The University Of St Adrews, Scotland, United Kingdoms.
Chang,R. 2005 .Kimia Dasar Kimia-kimia Inti. Edisi ketiga Jilid 2. Erlangga. Jakarta.
Gunstone, F.D. 2004. The Chemistry of Oil and Fats. Published in USA and Canada.
Holtzclaw,H.F.1988. College Chemistry With Qualitative Analysis. Eight Edition.
USA : D.C.Heath and Company
Hambali, E., Suryani, A., Dadang, Hariyadi, Hanafie, H., Reksowardojo, I. K., Rivai,
M., Ihsanur, M., Suryadarma, P., Tjitrosemito, S., Soerawidjaja, T. H.,
Prawitasari, T., Prakoso, T., dan Wahyu Purnama. 2006 .Jarak Pagar
Tanaman Penghasil Biodiesel. Penebar Swadaya, Jakarta.
Http : // www. Nguntoronadi. Wonogiri.org/ mod. Php.mod : informasi & op.viewinfo
Ketaren. S. 1986. Pengantar Teknologi Minyak Dan Lemak Pangan. Cetakan pertama.
Jakarta. Universitas Indonesia Press
Khan. A.K. 2002. Research Into Biodiesel Kinetics And Catalyst Development
Brisbane. Queensland. Australia
Leach,B.E.1983. Applied Industrial Catalysis.Volume 2. New York : Academic Press
Liu.X. et all. 2007. Tranesterification of soybean oil to biodiesel using CaO as
Liu, X. 2007. Transesterification of soybean oil to biodiesel using CaO as abase
catalyst, Elsevier Renewable Energy.
March,J.1992. Advanced Organic Chemistry.Fourth Edition.New York : John Wiley
& sons,Inc
Naughton. F.C 1973. Production Chemistry and Commercial Application of Various
Chemicals from Castor oil : Presented At the AOCS 64th Anual Spring
Meeting New Orleans. Loussiana
Ophardt.E.C. 2003. Virtual Chembook.. Elmhurst College
Saito. T. 1996. Buku Teks Kimia Anorganik. Iwawani Publishing company
Sudjana,M.A.,M.Sc. 2002. Metoda Statistika. Edisi ke-6. Penerbit Trasito. Bandung
Suppes G.J. 2001. Calsium Carbonate Catalyzed Alcoholysis Of Fats And Oil.
Meneghetti P.,Simoni M. 2006. Ethanolysis Of Castor and Cottonsed Oil: A
Systematic Study Using Classical Catalyst.
Viswanathan, B., Ramaswamy,A.V. 2005. Selection Of Solid Heterogenous Catalysts
Lampiran 1.
Tabel 1 Data hasil reaksi transesterifikasi Minyak Jarak (Ricinus Communis) Dengan
Katalis CaO
NO Mol Waktu reaksi (jam) Berat metil ester (g) Yield metil ester (%)
1 6 2 31.68 66.62
2 9 2 33.83 71.14
3 12 2 36.66 76.99
4 15 2 34.15 71.81
5 6 4 36.26 76.25
6 9 4 39.09 82.2
7 12 4 40.07 84.26
8 15 4 38.62 81.21
9 6 6 37.85 79.6
10 9 6 40.54 85.25
11 12 6 42.81 90.03
12 15 6 41.83 87.97
*13 12 4 86.23 90.8
(*) Reaksi transesterifikasi minyak jarak castor oil dengan perbandingan mol metanol
dan minyak jarak (12 : 1), waktu reaksi 4 jam, katalis CaO dengan co-solvent dietil
Lampiran 2
Tabel 2 Data hasil Reaksi transesterifikasi Minyak Jarak (Ricinus Communis) Dengan
Katalis MgO
NO Mol waktu reaksi (jam) berat metil ester (g) Yield metil ester (%)
1 6 2 30.75 6.8
2 9 2 32.06 7.15
3 12 2 35.24 7.86
4 15 2 35.18 7.85
5 6 4 31.69 7.07
6 9 4 33.61 7.5
7 12 4 35.69 7.9
8 15 4 35.4 7.9
9 6 6 34.18 7.628
10 9 6 35.69 7.965
11 12 6 36.81 8.21
Lampiran 3
Lampiran 4
Gambar 2. Analisis Kromatografi gas hasil transesterifikasi minyak jarak castor oil
Lampiran 5
Gambar 2. Analisis Kromatografi gas hasil transesterifikasi minyak jarak castor oil
Lampiran 6
Gambar 3. Analisis Kromatografi gas hasil transesterifikasi minyak jarak castor oil