IDENTIFIKASI DAN KARAKTERISASI SIFAT FISIKA DAN
KIMIA MADU ASLI DAN MADU YANG DIJUAL DARI
BERBAGAI SUMBER
TESIS
Oleh :ARDILLES OLO TUA SILITONGA
097006029/KIM
FAKULTAS MATEMATIKA DAN ILMU PENGETAHUAN ALAM
UNIVERSITAS SUMATERA UTARA
IDENTIFIKASI DAN KARAKTERISASI SIFAT FISIKA DAN
KIMIA MADU ASLI DAN MADU YANG DIJUAL DARI
BERBAGAI SUMBER
TESIS
Diajukan Sebagai Salah Satu Syarat Untuk Memperoleh Gelar Magister Sains Dalam Program Studi Ilmu Kimia pada Fakultas Matematika Dan Ilmu
Pengetahuan Alam Universitas Sumatera Utara
Oleh :
ARDILLES OLO TUA SILITONGA 097006029/KIM
FAKULTAS MATEMATIKA DAN ILMU PENGETAHUAN ALAM
UNIVERSITAS SUMATERA UTARA
PENGESAHAN TESIS
Judul Tesis : IDENTIFIKASI DAN KARAKTERISASI SIFAT FISIKA DAN KIMIA MADU ASLI DAN MADU YANG DIJUAL DARI BERBAGAI
SUMBER Nama Mahasiswa : ARDILLES OLO TUA SILITONGA Nomor Pokok : 097006029/KIM
Program Studi : Ilmu Kimia
Menyetujui Komisi Pembimbing
Dr. Ribu Surbakti, MS Drs. Firman Sebayang, MS
Ketua Anggota
Ketua Program Studi, Dekan,
Prof. Basuki Wirjosentono, MS, Ph.D Dr. Sutarman , MSc
PERNYATAAN ORISINALITAS
IDENTIFIKASI DAN KARAKTERISASI SIFAT FISIKA DAN
KIMIA MADU ASLI DAN MADU YANG DIJUAL DARI
BERBAGAI SUMBER
TESIS
Dengan ini saya menyatakan bahwa dalam tesis ini tidak terdapat karya yang pernah diajukan untuk memperoleh gelar kesarjanaan di suatu perguruan tinggi dan sepanjang pengetahuan saya juga tidak terdapat karya atau pendapat yang pernah ditulis atau diterbitkan oleh orang lain kecuali disebutkan sumbernya dalam daftar pustaka.
Medan, Juni 2011 Penulis
PERNYATAAN PERSETUJUAN PUBLIKASI KARYA ILMIAH UNTUK KEPENTINGAN
AKADEMIS
Sebagai sivitas akademika Universitas Sumatera Utara, saya yang bertanda tangan dibawah ini :
Nama : Ardilles Olo Tua Silitonga NIM : 097006029
Program Studi : Magister Ilmu Kimia Jenis Karya Ilmiah : Tesis
Demi pengembangan ilmu pengetahuan, menyetujui untuk memberikan kepada Universitas Sumatera Utara Hak Bebas Royalti Non – Eksklusif (Nonexclusif Royalty Free Right) atas Tesis saya yang berjudul :
IDENTIFIKASI DAN KARAKTERISASI SIFAT FISIKA DAN
KIMIA MADU ASLI DAN MADU YANG DIJUAL DARI
BERBAGAI SUMBER
Beserta perangkat yang ada (jika diperlukan). Dengan Hak Bebas Royalti Non-Eksklusif ini, Universitas Sumatera Utara berhak menyimpan mengalih media, memformat, mengelola dalam bentuk data-base, merawat dan mempublikasikan Tesis saya tanpa meminta izin dari saya selama tetap mencantumkan nama saya sebagai penulis dan sebagai pemegang dan atau sebagai pemilik hak cipta.
Demikian pernyataan ini dibuat dengan sebenarnya.
Medan, Juni 2011 Penulis,
Telah diuji pada
Tanggal 21 Juni 2011
PANITIA PENGUJI TESIS
Ketua : Dr. Ribu Surbakti, MS
Anggota : 1. Drs. Firman Sebayang, MS
2. Prof. Basuki Wirjosentono, MS,Ph.D 3. Dr. Hamonangan Nainggolan, MSc 4. Dra. Yuniarti Yusak , MS
RIWAYAT HIDUP
DATA PRIBADI
Nama lengkap berikut gelar : Ardilles Olo Tua Silitonga, S.Pd Tempat dan Tanggal Lahir : Siborongborong, 3 April 1983
Alamat Rumah : Jalan Horas No. 17 Kecamatan Siborongborong Kabupaten Tapanuli Utara
Telepon/ Faks/ HP : 081361157700
Email : ardilles_silitonga@yahoo.com Instansi Tempat Bekerja : SMK Negeri 1 Siborongborong
Alamat Kantor : Jln. Balige Km. 2,2 Pohan Tonga Siborongborong Telepon/Faks/HP : ( 0633 ) 41850
DATA PENDIDIKAN
KATA PENGANTAR
Tiada kata yang pantas terucap selain Puji syukur dan terimakasih kehadirat Tuhan Yang Maha Kuasa karena atas berkat dan kasihNya kepada penulis sehingga tesis dengan judul “Identifikasi Dan Karakterisasi Sifat Fisika Dan Kimia Madu Asli Dan Madu Yang Dijual Dari Berbagai Sumber” dapat diselesaikan.
Pada kesempatan ini penulis mengucapkan terima kasih kepada Gubernur Sumatera Utara c.q Ketua Bappeda Provinsi Sumatera Utara yang memprogramkan bantuan dana untuk guru-guru tingkat SMA untuk melanjutkan studi ke strata dua (S2) sehingga penulis dapat menyelesaikan pendidikan pada Program Studi Magister Ilmu Kimia Pascasarjana FMIPA Universitas Sumatera Utara.
Dengan selesainya tesis ini, penulis mengucapkan terima kasih yang sebesar-besarnya kepada:
Rektor Universitas Sumatara Utara Prof. Dr.dr.Syahril Pasaribu DTM & H. MSc (CTM).Sp.A (K) atas kesempatan dan fasilitas yang diberikan kepada penulis untuk mengikuti dan menyelesaikan pendidikan pada Program Magister Ilmu Kimia.
Dekan FMIPA Universitas Sumatera Utara Prof. Dr. Eddy Marlianto MSc atas kesempatan menjadi mahasiswa Program Magister Sains pada Program Pascasarjana FMIPA Universitas Sumatera Utara .
Ketua Program Studi Magister Kimia Prof. Basuki Wirjosentono, MS, Ph.D, Sekretaris Program Studi Dr. Hamonangan Nainggolan MSc beserta seluruh Staf Pengajar pada Program Studi Magister Ilmu Kimia.
Penulis juga mengucapkan terima kasih kepada Drs.Marulak Nababan beserta guru dan pegawai SMKN 1 Siborongborong atas dukungan dan bantuan doa hingga tesis ini diselesaikan.
Kepada keluarga penulis yakni istri tercinta Lamtiur Hutabarat dan kepada anakku terkasih Joelkai Salomo Silitonga, Orang tuaku Saut Manaor Silitonga dan Mangisi Silaban serta Mertuaku Pdt. ATH Hutabarat dan D. Pasaribu dan juga Semua saudaraku tercinta, terimakasih atas segala pengorbanan dan doa kalian baik berupa moril maupun materil, hanya Tuhanlah yang dapat membalas budi baik kalian.
Medan, Juni 2011 Penulis
IDENTIFIKASI DAN KARAKTERISASI SIFAT FISIKA DAN
KIMIA MADU ASLI DAN MADU YANG DIJUAL DARI
BERBAGAI SUMBER
ABSTRAK
Madu adalah zat manis alami menyehatkan yang dihasilkan lebah dengan bahan baku nektar bunga dimana nektar adalah senyawa kompleks yang dihasilkan kelenjar tanaman dalam bentuk larutan gula, karena berbagai alasan madu sering dipalsukan. Penelitian ini dilakukan untuk mengidentifikasi dan mengkarakterisasi sifat fisika dan sifat kimia dari madu asli dan madu yang dijual dari berbagai sumber yang kemudian membandingkannya. Teknik sampling yang digunakan adalah teknik sampling purposif dengan mengambil 7 buah sampel yang terdiri dari 2 bagian yaitu 2 sampel madu asli dan 5 sampel madu dari berbagai sumber disekitar lingkungan peneliti. Parameter yang diamati meliputi mengukur berat jenis, penyimpanan dalam freezer, tes Nyala, mengukur derajat keasaman, tes gula reduksi dan uji aktivitas enzim. Berdasarkan hasil analisa maka didapat adanya perbedaan berat jenis madu asli dan madu yang beredar dipasaran. Jika disimpan dalam freezer hanya madu asli yang membeku, dalam test nyala seluruh sampel menyala. Ada perbedaan derajat keasaman antara sampel madu asli dan sampel madu yang lain. Dalam test gula reduksi hasilnya tidak terjadi perbedaan yang signifikan, sedangkan dalam test aktivitas enzim sampel madu asli memiliki aktivitas enzim yang sangat tinggi dan 3 sampel yang lain memiliki aktivitas enzim yang sangat lambat dan 2 sampel tidak memiliki aktivitas enzim yang disimpulkan merupakan madu palsu.
IDENTIFICATION AND CHARACTERIZATION OF PHYSICAL AND CHEMICAL PROPERTIES OF NATURAL
HONEY AND ONES THAT ARE SOLD FROM VARIOUS SOURCES
ABSTRACT
Honey is a healthy natural sweet substance produced by bees with nectar as its raw material, in which the nectar is a complex compound produced by plant gland in the form of sugar solution. For various reasons, honey is often falsified. This research is conducted to identify and characterize the physical and chemical properties of the original honey and ones which are sold from various sources and then comparing them. The sampling tehnicque used is taking 7 samples consisting of 2 parts, i.e. 2 original honey samples and 5 samples of honey from various sources around the researcher’s environment. The parameters observed including measuring density, storage in a freezer, flame test, degree of acidity, sugar reduction and enzyme activity test. Based on the results of the analysis, there is a difference in density beetwen the natural honey and ones on the market. If stored in a freezer, only the natural honey freezes. In a flame test, all samples lit. There are differences in the degree of acidity between the natural honey samples and other honey samples. In sugar reduction tets, significant differences do not occur, where as in the enzyme activity test, the original honey samples have a very high enzyme activities and the other 3 samples have a very slow enzyme activity and 2 samples do not have enzyme activity which can be concluded as fake honey.
DAFTAR ISI
2.4.2 Proses Fisika Pembentukan Madu 8 2.5. Komposisi Madu 8
2.5.1. Monosakharida Dan Disakharida Dalam Madu 9 2.5.2. Trisakharida Dan Gula berantai Panjang
Dalam Madu 11
2.7 Asam Dalam Madu 18
3.3.1 Penyediaan Sampel 28 3.3.2Test / uji yang dilakukan
BAB 4 HASIL DAN PEMBAHASAN 4.1 Mengukur berat jenis 34 4.2 Disimpan dalam freezer & Tes Nyala 35 4.3 Mengukur derajat keasaman ( pH ) 37 4.4 Tes gula reduksi 39 4.5 Uji aktivitas Enzim 40
BAB 5 KESIMPULAN DAN SARAN
5.1 Kesimpulan 42
5.2 Saran 42
DAFTAR PUSTAKA 43
DAFTAR TABEL
Nomor Judul Tabel Halaman 2-1. Rataan Komposisi Madu Amerika Serikat 10 2-2. Rataan Komponen Kimia Madu Berasal Dari Berbagai Tumbuhan 12
2-3. Syarat Mutu Madu 18
2-4. Beberapa Jenis Asam Yang Dijumpai Dalam Madu 19 2-5. Pembentukan Aroma Pada Madu 22
2-6. Vitamin dalam madu 23
4-1. Mengukur berat jenis 34 4-2. Disimpan dalam freezer & Tes Nyala 35 4-3. Mengukur derajat keasaman 37
4-4. Tes gula reduksi 39
DAFTAR GAMBAR
Nomor Judul Gambar Halaman 2.1. Struktur terbuka α D (+) Glukosa 14
2.2. Struktur Fruktosa 14
2.3. Struktur Sukrosa 15 2.4. Penambahan amilum dengan iodin 16
Lampiran
IDENTIFIKASI DAN KARAKTERISASI SIFAT FISIKA DAN
KIMIA MADU ASLI DAN MADU YANG DIJUAL DARI
BERBAGAI SUMBER
ABSTRAK
Madu adalah zat manis alami menyehatkan yang dihasilkan lebah dengan bahan baku nektar bunga dimana nektar adalah senyawa kompleks yang dihasilkan kelenjar tanaman dalam bentuk larutan gula, karena berbagai alasan madu sering dipalsukan. Penelitian ini dilakukan untuk mengidentifikasi dan mengkarakterisasi sifat fisika dan sifat kimia dari madu asli dan madu yang dijual dari berbagai sumber yang kemudian membandingkannya. Teknik sampling yang digunakan adalah teknik sampling purposif dengan mengambil 7 buah sampel yang terdiri dari 2 bagian yaitu 2 sampel madu asli dan 5 sampel madu dari berbagai sumber disekitar lingkungan peneliti. Parameter yang diamati meliputi mengukur berat jenis, penyimpanan dalam freezer, tes Nyala, mengukur derajat keasaman, tes gula reduksi dan uji aktivitas enzim. Berdasarkan hasil analisa maka didapat adanya perbedaan berat jenis madu asli dan madu yang beredar dipasaran. Jika disimpan dalam freezer hanya madu asli yang membeku, dalam test nyala seluruh sampel menyala. Ada perbedaan derajat keasaman antara sampel madu asli dan sampel madu yang lain. Dalam test gula reduksi hasilnya tidak terjadi perbedaan yang signifikan, sedangkan dalam test aktivitas enzim sampel madu asli memiliki aktivitas enzim yang sangat tinggi dan 3 sampel yang lain memiliki aktivitas enzim yang sangat lambat dan 2 sampel tidak memiliki aktivitas enzim yang disimpulkan merupakan madu palsu.
IDENTIFICATION AND CHARACTERIZATION OF PHYSICAL AND CHEMICAL PROPERTIES OF NATURAL
HONEY AND ONES THAT ARE SOLD FROM VARIOUS SOURCES
ABSTRACT
Honey is a healthy natural sweet substance produced by bees with nectar as its raw material, in which the nectar is a complex compound produced by plant gland in the form of sugar solution. For various reasons, honey is often falsified. This research is conducted to identify and characterize the physical and chemical properties of the original honey and ones which are sold from various sources and then comparing them. The sampling tehnicque used is taking 7 samples consisting of 2 parts, i.e. 2 original honey samples and 5 samples of honey from various sources around the researcher’s environment. The parameters observed including measuring density, storage in a freezer, flame test, degree of acidity, sugar reduction and enzyme activity test. Based on the results of the analysis, there is a difference in density beetwen the natural honey and ones on the market. If stored in a freezer, only the natural honey freezes. In a flame test, all samples lit. There are differences in the degree of acidity between the natural honey samples and other honey samples. In sugar reduction tets, significant differences do not occur, where as in the enzyme activity test, the original honey samples have a very high enzyme activities and the other 3 samples have a very slow enzyme activity and 2 samples do not have enzyme activity which can be concluded as fake honey.
BAB 1 PENDAHULUAN 1.1Latar Belakang
Madu merupakan sumber energi serta bahan yang akan diubah menjadi lemak
dan glikogen. Lebah madu memperoleh sebagian besar energi dari karbohidrat dalam
bentuk gula.
Pada dasarnya madu adalah zat manis alami yang dihasilkan lebah dengan
bahan baku nektar bunga. nektar adalah senyawa kompleks yang dihasilkan kelenjar
tanaman dalam bentuk larutan gula. Nektar dikumpulkan lebah pekerja dari bunga
dengan cara mengisapnya melalui mulut dan asafagus, lalu masuk kedalam perut di
dalam abdomen. Sebagian air nektar diserap oleh sel sel dinding perut lebah dan
dibuang ke luar melewati pipa malfigi dan poros usus. Bersama air dibuang juga
asam oksalat dan turunannya, beberapa garam mineral, dan sebagian zat aromatik
yang terdapat dalam nektar. Zat aromatik yang tertinggal memberikan aroma khusus
pada madu (Sarwono, 2001).
Penyebaran lebah madu merata di seluruh dunia, jika dibandingkan dengan
penyebaran serangga dan hewan lainnya, dimana ada manusia disitu lebah berada.
Oleh karena itu kegunaan madu telah dikenal sejak ±10.000 tahun yang lalu, sejak
manusia hidup sangat primitif. Zaman dahulu madu dipakai untuk mengawetkan
daging dan kulit. Orang Mesir pada waktu itu mempergunakan madu sebagai bagian
dari ramuan rahasianya untuk mengawetkan jenazah raja raja, yang dikenal dengan
nama mumi, sejak itu pula madu telah dikenal sebagai bahan makanan, obat,
minuman, bahan kecantikan dan bahan yang penting dalam pesta upacara agama.
Begitu terkenalnya madu pada zaman itu sehingga pajak di Babylonia tidak dibayar
dengan uang tetapi dengan madu. Pada waktu itu gula tebu dan gula lain belum
diketemukan orang, karena madu merupakan zat manis satu satunya yang dipakai
Dahulu atlit – atlit selalu minum madu sebelum bertanding dengan harapan
untuk menang. Madu sebagai sumber tenaga yang mudah digunakan oleh tubuh.
Madu dicampur dengan air merupakan minuman kesayangan bangsa Inggris dan
Jerman. Minuman bir dengan madu adalah kegemaran umum. Petani Eropa sampai
sekarang masih memegang teguh pada tradisi kuno. Disana madu dihasilkan sebagai
makanan yang penting dan menyehatkan. Kata mereka tidak ada makanan yang lebih
nikmat kecuali sepotong roti yang dioleskan dengan madu dan mentega susu. Orang
Eropa memberikan madu kepada anak anaknya, disamping susu untuk mencegah
kekurangan gizi, ibu ibu di Amerika juga sekarang juga memberi madu kepada anak
anaknya dengan maksud yang sama.
Produksi madu Indonesia hingga dewasa ini masih belum tercatat dalam
statistik. Tetapi mengingat luasnya hutan ± 120 juta hektar yang penuh dengan
beraneka ragam tumbuh tumbuhan, bangsa Indonesia mempunyai potensi yang tidak
dapat diabaikan begitu saja dalam pengembangan madu untuk menjadi pengekspor
madu di dunia. (Sumoprastowo dan Suprapto,1993)
Akan tetapi dalam mencari keuntungan yang lebih besar dan cepat, banyak
orang yang kurang bertanggung jawab membuat madu palsu untuk dijual kepada
masyarakat, pemalsuan dilakukan dalam berbagai hal seperti pemalsuan jumlah,
pemalsuan mutu dan juga pemalsuan menyeluruh, banyak informasi dalam berbagai
media cetak dan elektronik yang memberitakan hal tersebut seperti dalam berita
Harian Kowar yang memberitakan bahwa Peredaran madu palsu di Indonesia sangat
tinggi.(KOWAR, 2008), Reskrim Polres Ogan Komering Ulu Baturaja yang berhasil
menggagalkan peredaran lebih dari 2 ton madu asli tapi palsu alias oplosan.(Sumatera
Ekspress, 2009). Waspadai madu palsu yang dijual dengan harga murah dan label
yang menarik padahal kandungan vitamin di dalamnya telah rusak (Griya
SOLOPOS,2010) dan juga Siaran Trans TV pada tanggal 28 Oktober 2010 yang
karena itu penulis merasa sangat perlu melakukan penelitian analisa perbandingan
madu asli dan madu yang beredar di pasaran.
1.2 Permasalahan
Permasalahan yang dapat dirumuskan dari penelitian ini adalah sejauh mana
perbedaan sifat sifat karakteristik yang meliputi pengukuran berat jenis, keadaan
disimpan dalam freezer, tes nyala, mengukur derajat keasaman , tes gula reduksi
dan tes aktivitas enzim dari madu asli ( madu alam ) dengan madu yang dijual di
apotek serta madu yang dijual keliling sehingga kita dapat membedakan antara
madu asli dengan madu palsu.
1.3 Pembatasan Masalah
Penelitian ini dilakukan terhadap sampel madu asli yang berasal dari 2 tempat
peliharaan madu yaitu dari kecamatan Lintong ni huta dan kecamatan Parranginan
kabupaten Humbang Hasundutan, sampel madu yang dijual dari 2 apotik di
kecamatan Siborongborong Kabupaten Tapanuli Utara dan sampel madu yang dijual
secara acak dari 3 tempat yang berbeda di sekitar daerah kecamatan Siborongborong
Kabupaten Tapanuli Utara tempat tinggal peneliti. Parameter yang diuji meliputi
pengukuran berat jenis, keadaan disimpan dalam freezer, tes nyala, mengukur derajat
keasaman , tes gula reduksi dan tes aktivitas enzim.
1.4 Tujuan Penelitian
Adapun tujuan dari penelitian ini adalah Untuk mengetahui sifat karakteristik
yang meliputi pengukuran berat jenis, keadaan disimpan dalam freezer, tes nyala,
mengukur derajat keasaman , tes gula reduksi dan tes aktivitas enzim madu asli yang
selanjutnya digunakan sebagai pembanding untuk menentukan madu oplosan dan
1.5 Manfaat Penelitian
Dari penelitian ini diharapkan dapat :
1. Untuk memberikan informasi kepada masyarakat tentang cara cara analisis sifat
karakteristik dari madu secara ilmiah.
2. Untuk memberikan informasi kepada masyarakat tentang perbedaan yang nyata antara madu asli dan madu palsu disamping sifat karakteristik yang telah
BAB 2
TINJAUAN PUSTAKA 1.1 Lebah Madu
Lebah termasuk hewan serangga atau insekta, penggolongan zoologisnya
adalah sebagai berikut :
Kelas : Insekta
Ordo : Hymenoptera
Famili : Apidae
Sub-famili : bombinae – Apini
Genus : Apis
Spesies : Apis andreniformis Smith 1858 – Apis mellifera syriaca.
Apis andreniformis, Apis cerana dan Apis dorsata adalah lebah alam Indonesia.
Hanya lebahlah insekta yang menghasilkan makanan yang biasa dikonsumsi
manusia. Ada sekitar 20.000 spesies lebah, namun hanya lebah madulah yang
menghasilkan madu dan malam yang dimanfaatkan manusia. Lebah membentuk satu
koloni yang terdiri dari 3 strata, yaitu ratu yang menghasilkan telur, lebah pekerja
yang menghasilkan makanan dan merawat telur dan bayi, jantan yang menunasi ratu.
Lebah madu adalah mahluk sosial yang berkembang sempurna.
Ratu lebah madu menghasilkan telur yang menetas menjadi ribuan lebah
pekerja, menghasilkan telur hanya itulah tugas ratu, selama periode bertelur ratu
dapat menelurkan 2.000 telur per hari, atau lebih dari 200.000 telur dalam satu musim
telur dengan harapan hidup lima tahun, ratu dapat menghasilkan satu juta telur selama
kecuali menghasilkan telur. Lebah jantan adalah mahluk kikuk, besar dan tegap
mereka tidak bekerja dan tidak memiliki sengat, tugas jantan hanyalah mengawini
ratu remaja.
Lebah sangat berfaedah terutama untuk penyerbukan tanaman buah, sayuran
dan tanaman biji bijian. Keuntungan yang diperoleh dari penyerbukan oleh lebah
mencakup seluruh dunia diperkirakan 20% lebih tinggi dari perolehan dari produk
lebah itu sendiri.(Sihombing,1994)
2.2 Madu
Lebah madu menghasilkan madu yang dibuat dari nektar ( senyawa kompleks
yang dihasilkan kelenjar tanaman dalam bentuk larutan gula ) sewaktu musim
tumbuhan berbunga. Sewaktu nektar dikumpulkan oleh lebah pekerja dari bunga,
bahan tersebut masih mengandung air tinggi (80%) dan juga gula (sukrosa tinggi).
Setelah lebah mengubah nektar menjadi madu, kandungan air menjadi rendah dan
sukrosa di ubah menjadi fruktosa (gula buah; levulosa) dan glukosa (dekstrosa).
Air disingkirkan melalui evaporasi, Lebah membantu proses evaporasi dengan
menempatkan nektar setengah penuh dalam rongga rongga sarang agar luas
permukaan meningkat dan lebah mengipaskan udara ke nektar segar tadi. Bunyi
sengung sayap mengipas nektar dalam sarang di sore hari adalah suatu tanda terdapat
nektar baik dan segar. Lebah pekerja meminum madu dan memuntahkannya kembali
sambil menambah enzim yang disebut enzim invertase. Enzim ini akan mengubah
sukrosa menjadi dekstrosa dan levulosa. Madu yang telah matang mengandung kadar
air yang rendah (17%) dan tinggi gula buah fruktosa. Kadar air yang rendah akan
menjaga madu dari kerusakan untuk jangka waktu relatif lama.
Dekstrosa akan membuat madu mengkristal membentuk madu permanen.
dapat dilelehkan dengan memanaskan madu sehingga kembali dalam keadaan cair.
(Sihombing,1994)
2.3 Penggolongan Madu
Berdasarkan asal nektar, madu biasa dibedakan atas tiga golongan, yaitu madu
flora, madu ekstraflora, dan madu embun.
Madu flora adalah madu yang dihasilkan dari nektar bunga. Yang berasal dari
satu jenis bunga disebut madu monoflora, yang berasal dari aneka ragam bunga
disebut madu poliflora. Madu flora sangat baik untuk pakan tambahan atau untuk
penambah tenaga, sedangkan madu poliflora baik sekali untuk mengobati orang yang
kelelahan, kepanasan, kedinginan, terkena luka bakar, mengalami luka sayat, dan
terkena luka tusuk . Madu poliflora mengandung enzim asam amino bebas yang
jumlahnya lebih banyak dibandingkan dengan madu monoflora.
Madu ekstraflora adalah madu yang dihasilkan dari nektar di luar bunga,
seperti daun, cabang, dan batang tanaman. Madu embun adalah madu yang dihasilkan
dari cairan hasil sekresi serangga, yang kemudian eksudatnya diletakkan dibagian
tanaman. Selanjutnya cairan itu diisap dan dikumpulkan oleh lebah madu. Madu ini
berwarna gelap dengan aroma merangsang.(Sarwono, 2001)
2.4 Proses Pembuatan Madu Lebah
Madu secara umum didefenisikan sebagi zat cair yang kental, manis, yang
dibuat oleh lebah dengan jalan proses peragian dari nektar bunga atau cairan manis
yang dihasilkan bagian-bagian lain selain bunga. Nektar adalah zat yang sangat
kompleks yang dihasilkan oleh kelenjar-kelenjar nektarifer dalam bentuk larutan gula
dengan konsentrasi yang bervariasi berkisar antara 5-70%. Konsentrasi ini
dipengaruhi oleh kelembaban udara, tanah, jenis tanaman dan lain-lain.
Komponen-komponen utama dari larutan gula ini antara lain adalah: sukrosa, glukosa dan
melbiosa, rafinosa, dan lain-lain. Selain dari zat gula nektar juga mengandung
protein, garam-garam mineral dan vitamin.
Pengolahan nektar menjadi madu, pada hakekatnya terdiri dari dua proses
kimia dan fisika.(Nainggolan, Dkk, 1992)
2.4.1 Proses Kimia Pembentukan Madu
Dalam proses kimia ini, terjadi reaksi yang disebut invertase dimana cairan
manis nektar dirobah menjadi gula yang lebih sederhana strukturnya. Invertase ini
berlangsung secara katalitik dengan bantuan enzim yang terdapat dalam nektar dan
didalam air ludah lebah sendiri.
2.4.2 Proses Fisika Pembentukan Madu
Proses fisika ini merupakan proses pengurangan kadar air dalam nektar yang
telah mengalami invertase. Proses ini terjadi dalam dua tahap:
Tahap pertama adalah membiarkan nektar yang telah mengalami invertase kena udara sehingga sebagian airnya menguap. Pada saat ini, enzim
ditambahlan pula oleh lebah melalui air liur kepada nektar sehingga disamping
proses penguapan, berlangsung pula proses invertase. Tahap pertama ini
dikenal pula sebagai manipulasi nektar terhadap lebah.
Tahap kedua adalah penguapan sisa kelebihan air dengan pengipasan sayap
oleh semua lebah didalam stup. Tahap kedua ini dilakukan setelah nektar
disimpan dalam sel-sel madu. Proses ini dihentikan setelah kadar air tinggal
lebih kurang dari 20%. Kemudian lebah menutup sel-sel yang sudah penuh
2.5 Komposisi Madu
Zat-zat atau senyawa yang terkandung dalam madu sangat kompleks dan kini
telah diketahui tidak kurang dari 181 macam zat atau senyawa dalam madu. Mungkin
di masa datang akan ditemukan lagi senyawa lain bila penelitian terus dilakukan oleh
para peneliti dalam bidang peternakan madu.
Komposisi madu ditentukan oleh dua faktor, yakni: 1) komposisi nektar asal
madu bersangkutan dan 2) faktor-faktor eksternal tertentu. Lagipula untuk penilaian
harus diingat bahwa kualitas atau mutu madu sebenarnya agak sulit menyamakan
mutu karena ada berbagai cara untuk menganalisis yang digunakan ion-change
chromatography, gas-liquid chromatography,dsb, lama penyimpanan sampel yang
dianalisis dan perbedaan jenis dan asal bunga penghasil nektar. Karena pengaruh
klimat, topografi dan pola pertanian yang berbeda sulit mengharapkan mutu madu
yang sama. Madu yang berasal dari Negara yang berlainan umumnya berbeda pula.
Rataan kandungan madu Amerika Serikat (tabel 2-1) disajikan sebagai salah satu
contoh zat-zat yang terkandung didalamnya.
Jenis tanaman sebagai sumber utama nektar dan polen mengakibatkan
komponen madu berbeda (tabel 2-2). Berbagai tumbuhan sebagai sumber nektar dan
polen di Indonesia, namun penelitian tentang hal ini masih sangat terbatas. Data yang
tercantum dalam tabel 2-2 diambil dari hasil-hasil penelitian di mancanegara.
Perbedaan komposisi madu asal berbagai Negara disebabkan oleh perbedaan
klimat, topografi, tumbuhan, lebah madu yang menghasilkan madu dan cara
pengolahan dan penyimpanan.(Sihombing, 1994)
2.5.1 Monosakarida Dan Disakarida Dalam Madu
Jenis gula yang dominan dalam hampir semua madu adalah levulosa dan
Levulosa dan dekstrosa mencakup 85-90 % dari karbohidrat yang terdapat dalam
madu dan hanya sebagian kecil oligasakarida dan polisakarida.
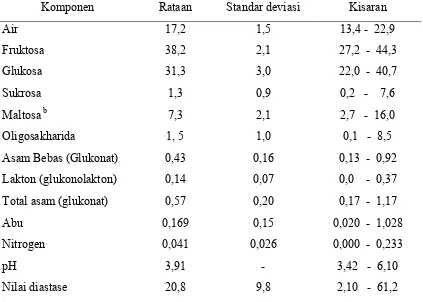
Tabel 2‐1. Rataan Komposisi Kimia Madu Amerika Serikat
Komponen Rataan Standar deviasi Kisaran
Air 17,2 1,5 13,4 - 22,9
data dalam persentase dari madu, kecuali dua kategori terakhir b
disakharida tereduser dihitung sebagai maltosa, Sumber : Sihombing, 1994
Hasil-hasil penelitian mutahir menunjukkan paling sedikit ada 11 disakarida
selain sukrosa, dalam madu dan merupakan yang pertama kali diisolasi dari bahan
alami. Disakarida yang telah diidentifikasi dalam madu adalah maltosa, isomaltosa,
nigerosa, turanosa, maltulosa, kojibiosa, eukrosa, neotrehalosa, gentiobiosa dan
2.5.2 Trisakarida Dan Gula berantai Panjang Dalam Madu
Sekitar tahun 50-an telah diketahui trisakarida yang terdapat dalam madu
adalah melezitosa, erlosa (fruktomaltosa), ketosa, rafinosa dan dekstrantriosa
Tahun 1968 dua peneliti melaporkan penemuan bagian karbohidrat
polisakarida dalam madu, yakni erlosa, 6G-α-glukosilsukrosa, isomaltotriosa,
isomaltotetraosa, isopanosa, 3 α-isomaltosilglukosa, 1-ketosa, melezitosa, panosa,
maltotriosa, dan dua lagi yang belum diidentifikasi. Kelak diketahui salah satu dari
dua terakhir diuraikan susunannya: O- α-D-glikopiranosil-(1,4)-O- α
-D-glukopiranosil-(1,2)-D-glukosa yang diberi nama Centosa dan diperkirakan terdapat
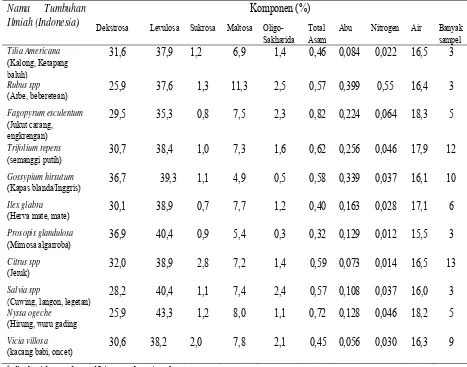
Tabel 2‐2. Rataan Komponen Madu Berasal Dari Berbagai Tumbuhan
Komponen (%) Nama Tumbuhan
Ilmiah (Indonesia)
Dekstrosa Levulosa Sukrosa Maltosa Oligo- Sakharida
Total Asam
Abu Nitrogen Air Banyak
sampel
disakarida tereduser dihitung sebagai maltosa b
dalam bentuk glukonat sumber : Sihombing, 1994
Para peneliti ini menyimpulkan bahwa hasil proses enzimatis zat-zat tersebut
belum diketahui pada tumbuhan, lebah madu ataupun insekta lain. Kebanyakan
Telah lama diketahui ada dekstrin dalam madu, bahan ini agak sulit dianalisis,
karena berat molekulnya tinggi. Ada pula ditemukan polisakarida bercabang yang
mereka namakan arabogalaktomanan dan terdapat 0,002 % dalam madu.
Madu mengandung berbagai gula tereduksi sehingga bila disimpan lama akan
mengalami perubahan. Bila madu disimpan dua tahun dalam tempat bersuhu kamar,
maltosa akan meningkat mencapai 69% dan dekstrosa serta levulosa turun mencapai
86% dari aslinya. Penyebabnya antara adalah suhu penyimpanan dan kadar air madu.
Penyimpanan selama 6-12 bulan pada suhu 28-380C akan meningkatkan gula berantai
panjang (oligosakarida/polisakarida) dan menurunkan monosakarida. Peningkatan
olisakarida dalam madu disebabkan oleh dua mekanisme, yakni oleh sukrosa yang
terdapat dalam madu sebenarnya merupakan suatu transglukosilase. Jadi sebenarnya
bila kadar air dalam madu rendah, akan menahan disakarida untuk tidak diubah
menjadi monosakarida. Namun kelangsungan kedua ini ada juga batasnya. Sebagai
gambaran, madu berumur 36 tahun setelah dianalisis ternyata mengandung 16,4
persen maltosa. (Sihombing, 1994)
2.5.3 Karbohidrat
Glukosa
Glukosa adalah suatu aldoheksosa dan sering disebut dekstrosa karena
mempunyai sifat dapat memutar bidang polarisasi cahaya kearah kanan. Di alam
glukosa terdapat dalam buah-buahan dan madu lebah. Glukosa dihasilkan dari
reaksi antara karbohidrat dan air dengan bantuan sinar matahari dan klorofil dalam
daun. Proses ini disebut fotosintesis dan glukosa yang terbentuk terus digunakan
untuk pembentukan amilum dan selulosa.
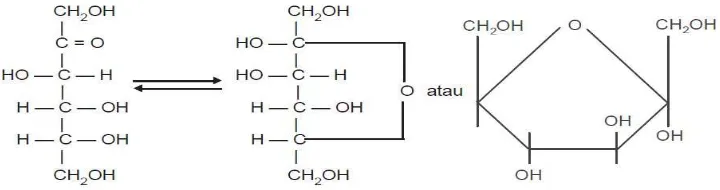
Sebagian besar monosakarida dikenal sebagai heksosa, karena terdiri atas
6-rantai atau cincin karbon. Atom-atom hidrogen dan oksigen terikat pada 6-rantai
atau cincin ini secara terpisah atau sebagai gugus hidroksil (OH). Ada tiga jenis
Gambar 2.1 Struktur terbuka α D (+) Glukosa Fruktosa
Selain glukosa Madu lebah juga mengandung fruktosa. Fruktosa adalah
suatu ketoheksosa yang mempunyai sifat memutar bidang polarisasi cahaya
ke kiri dan karenanya disebut levulosa. Pada umumnya monosakarida dan
disakarida mempunyai rasa manis. Fruktosa mempunyai rasa lebih manis daripada
glukosa, juga lebih manis daripada gula tebu dan sukrosa. Fruktosa berikatan
dengan glukosa membentuk sukrosa, yaitu gula yang biasa digunakan sehari-hari
sebagai pemanis, dan berasal dari tebu dan atau bit.
Gambar 2.2 Struktur Fruktosa
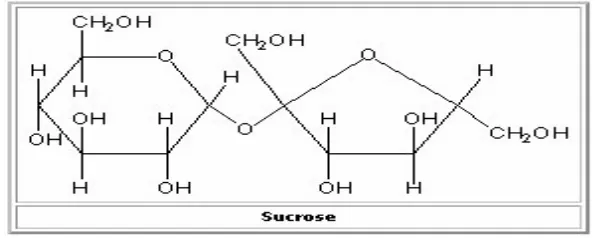
Sukrosa adalah gula yang kita kenal sehari-hari, baik yang berasal dari
tebu maupun dari bit. Selain pada tebu dan bit, sukrosa terdapat pula pada
tumbuhan lain, misalnya dalam buah nenas dan dalam wortel. Dengan hidrolisis
sukrosa akan terpecah dan menghasilkan campuran glukosa dan fruktosa yang
disebut gula invert. Madu lebah sebagian besar terdiri atas gula invert ini dan
dengan demikian madu mempunyai rasa lebih manis daripada gula (Poedjiadi,
1994).
Gambar 2.3 Struktur Sukrosa
Hidrolisis Asam
Hidrolisis merupakan proses pemecahan polisakarida di dalam biomasa
ligniselulosa yaitu selulosa dan hemiselulosa menjadi monomer gula yang dapat
dilakukan secara kimia ataupun enzimatis. Dibandingkan proses secara kimia,
hidrolisis secara enzimatis lebih menguntungkan karena ramah lingkungan.
Didalam metode hidrolisis asam, biomasa ligniselulosa dipaparkan dengan
asam pada suhu dan tekanan tertentu selama waktu tertentu, dan menghasilkan
monomer gula dari polimer selulosa dan hemiselulosa. Beberapa asam yang
umum digunakan untuk hidrolisis asam antara lain asam sulfat (H2SO4), asam
perklorat, dan HCl. Asam sulfat merupakan asam yang paling banyak diteliti dan
dimanfaatkan untuk hidrolisis asam. Hidrolisis asam dapat dikelompokkan menjadi
hidrolisis asam pekat dan hidrolisis asam yang menggabungkan 2 molekul
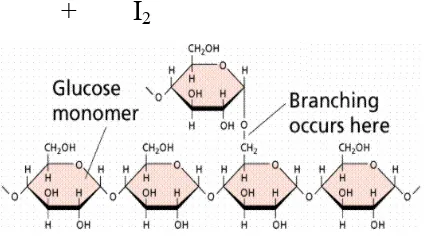
tepung dari karbohidrat dengan suatu polimer senyawa glukosa yang terdiri dari
dua komponen utama, yaitu amilosa dan amilopektin. Polimer linier dari
D-glukosa membentuk amilosa dengan α-(1 ,4)-gIukosa. Sedangkan polimer
amilopektin adalah α- (1,4)-glukosida dan membentuk cabang pada ikatan α
(1,6)-glukosida. http://eckonopianto. blogspot.com/2009/04/pati.html
Tes Iodin untuk karbohidrat
Hidrolisis pati dapat dilakukan oleh asam atau enzim. Jika pati dipanaskan
dengan asam akan terurai menjadi molekul-molekul yang lebih kecil secara
berurutan, dan hasil akhirnya adalah glukosa.
(C6H10O5)n + n H2O n C6H12O6
Pati air glukosa
Ada beberapa tingkatan dalam reaksi diatas. Molekul-molekul pati mula-mula
pecah menjadi unit-unit rantaian glukosa yang lebih pendek yang disebut dekstrin.
Dekstrin ini dipecah lebih jauh menjadi maltose (dua unit glukosa) dan akhirnya
maltosa pecah menjadi glukosa. (Murdijati Gardjito, 1992).
Proses perubahan pati menjadi glukosa yang dilakukan oleh enzim diastase
pada madu dalam uji aktivitas enzim dengan menggunakan iodin yang disertai
perubahan warna larutannya adalah sebagai berikut :
Pati (Biru ) dekstrin (Biru kecoklatan) akrodekstrin (coklat) Eritrodekstrin
(merah) Maltosa (kuning) Glukosa (Jernih/bening)
+
I
2Larutan Pati
Larutan Iodin
Larutan iodin digunakan untuk tes pati, warna biru tua menandai adanya
larutan pati. Diperkirakan bahwa larutan iodin (ion I3− dan I5−) tersubstitusi ke dalam pati, tersubstitusinya iodin setelah terputusnya ikatan glukosida dalam pati oleh
enzim dan terurai menjadi molekul molekul lebih sederhana, maka makin banyak
terbentuk gugus OH bebas yang dapat disubstitusi oleh iodin sehingga konsentrasi
iodin dalam larutan makin kecil dan molekul air semakin banyak terbentuk, apabila
pati terhidrolisis sempurna maka gugus iodin yang bakal diabsorbsi semakin banyak
atau dipihak lain konsentrasi molekul air akan bertambah, semakin kecil konsentrasi
iodin bebas maka larutan akan berubah menjadi jernih.
2.6 Kualitas Madu
Kualitas madu ditentukan oleh beberapa hal diantaranya waktu pemanenan
madu, kadar air, warna madu, rasa dan aroma madu. Waktu pemanenan madu
harus dilakukan pada saat yang tepat, yaitu ketika madu telah matang dan
rongga rongga madu mulai ditutup oleh lebah. Selain itu kadar air yang terkandung
dalam madu juga sangat berpengaruh terhadap kualitas madu. Madu yang baik
adalah yang mengandung kadar air sekitar 17-21 persen (Sihombing, 1997).
Di Indonesia, kualitas madu ditentukan oleh Standar Nasional Indonesia
(SNI) nomor 01-3545-2004 tahun 2004 (Tabel 2-3), standar tersebut merupakan
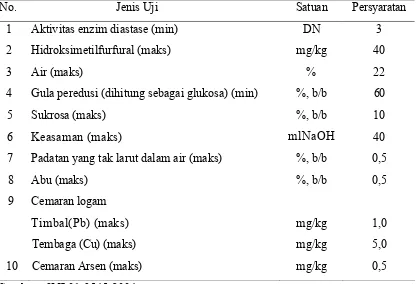
Tabel 2‐3. Syarat Mutu Madu
No. Jenis Uji Satuan Persyaratan
1 Aktivitas enzim diastase (min) DN 3
2 Hidroksimetilfurfural (maks) mg/kg 40
3 Air (maks) % 22
4 Gula peredusi (dihitung sebagai glukosa) (min) %, b/b 60
5 Sukrosa (maks) %, b/b 10
6 Keasaman (maks) mlNaOH 40
7 Padatan yang tak larut dalam air (maks) %, b/b 0,5
8 Abu (maks) %, b/b 0,5
9 Cemaran logam
Timbal(Pb) (maks) mg/kg 1,0
Tembaga (Cu) (maks) mg/kg 5,0
10 Cemaran Arsen (maks) mg/kg 0,5
Sumber : SNI 01-3545-2004
2.7 Asam Dalam Madu
Ciri rasa dan aroma madu sebagian disumbang oleh asam-asam yang
dikandungnya; sumbangan lain adalah perlindungan terhadap mikroorganisme (pH
madu = 3,91). Paling sedikit ada 11 jenis asam yang diketahui terdapat dalam madu
dan kemungkinan masih ada tambahan tujuh lagi terdapat dalam madu (tabel 2-4)
Keasaman madu ditentukan oleh disosiasi ion hydrogen dalam larutan air,
namun sebagian besar juga kandungan berbagai mineral antara lain Ca, Na, K dan
Tabel 2‐4. Beberapa Jenis Asam Yang Dijumpai Dalam Madu
Asam Tahun Ditemukan Dalam Madu
Asetat 1960
α-atau β-gliserofaosfat 1966
Glukose-6-fosfat 1966
Sumber : Sihombing, 1994
2.8 Enzim Yang Terkandung Dalam Madu
Dua enzim yang mencolok dalam madu yakni enzim diastase dan invertase.
Konsep enzim yang lama menggolongkan enzim amylase menjadi dua kelompok
yakni α-amilase (amiloklastik atau amilitik) yang memutuskan rantai pati secara acak
menjadi dekstrin dan menghasilkan hanya sedikit gula tereduksi. Kelompok kedua, β
pati. Derajat keasaman (pH) optimum bagi α-amilase berkisar antara 5,0 pada suhu
22-300C sampai 5,3 pada suhu 45-500C, sedang untuk β-amilase adalah 5,3. Laporan
terbanyak akan pH optimum bagi diastase madu adalah 5,3.
Pemanasan maupun penyimpanan lama terhadap madu mengakibatkan
inaktivasi enzim madu dan data kinetik enzim madu telah diketahui sehingga waktu
paruh hidupnya (half-life) dapat diketahui.
Lebah madu tidak dapat memanfaatkan pati mentah. Sumber diastase dalam
madu adalah lebah madu sendiri, meski ada juga yang menduga nektar sebagai
sebagian sumbernya. Enzim invertase (sukrase, sakharase) berperan mengubah nektar
menjadi madu; lebah madu menambah invertase ke nektar dan aktivitas invertase
berlanjut juga dalam madu yang diekstraksi. Ada dua tipe invertase umum dikenal
dalam madu, fruktoinvertase dan glukoinvertase, dan substrat bagi invertase adalah
sukrosa yang dihidrolisis menjadi glukosa dan fruktosa. Hidrolisis ini berlanjut dan
karena bereaksi atas sukrosa hingga terbentuk berbagai oligosakarida. Salah satu
oligosakarida pokok adalah trisakharida baru yakni α-maltosyl-β-fruktoside (juga
dikenal dengan nama frukromaltosa, gluko-sukrosa, erlosa). Melezitosa yang telah
lama diketahui terdapat dalam manna dan honeydew adalah juga produk hidrolisis
sukrosa oleh enzim lebah madu. (Sihombing, 1994)
Faktor faktor Yang Mempengaruhi Kerja Enzim :
Konsentrasi enzim, seperti pada katalis lain kecepatan suatu reaksi yang menggunakan enzim tergantung pada konsentrasi enzim tersebut, demikian
pula dengan penambahan konsentrasi substrak akan menaikkan kecepatan
reaksinya.
Suhu, karena reaksi kimia dapat dipengaruhi oleh suhu, maka reaksi yang
menggunakan katalis enzim dapat dipengaruhi oleh suhu. Pada suhu rendah
reaksinya berlangsung cepat. Khusus pada enzim dalam madu suhu
optimumnya adalah 37oC. Karena enzim adalah suatu protein maka kenaikan
suhu berlebih dapat menyebabkan terjadinya proses denaturasi.
Pengaruh pH, seperti protein pada umumnya, struktur ion enzim tergantung
pada pH lingkungannya. Enzim dapat bermuatan positif, ion negatif atau ion
bermuatan ganda. Dengan demikian perubahan pH lingkungan akan
berpengaruh terhadap efektifitas bagian aktif enzim dalam membentuk
kompleks enzim substrat. pH rendah atau tinggi dapat pula menyebabkan
enzim terdenaturasi dan ini mengakibatkan menurunnya aktivitas enzim.
Terakhir yang mempengaruhi aktivitas enzim adalah pengaruh inhibitor.
(Poedjiadi, 1994)
2.9 Warna Madu
Zat penyebab warna madu sebagian besar belum diketahui, namun ada yang
menduga terdiri dari fraksi yang larut air dan larut lemak. Pada madu yang berwarna
cerah, zat warna larut air lebih sedikit dari zat warna yang larut lemak. Ada juga yang
menduga oleh berbagai senyawa polifenol, terutama pada madu berwarna pekat.
Oksidasi yang berlangsung atas zat-zat ini akan semakin menimbulkan warna. Warna
yang timbul pada madu yang tersimpan lama disebabkan oleh kombinasi beberapa
faktor, misalnya gabungan tannat dan polifenol lain dengan zat besi dari kemasan
atau alat pengolah, reaksi dari gula tereduksi dengan senyawa mengandung nitrogen
amino (asam amino, polipeptida, protein) dan ketidakstabilan fruktosa dalam larutan
asam. Madu cerah hampir tak mengandung tirosin dan triptofan, sedang pada madu
berwarna pekat hal sebaliknya yang terdapat. (Sihombing, 1994)
2.10 Aroma Pada Madu
Maeda et al (1962) menganggap rasa madu disebabkan oleh kandungan gula,
banyaknya variasi penyebab rasa tersebut seperti oleh berbagai glukosida dan
alkaloid yang khas bagi tumbuhan sumber nektar. Dengan berkembangnya
penggunaan gas liquid chromatography semakin giat penelitian terhadap senyawa
asam-asam mudah menguap (volatile acids) yang terdapat diberbagai sumber madu,
banyak senyawa pembentukan aroma madu, antara lain formaldehida, asetaldehida,
aseton, isobutiraldehida dan diasetil (tabel 2-5). Aroma mencolok pada madu berasal
dari nektar jeruk citrun disebabkan oleh methyl anthranilate yang meski terdapat
hanya sedikit sekali. (Sihombing, 1994)
Tabel 2‐5. Pembentukan Aroma Pada Madu
Karbonil Alkohol Ester
Acetaldehyde Benzyl alcohol Dietyl ether
Acetone Β-methallyl alcohol Ethyl formate
Butyraldehyde Ethanol Methyl formate
Formaldehyde Isobuthanol
Isovalaradehyde 2-buthanol
Methacrolein 2-methyl-1-buthanol
Methyl ethyl ketone 3-methyl-1-buthanol
Propionaldehyde 3-methyl-2-buthanol
3-pentanol
n-butanol
n-pentanol
n-propanol
phenylethyl alcohol
2.11 Vitamin Dalam Madu
Sekitar tahun 1920 hingga 1930 hanya sedikit macam vitamin yang diketahui
dalam madu. Namun sejak 1930 penelitian dengan cara mikrobiologis terus dilakukan
dan kini menggunakan uji mikrokimiawi semakin banyak macam vitamin
diketemukan dalam madu, meskipun hanya sedikit terdapat dan mungkin kurang
dapat diandalkan sebagai sumber pokok kebutuhan vitamin pada manusia. Beberapa
vitamin larut-air terdapat dalam madu (tabel 2-6) antara lain tiamin (B1), riboflavin
(B2), piridoksin (B6), asam pantotenat, niasin, dan asam askorbat; namun
vitamin-vitamin lain seperti biotin, asam folat, kholin dan asetil kholin terdapat juga dalam
madu. Vitamin larut-lemak seperti vitamin K yang ekivalen dengan 25 µg menadion
per 100 gr madu juga ditemukan. (Sihombing, 1994)
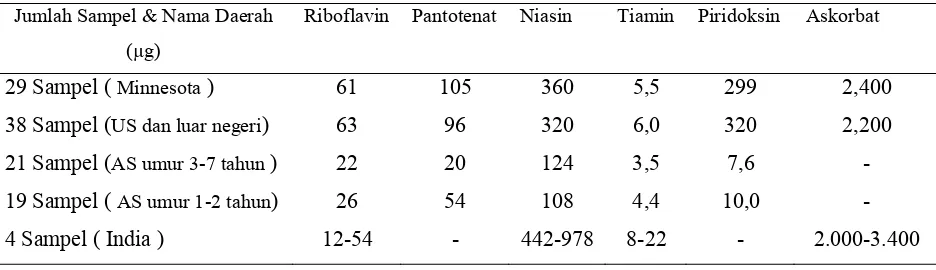
Tabel 2‐6. Vitamin dalam madu
Jumlah Sampel & Nama Daerah (µg)
Riboflavin Pantotenat Niasin Tiamin Piridoksin Askorbat
29 Sampel ( Minnesota ) 61 105 360 5,5 299 2,400
2.12 Mineral dalam Madu
Mineral-mineral dalam madu dikategorikan dalam tiga bahasan yakni total
abu (mineral), banyak mineral esensial dan keberadaan kandungan logam-logam yang
sangat sedikit terdapat.
Total abu dalam madu yang berasal dari Amerika Serikat misalnya, 0,17%
dan berkisar antara 0,02-1,03 persen. Sekitar awal abad ini pernah dipublikasikan
yang patut dicurigai. Patokan abu madu yang berasal dari Amerika Serikat
membolehkan maksimum 0,25% abu.
Dalam madu terdapat 18 unsur mineral esensial dan 19 unsur nonesensial
yang pernah diteliti.(Sihombing, 1994)
2.13 Kadar Air Madu
Banyaknya air dalam madu menentukan keawetan madu. Madu yang
kadarnya airnya tinggi, gampang berfermentasi. Fermentasi terjadi karena jamur yang terdapat dalam madu. Jamur ini tumbuh aktif bila air dalam madu tinggi. Sewaktu
madu masih tersimpan dalam sel sisiran yang tertutup rapat, selama itu madu tidak
mengalami fermentasi. Kandungan air dalam madu yang demikian ini sangat rendah sekali, berkisar 17,4%, massa jenis 1,4212 gr/cc pada temperatur 200C. Madu seperti
ini tidak akan berfermentasi meskipun dalam bentuk Kristal.
Pada waktu panen madu masih ramai-ramainya, madu yang dipanen mungkin
masih banyak yang belum masak, belum ditutup dalam sel. Oleh karena itu
kandungan airnya akan lebih tinggi dari angka tersebut di atas. Karena madu bersifat
higrokopis, kalau menyimpan madu harus memakai tempat yang tidak tembus udara.
Kandungan air dalam madu dapat diukur dengan menggunakan suatu alat
yang dinamakan hydrometer yang dilengkapi dengan thermometer. Dapat pula pengukuran air tersebut dengan alat yang dinamakan refractometer. Misalnya kadar air 17,4% refracto indeks sebesar 1,493 pada suhu 200C. Makin besar kadar air makin
kecil bilangan refracto indeksnya.
Cara mengetahui kadar air yang lebih mudah adalah dengan metode
gravimetri, tetapi perkiraan ini sedikit kasar, yaitu 1 cc madu yang mengandung
2.14 Manfaat Madu
Peradaban kuno menganggap madu adalah makanan dewa karena biasanya
membuat manusia berusia panjang. Orang Mesir, Yunani dan Romawi kuno telah
menggunakan madu untuk kue dan minuman serta bumbu daging. Madu merupakan
makanan manis alamiah yang tertua bagi manusia.
Pengobatan dengan madu telah dikenal orang Mesir kuno sejak 2600 SM.
Madu digunakan sebagai saleb antiseptik untuk mengobati luka oleh bangsa Yunani,
Romawi, Assyria, dan Cina kuno, bangsa Jerman pun memakainya ketika Perang
Dunia II. Madu dipakai karena memiliki kelebihan-kelebihan sebagai berikut:
Madu merupakan suplemen makanan yang baik
Madu mencegah terjadinya peragian dalam saluran pencernaan dan
kandungan gizinya cepat diserap tubuh
Madu mengandung elemen-elemen penting untuk membentuk darah baru
Madu memiliki efek laksatif sehingga mencegah rasa mual
Madu bertindak sebagai sedaktif sehingga dapat menyebabkan tidur nyenyak
Di dalam tubuh, madu dimetabolisir seperti halnya gula sehingga
menyebabkan kadar snotonin (suatu senyawa yang dapat meredakan aktivitas
otak) dalam otak yang menginduksi pada relaksasi dan keinginan untuk tidur
Madu tidak perlu dicerna terlebih dahulu dalam tubuh manusia karena sudah
lebih dulu dicerna dalam pencernaan lebah ketika masih berupa nektar
Madu mencegah pertumbuhan mikroba seperti salmonella, shigela, S.Coli, dan V. chlolrerae yang meyebabkan diare. Dalam percobaan madu sebagai antibiotika, kadar gulanya dihilangkan. Ternyata madu tanpa gula sama
Walaupun sejak abad ke-19 peranan madu sebagai pemanis telah tergeser gula
yang terbuat dari tebu dan bit, sampai sekarang madu masih dimanfaatkan orang
untuk berbagai pembuatan kue, es krim, dan pudding. Madu juga dapat dipakai untuk
pengoles roti. Madu bersifat mengikat molekul air. Kue yang diberi madu sebelum
dipanggang tak akan mengering dan mengeras.
Selain mengandung gula, madu juga mengadung garam mineral, protein,
lemak dan vitamin (A, B dan C). Berdasarkan hasil penelitian Balai Penelitian Kimia
Bogor dan Bagian Ilmu Gizi Fakultas Kedokteran Universitas Indonesia, dalam 100
gram madu terdapat 294 kalori. 9,5 gram karbohidrat, 24 gram air, 16 mgram fosfor,
5 mg kalsium, 4 mg vitamin C. Jumlah kalori madu itu jauh lebih banyak
dibandingkan dengan daging kambing (100 gram mengandung 206 kalori) dan
daging kornet (100 gram mengandung 241 kalori). (Sarwono, 2001)
2.15 Menentukan pH
Instrumen pH meter adalah peralatan laboratorium yang digunakan untuk
menentukan pH atau tingkat keasaman/kebasaan dari suatu larutan. Tingkat
keasaman/kebasaan dari suatu zat,ditentukan berdasarkan keberadaan jumlah ion
hidrogen dan ion hodroksida dalam larutan. Keuntungan dari penggunaan pH
meter dalam menentukan tingkat keasaman suatu senyawa adalah:
Pemakaiannya bisa berulang-ulang Nilai pH terukur relatif cukup akurat
Instrumen yang digunakan antara lain kertas lakmus universal, pH meter
bersifat analog maupun digital, Sebagaimana alat yang lain, untuk mendapatkan
hasil pengukuran yang baik, maka diperlukan perawatan dan kalibrasi pH meter.
Pada penggunaan pH meter, k a l i b r a s i a l a t h a r u s d i p e r h a t i k a n s e b e l u m
d i l a k u k a n p e n g u k u r a n . ( http ://images. agungrahmatgunawan. multiply, multiply
BAB 3
METODOLOGI PENELITIAN
3.1. Lokasi Penelitian
Penelitian dilakukan di Laboratorium Biokimia FMIPA Universitas Sumatera
Utara.
3.2. Alat & Bahan
3.2.1. Alat-alat yang digunakan
- Tabung reaksi
- Erlenmeyer
- Gelas kimia
- Labu ukur
- Gelas ukur
- Buret
- Pipet volum
- Penangas air
- prezeer
- Pipet tetes
- Termometer
- Tabel plate
- Stopwatch
- Timbangan digital
- Piknometer.
- pH meter digital
3.2.2. Bahan – bahan yang digunakan
- Sampel Madu terdiri dari 7 jenis sampel dari berbagai sumber
- Akuades
- Larutan fehling A
- Larutan fehling B
- Indicator metylen – blue
- Larutan pati 1%
- Larutan iodine 0.01 N
3.2.3. Pembuatan larutan
- Pembuatan larutan fehling A, Larutkan 3,5gr Tembaga Sulfat (CuSO4 5H2O)
dalam air sampai menjadi 50ml.
- Pembuatan larutan fehling B, Larutkan 17,3gr Kalium-Natrium Tartrat
(KNaC4H4O6 4H2O) dan 5g Natrium Hidorokisada (NaOH) dalam air
sampai menjadi 50ml.
- Pembuatan indikator metylen- blue, Larutkan 5gr Metylen Blue dalam 100ml
Etanol 95%, Kemudian tambahkan 10ml Kalium Hidrokisida ( KOH ) 0,01%.
- Pembuatan larutan pati 1 %, dilarutkan 1 gr pati ke dalam labu ukur
100 ml kemudian ditambahkan akuades sedikit demi sedikit sampai tanda
batas sambil dikocok sampai tercampur sempurna.
- Pembuatan larutan iodine 0,01 N, dilarutkan 0,126 gr kristal iodine kedalam
50 ml akuades, dikocok hingga tercampur sempurna.
3.3. Prosedur Penelitian 3.3.1. Penyediaan Sampel
Sampel madu diperoleh dari :
Sampel 1 berasal dari madu asli dari peternakan lebah milik Bapak H.
Sampel 2 berasal dari madu asli dari peternakan Bapak S. Siregar dari kecamatan Parranginan.
Sampel 3 berasal dari madu yang dijual di Toko Santa Lucia
Kecamatan Siborongborong.
Sampel 4 berasal dari madu yang dijual di Toko Marpahala Kecamatan Siborongborong
Sampel 5 berasal dari madu yang dijual Keliling di Kecamatan
Siborongborong
Sampel 6 berasal dari madu yang dijual Keliling di Kecamatan
Balige
Sampel 7 berasal dari madu yang dijual Keliling di Kecamatan Sidikalang
3.3.2. Test / uji yang dilakukan
3.3.2.1Mengukur Berat Jenis ( Bj )
Diambil piknometer kosong dan bersih kemudian ditimbang sampai berat
konstan.
Untuk kalibrasi, Piknometer diisi dengan Aqudes kemudian ditimbang sampai
beratnya konstan.
Piknometer diisi dengan sampel kemudian ditimbang, catat massa yang
didapat
Perlakuan diatas dilakukan pada seluruh sampel sebanyak 3 kali.
3.3.2.2Disimpan dalam freezer
3.3.2.3Tes Nyala
Penelitian ini menggunakan korek api sebanyak 3 biji Kepala korek api dicelupkan ke dalam sampel madu Didiamkan selama 3 menit
Dilakukan pemantikan, diamati apakah korek menyala Prosedur diatas dilakukan pada seluruh sampel.
3.3.2.4Mengukur derajat keasaman ( pH )
Pengukuran derajat keasaman dari sampel menggunakan alat pH meter digital Mengkalibrasi pH meter ke dalam aquades.
Memasukkan indikator pH meter sampai tanda batas ke dalam sampel Didiamkan sebentar dan catat hasilnya, dilakukan pada seluruh sampel.
3.3.2.5 Tes gula reduksi
Penentuan % Gula Reduksi Metode Lane – Eynon
Diencerkan 1 ml sampel ke dalam labu ukur 100 ml kemudian masukkan ke
dalam buret
Dimasukkan 5 mL Fehling A dan 5 mL Fehling B ke dalam gelas Erlenmeyer
lalu dipanaskan
Lalu ditambahkan 15 mL larutan sampel yang telah diencerkan dan 3 tetes
indikator Metylen – Blue ke dalam gelas Erlenmeyer tersebut dan lanjutkan
pemanasan sampai mendidih
Dititrasi campuran larutan yang dipanaskan tersebut dengan larutan sampel
yang telah di encerkan hingga Metylen – Blue berubah menjadi putih Metylen
(atau terbentuk endapan merah bata). Selama proses titrasi berlangsung,
pemanasan tetap dilanjutkan.
Perhitungan :
% Gula Reduksi =
Ket:
F = Faktor koreksi analisis gula reduksi (berdasarkan tabel)
FP = Faktor pengenceran
3.3.2.6Tes aktivitas enzim ( Tes iodin terhadap hasil hidrolisis Pati oleh enzim yang
terdapat dalam madu )
Ke dalam tabung reaksi yang berisi 3 ml sampel madu ditambahkan 10 ml
larutan pati 1% (di kocok sampai campuran homogen)
Kemudian sampel tersebut dipanaskan ke dalam waterbath yang bersuhu 370C Setelah didinginkan 3 menit, diambil 2 ml larutan sampel dan dimasukkan ke
dalam tabung reaksi lain untuk kemudian dicampurkan dengan 2 tetes cairan
iodium 0,01N
Kemudian larutan sampel dipanaskan kembali pada suhu 370C hingga terjadi
perubahan warna
Catat waktu yang dibutuhkan selama proses perubahan warna larutan dari
larutan biru hingga larutan bening
Dikerjakan pada seluruh sampel dengan cara yang sama dan lakukan 3 kali
3.3.2.7Bagan Penelitian Tes gula reduksi
Ditambahkan 5 mL Fehling A dan 5 mL Fehling B
Dipanaskan
15 mL larutan sampel
3 tetes indikator Metylen – Blue
Lanjutkan pemanasan sampai mendidih
Dititrasi campuran larutan sambil dipanaskan
Dititrasi dengan larutan sampel hasil pengenceran
hingga Metylen – Blue berubah menjadi putih Metylen
(merah bata )
Catat Volume Titran Dan Tentukan Kadar Gula Reduksi Dalam Sampel
3.3.2.8 Bagan Penelitian uji aktivitas enzim
3 ml Sampel Madu Dalam
Tabung
Reaksi
10 ml larutan pati 1% (di kocok sampai campuran
homogen)
Dipanaskan dalam waterbath hingga bersuhu 370C
Kemudian didinginkan 3 menit
Diambil 2 ml dari larutan sampel dan dimasukkan ke dalam
tabung reaksi A
Dicampurkan 2 tetes cairan iodium 0,01N
Dipanaskan kembali pada suhu 370C hingga terjadi
perubahan warna biru menjadi bening
2 ml Larutan Dalam Tabung Reaksi A
Tentukan waktu perubahan sampel hingga larutan
BAB 4
HASIL PENELITIAN DAN PEMBAHASAN
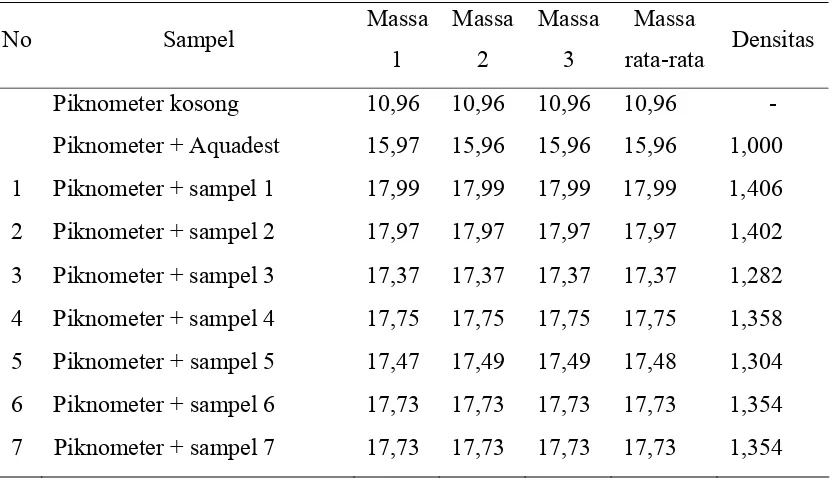
4.1 Mengukur berat jenis
Dari hasil pengukuran berat jenis seluruh sampel maka didapat data sebagai
berikut
Nb : Piknometer yang digunakan ukuran 5 ml
Pembahasan :
- Dari hasil penelitian didapat bahwa densitas sampel madu asli 1 dan 2 mempunyai
nilai densitas 1,406 dan 1,402 hal tersebut hampir sama bila dibandingkan dengan
densitas dari tinjauan literatur dimana madu mempunyai densitas 1,41
- Untuk sampel madu 3, 4, 5, 6, 7 memiliki densitas yang lebih rendah dari sampel
madu asli yaitu 1,282 . 1,358 . 1,304 . 1,354 . 1,354
- Perbedaan densitas antara sampel madu asli dan madu palsu dapat diasumsikan
terjadi karena kandungan zat terlarut yang lebih banyak pada madu asli jika
dibandingkan dengan madu palsu untuk jumlah (volume) yang sama.
- Sampel madu asli sampel 1 dan sampel 2 memiliki densitas yang lebih tinggi
dimungkinkan karena kandungan air yang lebih sedikit dimana madu yang
diperoleh dari pasaran (sampel 3, 4, 5, 6, 7) kemungkinan bercampur dengan air
ataupun uap air selama proses pemasarannya karena madu merupakan bahan
Higroskopis yang sangat dipengaruhi oleh kelembapan udara.( Sarwono, 2001)
4.2 Disimpan dalam freezer & Tes Nyala
Tabel 4.2 Disimpan dalam freezer & Tes Nyala
Disimpan dalam freezer Tes Nyala No Sampel
- Sampel 1 dan 2 yang merupakan sampel madu asli keadaannya membeku, hal ini
membantah asumsi yang berkembang di masyarakat yang mengatakan bahwa
madu asli tidak akan membeku. Madu asli tidak akan membeku saat disimpan di
lemari es. Kecuali jenis madu Karet, Kaliandra dan alpukat madu murni tersebut
akan mengkristal (Blog master madu murni). Sedangkan sampel madu 1 dan 2
diambil dari peternakan lebah pada pohon-pohon makadame ( dalam bahasa batak
toba dikenal dengan pohon Anti api)
- Untuk sampel 3,4,5,6,7 keadaan akhir setelah disimpan dalam freezer adalah
berwujud cairan
Tes fisik dengan tes Uji nyala terhadap seluruh sampel yang didapat adalah :
- Tes uji nyala ini menggunakan korek api, mencelupkan kepala korek api terhadap
madu ditunggu 3 menit kemudian dilakukan pemantikan.
- Dari hasil penelitian seluruh korek api menyala setelah dilakukan pemantikan,tes
ini memperlihat kandungan air yang ada dalam sampel madu sangat rendah, jika
kandungan airnya tinggi maka fospor merah yang terdapat dalam korek api akan
4.3 Mengukur derajat keasaman ( pH )
Dari hasil pengukuran derajat keasaman seluruh sampel maka didapat data
sebagai berikut :
Tabel 4.3. Mengukur derajat keasaman ( pH )
No Sampel Cek pH
1 1 4
2 2 4
3 3 3
4 4 3
5 5 3
6 6 3
7 7 2
Pembahasan :
Dari hasil pengukuran derajat keasaman dari keseluruhan sampel didapat
bahwa
- Mengukur derajat keasaman dari semua sampel diatas dilakukan dengan
menggunakan pH meter digital.
- sampel 1 dan 2 yang merupakan sampel madu asli memiliki derajat keasaman
sama dengan 4, data tersebut hampir sama jika dibandingkan dengan literatur
tinjauan pustaka (Crane ,1975) yang menyatakan bahwa bahwa madu memiliki
derajat keasaman sama dengan 3.91 atau berada dalam kisaran 3,42 - 6,10 dan
jika dibandingkan juga dalam uji kualitas madu berdasarkan Standar Nasional
Indonesia menyatakan bahwa madu dengan kualitas baik harus berada dalam
antara derajat keasaman 3,4 – 4,5. Berarti sampel madu 1 dan 2 termasuk dalam
- Sampel 3 , 4, 5 dan 6 yang merupakan sampel madu yang beredar dipasaran
memiliki derajat keasaman sama dengan 3 dimana hal tersebut menandakan
bahwa sampel sampel tersebut memiliki derajat keasaman yang lebih tinggi
(lebih bersifat asam ) dari sampel madu asli yang diteliti dan dapat disimpulkan
sampel sampel madu tersebut merupakan madu dengan kualitas rendah yang
diperhatikan dari derajat keasaamannya.
- Sampel 7 yang merupakan sampel madu yang beredar dipasaran memiliki derajat
keasaman sama dengan 2 dimana hal tersebut menandakan bahwa sampel tersebut
memiliki derajat keasaman yang lebih tinggi dari keseluruhan sampel
dibandingkan dalam uji kualitas madu berdasarkan Standar Nasional Indonesia
menyatakan bahwa madu dengan derajat keasaman antara 2,4 – 3,3 termasuk
dalam kualitas rendah. Maka dapat diasumsikan sampel madu tersebut merupakan
madu dengan kualitas yang terendah bila dibandingkan dengan seluruh sampel
penelitian.
- Sampel 1 dan 2 memiliki derajat keasaman yang lebih rendah dari sampel yang
lain, menurut peneliti hal ini disebabkan karena :
Sampel madu 3,4,5,6,7 kemungkinan berasal dari madu oplosan atau madu
palsu yang berasal dari bahan baku nenas, dimana sari nenasnya ditambahkan
dengan sari gula dan dipanaskan sampai tingkat kekentalan tertentu, dimana
bahan baku nenas tersebut sudah mengandung kadar asam yang tinggi maka
derajat keasaman sampel madu asli lebih rendah dibandingkan dengan sampel
madu dari apotik dan dari pasaran.
Madu yang tersimpan lama akan mengalami penyusutan karena terjadi proses
fermentasi yang selanjutnya berubah menjadi asam asetat, sehingga derajat
keasaman madu semakin lama akan semakin tinggi. Maka dapat diasumsikan
Sampel madu 3,4,5,6 dan 7 lebih tinggi derajat keasamannya dibandingkan
sampel 1 dan 2. Hal ini dapat dipengaruhi oleh kandungan berbagai mineral,
dimana semakin banyak kandungan mineral dalam madu maka pH madu akan
semakin tinggi (Sihombing, D.T.H, 106)
4.4Tes gula reduksi
Dari hasil pengukuran tes gula reduksi seluruh sampel maka didapat data sebagai
berikut :
Tabel 4.4. Tes gula reduksi
No Sampel Volume titran % gula reduksi ( gr / 100ml )
1 1 0,6 ml 32.4
2 2 1,2 ml 31.6
3 3 2,4 ml 30.1
4 4 0,1 ml 33.2
5 5 1,65 ml 31.0
6 6 0,8 ml 32.2
7 7 0,5 ml 32.6
Keterangan : perhitungan % gula reduksi = x F p ( mg/100 ml )
Pembahasan :
Dari hasil penelitian tes gula reduksi diatas didapat bahwa :
- Sampel madu asli 1 memiliki persentase gula pereduksi sebesar 32,4 gr/ 100 ml
- Sampel madu asli 2 memiliki persentase gula pereduksi sebesar 31,6 gr/ 100 ml
- Sampel madu 3 memiliki persentase gula pereduksi sebesar 30,1 gr/ 100 ml
- Sampel madu 4 memiliki persentase gula pereduksi sebesar 33,2 gr/ 100 ml
- Sampel madu 5 memiliki persentase gula pereduksi sebesar 31,0 gr/ 100 ml
- Sampel madu 7 memiliki persentase gula pereduksi sebesar 32,6 gr/ 100 ml
Dari keseluruhan sampel madu didapatkan data gula pereduksi yang hampir
sama sehingga tidak dapat menjadi patokan khusus dalam membedakan
sampel-sampel tersebut apakah madu asli, madu oplosan atau madu palsu.
Madu mengandung berbagai jenis gula pereduksi yaitu glukosa, fruktosa, dan
maltosa.
4.5 Uji aktivitas Enzim
Dari hasil uji aktivitas enzim seluruh sampel maka didapat data sebagai berikut : Tabel 4.5.
Percobaan I Percobaan II Percobaan III
Perubahan warna Perubahan warna Perubahan warna
Sampel
Sebelum Sesudah Waktu
(detik) Sebelum Sesudah
Waktu
(detik) Sebelum Sesudah
Waktu
Dari uji aktivitas enzim yang telah dilaksanakan maka didapat bahwa :
- Larutan pati yang ditambahkan larutan iodin akan menghasilkan warna biru.
Enzim diastase yang dihasilkan oleh lebah dalam pembentukan madu akan
mengubah pati menjadi glukosa. Dengan adanya aktivitas enzim diastase warna
biru pada larutan pati akan hilang. Semakin tinggi aktivitas enzim semakin cepat
- Proses perubahan pati menjadi glukosa yang dilakukan oleh enzim diastase pada
madu dalam uji aktivitas enzim dengan menggunakan iodin yang disertai
perubahan warna larutannya adalah sebagai berikut :
- Pati (Biru ) dekstrin (Biru kecoklatan) akrodekstrin (coklat)
Eritrodekstrin (merah) Maltosa (kuning) Glukosa (Jernih/bening)
Pembahasan Hasil percobaan :
- Untuk sampel 1 dan 2 membutuhkan waktu 7.3 detik dan 10.6 detik untuk
mengubah pati menjadi glukosa, hal ini menunjukkan bahwa aktivitas enzim
dalam madu sangat tinggi dimana perubahan warnanya berlangsung dengan cepat.
- Untuk sampel 3 , 4 dan 5 membutuhkan waktu 115 detik, 112.3 detik dan 247.3
detik untuk mengubah pati menjadi glukosa, hal ini menunjukkan adanya aktivitas
enzim dalam madu dengan kemungkinan jumlah yang lebih sedikit karena
perubahan warnanya berlangsung agak lambat.
Melihat perbedaan waktu yang sangat jauh dibandingkan antara sampel madu
asli 1 dan 2 dengan sampel madu 3, 4, 5 dapat diasumsikan bahwa :
Sampel madu 3,4 dan 5 kemungkinan adalah madu oplosan, dimana madu asli dicampur dengan madu palsu dalam perbandingan tertentu sehingga
aktivitas enzimnya akan berlangsung lambat yang berarti enzim dalam
sampel sangat sedikit.
Sampel madu 3, 4, 5 mungkin berasal dari madu asli tetapi telah
mengalami penyimpanan yang cukup lama sehingga enzim yang ada dalam
madu telah melewati batas half-lifenya yang mengakibatkan inaktivasi
enzim
- Untuk sampel 6 dan 7 tidak mengalami perubahan warna sama sekali, hal ini
menunjukkan tidak adanya aktivitas enzim di dalam sampel madu tersebut dan
BAB 5
KESIMPULAN DAN SARAN 5.1. Kesimpulan
Dari hasil penelitian dapat diambil kesimpulan sebagai berikut :
1. Densitas Sampel madu asli lebih tinggi daripada densitas dari sampel madu
apotik dan sampel madu yang berasal eceren di pasaran.
2. Sampel madu asli membeku jika disimpan dalam frezer pada suhu -5oC
sedangkan sampel madu apotik dan sampel madu yang berasal dari secara acak
tidak membeku, hal tersebut tergantung asal nektar madu tersebut diambil oleh
lebah.
3. Keseluruhan sampel madu menyala pada tes uji nyala dengan menggunakan
korek api.
4. Keseluruhan sampel memiliki persen gula reduksi yang hampir sama dimana
berkisar antara 30,1 gr/ml – 33,2 gr/ml.
5. Sampel madu asli 1 dan 2 memiliki waktu aktivitas enzim yang sangat tinggi
yaitu 7,3 detik dan 10,6 detik. Untuk sampel madu 3, 4, dan 5 memiliki waktu
aktivitas enzim 155 detik, 112,3 detik dan 247,3 detik, dan sampel madu 6 dan 7
tidak memiliki aktivitas enzim, dimana dapat disimpulkan bahwa kedua sampel
tersebut adalah madu palsu. Karena untuk menguji keaslian madu sesuai dengan
pengujian madu standar nasional Indonesia adalah dengan tes aktivitas enzim.
5.2. Saran
1. Diharapkan dari hasil penelitian ini dapat dilakukan penelitian lebih lanjut
mengenai sumber sumber madu yang lebih bervariasi untuk dibandingkan dan
alat sederhana untuk mengukur aktivitas enzim madu sehingga dapat digunakan
masyarakat luas.
2. Dilihat dari hasil penelitian diharapkan untuk tidak membuat madu palsu