ABSTRAK
PERBANDINGAN DOSIS TOKSIK ANTARA PEMBERIAN
AMOKSISILIN GENERIK BERLOGO DENGAN GENERIK BERMEREK TERHADAP AKTIVITAS SPESIFIK ENZIM KATALASE PADA HATI
TIKUS (Rattus norvegicus) GALUR Sprague dawley Oleh:
NICO ALDRIN AVESINA
Amoksisilin merupakan antibiotik yang banyak dikonsumsi masyarakat Indonesia karena obat ini sangat murah dan mudah didapat, namun banyak masyarakat membelinya tanpa resep dari dokter. Amoksisilin adalah obat yang dimetabolisme dihati, sehingga sering dikaitkan dengan peristiwa merugikan bagi hati. Efek pemberian amoksisilin salah satunya dapat dilihat dari aktivitas enzim katalase di hati. Tujuan penelitian ini adalah untuk mengetahui perbedaan efek pemberian obat generik berlogo dan obat generik bermerek amoksisilin dosis toksik terhadap aktivitas enzim katalase dan mengidentifikasi amoksisilin yang memberikan efek toksik maksimum dan minimum ditinjau dari aktivitas enzim katalase.
Penelitian ini merupakan penelitian eksperimental. Sampel berjumlah 27 hewan coba yang dibagi menjadi 9 kelompok dengan 3 kelompok kontrol dan 6 kelompok perlakuan. Sampel hati diukur aktivitas katalase spesifiknya. Kemudian dilakukan uji statistik dengan one way ANOVA untuk mengetahui hubungan kedua variabel tersebut.
Hasil penelitian menunjukan rerata aktivitas spesifik katalase hati kelompok yaitu kelompok kontrol (KN=0.0039U/mg, KA=0.0019U/mg, KB=0.0018U/mg), kelompok generik berlogo (A1=0.0024U/mg, A2=0.0020U/mg, A3=0.0016U/mg), dan kelompok generik bermerek (B1=0.0018U/mg, B2=0.0017U/mg dan B3=0.0014U/mg).
Kesimpulan dari penelitian ini terdapat perbedaan bermakna secara statistik antara amoksisilin generik berlogo dan amoksisilin generik bermerek, dan obat generik bermerek dengan dosis tertinggi memiliki aktivitas katalase spesifik terendah dan amoksisilin generik berlogo dosis terendah memiliki aktivitas katalase spesifik tertinggi.
ABSTRACT
COMPARISON OF TOXIC DOSE ADMINISTRATION OF GENERIC AMOXICILLIN AND BRANDED AMOXICILLIN TOWARD CATALASE
ACTIVITY SPESIFIC ENZYME OF RAT LIVER (Rattus norvegicus) Sprague dawley STRAINS
By:
NICO ALDRIN AVESINA
Amoxicillin is an antibiotics that widely used by Indonesian society because of it is affordable and easy to obtain, although many people buy it without prescription. Amoxicillin is metabolized in the liver, so often associated by adverse events to the liver. One of the effects amoxicillin administration is seen from the liver catalase activity. The sole purpose of this study is to know the difference between the effect of toxic dose generic and branded amoxicillin administration toward catalase enzyme activity and to identify which gives maximum and minimum toxic effect in terms of catalase enzyme activity.
This is an experimental study. Samples numbered 27 experimental animals divided into 9 groups, with 3 control groups and 6 treatment groups. Activity catalase spesific be measured from liver samples. Then performed a one way ANOVA statistical test to determine the correlation of two variables.
Result showed the mean liver catalase specific activity, that is control groups
(KN=0.0039U/mg, KA=0.0019U/mg, KB=0.0018U/mg), generic groups
(A1=0.0024U/mg, A2=0.0020U/mg, A3=0.0016U/mg), and branded groups (B1=0.0018U/mg, B2=0.0017U/mg dan B3=0.0014U/mg).
The conclusion of this study, there is significant difference statistically between generic amoxicillin with branded amoxicillin, and the highest dose of branded amoxicillin has the lowest liver catalase spesific activity and the lowest dose of generic amoxicillin have the highest liver catalase specific activity.
TERHADAP AKTIVITAS SPESIFIK ENZIM KATALASE PADA HATI TIKUS (Rattus norvegicus) GALUR Sprague dawley
Oleh:
NICO ALDRIN AVESINA
Skripsi
Sebagai Salah Satu Syarat Untuk Memperoleh Gelar SARJANA KEDOKTERAN
pada
Program Studi Pendidikan Dokter Fakultas Kedokteran Universitas Lampung
FAKULTAS KEDOKTERAN UNIVERSITAS LAMPUNG
Untuk Keluarga ZDTNC Tercinta,
yang selalu menemani,
mendukung, dan mendoakan untuk
keberhasilanku.
IKHTIAR DAN TAWAKAL
“Orang
-orang yang beriman dan mengerjakan
kebajikan, mereka mendapat kebahagiaan dan
tempat kembali yang lebih baik”
RIWAYAT HIDUP
Penulis dilahirkan di kota Jakarta pada tanggal 13 Juli 1994 sebagai anak kedua dari
Bapak Dr. sc. H. Zainal Nur Arifin, Dipl.-Ing. HTL, M.T. dan Hj. Kusumani Dewi
Panji Haryati, S.E.
Penulis menempuh pendidikan Taman Kanak-kanak (TK) diselesaikan di TK
Kemala Bhayangkari 18, Jakarta Barat. Pendidikan sekolah dasar (SD) di SD
Negeri 03, Jakarta Barat pada tahun 2000-2002 dan dilanjutkan di SD Negeri 02
Cibubur, Jakarta Timur dan diselesaikan pada tahun 2006. Penulis melanjutkan
pendidikan sekolah menengah pertama (SMP) di SMP Negeri 147 Jakarta Timur
yang diselesaikan pada tahun 2009, kemudian penulis melanjutkan pendidikan
sekolah menengah atas (SMA) di SMA Negeri 14 Jakarta yang diselesaikan pada
tahun 2012.
Tahun 2012, terdaftar sebagai Mahasiswa Fakultas Kedokteran Universitas
Lampung melalui jalur Seleksi Nasional Masuk Perguruan Tinggi Negeri
(SNMPTN) Tertulis. Selama menjadi mahasiswa, penulis pernah aktif pada
organisasi Forum Studi Islam (FSI) Ibnu Sina Fk Unila, dan PMPATD Pakis
SANWACANA
Segala puji dan syukur penulis panjatkan kehadirat Allah SWT, karena atas rahmat
dan hidayah-Nya, penulis dapat menyelesaikan skripsi ini. Shalawat serta salam
semoga senantiasa tercurahkan kepada Nabi Muhammad S.A.W.
Skripsi dengan judul “Perbandingan Dosis Toksik Antara Pemberian Amoksisilin
Generik Berlogo dengan Generik Bermerek terhadap Aktivitas Spesifik Enzim
Katalase pada Hati Tikus (Rattus norvegicus) galur Sprague dawley” adalah salah
satu syarat untuk memperoleh gelar Sarjana Kedokteran di Universitas Lampung.
Penghargaan dan ucapan terima kasih yang tak terhingga penulis haturkan kepada
semua pihak yang telah berperan atas dorongan, bantuan, saran, kritik dan
bimbingan sehingga skripsi ini dapat terselesaikan antara lain kepada:
1. Prof. Dr. Ir. Hasriadi Mat Akin selaku Rektor Universitas Lampung.
2. Dr. dr. Muhartono, S. Ked., M.Kes., Sp.PA. selaku Dekan Fakultas
Kedokteran Universitas Lampung.
3. Dr. dr. Asep Sukohar, M. Kes. selaku pembimbing pertama atas
kesediannya untuk memberikan bantuan, bimbingan, saran, dan kritik dalam
4. dr. Tiwuk Susantiningsih, M. Biomed. selaku pembimbing kedua atas
kesediannya untuk memberikan bantuan, bimbingan, saran, dan kritik dalam
proses penyelesaian skripsi ini.
5. dr. Evi Kurniawaty, M. Sc. selaku pembahas atas kesdiaannya untuk ilmu,
saran-saran yang telah diberikan dalam proses penyelesaian skripsi ini.
6. dr. Susianti, M. Sc. selaku pembimbing akademik atas semua bimbingan,
saran dan nasehat selama perkuliahan dan proses penyelesaian skripsi.
7. Bapak (Dr. sc. H. Zainal Nur Arifin, Dipl.-Ing. HTL, M.T.) dan Ibu (Hj.
Kusumani Dewi Panji Haryati, S.E.) tercinta yang selalu memberikan
mendukung, membantu, membimbing, mendoakan, dan memotivasi untuk
saya menjadi lebih baik.
8. Kakak (dr. Tiffano Taufan Firdaus) dan Adik (Clarissa Maharani Putri)
tercinta yang juga telah menghibur, membantu, mendoakan, dan
memotivasi hingga saat ini.
9. Seluruh staf Dosen Fakultas Kedokteran Universitas Lampung yang telah
memberikan ilmu dan motivasi dalam menjalani pendidikan kedokteran.
10.Kepala laboratorium biokimia dan biomolekuler Fakultas Kedokteran
Universitas Lampung yang telah membantu pengambilan data penelitian:
Nuriah, A.md.
11.Seluruh staf dan karyawan Fakultas Kedokteran Universitas Lampung yang
telah membantu dalam penyelenggaraan seminar proposal hingga ujian
skripsi.
12.Keluarga Besar Nurhendy dan Soemarno, terima kasih banyak untuk semua
Andika Yusuf Ramadhan, Ade Marantika, Airi Firdausia Kudsi, Dyah
Kartika Utami, dan Fetiara Nur Anisa;
14.Sahabat-sahabat lainnya yang telah memberikan semangat, dukungan, dan
canda tawa dalam menyelesaikan skripsi: Intan Siti Hulaima, Septina
Ashariani, Zygawindi Nur Hidayati, dan Muhammad Farrash Hadyan;
15.Sahabat-sahabat “bugenk” yang terus membantu, mendoakan dan
memberikan semangat dalam menyelesaikan skripsi: Fairuz Rabbaniyah,
Desti Nurul Q, Farida Hakim, Ferina Nur Haqiqi, Gheavani Legowo, Hani
Zahiyyah, Hanifah Rahmania, Idzni Mardhiyah, Nindriya Kurniandari, dan
Ratna Agustina;
16.Sahabat-sahabat “GP” lainnya yang telah memberikan semangat, dukungan,
dan canda tawa dalam menyelesaikan skripsi: Adietya Bima, Alexander
Dicky, Bobi Kurnia, Ivani Ridwan, Luqmanul Hakim, M. Ridho Anshori,
Radian Pandhika, dan Karina Nelova;
17.Sahabat-sahabat “babons” yang terus membantu, mendoakan, dan
memberikan semangat dalam menyelesaikan skripsi: Aulia Rahma N,
Indriasari Nurul P, Nani Indah, Radita Prasetyani, Ratu Balqis A, Seffia
Riandini, Silvia Marischa, Suci Widya P, Yvonne, dan Zahra Zettira;
18.Sahabat-sahabatku lainnya yang telah membantu saat penelitian,
memberikan semangat dan doa: Agam Anggoro, Andrian Prasetya, Andrian
Giovani Martin, Singgih Suhananto, Asoly Giovanno, Anasthasia F, dan
Stefani Gista Luvika;
19.Teman-teman angkatan 2012 yang tidak bisa disebutkan satu persatu yang
telah berjuang bersama dan memotivasi satu sama lain dari awal mulai
DAFTAR ISI
1.2. Perumusan Masalah ... 3
1.3. Tujuan Penelitian ... 4
1.4. Manfaat Penelitian ... 4
II. TINJAUAN PUSTAKA ... 6
2.1. Amoksisilin ... 6
2.1.1. Pengertian Amoksisilin ... 6
2.1.2. Amoksisilin Generik Berlogo ... 6
2.1.3. Amoksisilin Generik Bermerek ... 7
2.1.4. Farmakokinetik ... 8
2.1.5. Farmakodinamik ... 10
2.1.6. Toksikologi ... 11
2.2. Hati ... 12
2.2.1. Fisiologi Hati ... 12
2.2.2. Hepatotoksisitas ... 13
2.3. Oksidan dan Antioksidan ... 15
2.3.1. Stress Oksidatif ... 15
2.3.2. Oksidan ... 16
2.3.3. Antioksidan ... 17
2.4. Hewan Coba ... 19
2.5. Kerangka Teori ... 20
ii
2.7. Hipotesis ... 24
III. METODE PENELITIAN ... 25
3.1. Desain Penelitian ... 25
3.2. Tempat dan Waktu Penelitian ... 25
3.3. Populasi Penelitian ... 25
3.3.1. Populasi ... 25
3.3.1.1.Kriteria Inklusi ... 26
3.3.1.2.Kriteria Eksklusi ... 26
3.3.1.3.Kriteria Drop Out ... 26
3.3.2. Besar Sampel ... 26
3.4. Alat dan Bahan Penelitian ... 29
3.4.1. Alat Penelitian ... 29
3.4.2. Bahan Penelitian ... 29
3.5. Identifikasi Variabel dan Definisi Operasional ... 29
3.5.1. Variabel Penelitian ... 29
3.5.2. Definisi Operasional Variabel ... 30
3.6. Cara Kerja ... 31
3.6.1. Aklimatisasi Hewan Coba ... 31
3.6.2. Perhitungan Dosis ... 32
3.6.3. Perlakuan Induksi dengan Amoksisilin ... 33
3.6.4. Terminasi dan Penyimpanan ... 34
3.6.5. Pembuatan Homogenat Sampel ... 34
3.6.6. Penentuan Kinetik Katalase ... 35
3.6.7. Penentuan Kurva Standar Protein ... 36
3.6.8. Penentuan Konsentrasi Protein Hati ... 36
3.6.9. Penentuan Aktivitas Katalase ... 36
3.7. Pengolahan dan Analisis Data ... 37
3.8. Diagram Alir ... 39
3.9. Etika Penelitian ... 40
IV. HASIL PENELITIAN DAN PEMBAHASAN ... 41
4.1. Hasil Penelitian ... 41
4.1.1. Hasil Uji Pendahuluan ... 41
4.1.2. Hasil Uji Lanjutan ... 44
4.2. Pembahasan ... 47
4.2.1. Uji Pendahuluan ... 47
DAFTAR TABEL
Halaman
Tabel 1. Definisi operasional variabel ... 30
v
DAFTAR LAMPIRAN
Lampiran
1. Etik Penelitian
2. Tabel Dummy
3. Kurva Standar Protein
4. Tabel Hasil Uji Pendahuluan
5. Tabel Hasil Uji Lanjutan
6. Uji Statistik
DAFTAR GAMBAR
Halaman
Gambar 1. Kerangka Teori ... 23
Gambar 2. Bagan hubungan antar variabel ... 24
Gambar 3. Diagram alir... 39
BAB I PENDAHULUAN
1.1Latar Belakang
Obat adalah bahan atau paduan bahan-bahan, termasuk produk biologi yang
digunakan untuk mempengaruhi atau menyelidiki sistem fisiologi atau
keadaan patologi dalam rangka penetapan diagnosis, pencegahan,
penyembuhan, pemulihan, peningkatan kesehatan dan kontrasepsi (Menteri
Kesehatan RI, 2006). Obat-obat yang beredar di pasaran/masyarakat
beragam jenis dan harganya, dari obat generik yang murah sampai dengan
obat bermerek yang mahal harganya.
Obat generik adalah salinan (dari obat yang disetujui, innovator/ produk
dagang) yang sama dengan obat generik bermerek, dalam dosis,
keselamatan, kekuatan, daya absorbsi, kualitas, performa, dan tujuan
penggunaan. Obat generik lebih murah karena pembuatan generik tidak
memiliki harga investasi dari pengembangan obat baru. Obat generik
bermerek adalah produk inovator/original yang telah mengalami dan
melewati tes teliti dan terlibat evaluasi dalam pengembangan produk obat
Amoksisilin adalah antibiotik spektrum luas, secara farmakologi antibiotik
beta-laktam aktif efektif melawan bakteri gram positif dan gram negatif.
Antibiotik merupakan salah satu jenis obat yang sering diresepkan untuk
mengobati infeksi bakteri dan beberapa infeksi oleh parasit tertentu.
Amoksisilin (amoxicillin) merupakan antibiotik yang banyak dikonsumsi
masyarakat Indonesia karena obat ini sangat murah dan mudah didapat di
apotik maupun toko yang menjual obat, namun banyak masyarakat
membelinya tanpa resep dari dokter. (Ramos et al., 2012). Ampisilin dan
amoksisilin menyebabkan kerusakan hati dengan insidensi 0,3/10.000
peresepan, dan ketika amoksisilin dikombinasikan dengan asam klavulanat
insidensi kerusakan hati meningkat menjadi 1.7/10.000 peresepan (Murray
et al., 2008).
Hepatotoksisitas obat adalah penyebab utama dari gagal hati akut di amerika
serikat (Chang dan Schiano, 2007). Drug-induced liver injury (DILI)
didefinisikan sebagai cedera hati dikarenakan oleh berbagai obat yang
menyebabkan kelainan dalam pemeriksaan hati atau disfungsi hati dengan
alasan eksklusi dari etiologi lain (Suk dan Kim, 2012). Pemberian
amoksisilin kepada penderita fungsi hati perlu diperhatikan untuk mencegah
hepatotoksisitas karena metabolisme obat ini didominasi di hati, sehingga
apabila terjadi kesalahan pemberian dosis maka dapat mengakibatkan
kerusakan sel hati. Obat yang metabolismenya sebagian besar di hati lebih
sering dikaitkan dengan peristiwa merugikan bagi hati dibanding obat yang
3
Adapun efek pemberian amoksisilin salah satunya dapat dilihat dari
aktivitas enzim katalase di hati (Li et al., 2007; Łukaszewicz-Hussain dan
Moniuszko-Jakoniuk, 2004; Olayinke, 2012).
Dari penjelasan di atas terkait obat amoksisilin dengan aktivitas spesifik
enzim katalase hati pada hepatotoksisitas. Peneliti ingin mengetahui apakah
terdapat perbedaan efek pemberian dosis toksik obat generik dan obat
generik bermerek terhadap aktivitas enzim katalase hati tikus putih (Rattus
norvegicus) galur Sprague dawley.
1.2Perumusan Masalah
Berdasarkan latar belakang di atas, rumusan masalah yang dapat menjadi
fokus dari penelitian ini adalah
1.2.1 Apakah terdapat perbedaan pemberian dosis toksik antara obat
amoksisilin generik berlogo dengan generik bermerek terhadap
aktivitas enzim katalase pada hati tikus putih (Rattus norvegicus)
galur Sprague dawley?
1.2.2 Manakah yang memberikan efek toksik maksimum ditinjau dari
aktivitas enzim katalase?
1.2.3 Manakah yang memberikan efek toksik minimum ditinjau dari
1.3Tujuan Penelitian
Tujuan dari penelitian ini adalah:
1.3.1 Mengetahui perbedaan efek pemberian dosis toksik antara obat
amoksisilin generik berlogo dengan obat generik bermerek terhadap
aktivitas enzim katalase pada hati tikus putih (Rattus novergicus)
galur Sprague dawley.
1.3.2 Mengidentifikasi amoksisilin yang memberikan efek toksik
maksimum ditinjau dari aktivitas enzim katalase.
1.3.3 Mengidentifikasi amoksisilin yang memberikan efek toksik
minimum ditinjau dari aktivitas enzim katalase.
1.4Manfaat Penelitian
1.4.1 Bagi Penulis
1.4.1.1Penelitian ini sebagai wujud pengaplikasian disiplin ilmu yang
telah dipelajari sehingga dapat mengembangkan wawasan
keilmuan peneliti.
1.4.1.2Menambah pengetahuan mengenai perbedaan efek pemberian
obat generik berlogo dan obat generik bermerek amoksisilin
dosis toksik terhadap aktivitas enzim katalase hati tikus putih
(Rattus novergicus) galur Sprague dawley.
1.4.1.3Mendapatakn pengalaman dalam melakukan penelitian dan agar
5
1.4.2 Bagi Instansi
1.4.2.1Sebagai sumber pengetahuan dan referensi mahasiswa lain
untuk melanjutkan penelitian terkait perbedaan efek pemberian
obat generik dan obat generik bermerek terhadap aktivitas
enzim katalase pada hati.
1.4.3 Bagi Masyarakat
1.4.3.1Mengetahui perbedaan efek antara obat generik dengan obat
generik bermerek.
1.4.3.2Mengetahui perbedaan efek antara amoksisilin generik dan
amoksisilin bermerek terhadap enzim katalase pada hati.
1.4.3.3Menambah wawasan dalam memilih antibiotik yang
BAB II
TINJAUAN PUSTAKA
2.1Amoksisilin
2.1.1 Pengertian Amoksisilin
Amoksisilin memiliki nama lain
D(-)-a-amino-p-hydroxybenzylpenicillin, amoksisilin atau amoksisiline. Rumus
kimia amoksisilin adalah (2S,5R,
6R)-6[[(2R)-2-Amino-2-(4-
hydroxyphenyl)acetyl]amino]-3,3-dimetyl-7oxo-4-thia-1-aza-bicyclo[3.2.0] heptane-2-carboxylic acid (Badan Pengawas Obat
dan Makanan RI, 2014; Moffat et al., 2004). Amoksisilin termasuk
antibiotik spektrum luas yang sering diresepkan pada anak untuk
pengobatan pneumonia dan penyakit lain, termasuk infeksi bakteri
pada telinga, sinus, tenggorokan, saluran kemih, kulit, abdomen dan
darah. Amoksisilin diformulasikan dalam kapsul konvesional, tablet,
bubuk untuk suspensi oral, dan tablet dispersibel (UNICEF, 2013).
2.1.2 Amoksisilin Generik Berlogo
Obat generik adalah obat dengan nama resmi International Non
Propietary Names (INN) yang ditetapkan dalam Farmakope
7
dikandungnya (Menteri Kesehatan RI, 2010). Obat generik memiliki
kesamaan daftar nama referensi obat dengan berhubungan pada
kondisi penggunaan, bahan aktif, rute administrasi, bentuk dosis,
kekuatan, keselamatan, karakteristik performa dan labeling (Rohilla
et al., 2011).
Obat generik harus sama tujuan penggunaan dengan produk pelopor
yang menyediakan prototipe. Terkadang obat generik memiliki
warna, rasa, dan bahan aktif berbeda dan juga tidak terlihat sama satu
merek dengan yang lainnya karena merek dagang. Obat generik juga
telah melalui ulasan ilmiah yang ketat untuk memastikan keamanan
dan kemanjuran, tetapi ada banyak kesalahpahaman tentang kualitas,
efektivitas, durasi tindakan, dan khasiat mengenai produk obat
generik (Rohilla et al., 2011).
2.1.3 Amoksisilin Generik Bermerek
Obat generik bermerek/bernama dagang adalah obat generik dengan
nama dagang yang menggunakan nama milik produsen obat yang
bersangkutan (Menteri Kesehatan RI, 2010). Obat generik bermerek
adalah produk inovator/pelopor yang mengalami dan melewati tes
teliti dan terlibat evaluasi dalam pengembangan produk obat. Obat
generik bermerek/inovator lebih mahal dibanding obat generik
Obat generik bermerek dasarnya produk obat generik dan dipasarkan
oleh perusahaan farmasi dibawah nama merek yang popular dan
terkenal dalam perdagangan (Rohilla et al., 2011). Contoh nama
dagang amoksisilin antara lain amolin, amopenixin, amoxa,
amoxycillin, amoxypen, sumox, piramox, amoxil, amoxican (Badan
Pengawas Obat dan Makanan RI, 2014).
2.1.4 Farmakokinetik
Absorpsi dari amoksisilin tidak terganggu oleh makanan.
Amoksisilin berikatan dengan protein dalam plasma sekitar 20% dan
diekskresi dalam bentuk aktif didalam urin (Brunton et al., 2008;
Harvey et al., 2009).
Amoksisilin memiliki kegunaan klinik yang luas tidak hanya karena
sebagai antibakteri spektrum luas tetapi juga karena bioavailability
yang tinggi (70-90%) dengan kadar puncak pada plasma terjadi
dengan waktu 1–2 jam dan dosisnya tergantung, umumnya 1,5–3
kali lebih besar dibanding ampisillin setelah dosis oral. Amoksisilin
terdistribusi pada banyak jaringan termasuk hati, paru, prostat, otot,
empedu, asites, cairan pleura dan sinovial dan cairan okular,
terakumulasi dalam cairan amnion dan melewati plasenta tapi buruk
9
Amoksisilin memiliki oral availability 93%. Amoksisilin berikatan
dengan protein didalam plasma 18%. Amoksisilin diekskresikan
pada urine sekitar 86% dan pembersihannya 10,8 L/h/70kg.
Amoksisilin memiliki volume distribusi 19 L/70kg dan waktu paruh
1,7 jam (Katzung, 2006). Amoksisilin dapat melewati plasenta,
sedikit diekskresikan pada air susu ibu (ASI) dan sedikit melewati
cerebrospinal fluid (CSF) (Adesanoye et al., 2014).
Amoksisilin generik memiliki waktu paruh absorbsi 2,25 jam, laju
absorbsi (Ka) 0,308/jam, waktu paruh eliminasi 3,25 jam, laju
eliminasi (K) 0,185/jam, intersep 580 mg/jam, bioavailabilitas per
oral 93%, dan laju ekskresi 0,498/jam. Amoksisilin generik
bermerek memiliki waktu paruh absorbs 1,75 jam, laju absorbsi (Ka)
0,396/jam, waktu paruh eliminasi 5 jam, laju eliminasi (K)
0,139/jam, intersep 320 mg/jam, bioavalabilitas amoksisilin per oral
93% dan laju ekskresi amoksisilin 0,477/jam. Perbedaan dalam
farmokinetik antara obat generik dan generik bermerek dapat
mempengaruhi efikasi dan keamanan pada resipien obat (Wahyudin
et al., 2010).
Hasil penelitian menunjukan dua amoksisilin generik memiliki area
under curve 50,2 dan 51,9 hmg/l, konsentrasi plasma maksimal 14,1
dan 15,7 mg/l dan waktu untuk konsentrasi maksimal 2,08 dan 1,96
curve 54,9 hmg/l, konsentrasi plasma maksimal 16,1 mg/l dan waktu
untuk konsentrasi maksimal 2,04 jam (Tacca et al., 2009).
2.1.5 Farmakodinamik
Amoksisilin adalah bakterisidal yang rentan terhadap organisme
melalui penghambatan biosintesis dinding sel mukopeptida selama
tahap penggandaan bakteri (Imoisili, 2008). Amoksisilin lebih
efektif melawan mikroorganisme gram positif dibanding gram
negatif, dan mendemonstrasikan efikasi lebih baik dibanding
penisillin, penisillin V dan dibanding antibiotik lain dalam
pengobatan penyakit atau infeksi yang beragam (Kaur et al., 2011).
Amoksisilin bekerja dengan mengikat pada ikatan penisilin protein
1A (PBP-1A) yang berlokasi didalam dinding sel bakteri. Penisillin
(amoksisilin) mengasilasi penisilin-mensensitifkan transpeptidase
C-terminal domain dengan membuka cincin laktam menyebabkan
inaktivasi enzim, dan mencegah pembentukan hubungan silang dari
dua untai peptidoglikan linier, menghambat fase tiga dan terakhir
dari sintesis dinding sel bakteri, yang berguna untuk divisi sel dan
bentuk sel dan proses esensial lain dan lebih mematikan dari
penisillin untuk bakteri yang melibatkan mekanisme keduanya litik
11
2.1.6 Toksikologi
Amoksisilin menunjukan efek samping sebagai reaksi
hipersensitivitas seperti urtikaria, demam nyeri sendi, diare, syok
anafilaksis, ruam eritematosus, leukemia limfatik kronik, dan iritasi
gastrointestinal (Adesanoye et al., 2014). Studi farmacovigilance
dilakukan untuk mendokumentasikkan efek samping obat dalam
program WHO untuk International Drug Monitoring (IDM) dari
Januari 1988 sampai Juni 2005, database Pharmacovigilance
Inter-regional Group (GIF) mengumpulkan 37,906 laporan, yang 1095
terkait dengan amoksisilin. Persentase reaksi efek samping pada
kulit 82%, gastrointestinal 13%, hepatik 4%, dan hematologi 2%
(Kaur et al., 2011).
Beberapa dosis amoksisilin yang umum digunakan untuk per oral
yaitu 0,25–0,5 g tid untuk dosis dewasa, dan 20–40 mg/kg/hari
dalam tiga dosis untuk dosis anak (Katzung, 2006). Amoksisilin
memiliki toksisitas akut pada tikus, lethal dose oral pada referensi
Beecham Research Laboratories untuk tikus jantan lebih besar dari
5000mg/kgBB, lethal dose oral pada referensi Hardy, Palmer dan
Cozens untuk tikus jantan lebih besar dari 5500 mg/kgBB atau untuk
2.2Hati
2.2.1 Fisiologi Hati
Hati merupakan organ yang sangat penting bagi kehidupan karena
melakukan berperan dalam penyusunan biokimia yang luas dan
fungsi metabolik, termasuk membersihkan tubuh dari zat yang
merugikan jika dibiarkan menumpuk dan mengeluarkan metabolit
obat. Hati merupakan tempat pertama bagi sebagian besar nutrisi
yang diserap oleh dinding usus, pasokan sebagian besar protein
plasma dan mensintesis empedu yang optimal dalam penyerapan
lemak serta untuk mengekskresikan cairan Hati memiliki peran
dalam inaktivasi variasi substansi meliputi racun, steroid dan
hormon lainnya, dan sintesis protein (Barrett et al., 2010).
Hati memiliki peran penting dalam menentukan toksisitas obat
karena berperan dalam metabolisme, transportasi, dan pembersihan
zat asing. Metabolisme obat dapat digambarkan melalui dua fase
yaitu tahap I bioaktivasi/toksifikasi, dan tahap II reaksi detoksifikasi.
Pada reaksi fase I, biotransformasi dari obat induk melibatkan
penambahan dari hidroksi, karboksi, amino atau kelompok thiol
fungsional yang diperlukan untuk menyelesaikan fase berikutnya
dari detoksifikasi dan yang membuat senyawa lebih hidrofilik.
Reaksi Fase II melibatkan konjugasi dengan substansi kecil
13
memungkinkan metabolit akan diekspor ke sirkulasi sinusoidal
untuk pembersihan, atau ke empedu (Corsini dan Bortolini, 2013).
2.2.2 Hepatotoksisitas
Drug-induced liver injury (DILI) didefinisikan sebagai cedera hati
dikarenakan oleh berbagai obat, jamu atau xenobiotika lainnya, yang
menyebabkan kelainan dalam pemeriksaan hati atau disfungsi hati
dengan alasan eksklusi dari etiologi lain. DILI adalah salah satu dari
penyebab utama gagal hati akut di Amerika Serikat, terhitung sekitar
13% dari kasus akut gagal hati. Antimikroba dan agen untuk sistem
saraf pusat adalah penyebab paling umum dari DILI dan kesehatan
makanan atau suplemen makanan terhitung sekitar 7% dari kasus
DILI di Amerika Serikat (Suk dan Kim, 2012).
Obat yang metabolismenya didominasi di hati lebih sering dikaitkan
dengan peristiwa merugikan bagi hati dibandingkan dengan obat
yang tidak mengalami metabolisme signifikan di hati (Fisher et al.,
2015). Metabolisme dari xenobiotika seperti obat dapat mengarah
pada biotransformasinya menjadi substansi reaktif yang mencederai
sel dan kadar seluler. Obat dan xenobiotik juga dapat memberikan
peningkatan radikal bebas dan spesies reaktif yang berimplikasi
Tanda klinis hepatotoksisitas dapat terprediksi atau tidak terprediksi.
Reaksi terprediksi biasanya terkait dosis dan terjadi pada
kebanyakan orang yang terpapar setelah beberapa rentang untuk
toksisitas telah tercapai. Reaksi hepatotoksisitas tidak terprediski
terjadi tanpa tanda, tidak terkait dengan dosis, dan memiliki variasi
periode laten, rentang dari beberapa hari sampai 12 bulan. Banyak
obat membuat pola cedera yang memiliki karakteristik biokimia,
klinis, histologis, dan ciri kronologi atau kombinasinya (Navarro
dan Senior, 2006).
Tiga kelas antibakterisidal seperti quinolon, aminoglikosida, dan
beta-laktam menginduksi produksi Reactive Oxygen spesies (ROS)
pada sel mamalia, menyebabkan kerusakan DNA, protein dan lipid.
Antibiotik bakterisidal menghambat kompleks electron transport
chain (ETC) mitokondria, yang mengidentifikasikan sebagai sumber
major dari bentuk ROS. Gangguan pada ETC menyebabkan
penurunan membran potensial mitokondria, kadar adenosin trifosfat
(ATP), dan aktivitas metabolik rerata. Hal tersebut dapat
menyebabkan antibiotik bakterisidal menginduksi disfungsi
15
2.3Oksidan dan Antioksidan 2.3.1 Stres Oksidatif
Stres oksidatif adalah ketidakseimbangan antara oksidan dan
antioksidan yang berpotensi menyebabkan kerusakan sel (Birben et
al., 2012; Sies, 1997). Reactive Oxygen Species (ROS) memiliki
peran penting dalam patogenesis banyak penyakit, khususnya dalam
penyakit neurologik karena sistem saraf dan otak rentan terhadap
stres oksidatif (Nazıroğlu, 2012).
Peningkatan stres oksidatif meningkatkan ROS yang akan
meningkatkankan proses fosforilasi (Sukohar dan Muhartono,
2015). Ketika stres oksidasi terjadi, sel mencoba melawan efek
oksidan dan mengembalikan keseimbangan redoks dengan aktivasi
atau inaktivasi gen penyandi enzim pertahanan, faktor transkripsi
dan protein struktura. Stres oksidatif berkontribusi pada banyak
kondisi patologi termasuk kanker, gangguan neurologi,
aterosklerosis, hipertensi, iskemia, diabetes, sindrom distres
pernafasan akut, fibrosis pulmonary idiopatik, penyakit pulmonary
obstruktif kronik, dan asma (Birben et al., 2012).
Reactive Oxygen spesies dapat menyebabkan modifikasi DNA
dalam beberapa cara, yang melibatkan degradasi basa, pemutusan
DNA untai ganda atau tunggal, modifikasi, mutasi, delesi purin,
Sebagian besar modifikasi DNA ini sangat relevan dengan
karsinogen, aging, neurodegenerative, kardiovaskular, dan penyakit
autoimun (Birben et al., 2012).
2.3.2 Oksidan
Oksidan adalah bentuk produk normal dari metabolisme aerobik tapi
diproduksi pada kadar tinggi dibawah kondisi patofisiologi. Oksidan
dapat berasal dari endogen berasal dari ROS dan eksogen berasal
dari oksidan. Sumber endogen dari ROS dapat dibagi menjadi dua
kelompok yaitu radikal bebas dan non radikal. Sumber eksogen
oksidan dapat berasal dari asap rokok, paparan ozon, dan hiperoksia
(Birben et al., 2012; Sies, 1997).
Reactive Oxygen spesies diproduksi dari molekul oksigen sebagai
hasil metabolisme sel normal. Reactive Oxygen spesies pada
konsentrasi rendah atau sedang, memiliki proses fungsi sel fisiologi,
tapi pada konsentrasi tinggi, memproduksi modifikasi terbalik pada
komponen sel seperti lemak, protein dan DNA (Birben et al., 2012).
Obat dapat menginduksi stres oksidatif merupakan implikasi
mekanisme toksisitas dalam berbagai jaringan dan sistem organ
termasuk hati, ginjal, telinga, sistem kardiovaskular dan sistem
saraf. Mekanisme obat menginduksi stres oksidaktif dapat
17
yang dapat menurunkan oksigen molekuler secara langsung
meningkatkan ROS (Deavall et al., 2012).
Amoksisilin menyebabkan peningkatan cepat ROS pada 30 menit
selama terapi obat. Kadar ROS menurun secara signifikan saat 1
jam. Amoksisilin atau antibiotik lain yang biasanya dianggap tidak
genotoksik memiliki potensi untuk mencederai DNA genomik
kemungkinan melalui induksi intraseluler ROS (Li et al., 2007).
2.3.3 Antioksidan
Antioksidan adalah substansi yang ketika dalam konsentrasi rendah
dibandingkan dengan subtrat teroksidasinya, secara signifikan dapat
menghambat oksidasi dari substrat (Sies, 1997). Antioksidan dapat
dibagi menjadi dua kategori yaitu enzimatik, dan nonenzimatik.
Antioksidan enzimatik utama adalah SODs, katalase, dan GSH-Px.
Antioksidan non enzimatik termasuk komponen dengan berat
molekuler rendah seperti vitamin (vitamin C dan E), B-carotene,
asam urat, dan GSH (Birben et al., 2012).
Katalase adalah salah satu enzimatik antioksidan utama (Murray dan
Davis, 2009). Katalase adalah antioksidan enzimatik yang umum
ditemukan pada hampir semua organisme hidup yang terpapar
oksigen (Nazıroğlu, 2012). Katalase memiliki aktivitas peroksidase,
donor elektron dan molekul lain dari H2O2 sebagai oksidan atau
penerima elektron. Katalase dapat ditemukan dalam darah, sumsum
tulang, membran mukosa, ginjal dan hati (Murray dan Davis, 2009).
Katalase menggunakan H2O2 untuk mengoksidasi toksin termasuk
fenol, asam formik, formaldehid, dan alkohol. Katalase mungkin
berperan dalam bagian dengan menekan stres oksidasi mengaktivasi
aktivitas saluran potensial reseptor transien (TRP), sehingga
berpotensi menekan remodelling seluler yang tidak diinginkan
(Nazıroğlu, 2012).
Katalase dapat dihambat oleh ROS seperti anion superoksida yang
mengkonversi menjadi keadaan ferro dan feri yang merupakan
bentuk inaktivasi dari enzim. Katalase yang menerima H2O2
umumnya dapat didetoksifikasi oleh katalase yang menghapusnya
ketika pada konsentrasi tinggi (Olayinke, 2012). Peningkatan
aktivitas katalase hepatik dapat dijelaskan sebagai respon dari hati
terhadap tingginya kadar H2O2 (Łukaszewicz-Hussain dan
19
2.4Hewan Coba
Adapun taksonomi hewan coba yang akan digunakan adalah sebagai berikut
(Suckow et al., 2006):
Kingdom : Animalia
Filum : Chordata
Kelas : Mamalia
Bangsa : Rodentia
Suku : Muridae
Marga : Ratus
Jenis : Rattus norvegicus
Rattus norvegicus dan Mus musculus adalah yang paling sering digunakan
sebagai hewan eksperimen dalam banyak bidang penelitian medis dan
biologis (Suckow et al., 2006). Tikus menghindari daerah terbuka, dan
menggunakan urin sebagai penanda teritorinya. Indera penciuman dan
pendengarannya cepat berkembang dan sensitive pada ultrasound.
Penglihatan siang hari buruk, tapi penglihatan cahaya redup lebih efektif
pada beberapa galur pigmen tertentu. Tikus albino (putih) menghindari
daerah dengan kadar cahaya lebih dari 25 lux. Aktivitas tikus putih lebih
hebat pada waktu gelap (Aller dan Arias, 2009).
Hati pada tikus terdiri dari lobus kiri, lobus kanan dan lobus kaudatus. Lobus
kiri dibagi menjadi lobus lateral kiri dan lobus medial kiri, lobus kanan
kaudatus dibagi menjadi prosesus papilaris, prosesus papilaris anterior dan
prosesus kaudatus (Thoolen et al., 2010). Vena porta dibentuk oleh
pertemuan antara mesentrika superior dan vena splenikus. Hati tikus
diperdarahi oleh dua arteri yaitu arteri hepatik proria, dan arteri hepatik
sinistra (Aller dan Arias, 2009).
Hati memiliki dua perdarahan yaitu vena porta dan arteri hepatik. Hal yang
mendeskripsikan untuk unit struktural yaitu lobulus hepatik, dan unit
fungsional yaitu asinus hepatik. Selain hepatosit, hati memiliki berbagai tipe
sel termasuk sel biliaris, sel endotel, sel kuppfer, sel stellate, sel penyimpan
lemak dan sel pit selain sel hematopoetik dalam sinusoid dan pembuluh
darah (Thoolen et al., 2010).
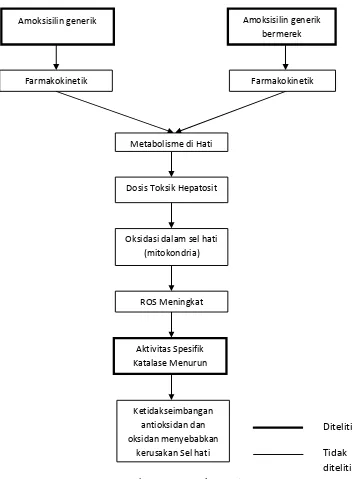
2.5Kerangka Teori
Obat generik merupakan salinan (dari obat yang disetujui, inovator/ produk
dagang) yang sama dengan obat dagang, dalam dosis, keselamatan,
kekuatan, absorpsi, kualitas, performa, dan tujuan penggunaan. Ada banyak
kesalahpahaman tentang kualitas, efektivitas, durasi tindakan, dan khasiat
mengenai produk obat generik.
Obat generik bermerek dasarnya produk obat generik dan dipasarkan oleh
perusahaan farmasi dibawah nama merek yang popular dan terkenal dalam
perdagangan. Pada penelitian sebelumnya terdapat perbedaan
21
farmokinetik antara obat generik dan branded dapat mempengaruhi efikasi
dan keamanan pada resipien obat.
Obat yang metabolismenya didominasi di hati lebih sering dikaitkan dengan
peristiwa merugikan bagi hati dibanding obat yang tidak mengalami
metabolisme signifikan di hati. Obat dan xenobiotik juga dapat memberikan
peningkatan generasi dari radikal bebas dan spesies reaktif yang
berimplikasi pada banyak kondisi dan penyakit patologi.
Obat menginduksi stres oksidatif merupakan implikasi sebagai mekanisme
dari toksisitas dalam berbagai jaringan dan sistem organ termasuk hati,
ginjal, telinga, dan sistem kardiovaskular dan saraf. Reactive Oxygen spesies
dapat menyebabkan modifikasi DNA dalam beberapa cara, yang melibatkan
degradasi basa, pemutusan DNA untai ganda atau tunggal, modifikasi,
mutasi, delesi purin, pirimidin, atau ikatan gula, dan penyilangan dengan
protein.
Amoksisilin menyebabkan peningkatan cepat ROS pada 30 menit selama
terapi obat. Kadar ROS menurun secara signifikan saat 1 jam. Amoksisilin
atau antibiotik lain yang biasanya dianggap tidak genotoksik memiliki
potensi untuk mencederai DNA genomik kemungkinan melalui induksi
Katalase dapat ditemukan dalam darah, sumsum tulang, membran mukosa,
ginjal dan hati. Katalase diketahui menjadi dihambat oleh ROS seperti anion
superoksida yang mengkonversi menjadi keadaan ferro dan feri yang bentuk
inaktivasi dari enzim. Katalase yang menerima H2O2 umumnya dapat
didetoksifikasi oleh katalase yang menghapusnya ketika pada konsentrasi
23
Gambar 1. Kerangka teori.
Farmakokinetik
Amoksisilin generik Amoksisilin generik
bermerek
Farmakokinetik
Metabolisme di Hati
Dosis Toksik Hepatosit
Oksidasi dalam sel hati (mitokondria)
ROS Meningkat
Aktivitas Spesifik
Katalase Menurun
Ketidakseimbangan antioksidan dan oksidan menyebabkan
kerusakan Sel hati
Diteliti
Tidak
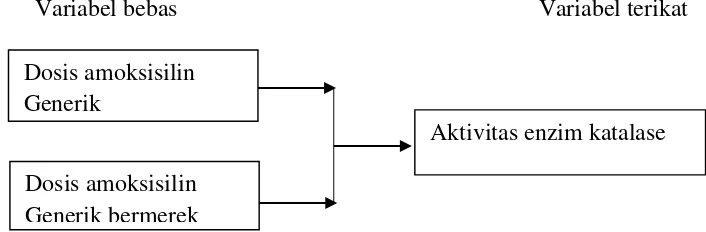
2.6Kerangka Konsep
Kerangka Konsep Penelitian
Variabel bebas Variabel terikat
Gambar 2. Bagan hubungan antar variabel.
2.7Hipotesis (H1) :
2.7.1 Terdapat perbedaan efek pemberian dosis toksik antara amoksisilin
generik berlogo dengan amoksisilin generik bermerek terhadap
aktivitas enzim katalase pada hati tikus
2.7.2 Obat yang memberikan efek toksik maksimum ditinjau dari aktivitas
enzim katalase adalah amoksisilin generik bermerek.
2.7.3 Obat yang memberikan efek toksik minimum ditinjau dari aktivitas
enzim katalase adalah amoksisilin generik berlogo. Dosis amoksisilin
Generik
Aktivitas enzim katalase
BAB III
METODOLOGI PENELITIAN
3.1Desain Penelitian
Penelitian ini merupakan penelitian eksperimental dengan rancangan Post
Test Only Control Group Design. Pengambilan data hanya dilakukan pada
akhir penelitian setelah dilakukan perlakuan dengan membandingkan hasil
kelompok yang diberikan perlakuan dengan kelompok yang tidak diberikan
perlakuan (kontrol).
3.2Tempat dan Waktu Penelitian
Penelitian ini akan dilaksanakan pada laboratorium Biokimia dan Biologi
Molekuler Fakultas Kedokteran Universitas Lampung. Penelitian
dilaksanakan selama bulan September-Desember 2015.
3.3Populasi dan Sampel Penelitian 3.3.1 Populasi
Populasi pada penelitian ini adalah tikus (Rattus novergicus) galur
Sprague Dawley berusia 6-7 minggu dengan berat antara 100-200
gram. Sampel adalah jaringan hati tikus populasi yang telah
3.3.1.1Kriteria Inklusi
a) Tikus putih jantan galur Sprague dawley.
b) Sehat dan tidak memiliki kelainan anatomis (cacat).
c) Berusia 6-7 minggu.
d) Memiliki berat 100-200 gram.
3.3.1.2Kriteria Eksklusi
a) Tikus sakit sebelum dilakukan penelitian.
b) Tikus mati sebelum dilakukan penelitian.
3.3.1.3Kriteria Drop Out
a) Tikus mati selama diberikan perlakuan.
b) Tikus tampak sakit selama diberikan perlakuan.
3.3.2 Besar Sampel
Pada uji eksperimental rancangan acak lengkap, besar sampel
penelitian yang digunakan ditentukan dengan menggunakan rumus
Federer yaitu (t) (n-1) ≥ 15, (t) adalah jumlah kelompok perlakuan,
(n) jumlah ulangan pada masing-masing kelompok
(t) (n-1) ≥ 15
(9) (n-1) ≥ 15
9n - 9 ≥ 15
9n ≥ 24
27
Berdasarkan perhitungan tersebut, dibutuhkan jumlah sampel
minimal sebanyak 3 ekor tikus untuk tiap kelompok. Untuk
menghindari dropout, ditambahkan 1 ekor tikus tiap kelompok
sehingga jumlah sampel adalah 4 ekor tiap kelompok.
Dalam penelitian ini digunakan 36 tikus yang terbagi dalam 9
kelompok (masing masing kelompok terdiri dari 4 ekor) yaitu :
a. Kelompok kontrol negatif (kelompok PKN) adalah kelompok
tikus dengan pemberian aquades 1 ml setiap hari selama 14 hari
dengan frekuensi 3 kali per hari diberikan secara per oral
menggunakan sonde lambung.
b. Kelompok kontrol positif A (kelompok PKA) adalah kelompok
tikus dengan pemberian amoksisilin generik A dengan dosis
yaitu 10 mg/kg BB dalam 1 ml dengan aquades selama 14 hari
dengan frekuensi 3 kali per hari diberikan secara per oral
menggunakan sonde lambung (Adesanoye et al., 2014).
c. Kelompok kontrol positif B (kelompok PKB) adalah kelompok
tikus dengan pemberian amoksisilin generik bermerek B dengan
dosis 10 mg/kg BB dalam 1 ml dengan aquades selama 14 hari
dengan frekuensi 3 kali per hari diberikan secara per oral
menggunakan sonde lambung (Adesanoye et al., 2014).
d. Kelompok perlakuan PA1 (obat A) adalah kelompok tikus
dengan pemberian amoksisilin generik dosis 102,8 mg/kg BB
kali per hari diberikan secara per oral menggunakan sonde
lambung.
e. Kelompok perlakuan PA2 (obat A) adalah kelompok tikus
dengan pemberian amoksisilin generik dosis 205,6 mg/kg BB
dalam 1 ml dengan aquades selama 14 hari dengan frekuensi 3
kali per hari diberikan secara per oral menggunakan sonde
lambung.
f. Kelompok perlakuan PA3 (obat A) adalah kelompok tikus
dengan pemberian amoksisilin generik dosis 411,2 mg/kg BB
dalam 1 ml dengan aquades selama 14 hari dengan dengan
frekuensi 3 kali per hari diberikan secara per oral menggunakan
sonde lambung.
g. Kelompok perlakuan PB1 (obat B) adalah kelompok tikus
dengan pemberian amoksisilin generik bermerek dosis 102,8
mg/kg BB dalam 1 ml dengan aquades selama 14 hari dengan
dengan frekuensi 3 kali per hari diberikan secara per oral
menggunakan sonde lambung.
h. Kelompok perlakuan PB2 (obat B) adalah kelompok tikus
dengan pemberian amoksisilin generik bermerek dosis 205,6
mg/kg BB dalam 1 ml dengan aquades selama 14 hari dengan
dengan frekuensi 3 kali per hari diberikan secara per oral
menggunakan sonde lambung.
i. Kelompok perlakuan PB3 (obat B) adalah kelompok tikus
29
mg/kg BB dalam 1 ml dengan aquades selama 14 hari dengan
dengan frekuensi 3 kali per hari diberikan secara per oral
menggunakan sonde lambung.
3.4Alat dan Bahan Penelitian 3.4.1 Alat Penelitian
Peralatan yang digunakan adalah sonde lambung, neraca analitik,
mikropipet volume 0.5-10μL, 10-100 μL, 100-1000 μL, mikrotube
1.5 mL dan 2 mL, micropestle, freezer -80oC, spektrofotometer UV
dengan panjang gelombang 210 nm, vortex, alat sentrifugasi, kuvet
kaca, alumunium foil, sarung tangan karet, alat tulis, dan alat
laboratorium lain seperti gelas kimia, pipet, pinset, sendok, labu
ukur, batang pengaduk, alat bedah minor, dan tabung reaksi.
3.4.2 Bahan Penelitian
Bahan yang digunakan adalah Organ hati tikus yang diberikan
perlakuan, H2O2 30%, PBS 0.05 pH 7, PBS 0.1 pH 7.4, bovine serum
albumin (BSA), aquadest, amoksisilin generik bermerek, dan
amoksisilin generik.
3.5Indentifikasi Variabel dan Definisi Operasional 3.5.1 Variabel Penelitian
Variabel bebas : dosis amoksisilin generik berlogo dan bermerek.
3.5.2 Definisi Operasional Variabel Tabel 1. Definisi operasional variabel
Variabel Definisi Skala
Dosis toksik amoksisilin generik berlogo
Ada 3 kelompok dengan pemberian dosis amoksisilin generik berlogo yang menyebabkan stres oksidatif pada jaringan hati tikus, yaitu ;
1. Kelompok kontrol A (PKA) adalah kelompok tikus yang diberikan amoksisilin generik A selama 14 hari dengan frekuensi 3 kali per hari dengan dosis 10 mg/kg BB dalam 1 ml aquades tikus diberikan secara per oral menggunakan sonde lambung (Adesanoye et al., 2014). 2. Kelompok perlakuan A-1 (PA1) adalah kelompok tikus
yang diberikan amoksisilin generik A selama 14 hari dengan frekuensi 3 kali per hari dengan dosis 102,8 mg/kg BB dalam 1 ml aquades tikus diberikan secara per oral menggunakan sonde lambung.
3. Kelompok perlakuan A-2 (PA2) adalah kelompok tikus yang diberikan amoksisilin generik A selama 14 hari dengan frekuensi 3 kali per hari dengan dosis 205,6 mg/kg BB dalam 1 ml aquades tikus diberikan secara per oral menggunakan sonde lambung.
4. Kelompok perlakuan A-3 (PA3) adalah kelompok tikus yang diberikan amoksisilin generik A selama 14 hari dengan frekuensi 3 kali per hari dengan dosis 411,2 mg/kg BB dalam 1 ml aquades tikus diberikan secara per oral menggunakan sonde lambung.
Ada 3 kelompok dengan pemberian dosis amoksisilin generik bermerek yang menyebabkan stres oksiatif pada jaringan hati tikus yaitu :
1. Kelompok kontrol B (PKB) adalah kelompok tikus yang diberikan amoksisilin generik B selama 14 hari dengan frekuensi 3 kali per hari dengan dosis 10 mg/kg BB dalam 1 ml aquades tikus diberikan secara per oral menggunakan sonde lambung (Adesanoye et al., 2014). 2. Kelompok perlakuan B-1 (PB1) adalah kelompok tikus
yang diberikan amoksisilin generik bermerek B selama 14 hari dengan frekuensi 3 kali per hari dengan dosis 102,8 mg/kg BB dalam 1 ml aquades tikus diberikan secara per oral menggunakan sonde lambung.
3. Kelompok perlakuan B-2 (PB2) adalah kelompok tikus yang diberikan amoksisilin generik bermerek B selama 14 hari dengan frekuensi 3 kali per hari dengan dosis 205,6 mg/kg BB dalam 1 ml aquades tikus diberikan secara per oral menggunakan sonde lambung.
4. Kelompok perlakuan B-3 (PB3) adalah kelompok tikus yang diberikan amoksisilin generik bermerek B selama 14 hari dengan frekuensi 3 kali per hari dengan dosis 411,2 mg/kg BB dalam 1 ml aquades tikus diberikan secara per oral menggunakan sonde lambung.
Numerik
Aktivitas enzim katalase
Katalase adalah antioksidan enzimatik umum. Katalasa salah satu enzim yang dapat ditemukan di hati terutama pada peroksisom. Aktivitas spesifik katalase dihitung berdasarkan penguraian H2O2
dan O2 pada panjang gelombang 210 nm. Dekomposisi H2O2
diamati secara spektofotometri, dan pengukuran dilakukan pada pH 7,0 (Susantiningsih, 2015. Peningkatan aktivitas katalase hepatik dapat dijelaskan sebagai respon dari hati terhadap tingginya kadar ROS (Łukaszewicz-Hussain dan Moniuszko-Jakoniuk, 2004)
31
3.6Cara Kerja
Penelitian diawali dengan uji pendahuluan untuk melihat apakah dosis
maksimum dapat digunakan sebagai dosis toksik. Jika dosis maksimum
menunjukan kerusakan yang bermakna, maka penelitian dilanjutkan dengan
menggunakan prinsip ½–1–2 kali dosis toksik dengan populasi tikus yang
sama dengan pengulangan sesuai rumus frederer. Jika tidak terdapat
kerusakan yang bermakna, maka 2 kali dosis maksimum akan dibuat
menjadi 3 variasi kembali menggunakan prinsip ½–1–2 kali dosis toksik
dengan pengulangan sesuai dengan rumus frederer dengan mengikuti
prosedur dibawah ini (Arome dan Chinedu, 2014).
3.6.1 Aklimatisasi Hewan Coba
Tikus percobaan diadaptasikan selama satu minggu. Kemudian
dilakukan penyeragaman cara hidup dan makanan sebelum
dilakukan percobaan. Tikus diberi makanan makanan dan minuman
secara ad libitum. Tikus ditempatkan dalam kandang plastik dengan
tutup terbuat dari kawat ram dan dialasi sekam. Lingkungan kandang
dibuat agar tidak lembab, dan suhu kandang dijaga sekitar 250C
sesuai dengan suhu ruangan. Masing-masing kelompok tikus
diletakkan dalam kandang tersendiri dan dijaga sedemikian rupa
sehingga tidak saling berinteraksi. Kesehatan tikus dipantau setiap
hari dan berat badan tikus ditimbang setiap minggu sampai tikus
3.6.2 Perhitungan Dosis
Pada penelitian ini, penulis menggunakan 2 jenis obat amoksisilin
yaitu tipe generik dan generik bermerek yang dipilih secara acak dan
terdapat di apotek di Bandar Lampung. Dosis amoksisilin yang
digunakan merupakan dosis maksimum untuk manusia yaitu 1000
mg yang dikonversikan menjadi dosis toksik tikus menggunakan
rumus BSA (Body Suraface Area) yang terangkum pada rumus
dibawah ini (Reagan-Shaw et al., 2008).
HED (mgKg) = dosishewancoba ��hewancoba
��manusia
HED ( Human Equivalent Dose) merupakan dosis yang digunakan
pada manusia. Satuan yang digunakan dalam HED berupa mg/kg BB
(Reagan-Shaw et al., 2008). Berat badan yang digunakan sebagai
pembagi merupakan rerata berat badan manusia yang digunakan
dalam konversi HED, yaitu 60 Kg. Sehingga jumlah HED
amoksisilin sebesar :
HED (mg/kg) = dosis obat / berat badan
HED (mg/kg) = 1000 mg / 60 kg
HED (mg/kg) = 16,67 mg/kg
HED yang didapat dikonversikan ke dosis hewan coba
menggunakan rumus BSA. Pada rumus BSA, Km berperan sebagai
konstanta (Reagan-Shaw et al., 2008). Km untuk manusia dewasa
normal sebesar 37 dan Km untuk hewan coba (tikus) sebesar 6.
33
HED (mg/kg) = dosis hewan x (Km hewan coba/ Km manusia)
16,67 mg/kg = dosis hewan coba x 6/37
Dosis hewan coba = 37 x 16,67 mg/kg
Dosis hewan coba = 102,79 mg/kg
Dosis yang digunakan dalam penelitian ini sebesar 102,79 mg/kg
dan dibulatkan menjadi 102,8 mg/kg BB. Dosis tikus dibuat menjadi
3 variasi dosis menggunakan prinsip ½-1-2 kali dosis tersebut
sehingga didapatkan dosis yaitu 51,4 mg/kg BB, 102,8 mg/kg BB
dan 205,6 mg/kg BB.
3.6.3 Perlakuan Induksi dengan Amoksisilin
Setelah 1 minggu aklimatisasi hewan coba atau tikus putih. Tikus
diberikan perlakuan dengan amoksisilin sesuai variasi dosis
kelompoknya baik amoksisilin generik berlogo maupun generik
bermerek dengan dosis 102,8 mg/kgBB tikus, 205,6 mg/kgBB tikus
dan 411,2 mg/kgBB tikus, masing masing dalam 1 ml dengan
aquades dengan frekuensi 3 kali per hari selama 14 hari pada
kelompok perlakuan. Masing-masing kelompok diberikan
amoksisilin secara per oral menggunakan sonde lambung. Hal
3.6.4 Terminasi dan Penyimpanan
Setelah perlakuan induksi pada setiap kelompok selama 14 hari,
tikus diterminasi dengan anastesi menggunakan ketamine:xylazine
dosis 75-100mg/kg : 5-10 mg/kg (perbandingan 10:1) secara Intra
peritoneal, kemudian di euthanasia dengan metode cervical
dislocation dan dilakukan laparotomi untuk mengambil organ hati
(Leary et al., 2013).
Berat hati masing-masing tikus ditimbang dan dicatat. Hati
ditempatkan ke dalam wadah steril pada suhu -4ºC dan disimpan di
dalam freezer (80ºC) sampai dilakukan pembuatan homogenat.
(Susantiningsih, 2015).
3.6.5 Pembuatan Homogenat Sampel
Sampel jaringan hati diambil dari upright freezer lalu dimasukkan
ke dalam lemari es dengan suhu -4oC selama 1 hari. Sampel jaringan
yang telah diambil kemudian dipotong dan ditimbang sebanyak 100
mg. Homogenat dibuat dengan menambahkan PBS 0,1 M dengan
PH 7.4 sebanyak 0,5 mL pada sampel dengan perbandingan
sampel:PBS = 1:1 secara bertahap sambil terus dihaluskan
menggunakan vortex dan micropleste. Homogenat kemudian
disentrifugasi dengan kecepatan 5.000 rpm pada suhu 4oC selama 10
35
ke testube kosong dan simpan pada suhu -20OC (Susantiningsih,
2015).
3.6.6 Penentuan Kinetik Katalase
Dilakukan pengukuran absorbansi H2O2 oleh blanko dan sample
setiap menit selama 2 menit. Pengukuran absorbansi blanko
dilakukan dengan memasukan 950 μl larutan H2O2 ke dalam kuvet
dengan pengenceran optimal adalah 1:4000 (Febrianti, 2009).
Kemudian ditambahkan dengan 50 μl PBS 0.05 M dengan pH 7, lalu
dilakukan homogenisasi dengan pengocokkan manual dan diukur
serapannya pada panjang gelombang 210 nm. Pada pengukuran
absorbansi sampel, 50 μL sampel ditambahkan pada 950 μL H2O2
dengan pengenceran 1:4000, untuk selanjutnya dilakukan prosedur
serupa dengan pengukuran blanko. Selanjutnya penguraian H2O2,
baik oleh blanko maupun sampel didapat dengan cara mengurangkan
absorbansi di awal (t1) dengan absorbansi pada menit-menit
selanjutnya (menit ke-x, tx). Selisih penguraian oleh sampel
dikurangkan dengan selisih penguraian H2O2 oleh blanko, kemudian
dihitung kecepatan reaksi setiap menit sehingga didapatkan waktu
terbaik penguraian H2O2 oleh sampel. Kemudian hasil pengamatan
dicatat (Susantiningsih, 2015).
Seluruh sampe diukur dengan prinsip triplet (tiga kali pengukuran
3.6.7 Penentuan Kurva Standar Protein
Untuk menentukan kurva standar protein, 50 mg BSA ditimbang
kemudian dilarutkan dengan aquadest dengan perbandingan 1:1.
Kemudian larutan BSA diencerkan dengan perbandingan 0,1, 0,2,
0,4, 0,6, dan 0,8 dan diukur serapannya pada panjang gelombang 280
nm. Hasil aktivitas spesifik pengukuran dicatat dalam tabel dan
dibuat kurvanya. Dari kurva tersebut dicari rumus untuk menghitung
konsentrasi protein jaringan.
3.6.8 Penentuan Konsentrasi Protein Hati
Untuk menentukan konsentrasi protein pada hati, dilakukan
pengukuran absorbansi homogenat yang telah diencerkan dengan
PBS pada pengenceran optimal pada 1:100 (Putri, 2009). Dengan
panjang gelombang 210 nm. Hasil pengukuran dicatat dalam tabel.
Konsentrasi protein (mg/ml) hati kemudian dihitung dengan
menggunakan rumus yang didapat dari kurva standar protein. Hasil
pengukuran dan penghitungan dicatat dalam bentuk tabel.
3.6.9 Penentuan Aktivitas Katalase
Katalase adalah antioksidan enzimatik yang mengkatalisis
dekomposisi H2O2 menjadi H2O dan molekul O2.
2 H2O2→H2O + O2
Dekomposisi H2O2 diamati secara spektrofotometri berdasarkan
37
Pengukuran aktivitas katalase dilakukan pada pH 7,0 karena suasana
yang terlalu asam atau basa dapat menyebabkan hilangnya aktivitas
katalase.
Perhitungan aktivitas katalase adalah sebagai berikut
(Susantiningsih, 2015):
Aktivitas Katalase (U/ml)=
((ΔAbsorbansi Uji-ΔAbsorbansi Blanko)/menit x faktor pengencer) / ((molaritas H2O2) x (volume sampel yang diukur))
Hasil perhitungan tersebut kemudian digunakan untuk menentukan
aktivitas spesifik katalase (U/mg). semua hasil dicatat dalam tabel.
Aktivitas spesifik katalase (U/mg) =
Aktivitas Katalase (U/mL) / Kadar Protein dalam Sampel (mg/mL)
3.7Pengolahan dan Analisis Data
Pengolahan dan analisis dengan membandingkan rerata aktivitas enzim
katalase antara kelompok. Analisis data yang digunakan adalah analisis
univariat dan analisis bivariat. Analisis univariat dilakukan untuk menilai
apakah data yang didapat memiliki distribusi normal atau tidak. Analisis
univariat yang digunakan adalah uji normalitas Shapiro-Wilk dikarenakan
jumlah sampel kurang dari 50. Analisis bivariat dilakukan menggunakan uji
parametrik One Way ANOVA apabila varians data berdistribusi normal dan
dilanjutkan dengan analisis non-parametrik uji Kruskal-Wallis. Jika pada uji
One Way ANOVA memberikan hasil p<0,05 (hipotesis dianggap bermakna)
maka akan dilakukan dengan analisis post-hoc LSD untuk menilai
kebermaknaan antar kelompok. Apabila pada uji Kruskal-Wallis
39
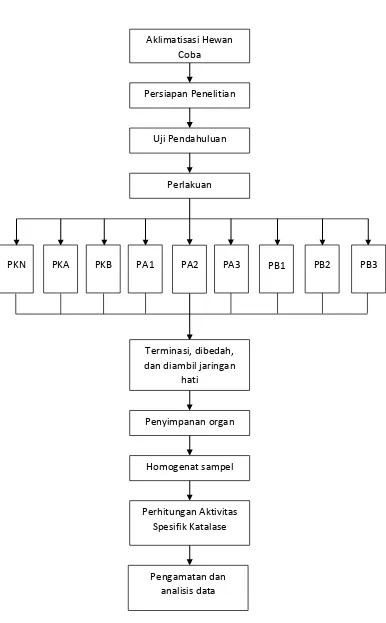
3.8Diagram Alir
Gambar 3. Diagram alir Aklimatisasi Hewan
Coba
Persiapan Penelitian
Uji Pendahuluan
Perlakuan
PKN PKA PKB PA1 PA2 PA3 PB1 PB2 PB3
Terminasi, dibedah, dan diambil jaringan
hati
Penyimpanan organ
Homogenat sampel
Perhitungan Aktivitas Spesifik Katalase
3.9Etika Penelitian
Ethical clearance untuk penelitian ini akan didapatkan dari Komisi Etika
Penelitian Kesehatan Fakultas Kedokteran Universitas Lampung dan akan
mengajukan ethical approval ke Komisi Etika Penelitian Kesehatan
Fakultas Kedokteran Universitas Lampung. Terminasi tikus dilakukan
setelah perlakuan terakhir. Tikus diterminasi dengan mengikuti prinsip 3R
yaitu replacement, reduction dan refinement, dan menggunakan prinsip 5F
yaitu freedom of hunger and thrist, freedom of discomfort, freedom of pain,
BAB V
SIMPULAN DAN SARAN
5.1. Simpulan
Berdasarkan hasil penelitian, dapat disimpulkan bahwa :
1. Terdapat perbedaan efek pemberian dosis toksik antara obat amoksisilin
generik berlogo dengan obat generik bermerek terhadap aktivitas enzim
katalase pada hati tikus putih (Rattus novergicus) galur Sprague dawley,
yang bermakna secara stastistik yaitu kelompok A1 dengan B1.
2. Obat yang memberikan efek toksik maksimum yaitu obat generik
bermerek dengan dosis 822,4 mg/kgBB, dengan hasil aktivitas katalase
spesifik yaitu 0,0014 U/mg.
3. Obat yang memberikan efek toksik minimum yaitu obat generik berlogo
dengan dosis 205,6 mg/kgBB, dengan hasil aktivitas katalase spesifik
yaitu 0,0024 U/mg.
5.2. Saran
Saran bagi peneliti lain adalah:
1. Perlu dilakukan penelitian lebih lanjut mengenai faktor-faktor yang
norvegicus yang diinduksi Amoksisilin generik berlogo dan
Amoksisilin generik bermerek.
2. Perlu dilakukan penelitian tentang dosis toksik pada amoksisilin.
3. Perlu dilakukan penelitian tentang perbandingan obat generik berlogo
DAFTAR PUSTAKA
Adesanoye OA, Ifezue AOC, & Farombi EO. 2014. Influence of Chloramphenicol and Amoxicillin on Rat Liver Microsomal Enzymes and Lipid Peroxidation.
African Journal of Biomedical Research, 17(March), 135–142.
Adnyana IK, Murtini S, Roni a, & Wardani IGK. 2013. Evaluation of antibacterial activity and determination amoxicillin concentration on generic and branded products. International Journal of Pharmacy and Pharmaceutical Sciences,
5(3), 1–5.
Aller M-A, & Arias J. 2009. Microsurgery in Liver Research. Madrid: Bentham Science.
Ameri MNAl, Nayuni N, Anil KKG, Perrett D, Tucker A, & Johnston A. 2012. The differences between the branded and generic medicines using solid dosage forms: In-vitro dissolution testing. Pharma Sciences, 2(1), 1–8.
Arome D, & Chinedu E. 2014. The importance of toxicity testing. Journal of Pharmaceutical and Biosciences, 4(2013), 146–148.
Badan Pengawas Obat dan Makanan RI. 2014. Amoksisilin (pp. 1–12).
Barrett KE, Barman SM, Boitano S, & Brooks HL. 2010. Ganong’s Review of
Medical Physiology (23rd ed.). New York: McGraw-Hill’s.
Bhaskar RK. 2015. Hepatotoxicity Induced By Antibiotics In Experimental Animals. Journal of Technological Advances and Scientific Research, 1(04), 283–292.
Birben E, Sahiner UM, Sackesen C, Erzurum S, & Kalayci O. 2012. Oxidative Stress and Antioxidant Defense. World Allergy Organization Journal.
Brunton L, Parker K, Blumenthal D, & Buxton L. 2008. Manual of Pharmacology and Therapeutics. New York: McGraw-Hill Companies.
Toxicological Sciences, (919), 1–47.
Corsini A, & Bortolini M. 2013. Drug-induced liver injury: The role of drug metabolism and transport. Journal of Clinical Pharmacology.
Deavall DG, Martin Ea, Horner JM, & Roberts R. 2012. Drug-induced oxidative stress and toxicity. Journal of Toxicology.
Del Tacca M, Pasqualetti G, Di Paolo A, Virdis A, Massimetti G, Gori G, et al. 2009. Lack of pharmacokinetic bioequivalence between generic and branded amoxicillin formulations. A post-marketing clinical study on healthy volunteers. British Journal of Clinical Pharmacology, 68(1), 34–42.
Del Tacca M, Pasqualetti G, Gori G, Pepe P, Di Paolo A, Lastella M, et al. 2013. Comparative pharmacokinetic and pharmacodynamic evaluation of branded and generic formulations of meloxicam in healthy male volunteers.
Therapeutics and Clinical Risk Management, 9, 303–311.
Dey P, Saha MR, & Sen A. 2013. An overview on drug-induced hepatotoxicity.
Asian Journal of Pharmaceutical and Clinical Research, 6(4), 1–4.
El-Sherbiny G, Taye A, & Abdel-Raheem I. 2009. Role of ursodeoxycholic acid in prevention of hepatotoxicity caused by amoxicillin-clavulanic acid in rats. Ann Hepatol, 134–140.
Febrianti S. 2009. Aktivitas Spesifik Katalase Jaringan Jantung Tikus Putih yang Diinduksi Hipoksia Akut Berulang [Skripsi]. Universitas Indonesia.
Fisher K, Vuppalanchi R, & Saxena R. 2015. Drug-Induced Liver Injury. Archives of Pathology & Laboratory Medicine, 139(7), 876–887.
Fontana RJ, Shakil AO, Greenson JK, Boyd I, & Lee WM. 2005. Acute Liver Failur Due To Amoxicillin and Amoxicillin/Clavulanate. Digestive Diseases and Sciences, 50(10), 1785–1790.
Harvey RA, Champe PC, Finkel R, Cubeddu LX, & Clark MA. 2009.
Pharmacology (4th ed.). Philadelphia: Lippincott Williams & Wilkins.
Hassan ZK, Elobeid Ma, Virk P, Omer Sa, ElAmin M, Daghestani MH, & AlOlayan EM. 2012. Bisphenol A induces hepatotoxicity through oxidative stress in rat model. Oxidative Medicine and Cellular Longevity, 2012, 194829.
Kalghati S, Spina CS, Costello JC, Liesa M, Morones-Ramirez JR., Slomovic S, et al. 2013. Bactericidal Antibiotics Induce Mitochondrial Dysfunction and Oxidative Damage in Mammalian Cells. Science Translation Medicine,
5(192).
Katzung BG. 2006. Basic and Clinical Pharmacology. San Francisco: McGraw-Hill’s.
Kaur SP, Rao R, & Nanda S. 2011. Amoxicillin: A broad spectrum antibiotic.
International Journal of Pharmacy and Pharmaceutical Sciences.
Kim JS, Jang YR, Lee JW, Kim JY, Jung YK, Chung DH, et al. 2011. A case of amoxicillin-induced hepatocellular liver injury with bile-duct damage. The Korean Journal of Hepatology, 17(3), 229–32.
Leary S, Underwood W, Lilly E, Anthony R, Cartner S, Corey D, et al. 2013.
Euthanasia.
Li PY, Chang YC, Tzang BS, Chen CC, & Liu YC. 2007. Antibiotic amoxicillin induces DNA lesions in mammalian cells possibly via the reactive oxygen species. Mutation Research - Genetic Toxicology and Environmental Mutagenesis, 629(2), 133–139.
Lin, P. (2014). A Case of Amoxicillin Induced Hepatocellular Injury, 18, 3–5.
Łukaszewicz-Hussain a, & Moniuszko-Jakoniuk J. 2004. Liver catalase,
glutathione peroxidase and reductase activity, reduced glutathione and hydrogen peroxide levels in acute intoxication with chlorfenvinphos, an organophosphate insecticide. Polish Journal of Environmental Studies, 13(3), 303–309.
Menteri Kesehatan RI. 2006. Keputusan Menteri Kesehatan Republik Indonesia Nomor 189/Menkes/SK/III/2006 tentang Kebijakan Obat Nasional.
Menteri Kesehatan RI. 2010. Peraturan Menteri Kesehatan Republik Indonesia Nomor HK.02.02/MENKES/068/I/2010 tentang Kewajiban Menggunakan Obat Generik di Fasilitas Pelayanan Kesehatan Pemerintah.
Moffat AA, Osselton MD, & Widdop B. 2004. Clarke’s Analysis of Drugs and
Poisons 3e (Pharma, 2007).
Murray KF, Hadzic N, Wirth S, Bassett M, & Kelly D. 2008. Drug-related hepatotoxicity and acute liver failure. Journal of Pediatric Gastroenterology and Nutrition, 47(4), 395–405.