ABSTRAK
PENGARUH VOLUME MEDIA TANAM DAN JUMLAH TANAMAN INANGPueraria javanicaPER POT PADA PERKEMBANGAN
DAN PRODUKSI FUNGI MIKORIZA ARBUSKULAR
Oleh
Ramadian Budi Santoso
Produksi mikoriza sangat dipengaruhi oleh tanaman inang dan juga volume media tanam yang digunakan. Oleh karena itu, diperlukan adanya pengaturan jumlah tanaman inang dan perbedaan volume media agar mikoriza dapat
berkembang dengan baik dan selanjutnya produksi spora dapat meningkat.
Penelitian ini bertujuan untuk (1) mendapatkan jumlah tanaman inang per pot yang paling sesuai untuk memproduksi FMA, (2) Bagaimanakah respon tanaman inang dalam memproduksi spora mikoriza terhadap setiap peningkatan volume
media yang digunakan, (3) menentukan volume media yang paling sesuai untuk memproduksi FMA, dan (4) untuk mengetahui apakah jumlah tanaman inang per
Ramadian Budi Santoso Penelitian ini dilaksanakan di rumah plastik, dan Laboratorium Produksi
Perkebunan Fakultas Pertanian, Universitas Lampung Bandar Lampung, dari bulan Februari 2010 sampai Mei 2010. Perlakuan diterapkan pada petak
percobaan dalam rancangan kelompok teracak sempurna (RKTS) dengan 4 ulangan. Faktor pertama adalah jumlah tanaman inang per pot terdiri atas 1, 2, 3, 4, dan 5 tanaman inang per pot. Faktor kedua adalah volume media tanam terdiri
atas 200 ml, 400 ml, 600 ml, 800 ml, dan 1100 ml. Pengelompokkan didasarkan atas perbedaan waktu tanam. Homogenitas ragam diuji dengan Uji Bartlett dan
aditivitas data diuji dengan Uji Tukey. Selanjtnya data dianalisis ragam dan perbedaan nilai tengah diuji denga Uji Beda Nyata Terkecil (BNT) pada taraf 5% dan uji Regresi.
Hasil penelitian menunjukkan bahwa penggunaan 5 tanaman inang Pj per pot dan
volume 200 ml lebih sesuai untuk produksi FMA karena menghasilkan jumlah spora yang terbanyak dari pada jumlah tanaman inang yang lain. Pengaruh
PENGARUH VOLUME MEDIA TANAM DAN JUMLAH TANAMAN INANGPueraria javanicaPER POT PADA PERKEMBANGAN
DAN PRODUKSI FUNGI MIKORIZA ARBUSKULAR
Oleh
RAMADIAN BUDI SANTOSO
Skripsi
Sebagai Salah Satu Syarat untuk Mencapai gelar SARJANA PERTANIAN
Pada
Program Studi Agronomi Jurusan Budidaya Pertanian
FAKULTAS PERTANIAN UNIVERSITAS LAMPUNG
PENGARUH VOLUME MEDIA TANAM DAN JUMLAH TANAMAN INANGPueraria javanicaPER POT PADA PERKEMBANGAN
DAN PRODUKSI FUNGI MIKORIZA ARBUSKULAR
(Skripsi)
Oleh
RAMADIAN BUDI SANTOSO
FAKULTAS PERTANIAN UNIVERSITAS LAMPUNG
DAFTAR GAMBAR
Gambar
Halaman
1. Letak tanaman yang diinokulasi dan yang tidak diinokulasi FMA ... 28
2. Tata letak percobaan di rumah plastik ... 29
3. Letak pengambilan sampel median tanam ... 31
4. Hubungan infeksi akar bulan ke- 2 dan volume media tanam ... 36
5. Hubungan infeksi akar bulan ke- 5 dan volume media tanam ... 37
6. Hubungan bobot kering tajuk tanaman dan volume media tanam ... 38
7. Hubungan bobot kering akar tanaman dan volume media tanam ... 40
8. Hubungan antara persen infeksi akar dan jumlah spora pada bulan ke-5 (akhir penelitian) ... 42
9. Hubungan antara bobot kering tajuk tanaman dengan jumlah spora pada bulan ke-5 (akhir penelitian) ... 45
10. Hubungan antara bobot kering akar tanaman dengan jumlah spora pada bulan ke-5 (akhir penelitian) ... 45
11. Hubungan antara bobot kering akar tanaman dengan jumlah spora pada bulan ke-5 (akhir penelitian) ... 47
DAFTAR ISI
Halaman
DAFTAR TABEL... ... vi
DAFTAR GAMBAR ... viii
I. PENDAHULUAN ... 1
1.1 Latar Belakang ... 1
1.2 Perumusan Masalah Penelitian ... 4
1.3 Tujuan Penelitian ... 5
1.4 Manfaat Penelitian ... 5
1.5 Kerangka Teoretis ... 5
1.5.1 Landasan teori ... 5
1.5.2 Kerangka pemikiran ... 9
1.5.3 Hipotesis ... 12
II. TINJAUAN PUSTAKA ... 13
2.1 Pengertian Fungi Mikoriza ... 13
2.2 Sifat-sifat Fungi Mikoriza ... 14
2.3 Manfaat Fungi Mikoriza ... 16
2.4 Faktor-Faktor Yang Mempengaruhi Perkembangan Mikoriza ... 18
2.5 Tanaman Inang ... 21
2.6 Media Tanam ... 22
III. BAHAN DAN METODE ... 24
3.1 Tempat dan waktu Penelitian ... 24
3.2 Bahan dan Alat Penelitian ... 24
3.3 Metode Penelitian ... 25
3.4 Pelaksanaan Penelitian ... 26
Halaman
IV. HASIL DAN PEMBAHASAN ... 33
4.1 Hasil ... 33
4.1.1 Jumlah spora bulan ke-2 ... 34
4.1.2 Jumlah spora bulan ke-5 ... 34
4.1.3 Persen infeksi akar bulan ke-2 ... 35
4.1.4 Persen infeksi akar bulan ke-5 ... 37
4.1.5 Bobot kering tajuk tanaman ... 38
4.1.6 Bobot kering akar tanaman ... 39
4.2 Pembahasan ... 41
V. KESIMPULAN DAN SARAN ... 49
5.1 Kesimpulan ... 49
5.2 Saran ... 50
DAFTAR PUSTAKA ... 51
DAFTAR PUSTAKA
Anas, I. 1997.Bioteknologi Tanah. Laboratorium Biologi Tanah. Jurusan Tanah. Fakultas Pertanian. IPB.
Anas, I. dan J. L. O. Tampubolon. 2004.Media campuran tanah pasir dan pupuk anorganik untuk memproduksi inokulum cendawan mikoriza arbuskular (CMA). Buletin Agronomi32 (1): 26–31.
Brundrett, M. 2004.Diversity and classification of mycorrhizal associations. Biology
Review. 79: 473–495.
Campbell, N.A. 2002.Biologi. Edisi kelima. Jilid 1. Penerjemah: Rahayu Lestari. Terjemahan dariBiology. Erlangga. Jakarta.
Cooper, K.M. 1984. Physiology of VA mycorrhizal associations. In C.L. Powell, D.J. Bagyaraj,VA Mycorrhizae. CRC Press, Boca Raton, FL, pp 155-186. Daft, M.J. and A.A. El-Giahmi. 1975.Effect of Glomus infection on three
legumes.. In F.E. Sanders, B. Mosse, and P.B. Tinker (Editors). Endomycorrhizas. Academic Press, London. Pp. 581-592.
De La Cruz, R.E. 1981.Mycorrhizae- indispensable allies in forest regeneration. Symposium on Forest Regeneration in Soult East Asia. BIOTROP, Bogor. Indonesia.
Gardner, F. P., R. B. Pearce, dan R. L. Mitchell, 1991.Fisiologi Tanaman Budidaya.Universitas Indonesia (UI) Press, Jakarta. 428 hal.
Gentili, F. and Jumpponen, A. 2006.Potential and possible uses of bacterial and fungal biofertilizers.In:Handbook of Microbial Biofertilizers.Haworth Press, Technology & Enginering, New York, pp 1-28.
Husin, E. F. dan R. Marlis, 2002.Aplikasi cendawan mikoriza arbuskular sebagai pupuk biologi pada pembibitan kelapa sawit.Prosiding Seminar Nasional BKS PTN Wilayah Indonesia Barat, FP USU Medan.
Imas, T., R. S. Hadiatomo, A. W. Gunawan, dan Y. Setiadi. 1989.Mikrobiologi Tanah II.Institut Pertanian Bogor. Jawa Barat. 144 hlm.
Krishna, K.R., and D. J. Bagyaraj. 1984. Growth and nutrient uptake of peanut inoculated with mycorrhizal fungus Glomus fasciculatum compared with uninaculated ones. Plant and Soil,17: 405-408.
Manjunath, A., and D. J. Bagyaraj. 1984.Effect of fungicides on mycorrhizal colonization and growht of onion. Plant and Soil78: 147-150.
Menge, J.A. 1984. Inoculum production. In : C.L Powell and D.J. Bagyaraj (Eds.) VA Mycorrhiza. Florida. CRC Press. Hal. 187-203.
Mosse, S. 1981. VesicularArbuscular Mycoriza research for tropical agriculture. Research Bulletin.
Naswir. 2003.Pemanfaatan urine sapi yang difermentasi sebagai nutrisi tanaman.
http://tumoutou.net/702_07134/naswir.htm.28 Februari 2009.
Nuhamara, S.T. 1994.Peranan mikoriza untuk reklamasi lahan kritis. Program Pelatihan Biologi dan Bioteknologi Mikoriza.
Pattimahu, D.V. 2004.Restorasi lahan kritis pasca tambang sesuai kaidah ekologi.Makalah Mata Kuliah Falsafah Sains, Sekolah Pasca Sarjana, IPB. Bogor.
Pujianto. 2001.Pemanfaatan jasad mikro jamur mikoriza dan bakteri dalam sistem
pertanian berkelanjutan di Indonesia. http://www.hayati-ip6.com/rudyet/indiv 2001/pujianto.htm. 13 Desember 2009.
Rao, N. and S. Subha, 1994.Mikroorganisme Tanah dan Pertumbuhan Tanaman. Edisi Kedua. Penerbit Universitas Indonesia. Jakarta.
Situmeang,R. 2006.Kimia Katalis. Diktat Kuliah. Bandar Lampung.
Sanusi, H. M. 2004.Pemanfaatan mikoriza sebagai pupuk hayati.Prosiding Seminar Mikoriza Teknologi dan Pemanfaatan Inokulum
Endo-Ektomikoriza untuk Pertanian, Perkebunan, dan Kehutanantanggal 16 September 2003. Universitas Padjadjaran. Bandung. hlm. 1–6.
Sieverding. E. 1991.Vesikular Arbuskular Mycorrhiza Management in Tropical Agrosystem. GTZ. Eastborn.
Simanungkalit, R. D. M. 2004.Teknologi cendawan mikoriza arbuskular: Produksi
Inokulum dan Pengawasan Mutunya. Prosiding Seminar Mikoriza. Teknologi dan Pemanfaatan Inokulum Endo-Ektomikoriza untuk Pertanian, Perkebunan, dan Kehutanantanggal 16 September 2003. Universitas Padjadjaran. Bandung. hlm. 7–17.
Smith, S.E. dan D.J. Read. 1997.Mycorrhizal Symbiosis. Edisi ke-2. Academic Press. California.
Subiksa, I.G.M. 2005.Pemanfaatan mikoriza untuk penanggulangan lahan kritis. Makalah Falsafah Sains Program Pasca Sarjana Institut Pertanian Bogor. Bogor.
Suhardi. 1989.Pedoman Kuliah Mikoriza Vesikular Arbuskular (MVA). Universitas
Gajah Mada. Yogyakarta. 178 hlm.
Suwandi, M. dan M. Siahaan. 1989.Pemupukan tanaman kelapa sawit, ha1 1 18 -128.Prosiding Pertemuan Teknis Kelapa Sawit Pekan baru, 19–21 Februari 1989.
Syib’li. M. A. 2008.Jati mikoriza, sebuah upaya mengembalikan eksistensi hutan dan ekonomi Indonesia.http://-www.kabarindonesia.com.
Vilarino A, J. Arines, H . Schuepp. 1992. Propagule Production by VA fungi in Red Clover Plants Subjected to Periodic Removal of the Aerial Parts. CAB International. Cambridge. 406 hlm.
Widodo, A. dan Marlin. 2006.Unsur hara tanaman. Bahan Ajar Nutrisi Tanaman. Jurusan Budidaya Pertanan Universitas Bengkulu, Bengkulu.
I. PENDAHULUAN
1.1 Latar Belakang dan Masalah
Kebutuhan pangan dari tahun ke tahun meningkat, hal ini sejalan dengan
pertumbuhan penduduk yang juga meningkat. Berbagai upaya dilakukan untuk meningkatkan produksi pangan yang berkesinambungan. Peningkatan produksi pangan dapat dilakukan dengan cara intensifikasi dan ekstensifikasi. Cara
ekstensifikasi tidak mungkin lagi dilakukan karena jumlah lahan pertanian yang semakin menyempit. Maka salah satu cara untuk meningkatkan produksi adalah dengan cara intensifikasi.
Intensifikasi dilakukan dengan cara meningkatkan produktivitas lahan pertanian yang telah tersedia. Para ilmuan terdahulu melakukan penambahan abu dan kapur untuk meningkatkan hasil, dan sekarang para ilmuan melakukan penelitian dengan
menambahkan mineral pada tanah pertanian untuk melihat pengaruh mineral-mineral yang ditambahkan. Dengan keberhasilan tersebut telah banyak
Upaya intensifikasi ini juga mengalami hambatan seperti semakin kecilnya
subsidi pemerintah terhadap sarana produksi pertanian seperti pupuk dan pestisida.
Penggunaan pupuk buatan serta input luar lainnya secara besar-besaran
menyebabkan pencemaran sumber-sumber air yang berarti penurunan kualitas lingkungan (Pujianto, 2001). Masalah lain dari pupuk buatan yang digunakan
selama ini adalah rusaknya struktur tanah akibat pemakaian pupuk buatan yang terus-menerus sehingga perkembangan akar tanaman menjadi tidak sempurna. Hal ini juga akan memberi dampak terhadap produksi tanaman yang diusahakan
pada tanah yang biasa diberi pupuk buatan. Penggunaan pupuk buatan yang terus-menerus menyebabkan ketergantungan dan lahan lebih sukar untuk diolah
(Naswir, 2003). Oleh sebab itu, perlu dicari suatu alternatif yang dapat
menghemat atau mengurangi penggunaan pupuk buatan. Salah satu cara untuk menggantikan sebagian atau seluruh fungsi pupuk buatan tersebut adalah dengan
memanfaatkan pupuk hayati berupa Fungi Mikoriza Arbuskular (FMA) (Husin dan Marlis, 2002).
Banyak penelitian yang membuktikan bahwa FMA mampu meningkatkan serapan hara, baik hara makro maupun hara mikro, sehingga penggunaan FMA dapat
dijadikan sebagai alat biologis untuk mengurangi dan mengefisienkan penggunaan pupuk buatan. De La Cruz (1981) membuktikan bahwa FMA mampu
jangkauan akar terhadap penyerapan unsur hara, maka serapan hara tanaman pun
meningkat sehingga hasil tanam juga akan meningkat. Selain itu menurut Subiksa (2005), pemanfaatan FMA juga diyakini mampu memperbaiki kondisi tanah.
Rehabilitasi lahan kritis dapat dilakukan dengan tanaman bermikoriza, baik untuk tanaman pangan, perkebunan, maupun hutan tanaman industri.
Peranan FMA dalam meningkatkan pertumbuhan dan produksi tanaman tidak saja
banyak dilaporkan dalam penelitian-penelitian dari berbagai negara tetapi juga beberapa tahun belakangan ini banyak laporan mengenai aplikasi dan usaha memproduksi inokulum FMA yang diusahakan secara komersil (Anas, 1997).
Cara yang paling umum dipakai dalam memproduksi inokulum FMA adalah
dengan metode kultur pot yaitu FMA yang telah diketahui keefektifannya diinokulasikan pada tanaman inang tertentu yang ditanam pada medium padat yang steril. Metode ini dikembangkan oleh Mosse pada tahun 1953 yang
menginokulasikan secara murni salah satu spesiesEndogone(sekarang namanya Glomus mosseae) pada akar tanaman arbei yang tumbuh pada tanah steril di
rumah kaca. Sampai sekarang metode ini masih tetap banyak digunakan untuk memproduksi inokulum FMA (Simanungkalit, 2004).
Menurut simanungkalit (2004), FMA hidup bersimbiosis dengan tanaman inang
yang responsif dan memiliki perakaran banyak. TanamanPueraria javanica merupakan tanaman yang mempunyai perakaran banyak sehingga diharapkan semakin banyak tanaman inang akan semakin banyak akar yang dihasilkan
sehingga menyebabkan tanaman stres. Kondisi tanaman yang stres sampai tingkat
tertentu akan memacu perkembangan spora mikoriza. Perbedaan volume media yang digunakan dalam produksi spora mikoriza akan berpengaruh pada
perkembangan mikoriza karena semakin besar volume media yang digunakan akan memperluas perakaran tanaman dan akan semakin banyak akar yang terinfeksi oleh mikoriza, sehingga akan semakin banyak pula spora yang
dihasilkan.
Untuk memproduksi FMA yang akan digunakan sebagai inokulum di lapangan dalam bentuk pupuk hayati, diperlukan teknik yang paling sesuai terutama dalam
penggunaan tanaman inang dan media tanam yang digunakan. Oleh karena itu, dalam penelitian ini digunakan tanaman inangPueraria javanica(PJ),yang
diujikan pada media zeolit dan pasir agar dapat dilihat hasilnya apakah efektif untuk produksi inokulum FMA.
1.2 Perumusan Masalah Penelitian
Berdasarkan identifikasi dan pembatasan masalah, penelitian ini dilakukan untuk menjawab masalah yang dirumuskan dalam pertanyaan sebagai berikut:
1. Berapakah jumlah tanaman inang per pot yang paling sesuai untuk produksi FMA?
2. Bagaimanakah respon tanaman inang dalam memproduksi spora mikoriza terhadap setiap peningkatan volume media yang digunakan?
3. Volume media berapakah yang paling sesuai untuk produksi FMA?
1.3 Tujuan Penelitian
Berdasarkan identifikasi dan perumusan masalah maka penelitian dilakukan
dengan tujuan sebagai berikut:
1. Untuk mendapatkan jumlah tanaman inang per pot yang paling sesuai untuk memproduksi FMA.
2. Untuk mengetahui respon tanaman inang dalam memproduksi spora mikoriza terhadap setiap peningkatan volume media yang digunakan?
3. Untuk menentukan volume media yang paling sesuai untuk memproduksi FMA.
4. Untuk mengetahui apakah jumlah tanaman inang per pot yang paling sesuai
untuk produksi FMA ditentukan oleh volume media yang digunakan.
1.4 Manfaat Penelitian
Penelitian ini bermanfaat dalam penyediaan pupuk hayati FMA untuk sistem pertanian organik yang ramah lingkungan dan upaya peningkatan produksi pertanian.
1.5 Kerangka Teoritis
1.5.1 Landasan teori
pemanfaatan FMA sebagai pupuk hayati di lapangan. Penyebab sulitnya
penyediaan FMA dalam jumlah banyak adalah karena fungi ini belum dapat ditumbuhkan dalam kultur buatan. Salah satu cara perbanyakan FMA yang
banyak dilakukan adalah dengan menggunakan kultur pot (Suhardi, 1989).
Pembentukan dan perkembangan FMA dipengaruhi oleh berbagai faktor, misalnya suhu tanah dan intensitas cahaya, kemasaman tanah, kadar hara tanah,
senyawa-senyawa kimia pertanian seperti pupuk, dan pestisida, jasad renik tanah dan hasil metabolisme tanaman inang (Smith dan Read, 1997)
Kandungan fosfor dan nitrogen yang tinggi dalam tanah maupun dalam media buatan akan menghambat terbentuknya koloni akar dan pada akhirnya akan
mengurangi terbentuknya spora. Pada kondisi tanah yang subur maka fotosintat pada akar akan berkurang yang mengakibatkan terhambatnya pembentukan koloni akar FMA (Suhardi, 1989).
Brown dan Gabor (1986) yang dikutip oleh Yusnaini (1998) menyatakan bahwa persen kolonisasi FMA pada akar tanaman kedelai tertinggi ditemukan pada kedelai yang diinokulasi Rhizobium tidak bersamaan dengan waktu inokulasi
FMA.
Proses infeksi akar oleh FMA dimulai dengan perkecambahan spora
menghasilkan hifa yang masuk ke dalam sel epidermis akar dan selanjutnya
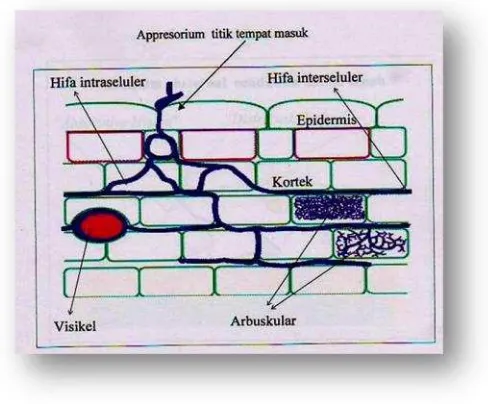
berkembang secara interseluler dan intraseluler. Hifa intraseluler dapat
masa protoplasma berbutir-butir dan bercampur dengan protoplasma sel inang. Arbuskular berfungsi sebagai tempat terjadinya transfer hara dua arah antara fungi dan inang (Harley dan Smith, 1983).
Struktur fungi mikoriza yang berperan dalam kelangsungan simbiosis dengan
[image:19.595.189.433.300.502.2]tanaman inang adalah hifa intraselular, hifa interselular, arbuskular, dan vesikular yang terdapat dalam sel korteks akar (Gambar 1).
Gambar 1. Struktur FMA dalam akar (Brundrett, 2004).
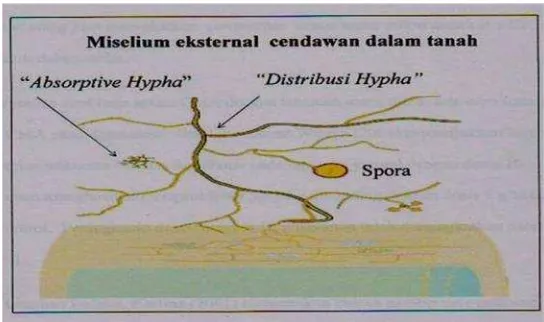
Pada sistem perakaran yang terinfeksi fungi mikoriza akan muncul hifa eksternal
yang menyebar di sekitar rhizosfer dan berfungsi sebagai alat absorbsi unsur hara. Hifa eksternal ini berfungsi untuk memperluas sistim perakaran tanaman yang
digunakan untuk menyerap unsur hara dan air serta mampu melarutkan fosfat dalam tanah yang semula berada dalam bentuk yang tidak dapat diserap oleh akar tanaman. Selain itu, hifa eksternal juga berfungsi untuk menghasilkan spora.
Gambar 2. Struktur hifa eksternal dalam tanah (Brundrett, 2004).
Tanaman inang yang akan digunakan untuk memproduksi spora FMA harus
mempunyai daya adaptasi yang baik, berasosiasi dengan FMA, cepat tumbuh dengan perakaran yang ekstensif, dan tidak rentan terhadap patogen. Karena sebagian besar tanaman berasosiasi dengan FMA, maka berbagai jenis tanaman
dapat digunakan sebagai tanaman inang FMA. Umumnya kesehatan tanaman adalah lebih penting daripada jenis tanamannya (Vilarinoet al.,1992)
Kebanyakan tumbuhan yang mempunyai nilai ekonomi seperti Graminae dan
Leguminosae umumnya bermikoriza. Tanaman legume pada umumnya terinfeksi lebih berat dibandingkan dengan sorghum (Imaset al., 1989).
Daft dan El-Giahmi (1975) dalam percobaan mereka dengan tiga jenis
2004). Varietas Pelanduk memberikan respon yang paling besar dengan kenaikan
bobot kering biji sebesar 26%. Krishna dan Bagyaraj (1984) menemukan adanya pengaruh sinergistik dari interaksi antara FMA dengan Rhizobium terhadap
pertumbuhan kacang tanah.
Pemilihan media tumbuh dalam produksi inokulum FMA merupakan salah satu aspek paling penting dalam memperbanyak FMA (Menge, 1984).
Dianjurkan menggunakan media yang sedikit mengandung unsur hara dengan kapasitas tukar kation (KTK) tinggi dan ketersediaan unsur P yang rendah serta bebas dari patogen. Media tanam dengan kandungan P tersedia yang tinggi akan
menghambat kolonisasi dan produksi spora FMA (Cooper, 1984).
Semakin besar ukuran pot menambah kemungkinan terbentuknya jumlah produksi FMA lebih besar pula, ukuran pot 15.000 cm³ ternyata memproduksi spora 90 kali lebih banyak dibandingkan dengan ukuran pot yang hanya 750 cm3(Siverding,
1991).
Semakin banyak tanaman inang maka semakin banyak jumlah akar yang dihasilkan sehingga akar yang terinfeksi oleh FMA pun semakin banyak dan
menghasilkan hifa eksternal yang membentuk spora akan banyak pula.
1.5.2Kerangka pemikiran
mengeluarkan hifa yang kemudian masuk ke akar apabila kondisi di daerah
rhizosfer sesuai atau cocok bagi FMA. Kondisi di daerah rhizosfer ditentukan oleh tanaman inang yang berhubungan dengan jumlah serta jenis eksudat yang
dikeluarkan akar tanaman.
Pada keadaan tidak adanya tanaman inang, hifa yang terbentuk dari spora sebelum bersimbiosis berhenti tumbuh dan akhirnya mati. Jika ada akar tanaman inang,
fungi melalui hifanya akan kontak dengan tanaman inang dan memulai proses simbiotik. Fungi menyempurnakan proses morfogenesis kompleks dengan memproduksi hifa interseluler dan intraseluler, vesikula, dan arbuskula.
Hifa fungi akan mengisi korteks akar, bercabang-cabang diantara sel dan titik
penetrasinya. Bentuk yang khusus pada fungi adalah struktur yang seperti “haustorium” (arbuskula atau kumparan hifa) di dalam sel korteks, dipisahkan
dari sitoplasma inang oleh membran sel inang dan dinding sel fungi. Hifa yang
masuk ke dalam sel terus bercabang secara dikotomi disebut sebagai arbuskular, sementara hifa yang berkembang pada ruang antar sel ada yang menggelembung
membentuk vesikular yang berisi cadangan makanan berupa lemak dan dapat dipergunakan untuk perkembangan FMA.
Selain berkembang di dalam akar, hifa juga ada yang berkembang di luar akar.
Hifa ini berfungsi untuk menyerap unsur hara dari tanah kemudian
ditranslokasikan melalui arbuskular yang merupakan tempat pertukaran unsur hara dari FMA dengan senyawa organik yang bersumber dari tanaman inang.
Volume pot yang berukuran besar lebih banyak menghasilkan infeksi dan jumlah
spora dibandingkan dengan volume pot yang berukuran kecil, hal ini dikarenakan volume pot yang kecil akan menyebabkan terhambatnya pembentukan akar serta
makin sedikitnya eksudat akar yang dikeluarkan tanaman inang sehingga mengakibatkan terhambatnya perkembangan mikoriza. Semakin besar volume pot sampai batas tertentu, akar mempunyai ruang yang lebih luas untuk
perkembangan serta makin banyak eksudat akar yang dikeluarkan tanaman inang sehingga memungkinkan infeksi FMA yang lebih luas.
Tanaman inang yang ditanam dalam jumlah yang sedikit akan menghasilkan
infeksi akar dan jumlah spora yang sedikit, karena jumlah akar yang dihasilkan oleh tanaman sedikit sehingga hifa eksternal yang membentuk spora pun akan
sedikit. Semakin banyak tanaman inang yang ditanam semakin banyak pula infeksi akar dan spora yang akan dihasilkan, hal ini dikarenakan dengan jumlah tanaman inang yang banyak sampai batas tertentu akan menghasilkan akar yang
banyak pula sehingga hifa eksternal yang dikeluarkan oleh mikoriza akan membentuk spora yang banyak pula.
Tanaman inang dengan jumlah yang sama pada volume pot yang berbeda atau volume pot yang sama pada jumlah tanaman inang yang berbeda akan
menghasilkan persen infeksi akar dan jumlah spora yang berbeda. Setiap volume pot memerlukan jumlah tanaman inang tertentu untuk menghasilkan infeksi akar
1.5.3 Hipotesis
Dari kerangka pemikiran yang telah dikemukakan, maka hipotesis yang diajukan
adalah sebagai berikut:
1. Semakin banyak tanaman inang sampai jumlah tertentu akan meningkatkan
jumlah produksi FMA, peningkatan jumlah tanaman inang seterusnya akan menurunkan sampai jumlah tertentu produksi spora.
2. Semakin besar volume pot sampai volume tertentu akan meningkatkan
jumlah produksi FMA, peningkatan volume media seterusnya akan menurunkan produksi spora.
II. TINJAUAN PUSTAKA
2.1 Pengertian Fungi Mikoriza
Fungi Mikoriza Arbuskular (FMA) merupakan asosiasi antara fungi tertentu
dengan akar tanaman dengan membentuk jalinan interaksi yang komplek. Mikoriza berasal dari kata miko (mykes = fungi) dan rhiza yang berarti akar. Mikoriza dikenal dengan fungi tanah karena habitatnya berada di dalam tanah dan
berada di area perakaran tanaman (rizosfer). Selain disebut sebagai fungi tanah, FMA juga biasa dikatakan sebagai fungi akar. Keistimewaan dari fungi ini adalah kemampuannya dalam membantu tanaman untuk menyerap unsur hara
terutama unsur hara fosfor atau P (Syib’li, 2008).
Fungi Mikoriza Arbuskular merupakan tipe asosiasi mikoriza yang tersebar sangat luas dan ada pada sebagian besar ekosistem yang menghubungkan antara tanaman
dengan rizosfer. Simbiosis terjadi di dalam akar tanaman yaitu fungi mengolonisasi apoplast dan sel korteks untuk memperoleh karbon hasil
fotosintesis dari tanaman.
Berdasarkan struktur dan cara fungi menginfeksi akar, mikoriza dapat
dikelompokkan ke dalam tiga tipe yaitu ektomikoriza, endomikoriza, dan
ektendomikoriza. Jenis ektomikoriza mempunyai sifat antara lain akar yang kena
infeksi membesar, bercabang, rambut-rambut akar tidak ada, hifa menjorok ke luar dan berfungsi sebagi alat yang efektif dalam menyerap unsur hara dan air. Hifa fungi tidak masuk ke dalam sel tetapi hanya berkembang di antara
dinding-dinding sel jaringan korteks membentuk struktur seperti pada jaringan hartiq. Fungi jenis endomkoriza memiliki jaringan hifa yang masuk kedalam sel kortek
akar dan membentuk struktur yang khas berbentuk oval yang disebut vesikular dan sistem percabangan hifa yang disebut arbuskul, sehingga endomikoriza disebut juga vesikular-arbuskular mikoriza. Sedangkan ektendomikoriza
merupakan bentuk antara (intermediet) kedua mikoriza yang lain. Ciri-cirinya antara lain adanya selubung akar yang tipis berupa jaringan Hartiq, hifa dapat menginfeksi dinding sel korteks dan juga sel-sel korteknya. Penyebarannya
terbatas dalam tanah-tanah hutan sehingga pengetahuan tentang mikoriza tipe ini sangat terbatas (Brundrett, 2004).
2.2 Sifat-sifat Fungi Mikoriza
Fungi mikoriza arbuskular tergolong ke dalam endomikoriza, membentuk
2.2.1 Vesikular
Vesikular merupakan struktur fungi yang berasal dari pembengkakan hifa internal,
berbentuk bulat telur yang berukuran 30-50μm–sampai 80μm- 100μm, dan
berisi banyak senyawa lemak sehingga merupakan organ penyimpanan cadangan makanan dan pada kondisi tertentu dapat berperan sebagai spora atau alat untuk
mempertahankan kehidupan fungi. Jika suplai metabolik dari tanaman inang berkurang, maka cadangan makanan itu akan digunakan oleh fungi sehingga vesikular mengalami degenerasi (Brundrett, 2004).
Tipe FMA yang bervesikular memiliki fungsi yang paling menonjol dari tipe fungi mikoriza lainnya. Hal ini dimungkinkan karena kemampuannya dalam berasosiasi dengan hampir 90% jenis tanaman, sehingga dapat digunakan secara
luas untuk meningkatkan ketahanan tanaman (Brundrett, 2004).
2.2.2 Arbuskular
Fungi mikoriza arbuskular di dalam akar membentuk struktur khusus yang disebut arbuskular. Arbuskular merupakan hifa yang bercabang halus yang dibentuk oleh
percabangan dikotomi yang berulang-ulang sehingga menyerupai pohon di dalam sel inang. Struktur ini mulai terbentuk 2-3 hari setelah infeksi, dimulai dengan
penetrasi cabang hifa lateral yang dibentuk oleh hifa ekstraseluler dan intraseluler ke dalam dinding sel inang (Brundrett, 2004).
Arbuskular merupakan percabangaan hifa yang masuk kedalam sel tanaman inang. Arbuskul dianggap aliran hara dua arah antara simbion fungi dan tanaman
Dengan bertambahnya umur, arbuskular berubah menjadi suatu struktur yang
menggumpal dan cabang-cabang pada arbuskular tidak dapat dibedakan lagi. Pada akar yang telah dikolonisasi oleh FMA dapat dilihat berbagai arbuskular
dewasa yang dibentuk berdasarkan umur dan letaknyaa. Arbuskular dewasa terletak dekat pada sumber unit kolonisasi tersebut (Pattimahu, 2004).
2.2.3 Spora
Spora terbentuk pada ujung hifa eksternal. Spora ini dapat dibentuk secara
tunggal, berkelompok atau di dalam sporokarp tergantung pada jenis funginya. Perkecanbahan spora sangat sensitif tergantung pada lingkungan seperti pH, temperatur, dan kelembaban tanah. Spora dapat hidup di dalam tanah sampai
beberapa tahun. Namun untuk perkembangan, FMA memerlukan tanaman inang. Spora dapat disimpan dalam waktu yang lama sebelum digunakan lagi (Mosse,
1981). Ukuran spora fungi sangat bervariasi dari sekitar 100m sampai 600m.
Karena ukuranya yang cukup besar, maka spora ini dapat dengan mudah diisolasi dari dalam tanah dengan menyaringnya (Simanungkalit, 2004).
2.3 Manfaat Fungi Mikoriza
Tanaman yang bermikoriza tumbuh lebih baik dari tanaman tanpa mikoriza. Penyebab utama adalah mikoriza secara efektif dapat meningkatkan penyerapan
unsur hara baik unsur hara makro maupun mikro. Selain itu, akar yang bermikoriza dapat menyerap unsur hara dalam bentuk terikat dan yang tidak tersedia bagi tanaman (Anas, 1997).
akan permanen pengaruhnya pada akar yang bermikoriza. Setelah periode
kekurangan air (water stress), akar yang bermikoriza akan cepat kembali normal. Hal ini disebabkan karena hifa fungi mampu menyerap air yang ada pada
pori-pori tanah saat akar tanaman tidak mampu lagi menyerap air. Penyebaran hifa yang sangat luas di dalam tanah menyebabkan jumlah air yang diambil meningkat (Anas, 1997).
Beberapa keuntungan yang diperoleh dengan adanya simbiosis ini adalah: (1) miselium fungi meningkatkan area permukaan akuisisi hara tanah oleh tanaman, (2) meningkatkan toleransi terhadap kontaminasi logam berat,
kekeringan, serta patogen akar, dan (3) memberikan akses bagi tanaman untuk dapat memanfaatkan hara yang tidak tersedia menjadi tersedia bagi tanaman
(Gentili dan Jumpponen, 2006).
Anas (1997) mengungkapkan bahwa adanya mikoriza berpengaruh terhadap (1)
adanya peningkatan absorpsi hara oleh tanaman, sehingga waktu yang diperlukan untuk mencapai akar lebih cepat, (2) meningkatkan toleransi terhadap erosi,
pemadatan, keasaman, dan salinitas, dan (3) memperbaiki agregasi partikel tanah.
Penggunaan mikoriza lebih menarik ditinjau dari segi ekologi karena aman dipakai, tidak menyebabkan pencemaran lingkungan. Bila mikoriza tertentu telah
berkembang dengan baik di suatu tanah, maka manfaatnya akan diperoleh untuk selamanya. Mikoriza juga membantu tanaman untuk beradaptasi pada pH yang rendah. Demikian pula vigor tanaman bermikoriza yang baru dipindahkan ke
2.4 Faktor-Faktor yang Mempengaruhi Perkembangan Fungi Mikoriza
Banyak faktor abiotik yang menentukan perkembangan FMA. Faktor-faktor tersebut antar lain suhu, tanah, kadar air tanah, pH, bahan organik tanah, intensitas cahaya dan ketersediaan hara, logam berat dan fungisida.
Suhu. Suhu yang relatif tinggi akan meningkatkan aktivitas fungi. Untuk daerah
tropika basah, hal ini menguntungkan. Proses perkecambahan dan pembentukan FMA melalui 3 tahap yaitu perkecambahan spora di tanah, penetrasi hifa ke dalam
sel akar, dan perkembangan hifa di dalam korteks akar. Suhu optimimum untuk perkecambahan spora sangat beragam tergantung pada jenisnya. Suhu yang tinggi pada siang hari (350C) tidak menghambat perkembangan akar dan aktivitas
fisiologi FMA. Peran mikoriza hanya menurun pada suhu diatas 400C. Suhu bukan merupakan faktor pembatas utama bagi aktivitas FMA. Suhu yang sangat tinggi lebih berpengaruh terhadap pertumbuhan tanaman inang (Mosse, 1981).
Kadar Air tanah. Untuk tanaman yang tumbuh di daerah kering, dengan adanya
FMA sangat menguntungkan karena dapat meningkatkan kemampuan tanaman untuk tumbuh dan bertahan pada kondisi yang kurang air. Dengan adanya FMA
dapat memperbaiki dan meningkatkan kapasitas serapan air tanaman inang. Mosse (1981) mengamati kenampakan aneh pada bibit tanaman alpukat (Acacua raddiana)yang dinikolasi dengan FMA. Pada tengah hari, saat kelembaban air
rendah, daun bibit alpukat dengan FMA tetap terbuka sedangkan tanaman yang tidak dinokulasi tertutup. Hal ini menandakan bahwa tanaman yang tidak
Meningkatnya kapasitas serapan air pada tanaman alpukat ber FMA menyebabkan
bibit lebih tahan terhadap pemindahan.
pH tanah. Fungi pada umumnya lebih tahan terhadap perubahan pH tanah.
Meskipun demikian, daya adaptasi masing-masing spesies fungi FMA terhadap
pH tanah berbeda-beda karena pH tanah mempengaruhi perkecambahan, perkembangan, dan peran mikoriza terhadap pertumbuhan tanaman (Mosse,
1981).
Bahan Organik. Bahan organik merupakan salah satu komponen penyusun tanah yang penting disamping bahan anorganik, air, dan udara. Jumlah spora FMA berhubungan erat dengan kandungan bahan organik di dalam tanah. Jumlah
maksimum spora ditemukan pada tanah-tanah yang mengandung bahan organik 1-2 persen sedangkan pada tanah-tanah berbahan organik kurang dari 0.5 persen kandungan spora sangat rendah (Anas, 1997).
Residu akar mempengaruhi ekologi fungi FMA, karena serasah akar yang terinfeksi mikoriza merupakan sarana penting untuk mempertahankan generasi FMA dari satu tanaman ke tanaman berikutnya. Serasah tersebut mengandung
hifa, vesikular dan spora yang dapat menginfeksi akar. Disamping itu juga, berfungsi sebagai inokulan untuk generasi tanaman berikutnya (Anas, 1997).
Cahaya dan Ketersediaan Hara. Anas (1997) menyimpulkan bahwa intensitas
Derajat infeksi terbesar terjadi pada tanah-tanah yang mempunyai kesuburan yang
rendah. Pertumbuhan perakaran yang sangat aktif jarang terinfeksi oleh FMA. Jika pertumbuhan dan perkembangan akar menurun, maka infeksi FMA
meningkat.
Peran mikoriza yang erat dengan penyediaan P bagi tanaman menunjukkan keterikatan khusus antara mikoriza dengan status P tanah. Pada wilayah beriklim
sedang, konsentrasi P tanah yang tinggi menyebabkan menurunnya infeksi FMA yang mungkin disebabkan konsentrasi P internal yang tinggi dalam jaringan inang (Anas,1997).
Beberapa spesies FMA diketahui mampu beradaptasi dengan tanah yang tercemar
seng (Zn), tetapi sebagian besar spesies FMA peka terhadap kandungan Zn yang tinggi. Pada beberapa penelitian lain diketahui bahwa strain-strain FMA tertentu toleran terhadap kandungan Mn, Al, dan Na yang tinggi (Mosse, 1981).
Fungisida. Fungisida merupakan racun kimia yang dirakit untuk membunuh
fungi penyebab penyakit pada tanaman. Di samping mampu memberantas fungi penyebab penyakit, fungisida Agrosan, Benlate, Plantavax meskipun dalam
konsentrasi yang sangat rendah (2.5g per g tanah) menyebabkan turunnya
kolonisasi FMA yang mengakibatkan terhambatnya pertumbuhan tanaman dan pengambilan P (Manjunath dan Bagyaraj, 1984).
Pemakaian fungisida menjadi dilematis, di satu pihak jika fungisida tidak dipakai
Pada masa depan perlu dicari satu cara untuk mengendalikan penyakit tanaman
tanpa menimbulkan pengaruh yang merugikan terhadap jasad renik berguna di dalam tanah (Marx, 1982 yang dikutip oleh Anas, 1997).
2.5 Tanaman Inang
Mikoriza sebenarnya bukan merupakan jenis fungi yang sangat spesifik pada
tanaman inang terentu. Walaupun mikoriza dapat membentuk koloni pada hampir setiap tanaman inang tetapi satu spesies dapat lebih efisien membentuk asosiasi
pada tanaman inang tertentu (Suhardi, 1989). Hal ini berhubungan dengan
kecocokan mikoriza dengan tanaman inang yang mengeluarkan eksudat akar yang merupakan makanan bagi fungi.
Bagi tanaman inang, adanya asosiasi dengan fungi mikoriza dapat memberikan manfaat yang sangat besar bagi pertumbuhannya baik secara langsung maupun tidak langsung. Secara tidak langsung fungi mikoriza berperan dalam perbaikan
stuktur tanah, meningkatkan kelarutan hara, dan proses pelapukan batu induk. Secara langsung, fungi mikoriza dapat meningkatkan serapan air, hara, dan melindungi tanaman dari pathogen akar dan unsur toksik (Subiksa, 2005).
Hampir semua tanaman pertanian akarnya terinfeksi fungi mikoriza. Gramineae
danLeguminosae umumnya bermikoriza. Jagung merupakan contoh tanaman yang terinfeksi hebat oleh mikoriza. Tanaman pertanian yang telah dilaporkan
perkebunan yang telah dilaporkan akarnya terinfeksi mikoriza adalah tebu, teh,
tembakau, palem, kopi, karet, kapas, jeruk, kakao, apel, dan anggur (Rao, 1994)
2.6 Media Tanam
Pemilihan media tumbuh dalam produksi inokulum FMA merupakan salah satu aspek paling penting dalam memperbanyak FMA. Dianjurkan
menggunakan media yang sedikit mengandung unsur hara dengan kapasitas tukar kation (KTK) tinggi dan ketersediaan unsur P yang rendah serta bebas dari
patogen. Media tanam dengan kandungan P tersedia yang tinggi akan menghambat kolonisasi dan produksi spora FMA (Subiksa, 2005).
Zeolit umumnya didefinisikan sebagai kristal alumina silika yang berstruktur tiga
dimensi, yang terbentuk dari tetrahedral alumina dan silika dengan rongga-rongga di dalam yang berisi ion-ion logam. Secara empiris, rumus molekul zeolit adalah Mx/n.(AlO2)x.(SiO2)y.xH2O. Struktur zeolit sejauh ini diketahui bermacam-macam,
tetapi secara garis besar strukturnya terbentuk dari unit bangun primer, berupa tetrahedral yang kemudian menjadi unit bangun sekunder polihedral dan membentuk polihendra dan akhirnya unit struktur zeolit (Situmeang, 2006).
Zeolit mempunyai sifat dehidrasi (melepaskan molekul H20) apabila dipanaskan. Pada umumnya struktur kerangka zeolit akan menyusut. Tetapi kerangka
dasarnya tidak mengalami perubahan secara nyata. Molekul H2O seolah-olah mempunyai posisi yang spesifik pada zeolit dan dapat dikeluarkan secara reversibel. Sifat zeolit sebagai adsorben dan penyaring molekul, dimungkinkan
Selain itu, kristal zeolit yang telah terdehidrasi merupakan adsorben yang selektif
dan mempunyai efektivitas adsorpsi yang tinggi (Nuhamara, 1994)
Media zeolit tidak perlu disterilisasi dengan cara memberi perlakuan uap panas
tetapi perlu dicuci untuk menghilangkan tepung zeolit yang halus. Jika tidak dicuci akan menyebabkan kondisi media tanam yang basah sehingga drainase kurang baik. Tepung zeolit tersebut selanjutnya masih menjadi kendala karena
tepung zeolit akan mengeras jika telah kering sehingga aerasi untuk akar dan mikoriza berkurang (Sanusi, 2004).
Menurut Subiksa (2005), golongan pasir mencakup semua tanah yang pasirnya
meliputi 70% atau lebih dari berat tanah itu. Sifat tanah semacam ini mencirikan sifat pasirnya. Lain halnya dengan golongan tanah yang lebih berat dan lebih
lekat yang menunjukkan sifat kelempungan. Dua kelas khusus tersebut adalah pasir dan pasir geluhan. Pasir memiliki KTK 2-4 meq/100 g. Menurut Pattimahu (2004), pasir mempunyai kemampuan menahan air yang rendah dan daya
III. BAHAN DAN METODE PENELITIAN
3.1 Tempat dan Waktu Penelitian
Percobaan ini dilaksanakan di rumah plastik, dan Laboratorium Produksi
Perkebunan Fakultas Pertanian, Universitas Lampung Bandar Lampung, dari bulan Februari 2010 sampai Mei 2010.
3.2 Bahan dan Alat Penelitian
Alat-alat yang digunakan dalam penelitian ini adalah alat tulis, mikroskop stereo dan mikroskop majemuk, saringan (ukura 250 µm, dan 45 µm), cawan petri,
cawan arloji, tabung reaksi, gelas preparat, timbangan, gunting, pinset makro, hand sprayer, dan nampan plastik.
Bahan yang digunakan antara lain inokulum fungi mikoriza Glomus sp. (P186-2
dengan jumlah spora + 100 spora/ 5g) deskripsi untuk FMA jenis Glomus dapat dilihat pada Tabel 1, zeolit jenis P-3, pasir, air, pot plastik dengan volume 200 ml,
400 ml, 600 ml, 800 ml, 1100 ml,Trypan blue, aquades, pupuk Hyponex merah yang merupakan pupuk lengkap mengandung (25% unsur N, 5% unsur P, 20% unsur K dan unsur-unsur lain seperti boron, kalsium, kobalt, tembaga, besi,
Tabel 1. Deskripsi spora P-186-2. Uraian Keterangan
Genus Glomus
Ciri spora
- Warna : Kuning orange kemerahan - Bentuk : Bulat
- Ukuran : Sedang Reaksi spora Spora tidak berubah warna terhadap
larutan Melzer
Asal Kebun Kelapa Sawit Tidar Kerinci Agung Sumatera Barat
Spora akhir 2527/100g
Media Pasir sungai : Zeolit P2= 1:1
Foto spora
3.3 Metode Penelitian
Untuk menjawab pertanyaan dalam perumusan masalah dan untuk menguji
hipotesis, maka perlakuan diterapkan dalam rancangan perlakuan faktorial (5x5) dengan 4 ulangan. Faktor pertama adalah volume media tanam yaitu v1(pot dengan volume 200 ml), v2(pot dengan volume 400 ml), v3(pot dengan volume
600 ml), v4(pot dengan volume 800 ml), v5(pot dengan volume 1100 ml) dan faktor kedua adalah jumlah tanaman per pot yaitu t1(1 tanaman per pot), t2(2
kelompok teracak sempurna (RKTS). Pengelompokan didasarkan pada perbedaan
waktu tanam yang dilakukan.
Kehomogenan nilai tengah antar perlakuan data yang diperoleh diuji dengan uji Bartlet dan kemenambahan data diuji dengan uji Tukey. Jika data homogen dan
bersifat menambah, maka data kemudian dianalisis ragam. Pemisahan nilai tengah antar perlakuan dilakukan dengan menggunakan uji Beda Nyata Terkecil
(BNT 5%) dan uji Regresi.
3.4 Pelaksanaan Penelitian
3.4.1 Menyiapkan Media tanam
Media tanam yang digunakan terdiri dari pasir dan zeolit yang telah dicampur dengan perbandingan 1:1. Sebelum dimasukkan kedalam pot, media tanam yang digunakan disterilkan terlebih dahulu. Pasir disterilkan dengan autoclave dengan
suhu 121 °C selama±1 jam sebanyak 2 kali dengan selang 1 hari. Dan untuk
zeolit tidak perlu di sterilkan tetapi dicuci untuk menghilangkan tepung zeolit yang halus. Media tanam yang telah steril tersebut kemudian dimasukkan ke dalam pot sesuai dengan perlakuan. Jumlah pot yang diisi dengan media tanam
sebanyak 100 buah (5 volume pot x 5 tanaman inang x 4 ulangan), lalu masing-masing pot disiram dengan volume yang sama.
3.4.2 Inokulasi Mikoriza dan Penanaman
Inokulasi FMA dilakukan setelah benih Pj berkecambah (3 hari). Benih Pj
sudah dilapisi dengan kertas merang yang lembab. Inokulasi dilakukan dengan
cara menempelkan spora mikoriza P 186-2 sebanyak 3 spora pada akar tanaman Pj. Pada bagian pot yang akan ditanami kecambah dibuat lubang dengan diameter
± 5mm dengan kedalaman ±10 mm, kemudian kecambah yang akan ditanam dimasukkan ke dalam lubang tanam, kemudian ditutup kembali dengan media. Kecambah yang telah diinokulasi dengan spora ditanam di tengah-tengah pot, dan
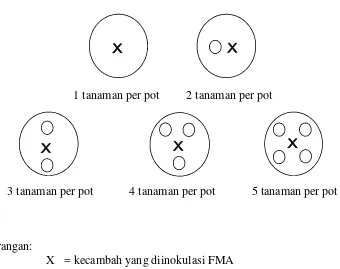
untuk perlakuan dengan jumlah tanaman inang lebih dari satu, maka kecambah yang lain diletakkan di sekeliling kecambah yang diinokulasi (Gambar 1). Setelah
selesai penanaman dan penempelan label sesuai dengan volume media dan jumlah tanaman, pot-pot disusun di dalam rumah plastik sesuai dengan tata letak
1 tanaman per pot 2 tanaman per pot
3 tanaman per pot 4 tanaman per pot 5 tanaman per pot
Keterangan:
[image:40.595.139.479.135.404.2]X = kecambah yang diinokulasi FMA O = kecambah yang tidak diinokulasi FMA
v5t1
v3t2
v1t1
v1t5
v1t3
v
5t
5v
4t
2v
3t
5v
4t
4v
2t
1v2t4
v2t2
v3t1
v5t4
v5t2
v
2t
5v
4t
3v
2t
3v
4t
1v
3t
3v4t5
v1t2
v3t4
v5t3
v1t
4v1t3
v2t1
v3t5
v1t2
v3t1
v5t1
v4t4
v4t2
v5t5
v1t4
v1t1
v1t5
v2t3
v5t3
v2t4
v
4t
3v
3t
4v
5t
4v
3t
2v
3t
3v2t5
v4t1
v2t2
v5t2
v4t5
v3t4
v4t4
v3t1
v5t2
v2t3
v
5t
1v
1t
3v
3t
3v
5t
3v
3t
2v1t1
v1t2
v2t2
v1t5
v4t1
v
5t
5v
3t
5v
4t
2v
1t
4v
4t
5Keterangan:
v1
= pot dengan volume 200 mlt1
= 1 tanaman inang per pot [image:42.595.110.512.3.258.2]v2
= pot dengan volume 400 mlt2
= 2 tanaman inang per potv3
= pot dengan volume 600 mlt3
= 3 tanaman inang per potv4
= pot dengan volume 800 mlt4
= 4 tanaman inang per potv5
= pot dengan volume 1100 mlt5
= 5 tanaman inang per potGambar 2. Tata letak percobaan di rumah plastik.
v4t4
v1t2
v5t2
v4t3
v5t5
v
2t
3v
4t
5v
1t
5v
3t
4v4t
1v2t2
v2t4
v2t5
v1t3
v3t3
v
1t
1v
3t
1v
5t
3v
5t
4v
4t
23.4.3 Pemupukan
Pemupukan dilakukan dengan menggunakan pupuk Hyponex merah dengan konsentrasi 2 g/liter, dan pupuk Hoagland (Lampiran pada Tabel 25). Jumlah pupuk yang diberikan setiap kali pemupukan adalah:
1. Volume media 200 ml diberikan dosis 10 ml 2. Volume media 400 ml diberikan dosis 20 ml
3. Volume media 600 ml diberikan dosis 30 ml 4. Volume media 800 ml diberikan dosis 40 ml 5. Volume media 1100 ml diberikan dosis 55 ml.
3.4.4 Perawatan tanaman
Tanaman disiram setiap pagi dan sore hari. Pengendalian gulma dilakukan secara manual dengan mencabut gulma yang tumbuh di dalam pot.
3.5 Pengamatan
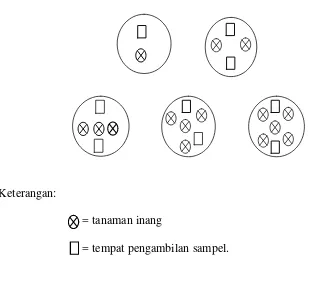
1. Jumlah spora. Spora dihitung saat tanaman berumur 2 bulan dan pada saat panen (umur tanaman 4 bulan). Pengambilan sampel media tanam dilakukan
dengan alat ’soil sampler’ pada dua titik setiap pot (Gambar 3), kemudian sampel
tersebut dikeringkan, apabila terdapat akar dipisahkan dari sampel untuk
pengamatan infeksi akar. Sampel media kemudian ditimbang (± 18 gram) dan dimasukkan ke dalam gelas ukur, ditambahkan air keran ± 500 ml kemudian diaduk agar spora terlepas dan mengambang di dalam air. Air dalam gelas ukur
-masing saringan dikumpulkan dalam cawan petri dan diamati dengan mikroskop
stereo dengan perbesaran 40 kali. Spora kemudian dihitung secara manual.
Keterangan:
= tanaman inang
[image:44.595.115.441.175.456.2]= tempat pengambilan sampel.
Gambar 3. Letak pengambilan sampel media tanam.
2. Persen infeksi akar oleh FMA. Persen infeksi dihitung saat tanaman berumur dua bulan dan pada saat panen. Sampel akar diambil secara acak (± 1 gram)
kemudian dicuci sampai bersih dan dimasukkan ke dalam botol film. Botol yang telah berisi sampel akar diisi dengan larutan KOH 10% sampai seluruh sampel
akar terendam dan dikukus dalam water bath dengan suhu 80 °C selama 15 menit untuk membersihkan sel dari sitoplasma. Larutan KOH lalu dibuang, dan akar dicuci dengan air yang mengalir. Kemudian sampel akar direndam kembali
merendamnya dalam larutanTrypan Blue0,05% (0,5 gramTrypan bluedalam
450 ml glycerol + 50 ml HCL 1% + 500 ml aquades) dan dikukus dalam water bath dengan suhu 80 °C selama 10 menit. Akar yang sudah diwarnai kemudian
disusun di atas preparat untuk diamati di bawah mikroskop majemuk dengan perbesaran 100 kali. Rumus yang digunakan untuk menghitung persentase infeksi akar oleh FMA adalah sebagai berikut:
Infeksi akar (%) =∑ akar yang terinfeksix 100% pengamatan
3. Bobot kering akar. Bobot kering akar ditimbang setelah pemanenan (umur tanaman 5 bulan) dengan cara media dibongkar lalu akar dipisahkan, dioven pada
suhu 70°C selama 48 jam lalu ditimbang.
4. Bobot kering tajuk. Bobot kering tajuk ditimbang setelah pemanenan (umur tanaman 5 bulan) dengan cara tajuk yang telah dipotong lalu dipisahkan dan
Diri ini akan sengsara bila selalu menginginkan orang lain menilai lebih dari kenyataan, jadilah manusia yang merdeka
yang berani tampil apa adanya
Sesungguhnya semua urusan (perintah)
apabila Allah menghendaki segala sesuatunya, Allah hanya berkata: “Jadilah”, maka jadilah
Judul Skripsi : PENGARUH VOLUME MEDIA TANAM DAN JUMLAH TANAMAN INANG (Pueraria javanica) PER POT PADA
PERKEMBANGANDAN PRODUKSI FUNGI MIKORIZA
ARBUSKULAR
Nama Mahasiswa : Ramadian Budi Santoso
No. Pokok Mahasiswa : 0614011047
Jurusan : Budidaya Pertanian
Program Studi : Agronomi
Fakultas : Pertanian
MENYETUJUI 1. Komisi Pembimbing
Dr. Ir. Maria Viva Rini, M.Sc. Ir. Sugiatno, M.S. NIP 196603041990122001NIP 196002261986031004
2. Ketua Jurusan Budidaya Pertanian
MENGESAHKAN
1. Tim Penguji
Ketua : Dr. Ir. Maria Viva Rini, M.Sc.
Sekretaris : Ir. Sugiatno, M.S.
Penguji
Bukan Pembimbing : Dr. Ir. Agus Karyanto, M.Sc.
2. Dekan Fakultas Pertanian
Prof. Dr. Ir. Wan Abbas Zakaria, M.S. NIP 196108261987021001
RIWAYAT HIDUP
Penulis dilahirkan di Bandar Lampung pada tanggal 23 April 1988 sebagai putera
kedua dari empat bersaudara pasangan Bapak Sukoco dan Ibu Mariana.
Penulis mengawali pendidikan formal pada tahun 1993 di Taman Kanak-kanak
Pratama Bandar Lampung. Pada tahu 1994, penulis melanjutkan pendidikan dasar di Sekolah Dasar Negeri 1 Kampung Sawah Lama Bandar Lampung,
Sekolah Lanjutan Tingkat Pertama Negeri 5 Bandar Lampung pada tahun 2000, dan Sekolah Menengah Atas Perintis Bandar Lampung pada tahun 2003. Tahun 2006 penulis menjadi mahasiswa Fakultas Pertanian Jurusan Budidaya Pertanian
Program Studi Agronomi Universitas Lampung melalui jalur Seleksi PenerimaanMahasiswa Baru (SPMB).
Selama menjadi mahasiswa, penulis aktif dalam organisasi kemahasiswaan diantaranya menjadi pengurus dalam Himpunan Mahasiswa Budidaya Pertanian
(Himadita) Fakultas Pertanian Universitas Lampung pada tahun 2007, pengurus Badan Ekskutif Mahasiswa (BEM) Fakultas Pertanian pada tahun 2007. Penulis
juga tergabung dalam Organisasi Agronomi Pecinta Alam (Agropala) sebagai: 1. Ketua Divisi Kesekretariatan pada tahun 2007.
2. Bendahara Umum pada tahun 2008.
Penulis pernah mengikuti kegiatan kemahasiswaan seperti:
1. Materi Ruang dan Materi Lapang (MRML) Agronomi Pecinta Alam pada tahun 2006.
2. Latihan Dasar (Landas) Agronomi Pecinta Alam (Agropala) pada tahun 2006. 3. Pendakian bersama 5 gunung Lampung pada tahun 2009-2010.
4. Kegiatan Training Organisasi Profesi Budidaya Pertanian (TOP BDP) pada
tahun 2006.
5. Peserta Kemah Pengenalan Lingkungan Budidaya Pertanian (Kenali BDP)
pada tahun 2007.
SANWACANA
Puji syukur penulis panjatkan ke hadirat Allah SWT karena atas izin, rahmat, dan
hidayah-Nya penulis dapat menyelesaikan penelitian dan penulisan skripsi ini. Pada kesempatan ini penulis mengucapkan terima kasih kepada:
1. Ibu Dr. Ir. Maria Viva Rini, M.Sc. selaku ketua tim penguji dan
pembimbing pertama yang telah memberikan kesempatan, bimbingan, arahan, pengetahuan, kesabaran dan saran selama penulis menyelesaikan
penelitian dan skripsi ini.
2. Bapak Ir. Sugiatno, M.S. selaku sekretaris tim penguji dan pembimbing kedua yang telah memberikan arahan, pengetahuan, kesabaran dan saran
selama penulis menyelesaikan penelitian dan skripsi ini.
3. Bapak Dr. Ir. Agus Karyanto, M.Sc. selaku penguji bukan pembimbing yang telah memberikan saran, bantuan, dan arahan untuk perbaikan skripsi
ini.
4. Ibu Ir. Niar Nurmauli, M.S. selaku Pembimbing Akademik yang telah
memberikan arahan dan saran selama menjadi mahasiswa di Jurusan Budidaya Pertanian.
5. Bapak Prof. Dr. Ir. Setyo Dwi Utomo, M.Sc. selaku Ketua Jurusan
6. Bapak Prof. Dr. Ir. Wan Abbas Zakaria, M.S. selaku Dekan Fakultas
Pertanian Unila yang telah mensahkan skripsi ini.
7. Seluruh dosen-dosen Jurusan Budidaya Pertanian yang telah memberikan
pengetahuan dan ilmu yang berharga selama menjadi mahasiswa di Jurusan Budidaya Pertanian.
8. Malaysian Agry Hi Tech atas bantuan dana penelitian yang telah diberikan
sehingga penelitian ini dapat dilaksanakan.
9. Kedua orang tua penulis, Bapak Sukoco dan Ibu Mariana serta
saudara-saudara penulis yang telah memberikan kasih sayang, dukungan dan doa sehingga dapat menyelesaikan penelitian dan skripsi ini.
10.Teman-teman di Laboratorium Mikoriza: Vida Rozalinda, S.P., Triani Wahyuningsih, S.P., Anggun Dewi Puspita Sari, S.P., M.Gary
Warganegara, S.P., Sigit Wahyudi S.P., atas bantuan, saran serta nasehat
kepada penulis.
11.Saudara-saudara seperjuangan (SPX TEAM): Novalim Purlasyanko, Ari Dwinara Januarsyah, Gustiawan dan Virgio Koriyando. Kita dilahirkan
untuk sebuah persahabatan dan persaudaraan.
Penulis berharap skripsi ini dapat bermanfaat bagi kita semua. Kritik dan saran
yang bersifat membangun dan membantu kesempurnaan skripsi ini akan selalu diterima dengan terbuka. Semoga Allah SWT membalas semua kebaikan yang telah diberikan dan semoga skripsi ini dapat bermanfaat.
Bandar Lampung, 31 Januari 2012
V. KESIMPULAN DAN SARAN
5.1 Kesimpulan
Berdasarkan hasil penelitian yang diperoleh, dapat dibuat kesimpulan sebagai berikut:
1. Jumlah tanaman inang 5 tanaman per pot lebih sesuai untuk produksi FMA
karena menghasilkan jumlah spora yang terbanyak dari pada jumlah tanaman inang yang lain.
2. Terjadi peningkatan jumlah spora dari volume pot 200 ml ke volume pot 400
ml, selanjunya setiap peningkatan volume pot akan menurunkan jumlah spora.
3. Volume pot dengan ukuran terkecil yaitu 200 ml lebih sesuai untuk produksi FMA karena menghasilkan persen infeksi dan jumlah spora yang tinggi dibandingkan dengan volume media tanam yang lain.
5.2 Saran
Berdasarkan hasil penelitian, disarankan untuk melakukan penelitian lanjutan dengan menggunakan jenis FMA lainnya yang diharapkan dapat lebih