ABSTRACT
The Study of Organic Acid Addition Against Characteristics of The Ethanolysis Product Of Palm Kernel Oil (PKO) as Emulsifier
By
PAMELIA MERTI ASTUTI
The aims of this research were knowing the effect of organic acids (lactic acid, succinic acid and tartaric acid) in different concentration against pH value, antimicrobial activity and stability of the power emulsion product of etanolisis palm kernel oil (PKO). The experiment method used descriptive method with 3 replications, which consist of 2 factors investigated. The first factors investigated in this research is the kind of organic acids (A) consists of 4 level: (1) without the addition of acid (Control), (2) addition of lactic acid (A1), (3) the addition of succinic acid (A2), and (4) the addition of tartaric acid (A3). The second factors is concentration (K): 10% (K1), 20% (K2), 30% (K3) and 40% (K4) (w/w).
Pamelia Merti Astuti
10.02 mm (S. aureus), and 3.36 mm (natural microbial cultures). Highest value in test of S.cerevisiae were on the addition of 40% of tartaric acid with value is 4.74 mm (S.cerevisiae). The best treatment in the test of the stability of the emulsion were on the addition of lactic acid treatment with range of changes in the power emulsion stability of 13.08% - 13.97%.
ABSTRAK
Kajian Penambahan Asam Organik Terhadap KarakteristikProduk Etanolisis Minyak Inti Sawit (PKO) Sebagai Emulsifier
Oleh
PAMELIA MERTI ASTUTI
Penelitian ini bertujuan untuk mengetahui pengaruh jenis asam organik (asam laktat, asam suksinat dan asam tartarat) dengan konsentrasi berbeda terhadap nilai pH, aktivitas antimikroba dan daya stabilitas emulsi produk etanolisis kasar minyak inti sawit (PKO). Metode penelitian yang digunakan adalah metode deskriptif dengan 3 kali ulangan, terdiri dari dua faktor perlakuan. Faktor perlakuan pertama adalah jenis asam organik (A), terdiri dari 4 taraf: (1) tanpa penambahan asam (Kontrol), (2) penambahan asam laktat (A1), (3) penambahan asam suksinat (A2), dan (4) penambahan asam tartarat (A3). Faktor kedua yaitu konsentrasi (K): 10% (K1), 20% (K2), 30% (K3) dan 40% (K4) (b/b).
Pamelia Merti Astuti
(E. coli), 10,02 mm (S. aureus), dan 3,36 mm (kultur mikroba alami). Pada uji
S.cerevisiae nilai tertinggi terjadi pada perlakuan penambahan asam tartarat 40%
yaitu sebesar 4,74 mm (S.cerevisiae). Perlakuan terbaik pada uji stabilitas emulsi terjadi pada perlakuan asam laktat dengan kisaran perubahan daya stabilitas emulsi 13,08% - 13,97%.
RIWAYAT HIDUP
Penulis dilahirkan di Bandar Lampung pada tanggal 23 Januari 1991, sebagai anak kedua dari tiga bersaudara dari pasangan Bapak Pawit Saridi dan Ibu Haryani.
Pendidikan penulis diawali di Taman Kanak-kanak Bina Harapan yang diselesaikan pada tahun 1997, kemudian melanjutkan Sekolah Dasar di SD Negeri 1 Karang Maritim yang diselesaikan tahun 2003, melanjutkan Sekolah Menengah Pertama di MTsN 1 Tanjung Karang, diselesaikan pada tahun 2006, dan Sekolah Menengah Atas di MAN 1 Bandar Lampung yang diselesaikan pada tahun 2009.
SANWACANA
Puji dan syukur penulis ucapkan ke hadirat Allah SWT, karena atas berkat dan kuasa-Nya penulis dapat menyelesaikan skripsi ini.
Dengan selesainya skripsi ini, penulis mengucapkan terima kasih kepada :
1. Bapak Prof. Dr. Ir. Wan Abbas Zakaria, M.S., selaku Dekan Fakultas Pertanian Universitas Lampung.
2. Ibu Ir. Susilawati, M.S., selaku Ketua Jurusan Teknologi Hasil Pertanian Fakultas Pertanian Universitas Lampung atas izin penelitian yang diberikan. 3. Dr. Ir. Murhadi, M.Si., selaku pembimbing satu skripsi yang telah banyak
memberikan pengarahan, saran dan masukan dalam menyelesaikan skripsi ini.
4. Dr. Sri Hidayati, S.T.P., M.P., selaku pembimbing dua yang telah banyak memberikan pengarahan, saran dan masukan dalam menyelesaikan skripsi ini.
5. Ir. Samsul Rizal, M.Si., selaku penguji yang telah memberikan saran-saran guna terselesaikanya skripsi ini.
6. Ir. Fibra Nurainy, M.T.A., selaku Dosen Pembimbing Akademik yang telah memberikan nasihat dan arahan selama ini.
8. Teman-teman THP angkatan 2010 yang selalu memberikan dukungan serta adik-adik dan kakak-kakak THP FP Unila atas kebersamaan, suka cita dan persahabatan yang luar biasa.
9. Seluruh pihak yang telah membantu penulis selama ini hingga terselesaikannya skripsi ini.
Penulis berharap semoga Allah SWT membalas kebaikan mereka dan semoga laporan skripsi ini dapat memberikan manfaat bagi kita semua.
Bandar Lampung, Desember 2014 Penulis
DAFTAR ISI
Halaman
DAFTAR TABEL ... iii
DAFTAR GAMBAR ... iv
I. PENDAHULUAN ... 1
1.1. Latar Belakang dan Masalah ... 1
1.2. Tujuan Penelitian ... 4
1.3. Kerangka Pemikiran ... 4
1.4. Hipotesis ... 6
II. TINJAUAN PUSTAKA ... 7
2.1. Minyak Inti Sawit (PKO) ... 7
2.2. Etanolisis Trigliserida ... 8
2.3. Antimikroba ... 10
2.4. Emulsi ... 12
2.5. Pengemulsi (emulsifier) ... 13
2.6. Asam Organik ... 15
2.6.1. Asam laktat ... 15
2.6.2. Asam suksinat ... 17
2.6.3. Asam tartarat ... 18
III. BAHAN DAN METODE ... 19
3.1. Tempat dan Waktu Penelitian ... 19
3.2. Bahan dan Alat ... 19
ii
3.4. Pelaksanaan Penelitian ... 20
3.4.1. Persiapan Bahan PKO ... 20
3.4.2. Persiapan Pelarut Etanol-NaOH 1% ... 21
3.4.3. Produksi Produk Etanolisis dari PKO ... 21
3.4.4. Penambahan Asam Organik Pada Produk Etanolisis PKO .. 22
3.4.5. Persiapan Kultur Mikroba ... 23
3.5. Pengamatan ... 24
3.5.1. Pengujian pH ... 24
3.5.2. Pengujian Antivitas Antimikroba ... 24
3.5.3. Pengujian Daya Stabilitas Emulsi Produk Etanolisis kasar PKO dengan Penambahan Asam Organik ... 26
IV. HASIL DAN PEMBAHASAN ... 28
4.1. Derajat Keasaman (pH) ... 29
4.2. Aktivitas Antimikroba ... 31
4.2.1. Aktivitas Antibakteri (E.coli, S. Aureus dan kultur mikroba alami) ... 31
4.2.2. Aktivitas Antikhamir (Saccharomyces cereviciae) ... 35
4.3. Daya Stabilitas Emulsi ... ... 36
V. KESIMPULAN DAN SARAN ... 39
5.1. Kesimpulan ... 39
5.2. Saran ... 39
DAFTAR PUSTAKA ... 40
DAFTAR TABEL
Tabel Halaman
1. Kandungan asam lemak dalam PKO ... 8 2. pH produk etanolisi PKO dengan penambahan asam... 45 3. Aktivitas antimikroba (E.coli) produk etanolisi PKO dengan
penambahan asam ... 46 4. Aktivitas antimikroba (S.aureus) produk etanolisi PKO dengan
penambahan asam ... 48 5. Aktivitas antimikroba (kultur mikroba alami) produk etanolisi PKO
dengan penambahan asam ... 51 6. Aktivitas antimikroba (S. cereviae) produk etanolisi PKO dengan
DAFTAR GAMBAR
Gambar Halaman
1. Tahapan reaksi etanolisis trigliserida (TG) menghasilkan
digliserida (DG), monogliserida (MG), dan etil ester asam lemak ... 9
2. Reaksi pembentukan emulsifier dengan penambahan asam laktat ... 14
3. Struktur kimia lactem dan datem ... 14
4. Struktur kimia asam laktat ... 16
5. Struktur kimia asam suksinat ... 18
6. Struktur kimia asam tartarat... 18
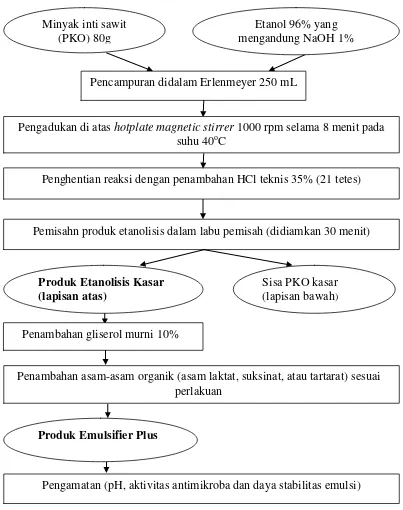
7. Diagram alir produksi produk etanolisis PKOdengan perlakuan penambahan asam organik ... 23
8. Hasil etanolisis PKO ... 28
9. Produk etanolisis dengan penambahan asam ... 29
10. pH produk etanolisis PKO dengan penambahan asam pada berbagai konsentrasi ... 29
11. Zona bening anti-E. coli, S. aureus, kultur mikroba alami dan S. cereviciae pada produk etanolisis PKO dengan penambahan asam organik ... 31
12. Grafik aktivitas anti-E. coli dan aktivitas anti-S. aureus pada produk etanolisis PKO dengan penambahan asam organik pada berbagai konsentrasi ... 32
v
15. Produk emulsi santan (w/o) dengan penambahan produk (produk etanolisis PKO dengan penambahan asam organik
sebanyak 5% (b/b) ... 36
16. Grafik perubahan stabilitas emulsi santan (w/o) dengan penambahan produk sebanyak 5% (b/b) ... 37
17. Proses etanolisis PKO ... 59
18. Proses penambahan asam organik pada produk etanolisis PKO ... 60
I. PENDAHULUAN
1.1. Latar Belakang dan Masalah
Indonesia merupakan salah satu negara penghasil kelapa sawit terbesar di dunia dengan volume ekspor minyak kelapa sawit mencapai16,436 juta ton pada tahun 2012 (Ditjen Perkebunan, 2012). Harga minyak sawit mentah (Crude Palm Oil/CPO) dan produk turunannya di pasar internasional diprediksi mampu menembus US$ 1.100 per ton pada tahun 2014. Nilai ini diperkirakan akan terus mengalami peningkatan seiring dengan meningkatnya kebutuhan dunia akan minyak kelapa sawit dan turunannya (Dahono, 2014).
2
produksi sebesar 173.376 ton pada tahun 2012 (Badan Pusat Statistik Provinsi Lampung, 2014).
3
Menurut penelitian sebelumnya diketahui bahwa produk etanolisis PKO memiliki daya aktivitas antimikroba cukup tinggi, dengan menggunakan mikroba uji
S.aureus, B.cereus dan E. coli diperoleh zona hambat rata-rata: 24, 25 mm; 21, 28
mm dan 22,22 mm. Namun memiliki daya stabilitas emulsi kurang optimal terutama produk emulsi minyak dalam air (o/w) (Rahman, 2010), karena itu perlu dilakukan penambahan asam organik untuk meningkatkan aktivitas antimikroba dan stabilitas emulsi penambahan asam organik juga berfungsi sebagai pengawet karena umumnya asam organik termasuk dalam golongan asam lemah yang dapat bersifat sebagai pengawet pangan.
4
1.2. Tujuan Penelitian
Tujuan penelitian ini untuk mengetahui pengaruh jenis asam organik (asam laktat, asam suksinat dan asam tartarat) dan konsentrasi terhadap nilai pH, aktivitas antimikroba dan daya stabilitas emulsi produk etanolisis kasar minyak inti sawit (PKO).
1.3. Kerangka Pemikiran
5
dan antibakteri relatif tinggi dihasilkan pada suhu optimum 40oC dengan nisbah etanol 95% NaOH 1% terhadap PKO = 1,6 (v/b) selama 8 menit.
Produk hasil etanolisis menghasilkan dua lapisan yang terdiri dari lapisan atas (produk yang berwarna kuning cerah) dan lapis bawah (produk yang berwarna putih keruh). Menurut Murhadi (2010), produk mono-digliserida yang dihasilkan dari PKO memiliki aktivitas antibakteri terutama terhadap S. aureus dan E. coli
dengan diameter zona hambat antara 5,91 mm – 7,16 mm/10 mg ekstrak dan 5,07 mm – 8,33 mm/10 mg ekstrak (Lestari dan Murhadi, 2008). Daya aktivitas anti bakteri yang tinggi dalam produk etanolisis PKO ini utamanya disebabkan oleh kandungan asam laurat dalam minyak inti sawit.
6
organik adalah substansi antimikrobial yang telah diakui oleh FDA sebagai bahan tambah makanan yang aman, dapat memperpanjang masa simpan produk dan menghambat proses kerusakan bahan pangan.
Sejauh ini pembuatan emulsifier dengan tambahan asam organik umumnya mengunakan bahan baku MG murni berdasarkan Paten Kanada dengan Nomor Paten Lactem WO 2004105508 A1 (2003), dengan menggunakan bahan baku berbeda yaitu produk etanolisis PKO yang mengandung MG-DG diduga akan mempengaruhi karakteristik produk sebagai emulsifier selain itu penambahan asam organik juga diduga dapat bersifat sebagai pengawet pada produk. Karena itu penelitian ini dilakuan untuk mengkaji pengaruh jenis asam dan konsentrasi terhadap karakteristik produk etanolisis PKO.
Penelitian ini dilakukan dengan perlakuan penambahan asam organik yaitu: asam laktat, asam suksinat dan asam tartarat. Ketiga jenis asam tersebut digunakan karena memiliki berat molekul yang hampir sama dan umum digunakan sebagai bahan tambah pangan. Pengamatan yang dilakukan meliputi: pH, aktivitas antimikroba dan daya stabilitas emulsi.
1.4. Hipotesis
II. TINJAUAN PUSTAKA
2.1. Minyak Inti Sawit (PKO)
Minyak inti sawit merupakan hasil pengolahan biji inti sawit dengan cara ekstraksi terutama secara mekanis (mechanical extraction). Metode ekstraksi dilakukan dengan menggunakan mesin screw press (press ulir), hasil dari ekstraksi ini kemudian ditampung dalam bak penampungan yang kemudian dilanjutkan dengan proses penyaringan menggunakan oil filter. Setelah diperoleh minyak inti sawit kemudian dilakukan analisis mutu produk, hal ini bertujuan agar produk yang dihasilkan sesuai dengan standar yang ditentukan analisis mutu minyak inti sawit meliputi analisis kadar air (maks 0,5%), kadar kotoran (maks 0,05%), kadar FFA (maks 5,00%) dan bilangan peroksida (maks 2,2 meq) (Herlinda, 2003).
8
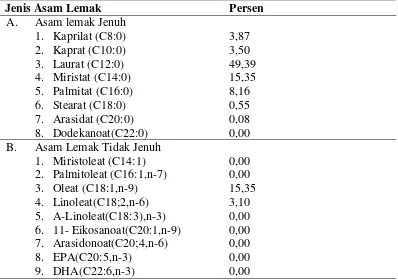
Tabel 1. Kandungan asam lemak dalam PKO
Jenis Asam Lemak Persen
A. Asam lemak Jenuh 1. Kaprilat (C8:0) 2. Kaprat (C10:0) 3. Laurat (C12:0) 4. Miristat (C14:0) 5. Palmitat (C16:0) 6. Stearat (C18:0) 7. Arasidat (C20:0) 8. Dodekanoat(C22:0) 3,87 3,50 49,39 15,35 8,16 0,55 0,08 0,00 B. Asam Lemak Tidak Jenuh
1. Miristoleat (C14:1) 2. Palmitoleat (C16:1,n-7) 3. Oleat (C18:1,n-9) 4. Linoleat(C18;2,n-6) 5. A-Linoleat(C18:3),n-3) 6. 11- Eikosanoat(C20:1,n-9) 7. Arasidonoat(C20;4,n-6) 8. EPA(C20:5,n-3) 9. DHA(C22:6,n-3) 0,00 0,00 15,35 3,10 0,00 0,00 0,00 0,00 0,00 Sumber: Murhadi (2010).
2.2. Etanolisis Trigliserida
9
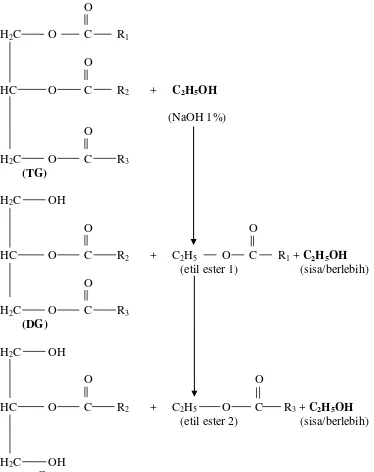
ester ketiga dari posisi asam lemak ke-2/ sn-2 (Hasanuddin dkk., 2003). Tahapan reaksi etanolisis trigliserida (TG) dapat dilihat pada Gambar 1.
O H2C O C R1
O
HC O C R2 + C2H5OH
(NaOH 1%) O
H2C O C R3 (TG)
H2C OH
O O
HC O C R2 + C2H5 O C R1 + C2H5OH
(etil ester 1) (sisa/berlebih) O
H2C O C R3 (DG)
H2C OH
O O
HC O C R2 + C2H5 O C R3 + C2H5OH
(etil ester 2) (sisa/berlebih)
H2C OH
(MG)
Gambar 1. Tahapan reaksi etanolisis trigliserida (TG) menghasilkan digliserida (DG), monogliserida (MG), dan etil ester asam lemak (Hasanuddin
10
2.3. Antimikroba
MG yang dihasilkan oleh inti sawit selain dapat berfungsi sebagai emulsifier juga dapat berfungsi sebagai senyawa antimikroba. Menurut Davidson dan Branen (1993) dalam Anggasari (2005) senyawa antimikroba adalah jenis bahan tambahan makanan yang digunakan dengan tujuan untuk mencegah kebusukan atau keracunan oleh mikroorganisme pada bahan pangan. Beberapa jenis senyawa yang mempunyai aktivitas antimikroba adalah sodium benzoate, senyawa fenol, asam-asam organik, asam lemak rantai medium dan esternya, sorbat, sulfur dioksida dan sulfit, nitrit, senyawa kolagen dan surfaktan, dimetil karbonat dan metal askorbat (Luthanan, 2008). Zat antimikroba dapat bersifat bakterisidal (membunuh bakteri), bakteristatik (menghambat pertumbuhan bakteri), fungisidal (membunuh kapang), fungistatik (menghambat pertumbuhan kapang), dan germisidal (menghambat germinasi spora bakteri) (Fardiaz, 1992).
11
antibakteri. Berdasarkan spektrum aksinya, zat antibakteri dibagi menjadi tiga yaitu:
1. Spektrum luas; zat antibakteri yang efektif melawan prokariot baik membunuh atau menghambat bakteri Gram positif dan Gram negatif dalam ruang lingkup yang luas.
2. Spektrum sempit; zat antibakteri yang efektif melawan sebagian bakteri Gram positif atau Gram negatif.
3. Spektrum terbatas; zat antibakteri yang efektif melawan satu spesies bakteri tertentu.
12
Sehubungan dengan aktivitas antimikroba asam-asam lemak dari sumber minyak/lemak tanaman. Diketahui bahwa: (1) Lemak atau Trigliserida, tidak memiliki penghambatan terhadap mikroba, kecuali yang mengandung asam-asam lemak berantai karbon rendah-sedang terutama dalam bentuk monogliserida; (2) Secara umum, asam lemak jenuh yang paling efektif sebagai senyawa antibakteri adalah asam laurat (12:0) dalam bentuk monolaurin, sedangkan untuk asam lemak tidak jenuh tunggal dan asam lemak tidak jenuh ganda/jamak, masing-masing adalah asam palmitoleat (16:1) dan asam linolenat (18:3) relatif tidak memiliki sifat antimikroba; (3) Letak dan jumlah ikatan rangkap pada asam lemak C12-C22 lebih mempengaruhi aktivitas mikroba asam lemak tersebut, dibandingkan pada asam lemak dengan jumlah atom C kurang dari 12; (4) Konfigurasi geometri struktur asam lemak yang aktif (antimikroba) adalah bentuk cis, sementara bentuk isomer trans tidak aktif; dan (5) Asam lemak dalam bentuk ester alkohol monohidrat mengakibatkan inaktivasi antibakteri, sementara dalam bentuk ester polizol atau gliserol dapat meningkatkan aktivitas antibakterinya (Kabara, 1984 dalam Maulidha, 2014 ).
2.4. Emulsi
13
terlihat seolah-olah salah satu fase berada dalam fase yang lainnya. Bila proses pengocokan dihentikan, maka dengan sangat cepat akan terjadi pemisahan kembali menjadi dua fase yang terpisah (Ibnuhayan, 2008). Terdapat dua jenis utama emulsi yaitu emulsi minyak dalam air (oil in water, o/w) misalnya susu, es krim dan emulsi air dalam minyak (water in oil, o/w) misalnya margarine dan mentega (Hartomo dan Widiatmoko, 1993). Menurut Winarno (1992), emulsi adalah suatu dispersi atau suspensi suatu cairan dalam cairan yang lain, dimana molekul-molekul kedua cairan tersebut tidak saling berbaur tetapi saling antagonistik.
2.5. Pengemulsi (emulsifier)
Emulsifier adalah suatu bahan dengan karakteristik khusus yang dapat
menyatukan air dengan minyak (Haryadi, 2007). Menurut Krog (1990),
emulsifier didefinisikan sebagai senyawa yang mempunyai aktivitas permukaan
(surface-active agents) sehingga dapat menurunkan tegangan permukaan (surface
tension) antara udara-cairan dan cairan-cairan yang terdapat dalam satu sistem makanan. Kemampuannya dalam menurunkan tegangan permukaan disebabkan
emulsifier memiliki struktur kimia yang mampu menyatukan dua senyawa yang
14
yang menggunakan campuran air dan minyak menggunakan emulsifier, seperti margarin, mayonnaise, obat-obatan dan kosmetik (Haryadi, 2007).
Menurut Fennema (1985) asam organik dapat digunakan dalam pembentukan
emulsifier. Reaksi pembentukan emulsifier dapat dilihat pada Gambar 2.
CH2OH CH3 CH2–OCO –R
RCOOH + CHOH + CHOH CHOH
[image:30.595.113.492.208.335.2]CH2OH COOH CH2 –OCO –CHOH –CH3 Asam lemak Gliserol Asam laktat laktat monogliserol Gambar 2. Reaksi pembentukan emulsifier dengan penambahan asam laktat (Sumber: Fennema, 1985).
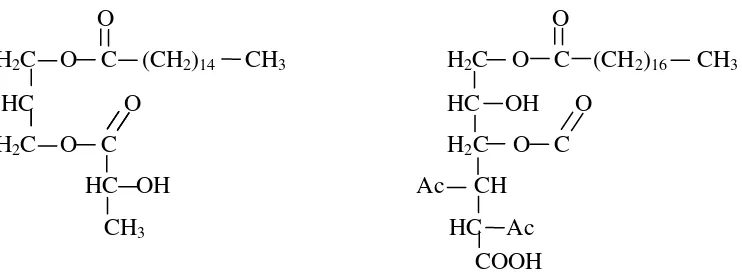
Beberapa produk emulsifier dapat dibuat dari proses hidrogenasi minyak sawit, misalnya lactem dan ester diacetyl tartaric acid monogliserida (DATEM). Lactem adalah ester dari asam laktat dan mono-digliserida (MG-DG) minyak sawit, dan datem adalah ester dari asam tartarat dengan (MG-DG) minyak sawit. Struktur kimia lactem dan datem dapat dilihat pada Gambar 3.
O O
H2C O C (CH2)14 CH3 H2C O C (CH2)16 CH3
c
HC O HC OH O H2C O C H2C O C HC OH Ac CH
CH3 HC Ac COOH
[image:30.595.116.487.552.691.2]15
2.6. Asam Organik
Asam organik merapakan sejenis asam yang merupakan senyawa organik yang dapat melepasakan ion H+ dalam larutannya. Senyawa organik merupakan senyawa yang mengandung atom karbon yang senyawanya diperoleh dari makhluk hidup (Anonim, 2009). Asam organik dikenal sebagai bakteriostatik (zat yang dapat menghambat pertumbuhan bakteri) maupun bakterisidal (zat yang dapat membunuh bakteri). Karena kemampuannya tersebut, asam-asam organik sering digunakan sebagai bahan pengawet. Asam-asam organik yang sering digunakan sebagai bahan pengawet adalah asam asetat, asam laktat, asam propionat, asam benzoat, asam sorbat, asam sitrat, dan turunan-turunannya (Nychas, 1995 dalam Ferdiani, 2008).
2.6.1. Asam laktat
Asam laktat atau yang sering disebut dengan 2-hydroxypropanoic acid, CH3CH(OH)COOH merupakan asam hidroksi organik yang paling sederhana dengan atom karbon tidak simetris yang tersebar secara luas di alam yang memiliki sifat multifungsi dan potensial diproduksi dalam jumlah besar. Senyawa ini termasuk asam lemah dengan daya penguapan yang rendah. Asam laktat diperoleh dari hasil fermentasi gula (glukosa) oleh bakteri asam laktat. Bakteri asam laktat merupakan bakteri gram-positif yang tidak membentuk spora dan dapat memfermentasikan karbohidrat menjadi asam laktat contohnya bakteri
16
a. Sifat Fisika
Asam laktat memiliki berat molekul 90,08 dan Specific gravity 1,249. Titik didihnya 125-140oC pada 27 kPa sedangkan titik lelehnya adalah 52,7-52,8oC. Asam laktat memiliki bentuk liquid dan asam laktat tidak memiliki warna dan juga aroma. Kelarutan dari asam laktat yakni larut dalam air, etanol, dietil eter dan pelarut organik lainya yang dapat larut dengan air. Akan tetapi asam laktat tidak larut dalam benzene dan kloroform.
b. Sifat Kimia
Asam laktat merupakan asam karboksilat dengan rumus molekul C3H6O3 (CH3.CHOH.COOH). Asam laktat memiliki gugus hidroksil berdekatan dengan gugus asam karboksilat, sehingga membentuk sebuah alpha hydroxyl acid (AHA). Asam laktat dalam larutan dapat melepaskan sebuah proton dari gugus asam yang menghasilkan ion lactate CH3(OH)COO dan memiliki dua isomer optikal yaitu L(+)-lactic acid dan D(-)_lactic acid.
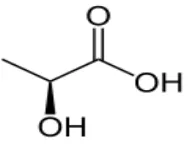
[image:32.595.266.360.567.640.2]Dalam air, ia terlarut lemah dan melepas proton (H+), membentuk ion laktat. Asam ini juga larut dalam alkohol dan bersifat menyerap air (higroskopik).
Gambar 4. Struktur kimia asam laktat (Sumber: Anonim, 2013a).
)-17
laktat. Hanya isomer yang pertama (S) aktif secara biologi. Asam laktat memiliki densitas sebesar 1.206 g/mL (25oC) dengan pKa 3,86 (25oC) dan memiliki kelarutan dalam air sebesar 10 mg/mL, asam laktat juga mampu larut dalam etanol dalam segala perbandingan (Anonim, 2013a).
Selain memiliki sifat fisika dan kimiawi diatas asam laktat juga mempunyai banyak sekali fungsi dan kegunaan diantaranya garam kalsium dari asam laktat di produksi dalam bentuk granular atau serbuk, digunakan sebagai sumber kalsium diet dan zat pembeku darah dan juga sebagai bahan penolong industri antibiotik dan berfungsi buffer pada sediaan farmasi. Asam laktat dalam bentuk ester digunakan sebagai bahan pengemulsi makanan yang dipanggang pada industri roti, biscuit dan juga sebagai bahan perasa asam makanan, dalam dunia pertanian juga memiliki banyak fungsi misalnya dipakai pada industri pestisida, herbisida dan fungisida (Febriana, 2011).
2.6.2. Asam suksinat
18
Gambar 5. Struktur kimia asam suksinat(Sumber: Anonim, 2014).
2.6.3. Asam tartarat
Asam tartarat (HO2CCH(OH)CH(OH)CO2H) merupakan senyawa organik turunan asam askorbat, seperti asam oksalat dan asam treonat. Asam tartarat memiliki 4 gugus hidroksil dan merupakan salah satu asam primer yang dijumpai pada anggur selain asam malat dan asam sitrat. Asam tartarat memiliki dua buah ikatan rangkap pada struktur kimianya memiliki masa molekul 150,087 g/mol dengan densitas 1,79 g/ml (H2O) dengan titik lebur 171-174oC dan kelarutan dalam air sebesar 133g/100 ml (20oC) dan memiliki nilai pKa 2,95. Struktur kimia asam tartarat dapat dilihat pada Gambar 6.
[image:34.595.251.376.500.561.2]III. BAHAN DAN METODE
3.1. Tempat dan Waktu Penelitian
Penelitian ini dilaksanakan di Laboratorium Analisis Hasil Pertanian Jurusan Teknologi Hasil Pertanian, Fakultas Pertanian, Universitas Lampung pada bulan Januari 2014 – Desember 2014.
3.2. Bahan dan Alat
Bahan baku yang digunakan dalam penelitian ini adalah PKO yang diperoleh langsung dari industri pengolahan minyak inti sawit di Ganjar Agung Metro, Lampung. Bahan lain yang digunakan yaitu asam laktat, asam suksinat, asam tartarat, gliserol, buah kelapa tua (untuk pengujian daya stabilitas emulsi produk etanolisis PKO). Bahan kimia yang digunakan terdiri dari etanol teknis 96%, etanol absolute, HCl 35%, NaOH 1% dan akuades. Kultur mikroba yang digunakan dalam penelitian ini yaitu Escherichia coli (Bakteri Gram negatif ATCC 25922), Staphylococcus aureus (bakteri Gram positif), Sacharomyces
cerevisiae dan campuran kultur mikroba alami. Media yang digunakan adalah
NA (Nutrient Agar) dan NB (Nutrient Broth).
20
petri, mikropipet, lampu bunsen, jarum ose, jangka sorong, timbangan analitik, thermometer, pH meter, sentrifuse 4000 rpm dan alat-alat gelas penunjang.
3.3. Metode Penelitian
Penelitian ini menggunakan metode deskriptif dengan 3 kali ulangan dan terdiri dari dua faktor perlakuan. Faktor perlakuan pertama adalah jenis asam organik (A), terdiri dari 4 taraf: (1) tanpa penambahan asam (kontrol) (2) penambahan asam laktat, (3) penambahan asam suksinat, dan (4) penambahan asam tartarat. Faktor perlakuan kedua yaitu konsentrasi (K): 10%, 20%, 30% dan 40%. Data yang diperoleh disajikan dalam bentuk tabel kemudian dibahas secara deskriptif.
3.4. Pelaksanaan Penelitian
Pelaksanaan penelitian ini dilakukan dalam empat tahap yang meliputi: (1) Persiapan bahan PKO, (2) Persiapan Pelarut Etanol-NaOH, (3) Produksi produk etanolisis PKO dan (4) Kajian penambahan asam organik pada produk etanolisis PKO. Pengamatan terdiri dari pH, pengujian aktivitas antimikroba, dan daya stabilitas emulsi pada produk emulsi (o/w) (Malik dkk., 1987; Murhadi dan Zuidar, 2009).
3.4.1. Persiapan bahan PKO
21
3.4.2. Persiapan pelarut Etanol–NaOH 1%
Pelarut etanol-NaOH 1% adalah bahan yang digunakan untuk produksi produk etanolisis kasar. Nisbah etanol yang telah mengandung NaOH 1% terhadap PKO yang digunakan adalah 1,6 (v/b) berdasarkan penelitian sebelumnya (Murhadi dan Zuidar, 2009). Sebelumnya NaOH ditimbang sesuai dengan yang dibutuhkan yaitu 0,8 gram. Reaksi etanolisis pada penelitian ini menggunakan etanol 96%, sedangkan etanol yang tersedia adalah etanol 100% sehingga dilakukan pengenceran menggunakan akuades (4/100 x 128 mL = 5,12 mL akuades di dalam 122,88 mL etanol 100%).
Pelarut etanol-NaOH 1% dibuat dengan cara mencampurkan akuades dengan NaOH yang telah ditimbang, dalam gelas beker secara perlahan-lahan karena akan menimbulkan panas. Larutan yang telah mengandung NaOH 1% dan akuades kemudian ditambahkan etanol dan di campur hingga homogen. Pelarut tersebut disimpan di dalam botol kaca dan digunakan sebagai bahan untuk proses etanolisis.
3.4.3. Produksi produk etanolisis dari PKO
22
meneteskan sebanyak 21 tetes larutan HCl 35%. Campuran produk reaksi dimasukan ke dalam labu pemisah dan dibiarkan selama 30 menit, sehingga telah terlihat jelas pemisahan antar lapisan. Lapisan atas (produk etanolisis kasar, berwarna putih kuning pucat) dipisahkan dari lapisan bawah (sisa PKO dll, berwarna kuning cerah). Secara fisik lapisan atas (bahan baku) berbentuk cair sedangkan lapisan bawah berbentuk semi padat (gel). Produksi produk etanolisis PKO tersebut dilakukan sebanyak 8 kali untuk mendapatkan produk etanolisis PKO yang cukup untuk penelitian tahap berikutnya. Seluruh lapisan atas yang diperoleh digabung sebagai produk etanolisis kasar dari PKO dan digunakan sebagai bahan baku tahap berikutnya.
3.4.4. Penambahan asam organik pada produk etanolisis PKO
23
Gambar 7. Diagram alir produksi etanolisis PKO dengan perlakuan penambahan asam organik (Sumber : Murhadi dkk., 2010 (dimodifikasi)).
3.4.5. Persiapan kultur mikroba
Kultur bakteri Staphylococcus aureus (bakteri Gram positif), bakteri Escherichia coli Gram negatif (bakteri Gram negatif ATCC 25922), Sacharomyces cerevisiae
Minyak inti sawit (PKO) 80g
Etanol 96% yang mengandung NaOH 1%
Pencampuran didalam Erlenmeyer 250 mL
Pengadukan di atas hotplate magnetic stirrer 1000 rpm selama 8 menit pada suhu 40oC
Penghentian reaksi dengan penambahan HCl teknis 35% (21 tetes)
Pemisahn produk etanolisis dalam labu pemisah (didiamkan 30 menit)
Penambahan gliserol murni 10%
Penambahan asam-asam organik (asam laktat, suksinat, atau tartarat) sesuai perlakuan
Pengamatan (pH, aktivitas antimikroba dan daya stabilitas emulsi) Produk Etanolisis Kasar
(lapisan atas)
Sisa PKO kasar (lapisan bawah)
24
dan campuran kultur mikroba alami diambil sebanyak satu mata ose dari biakan agar miring atau stok kultur untuk dibiakan kembali (penyegaran) dalam agar miring baru (NA), lalu diinkubasi pada suhu 37oC selama 24 jam. Stok agar miring tersebut disimpan dalam lemari pendingin sebagai stok bakteri dan khamir.
3.5. Pengamatan
3.5.1. Pengujian pH
Pengujian pH dilakukan dengan menggunakan pH meter dengan cara memasukan pH meter kedalam produk etanolisi PKO pada masing–masing perlakuan. Sebelumnya pH meter telah dikalibrasi terlebih dahulu. Nilai yang tercantum dalam pH meter merupakan nilai pH sampel yang diuji, kemudian diamati dan dicatat nilainya.
3.5.2. Pengujian aktivitas antimikroba
25
(NA, 44-45oC) steril, dikocok merata dan dibiarkan sampai membeku. Selanjutnya dibuat 2-4 lubang (sumur) secara aseptis dengan diameter sumur 6.0 mm, kedalam tiap lubang, diinokulasi dengan 60 µL produk etanolisis PKO dengan penambahan asam organik dan produk etanolisis PKO tanpa penambahan asam sebagai kontrol.
Zona penghambatan yang diukur adalah radius (r, mm) penghambatan berupa areal bening di sekeliling sumur uji, setelah diinkubasi selama 24 jam pada suhu 37oC. Pengukuran jari-jari (r, mm) zona hambat di sekeliling sumur uji dilakukan dengan cara mengukur jarak dari tepi sumur uji ke batas lingkaran zona hambat menggunakan jangka sorong (ketelitian 0.01 mm) pada beberapa sisi sumur uji, lalu dirata-ratakan. Selanjutnya dengan asumsi tinggi atau tebal media agar di dalam cawan petri uji adalah sama (9,0 cm) dan volume media agar cair yang ditambahkan sama (20 mL), maka perhitungan diameter zona hambat riil dapat menggunakan konsep dimensi luas lingkaran (dua dimensi). Perhitungannya sebagai berikut (Murhadi, 2010):
1. Dihitung luas kotor (L1, mm2) lingkaran areal bening akibat daya hambat bakteri uji disekeliling sumur uji dengan persamaan luas :
L1= π. r12, dimana r1 = rp + rs
rp = jarak dari lingkaran luar sumur ke lingkaran terluar areal bening di sekeliling sumur uji (mm),
rs = jari-jari sumur uji (mm),
π = 3,14
26
L2= π. r22, dimana r2 = rk + rs
rk = jarak dari lingkaran luar sumur ke lingkaran terluar areal bening di sekeliling sumur uji (mm) akibat daya hambat/pengencer organik,
rs = jari-jari sumur uji (mm),
π = 3,14
3. Dihitung luas bersih (L3, mm2) dengan persamaan : L3 = L1 - L2 4. Dihitung jari-jari zona hambat riil (rr, mm) dengan persamaan :
rr= √(L3/3,14)
5. Dihitung nilai diameter zona hambat riil (dr, mm) dengan persamaan : dr = 2. rr
Akhirnya dapat dihitung nilai diameter zona hambat hasil konversi (dc, mm) dengan persamaan : dc = 2. rc
3.5.3. Pengujian daya stabilitas emulsi produk etanolisis kasar PKO dengan penambahan asam organik
Pengujian daya stabilitas pengemulsi produk santan kelapa segar (kental) yang ditambahkan dengan produk etanolisis kasar PKO, dilakukan dengan mengukur stabilitas emulsi secara pemusingan dengan sentrifuge (Murhadi dan Suharyono, 2008). Pembuatan santan kelapa kental dilakukan sebagai berikut: santan kelapa kental dibuat dengan cara meremas-remas parutan kelapa tua sebanyak 1 kg di dalam 500 mL air hangat (sebelumnya dididihkan), lalu disaring.
27
dengan penambahan asam organik sebanyak 5% (v/v) ke dalam tabung pemisah (sentrifuge). Selanjutnya semua tabung sampel dihomogenkan dengan alat
vorteks. Semua tabung (perlakuan) dimasukkan ke dalam penangas air pada suhu
konstan 70oC selama 30 menit, lalu dipusing selama 45 detik pada kecepatan 1000 rpm (Murhadi dan Suharyono, 2008).
Fraksi minyak yang terpisah (sebagai santan/krim dan skim/air) diukur volumenya untuk digunakan dalam penentuan stabilitas emulsi relatif menggunakan persamaan berikut:
Stabilitas emulsi (%) =
V. KESIMPULAN DAN SARAN
5.1. Kesimpulan
Berdasarkan penelitian dan pembahasan yang telah dilakukan maka dapat diambil kesimpulan, yaitu :
1. pH terendah produk etanolisis PKO dengan penambahan asam organik didapatkan pada perlakuan penambahan asam tartarat 40% yaitu 1,60. 2. Zona hambat uji aktivitas antimikroba (E.coli, S.aureus dan kultur) paling
besar di dapatkan pada perlakuan dengan penambahan asam suksinat 40% yaitu sebesar 9,59 mm, 10,2 mm dan 3,36 mm. Zona hambat uji aktivitas antikhamir (S. Cereviciae) paling besar besar di dapatkan pada perlakuan dengan penambahan asam tartarat 40% yaitu sebesar 4,74 mm.
3. Daya stabilitas emulsi santan paling tinggi adalah pada perlakuan dengan penambahan asam laktat yaitu 11,68%–13,97%.
5.2. Saran
DAFTAR PUSTAKA
Anggasari, H.D. 2005. Kajian Lama Reaksi Gliserolisis Terhadap Rendemen Massa dan Sifat Antimikroba Monogliserol (MAG) dari Minyak Inti Sawit. (Skripsi). Teknologi Hasil Pertanian. Universitas Lampung. Bandar Lampung.
Anonim. 2009. Jenis-Jenis Asam. http://kimia.upi.edu/utama/bahanajar/kuliah web/2009/0700751/jenis.htm. Diakses pada tanggal 11 Oktober 2013. Anonim. 2013a. Asam Laktat. http://id.wikipedia.org/wiki/Asam_laktat. Diakses
23 Oktober 2013.
Anonim. 2013b. Asam Tartarat. http://id.wikipedia.org/wiki/Asam_tartarat. Diakses 23 Oktober 2013.
Anonim. 2014. Succinic acid. http://en.wikipedia.org/wiki/Succinic_acid. Diakses 20 Juli 2014.
Badan Pusat Statistik Provinsi Lampung. 2014. Potensi Kelapa Sawit di Lampung. http://regionalinvestment.bkpm.go.id/newsipid/id/commodit yar ea php?ic=2&ia=18. Bandar Lampung 9 Mei 2014. Diakses 12 Mei 2014.
Branen, L.A. and P.M. Davidson. 1983. Antimicrobials in Foods. Marcel Dekker., Inc. New York.p: 1640-2008.
Buckle, K.A.,R.A. Edwards, G.H. fleet and M.Wooton. 1987. Ilmu Pangan. Diterjemahkan oleh Purnomo dan Aldino. UI-Press. Jakarta. 365 hlm. Dahono, Y. 2014. Prospek Industri Kelapa Sawit 2014 Makin Cerah. http://www.
beritasatu.com/ekonomi/168340-prospek-industri-kelapa-sawit2014 makin-cerah.html. 26 Februari 2014. Diakses pada tanggal 23 Maret 2014.
Davidson, P.M. and A.L. Branen. 1993. Antimicrobials in Foods. Marcel dekker.,inc. New York. 675 pp.
41
indonesia-927. Jakarta 12 September 2012. Diakses pada tanggal 11 Oktober 2013.
Fardiaz, S. 1989. Mikrobiologi Pangan. Bogor: Pusat Antar Universitas Pangan dan Gizi. Institut Pertanian Bogor.
Fardiaz, S. 1992. Mikrobiologi Pangan I. Gramedia Pustaka Utama. Jakarta. 106 hlm.
Febrina, D. P. 2012. Sifat Asam Laktat. http://blog.ub.ac.id/febrina/2012/06/08/ Diakses tanggal 18 Desenber 2013.
Ferdiani, I. 2008. Pengaruh Pencelupan Asam Organik Terhadap Mutu Sensori dan Umur Simpan Mie Basah Matang pada Suhu Ruang. (Skripsi). IPB. http://reporsitoryipb.com/. Diakses pada tanggal 11 Oktober 2013.
Fennema, O.R. 1985. Food Chemistry (2nd). Marcel Dekker, Inc. New York. 991 pp.
Friberg, S., Larsson, K. and Sjoblom, J. 2003. Food Emulsions (4nd) CRC Press.
(e-Book). http://books.google.co.id/books?id=2XvHZtRRA7sC&dq=
lactem&hl=id&source=gbs_navlinks_s. Diakses 17 September 2014. Haryadi, P. 2007. Produksi Minyak Sawit yang Berkelanjutan sebagai Bahan
Dasar untuk Bahan Bakar Bio (Biofuel). IPB. Bogor. 3 hlm.
Hartomo, A.J. dan M.C. Widiatmoko. 1993. Emulsi dan Pangan Instan Ber-lesitin. Andi offset. Yogyakarta. 74 hlm.
Hasanuddin, A., Mappiratu, dan G.S. Hutomo, 2003. Pola Perubahan Mono dan Diasilgliserol dalam Reaksi Etanolisis Minyak Sawit Mentah. Jurnal Teknologi dan Industri Pangan. XIV(3): hlm 241-246.
Herlinda, 2003. Mempelajari Analisis Mutu Minyak Inti Sawit (PKO) dalam Proses Pengolahan Minyak Inti Sawit di PT. Sinar Jaya Inti Mulya Kodya Metro. Laporan PU Jurusan THP. Fakultas Pertanian UNILA. Bandar Lampung.
Ibnuhayan. 2008. Emulsi Kimia Koloid. Komunitas Bloger Palembang. 4 hlm. Diakses tanggal 18 Desenber 2013.
42
Krog, N.J. 1990. Food Emulsifier and Their Chemical and Physical Properties. In Food Emulsions, (ED) K. Larsson are S.E. Friberg. P. Marcel Dekker, New York. 127-180.
Lestari, M dan Murhadi. 2008. Pengaruh Nisbah Etanol-PKO dan Waktu Reaksi terhadap Rendemen dan Aktivitas Produk Etanolisis Minyak Inti Sawit (PKO). Jurnal Tek. dan Industri Hasil Pertanian. 13(2): 95-107.
Liang, T. 2009. Seluk Beluk Kelapa Sawit Bab VIII. Produk dan Standarisasi. PT. Harapan Sawit Lestari, Kab. Ketapang. Kalimantan Barat.15 hlm.
Luthanan, K.Y. 2008. Antibakteri. Brawijaya University Wordpress. Malang 2.html. http://yongkikastanyaluthana.wordpress.com/. Diakses tanggal 30 Desember 2013.
Malik, D., D. Fardiaz dan B.S.L. Jenie. 1987. Pengaruh Karboksimetil Selulosa Terhadap Kestabilan Emulsi dan Mutu Krim Kelapa. Media Teknologi Pangan 3(1-2): 62.
Maulidha, N. 2014. Kajian Fraksinasi Dingin Terhadap Aktivitas Antimikroba dan Daya Emulsi Fraksi Produk Etanolisis dari Campuran CPO dan PKO. (Skripsi). Teknologi Hasil Pertanian. Universitas Lampung. Bandar Lampung.
Murhadi dan Suharyono AS. 2008. Kajian Aktivitas Antibakteri Produk Etanolisis dari Campuran Minyak Inti Sawit (Elaeis guineensis Jacq.) dan Minyak Biji Mengkudu (Morinda citrifolia L.). Jurnal Teknologi dan Industri Hasil Pertanian. Universitas Lampung. Bandar Lampung. Hlm 47-58. Murhadi. 2009. Senyawa dan Aktivitas Anti Mikroba Golongan Asam Lemak dan
Esternya dari Tanaman. Jurnal Teknologi dan Industri Hasil Pertanian Volume 14, No. 1. Universitas Lampung. Bandar Lampung.
Murhadi dan A.S. Zuidar. 2009. Penganekaragaman Bahan Tambahan Pangan (BTP) Berbasis Minyak Inti Sawit. Laporan Usul Penelitian HB Tahun ke II. Lembaga Penelitian Unila. Bandar Lampung.
Murhadi, 2010. Antimikroba dari Tanaman; Golongan Senyawa, Sumber dan Aktivitasnya. Lembaga Penelitian. Universitas Lampung.
Paten Lactem Nomer Paten WO 2004105508 A1. 2003. a Composition Comprising Lactic Acid Esters of Mono- and Diglycerides of Fatty Acids,
an Emulsifier Containing the Same and its Use. http://www.google.com/
patents/WO 2004_105508A1?cl=en. Diakses 1 November 2013.
43
Rahman, A. 2010. Daya Antibakteri dan Stabilitas Emulsi Produk Etanolisis Kasar dari Minyak Inti Sawit yang Dihasilkan pada Suhu 20, 30, 40, 50, dan 60oC. (Skripsi). Universitas Lampung. Bandar Lampung.
Riskawati, T. 2014. Luas Kebun Sawit Mencapai 13,5 Juta Hektar. http://www.
tempo.co/read/news/2013/12/05/090534988/Luas-Kebun-Sawit-Mencapai-135-Juta-Hektare. Diakses pada tanggal 23 Maret 2014.
Siregar, T.U. 2006. Kinetika Biotransformasi Suksinonitril Menjadi Asam Suksinat oleh Pseudomonas sp. (Skripsi). Fakultas Matematika dan Ilmu Pengetahuan Alam. IPB. Bogor. http://reporsitoryipb.com. Diakses 23 Oktober 2013.
Stauffer, C. E. 1990. Functional Additives for Bakery Foods. (e-Book).
http://books.google.co.id/books?id=ckfdE5sRbqAC&pg=PA88&lpg=PA 88&dq=succinic+acid+esters+of+monoglycerides&source=bl&ots=3Sb4 qdKDhe&sig=tfdG2OeCIaJqO2kgCuAkrJ56H0&hl=id&sa=X&ei=tys_ VP6SI9ahugS0mYLQCg&redir_esc=y#v=onepage&q=succinic%20acid %20esters%20of%20monoglycerides&f=false. Diakses 17 September 2014.
Suryani. A., Sailah. I., Hambali. E. 2002. Teknologi Emlsi. IPB. Bogor. 117 hlm. Todar, K. 1997. The Control of Microbial Growth. University of Wiosconsin. Vincent, G. 1987. Farmakologi dan Terapi. Edisi ke-3. Bagian Farmakologi
Fakultas Kedokteran UI. Jakarta.
Winarno, F.G. 1992. Kimia Pangan dan Gizi. Gramedia Pustaka Utama. Jakarta. 251 hlm.