GLISEROL
ANDRIAWAN SUBEKTI
DEPARTEMEN KIMIA
FAKULTAS MATEMATIKA DAN ILMU PENGETAHUAN ALAM
INSTITUT PERTANIAN BOGOR
GLISEROL
ANDRIAWAN SUBEKTI
Skripsi
sebagai salah satu syarat untuk memperoleh gelar
Sarjana Sains pada
Departemen Kimia
DEPARTEMEN KIMIA
FAKULTAS MATEMATIKA DAN ILMU PENGETAHUAN ALAM
INSTITUT PERTANIAN BOGOR
RIWAYAT HIDUP
Penulis dilahirkan di Jakarta pada tanggal 2 Agustus 1986 dari Ayah
Sagiman dan Ibu Titi Komalawati. Penulis merupakan anak ketiga dari 5
bersaudara. Penulis menyelesaikan studi di SMA Negeri 42 Jakarta pada Tahun
2004. Pada tahun yang sama penulis diterima di Institut Pertanian Bogor (IPB)
pada Program Studi Kimia FMIPA melalui jalur Undangan Seleksi Masuk IPB
(USMI).
ABSTRAK
ANDRIAWAN SUBEKTI. Sintesis Co/Cu(II)-Salen yang Tertambatkan pada
Silika sebagai Katalis Padat untuk Oksidasi Gliserol. Dibimbing oleh TUN
TEDJA IRAWADI dan ZAINAL ALIM MAS’UD.
Telah disintesis katalis padat Co/Cu(II)-salen yang tertambatkan pada silika
dengan baik. Pencirian katalis yang dihasilkan dilakukan menggunakan
spektrofotometer infrmerah transformasi Fourier dan spektrofotometer serapan
atom. Kinerja kedua katalis dalam mengoksidasi gliserol dan penggunaannya
kembali dalam reaksi yang sama telah dibandingkan dengan baik dalam penelitian
ini. Oksidasi gliserol dilakukan dengan penambahan katalis sebanyak 3 mol%
gliserol dalam campuran gliserol-asetonitril. Reaksi dilakukan dengan
melewatkan gas oksigen selama 4 jam pada suhu ruang dalam campuran tersebut.
Hasil oksidasi dianalisis menggunakan kromatografi cair kinerja tinggi. Puncak
kromatogram dari hasil oksidasi yang muncul setelah menit ke-8 menunjukkan
terjadinya pengubahan gliserol. Kromatogram yang diperoleh menunjukkan
bahwa katalis Co(salen)-silika mengoksidasi gliserol lebih baik dan selektif
dibandingkan dengan Cu(salen)-silika. Oksidasi dengan Co(salen)-silika
menghasilkan satu produk oksidasi, sedangkan dengan Cu(salen)-silika
menghasilkan dua produk oksidasi. Penggunaan kembali katalis padat dalam
pekerjaan ini tidak mampu menunjukkan pengubahan terhadap gliserol.
ABSTRACT
ANDRIAWAN SUBEKTI. Synthesis of Co/Cu(II)-Salen Anchored on Silica as
Solid Catalyst for Oxidation of Glycerol. Supervised by TUN TEDJA IRAWADI
dan ZAINAL ALIM MAS’UD.
Judul
: Sintesis Co/Cu(II)-Salen yang Tertambatkan pada Silika sebagai
Katalis Padat untuk Oksidasi Gliserol
Nama
: Andriawan Subekti
NIM
: G44204024
Disetujui
Pembimbing I,
Pembimbing II,
Prof. Dr. Ir. Tun Tedja Irawadi, MS
NIP 130 536 664
Dr. Zainal Alim Mas’ud, DEA
NIP 131 578 815
Diketahui
Dekan Fakultas Matematika dan Ilmu Pengetahuan Alam
Institut Pertanian Bogor,
Dr. drh. Hasim, DEA
NIP 131 578 806
DAFTAR
ISI
Halaman
DAFTAR ISI ... i
DAFTAR GAMBAR ... ii
DAFTAR LAMPIRAN ... ii
PENDAHULUAN ... 1
TINJAUAN PUSTAKA ... 1
Katalis ... 1
Ligan Salen... 1
Silika ... 2
Produk Oksidasi Gliserol ... 2
BAHAN DAN LINGKUP KERJA ... 2
Bahan dan Alat ... 2
Lingkup Kerja ... 2
HASIL DAN PEMBAHASAN ... 4
Ciri Katalis Heterogen... 4
Oksidasi Gliserol ... 7
SIMPULAN DAN SARAN ... 8
Simpulan ... 8
Saran ... 9
DAFTAR PUSTAKA ... 9
DAFTAR
GAMBAR
Halaman
1 Produk-produk oksidasi gliserol ... 3
2 Sintesis
kompleks
logam(II)-salen
dan
penyiapan
katalis
heterogennya ... 5
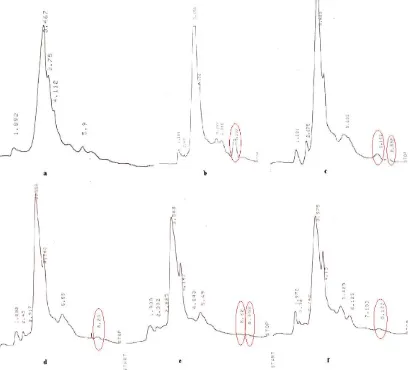
3 Kromatogram HPLC gliserol (a), hasil oksidasi dengan
Co(salen)-silika (b), hasil oksidasi dengan Cu(salen)-Co(salen)-silika (c), hasil oksidasi
dengan penggunan kembali Co(salen)-silika (d), hasil oksidasi
dengan penggunaan kembali Cu(salen)-silika (e), dan hasil oksidasi
dengan silika (f)... 8
DAFTAR LAMPIRAN
Halaman
1 Bagan Alir Penelitian ... 12
2 Data Perolehan 5-Klorometilsalisilaldehida ... 13
3 Data Perolehan Salen ... 14
4 Spektrum FTIR Salen ... 15
5 Data Perolehan Kompleks Co(II)-Salen ... 16
6 Data Perolehan Kompleks Cu(II)-Salen ... 17
7 Spektrum FTIR Co(II)-Salen ... 18
8 Spektrum FTIR Cu(II)-Salen ... 18
9 Data Hasil Analisis AAS Kompleks Logam(II)-Salen ... 19
10 Spektrum FTIR Co(Salen)-Silika ... 20
11 Spektrum FTIR Cu(Salen)-Silika ... 20
12 Spektrum FTIR Silika Terfungsionalisasi ... 21
PRAKATA
Alhamdulillah, segala puji syukur kehadirat Allah SWT selalu penulis ucapkan
atas rahmat, hidayah, dan ridho-Nya sehingga penulis dapat menyelesaikan skripsi
yang berjudul Sintesis Co/Cu(II)-Salen yang Tertambatkan pada Silika sebagai
Katalis Padat untuk Oksidasi Gliserol, sebagai salah satu syarat untuk
memperoleh gelar Sarjana Sains pada Departemen Kimia Fakultas Matematika
dan Ilmu Pengetahuan Alam Institut Pertanian Bogor. Shalawat serta salam
semoga tetap tercurah kepada Nabi Muhammad SAW, keluarga, sahabat serta
pengikut beliau hingga akhir zaman.
Penulis mengucapkan terima kasih kepada berbagai pihak yang telah
membantu dalam penyelesaian skripsi ini, terutama: Ibu Prof Dr. Ir. Tun Tedja
Irawadi, MS selaku pembimbing I dan Bapak Dr. Zainal Alim Mas’ud, DEA
selaku pembimbing II, dan kepada seluruh anggota keluarga: Bapak, Mama, Mbak
Mita, Mbak Dwi, Nuki, dan Surya atas segala bantuan baik doa, moril, materil dan
kasih sayangnya. Selain itu, terima kasih kepada rekan tim sintesis katalis,
Miqdad Abdullah, Robi Mustofa, dan Rachmadi, rekan Kimia 41, terutama Andre
Gunawan, Yockie A Fabianto, Panji H, Ihsan K Hanifa, Dedi Sofyan, Noviadi,
Ramzy, Faiz Sutanto, Satria H, Yunia Anggi, dan Rini S Asnel, serta rekan
Laboratorium Kimia Organik, Mariana H, Titik H, dan Tuti Wukirsari. Terima
kasih juga kepada staf bagian Kimia Organik, Bapak Sabur, Ibu Yeni Karmila,
dan Ibu Siti Robiah, serta dukungan dari Mbak Irmanida B, Mas Ken A Irawadi,
dan Mas Khotib. Terima kasih sebesar-besarnya kepada Laboratorium Terpadu
IPB atas dukungan finansial yang telah diberikan.
Jazakumullah khoiron katsiron
.
Semoga skripsi ini dapat bermanfaat baik bagi penulis maupun bagi pembaca.
Bogor, Januari 2009
PENDAHULUAN
Gliserol, 1,2,3-propanatriol, merupakan bahan kimia yang telah dikenal lebih dari dua abad dan dewasa ini produksinya meningkat tajam disebabkan oleh pengembangan biodiesel. Dalam setiap produksi biodiesel, gliserol dihasilkan dengan jumlah 10%. Departemen Perindustrian (Depperin) (2007) melaporkan bahwa produksi biodiesel di Indonesia pada tahun 2007 mencapai 1.1 juta ton sehingga dapat ditentukan bahwa jumlah gliserol yang dihasilkan dari produksi biodiesel Indonesia pada tahun tersebut adalah 110,000 ton. Nilai tersebut akan terus meningkat sesuai dengan kebutuhan terhadap bahan bakar hayati. Kecenderungan ini telah berdampak pada penurunan harga jual gliserol hingga 50% (Behr et al. 2008).
Pemanfaatan gliserol telah banyak dilakukan, yaitu dalam industri kosmetik, farmasetika, sabun, dan pasta gigi. Selain itu, gliserol terutama digunakan sebagai pemanis pada permen dan agen pembasah dalam tembakau. Pengembangan aplikasi gliserol sebagai bahan baku produk yang lebih bernilai jual telah banyak dilakukan untuk pemanfaatan jumlahnya yang kian meningkat. Salah satunya adalah pengubahan gliserol menjadi produk oksidasinya, seperti dihidroksiaseton (DHA), gliseraldehida, asam gliserat, asam tartronat, asam oksalat, asam glikolat, dll. (Behr et al. 2008; Pachauri & He 2006).
Dalam dasawarsa terakhir ini, ligan salisilaldehidaetilenadiamina (salen) beserta turunannya telah memperoleh perhatian lebih, terutama disebabkan oleh pembuatannya yang mudah dan murah serta penerapannya yang luas dalam bidang sintesis dan katalisis. Ligan salen mampu mengikat logam dan membentuk kompleks yang memiliki aktivitas katalitik yang sangat baik pada berbagai reaksi, seperti yang terbentuk dengan Co dan Cu. Beberapa kajian baru-baru ini telah melaporkan aktivitas yang baik dari kompleks kobalt(II) salen (Co(II)-salen) dan tembaga(II) salen (Cu(II)-salen) dalam mengkatalisis berbagai jenis reaksi oksidasi (Amarekasera et al. 2007; Gupta & Sutar 2007; Kervinen 2005; Karandikar et al. 2004; dan Sharma et al.
2004). Sharma et al. 2004 menunjukkan
bahwa kompleks Co(II)-salen mampu
mengoksidasi alkohol sekunder menjadi senyawa ketonnya. Selain itu, Co(II)-salen bersama Cu(II)-salen juga telah dilaporkan kemampuannya yang cukup baik dalam
oksidasi yang menghasilkan keton
(Karandikar et al. 2004).
Dalam proses katalisis, kecenderungan penggunaan katalis heterogen lebih banyak dilakukan. Hal ini disebabkan oleh keuntungannya, yaitu mudah dipisahkan dari reaktan dan produk. Selain itu, katalis heterogen dapat dipulihkan dan digunakan kembali dalam proses katalisis yang sama. Pengembangan katalis heterogen dari kompleks salen telah banyak dilakukan, salah satunya yaitu penambatan kompleks salen pada padatan pendukung, seperti silika, MCM-41, ITQ-2, dll. (Karandikar et al. 2004; Baleizão et al. 2002, 2003).
Penelitian ini melaporkan keberhasilan sintesis kompleks Co(II)-salen dan Cu(II)-salen dengan tipe salen [N,N ’-bis(5-klorometilsalisilidena)-etilenadiamina] yang tertambatkan pada silika terfungsionalisasi. Kedua katalis tersebut terbukti mampu mengoksidasi gliserol. Kemampuan katalitik kedua jenis katalis dalam oksidasi telah dibandingkan dalam penelitian ini. Pencirian katalis ditunjukkan dengan baik menggunakan spektrofotometer inframerah transformasi Fourier (FTIR) dan spektrofotometer serapan atom (AAS).
TINJAUAN PUSTAKA
KatalisPerkembangan teknologi yang ramah lingkungan telah mendorong pengembangan penelitian katalis heterogen, salah satunya adalah heterogenisasi katalis homogen untuk oksidasi. Katalis heterogen memiliki beberapa kelebihan, antara lain dapat dipisahkan dari campuran reaksi, dapat dipulihkan, dan digunakan kembali. Usaha heterogenisasi katalis homogen telah banyak dilakukan dengan penambatan katalis homogen pada suatu padatan pendukung (Baleizão et al.
2003 dan 2002; Chorkendorff & Niemantsverdriet 2003).
Ligan Salen
Salen adalah suatu basa Schiff yang terbentuk dari salisilaldehida dan etilenadiamina ataupun turunan keduanya sebagai prazat. Sejumlah ragam salen
diketahui memiliki perbedaan pada
Penggunaan kompleks logam salen dewasa ini telah banyak diterapkan dalam berbagai reaksi katalitik. Sejumlah besar kompleks menunjukkan aktivitas katalitik yang baik pada beberapa reaksi, salah satunya pada reaksi oksidasi (Pui & Mahy 2007; Sharma et al. 2004). Aktivitas yang baik tersebut ditunjukkan baik sebagai katalis homogen (Pui & Mahy 2007; Sharma et al. 2004) maupun heterogen yang ditambatkan pada suatu padatan pendukung, seperti silika, MCM-41, ITQ-2, dll (Karandikar et al. 2004; Baleizão et al. 2003 dan 2002).
Silika
Silika merupakan padatan pendukung untuk katalis homogen yang digunakan dalam proses-proses yang biasanya dijalankan pada suhu rendah (di bawah 300 °C), seperti hidrogenasi, polimerisasi, atau beberapa oksidasi. Sifatnya, seperti ukuran pori, ukuran partikel, daerah permukaan dapat disesuaikan
dengan mudah untuk mempertemukan
kebutuhan khusus dalam sebagian aplikasi. Sebagian besar pendukung silika dibuat dengan satu dari dua jalur preparasi berbeda: pengendapan gel sol untuk menghasilkan silika xerogel dan hidrolisis kobaran api untuk menghasilkan yang biasa disebut silika berasap. Silika xerogel dibuat dari natrium silikat basa (pH = 12) dan asam sulfat yang menghasilkan Si(OH)4 sebagai prazat,
sedangkan silika berasap dibuat dari SiCl4
dalam kehadiran hidrogen dan oksigen. Keuntungan silika berasap adalah memiliki sifat mekanik yang lebih baik dan kemurnian yang lebih tinggi pada pembentuknya bila dibandingkan dengan silika xerogel (Chorkendorff & Niemantsverdriet 2003). Oleh karena itu, silika berasap lebih banyak digunakan sebagai padatan pendukung untuk berbagai katalis homogen.
Produk Oksidasi Gliserol
Oksidasi gliserol merupakan jalur yang
cukup kompleks pada reaksi yang
menghasilkan sejumlah besar produk, seperti DHA, gliseraldehida, asam gliserat, asam tartronat, asam hidroksi piruvat, asam oksalat, asam glikolat, dll. (Gambar 1). Sejumlah produk-produk oksidasi gliserol sangat berguna sebagai bahan intermediet atau bahan kimia yang sangat bernilai. Namun, hingga
sekarang produk-produk tersebut masih diproduksi melalui proses yang mahal dan oleh sebab itu pemanfaatannya dalan skala industri masih rendah (Behr et al. 2008).
Oksidasi gugus alkohol sekunder pada gliserol akan membentuk DHA. Hal ini telah dilakukan menggunakan katalis platina (Kimura 2001 dan Garcia et al. 1994) atau fermentasi (Bauer et al. 2005; Svitel & Sturdik 1994). DHA merupakan bahan kimia penting yang digunakan dalam industri kosmetik sebagai bahan pelindung kulit. DHA adalah bahan aktif utama dalam semua penyiapan perawatan kulit anti-pencoklatan karena matahari sejak DHA diketahui sebagai bahan tambahan pelindung kulit yang paling efektif (Cirriminna et al. 2006). Selain itu, DHA juga digunakan sebagai biomaterial polimerik.
Oksidasi gugus alkohol primer pada gliserol menghasilkan gliseraldehida, suatu intermediet dalam metabolisme karbohidrat. Gliseraldehida juga digunakan sebagai standard pembanding molekul kiral seri D- atau L-. Oksidasi gliseraldehida lebih lanjut menghasilkan asam karboksilat, seperti asam gliserat, asam tartronat, dan mesoksalat (Gambar 1). Asam-asam ini merupakan prazat produk polimer dan pengemulsi biodegradabel (Behr et al. 2008).
BAHAN DAN LINGKUP KERJA
Bahan dan AlatBahan-bahan yang digunakan antara lain salisilaldehida, etilenadiamina, HCl pekat, formaldehida 37%, silika (N2 = 350 m2 g-1,
Si/Al = ) dan Co(OAc)2·4H2O yang dibeli
dari Sigma-Aldrich, Cu(OAc)2·H2O,
3-aminopropiltrietoksisilana, asetonitril, dan gliserol. Alat-alat yang digunakan antara lain alat penentu titik leleh, spektrofotometer serapan atom (AAS), spektrofotometer inframerah transformasi Fourier (FTIR), dan kromatografi cair kinerja tinggi (HPLC).
Lingkup Kerja
Gambar 1 Produk-produk oksidasi gliserol
(Sumber: Behr et al. 2008)
Penyiapan kompleks logam salen Sintesis 5-klorometilsalisilaldehida
Mengacu pada prosedur Angyal et al.
(1950) yang telah dijelaskan dengan baik, yaitu salisilaldehida 1 (6 g), formaldehida 37% b/b dalam H2O (3.7 mL), dan asam
klorida pekat (51 mL) dicampurkan dan diaduk selama 3 jam, sementara gas hidrogen klorida dilewatkan ke dalamnya. Padatan yang dihasilkan dipisahkan dari campuran reaksi dengan penyaringan, dilarutkan kembali dalam dietil eter (50 mL), dan dikeringkan dengan natrium sulfat. Selanjutnya, dietil eter dihilangkan dengan penguap putar dan
padatan yang dihasilkan kemudian
direkristalisasi dengan n-heksana panas (100 mL, 50 °C) sehingga diperoleh padatan putih 5-klorometilsalisilaldehida 2. Pencirian senyawa yang terbentuk dilakukan dengan penentuan titik lelehnya.
Sintesis ligan salen
Penyiapan ligan salen dilakukan mengikuti prosedur yang dijelaskan oleh Aranha et al.
(2006), yaitu ke dalam larutan 2 (4.0 mmol)
dalam etanol (25 mL) ditambahakan tetes demi tetes larutan etanol (10 mL) dari 2.0 mmol etilenadiamina 3. Campuran tersebut kemudian dipanaskan selama 2 jam. Setelah itu, campuran didinginkan pada suhu ruang, lalu didinginkan pada suhu 5 °C selama semalam. Padatan salen 4 yang terbentuk kemudian disaring dan dicuci dengan etanol dingin (5 mL pada 5 °C). Pencirian padatan dilakukan dengan menggunakan FTIR.
Sintesis kompleks logam(II)-salen
Prosedur sintesis kompleks ini didasarkan pada prosedur umum yang dilaporkan oleh Wei et al. (2004). Co(OAc)2·4H2O atau
Cu(OAc)2·H2O (2.0 mol) dalam EtOH (10
mL) ditambahkan ke dalam suspensi salen (2.0 mol) dalam EtOH (5 mL) dan diaduk selama 2 jam di bawah atmosfer N2 pada suhu
Penyiapan silika terfungsionalisasi
Fungsionalisasi silika ini mengikuti prosedur yang dilaporkan oleh Baleizão et al.
(2003). Setelah dehidrasi padatan silika (pada suhu 200 °C, selama 24 jam), 3-aminopropiltrietoksisilana dalam toluena kering ditambahkan dengan nisbah mol amina /mol SiO2 = 4 dan mol toluena/mol SiO2 = 2.
Suspensi tersebut kemudian diaduk pada suhu refluks di bawah atmosfer N2 selama 24 jam.
Padatan disaring dan diekstraksi Soxhlet dengan CH2Cl2 selama 24 jam, dan
dikeringkan (pada 45 °C selama 24 jam). Padatan yang dihasilkan selanjutnya dicirikan dengan FTIR.
Penambatan kompleks pada silika
Mengacu pada prosedur penambatan Baleizão et al. (2003), sejumlah kompleks logam salen yang diketahui ditambahkan ke dalam suspensi silika termodifikasi dalam toluena kering (2 mL) dan diaduk pada suhu refluks selama 48 jam di bawah atmosfer N2.
Padatan yang diperoleh dari penyaringan suspensi tersebut kemudian diekstraksi Soxhlet dengan CH2Cl2 selama 24 jam, dan
dikeringkan (pada 45 °C selama 24 jam). Nisbah kompleks/silika yang disiapkan adalah 40 mg kompleks/100 mg silika termodifikasi. Kelebihan sisa kompleks selanjutnya dihilangkan dengan ekstraksi padat-cair. Hasil penambatan selanjutnya dicirikan dengan FTIR dan AAS.
Oksidasi gliserol
Metode oksidasi gliserol yang digunakan disesuaikan dengan metode oksidasi alkohol sekunder yang dijelaskan oleh Sharma et al.
(2004). Gliserol (1 mmol), kompleks logam(II)-salen tetrambatkan (0.03 mmol atau 3 mol%), dan asetonitril kering (5 mL) dimasukkan ke dalam labu leher-dua 50 mL yang disesuaikan dengan tabung penyalur gas dan pengaduk. Campuran kemudian diaduk pada suhu ruang dan gas oksigen dilewatkan ke dalamnya dengan kecepatan rendah. Setelah proses tersebut dihentikan, katalis dipisahkan melalui penyaringan. Filtrat kemudian dianalisis menggunakan HPLC dan katalis digunakan untuk reaksi lain yang sama. Oksidasi dengan silika juga dilakukan untuk
menghilangkan faktor silika dalam
mengoksidasi. Hasil oksidasi dalam penelitian ini dianalisis dengan HPLC, kolom C18, fase gerak asetonitiril:air (9:1), dan detektor UV pada 262 nm.
HASIL DAN PEMBAHASAN
Ciri Katalis HeterogenPenambatan suatu kompleks pada padatan pendukung dapat dilakukan dengan 2 strategi, yaitu melalui ligan dan melalui logam.
Penambatan melalui ligan memiliki
keuntungan, yaitu lapisan koordinasi pada ion logam (Co dan Cu) aktif tidak terikat dalam penambatan sehingga keaktifan kompleks tertambatkan ini diharapkan sama dengan
yang belum tertambatkan. Namun,
penambatan dengan cara ini juga memiliki kekurangan, yaitu jumlah tahapan sintesis yang banyak dan kemungkinan gugus aminopropil untuk dapat terikat pada bagian logam.
Dalam setiap penambatan kompleks, kehadiran suatu gugus yang dapat membentuk ikatan kovalen antara kompleks dengan padatan sangat dibutuhkan. Oleh karena itu, sintesis kompleks logam salen dalam penelitian ini diawali dengan adisi gugus klorometil pada prazat salisilaldehida sehingga penambatan kompleks ini dilakukan melalui ligan. Tahapan reaksi sintesis dan penambatan kompleks logam ditunjukkan dalam Gambar 2.
Sintesis 5-klorometilsalisilaldehida telah dilakukan dengan baik dalam penelitian ini menggunakan metode yang dilaporkan oleh Angyal et al. (1950). Sintesis dilakukan dengan dijenuhkan menggunakan gas HCl. Kondensasi yang terjadi menghasilkan padatan berwarna ungu muda. Penjenuhan reaksi dengan gas HCl ditujukan untuk mempercepat pembentukkan padatan. Sintesis yang dilakukan menggunakan gas HCl dalam
penjenuhan akan menghasilkan
5-klorometilsalisilaldehida lebih cepat dan lebih baik dibandingkan dengan yang tidak menggunakan gas HCl (Cort et al. 2006; Angyal et al. 1950).
.
Gambar 2 Sintesis kompleks logam(II)-salen dan penyiapan katalis heterogennya
menentukan titik lelehnya, pencirian menunjukkan bahwa titik leleh 5-klorometilsalisilaldehida adalah 84–86 °C. Hasil ini cukup sesuai dengan metode acuan (Angyal et al. 1950) yang menyebutkan bahwa senyawa 5-klorometilsalisilaldehida merupakan padatan putih dengan titik leleh sebesar 85–86 °C.
Padatan 5-klorometilsalisilaldehida yang diperoleh direaksikan dengan etilenadiamina untuk menghasilkan ligan salen. Salen yang dihasilkan merupakan tipe salen-H2
N,N'-bis(salisilidena)etilenadiamina. Hal ini berarti bahwa ikatan yang terbentuk antara gugus amina pada etilenadiamina dan gugus karbonil pada 5-klorometilsalisilaldehida merupakan ikatan rangkap 2 C=N (imina) sehingga jumlah H pada gugus yang akan berikatan kompleks hanya diberikan oleh gugus –OH.
Seperti yang dilaporkan dalam beberapa kajian (Aranha et al. 2006; Kervinen 2005) bahwa salen merupakan padatan kuning cerah, sintesis salen ini menghasilkan padatan dengan warna yang sama. Dari
prosedur yang dilakukan, dihasilkan padatan kuning salen dengan rendemen mencapai 70% (Lampiran 3). Padatan salen yang terbentuk dicirikan dengan FTIR untuk mengetahui terbentuknya gugus fungsi imina. Lampiran 4 menunjukkan spektrum FTIR dari salen yang dihasilkan. Adanya gugus imina ditunjukkan dengan vibrasi ulur C=N ( C=N) pada bilangan
gelombang 1636 cm-1. Vibrasi ulur gugus O–H ( O–H) ditunjukkan pada 3431 cm-1. Adisi gugus
klorometil ditunjukkan dengan baik oleh puncak vibrasi ulur C–Cl ( C–Cl) pada 1090 cm-1. Selain
itu, beberapa pita terpilih juga ditunjukkan oleh spektrum FTIR salen, yaitu C-H aromatik
(2799-3010 cm-1), C=C aromatik (1509–1590
cm-1), C–N (1350 cm-1), C–O (1314 cm-1).
berwarna coklat dengan rendemen 56% (Lampiran 5). Berbeda dengan sintesis Co(II)-salen, sintesis kompleks Cu(II)-salen tidak memberikan padatan sehingga sintesis dilakukan dengan mengubah sedikit prosedur. Dalam sintesis Cu(II)-salen, hasil reaksi campuran logam asetat dan salen dihilangkan pelarutnya dengan penguap putar. Cara ini memberikan padatan hijau yang kemudian direkristalisasi sehingga pada akhirnya menghasilkan kembali padatan hijau dengan rendemen 69% (Lampiran 6). Kedua padatan yang dihasilkan dicirikan dengan FTIR untuk dapat dibandingkan dengan hasil pencirian salen.
Hasil pencirian FTIR kompleks-kompleks menunjukkan pergeseran yang tidak berarti pada beberapa puncak.
Spektrum yang diperoleh tidak
menunjukkan adanya perubahan puncak seperti yang terpencirian pada salen. Penambahan 2 buah puncak pada daerah 530–680 cm-1 merupakan penunjuk penting terbentuknya ikatan M–N dan M–O. Hasil spektrum Co(II)-salen yang diproleh menunjukkan masih adanya vibrasi ulur C=N ( C=N) pada bilangan gelombang 1640
cm-1. Vibrasi lain seperti pada salen juga ditunjukkan dalam spektrum FTIR ini, antara lain C-H aromatik (2799-3009 cm-1),
C=C aromatik (1511–1600 cm-1), C–N (1350
cm-1), C–O (1314 cm-1), C–Cl (1036 cm-1).
Vibrasi ulur O–H masih tampak dalam spektrum pada 3400 cm-1. Hal ini disebabkan oleh penggunaan metanol dalam rekristalisasi sehingga memungkinkan adanya sisa pelarut tersebut pada padatan. Adanya ikatan Co–N dan Co–O berturut-turut ditunjukkan dengan puncak pada 665 cm-1 dan 550 cm-1 (Lampiran 7).
Seperti hasil spektrum Co(II)-salen,
spektrum FTIR Cu(II)-salen juga
menunjukkan beberapa vibrasi ulur, yaitu
O–H (3400 cm-1), C-H aromatik (2795-3100
cm-1), C=C aromatik (1509–1598 cm-1), C–N
(1385 cm-1), C–O (1347 cm -1
), dan C–Cl
( C=N (1642 cm-1), C–Cl (1038 cm-1). Adanya
ikatan Cu–N dan Cu–O berturut-turut ditunjukkan dengan puncak pada 682 cm-1 dan 530 cm-1. Dengan demikian, kompleks logam salen dalam penelitian ini telah terbentuk (Lampiran 8).
Analisis AAS pada kompleks-kompleks dilakukan untuk mengetahui keberhasilan reaksi pengompleksan. Keberhasilan
pengompleksan dapat dilihat dari kadar logam dalam rendemen padatan kompleks yang dihasilkan. Hasil analisis AAS logam(II)-salen bila dibandingkan dengan hasil teoritis menunjukkan bahwa rendemen kompleks Co(II)-salen adalah sebesar 30%, sedangkan untuk Cu(II)-salen sebesar 69% (Lampiran 9). Penggunaan prosedur yang sedikit berbeda pada pembentukan Cu(II)-salen menghasilkan kadar logam yang lebih tinggi. Namun, hasil di atas belum secara pasti menunjukkan bahwa pengompleksan dengan cara tersebut lebih baik. Hal ini disebabkan oleh adanya kemungkinan tembaga asetat yang tidak membentuk kompleks tertinggal bersama padatan karena proses penguapan pelarut. Hasil yang baik sebaiknya dilihat dari hasil analisis AAS katalis padat yang dihasilkan.
Tahap akhir dari penyiapan katalis-katalis heterogen adalah penambatan kompleks logam
salen pada padatan silika yang
terfungsionalisasi 3-aminopropil. Penggunaan padatan silika dalam penambatan ini disebabkan oleh ketersediaannya yang mudah didapatkan. Selain itu, silika memiliki area permukaan yang luas sehingga diharapkan dapat mengikat lebih banyak kompleks logam salen yang pada akhirnya meningkatkan kemampuan katalitik katalis yang terbentuk. Penggunaan 3-aminopropiltrietoksisilana merupakan salah satu cara yang mudah untuk menghubungkan kompleks dengan padatan silika. Jumlah
aminopropil yang berlebih dalam
fungsionalisasi silika bertujuan memastikan pemasukan gugus tersebut pada permukaan silika sehingga diharapkan gugus silanol dapat tersubtitusi.
Silika yang digunakan dalam penelitian ini mempunyai ciri struktur amorf, luas area 350 m2 g-1, dan derajat sililasi >95%. Pemanasan silika sebelum fungsionalisasi pada 200 °C selama 24 jam bertujuan menghilangkan pengaruh air yang teradsorbsi. Adanya molekul air dalam reaksi fungsionalisasi dapat mengganggu pembentukkan ikatan antara gugus silanol dari silika dan etoksi dari pereaksi 3-aminopropiltrietoksisilana. Penghilangan sisa pereaksi 3-aminopropiltrietoksisilana, toluena dan pengotor lain yang mungkin terbentuk selama fungsionalisasi dihilangkan dengan ekstraksi Soxhlet menggunakan CH2Cl2 selama
24 jam. Setelah ekstraksi Soxhlet, penghilangan sisa pelarut dilakukan dengan pengeringan padatan pada 45 °C selama 24 jam.
kinerja kompleks logam salen yang tertambatkan pada silika dengan 2 nisbah, yaitu 15 mg komplek/100 mg silika dan 40 mg kompleks/100 mg silika. Pekerjaan tersebut menunjukkan bahwa pengunaan nisbah kompleks/silika yang lebih tinggi meningkatkan selektivitas hasil yang diperoleh. Hal ini disebabkan oleh pemasukan kompleks yang lebih banyak pada nisbah yang lebih tinggi.
Penambatan kompleks dalam penelitian ini menggunakan toluena kering sebagai media. Penggunaan tersebut bertujuan meniadakan pengaruh air yang dapat menggangu terbentuknya pembentukan ikatan antara gugus amino dari silika terfungsionalisasi dengan gugus klorometil dari kompleks, serta mencegahnya terikat dengan logam pada kompleks. Pengeringan
toluena hanya dilakukan dengan
menambahkan Na2SO4 anhidrat ke
dalamnya.
Reaksi pembentukan katalis padat pada suhu refluks selama 48 jam memberikan hasil padatan berwarna coklat kemerahan
untuk kompleks dengan logam Co
(Co(salen)-silika) dan hijau untuk kompleks dengan logam Cu (Cu(salen)-silika). Penghilangan pengotor dari padatan katalis dilakukan dengan ekstraksi Soxhlet dengan CH2Cl2 selama 24 jam. Pengeringan padatan
setelah ekstraksi dilakukan pada 45 °C selama 24. Pengeringan dengan suhu rendah bertujuan mencegah rusaknya ikatan yang telah terbentuk. Katalis yang dihasilkan dalam penelitian ini dicirikan dengan FTIR dan AAS. Pencirian FTIR pada silika juga dilakukan untuk memastikan terjadinya penambatan.
Beberapa puncak serapan penting ditunjukkan dalam ketiga spektrum (Lampiran 10, 11, & 12). Kedua katalis menunjukkan beberapa kesamaan spektrum terhadap silika terfungsionalisasi. Perbedaan signifikan antara spektrum silika dan kedua katalis terdapat pada daerah 1630 cm-1. Katalis Co/Cu(salen)-silika menunjukkan adanya vibrasi ulur C=N yang jelas, berturut-turut pada 1633 cm-1 dan 1637 cm-1 (Lampiran 10 & 11). Vibrasi ulur tersebut tidak terlihat jelas pada silika terfungsionalisasi (Lampiran 12). Dengan demikian, hasil-hasil spektrum di atas menunjukkan bahwa kompleks logam salen telah tertambat pada silika. Beberapa puncak serapan lain seperti yang ditunjukkan dalam spektrum FTIR kompleks-kompleks yang dapat lebih mendukung terjadinya
penambatan tidak ditunjukkan dengan jelas dalam spektrum katalis. Hal ini diduga disebabkan oleh tertutupnya puncak-puncak tersebut akibat penambatan pada silika. Bagaimanapun, spektrum tersebut telah menunjukkan adanya penambatan. Adanya gugus amina pada silika terfungsonalisasi ditunjukkan dengan puncak pada daerah 3400
cm-1. Hal ini menunjukkan bahwa
fungsionalisasi silika telah terjadi. Perlindungan terhadap sisa gugus silanol setelah fungsionalisasi silika perlu dilakukan untuk memastikan ketiadaan gugus tersebut agar penambatan tidak terganggu.
Analisis AAS pada katalis-katalis yang dihasilkan dilakukan untuk mengetahui keberadaan kompleks logam(II)-salen yang tertambat pada silika. Hasil analisis menunjukkan terjadinya penambatan pada kedua kompleks. Hal ini ditunjukkan dengan kadar Co dalam katalis Co(salen)-silika sebesar 1.0% dan kadar Cu dalam Cu(salen)-silika sebesar 1.4% (Lampiran 13). Hasil ini menunjukkan bahwa penggunaan cara yang
berbeda pada pembentukan kompleks
sebelumnya tidak berpengaruh besar terhadap penambatan kompleks.
Oksidasi Gliserol
Pengujian aktivitas katalitik hasil sintesis katalis padat, kompleks logam(II)-salen yang tertambatakan pada silika terhadap oksidasi gliserol dilakukan sesuai dengan prosedur yang telah dijelaskan. Oleh karena itu, dalam penelitian ini diperoleh 5 contoh hasil oksidasi, yaitu contoh dengan Co/Cu(salen)-silika, Co/Cu(salen)-silika setelah digunakan sekali, dan silika terfungsionalisasi. Oksidasi dengan silika terfungsionalisasi dilakukan dengan tujuan mengoreksi kinerja katalis padat yang digunakan. Hasil analisis contoh dengan HPLC ditampilkan dalam Gambar 3.
Dalam penelitian ini, analisis kualitatif hasil oksidasi dilakukan dengan membandingkan kromatogram kelima contoh di atas dengan kromatogram gliserol. Kromatogram kelima contoh menunjukkan kesamaan puncak dengan yang ditunjukkan pada kromatogram gliserol. Namun, puncak baru setelah menit ke-8 muncul
dalam kromatogram kelima contoh.
Kromatogram dengan Co(salen)-silika
(Gambar 3c & 3e). Puncak yang muncul pada menit 8.2 diduga merupakan produk oksidasi gliserol. Area puncak pada menit 8.2 dengan Co(salen)-silika lebih luas daripada dengan Cu(salen)-silika Hal ini menunjukkan bahwa oksidasi menggunakan Co(salen)-silika lebih baik dan lebih selektif dalam mengoksidasi gliserol dibandingkan dengan menggunakan Cu(salen)-silika. Penggunaan kembali kedua katalis dalam
penelitian ini tidak memberikan hasil yang memuaskan. Hasil analisis HPLC pada
penggunaan kembali kedua katalis
dibandingkan dengan yang menggunakan silika menunjukkan bahwa penggunaan kembali katalis tidak mampu mengoksidasi gliserol. Hal ini menunjukkan bahwa pemulihan lebih lanjut dibutuhkan agar katalis dapat digunakan kembali dengan kinerja yang baik. Pengubahan
gliserol menjadi produk oksidasinya
Gambar 3 Kromatogram HPLC gliserol (a), hasil oksidasi dengan Co(salen)-silika (b), hasil oksidasi dengan Cu(salen)-silika (c), hasil oksidasi dengan penggunan kembali Co(salen)-silika (d), hasil oksidasi dengan penggunaan kembali Cu(salen)-silika (e), dan hasil oksidasi dengan silika (f).
dalam penelitian ini belum sempurna. Hal ini disebabkan oleh belum dilakukannya optimisasi reaksi oksidasi terhadap nisbah substrat/katalis, waktu dan suhu reaksi, serta kondisi lainnya.
SIMPULAN DAN SARAN
Simpulan [image:17.595.120.528.231.601.2]dengan baik dalam penelitian ini. Hasil analisis HPLC pada hasil oksidasi menunjukkan bahwa kedua katalis mampu mengoksidasi gliserol. Produk yang terbentuk ditunjukkan dengan puncak yang muncul setelah menit ke-8 dalam setiap kromatogram. Oksidasi menggunakan Co(salen)-silika menunjukkan pengubahan dengan selektivitas yang baik dibandingkan dengan menggunakan Cu(salen)-silika. Jumlah produk yang dihasilkan dengan menggunakan Co(salen)-silika adalah satu, sedangkan dengan Cu(salen)-silika adalah dua. Dalam penelitian ini, katalis yang telah digunakan dalam oksidasi tersebut tidak dapat digunakan kembali dalam reaksi oksidasi yang sama.
Saran
Perlindungan gugus silanol setelah fungsionalisasi silika perlu dilakukan menggunakan etoksitrimetilsilana agar penambatan tidak terganggu. Optimisasi oksidasi gliserol menggunakan katalis yang diperoleh perlu dilakukan. Selain itu, analisis puncak baru yang muncul pada kromatogram HPLC hasil oksidasi perlu dilakukan untuk memastikan terbentuknya produk oksidasi.
DAFTAR PUSTAKA
Amarekasera AS, Oki AR, McNeal I, Uzoezie U. 2007. One-pot synthesis of cobalt-salen catalyst immobilized in silica by sol-gel process and apllication in selective oxidations of alkanes and alkenes. Catal Commun
8:1132-1136.
Angyal SJ, Morris PJ, Tetaz JR, Wilson JG. 1950. The sommelet reaction: the choice of solvent and the effect of subtituents. J Chem Soc: 2141–2145. Aranha PE, dos Santos MP, Romera S, Dockal ER. 2006. Synthesis, characterization, and spectroscopic studies of tetradentate Schiff base
chromium(III) complexes.
Polyhedron 26:1373-1382.
Baleizão C, Gigante B, Garcia H, Corma A. 2003. Chiral vanadyl Schiff base complex anchored on silicas as solid enantioselective catalyst for
formation of cyanohydrins:
optimization of the asymmetric induction by support modification. J Catal 215:199-207.
Baleizão C, Gigante B, Sabater MJ, Garcia H, Corma A. 2002. On the activity of chiral chromium salen complexes covalently bound to solid silicates for the enantioselective epoxide ring opening.
Appl Catal A: General 228:279-228. Bauer R, N Katsikis, S Varga, dan D Hekmat.
2005. Study of the inhibitory effect of the product dihydroxyacetone on
Gluconobacter oxydans in a semi-continuous two-stage repeated-fed-batch process. Bioprocess and Biosystem Engineering 28:37-43.
Behr A, Eilting J, Irawadi K, Leschinski J, Linder F. 2008. Improved utilization of renewable resources: New important derivatives of glycerol. Green Chem
10:13-30.
Chorkendorff I, Niemantsverdriet JW. 2003.
Concepts of Modern Catalysis and Kinetics. Weinheim: Wiley-VCH. Cirriminna R, Palmisano G, Pina GD, Rossi M,
Pagliaro M. 2006. One-pot
electrocatalytic oxidation of glycerol to DHA. Tetrahedron Lett 47:6993-6995. Cort AD, Mandolini L, Pasquini C, Schiaffino
L. 2006. A novel ditopic zinc-salophen macrocycle: a potential two-stationed wheel for [2]-pseudorotaxanes. Org Biomol Chem 4:4543-4546.
[Depperin] Departemen Perindustrian. 2007. Bersiap menghadapi dampak gejolak ekonomi dunia. Media Industri 5. Garcia R, Besson M, Gallezot P. 1994.
Chemoselective catalytic oxidation of glycerol with air on platinum metals.
Appl Catal A: General 127:1-2.
Gupta KC, Sutar AK. 2007. Catalytic activities if Schiff base transition metal complexes.
Coordination Chem rev, in press. Karandikar P et al. 2004. Cu/Co-salen
immobilized MCM-41: characterization and catalytic reaction. Catal Commun
5:69-74.
Kervinen K. 2005. Studies of veratryl alcohol oxidation catalyzed by Co(salen) type complexes and molecular oxygen in aqueous solution [disertasi]. Helsinski: Faculty of Science, University of Helsinski.
Kimura H. 2001. Oxidation assisted new reaction of glycerol. Polym Adv Technol
12:11-12.
Pui A, Mahy J. 2007. Synthesis, characterization and catalytic activity
of
halo-methyl-bis(salicylaldehyde)ethylenediamine cobalt(II) complexes. Polyhedron
26:3143-3152.
Sharma VB, Jain SL, Bir Sain. 2004. Cobalt (II) Schiff base catalyzed aerobic oxidation of secondary alcohols to ketones. J Mol Catal A: Chem
212:55-59.
Svitel J dan E Sturdik. 1994. Product yield and byproduct formation in glycerol conversion to dihydroxyacetone by
Gluconobacter oxydans. J Ferment Bioeng 78:351-355.
Lampiran 1 Bagan Alir Penelitian
Sintesis of 5-klorometil
salisilaldehida
Sintesis of ligan salen
Sintesis of kompleks logam-
(II) salen
Penyiapan silika
terfungsionalisasi-aminopropil
Penambatan kompleks
logam-(II) salen pada silika
terfungsionalisasi
Lampiran 2 Data Perolehan 5-Klorometilsalisilaldehida
Penyiapan:
Bobot salisilaldehida
1
= 6.0125 g (0.0492 mol)
Volume formaldehida
= 3.7 mL
Volume HCl pekat
= 51 mL
Reaksi:
Perhitungan bobot teoritis:
Mol 5-klorometilsalisilaldehida
2
=
mol
1
1
koefisien
2
koefisien
×
Mol 5-klorometilsalisilaldehida
= mol salisilaldehida
Bobot 5-klorometilsalisilaldehida = mol
2
× BM
2
= 0.0492 mol × 171 g mol
-1×
mmol
1
mol
10
-3= 8.4132 g
Hasil percobaan:
Bobot gelas piala + isi
= 66.2501 g
Bobot gelas piala kosong
= 62.9531g
Bobot isi (5-klorometilsalisilaldehida) = 66.2501 g – 62.9531 g = 3.2970 g
Rendemen =
100%
teoritis
hasil
percobaan
hasil
×
=
100%
g
8.4132
g
3.2970
×
Lampiran 3 Data Perolehan Salen
Penyiapan:
Bobot 5-klorometilsalisilaldehida
2
= 8.5295 g (50 mmol)
Bobot etilenadiamina
3
= 1.5025 g (25 mmol)
Reaksi:
Perhitungan bobot teoritis:
Mol salen
4
=
mol
3
3
koefisien
4
koefisien
×
Mol salen
= mol etilenadiamina = 25 mmol
Bobot salen teoritis = mol salen × BM salen
= 25 mmol × 365 g mol
-1×
mmol
1
mol
10
-3= 9.1250 g
Hasil percobaan:
Bobot kertas saring + isi
= 7.3880 g
Bobot kertas saring kosong = 1.0256 g
Bobot isi (salen)
= 7.3880 g – 1.0256 g = 6.3624 g
Rendemen =
100%
teoritis
hasil
percobaan
hasil
×
=
100%
g
9.1250
g
6.3624
×
= 69.72%
O
OH
Cl
2
N
H2 NH2
3 4
OH
Cl
N
O H
Cl N
Lampiran 4 Spektrum FTIR Salen
1
Lampiran 5 Data Perolehan Kompleks Co(II)-Salen
Penyiapan:
Bobot salen
= 1.4601 g (4 mmol)
Bobot Co(OAc)
2·4H
2O = 0.9964 g (4 mmol)
Reaksi:
Perhitungan bobot teoritis:
Mol kompleks
5(i)
= mol salen = 4 mmol
Bobot kompleks
5(i)
teoritis = mol kompleks × BM kompleks
5(i)
= 4 mmol × 422 g mol
-1×
mmol
1
mol
10
-3= 1.6880 g
Hasil percobaan:
Bobot kertas saring + isi
= 1.5184 g
Bobot kertas saring kosong = 0.5758 g
Bobot isi (salen)
= 1.1584 g – 0.5758 g = 0.9426 g
Rendemen =
100%
teoritis
hasil
percobaan
hasil
×
=
100%
g
1.6880
g
0.9426
×
Lampiran 6 Data Perolehan Kompleks Cu(II)-Salen
Penyiapan:
Bobot salen
= 0.7305 g (2 mmol)
Bobot Cu(OAc)
2·H
2O = 0.3994 g (2 mmol)
Reaksi:
Perhitungan bobot teoritis:
Mol kompleks
5(ii)
= mol salen = 2 mmol
Bobot kompleks
5 (ii)
teoritis
= mol kompleks × BM kompleks
5(ii)
= 2 mmol × 427 g mol
-1×
mmol
1
mol
10
-3= 0.8540 g
Hasil percobaan:
Bobot labu + isi
= 64.3891 g
Bobot labu kosong = 63.8024 g
Bobot isi (salen)
= 64.3891 g – 63.8024 g = 0.5867 g
Rendemen =
100%
teoritis
hasil
percobaan
hasil
×
=
100%
g
0.8540
g
0.5867
×
Lampiran 7 Spektrum FTIR Co(II)-Salen
Lampiran 9 Data Hasil Analisis AAS Kompleks Logam(II)-Salen
Contoh
Kadar logam
dalam contoh
(bpj)
Kadar logam
dalam contoh
(% b/b)
Kadar logam
teoritis dalam
contoh (% b/b)
Rendemen
(%)
Co(II)-salen
41,259
4.13
13.98
29.54
Cu(II)-salen
102,182
10.22
14.88
68.68
Contoh perhitungan (contoh Co(II)-salen)
Koversi ppm menjadi % b/b
41,259 bpj =
100%
salen
-Co(II)
mg
1
salen
-Co(II)
Kg
10
salen
-Co(II)
Kg
1
Co
mg
41,259
×
-6×
= 4.13%
Penentuan kadar logam teoritis dalam kompleks
Bobot moleku Co(II)-salen = 422 g mol
-1Bobot molekul Co
= 59 g mol
-1% Co dalam kompleks
=
100%
salen
-Co(II)
molekul
bobot
Co
atom
bobot
×
=
100%
mol
g
422
mol
g
59
1 --1×
= 13.98%
Rendemen
=
100%
teoritis
hasil
percobaan
hasil
×
=
100%
13.98%
4.13%
×
Lampiran 10 Spektrum FTIR Co(Salen)-Silika
Lampiran 12 Spektrum FTIR Silika Terfungsionalisasi
Lampiran 13 Data Hasil Analisis AAS Katalis Heterogen
Contoh
Kadar logam
dalam contoh
(bpj)
Kadar logam dalam
contoh
(% b/b)
Co(salen)-silika
10,271
1.03
Cu(salen)-silika
13,812
1.38
Contoh perhitungan (Co(salen)-silika):
Koversi ppm menjadi % b/b
10,271 bpj =
100%
silika
-Co(salen)
mg
1
silika
-Co(salen)
Kg
10
silika
-Co(salen)
Kg
1
salen
-Co(II)
mg
10,271
-6×
×