Informasi Dokumen
- Penulis:
- Jamal Lulail
- Pengajar:
- Ir. Subarna, MSi
- Prof. Dr. Winiati P. Rahayu
- Sekolah: Institut Pertanian Bogor
- Mata Pelajaran: Teknologi Pertanian
- Topik: Kajian Hasil Riset Potensi Antioksidan Di Pusat Informasi Teknologi Pertanian Fateta Ipb Serta Aplikasi Ekstrak Bawang Putih, Lada Dan Daun Sirih Pada Dendeng Sapi
- Tipe: Skripsi
- Tahun: 2009
- Kota: Bogor
Ringkasan Dokumen
I. Pendahuluan: Relevansi dengan Objektif Pendidikan dan Hasil Pembelajaran
Pendahuluan skripsi ini memperkenalkan masalah ketengikan dalam bahan pangan, khususnya dendeng sapi, sebagai akibat reaksi oksidasi lemak. Ini langsung relevan dengan objektif pembelajaran dalam bidang teknologi pangan, khususnya mengenai pengawetan makanan dan pemeliharaan mutu. Penggunaan antioksidan sebagai solusi diajukan, menghubungkan topik dengan konsep dasar kimia pangan dan teknologi pengolahan. Tujuan penelitian, yaitu mengkaji hasil riset antioksidan yang ada dan mengaplikasikannya pada dendeng sapi, selaras dengan hasil pembelajaran yang menekankan kemampuan analisis data riset, aplikasi pengetahuan ilmiah dalam konteks praktis, dan penyelesaian masalah. Sasaran penelitian, untuk merekomendasikan hasil kajian kepada pihak yang berkepentingan, melatih mahasiswa dalam hal penyampaian informasi ilmiah secara efektif dan komunikasi sains.
1.1 Rumusan Masalah dan Hipotesis
Bagian ini merumuskan permasalahan utama skripsi, yang berfokus pada potensi dan aplikasi antioksidan alami dalam mencegah ketengikan dendeng sapi. Ini relevan dengan keterampilan pemecahan masalah dan merumuskan hipotesis yang teruji secara ilmiah. Rumusan masalah yang terstruktur akan membantu mahasiswa untuk menganalisis isu secara sistematis dan membimbing proses penelitian. Bagian ini juga membantu mahasiswa mengaplikasikan kemampuan berpikir kritis untuk membangun argumen ilmiah dan menguji hipotesis melalui metode penelitian yang tepat.
1.2 Tujuan dan Manfaat Penelitian
Tujuan penelitian yang tertera, yaitu mengkaji riset antioksidan dan aplikasinya pada dendeng sapi, merupakan contoh objektif pembelajaran yang jelas dan terukur. Ini melatih mahasiswa untuk menetapkan tujuan yang spesifik dan terarah dalam penelitian. Manfaat penelitian, yang berupa rekomendasi bagi masyarakat dan industri pangan, mengajarkan mahasiswa tentang dampak praktis dari riset ilmiah dan pentingnya penerapan pengetahuan untuk menyelesaikan masalah nyata di dunia industri. Mahasiswa juga mempelajari penyusunan laporan ilmiah yang dapat diakses oleh publik.
II. Tinjauan Pustaka: Pengayaan Teori dan Prinsip
Bab tinjauan pustaka memberikan gambaran komprehensif tentang antioksidan, baik sintetik maupun alami, serta mekanisme kerjanya dalam mencegah oksidasi lemak. Ini relevan dengan objektif pembelajaran dalam memahami konsep dasar kimia pangan, khususnya reaksi oksidasi dan antioksidan. Pembahasan mengenai berbagai metode ekstraksi dan pengujian aktivitas antioksidan memperkaya pemahaman mahasiswa tentang metodologi penelitian dan teknik laboratorium. Penjelasan detail tentang ketengikan dan dampaknya terhadap mutu pangan memperluas pengetahuan mahasiswa tentang aspek keamanan dan kualitas pangan.
2.1 Definisi dan Jenis Antioksidan
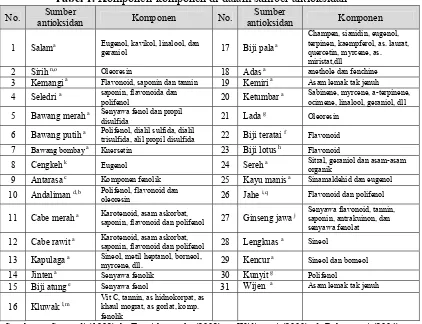
Subbab ini menjelaskan definisi antioksidan dan mengklasifikasikannya berdasarkan sumber (sintetik dan alami). Ini penting untuk memahami dasar-dasar kimia pangan dan bagaimana antioksidan berfungsi. Pengenalan berbagai jenis antioksidan, termasuk sifat dan aplikasi masing-masing, memperkaya wawasan mahasiswa tentang pilihan yang tersedia dalam pengawetan makanan dan meningkatkan kemampuan mereka untuk menganalisis literatur ilmiah.
2.2 Metode Ekstraksi dan Pengujian Antioksidan
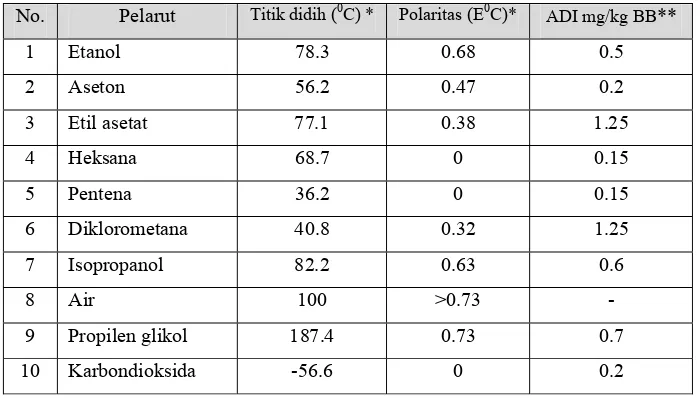
Subbab ini membahas berbagai metode ekstraksi komponen antioksidan dari bahan alami, seperti maserasi, perkolasi, dan soxhlet, beserta prinsip kerja masing-masing. Ini membantu mahasiswa memahami teknik laboratorium yang digunakan dalam penelitian pangan dan keterampilan untuk memilih metode yang paling sesuai. Penjelasan tentang metode pengujian aktivitas antioksidan (AOM, TBA, dll.) mengajarkan mahasiswa tentang analisis kuantitatif dan pentingnya validitas data dalam penelitian. Mahasiswa juga mempelajari pengaplikasian teori dan prinsip ke dalam praktek laboratorium.
2.3 Ketengikan dan Kerusakan Pangan
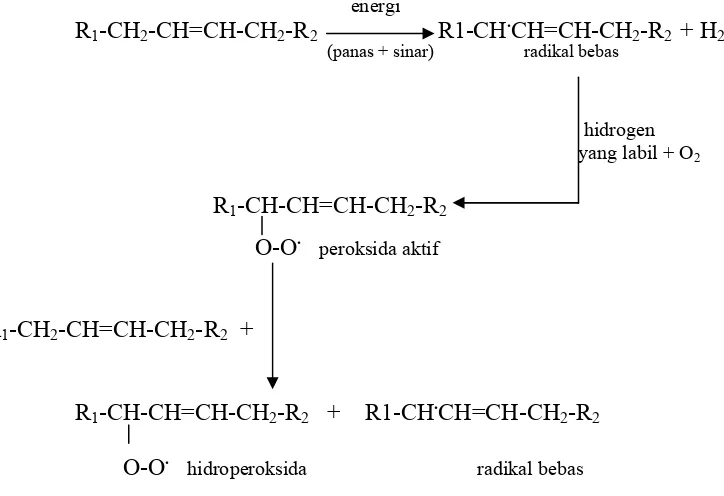
Subbab ini membahas proses ketengikan dalam bahan pangan sebagai akibat dari oksidasi lemak, beserta mekanisme reaksi dan faktor-faktor yang mempengaruhinya. Ini penting untuk memahami permasalahan yang dikaji dalam skripsi dan menghubungkan pengetahuan teori dengan permasalahan praktis di industri pangan. Pemahaman tentang dampak ketengikan terhadap mutu dan keamanan pangan melatih mahasiswa untuk mengkaji aspek keamanan dan kualitas produk pangan.
III. Metodologi Penelitian: Penerapan Prinsip Ilmiah
Bab metodologi menjelaskan langkah-langkah penelitian yang dilakukan, mulai dari kajian pustaka hingga uji aplikasi ekstrak antioksidan pada dendeng sapi. Ini relevan dengan objektif pembelajaran dalam merancang penelitian, mengumpulkan dan menganalisis data, dan menguji hipotesis. Penggunaan metode maserasi untuk ekstraksi dan uji TBA untuk menentukan ketengikan menunjukkan aplikasi praktis dari prinsip-prinsip yang telah dipelajari di bab tinjauan pustaka.
3.1 Kajian Kepustakaan
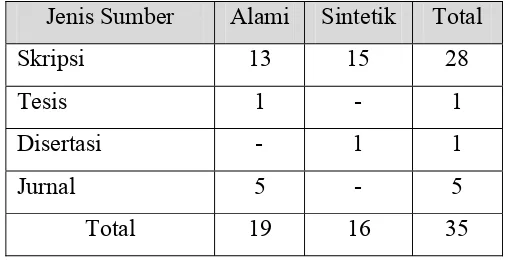
Bagian ini menjelaskan proses identifikasi dan pengkajian sumber informasi tentang antioksidan dari Pusat Informasi Teknologi Pertanian FATETA IPB. Ini melatih mahasiswa dalam pencarian literatur, penilaian kritis terhadap sumber informasi, dan sintesis informasi dari berbagai sumber. Penggunaan sumber-sumber ilmiah yang valid memastikan kualitas riset dan melatih mahasiswa dalam keterampilan mencari informasi yang akurat dan terpercaya.
3.2 Validasi dan Uji Aplikasi
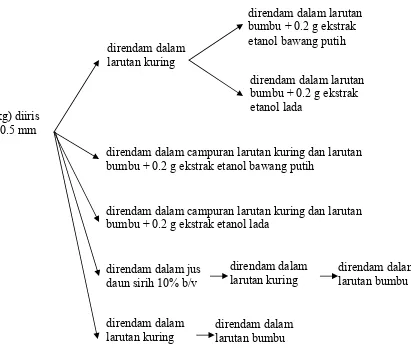
Bagian ini menjelaskan prosedur validasi dan uji aplikasi ekstrak bawang putih, lada, dan daun sirih pada dendeng sapi. Ini merupakan contoh aplikasi metodologi penelitian kuantitatif dan kualitatif dalam bidang teknologi pangan. Pengujian organoleptik melatih mahasiswa dalam pengumpulan data sensori dan analisis data statistik. Prosedur penelitian ini mengajarkan mahasiswa cara mengolah dan menafsirkan data secara ilmiah dan mengelola data penelitian yang tepat.
3.3 Penyusunan Leaflet
Bagian ini menjelaskan proses penyusunan leaflet sebagai bentuk diseminasi hasil penelitian. Ini melatih mahasiswa dalam komunikasi ilmiah dan penyampaian informasi kepada khalayak awam. Pembuatan leaflet sebagai media edukasi menunjukkan kemampuan mahasiswa untuk menyederhanakan informasi ilmiah yang kompleks menjadi bentuk yang mudah dipahami dan diakses oleh masyarakat umum.
IV. Hasil dan Pembahasan: Analisis Data dan Interpretasi
Bab hasil dan pembahasan menyajikan data hasil penelitian dan interpretasinya. Ini relevan dengan objektif pembelajaran dalam menganalisis data, menguji hipotesis, dan menarik kesimpulan berdasarkan bukti empiris. Pembahasan mengenai data TBA dan uji hedonik menunjukkan kemampuan mahasiswa dalam menginterpretasikan data kuantitatif dan kualitatif, serta menghubungkannya dengan teori yang telah dipelajari. Analisis data yang teliti dan sistematis akan meningkatkan keterampilan mahasiswa dalam menyelesaikan masalah penelitian.
4.1 Kajian Kepustakaan: Sintesis Informasi
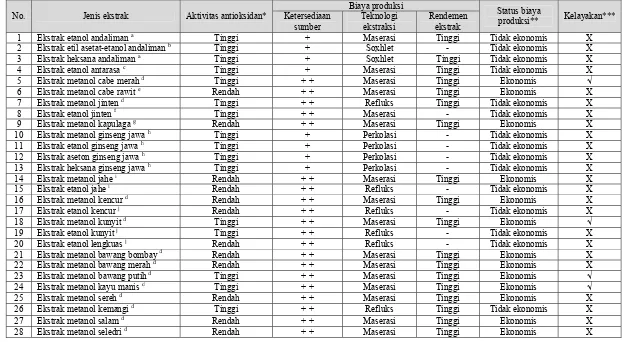
Subbab ini memaparkan hasil kajian kepustakaan mengenai potensi antioksidan alami dan aplikasinya dalam bahan pangan. Ini menunjukkan kemampuan mahasiswa dalam menyaring, menganalisis dan mensintesis informasi dari berbagai sumber ilmiah. Analisis ini melatih mahasiswa dalam kemampuan literasi sains, berpikir kritis dan mengintegrasikan pengetahuan dari berbagai sumber. Penulisan subbab ini juga melatih mahasiswa dalam penulisan ilmiah yang baik.
4.2 Validasi dan Uji Aplikasi: Analisis Data Empiris
Subbab ini memaparkan hasil validasi dan uji aplikasi ekstrak antioksidan pada dendeng sapi. Ini menunjukkan kemampuan mahasiswa dalam menganalisis data empiris secara kuantitatif dan kualitatif. Analisis data TBA dan hasil uji hedonik menunjukkan keterampilan mahasiswa dalam mengolah dan menafsirkan data statistik dan data sensori. Pembahasan yang kritis menguji hipotesis yang diajukan dan memberikan kesimpulan yang berdasar pada bukti empiris.
4.3 Rekomendasi Aplikasi Antioksidan dan Leaflet
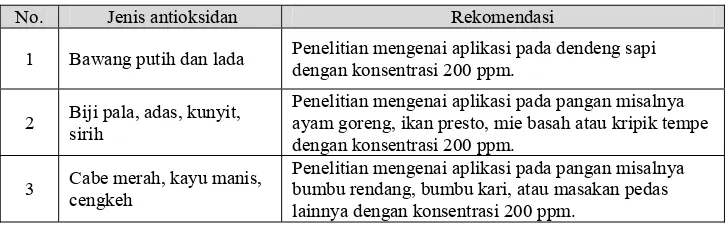
Subbab ini memberikan rekomendasi aplikasi antioksidan berdasarkan hasil penelitian dan menjelaskan mengenai leaflet yang dibuat. Ini menunjukkan kemampuan mahasiswa dalam memberikan rekomendasi berbasis data ilmiah dan kemampuan dalam penyampaian informasi yang efektif. Rekomendasi yang diberikan akan membantu pembaca dalam memahami implikasi praktis dari penelitian dan penerapannya dalam kehidupan sehari-hari. Pembuatan leaflet yang informatif dan mudah dipahami menunjukkan kemampuan mahasiswa dalam menyampaikan hasil penelitian kepada khalayak luas.
V. Kesimpulan dan Saran: Refleksi dan Rekomendasi
Bab kesimpulan dan saran merangkum temuan penelitian dan memberikan saran untuk penelitian selanjutnya. Ini relevan dengan objektif pembelajaran dalam menarik kesimpulan berdasarkan bukti empiris dan merumuskan implikasi penelitian. Saran yang diberikan dapat memandu penelitian selanjutnya dan meningkatkan pemahaman tentang topik yang dikaji. Bab ini melatih mahasiswa untuk merefleksikan proses penelitian dan memberikan rekomendasi yang konstruktif untuk penelitian di masa mendatang.
5.1 Kesimpulan
Bagian kesimpulan meringkas temuan utama penelitian, menekankan kontribusi penelitian terhadap pengetahuan dan praktik di bidang teknologi pangan. Ini penting untuk merangkum inti dari penelitian dan menunjukkan kemampuan mahasiswa dalam mengkomunikasikan hasil penelitian secara ringkas dan jelas. Kesimpulan yang terstruktur dan sistematis akan mempermudah pembaca dalam memahami pokok bahasan dan hasil utama penelitian.
5.2 Saran
Bagian saran memberikan rekomendasi untuk penelitian selanjutnya, menunjukkan kemampuan mahasiswa dalam menentukan arah penelitian di masa depan. Saran yang diberikan dapat berupa pengembangan metode penelitian, perluasan cakupan penelitian, atau topik penelitian terkait. Saran yang konstruktif dan relevan akan bermanfaat bagi peneliti lain yang ingin melanjutkan atau mengembangkan riset serupa.