KARAKTERISTIK DEHIDRASI OSMOTIK IRISAN MANGGA
CENGKIR (
Mangifera indica
L.) PADA BERBAGAI KETEBALAN
DAN KONSENTRASI LARUTAN GULA
SKRIPSI
YULIANA
F14080075
FAKULTAS TEKNOLOGI PERTANIAN
INSTITUT PERTANIAN BOGOR
OSMOTIC DEHYDRATION CHARACTERISTICS OF SLICE MANGO
CENGKIR (Mangifera indica L.) IN VARIOUS THICKNESSES AND
CONCENTRATION OF SUGAR SOLUTIONS
Yuliana and Leopold Oscar Nelwan
Department of Mechanical and Biosystem Engineering, Faculty of Agricultural Technology, Bogor Agricultural university, IPB Darmaga Campus, PO Box 220, Bogor, West Java, Indonesia.
Phone 62 251 864622, e-mail : yulianna_tepipb45@yahoo.com
ABSTRACT
Osmotic dehydration is one of the alternative methods commonly applied on pre-drying fruits like mango.The objectives of this study were to obtain effect of sugar concentration and thickness of mango slice on changes of osmotic dehydration characteristic and physical properties changes of mango slice in osmotic dehydration using temperature 30ºC, and in osmotic dehydration at room temperature for 48 hours. Thickness of mango slice that used were 0.5 cm, 1 cm, and 1.5 cm, while concentration of osmotic solution were 30ºBx, 45°Bx and 60°Bx. Observations were carried out for 6 hours at 30ºC and 48 hours at room temperature. High concentration of osmotic solution increased WL, but high solid gain trend in medium concentration of osmotic solution (45ºBx) was found. Increasing of concentration osmotic solution increased shrinkage, WR, density and porosity. Decreasing of thickness mango slice increased value of WL, WR and shrinkage. While the thickness of mango slice didn’t affect SG value, density and porosity of sampel increased during the process or osmotic dehydration. The best sample was thickness 0.5 cm using 60ºBx osmotic solution. It has lower water content, high value of WL, and lower SG value. Azuara modeling can be used as data validation WL obtained of R2 values 0.954 to 0.993.
YULIANA. F14080075.
Karakteristik Dehidrasi Osmotik Irisan Mangga
Cengkir (Mangifera indica L.) pada Berbagai Ketebalan dan Konsentrasi
Larutan Gula. Di bawah bimbingan Leopold Oscar Nelwan. 2012
RINGKASAN
Mangga (Mangifera indica L.) adalah salah satu jenis buah-buahan khas daerah tropis yang banyak dibudidayakan di Indonesia. Menurut Badan Pusat Statistik Nasional jumlah produksi mangga pada tahun 2011 mencapai 2.13 juta ton. Mangga merupakan buah musiman yang jumlah produksinya melimpah saat musim panen dan akan sulit dijumpai pada waktu di luar musim panen. Besarnya produksi buah mangga yang melimpah tidak diikuti dengan besarnya konsumsi buah mangga. Jumlah produksi lebih besar dibandingkan konsumsinya sehingga masih banyak buah yang dikonsumsi secara tidak langsung, maka peran teknologi pascapanen sangat penting untuk meningkatkan nilai mutu buah mangga yang tidak dikonsumsi secara langsung. Mangga memiliki kadar air yang cukup tinggi sehingga mudah mengalami kerusakan. Oleh karena itu, diperlukan pengolahan pascapanen untuk memperpanjang daya simpan. Salah satu pengolahan pascapanen yang dapat dilakukan adalah metode pengeringan, namun metode tersebut menyebabkan susut yang cukup tinggi dan pada metode penjemuran produk yang dikeringkan dapat terkontaminasi oleh kotoran sehingga produk menjadi kurang steril. Dehidrasi osmotik merupakan salah satu metode prapengeringan alternatif yang umumnya digunakan untuk mencegah penyusutan bahan yang lebih besar.
Tujuan dari penelitian ini adalah mengetahui pengaruh konsentrasi larutan gula dan ukuran ketebalan buah terhadap karakteristik dehidrasi osmotik irisan mangga yaitu kadar air, water loss
(WL) dan solid gain (SG) serta mengamati perubahan sifat fisik yang terjadi pada proses dehidrasi osmotik irisan buah mangga antara lain penyusutan berat, penyusutan volume, densitas dan porositas.
Penelitian dilaksanakan dari bulan April 2012 hingga September 2012 di Laboratorium Energi dan Elektrifikasi Pertanian, Institut Pertanian Bogor. Rancangan percobaan yang digunakan dalam penelitian ini adalah dengan 2 perlakuan yaitu ukuran ketebalan irisan mangga, serta konsentrasi larutan osmotik. Ukuran ketebalan irisan mangga yang digunakan yaitu 0.5 cm, 1 cm, dan 1.5 cm, sedangkan konsentrasi larutan osmotik yang digunakan yaitu 30ºBx, 45ºBx, dan 60ºBx. Dehidrasi osmotik dilakukan pada suhu rendah yaitu 30ºC dan suhu ruang. Sampel irisan mangga yang telah siap dimasukkan ke dalam wadah sampel, kemudian sampel tersebut dimasukkan ke dalam osmotic dehydrator. Larutan gula yang digunakan sebagai larutan osmotik juga dimasukkan ke dalam osmotic dehydrator. Perbandingan massa antara sampel dengan larutan osmotik yang digunakan adalah 1:15. Pengamatan dilakukan selama 6 jam dan 48 jam. Masing-masing sampel dilakukan pengukuran kadar air, massa, dan volume setelah osmotik. Dari data yang diperoleh dapat dihitung kadar air, densitas, penyusutan volume dan penyusutan berat, WL, SG, densitas dan porositas. Pada dehidrasi osmotik suhu ruang, kadar air, WL, SG, densitas dan porositas hanya diukur pada saat awal dan akhir proses.
Water loss (WL) merupakan salah satu parameter yang menunjukkan adanya air yang keluar dari sampel. Konsentrasi larutan osmotik sangat mempengaruhi besarnya WL sampel. Sampel yang memiliki nilai WL terbesar adalah sampel yang memiliki ukuran ketebalan 0.5 cm dengan menggunakan larutan osmotik 60ºBx (M0C2). Selain WL, SG juga dialami oleh sampel selama dehidrasi osmotik. Solid gain (SG) merupakan besarnya padatan terlarut yang masuk ke dalam sampel. Konsentrasi larutan osmotik mempengaruhi perubahan nilai SG yang terjadi pada sampel. Proses dehidrasi osmotik juga menyebabkan perubahan densitas dan porositas. Densitas dan porositas dipengaruhi oleh konsentrasi larutan osmotik yang digunakan selama proses dehidrasi.
KARAKTERISTIK DEHIDRASI OSMOTIK IRISAN MANGGA CENGKIR
(Mangifera indica L.) PADA BERBAGAI KETEBALAN DAN KONSENTRASI
LARUTAN GULA
SKRIPSI
Sebagai salah satu syarat untuk Memperoleh gelar
SARJANA TEKNOLOGI PERTANIAN
pada Departemen Teknik Mesin dan Biosistem
Fakultas Teknologi Pertanian
Institut Pertanian Bogor
Oleh
YULIANA
F14080075
FAKULTAS TEKNOLOGI PERTANIAN
INSTITUT PERTANIAN BOGOR
BOGOR
Judul Skripsi : Karakteristik Dehidrasi Osmotik Irisan Mangga Cengkir (Mangifera indica L.) pada Berbagai Ketebalan dan Konsentrasi Larutan Gula
Nama : Yuliana NIM : F14080075
Menyetujui,
Dosen Pembimbing Akademik
Dr. Ir. Leopold Oscar Nelwan, M.Si. NIP. 19701208 199903 1 001
Mengetahui : Ketua Departemen,
PERNYATAAN MENGENAI SKRIPSI DAN
SUMBER INFORMASI
Saya menyatakan dengan sebenar-benarnya bahwa skripsi dengan judul Karakteristik Dehidrasi Osmotik Irisan Mangga Cengkir (Mangifera indica L.) pada Berbagai Ketebalan dan Konsentrasi Larutan Gula adalah hasil karya saya sendiri dengan arahan dosen pembimbing akademik, dan belum diajukan dalam bentuk apapun pada perguruan tinggi manapun. Sumber informasi yang berasal atau dikutip dari karya yang diterbitkan maupun tidak diterbitkan dari penulis lain telah disebutkan dalam teks dan dicantumkan dalam Daftar Pustaka di bagian akhir skripsi ini.
Bogor, November 2012 Yang membuat pernyataan
BIODATA PENULIS
v
KATA PENGANTAR
Puji syukur kehadirat Allah SWT atas segala rahmat dan karunia-Nya yang telah diberikan kepada penulis, sehingga pada akhirnya penulis dapat meyelesaikan pelaksanaan Penelitian dan penulisan laporan skripsi. Penelitian dilaksanakan di Laboratorium Energi dan Elektrifikasi Pertanian dengan judul Karakteristik Dehidrasi Osmotik Irisan Mangga Cengkir (Mangifera Indica L.) pada Berbagai Ketebalan dan Konsentrasi Larutan Gula. Pelaksanaan penelitian dilaksanakan antara bulan April – September 2012.
Pada kesempatan ini penulis menyampaikan terima kasih kepada
1. Dr. Ir. Leopold O. Nelwan, M. Si selaku dosen pembimbing akademik yang telah memberikan bimbingan dan arahan kepada penulis.
2. Prof. Dr. Ir. Tineke Mandang, M.S dan Dr. Ir. Dyah Wulandani, M.Si selaku dosen penguji skripsi yang telah memberikan kritik dan saran yang membangun bagi penulis.
3. Ayah (Muhammad Asrori), ibu (Suharti), dan adik-adikku (Helmi Wildan Rizaldi dan Almeyra Hafista Fauzia) yang selalu memberikan dukungan dan doannya.
4. Teman-teman satu bimbingan Fibula Yudisaputro, Yulfi Nizzatal Maulia, Delimy Okta Riski, dan Rizki Muhammad Thariq yang telah membantu dalam penelitian.
5. Pak Harto, mas Firman dan pak Suliyaden yang telah memberikan bantuan dalam penelitian. 6. Teman-teman satu istana “wisma agung 2”, nenek Derry, ibu tiri Icha, dan adik-adik tiriku gita
dan tia, Tri novita Sari dan Raizummi Fil’aini yang telah memberikan semangat serta bantuannya dalam penelitian.
7. Seluruh keluarga besar Magenta TEP 45 yang telah memberikan bantuan.
8. Seluruh pihak yang telah mendukung dan membantu penulis dalam menyelesaikan penelitian. Penulis berharap agar skripsi ini dapat bermanfaat dan memberikan kontribusi yang nyata terhadap perkembangan ilmu pengetahuan.
Bogor, November 2012
vi
DAFTAR ISI
halaman
KATA PENGANTAR ...v
DAFTAR ISI ...vi
DAFTAR TABEL ...vii
DAFTAR GAMBAR ...ix
DAFTAR LAMPIRAN ...xi
I. PENDAHULUAN ...1
1.1LATAR BELAKANG ...1
1.2TUJUAN ...2
II. TINJAUAN PUSTAKA ...3
2.1MANGGA ...3
2.2 DEHIDRASI OSMOTIK ...5
III. METODE PENELITIAN ...9
3.1WAKTU DAN TEMPAT ...9
3.2BAHAN DAN ALAT ...9
3.3PROSEDUR PENELITIAN ...10
3.4RANCANGAN PENELITIAN ...13
3.5PENGAMATAN ...13
3.6ANALISIS DATA ...14
IV. HASIL DAN PEMBAHASAN ...18
4.1 DEHIDRASI OSMOTIK PADA SUHU 30ºC ...18
4.1.1KADAR AIR ...18
4.1.2TINGKAT KEHILANGAN AIR (WATER LOSS/WL) ...19
4.1.3SOLID GAIN (SG) ...22
4.1.4PENYUSUTAN VOLUME (SHRINGKAGE) DAN PENYUSUTAN BERAT (WEIGHT REDUCTION) ...23
4.1.6DENSITAS DAN POROSITAS ...27
4.2 DEHIDRASI OSMOTIK PADA SUHU RUANG ...30
V. SIMPULAN DAN SARAN ...36
5.1 SIMPULAN ...36
5.2 SARAN ...36
DAFTAR PUSTAKA ...37
vii
DAFTAR TABEL
halaman
Tabel 1. Produksi buah mangga di Indonesia ... 3
Tabel 2. Sifat fisika dan kimia daging buah beberapa varietas mangga ... 5
Tabel 3. Kombinasi perlakuan dehidrasi osmotik ... 13
Tabel 4. Nilai parameter dan koefisien determinasi dari perhitungan WL dengan menggunakan permodelan Azuara ... 22
Tabel 5. Data massa dan penyusutan massa sampel 0.5 cm 60ºBx ... 44
Tabel 6. Data massa dan penyusutan massa sampel 1 cm 60ºBx ... 45
Tabel 7. Data massa dan penyusutan massa sampel 1.5 cm 60ºBx ... 46
Tabel 8. Data massa dan penyusutan massa sampel 0.5 cm 45ºBx ... 47
Tabel 9. Data massa dan penyusutan massa sampel 1 cm 45ºBx ... 48
Tabel 10. Data massa dan penyusutan massa sampel 1.5 cm 45ºBx ... 49
Tabel 11. Data massa dan penyusutan massa sampel 0.5 cm 30ºBx ... 50
Tabel 12. Data massa dan penyusutan massa sampel 1 cm 30ºBx ... 51
Tabel 13. Data massa dan penyusutan massa sampel 1.5 cm 30ºBx ... 52
Tabel 14. Data volume dan penyusutan volume sampel 0.5 cm 60ºBx ... 53
Tabel 15. Data volume dan penyusutan volume sampel 1 cm 60ºBx ... 54
Tabel 16. Data volume dan penyusutan volume sampel 1.5 cm 60ºBx ... 55
Tabel 17. Data volume dan penyusutan volume sampel 0.5 cm 45ºBx ... 56
Tabel 18. Data volume dan penyusutan volume sampel 1 cm 45ºBx ... 57
Tabel 19. Data volume dan penyusutan volume sampel 1.5 cm 45ºBx ... 58
Tabel 20. Data volume dan penyusutan volume sampel 0.5 cm 30ºBx ... 59
Tabel 21. Data volume dan penyusutan volume sampel 1 cm 30ºBx ... 60
Tabel 22. Data volume dan penyusutan volume sampel 1.5 cm 30ºBx ... 61
Tabel 23. Data kadar air sampel 0.5 cm 60ºBx ... 62
Tabel 24. Data kadar air sampel 1 cm 60ºBx ... 63
Tabel 25. Data kadar air sampel 1.5 cm 60ºBx ... 64
Tabel 26. Data kadar air sampel 0.5 cm 45ºBx ... 65
Tabel 27. Data kadar air sampel 1 cm 45ºBx ... 66
Tabel 28. Data kadar air sampel 1.5 cm 45ºBx ... 67
Tabel 29. Data kadar air sampel 0.5 cm 30ºBx ... 68
Tabel 30. Data kadar air sampel 1 cm 30ºBx ... 69
Tabel 31. Data kadar air sampel 1.5 cm 30ºBx ... 70
Tabel 32. Data solid gain, water loss, dan porositas sampel 0.5 cm 60ºBx ... 71
Tabel 33. Data solid gain, water loss, dan porositas sampel 1 cm 60ºBx ... 72
Tabel 34. Data solid gain, water loss, dan porositas sampel 1.5 cm 60ºBx ... 73
Tabel 35. Data solid gain, water loss, dan porositas sampel 0.5 cm 45ºBx ... 74
Tabel 36. Data solid gain, water loss, dan porositas sampel 1 cm 45ºBx ... 75
Tabel 37. Data solid gain, water loss, dan porositas sampel 1.5 cm 45ºBx ... 76
Tabel 38. Data solid gain, water loss, dan porositas sampel 0.5 cm 30ºBx ... 77
Tabel 39. Data solid gain, water loss, dan porositas sampel 1 cm 30ºBx ... 78
viii
Tabel 41. Data sampel 0.5 cm 60 Bx ... 80
Tabel 42. Data sampel 1 cm 60 Bx ... 80
Tabel 43. Data sampel 1.5 cm 60 Bx ... 81
Tabel 44. Data sampel 0.5 cm 45 Bx ... 81
Tabel 45. Data sampel 1 cm 45 Bx ... 82
Tabel 46. Data sampel 1.5 cm 45 Bx ... 82
Tabel 47. Data sampel 0.5 cm 30 Bx ... 83
Tabel 48. Data sampel 1 cm 30 Bx ... 83
ix
DAFTAR GAMBAR
halaman
Gambar 1. Mangga cengkir (indramayu) ... 4
Gambar 2. Proses osmosis dua liquid ... 6
Gambar 3. Rangkaian osmotic dehydrator ... 9
Gambar 4. Diagram alir penelitian ... 12
Gambar 5. Skema pengukuran volume sampel ... 15
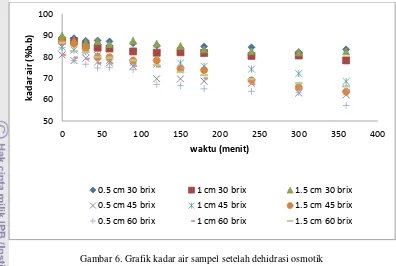
Gambar 6. Grafik kadar air sampel setelah dehidrasi osmotik ... 19
Gambar 7. Grafik water loss dehidrasi osmotik untuk berbagai ukuran dan konsentrasi larutan gula setelah 6 jam ... 20
Gambar 8. Grafik water loss menggunakan perhitungan dari persamaan Azuara dan data pada larutan osmotik 30ºBx ... 20
Gambar 9. Grafik water loss menggunakan perhitungan dari persamaan Azuara dan data pada larutan osmotik 45ºBx ... 21
Gambar 10. Grafik water loss menggunakan perhitungan dari persamaan Azuara dan data pada larutan osmotik 60ºBx ... 21
Gambar 11. Grafik solid gain selama dehidrasi osmotik ... 22
Gambar 12. Grafik penyusutan volume sampel setelah dehidrasi osmotik ... 24
Gambar 13. Grafik penyusutan berat sampel setelah dehidrasi osmotik ... 25
Gambar 14. Grafik rasio antara penyusutan volumedan penyusutan berat ... 25
Gambar 15. Grafik hubungan antara penyusutan volumedan penyusutan berat ... 26
Gambar 16. Skema penyusutan volume sampel ... 26
Gambar 17. Grafik densitas riil sampel setelah dehidrasi ... 27
Gambar 18. Grafik densitas apparent sampel setelah dehidrasi... 27
Gambar 19. Grafik hubungan antara densitas riil dengan penyusutan berat selama dehidrasi Osmotik ... 28
Gambar 20. Grafik porositas sampel selama dehidrasi osmotik... 28
Gambar 21. Grafik rasio porositas terhadap penyusutan volume sampel selama dehidrasi Osmotik ... 29
Gambar 22. Grafik hubungan antara porositas dan penyusutan berat ... 30
Gambar 23. Kadar air akhir bahan pada dehidrasi osmotik dengan suhu ruang... 31
Gambar 24. Water loss sampel pada dehidrasi osmotik dengan suhu ruang ... 32
Gambar 25. Solid gain sampel pada dehidrasi osmotik dengan suhu ruang ... 32
Gambar 26. Penyusutan volumesampel setelah dehidrasi osmotik dengan suhu ruang ... 33
Gambar 27. Penyusutan beratsampel setelah dehidrasi osmotik dengan suhu ruang ... 34
Gambar 28. Densitas sampel setelah dehidrasi osmotik dengan suhu ruang ... 34
Gambar 29. Porositas sampel setelah dehidrasi osmotik dengan suhu ruang ... 35
Gambar 30. Pengukuran volume ... 40
Gambar 31. Saringan sampel ... 40
Gambar 32. Foto sampel dengan ukuran ketebalan 0.5 cm dan larutan osmotik 60ºBx ... 41
Gambar 33. Foto sampel dengan ukuran ketebalan 0.5 cm dan larutan osmotik 45ºBx ... 41
Gambar 34. Foto sampel dengan ukuran ketebalan 0.5 cm dan larutan osmotik 30ºBx ... 41
x
Gambar 36. Foto sampel dengan ukuran ketebalan 1 cm dan larutan osmotik 45ºBx ... 42
Gambar 37. Foto sampel dengan ukuran ketebalan 1 cm dan larutan osmotik 30ºBx ... 42
Gambar 38. Foto sampel dengan ukuran ketebalan 1.5 cm dan larutan osmotik 60ºBx ... 42
Gambar 39. Foto sampel dengan ukuran ketebalan 1.5 cm dan larutan osmotik 45ºBx ... 42
xi
DAFTAR LAMPIRAN
halaman
Lampiran 1. Pengukuran volume sampel dan saringan ... 40
Lampiran 2. Foto sampel sebelum dan setelah dehidrasi osmotik ... 41
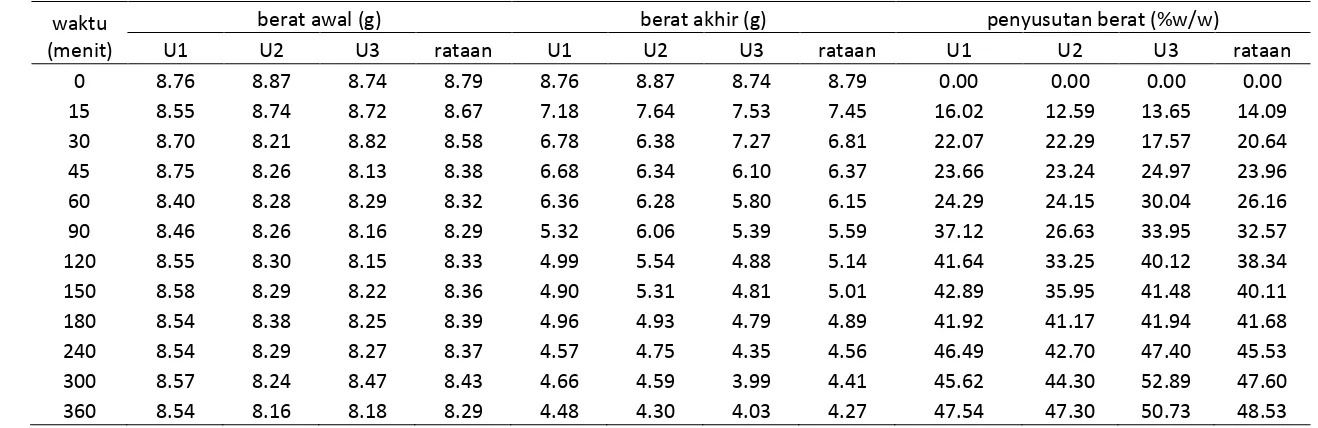
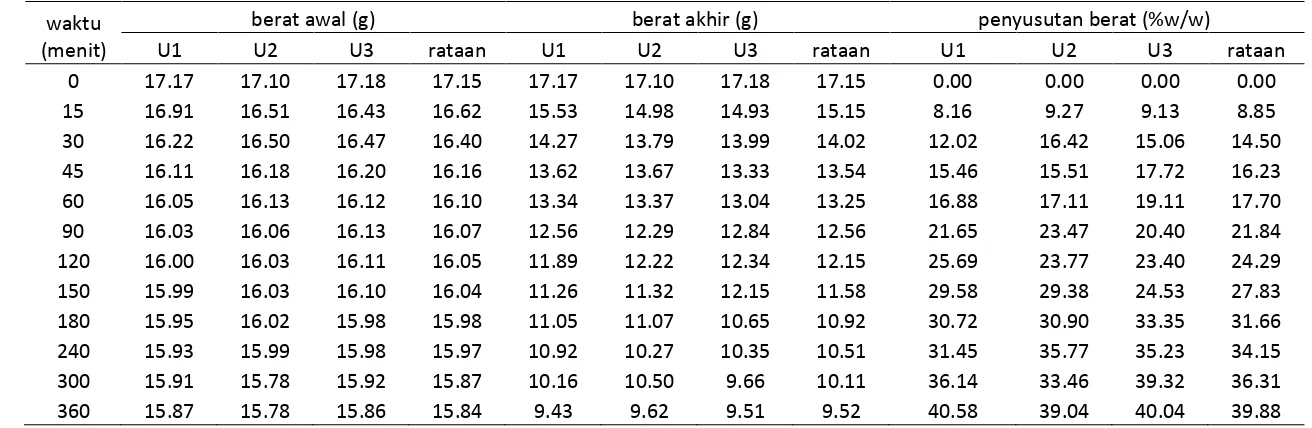
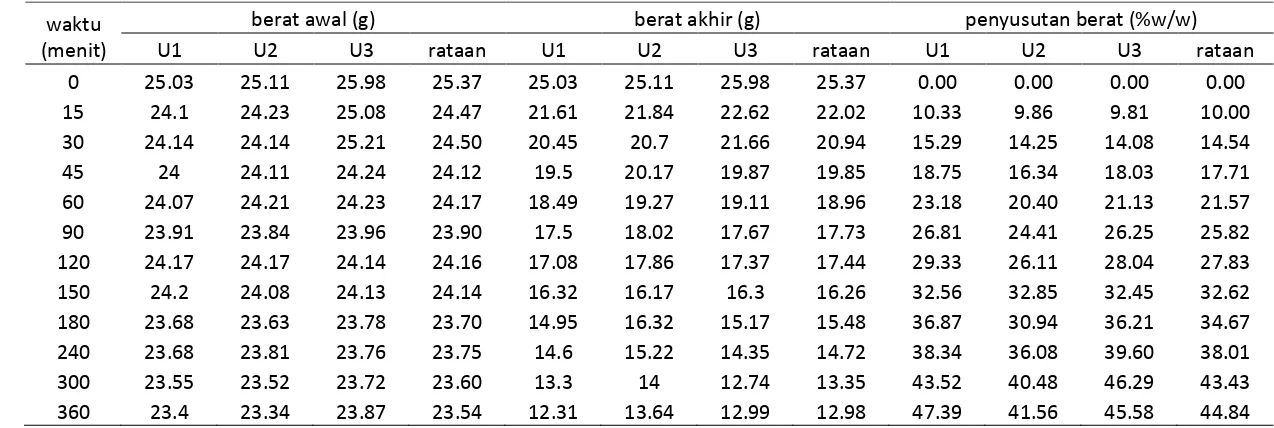
Lampiran 3. Data berat dan penyusutan berat pada suhu 30ºC ... 44
Lampiran 4. Data volume dan penyusutan volume pada suhu 30ºC ... 53
Lampiran 5. Data kadar air pada suhu 30ºC ... 62
Lampiran 6. Data solid gain, water loss, dan porositas pada suhu 30ºC ... 71
1
I.
PENDAHULUAN
1.1
LATAR BELAKANG
Mangga (Mangifera indica L.) adalah salah satu jenis buah-buahan khas daerah tropis yang banyak dibudidayakan di Indonesia. Buah ini banyak dibudidayakan karena mengandung gizi yang diperlukan oleh tubuh yaitu protein, lemak, karbohidrat, kalsium, fosfor, zat besi, vitamin A, vitamin C dan air. Menurut Badan Pusat Statistik Nasional jumlah produksi mangga pada tahun 2011 mencapai 2.13 juta ton. Mangga merupakan buah musiman sehingga jumlah produksi mangga melimpah pada bulan tertentu yaitu saat musim panen dan mangga akan sulit dijumpai pada waktu di luar musim panen. Buah-buahan merupakan bahan pangan sumber vitamin yang mudah rusak. Kerusakan buah di Indonesia cukup tinggi. Hal ini disebabkan oleh penerapan teknologi pascapanen dan teknologi pengolahan buah-buahan yang kurang baik. Warna buah cepat sekali berubah oleh pengaruh fisika misalnya sinar matahari dan pemotongan, serta pengaruh biologis (jamur) sehingga mudah menjadi busuk. Besarnya produksi buah mangga yang melimpah pada saat musimnya tidak diikuti dengan besarnya konsumsi buah mangga. Jumlah produksi lebih besar dibandingkan konsumsinya menyebabkan banyaknya buah yang dikonsumsi secara tidak langsung, maka peran teknologi pascapanen sangat penting untuk meningkatkan nilai mutu buah mangga yang tidak dikonsumsi secara langsung.
Mangga memiliki kadar air yang cukup tinggi sehingga mudah mengalami kerusakan akibat aktivitas mikroba. Oleh karena itu, diperlukan pengolahan pascapanen sehingga buah mangga dapat disimpan lebih lama. Selain disimpan dalam bentuk mangga utuh, mangga juga dapat diolah menjadi produk olahan yang memiliki nilai ekonomi lebih tinggi dan memiliki daya simpan yang lebih lama. Salah satu pengolahan pascapanen yang dapat dilakukan adalah dengan metode pengeringan. Pengeringan merupakan suatu proses pengurangan kadar air sehingga buah dapat disimpan lebih lama. Terdapat beberapa metode pengeringan yang dapat digunakan untuk pengolahan pascapanen mangga antara lain penjemuran, pengeringan buatan dengan menggunakan alat pengering, dan pengeringan dengan cara pembekuan, namun dengan menggunakan metode-metode tersebut produk yang dikeringkan akan mengalami susut yang cukup tinggi dan pada metode penjemuran produk yang dikeringkan dapat terkontaminasi oleh kotoran sehingga produk menjadi kurang steril.
2
Proses dehidrasi menggunakan larutan hipertonik seperti larutan gula dan garam. Dehidrasi osmotik mampu mengeluarkan air dari bahan tanpa ada perubahan fase air sehingga energi yang dibutuhkan lebih rendah karena tidak memerlukan panas laten untuk merubah fase air dari cair menjadi uap. Pada prinsipnya proses difusi mendasari dehidrasi osmotik, oleh karena itu jarak tempuh air yang keluar dari bahan dapat mempengaruhi laju kehilangan air (WL) ataupun perolehan padatan yang masuk ke dalam bahan (SG). Pada penelitian ini akan diinvestigasi mengenai keterkaitan produk pada berbagai konsentrasi larutan terhadap karakteristik dan sifat fisiknya.
Suhu memberikan pengaruh positif (sebanding) terhadap kehilangan air (water loss/WL) dan perolehan padatan (solid gain/SG) pada buah mangga dengan perlakuan pengeringan osmotik (Ramalo dan Mascheroni 2005 diacu dalam Jannah 2011). Akan tetapi dalam rangka penghematan energi, perlu dikaji proses dehidrasi osmotik yang dilakukan pada suhu rendah yaitu 30ºC dan suhu ruang. Selain suhu, waktu yang digunakan dalam dehidrasi osmotik juga mempengaruhi perubahan karakteristik pada dehidrasi osmotik. WL, SG dan penyusutan berat akan meningkat terhadap waktu (Nowakunda et al. 2004). Sifat fisik yang mencakup penyusutan volume, perubahan densitas dan porositas sangat terkait erat dengan proses pengeringan termasuk dehidrasi osmotik. Selain mempengaruhi kualitas, sifat fisik ini juga mempengaruhi fenomena pindah panas dan massa. Oleh karena itu, diperlukan kajian mengenai beberapa parameter yang mempengaruhi dehidrasi osmotik seperti pengaruh konsentrasi larutan gula dan ukuran irisan mangga dalam dehidrasi osmotik serta karakteristik fisiknya yaitu kadar air, penyusutan berat, penyusutan volume, densitas, WL, SG, dan porositas irisan mangga setelah diberikan perlakuan dehidrasi osmotik.
Percobaan dehidrasi osmotik pada suhu 30ºC membutuhkan heater dan untuk menyeragamkan suhu diperlukan pengaduk. WL, SG, dan sifat-sifat fisik yang telah dijelaskan di atas diamati setiap interval waktu tertentu untuk mendapatkan perubahannya sepanjang waktu. Percobaan pada suhu ruang tidak menggunakan heater sehingga pengadukan tidak dilakukan. Fokus pada percobaan ini adalah untuk melihat potensi dehidrasi osmotik pada kondisi tersebut dengan waktu proses yang panjang yaitu 48 jam. Parameter yang diamati (kadar air, WL, SG, densitas apparent, dan porositas) hanya dilakukan pada awal dan akhir proses.
1.2
TUJUAN
3
II.
TINJAUAN PUSTAKA
2.1
MANGGA
Mangga merupakan tanaman buah tahunan berupa pohon yang berasal dari India. Tanaman ini kemudian menyebar ke wilayah Asia Tenggara termasuk Malaysia dan Indonesia. Tanaman mangga dapat dijumpai tumbuh dan berproduksi di semua provinsi di Indonesia. Pulau jawa, khususnya Jawa Timur merupakan daerah yang paling banyak membudidayakan tanaman mangga dengan pangsa produksi hampir 50% dari total produksi nasional tahun 2000 (Broto 2003). Klasifikasi buah mangga berdasarkan sifat-sifatnya adalah sebagai berikut :
Divisi :Spermatophyta Subdivisi :Angiospermae Kelas :Dicotyledoneae Ordo :Sapindales Keluarga :Anacardiaceae Genus :Mangifera
Spesies :Mangifera indica L.
Mangga dapat tumbuh pada berbagai jenis dan struktur tanah, asal tanah tersebut tidak menunjukakan lapisan cadas dan dangkal. Musim kemarau yang cocok untuk tanaman mangga adalah sekitar 2–8 bulan dalam setahun. Ketinggian tempat antara 0–300 m dpl cocok untuk tanaman mangga, karena bisa menghasilkan produksi yang berkualitas tinggi, sedangkan mangga yang di tanam dengan ketinggian lebih dari 300 m dpl, memberikan hasil dan kualitas yang kurang baik. Kisaran pH yang cocok untuk tanaman mangga antara 5.5-7.0 (Broto et al. 1994).
Mangga masih dapat tumbuh sehat pada temperatur 4ºC-10ºC. Namun kondisi itu bukan merupakan temperatur optimum untuk pertumbuhan mangga. Temperatur pertumbuhan mangga yang optimum berkisar antara 24ºC-27ºC. Mangga membutuhkan curah hujan minimal 1000 mm, dan musim kering 4-6 bulan per tahun. Setiap bulan rata-rata hujan tidak lebih dari 60 mm. Di Jawa, mangga berbunga pada bulan Juli-Agustus, panen antara bulan September-November (Pracaya 2001). Produksi buah mangga di Indonesia dapat di lihat pada Tabel 1.
Tabel 1. Produksi buah mangga di Indonesia
Tahun Jumlah Produksi (ton) 2007 2008 2009 2010 2011*) 1,818,619 2,105,085 2,243,440 1,287,287 2,129,608
4
Menurut Pracaya (2011) buah mangga termasuk kelompok buah batu berdaging dengan panjang buah antara 2.5 – 30 cm. Bentuknya ada yang bulat, bulat telur, bulat memanjang, dan pipih. Warna buah bermacam-macam tergantung varietasnya, ada yang hijau, kuning, merah, atau campuran masing-masing warna itu. Komponen daging buah mangga yang paling banyak adalah air dan karbohidrat. Selain itu, juga mengandung protein, lemak, macam-macam asam, vitamin, mineral, tanin, zat warna dan zat yang mudah menguap sehingga menciptakan aroma harum khas buah mangga. Buah mangga mengandung 4800 I.U (International Unit) vitamin A, sekitar 13-80 mg vitamin C per 100 g daging buah masak, 0.04 mg vitamin B1 dan 0.05 mg vitamin B2.
Mangga mempunyai kulit buah agak tebal, berbintik-bintik kelenjar, berwarna hijau kekuning-kuningan atau kemerahan bila masak. Ciri warna buah masak yaitu berwarna merah jingga, kunig atau
krem, manis sampai masam dengan banyak air, berbau kuat sampai lemah, penebalan lapisan „bedak‟,
pemunculan bintik coklat pada 2/3 lebih bagian panjang buah dan menghasilkan nada tinggi jika buah diketuk dengan jari (Jannah 2011). Selama proses pematangan buah, ternyata kadar pati yang terakumulasi berkurang tajam dimana ukuran granula pati yang ada dalam kloroplas mengecil (Seymour et al. 1993 diacu dalam Jannah 2011). Hilangnya pati diiringi dengan kenaikan kadar
amylase setelah proses pematangan selesai. Sebagai akibat hidrolisis pati, maka kadar gula juga meningkat selama proses pematangan. Gula yang dibentuk pada saat proses pematangan adalah fruktosa dan glukosa yang menggantikan monosakarida. Pada kebanyakan varietas mangga ternyata fruktosa ditemukan paling dominan (Jannah 2011).
Gambar 1. Mangga cengkir (indramayu)
5
Tabel 2. Sifat fisika dan kimia daging buah beberapa varietas mangga Sifat Fisika dan Kimia Varietas Mangga
Arumanis Cengkir Gadung Gedong Padatan terlarut total (o Bx) 14.8-16.6 13.0-15.0 20.8-21.2 16.0-17.8 Asam total (%) 0.22-0.56 0.26-0.88 0.18-0.47 0.12-17.8 Vitamin C (mg/100g) 22.0-46.9 37.8-58.2 20.0-21.5 36.2-96.2 Kadar air (%) ± 81.1 ± 84.3 ± 80.34 ± 82.9 Bobot utuh (g) ± 376.2 ± 320.1 ± 411.1 ± 232.4 Bagian yang dapat dimakan (%) ± 66.0 ± 65.8 ± 66.0 ± 59.0 Warna daging buah Kuning Kekuningan Kuning Jingga
Sumber : Broto 2003
Hasil panen mangga pertama berjumlah sekitar 10-13 buah per pohon. Hasil akan terus meningkat seiring dengan pertambahan umur dan perawatan yang intensif. Tahun-tahun yang dianggap subur untuk mangga adalah saat berumur 10-40 tahun. Lebih dari umur 40 tahun, hasil panen mangga mulai turun. Mangga yang tumbuh dari biji memiliki umur yang lebih panjang dari pada mangga yang berasal dari okulasi dan sambungan. Bahkan, setelah berumur 60-70 tahun masih produktif dan dapat menghasilkan 10000 buah per pohon (Pracaya 2011). Mangga termasuk buah klimakterik dengan umur simpan 6-8 hari dengan suhu kamar yaitu 25±2ºC dan RH 85±5ºC (Jagatiani
et al. 1988).
Penanganan pascapanen mangga adalah kegiatan penanganan yang dilakukan terhadap buah mangga di bangsal penanganan. Umumnya, kegiatan di bangsal penanganan diawali dengan penerimaan hasil panen dari kebun, pencucian, trimming (pemangkasan bagian tanaman misalnya daun atau tangkai yang terlalu panjang), pemilihan, pemilahan, pengukuran, perlakuan khusus (pemberian lilin, penyemprotan pertisida), pengemasan, dan pengangkutan. Mangga merupakan komoditas yang mudah rusak (perishable) sehingga memerlukan penanganan yang ekstra hati-hati agar mutunya tetap terjaga hingga ke tangan konsumen (Broto 2003).
Untuk menigkatkan nilai tambah buah, pengolahan merupakan alternatif terbaik. Hasil olahan buah mangga yang banyak dijumpai di Indonesia adalah sari buah, manisan basah dan kering, asinan, selai, dan jam. Buah mangga yang akan diolah harus dalam kondisi matang sempurna sehingga memberikan nilai gizi, cita rasa, aroma, dan warna optimun sesuai karakteristik varietas mangga yang bersangkutan (Broto 2003).
2.2
DEHIDRASI OSMOTIK
6
Gambar 2. Proses osmosis dua liquid
Sumber : Jannah 2011
Pori dalam membran semipermeabel terlalu kecil untuk dapat dilewati oleh molekul zat terlarut misalnya gula, tetapi cukup besar untuk dilewati molekul air. Molekul air dari larutan maupun dari pelarut murni secara random dapat melewati membran semipermeabel. Akan tetapi laju pergerakan molekul air dari air-larutan dengan laju pergerakan molekul air dari larutan-air ditentukan oleh besarnya entropi dan tekanan yang diaplikasikan ke salah satu kaki. Karena entropi larutan adalah lebih besar dibandingkan dengan entropi pelarut murni maka secara spontan laju molekul air yang melewati air-larutan akan lebih cepat dibandingkan dengan laju molekul air dari larutan-air. Oleh sebab itu, bila kita membiarkan kedua larutan untuk selang waktu tertentu maka ketinggian permukaan larutan pada salah satu kaki akan mengalamai kenaikan. Proses ini akan terus berlangsung
sampai ketinggian “h” mencapai tinggi tertentu dimana pada ketinggian tekanan larutan memiliki
tekanan yang dapat menyeimbangkan laju pergerakan molekul air dari larutan-air dan air-larutan. Tekanan inilah yang disebut sebagai tekanan osmotik (Jannah 2011).
Prinsip osmosis dapat juga diaplikasikan sebagai metode pengolahan pangan dalam proses pengawetan pangan yaitu dehidrasi osmotik. Penelitian mengenai dehidrasi osmotik telah berjalan lebih dari 25 tahun, tetapi masih sedikit industri yang menerapkan metode tersebut (Raoult 1994). Pada dasanya proses pengeringan merupakan proses pengurangan kadar air hingga bahan mencapai kadar air tertentu untuk mengurangi resiko kerusakan bahan yang diakibatkan oleh mikroba.
Dehidrasi osmotik melibatkan dua aliran material yang berlawanan arah dan terjadi secara simultan yaitu keluarnya air dari jaringan produk ke larutan osmotik dan aliran padatan terlarut dari larutan osmotik ke dalam jaringan produk. Dehidrasi osmotik dilakukan dengan merendam bahan pangan di dalam larutan (garam, gula atau bahan lainnya) dengan tekanan osmosis yang lebih tinggi dibandingkan tekanan osmosis intraseluler bahan pangan tersebut. Khan et al. (2008) menjelaskan bahwa laju kehilangan air dari jaringan produk dipengaruhi oleh beberapa faktor diantaranya, suhu, komposisi dan konsentrasi larutan osmotik, fase kontak, karakteristik produk, perlakuan awal terhadap produk, ukuran dan bentuk geometri produk, tingkat pengadukan serta lamanya proses pengeringan.
Pada dasarnya dehidrasi osmotik sama dengan teknologi pengeringan yaitu mengurangi kadar air hingga mencapai kadar air tertentu sehingga pertumbuhan mikroorganisme perusak bahan makanan dapat dihambat. Air merupakan salah satu unsur penting dalam bahan makanan. Air dalam suatu bahan makanan terdiri atas air bebas dan air terikat. Air bebas terdapat dalam ruang-ruang antar sel dan inter-granular dan pori-pori yang terdapat pada bahan. Air yang terikat secara lemah karena terserap (teradsorbsi) pada permukaan koloid makromolekuler seperti protein, pektin pati dan selulosa. Air yang ada dalam bentuk ini masih tetap mempunyai sifat air bebas dan dapat dikristalkan pada proses pembekuan sedangkan air dalam keadaan terikat kuat yaitu membentuk hidrat, ikatannya bersifat ionik sehingga relatif sukar dihilangkan atau diuapkan. Air dalam bentuk bebas dapat
Membran semipermeabel Larutan gula Pelarut murni (air)
7
membantu terjadinya proses kerusakan bahan makanan misalnya proses mikrobiologis, kimiawi, enzimatik, bahkan oleh aktivitas serangga perusak (Sudarmadji 2007).
Dehidrasi osmotik dapat digunakan untuk perlakuan awal sebelum proses pengeringan yang dapat menurunkan kadar air bahan sampai 50% dari kadar air awal (Khan et al. 2008). Proses dehidrasi osmotik digunakan pada pengeringan buah-buahan dengan menggunakan larutan hipertonik seperti larutan gula. Gula banyak digunakan untuk pengawetan bahan makanan yang berasal dari buah-buahan (Satuhu 2004). Gula digunakan pada berbagai produk makanan. Selain memberikan rasa manis, gula dalam konsentrasi tinggi digunakan sebagai pengawet. Menurut Buckle et al. (1985) diacu dalam Lutfi (2010) apabila gula ditambahkan ke dalam bahan pangan dalam konsentrasi tinggi minimum 40% padatan terlarut, menyebabkan sebagian air yang ada menjadi tidak tersedia untuk pertumbuhan mikroorganisme dan aktivitas air (aw) bahan pangan akan berkurang. Konsentrasi gula yang tinggi (sampai 70%) sudah dapat menghambat pertumbuhan mikroba perusak makanan.
Kadar gula yang tinggi (minimun 40%) bila ditambahkan ke dalam bahan pangan menjadi terikat sehingga menurunkan nilai aktivitas air dan tidak dapat digunakan oleh mikroba (Estiasih et al. 2011). Buah yang direndam dalam larutan gula panas dengan konsentrasi lebih tinggi dari 75% akan menyebabkan air keluar dari dinding sel buah lebih cepat dibandingkan dengan masuknya larutan gula ke dalam buah. Dengan adanya perbedaan yang besar antara kecepatan keluarnya air dan masuknya gula menyebabkan struktur sel dan tekstur buah menjadi lebih keras dan berkerut (Minifie et al.
1982).
Broto (2003) menyatakan bahwa pengeringan buah mangga dapat dilakukan dengan metode osmotik pada tahap awal, yakni merendan daging buah mangga ke dalam larutan gula pada konsentrasi dan jangka waktu tertentu. Setelah itu, dikeringkan pada suhu 45-55°C dan kelembaban nisbi yang rendah. Metode pengeringan tersebut terbukti mampu memberikan hasil buah kering yang awet dengan kadar air sekitar 14%, sehingga kerusakan kimiawi, biologis, dan enzimatik dapat dihindari. Perendaman irisan daging buah mangga kweni ke dalam larutan gula 60°Bx selama 10 jam, kemudian dikeringkan pada suhu 55°C dan kelembaban (RH) 60% selama 9 jam menghasilkan manisan mangga kweni kering, berpenampilan menarik,warna kuning merata, manis, dan memiliki kadar air optimum 14.4%. Jenis dan konsentrasi larutan osmotik sangat mempengaruhi laju pengeringan dan mutu yang dihasilkan. Larutan glukosa dengan konsentrasi 45% memberikan laju kehilangan air yang paling tinggi dibandingkan dengan konsentrasi larutan 30% dan 15% (Karathanos
et al. 1995 diacu dalam Jannah 2011).
Dehidrasi osmotik menyebabkan sampel kehilangan sejumlah air (WL) dan masuknya padatan terlarut dari larutan osmotik ke sampel (SG). Semakin tinggi nilai WL maka menunjukkan tingkat tingginya kehilangan air pada sampel. Sedangkan nilai SG merupakan parameter yang menujukkan banyaknya jumlah padatan terlarut yang masuk ke dalam sampel. Nilai SG dipengaruhi oleh pemberian kitosan, suhu larutan, dan konsentrasi dari larutan osmotik (Jannah 2011). Bahan pangan yang dikeringkan menggunakan dehidrasi osmotik akan memiliki kualitas yang lebih baik dibandingkan dengan bahan pangan yang dikeringkan menggunakan sinar matahari, namun dehidrasi osmotik merupakan teknologi pengeringan yang masih memerlukan biaya yang lebih tinggi.
8
Mavroudis et al. (1998) dalam Mayor et al. (2011) menjelaskan selama dehidrasi osmotik apel (varietas Granny smith) terjadi penurunan secara linear antara volume dan air dalam bahan. Suhu dalam proses tidak mempengaruhi penyusutan (shrinkage). Mayor et al. (2011) menjelaskan bahwa terjadi penurunan secara non-linear antara shrinkage dengan kadar air bahan baik pada proses dehidrasi osmotik maupun pengeringan udara.
Bulk density bahan (pumkins) pada awalnya akan meningkat hingga mencapai nilai maksimum dan kemudian menurun atau berfluktuasi hingga proses akhir dehidrasi osmotik (Mayor et al. 2011). Nieto et al. (2004) juga menjelaskan bahwa selama dehidrasi osmotik apel dengan menggunakan larutan sukrosa dan glukosa menyebabkan bulk density meningkat pada saat awal perlakuan (sekitar 1 jam perlakuan) kemudian bulk density berfluktuasi hingga proses akhir. Namun, Lozano et al. (1983) dan Krokida et al. (1997) menyatakan bahwa pada beberapa kasus bulk density meningkat selama dehidrasi (pisang dan wortel), pada kasus lain awalnya bulk density meningkat hingga mencapai nilai maksimum kemudian menurun (kentang, bawang putih). Perbedaan perilaku tersebut dapat berhubungan dengan perbedaan karakteristik fisika dan kimia dari bahan mentah, komposisi kimia, porositas awal atau keras/halusnya struktur bahan yang dapat menyebabkan perbedaan tekanan (stress) selama proses.
Kehilangan air yang terjadi pada dehidrasi osmotik dapat menyebabkan perubahan porositas yang terjadi pada bahan selama proses dehidrasi osmotik berlangsung. Porositas awal bahan yang rendah dapat menunjukkan bahwa sampel terdiri oleh air dan padatan terlarut. Mavroudis et al. (1998) menjelaskan bahwa porositas sampel meningkat diakhir proses dehidrasi osmotik apel. Sedangkan Giraldo et al. (2003) juga menjelaskan bahwa pada dehidrasi osmotik mangga, porositas awal sampel rendah kemudian meningkat selama proses dehidrasi osmotik berlangsung. Semakin banyaknya air yang keluar dari sampel menyebabkan meningkatnya porositas sampel.
9
III.
METODE PENELITIAN
3.1
WAKTU DAN TEMPAT
Penelitian dilaksanakan dari bulan April 2012 hingga September 2012 di Laboratorium Energi dan Elektrifikasi Pertanian, Departemen Teknik Mesin dan Biosistem, Fakultas Teknologi Pertanian, Institut Pertanian Bogor.
3.2
BAHAN DAN ALAT
3.2.1
Bahan
Bahan utama yang digunakan sebagai sampel dalam penelitian adalah buah mangga varietas cengkir (indramayu) yang telah dipotong dengan 3 macam ukuran yaitu 4.5 cm x 4 cm x 1.5 cm, 4.5 cm x 4 cm x 1 cm, dan 4.5 cm x 4 cm x 0.5 cm. Bahan lain yang digunakan adalah larutan osmotik berupa campuran antara gula dan aquades dengan konsentrasi larutan 30°Bx, 45°Bx dan 60°Bx.
3.2.2
Alat
Peralatan yang digunakan dalam penelitian ini adalah :
a. Osmotic Dehydrator berupa panci terbuat dari baja tahan karat (stainless steel) yang dirangkai dengan elemen pemanas (heater), termostat, pengaduk (stirer), dan saringan sampel. Pemanas air ini dilengkapi dengan pengaduk/stirer yang digerakkan oleh motor DC. Rangkaian osmotic dehydrator dapat dilihat pada Gambar 3. Pengaduk digunakan untuk mengaduk larutan osmotik agar panas yang diterima dapat merata ke semua sisi. Termostat digunakan untuk mengontrol suhu larutan osmotik agar konstan selama pengukuran.
Gambar 3. Rangkaian osmotic dehydrator
Keterangan gambar : a. Motor DC b. Panci
c. Pengaduk (stirer) d. Elemen pemanas (heater) e. Penyangga panci
f. Pengatur suhu pada termostat
a
b
c
d
e
f
g
h
10
g. Tombol “on-off” elemen pemanas
h. Penyangga stirer
i. Adaptor AC-DC
b. Wadah sampel terbuat dari stainless steel. Wadah untuk potongan buah mangga agar mudah dalam pengambilan potongan buah mangga yang akan ditimbang. Setiap saringan berisi 3 buah potongan mangga yang terdiri dari ulangan 1, ulangan 2, dan ulangan 3 yang memiliki ukuran hampir sama. Gambar wadah sampel dapat dilihat pada Lampiran 1.
c. Drying oven SS-204D digunakan untuk mengukur kadar air awal dan kadar air akhir sampel secara tidak langsung.
d. Cawan, tray, dan penjepit cawan. e. Desikator
f. Hand Refractometer K Fuji 13976 digunakan untuk mengukur kadar brix dari larutan osmotik sebesar 45ºBx dan 60ºBx, dan Hand Refractometer Atago N1 untuk mengukur kadar brix dari larutan osmotik sebesar 30ºBx.
g. Timbangan digital Excellent DJ-series. h. Termometer alkohol.
i. Pipet tetes j. Pisau k. Stopwatch
l. Kertas saring/tissue
m. Mistar
3.3
PROSEDUR PENELITIAN
3.3.1
Pembuatan Larutan Osmotik
Larutan osmotik yang digunakan adalah campuran dari larutan gula dan aquades. Konsentrasi larutan osmotik yang digunakan pada penelitian terdiri dari larutan gula 30oBx, 45oBx, dan 60oBx. Dalam pembuatan larutan gula 30oBx, gula dilarutkan dalam sejumlah aquades. Kemudian diukur kadar Total Padatan Terlarut (TPT) dengan menggunakan refraktometer. Jika angka menunjukkan <30oBx maka ditambahkan gula ke dalam larutan, dan sebaliknya ditambahkan air jika angka menunjukkan >30oBx. Begitu pula dalam pembuatan larutan gula 45oBx, dan 60oBx.
3.3.2
Prosedur Penelitian Dehidrasi Osmotik
Langkah kerja dalam pengeringan osmotik adalah sebagai berikut:
a. Mangga dicuci, dibersihkan, dikupas kulitnya, dan dipotong dengan 3 macam ukuran 4.5 cm x 4 cm x 1.5 cm, 4.5 cm x 4 cm x 1 cm, dan 4.5 cm x 4 cm x 0.5 cm.
b. Potongan mangga sebagai sampel ditimbang untuk mengetahui massa awal dan pengukuran volume awal sampel, serta pengukuran kadar air awal sampel sebelum dehidrasi osmotik. c. Sampel yang telah dimasukkan ke dalam wadah kemudian dimasukkan ke dalam osmotic
dehydrator.
11
e. Larutan osmotik yang dimasukkan ke dalam osmotic dehydrator memiliki perbandingan massa 1:15 (sampel : larutan). Heater dinyalakan dan termostat diatur sesuai suhu yang digunakan yaitu 30°C. Selain itu, stirer juga dinyalakan dengan kecepatan sedang yaitu ±250 rpm. Namun pada dehidrasi osmotik suhu ruang, sampel dan larutan osmotik yang telah siap dimasukkan ke dalam wadah tanpa heater dan tanpa pengaduk.
f. Pengamatan dilakukan selama 6 jam untuk perlakuan pada suhu 30°C, sedangkan pengamatan dilakukan selama 48 jam pada suhu ruang. Selang waktu yang digunakan untu perlakuan suhu 30°C adalah menit ke 0, 15, 30, 45, 60, 90, 120, 150,180, 240, 300, dan 360. Selang waktu yang digunakan untuk perlakuan suhu ruang adalah menit ke 0, 45, 90, 180, 360, 1080, 1440, dan 2880.
12
Gambar 4. Diagram alir penelitian Analisis data
selesai Pada suhu 30ºC pengukuran berat,
volume dan kadar air dilakukan pada menit ke 0, 15, 30, 45, 60, 90, 120, 150,180, 240, 300, dan 360
Pada suhu ruang pengukuran berat dan volume sampel dilakukan pada menit ke 0, 45, 90, 180, 360, 1080, 1440, dan 2880. Kadar air diukur pada menit ke-0 dan 2880.
30ºC dan suhu ruang 30ºBx
30ºC dan suhu ruang 45ºBx
30ºC dan suhu ruang 60ºBx Pengukuran awal
sampel:
1. Berat awal 2. Volume awal 3. Kadar air awal
Mulai
Penentuan sampel : 1. Buah Mangga
2. Memiliki kadar air yang hampir sama
Persiapan alat dan bahan
penentuan dimensi sampel
penelitian
Pembuatan larutan
13
3.4
RANCANGAN PENELITIAN
Perlakuan yang digunakan dalam penelitian terdiri dari :
Perlakuan 1 : M0 = irisan buah mangga dengan ketebalan 0.5 cm (berat ± 8 g) M1 = irisan buah mangga dengan ketebalan 1 cm (berat ± 16 g)
M2 = irisan buah mangga dengan ketebalan 1.5 cm (berat ± 24 g) Perlakuan 2 : C0 = konsentrasi larutan osmotik 30ºBx
C1 = konsentrasi larutan osmotik 45ºBx C2 = konsentrasi larutan osmotik 60ºBx
Rancangan percobaan yang digunakan dalam penelitian ini adalah rancangan faktorial dengan 2 perlakuan yang masing-masing memiliki 3 taraf perlakuan. Dari ketiga perlakuan tersebut akan diperoleh 9 kombinasi perlakuan yang dapat dilihat pada tabel 3. Rancangan percobaan yang sama juga digunakan pada suhu ruang yang diperoleh 9 kombinasi perlakuan seperti pada suhu 30°C.
Tabel 3. Kombinasi perlakuan dehidrasi osmotik
Perlakuan Notasi perlakuan Suhu larutan Konsentrasi
larutan
Ukuran
30°C/suhu ruang 30°Bx 0.5 cm M0C0 1.0 cm M1C0 1.5 cm M2C0 30°C/suhu ruang 45°Bx 0.5 cm M0C1 1.0 cm M1C1 1.5 cm M2C1 30°C/suhu ruang 60°Bx 0.5 cm M0C2 1.0 cm M1C2 1.5 cm M2C2
3.5
PENGAMATAN
Pengamatan yang dilakukan terhadap massa bahan dan kadar air bahan selama dehidrasi osmotik berlangsung. Pengamatan terhadap massa bahan dan kadar air bahan dijelaskan berikut ini :
3.5.1
Massa Bahan
14
3.5.2
Kadar Air dengan Metode Oven
Kadar air suatu bahan menunjukkan banyaknya kandungan air persatuan bobot bahan yang dapat dinyatakan dalam persen berat basah (wet basis) atau dalam persen berat kering (dry basis). Kadar air diukur secara tidak langsung dengan menggunakan metode oven. Sebelumnya cawan yang akan digunakan untuk sampel dikeringkan terlebih dahulu dalam oven bersuhu 105°C selama ±15 menit. Kemudian cawan didinginkan di dalam desikator dan timbang. Sejumlah sampel yang telah disiapkan untuk pengukuran kadar air awal dimasukkan ke dalam cawan dan dikeringkan dalam oven bersuhu 105°C sampai perubahan massa tidak terjadi lagi. Kemudian sampel yang telah dikeringkan didinginkan dalam desikator dan ditimbang, sedangkan untuk kadar air akhir digunakan sampel yang telah diberi perlakuan dehidrasi osmotik. Sampel dimasukkan ke dalam cawan dan dikeringkan dalam oven bersuhu 105°C sampai perubahan massa tidak terjadi lagi. Kadar air berat basah dapat ditentukan dengan persamaan 1.
x 100% (1)
Dimana : m = kadar air berat basah (% b.b) a = massa sampel awal (g)
b = massa sampel setelah dioven (g)
Air yang terkandung dalam bahan tidak dapat seluruhnya diuapkan, meskipun demikian hasil yang diperoleh disebut juga sebagai berat bahan kering. Kadar air berat basah mempunyai batas maksimum teoritis sebesar 100 %.
3.6
ANALISIS DATA
Analisis data dilakukan untuk menentukan volume, densitas, penyusutan volume, penyusutan berat, water loss, solid gain, dan porositas, sedangkan permodelan Azuara digunakan untuk validasi data water loss.
3.6.1
Volume
Volume merupakan salah satu sifat fisik bahan pangan yang digunakan dalam perhitungan awal dan akhir untuk menduga sifat fisik yang lain seperti densitas. Volume sampel diukur menggunakan prinsip Archimedes. Volume sampel ditentukan menggunakan persamaan 2.
( )
(2)
Dimana : = berat sampel (gf) ‟= berat sampel di air (gf) = berat jenis air ( 0.9957 gf/ml)
15
terbaca massa sampel saat berada di dalam air. Gambar pengukuran volume dapat dilihat pada Lampiran 1. Volume sampel dinyatakan dalam satuan mililiter (ml). Skema pengukuran volume sampel dapat dilihat pada Gambar 5.
Gambar 5. Skema pengukuran volume sampel
3.6.2
Densitas
Densitas atau massa jenis merupakan sifat fisika dari sebuah bahan, setiap unsur dan senyawa memiliki nilai densitas yang khas. Massa jenis didefinisikan sebagai perbandingan antara massa sampel dan volume sampel yang dinyatakan dengan persamaan 3.
ρr (3)
Dimana : ρr = massa jenis/kerapatan (g/ml)
m = massa sampel (g) = volume sampel (ml)
3.6.3
Penyusutan Volume (Shrinkage)
Penyusutan terjadi pada volume bahan akibat kehilangan kandungan air dalam bahan. Penyusutan dinyatakan dalam persen sehingga jika dirumuskan:
Penyusutan volume (%v/v) = x 100% (4) Dimana : Vt = volume sampel pada waktu t (ml)
Vo = volume sampel pada waktu ke-0 menit (ml)
3.6.4 Penyusutan Berat (Weight Reduction/WR)
Penyusutan terjadi pada berat bahan akibat kehilangan kandungan air dalam bahan. Penyusutan dinyatakan dalam persen sehingga jika dirumuskan:
Penyusutan berat (%w/w) = x 100% (5) Wadah berisi air
Penyangga Timbangan
papan
pemberat
16
Dimana : Wt = massa sampel pada waktu t (g)
Wo= massa sampel pada waktu ke-0 menit (g)
3.6.5 Tingkat Kehilangan Air (Water Loss/WL)
Water loss menunjukan banyaknya air yang keluar dari sampel selama proses dehidrasi osmotik. Water loss dinyatakan dalam gram sampel per gram sampel awal. Untuk mengetahui besarnya WL dapat dihitung dengan menggunakan persamaan berikut (Souza et al. 2007):
WLt (6)
Dimana : w0 = massa sampel pada waktu ke-0 menit (g) wt = massa sampel pada waktu t (g)
m0 = kadar air sampel pada waktu ke-0 menit (%b.b) wt = kadar air sampel pada waktu t (%b.b)
WLt = water loss pada waktu t (%)
3.6.6
Solid Gain (SG)
Solid gain menunjukan banyaknya padatan terlarut yang masuk ke dalam sampel. Solid gain
dinyatakan dalam gram sampel per gram sampel awal. Untuk mengetahui besarnya SG dapat dihitung dengan menggunakan persamaan 7 (Souza et al 2007) :
SGt (7)
Dimana : w0 = massa sampel pada waktu ke-0 menit (g) wt = massa sampel pada waktu t (g)
m0 = kadar air sampel pada waktu ke-0 menit (%b.b) wt = kadar air sampel pada waktu t (%b.b)
SGt = solid gain pada waktu t (%)
3.6.7
Porositas
Porositas merupakan fraksi udara dalam suatu bahan. Porositas berperan penting dalam proses pengeringan atau dehidrasi osmotik karena mempengaruhi pergerakan air dan udara dalam bahan. Porositas dapat dinyatakan dengan menggunakan persamaan 8 (Giraldo et al. 2003):
ε = (8)
Dimana :ɛ = porositas sampel (-)
17
Densitas riil sampel (ρr) diperoleh dari perbandingan massa dan volume sampel yang diperoleh. Sedangkan densitas apparent (ρ) sampel dari padatan karbohidrat dapat didekati oleh persamaan 9 (Lewis 1996 diacu dalam Giraldo 2003 ) :
(9) Dimana : xw = kadar air sampel (%b.b)
1000 = kerapatan air (kg/m3)
1590 = kerapatan karbohidrat rata-rata (kg/m3)
Mangga mengandung karbohidrat berupa gula yang membuat mangga memiliki rasa manis. Gula dalam mangga didominasi oleh sukrosa 7-12%, sedangkan jenis mangga manis kandungan gulanya mencapai 16-18% (Ide 2010).
3.6.8
Permodelan dalam Dehidrasi Osmotik
Azuara et al. (1992) diacu dalam Jannah (2011) menghitung water loss selama dehidrasi osmotik melalui persamaan 10 dengan dua parameter yang diperoleh dari kesetimbangan berat :
(10) Dimana : S1 = konstanta yang berkaitan dengan water loss (-)
18
IV.
HASIL DAN PEMBAHASAN
4.1
Dehidrasi Osmotik pada Suhu 30ºC
4.1.1
Kadar Air
Kadar air dalam penelitian diukur sebelum dehidrasi osmotik, selama dehidrasi osmotik dan setelah dehidrasi osmotik. Kadar air awal diukur untuk masing-masing sampel yang digunakan dalam dehidrasi osmotik. Kadar air awal sampel berkisar antara 80.70 %b.b hingga 89.95 %b.b. Setelah mengalami proses dehidrasi maka kadar air sampel semakin lama akan semakin menurun yang diakibatkan karena adanya perbedaan konsentrasi antara sampel dan larutan gula sehingga tejadi perbedaan tekanan osmotik.
Pada awal proses dehidrasi air yang keluar lebih cepat karena air yang dikeluarkan merupakan air bebas yang dikandung oleh sampel. Jumlah air bebas dalam sampel lebih besar dibandingkan dengan jumlah air yang terikat di dalam sampel. Semakin lama penurunan kadar air akan terjadi karena dehidrasi digunakan untuk melepaskan air terikat yang terkandung dalam sampel. Terdapat dua jenis air terikat yaitu air terikat secara fisik dan air terikat secara kimia. Apabila air permukaan telah habis, migrasi air dari dalam sampel terjadi secara difusi. Migrasi air tersebut terjadi karena adanya perbedaan konsentrasi air di bagian dalam sampel dengan konsentrasi air di bagian permukaan sampel.
Air yang keluar dari sampel saat dehidrasi osmotik dapat menyebabkan konsentrasi larutan gula menjadi menurun sehingga kemampuan larutan gula untuk mengeluarkan air dari sampel juga akan berkurang. Selain itu, padatan terlarut yang terdapat pada larutan osmotik juga akan berkurang karena sebagian akan masuk ke dalam sampel. Akan tetapi penurunan yang terjadi sangat kecil yaitu ±1ºBx karena menggunakan perbandingan massa yang tinggi 1:15 (sampel:larutan).
19
Gambar 6. Grafik kadar air sampel setelah dehidrasi osmotik
Pada awal proses dehidrasi osmotik, penurunan kadar air berlangsung cepat dan semakin lambat di akhir proses dehidrasi osmotik. Hal tersebut terlihat pada Gambar 6, di mana grafik penurunan kadar air terlihat lebih curam pada waktu awal dan semakin landai pada waktu akhir proses dehidrasi. Kadar air terbesar terdapat pada sampel yang memiliki ketebalan 0.5 cm dengan menggunakan larutan gula sebesar 30ºBx (M0C0). Hal ini dapat terjadi karena pada dehidrasi osmotik menggunakan larutan gula 30ºBx memiliki kemampuan yang lebih rendah dibandingkan dengan larutan osmotik 45ºBx dan 60ºBx. Sampel dengan ukuran ketebalan 0.5 cm (M0C0) memiliki luas permukaan yang lebih besar dibandingkan dengan sampel yang memiliki ukuran ketebalan 1 cm (M1C0) dan 1.5 cm (M2C0) seharusnya sampel yang lebih tipis memiliki kadar air yang lebih rendah dibandingkan sampel yang lebih tebal, namun dalam hal ini konsentrasi larutan osmotik yang rendah mengakibatkan air yang keluar dari sampel menjadi lebih lambat.
Penurunan kadar air dalam sampel dapat dipengaruhi oleh besarnya konsentrasi larutan dan ukuran sampel yang digunakan selama dehidrasi osmotik. Semakin tipis sampel dan semakin besar konsentrasi larutan osmotik maka penurunan kadar air akan semakin tinggi sehingga proses dehidrasi menjadi lebih cepat. Selain itu, suhu juga dapat mempengaruhi penurunan kadar air pada sampel, namun pada penelitian ini besarnya suhu disamakan untuk semua perlakuan yaitu 30°C.
4.1.2
Tingkat Kehilangan Air (Water Loss/WL)
Water loss merupakan salah satu parameter yang menunjukkan adanya air yang keluar dari sampel. Secara umum besarnya nilai WL berbanding terbalik dengan besarnya nilai kadar air yang diperoleh selama proses dehidrasi. Semakin besar nilai WL maka kadar air sampel akan semakin rendah. Konsentrasi larutan osmotik sangat mempengaruhi besarnya WL sampel. Semakin besar konsentrasi larutan osmotik maka akan semakin besar pula nilai WLsampel.
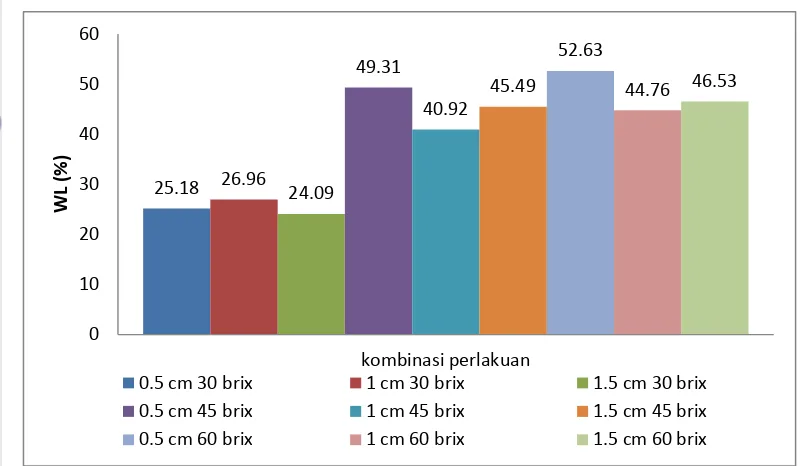
Gambar 7 menunjukkan bahwa sampel yang memiliki nilai WL terbesar adalah sampel yang memiliki ukuran ketebalan 0.5 cm dengan menggunakan larutan osmotik sebasar 60ºBx (M0C2) yaitu sebesar 52.63%. Sedangkan nilai WL yang paling rendah terdapat pada sampel yang menggunakan
50 60 70 80 90 100
0 50 100 150 200 250 300 350 400
kad ar ai r ( % b .b ) waktu (menit)
0.5 cm 30 brix 1 cm 30 brix 1.5 cm 30 brix
0.5 cm 45 brix 1 cm 45 brix 1.5 cm 45 brix
20
larutan osmotik dengan konsentrasi 30ºBx, baik sampel yang memiliki ukuran 0.5 cm, 1 cm, maupun 1.5 cm. Besarnya nilai WL dipengaruhi oleh besarnya konsentrasi larutan osmotik yang digunakan. Semakin besar konsentrasi larutan osmotik maka akan semakin besar WL yang dimiliki oleh sampel. Data WLdapat dilihat pada Lampiran 6.
Gambar 7. Water loss dehidrasi osmotik untuk berbagai ketebalan dan konsentrasi larutan gula setelah 6 jam
Pada awalnya kehilangan air pada sampel terjadi dengan cepat sehingga nilai WL meningkat dengan cepat, namun lama-kelamaan air yang hilang tidak sebesar pada menit-menit awal sehingga perubahan nilai WL tidak begitu besar yang ditunjukkan dengan kurva yang lebih landai pada grafik. Bentuk grafik lama-kelamaan akan semakin konstan hingga sampel mencapai tingkat WL∞ (water loss untuk waktu yang tak hingga). Bentuk grafik yang konstan menunjukkan bahwa sampel telah mencapai kadar air kesetimbangan. Hasil grafik pehitungan nilai WL dengan permodelan Azuara dan data dapat dilihat pada Gambar 8, Gambar 9 dan Gambar 10.
Gambar 8. Grafik water loss menggunakan perhitungan dari persamaan Azuara dan data pada larutan osmotik 30ºBx
25.18 26.96 24.09
49.31
40.92
45.49 52.63
44.76 46.53
0 10 20 30 40 50 60 kombinasi perlakuan WL (% )
0.5 cm 30 brix 1 cm 30 brix 1.5 cm 30 brix
0.5 cm 45 brix 1 cm 45 brix 1.5 cm 45 brix
0.5 cm 60 brix 1 cm 60 brix 1.5 cm 60 brix
0 10 20 30
0 100 200 300 400
WL
(%
)
waktu (menit)
azuara 0.5 cm 30 brix azuara 1 cm 30 brix
azuara 1.5 cm 30 brix 0.5 cm 30 brix
[image:35.595.125.525.151.384.2]21
Gambar 9. Grafik water loss menggunakan perhitungan dari persamaan Azuara dan data pada larutan osmotik 45ºBx
Gambar 10. Grafik water loss menggunakan perhitungan dari persamaan Azuara dan data pada larutan osmotik 60ºBx
Tabel 4 menunjukkan besarnya WL∞ yang dicapai oleh sampel. Nilai WL∞, S1, dan R2 dengan menggunakan pemodelan Azuara. Pemodelan Azuara digunakan untuk menentukan tingkat validasi WL dari pengukuran dan perhitungan. Besarnya nilai koefisien determinasi pada validasi tersebut berkisar antara 0.954 hingga 0.993. Kisaran nilai koefisien determinasi tersebut menunjukkan bahwa permodelan Azuara layak untuk digunakan. Pada Tabel 4 terlihat bahwa nilai WL∞ pada sampel M0C2 memiliki nilai yang sangat tinggi yaitu 82.921%. Seharusnya nilai WL yang konstan dicapai pada waktu tak hingga, diduga nilai tersebut menunjukkan bahwa grafik WL∞ tidak dalam kondisi konstan namun mengalami peningkatan.
0 20 40 60
0 100 200 300 400
WL
(%
)
waktu (menit)
azuara 0.5 cm 45 brix azuara 1 cm 45 brix
azuara 1.5 cm 45 brix 0.5 cm 45 brix
1 cm 45 brix 1.5 cm 45 brix
0 20 40 60
0 100 200 300 400
WL
(%
)
waktu (menit)
azuara 0.5 cm 60 brix azuara 1 cm 60 brix
azuara 1.5 cm 60 brix 0.5 cm 60 brix
22
Tabel 4. Nilai parameter dan koefisien determinasi dari perhitungan WL dengan menggunakan permodelan Azuara
Perlakuan sampel WL∞ S1 R2 M0C0 28.511 1.689 0.954 M1C0 46.962 0.884 0.990 M2C0 37.254 1.134 0.980 M0C1 63.399 1.733 0.954 M1C1 56.863 1.162 0.979 M2C1 82.921 2.859 0.988 M0C2 60.143 1.829 0.988 M1C2 54.583 2.020 0.993 M2C2 57.449 1.645 0.973
4.1.3
Solid Gain (SG)
Selama dehidrasi osmotik terjadi dua aliran material yang berlawanan arah yaitu keluarnya air dari sampel dan masuknya padatan terlarut dari larutan osmotik ke dalam sampel. Air yang keluar dari sampel menyebabkan terjadinya ruang kosong pada sampel yang kemudian diisi oleh padatan terlarut yang mengalir dari larutan osmotik yang digunakan dalam proses dehidrasi. Solid gain merupakan nilai yang menunjukkan besarnya padatan terlarut yang masuk ke dalam sampel. Semakin besar nilai SG maka semakin besar padatan terlarut yang masuk ke dalam sampel selama proses dehidrasi berlangsung. Masuknya padatan terlarut ke dalam sampel akan mempengaruhi rasa sampel sehingga diusahakan nilai SG serendah mungkin agar rasa sampel tidak mengalami banyak perubahan.
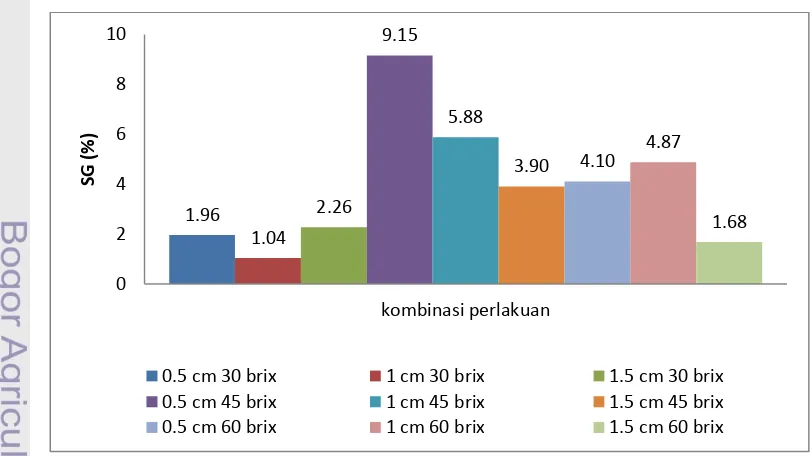
Gambar 11. Solid gain dehidrasi osmotik selama 6 jam
1.96 1.04
2.26 9.15
5.88
3.90 4.10
4.87 1.68 0 2 4 6 8 10 kombinasi perlakuan S G (% )
0.5 cm 30 brix 1 cm 30 brix 1.5 cm 30 brix
0.5 cm 45 brix 1 cm 45 brix 1.5 cm 45 brix
[image:37.595.111.516.471.699.2]23
Gambar 11 menunjukkan besarnya nilai SG yang dimiliki oleh masing-masing sampel saat proses dehidrasi osmotik berlangsung. Pada Gambar 11 terlihat bahwa sampel yang memiliki nilai SG paling besar terlihat pada sampel dengan ukuran ketebalan 0.5 cm dengan menggunakan larutan osmotik 45ºBx (M0C1) sebesar 9.15%, sedangkan sampel yang memiliki nilai SG paling sedikit adalah sampel dengan ukuran ketebalan 1 cm dengan larutan osmotik 30ºBx (M1C0) sebesar 1.04%. Hal ini dapat terjadi karena besarnya konsentrasi larutan 30ºBx lebih rendah dibandingan dengan konsentrasi larutan 45ºBx. Data SGdapat dilihat pada Lampiran 6.
Kecenderungan nilai SG yang sedang membuktikan bahwa nilai SG menjadi lebih tinggi. Pada penelitian Jannah (2011) menghasilkan nilai SG terbesar pada konsentrasi larutan osmotik 42ºBx, sedangkan pada penelitian ini menghasilkan nilai SG terbesar pada larutan osmotik 45ºBx. Jannah (2011) menyatakan bahwa nilai SG yang paling tinggi terjadi pada dehidrasi osmotik dengan perlakuan E0T2C1 (tanpa kitosan, suhu larutan 50ºC, dan konsentrasi larutan 42ºBx) sebesar 12.75%.
Konsentrasi larutan osmotik mempengaruhi besarnya nilai SG sampel. Pada Gambar 11, sampel dengan konsentrasi larutan osmotik 30ºBx cenderung memiliki nilai SG yang lebih rendah dibandingkan dengan larutan osmotik 45ºBx dan 60ºBx. Hal tersebut dapat disebabkan karena konsentrasi larutan osmotik yang terlalu tinggi akan menyebabkan nilai SG yang rendah sehingga laju kehilangan air (WL) lebih besar dibandingkan laju masuknya padatan (SG) ke dalam sampel, sedangkan konsentrasi larutan osmotik yang terlalu rendah menyebabkan laju kehilangan air (WL) yang rendah sehingga pori-pori sampel masih terisi oleh air dan menyebabkan masuknya padatan terlarut menjadi lebih lambat.
4.1.4
Penyusutan Volume (Shrinkage) dan Penyusutan Berat (weight
reduction/WR)
Penyusutan bahan yang terjadi meliputi penyusutan volume dan penyusutan berat. Penyusutan volume diperoleh dari perbandingan antara perubahan volume sampel setelah dehidrasi osmotik dengan volume sampel sebelum dehidrasi osmotik. Selain itu, penyusutan berat juga diperoleh dari perbandingan antara perubahan berat sampel dengan berat sampel awal. Penyusutan yang terjadi pada sampel baik penyusutan volume ataupun berat disebabkan WL dan SG. Penyusutan volume dan penyusutan berat yang terjadi pada sampel akan meningkat terhadap waktu. Semakin lama waktu dehidrasi maka akan semakin besar pula penyusutan yang terjadi.
Penyusutan volume (Gambar 12) yang terjadi pada sampel diakibatkan oleh air yang keluar dari sampel sehingga menyebabkan sampel menjadi menyusut dan mengerut. Penyusutan volume dapat terjadi akibat adanya perpindahan berat air secara drastis yang tidak diikuti dengan perpindahan padatan terlarut ke dalam bahan. Perpindahan air ini menyebabkan tekanan yang kuat pada dinding sel sehingga menimbulkan kerusakan pada membran sel.
24
Gambar 12. Grafik penyusutan volume sampel setelah dehidrasi osmotik
Gambar 12 memperlihatkan bahwa penyusutan volume yang terjadi pada sampel dengan ukuran 0.5 cm menggunakan larutan osmotik 60ºBx adalah penyusutan yang paling besar yang ditunjukkan oleh grafik yang lebih curam dibandingkan grafik sampel yang lain. Konsentrasi larutan osmotik, ketebalan sampel, kadar air, WL dan SG menjadi faktor yang menyebabkan besarnya penyusutan volume yang terjadi. Rendahnya konsentrasi larutan osmotik menyebabkan penyusutan volume yang terjadi juga semakin rendah. Penyusutan volume paling rendah terjadi pada sampel yang memiliki ukuran ketebalan 1.5 cm menggunakan larutan 30ºBx (M2C0) karena sampel tersebut masih memiliki kadar air yang cukup tinggi setelah dehidrasi yaitu sebesar 82.46%b.b dari kadar air awal 88.53%b.b.
Selain penyusutan yang terjadi pada volume sampel, penyusutan berat juga terjadi pada sampel. Sampel buah mangga yang digunakan merupakan buah yang memiliki kadar air tinggi, sehingga sampel yang mengalami dehidrasi osmotik akan mengalami penyusutan berat sampel karena terjadi penurunan kadar air. Air yang semakin berkurang ketika dehidrasi menyebabkan semakin meningkatnya penyusutan berat sampel. Penyusutan berat dapat terjadi apabila nilai WL lebih besar dibandingkan dengan nilai SG. Dari Gambar 13 dapat dilihat bahwa penyusutan berat paling besar terjadi pada sampel yang memiliki ukuran ketebalan 0.5 cm dan menggunakan larutan osmotik 60ºBx (M0C2), sedangkan penyusutan volume paling rendah terjadi pada sampel yang memiliki ukuran ketebalan 1.5 cm dengan menggunakan larutan osmotik 30ºBx (M2C0). Hal tersebut sama dengan penyusutan volume yang terjadi pada sampel. Data penyusutan berat dapat dilihat pada Lampiran 3.
0 10 20 30 40 50 60
0 50 100 150 200 250 300 350 400
sh ri n ka ge (% v /v ) waktu (menit)
0.5 cm 30 brix 1 cm 30 brix 1.5 cm 30 brix
0.5 cm 45 brix 1 cm 45 brix 1.5 cm 45 brix
25
Gambar 13. Grafik penyusutan berat sampel setelah dehidrasi osmotik
Gambar 14 menunjukkan besarnya perbandingan antara penyusutan volume dan penyusutan berat yang terjadi pada sampel. Apabila nilai (∆v/v0)/(∆w/w0) pada grafik lebih besar dari 1 maka penyusutan volume yang terjadi lebih besar dibandingkan dengan penyusutan berat, sebaliknya apabila (∆v/v0)/(∆w/w0) pada grafik lebih kecil dari 1 maka penyusutan volume yang terjadi lebih kecil dibandingkan penyusutan berat. Penyusutan volume yang terjadi pada sampel dengan ketebalan 0.5 cm dengan larutan osmotik 30ºBx (M0C2) lebih besar dibandingkan dengan penyusutan berat.
Nilai (∆v/v0)/(∆w/w0) pada grafik berkisar antara 0.98 hingga 1.22. Nilai tersebut menunjukkan sebagian besar sampel mengalami penyusutan volume yang lebih besar dibandingkan dengan penyusutan beratnya.
Gambar 14. Grafik rasio antara penyusutan volume dan penyusutan berat
0 10 20 30 40 50 60
0 50 100 150 200 250 300 350 400
WR
(%
w/
w)
waktu (menit)
0.5 cm 30 brix 1 cm 30 brix 1.5 cm 30 brix
0.5 cm 45 brix 1 cm 45 brix 1.5 cm 45 brix
0.5 cm 60 brix 1 cm 60 brix 1,5 cm 60 brix
0.00 0.20 0.40 0.60 0.80 1.00 1.20 1.40
0 50 100 150 200 250 300 350 400
∆ / 0/ ∆ / 0 waktu (menit)
0.5 cm 30 brix 1 cm 30 brix 1.5 cm 30 brix
0.5 cm 45 brix 1 cm 45 brix 1.5 cm 45 brix
26
Gambar 15. Grafik hubungan antara penyusutan volume dan penyusutan berat
Penyusutan volume dan penyusutan berat memiliki hubungan berbanding lurus (linear) yang ditunjukkan oleh Gambar 15. Jika penyusutan berat semakin besar maka penyusutan volume juga semakin besar. Besarnya tingkat WL dan SG sangat mempengaruhi kurva hubungan penyusutan volume dan penyusutan berat pada sampel. Mayor et al. (2011) dalam dehidrasi osmotik pumkins, dihasilkan volume sampel berkurang secara linear dengan meningkatnya nilai WR secara bebas pada kondisi proses dehidrasi osmotik. Namun, dalam dehidrasi osmotik apel dengan menggunakan larutan gula ditemukan hubungan linear antara WR dan penyusutan volume (Moreira et al.2003).
Dehidrasi osmotik menyebabkan perubahan fisik yang terjadi pada sampel seperti perubahan bentuk dan ukuran. Sampel menjadi menyusut karena kandungan air pada sampel berkurang. Sampel sebelum dan setelah dehidrasi osmotik dapat dilihat pada Lampiran 2 sedangkan skema penyusutan volume sampel dapat dilihat pada Gambar 16. Setelah dehidrasi osmotik terjadi pengecilan ukuran dan perubahan bentuk sampel. Penyusutan lebih terlihat pada bagian tengah dari panjang dan lebar sampel, serta bagian tengah dari tebal sampel, sedangkan penyusutan yang terjadi pada sudut sampel lebih kecil.
(a) Tampak samping
(b) Tampak atas
Gambar 16. Skema penyusutan volume sampel
0 10 20 30 40 50 60
0 10 20 30 40 50 60
sh ri n ka ge (% v /v ) WR (%w/w)
0.5 cm 30 brix 1 cm 30 brix 1.5 cm 30 brix
0.5 cm 45 brix 1 cm 45 brix 1.5 cm 45 brix
27
4.1.5
Densitas dan Porositas
Densitas merupakan rasio antara massa sampel (kg) dengan volume sampel (m3). Nilai densitas
riil (Gambar 17) sampel diperoleh dari perbandingan massa sampel dan volume sampel yang telah mengalami dehidrasi, sedangkan densitas apparent (Gambar 18) sampel diperoleh dari persamaan 10. Besarnya nilai densitas apparent sampel dipengaruhi oleh besarnya kadar air sampel setelah dehidrasi osmotik. Densitas riil sampel berkisar antara 954.38 kg/m3 hingga 1129.18 kg/m3. Pada dehidrasi osmotik dengan larutan 30ºBx terlihat bahwa densitas sampel tidak banyak berubah (Gambar 18), hal tersebut terjadi karena sampel tidak mengalami perubahan kadar air yang cukup besar. Pada Gambar 19 menunjukkan bahwa semakin besar penyusutan berat sampel maka densitas riil sampel meningkat. Hal tersebut