BIOETANOL DARI DAGING BUAH AREN
RAHMI NURHIDAYAH
DEPARTEMEN HASIL HUTAN FAKULTAS KEHUTANAN INSTITUT PERTANIAN BOGOR
PERNYATAAN MENGENAI SKRIPSI DAN
SUMBER INFORMASI SERTA PELIMPAHAN HAK CIPTA*
Dengan ini saya menyatakan bahwa skripsi yang berjudul Bioetanol dari Daging Buah Aren adalah benar karya saya dengan arahan dari komisi pembimbing dan belum diajukan dalam bentuk apa pun kepada perguruan tinggi mana pun. Sumber informasi yang berasal atau dikutip dari karya yang diterbitkan maupun tidak diterbitkan dari penulis lain telah disebutkan dalam teks dan dicantumkan dalam Daftar Pustaka di bagian akhir skripsi ini.
Dengan ini saya melimpahkan hak cipta dari karya tulis saya kepada Institut Pertanian Bogor.
Bogor, Juli 2013
Rahmi Nurhidayah
ABSTRAK
RAHMI NURHIDAYAH. Bioetanol dari Daging Buah Aren. Dibimbing oleh I Nyoman Jaya Wistara.
Daging buah aren tua dapat digunakan sebagai alternatif bioetanol karena merupakan sumber karbohidrat yang bukan menjadi sumber makanan utama. Serbuk daging buah aren dihidrolisis secara enzimatis dan asam dengan pemanasan autoclave dan microwave. Fermentasi gula pereduksi menggunakan
Saccharomyces cerevisiae pada konsentrasi 3%, 10%, dan 17% selama 24 jam, 48 jam, dan 72 jam. Berdasarkan hasil penelitian, efisiensi hidrolisis tertinggi diperoleh dari hidrolisis asam dengan autoclave (92.52%). Selain itu, efisiensi fermentasi tertinggi diperoleh dari hidrolisis enzim dengan pemanasan autoclave
dan fermentasi dengan S. cerevisiae 17% selama 24 jam (97.36%), serta rendemen etanol tertinggi dari hidrolisis asam dengan pemanasan autoclave dan fermentasi menggunakan S. cerevisiae 17% selama 72 jam (76.49%).
Kata kunci: Bioetanol, daging buah aren, hidrolisis, fermentasi, S. cerevisiae.
ABSTRACT
RAHMI NURHIDAYAH. Bioethanol from the Kernel of Sugar Palm.Supervised by Nyoman J. Wistara.
It is paramount to develop bioethanol production based on the utilization of less important carbohydrate based feedstock such as the sugar palm kernel. In the present works, the kernel powder of sugar palm was hydrolyzed by enzymatic and acidic procedures heated either by autoclaving or microwaving. Fermentation of the resulting reducing sugars was then carried out by Saccharomyces cerevisiae at the concentration of 3%, 10%, and 17% for 24, 48, and 72 hours. It was found that the highest hydrolysis efficiency was by autoclaved acid hydrolysis (92.52%). On the other hand, the highest fermentation efficiency was obtained by 24 hours fermentation with a 17% S. cerevisiae of the resulting sugar from autoclaved enzymatic hydrolysis (97.36%), and the highest ethanol yield was obtained from autoclaved acid hydrolysis fermented for 72 hours with 17 % S. cerevisiae
(76.49%).
Skripsi
sebagai salah satu syarat untuk memperoleh gelar Sarjana Kehutanan
pada
Departemen Hasil Hutan
BIOETANOL DARI DAGING BUAH AREN
RAHMI NURHIDAYAH
DEPARTEMEN HASIL HUTAN FAKULTAS KEHUTANAN INSTITUT PERTANIAN BOGOR
Judul Skripsi : Bioetanol dari Daging Buah Aren Nama : Rahmi Nurhidayah
NIM : E24080014
Disetujui oleh
I Nyoman J. Wistara, Ph. D Pembimbing
Diketahui oleh
Prof. Dr. Ir. I Wayan Darmawan, M. Sc Ketua Departemen
PRAKATA
Alhamdulillah segala puji dan syukur penulis panjatkan ke hadirat Allah SWT yang telah melimpahkan rahmat serta hidayah-Nya sehingga dapat
menyelesaikan penelitian dan menyusun karya ilmiah dengan judul “ Bioetanol dari Daging Buah Aren” yang merupakan salah satu syarat untuk memperoleh gelar Sarjana Kehutanan pada Fakultas Kehutan Institut Pertanian Bogor. Penelitian ini dilaksanakan dari bulan Agustus 2012 sampai Mei 2013 di Laboratorium Kimia Hasil Hutan, Laboratorium Analisis Makanan dan Kimia Departemen Gizi Masyarakat, Laboratorium Bersama Hasil Hutan Fakultas Kehutanan, dan Laboratorium Teknologi Kimia Departemen Teknologi Industri Pertanian IPB.
Penulis mengucapkan terimakasih kepada Bapak I Nyoman J. Wistara, Ph.D yang selalu memberikan bimbingan serta masukan selama penelitian hingga skripsi ini selesai, kepada kedua orang tua dan keluarga yang selalu memberikan doa dan dukungan selama penyelesaian tugas akhir ini, serta kepada semua pihak yang telah membantu dalam penyelesaian skripsi ini. Penulis menyadari bahwa dalam penyusunan skripsi ini masih jauh dari sempurna, sehingga segala kritik dan saran yang membangun penulis harapkan dan terima dengan senang hati. Semoga penyusunan skripsi ini dapat memberikan manfaat untuk kita semua.
Bogor, Juli 2013
DAFTAR ISI
DAFTAR TABEL vi
DAFTAR GAMBAR vi
PENDAHULUAN 1
METODE 2
Penelitian Pendahuluan 2
Perlakuan Awal Buah Aren 2
Pengukuran Aktivitas Enzim 3
Penentuan Konsentrasi Enzim 3
Proses Hidrolisis dan Fermentasi 3
Pengujian Hasil dan Perhitungan Rendemen 4
Prosedur Analisis Data 4
HASIL DAN PEMBAHASAN 5
Karakteristik Bahan 5
Karakteristik Enzim 6
Efisiensi Hidrolisis 7
Efisiensi Fermentasi 9
Rendemen Etanol 11
SIMPULAN DAN SARAN 12
Simpulan 12
Saran 13
DAFTAR PUSTAKA 13
DAFTAR TABEL
1 Rendemen etanol berdasarkan hasil etanol terhadap kadar karbohidrat
kolang-kaling (%, w/w) 11
2 Rendemen etanol berdasarkan hasil etanol terhadap berat kering serbuk
kolang-kaling (%, w/w) 12
DAFTAR GAMBAR
1 Aktivitas enzim amilase dan glukoamilase optimum pada (a) variabel
suhu dan (b) variabel pH 6
2 Nilai efisiensi hidrolisis untuk (a) aktivitas enzim amylase dan (b) aktivitas enzim glukoamylase pada serbuk kolang-kaling 7 3 Efisiensi konversi karbohidrat menjadi glukosa (efisiensi hidrolisis)
dengan katalis asam dan enzim serta menggunakan autoclave dan
microwave 8
PENDAHULUAN
Pemerintah mencanangkan 6.40 juta ha lahan disediakan untuk ditanami tanaman penghasil biofuel pada tahun 2005-2015 (Efendi 2010). Aren adalah salah satu tanaman biofuel potensial untuk dikembangkan. Tanaman aren merupakan jenis tanaman palma yang tidak asing bagi masyarakat Indonesia, dan banyak tumbuh tersebar hampir di seluruh bagian wilayah Indonesia, diantaranya Sumatera, Jawa, Bali, Nusa Tenggara, Sulawesi, dan Maluku. Tanaman aren juga dapat tumbuh di beberapa negara Asia Tenggara lainnya (Filipina, Malaysia, Laos, Kamboja, Vietnam, dan Thailand) serta Asia Selatan (India dan Srilangka) (Muhaemin 2012).
Hampir seluruh bagian tanaman aren dapat dimanfaatkan, misalnya pemanfaatan ijuk untuk tali dan keperluan rumah tangga, nira untuk gula semut dan arak, serta daging buah untuk dikonsumsi. Tanaman aren mulai berproduksi/ berbuah sejak umur 5 tahun, dan masa produktifnya sekitar 5-8 tahun (Dinas Kehutanan Provinsi Jawa Tengah 2010). Selain memiliki nilai ekonomi, tanaman aren juga memiliki nilai konservasi. Menurut Dinas Kehutanan Provinsi Jawa Tengah (2010), sistem perakaran tanaman aren berfungsi untuk mencegah erosi dan mengikat air.
Nira aren saat ini disukai untuk digunakan sebagai bahan baku bioetanol karena telah berbentuk gula sederhana. Potensi nira aren sebagai sumber bahan baku bioetanol dapat mendorong pengembangan budidaya aren, sehingga menyebabkan ketersediaan kolang-kaling juga melimpah dan mungkin dapat menjadi limbah karena pemanfaatannya yang hanya sebagai makanan pelengkap dan terbatas. Ketersediaan yang melimpah ini menjadikan kolang-kaling berpotensi sebagai sumber alternatif bioetanol. Sementara itu, kendala yang dihadapi saat ini masih belum banyak dilakukannya budidaya aren. Pertumbuhan tanaman aren masih secara liar, meskipun sudah dicanangkan pembudidayaan tanaman penghasil biofuel.
Bioetanol merupakan salah satu bioenergi yang dapat dimanfaatkan untuk bahan bakar, berbentuk senyawa alkohol, hasil fermentasi gula atau pemecahan pati dan selulosa. Menurut Dodic et al. (2009), bioetanol memiliki bilangan oktan tinggi dan menghasilkan panas lebih tinggi untuk penguapan, sehingga dapat digunakan sebagai campuran bensin. Bioetanol sebagai bahan bakar bersifat lebih ramah lingkungan dibandingkan bensin, karena emisi yang dihasilkan sangat kecil (Demirbas T & Demirbas A 2010). Bioetanol juga dapat dimanfaatkan sebagai bahan tambahan di industri minyak wangi dan kosmetik, serta pelarut beberapa bahan kimia.
2
Shanavas et al. (2011) dalam penelitiannya juga mencari kondisi optimum aktivitas enzim untuk produksi bioetanol dari pati singkong.
Sumber alternatif bioetanol dapat berbentuk pati, selulosa, atau gula sederhana. Bahan yang berupa pati atau selulosa, sebelum difermentasi perlu dikonversi menjadi gula sederhana, atau disebut hidrolisis. Proses hidrolisis sering dimodifikasi dalam proses pemanasannya, untuk mendapatkan hasil dan proses yang lebih optimum dibandingkan dengan proses konvensional. Menurut Nitayavardhana et al. (2009), kelemahan proses konvensional yaitu diperlukannya konsentrasi enzim yang tinggi, waktu fermentasi yang lama, dan kadar etanol yang dihasilkan rendah. Adapun beberapa modifikasi prahidrolisis yang telah digunakan yaitu pemanfaatan ultrasonik pada singkong (Nitayavardhana et al.
2009) dan biji jagung (Nikolic et al. 2010), penggunaan microwave pada pati sagu (Saifuddin dan Hussain 2011) dan ampas sorgum (Choudhary et al. 2012), serta penggunaan microwave pada kombinasi hidrolisis asam dan enzim untuk bahan lignoselulosa (El-Zawawy et al. 2011).
Banyak jenis katalis yang dapat digunakan dalam proses hidrolisis, seperti enzim, asam, dan basa. Pemilihan jenis enzim tergantung dari senyawa yang akan dipecah karena kinerja enzim yang spesifik terhadap senyawa tertentu, sedangkan untuk katalis asam tidak tergantung pada senyawa yang dipecahnya. Penggunaan jenis asam tidak memberikan pengaruh nyata terhadap gula pereduksi yang dihasilkan, karena asam memecah substrat secara acak (Putri dan Sukandar 2008).
Penelitian mengenai “Bioetanol dari Daging Buah Aren” bertujuan untuk mengetahui potensi kolang-kaling sebagai sumber alternatif bioetanol. Potensi tersebut dilihat dari nilai gula pereduksi dan etanol yang dihasilkan. Pemanfaatan kolang-kaling sebagai alternatif bioetanol diharapkan dapat lebih meningkatkan nilai ekonomi tanaman aren serta sumber bioetanol menjadi lebih beragam dan dapat menjadi bahan substitusi apabila mengalami penurunan ketersediaan sumber bioetanol. Keberagaman sumber bahan baku bioetanol ini dapat mencegah pelonjakan harga bahan. menggunakan golok. Kolang-kaling diiris halus menggunakan pisau dan dibuat serbuk berukuran 40-60 mesh menggunakan blender dan willey mill.
Kandungan karbohidrat kolang-kaling dianalisis menggunakan metode Luff Schrool. Larutan kolang-kaling dalam HCl 3% dipanaskan selama 3 jam. Kemudian dinetralkan dengan NaOH 30% dan indikator PP. Larutan sebanyak 10 ml ditambahkan 25 ml larutan luff, 15 ml akuades, dan dipanaskan selama 10 menit. Setelah dingin larutan ditambahkan 15 ml KI 20%, 25 ml H2SO4 25%, dan
3 pada blanko dengan sampel. Kadar glukosa tersebut dapat digunakan untuk menentukan kadar karbohidrat dalam kolang-kaling.
Pengukuran Aktivitas Enzim
Aktifitas enzim α-amilase dan glukoamilase ditentukan sebelum dipergunakan untuk memecah molekul karbohidrat atau pati. Aktifitas enzim ditentukan pada suhu 60-90oC dan pH 4-6. Variasi suhu dan pH dalam menentukan aktifitas enzim ditujukan untuk mengetahui kondisi yang menghasilkan aktifitas enzim optimum.
Penentuan Konsentrasi Enzim
Penggunaan konsentrasi enzim untuk setiap bahan berbeda, tergantung kadar karbohidrat dan komposisinya pada bahan. Penentuan konsentrasi enzim amilase yang optimum dilakukan dengan pembentukan larutan kolang-kaling dalam buffer fosfat 50 mM pH 6. Larutan dipanaskan dengan autoclave pada suhu 121oC selama 30 menit. Enzim amilase ditambahkan pada konsentrasi 12, 48, 96, dan 144 U/g serta dipanaskan dalam waterbath shaker pada suhu 80oC selama 3 jam. Hasil hidrolisis dengan amilase diukur glukosanya menggunakan 6505 UV/ Vis. Spectrophotometer dengan pereaksi DNS.
Konsentrasi amilase dengan glukosa tertinggi digunakan untuk menentukan konsentrasi enzim glukoamilase. Larutan diatur hingga pH 5, ditambahkan glukoamilase dan dipanaskan pada suhu 50oC selama 48 jam. Konsentrasi glukoamilase yang digunakan yaitu 1.2, 6, 12, dan 18 U/g. Konsentrasi amilase dan glukoamilase yang memberikan nilai glukosa tertinggi digunakan dalam proses hidrolisis.
Proses Hidrolisis dan Fermentasi
Hidrolisis kolang-kaling dilakukan secara enzimatis dan asam. Serbuk kolang-kaling ditambahkan buffer fosfat 50 mM sehingga terbentuk larutan pada konsentrasi 10% w/v (berat kering serbuk) (Shanavas et al. 2011; Saifuddin & Hussain 2011). Larutan ditepatkan pada pH 6 serta dipanaskan dengan autoclave
pada suhu 121oC selama 30 menit dan microwave SHARP tipe R-348 pada daya 50% (500 watt) selama 3 menit. Enzim amilase ditambahkan pada konsentrasi 144 U/g dan diinkubasi pada waterbath shaker dengan suhu 80oC selama 3 jam. Suhu diturunkan hingga 50oC dan pH diatur hingga 5 untuk penambahan enzim glukoamilase pada konsentrasi 6 U/g, kemudian diinkubasi kembali selama 48 jam. Proses hidrolisis asam menggunakan pelarut HCl 3% dengan pemanasan
autoclave dan microwave pada kondisi yang sama dengan hidrolisis enzim. Semua perlakuan hidrolisis ini dibuat menjadi faktor metode hidrolisis, yaitu hidrolisis asam-autoclave (AO), asam-microwave (AM), enzim- autoclave (EO), dan enzim- microwave (EM)
Filtrat hasil hidrolisis diatur pada pH 5.5 menggunakan NaOH dan masing-masing sampel diambil 50 ml untuk difermentasi menggunakan inokulum
4
dalam ruang laminar flow untuk menghindari kontaminasi mikroorganisme lain. Proses fermentasi dilakukan dengan variabel waktu 24, 48, dan 72 jam dalam
shaker pada suhu ruang. Setelah inkubasi, media dipanaskan dalam air mendidih selama 5 menit untuk mendormankan kerja S. cerevisiae dan disimpan dalam lemari pendingin pada suhu 0-4oC.
Pengujian Hasil dan Perhitungan Rendemen
Pengujian dilakukan untuk pengukuran kadar gula pereduksi dengan metode 3.5-dinitrosalisilat (DNS) menggunakan spektrofotometer pada panjang gelombang 540 nm dan kadar etanol. Kadar etanol ditentukan dengan memasukkan 1 µl sampel ke dalam GC-2014 Shimadzu AOC-20i (kromatografi gas). GC tersebut menggunakan kolom RTX WAX pada suhu 150oC, suhu injector 180oC, suhu detector 200oC, tekanan injeksi 84.6 kPa, colomn flow 0.65 ml/menit, dan total flow 55.5 ml/menit. Etanol akan terdeteksi pada waktu retensi 3.3-3.5 menit. Kadar etanol ditentukan menggunakan kurva standar sebagai nisbah luas area kromatogram etanol dengan konsentrasi standar sampel yang dimasukkan. Standar dibuat pada konsentrasi 0, 0.02, 0.04, 0.06, 0.1, 0.2, 0.5, 0.8, dan 1.2 % (v/v).
Dari hasil analisis tersebut, maka dapat ditentukan efisiensi hidrolisis, efisiensi fermentasi, dan rendemen etanol secara teoritis sebagai berikut:
Efisiensi hidrolisis (%) =
x 100
Ef. fermentasi (%) =
x100
Rendemen etanol (%) = ⁄
x 100 atau
Rendemen etanol (%) = ⁄
x 100 (Ket. 1.111 adalah faktor konversi menjadi glukosa, 0.51 merupakan faktor konversi menjadi etanol dan BJ etanol dalam kondisi standar yaitu 0.789 g/mL).
Prosedur Analisis Data
Data hasil gula pereduksi, kadar etanol, rendemen etanol dan konversi pati menjadi etanol diolah dengan menggunakan SPSS 16.0 for Windows dengan uji lanjut Duncan. Adapun data rendemen etanol dianalisis menggunakan rancangan faktorial berblok dengan 2 kali ulangan. Model matematisnya yaitu sebagai berikut:
5 Keterangan
Yijkl = Nilai respon pada blok ke-i metode hidrolisis, taraf ke-j konsentrasi S.
cerevisiae, dan taraf ke-k waktu fermentasi pada ulangan ke-l µ = Nilai tengah populasi (rata-rata yang sebenarnya)
ai = Pengaruh penggunaan blok-i dari metode hidrolisis (i = asam-autoclave,
asam-microwave, enzim- autoclave, enzim- microwave)
bj = Pengaruh penambahan taraf ke-j dari konsentrasi S. cerevisiae ( j = 3%,
10%, dan 17%)
ck = Pengaruh penambahan taraf ke-k dari waktu fermentasi ( k = 24 jam, 48
jam, dan 72 jam)
(bc)jk = Pengaruh interaksi konsentrsi S. cerevisiae dan waktu fermentasi antara
taraf ke-j dan taraf ke-k
εijk = Pengaruh galat dari ulangan ke-l yang memperoleh perlakuan metode hidrolisis ke-i, konsentrasi S. cerevisiae ke-j, dan waktu fermentasi ke-l
HASIL DAN PEMBAHASAN
Karakteristik Bahan
Bahan yang digunakan dalam penelitian ini yaitu serbuk kolang-kaling dari daging buah aren (Arenga pinnata Merr) tua. Pembuatan serbuk kolang-kaling bertujuan memudahkan proses hidrolisis. Semakin kecil ukuran serbuk, luas permukaan kontak dengan katalis (asam/ enzim) akan semakin besar. Jiping et al.
(2007) juga mengatakan bahwa granular pati yang kecil lebih cepat dihidrolisis karena area permukaannya lebih luas.
Bahan yang berbentuk serbuk memiliki sifat kimia yang berbeda dengan pati. Serbuk memiliki matriks yang lebih komplek dibandingkan pati. Dalam serbuk banyak mengandung senyawa lain, misalnya serat, dan memiliki kandungan amilosa yang lebih rendah (Adinoyl et al. 2012). Kolang-kaling merupakan suatu bahan yang kaya akan karbohidrat, namun tidak hanya satu jenis, yaitu ada bentuk pati dan serat (serat pangan dan serat kasar) (Yasni 1982; Alim 2002).
Kandungan karbohidrat total (pati, serat, dan gula sederhana) kolang-kaling yang diperoleh yaitu 45.40% (b/b, kering tanur). Nilai ini lebih tinggi dibandingkan hasil penelitian Yasni (1982) dengan metode Anthrone, yang yang hanya mengandung pati dan gula sederhana sebesar 32.38% (b/b, kering tanur). Perbedaan tersebut dapat disebabkan karena perbedaan umur, tempat tumbuh, dan metode pengujian.
6
Karakteristik Enzim
Enzim merupakan salah satu katalis yang bersifat spesifik dalam menguraikan bahan tertentu. Enzim yang digunakan dalam hidrolisis kolang-kaling adalah enzim amilase dan glukoamilase. Amilase hanya dapat memecah rantai lurus glukosa secara acak menjadi rantai glukosa yang lebih pendek, sedangkan rantai cabang glukosa dan oligosakarida hasil pemecahan amilase dipecah oleh glukoamilase dari ujung rantai oligosakarida menjadi glukosa.
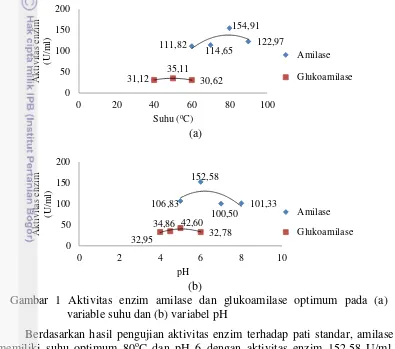
Berdasarkan hasil pengujian aktivitas enzim terhadap pati standar, amilase memiliki suhu optimum 80oC dan pH 6 dengan aktivitas enzim 152.58 U/ml. Kondisi tersebut tidak berbeda jauh dengan penelitian Kolusheva dan Marinova (2007) yang memiliki suhu optimum amilase 90oC dan pH 7. Sedangkan suhu optimum glukoamilase yaitu 50oC dan pH 5 dengan aktivitas enzim 42.60 U/ml. Suhu dan pH optimum glukoamilase ini sesuai dengan penelitian Naiola (2006) dan Risnoyatiningsih (2011), yaitu memiliki suhu optimum 40-60oC dan pH 4-6. Aktivitas kedua enzim tersebut terbilang kecil dibandingkan dengan enzim yang biasa digunakan dalam beberapa penelitian, karena enzim yang digunakan adalah enzim teknis.
Kinerja enzim terhadap setiap bahan berbeda, tergantung dari kadar karbohidrat dan komposisi senyawa lain, sehingga perlu dilakukan penentuan konsentrasi optimum enzim dalam pemecahan substrat pada kondisi suhu dan pH optimum. Berdasarkan hasil penelitian, konsentrasi optimum untuk pemecahan karbohidrat kolang-kaling yaitu 144 U/g untuk enzim amilase dan 6 U/g untuk
(a)
(b)
Gambar 1 Aktivitas enzim amilase dan glukoamilase optimum pada (a) variable suhu dan (b) variabel pH
7 enzim glukoamilase (Gambar 2). Konsentrasi tersebut digunakan untuk proses hidrolisis dengan tujuan menghasilkan glukosa maksimum.
Efisiensi Hidrolisis
Pati dan selulosa merupakan jenis polisakarida yang tersusun atas rantai glukosa. Pati dan selulosa memiliki banyak ikatan hidrogen, sehingga sulit larut dalam pelarut organik, sulit memperpanjang processability, fusibility, serta fungsi dari selulosa dan pati (Kadokawa et al. 2009). Oleh sebab itu perlu proses hidrolisis untuk menguraikan rantai glukosa tersebut. Proses hidrolisis merupakan proses yang sangat penting, terutama dalam menghasilkan glukosa yang akan diuraikan oleh S. cerevisiae menjadi etanol. Muljadi et al. (2009) menyebutkan bahwa hidrolisis dapat dilakukan dengan berbagai metode, diantaranya hidrolisis murni (hanya menggunakan air), hidrolisis enzim, hidrolisis asam, hidrolisis basa, dan hidrolisis fusion (penggunaan suhu tinggi, baik menggunakan air ataupun tidak). Akan tetapi metode hidrolisis yang paling umum digunakan dalam proses bioetanol dari bahan pati atau selulosa adalah hidrolisis enzim dan asam.
Hidrolisis enzim dan asam masing-masing memiliki kelebihan dan kekurangan. Enzim lebih disukai untuk proses hidrolisis dibanding jenis hidrolisis lainnya, karena kerja enzim lebih spesifik dan selektif pada senyawa tertentu sehingga dapat meningkatkan produk etanol dan mengurangi terbentuknya senyawa lain yang dapat menghambat proses fermentasi. Hidrolisis enzim juga dapat bekerja pada suhu rendah dan pH netral (Muljadi et al. 2009). Proses enzim juga memiliki kelemahan yaitu memerlukan waktu yang lama, bekerja aktif pada kondisi tertentu, serta memerlukan jenis enzim yang beragam untuk bahan yang mengandung senyawa lebih dari satu. Bahan dengan kandungan senyawa yang beragam terkadang menggunakan hidrolisis asam, karena dapat memecah beberapa jenis senyawa secara bersamaan, serta memerlukan waktu yang lebih cepat. Kelemahan hidrolisis asam yaitu dapat menghasilkan senyawa lain selain gula pereduksi yang dapat menghambat proses fermentasi seperti HMF (hidroximetil furfural) dan furfural.
Senyawa pati tersusun atas amilosa dan amilopektin. Amilosa merupakan rantai lurus glukosa dari pati pada ikatan glikosidik α-(1,4), sedangkan amilopektin merupakan rantai cabang glukosa dari senyawa pati dengan cabang pada ikatan glikosidik α-(1,6). Senyawa amilopektin lebih mudah diuraikan
(a) (b)
Gambar 2 Nilai efisiensi hidrolisis untuk (a) aktivitas enzim amylase dan (b) aktivitas enzim glukoamylase pada serbuk kolang-kaling
8
menjadi glukosa dibandingkan dengan amilosa (Sharma et al. 2010). Kemungkinan hal tersebut karena amilopektin lebih bersifat amorf dibandingkan amilosa, yang dapat dilihat dari seringnya penggunaan pati dengan kandungan amilopektin tinggi untuk bahan yang memerlukan tingkat pengembangan (swelling) yang tinggi. Pemecahan pati akan terjadi pada daerah amorf terlebih dahulu sebelum memecah daerah kristalin (Jiping et al. 2007).
Proses hidrolisis umumnya dilakukan pada suhu tinggi, untuk lebih memudahkan pemecahan pati. Dengan suhu tinggi, granula pati akan mengembang atau tergelatinasi. Umumnya pati dapat tergelatinasi pada suhu pemanasan sampai 95oC. Dengan adanya air, akan terjadi pembengkakan dan pemecahan struktur granular pati (Zhang et al. 2012). Suhu gelatinasi pati dari setiap bahan akan berbeda, tergantung dari senyawa lain dan komposisi antara amilosa dengan amilopektin. Apabila bahan pati dipanaskan melebihi suhu gelatinasinya, kemungkinan dapat merusak sebagian glukosa yang terbentuk.
Proses pemanasan dapat dilakukan dengan berbagai metode, misalnya secara konvensional (pemanasan langsung), autoclave, microwave, atau ultrasonik. Penggunaan microwave dan ultrasonik memberikan hasil yang lebih baik pada prahidrolisis untuk hidrolisis enzimatis, karena pemanasannya lebih merata, dengan waktu lebih singkat. Penggunaan microwave, diantara keduanya, memberikan peningkatan glukosa dan konsentrasi etanol lebih tinggi dibanding ultrasonik (Nikolic et al. 2011). Microwave dapat membantu pelepasan pati dan melarutkan bahan, sehingga menghasilkan gula yang lebih tinggi (Choudhary et al.
2012), serta dapat merusak struktur pati menjadi lebih amorf, dan lebih memudahkan enzim memecah struktur pati (Saifuddin & Hussain 2011). Berbeda dengan hasil penelitian, nilai kadar glukosa tertinggi justru diperoleh dengan menggunakan autoclave (Gambar 3).
Hidrolisis asam dengan pemanasan autoclave memberikan efisiensi konversi menjadi glukosa (efisiensi hidrolisis) tertinggi yaitu 92.52%. Hidrolisis asam dengan pemanasan microwave memiliki efisiensi hidrolisis terendah (2.01%). Berdasarkan uji Anova pada tingkat kepercayaan 95% dan uji lanjut Duncan, metode hidrolisis berpengaruh nyata terhadap efisiensi hidrolisis, dan pengaruh metode hidrolisis berbeda nyata terhadap efisiensi hidrolisis untuk semua metode.
Gambar 3 Efisiensi konversi karbohidrat menjadi glukosa (efisiensi hidrolisis) dengan katalis asam dan enzim serta pemanasan autoclave dan
Asam - Otoklaf Asam - Microwave Enzim - Otoklaf Enzim - Microwave
9 Rendahnya konversi karbohidrat pada metode EO dan EM dimungkinkan karena ada jenis karbohidrat lain selain pati, sedangkan rendahnya konversi karbohidrat pada metode AM karena tidak ditentukannya waktu dan suhu yang optimum. Waktu pemanasan microwave terlalu singkat, terutama untuk metode AM, karena proses pemanasan berlangsung bersamaan dengan pemecahan karbohidrat, sehingga struktur karbohidrat belum sempat terurai menjadi glukosa. Peningkatan kondisi hidrolisis (konsentrasi asam, suhu, dan waktu) melebihi kondisi optimum, dapat meningkatkan kandungan senyawa toxic, terutama pada hidrolisis asam (Gupta et al. 2009). Konsentrasi asam terendah yang memberikan kadar glukosa tertinggi digunakan, karena peningkatan konsentrasi asam tidak berpengaruh nyata pada gula pereduksi yang dihasilkan (Hashem & Darwish 2010). Penggunaan asam pada konsentrasi tertentu juga akan berpengaruh pada efektivitas biaya produksi gula (Iranmahboob et al. 2002).
Efisiensi Fermentasi
Bioetanol merupakan etanol atau etil alkohol yang diproduksi dari beberapa biomassa yang mengandung sejumlah gula atau bahan yang dapat dikonversi menjadi gula, seperti pati dan selulosa. Fermentasi adalah proses biokimia berbentuk gula, seperti glukosa, fruktosa, dan sukrosa, dikonversi menjadi etanol dan karbondioksida menggunakan khamir/ mikroorganisme. Glukosa dan fruktosa adalah monosakarida dengan enam atom karbon (gula 6-C). Sukrosa termasuk disakarida yang tersusun dari glukosa dan fruktosa yang saling berikatan, sedangkan pati adalah polisakarida yang tersusun dari rantai panjang molekul glukosa (Ruane et al. 2010).
Faktor pembatas utama dari aktivitas dan pertumbuhan S. cerevisiae yaitu keterbatasan jumlah substrat (glukosa) yang tersedia (Shanavas et al. 2011). Jika jumlah glukosa yang tersedia hingga akhir fermentasi mencukupi, pertumbuhan sel akan kembali normal (Tibayrenc et al. 2011). Peningkatan konsentrasi S. cerevisiae dapat meningkatkan konsentrasi etanol, selama jumlah kadar glukosa mencukupi. Kinerja S. cerevisiae pada konsentrasi tertentu dengan waktu fermentasi yang berbeda terhadap gula pereduksi dapat dilihat dari efisiensi fermentasi. Efisiensi fermentasi yaitu banyaknya glukosa yang dimanfaatkan oleh mikroorganisme untuk menghasilkan etanol dengan memperhitungkan kadar glukosa sebelum dan setelah fermentasi (Su et al. 2010). Kadar glukosa sisa juga dapat dihubungkan dengan pasokan ketersediaan nitrogen yang mempengaruhi kapasitas konsumsi S. cerrevisiae (Gomez et al. 2011).
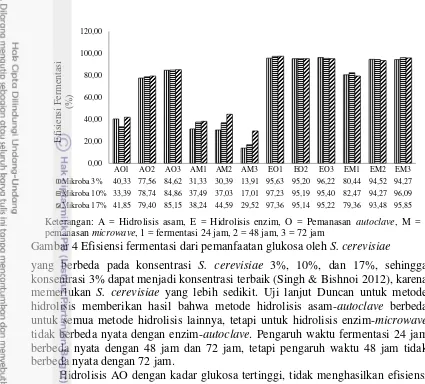
Metode hidrolisis EO dengan fermentasi S. cerevisiae 17% selama 24 jam (EO1-S. cerevisiae 17%) memiliki efisiensi fermentasi tertinggi (97.36%). Waktu fermentasi 24 jam merupakan waktu bagi S. cerevisiae untuk mulai menghasilkan etanol, bahkan terkadang sudah dapat mencapai kadar etanol maksimum, dan setelahnya peningkatan kadar etanol mengalami penurunan (Hashem & Darwish 2010).
Metode hidrolisis dan waktu fermentasi berpengaruh nyata terhadap efisiensi fermentasi, sedangkan konsentrasi S. cerevisiae tidak berpengaruh nyata
10
yang berbeda pada konsentrasi S. cerevisiae 3%, 10%, dan 17%, sehingga konsentrasi 3% dapat menjadi konsentrasi terbaik (Singh & Bishnoi 2012), karena memerlukan S. cerevisiae yang lebih sedikit. Uji lanjut Duncan untuk metode hidrolisis memberikan hasil bahwa metode hidrolisis asam-autoclave berbeda untuk semua metode hidrolisis lainnya, tetapi untuk hidrolisis enzim-microwave
tidak berbeda nyata dengan enzim-autoclave. Pengaruh waktu fermentasi 24 jam berbeda nyata dengan 48 jam dan 72 jam, tetapi pengaruh waktu 48 jam tidak berbeda nyata dengan 72 jam.
Hidrolisis AO dengan kadar glukosa tertinggi, tidak menghasilkan efisiensi fermentasi tertinggi. Kemungkinan pada konsentrasi etanol tersebut aktivitas
S.cerevisiae sudah terganggu atau terhambat. Aktivitas S. cerevisiae dapat terganggu oleh penumpukan etanol hingga konsentrasi tertentu (Stanley et al.
2010; Kasavi et al. 2012). Selain itu pada hidrolisis asam dapat terbentuk senyawa lain yang menjadi inhibitor bagi pertumbuhan S. cerevisiae, seperti HMF, furfural, dan asam asetik, terutama apabila waktunya terlalu lama. Senyawa-senyawa tersebut yang kemungkinan terbaca pada saat pembacaan etanol dengan GC. Senyawa-senyawa inhibitor tersebut sebagian terdapat pula pada hidrolisis EO, tetapi tidak untuk hidrolisis EM.
Proses fermentasi terkadang dapat digabungkan dengan hidrolisis (secara enzimatis), disebut metode Simultaneous Saccharification and Fermentation
(SSF), sehingga lebih mengefisiensikan waktu. Kelebihan metode SSF juga dapat mengurangi penumpukan gula, terbentuknya pengotor, dan produk lain yang dapat menghambat proses fermentasi (Santos et al. 2012). Pada proses SSF terkadang ada perbedaan suhu dan pH optimum antara enzim untuk sakarifikasi dengan mikroorganisme untuk fermentasi. S. cerevisiae memerlukan suhu antara 27-42oC (suhu ruang) dan pH 5.5-7 untuk dapat bekerja dalam tahap fermentasi (Jamai et al. 2007), sementara suhu optimum untuk tahapan sakarifikasi umumnya sekitar 55 – 60oC (Nikolic et al. 2010).
Keterangan: A = Hidrolisis asam, E = Hidrolisis enzim, O = Pemanasan autoclave, M = pemanasan microwave, 1 = fermentasi 24 jam, 2 = 48 jam, 3 = 72 jam
Gambar 4 Efisiensi fermentasi dari pemanfaatan glukosa oleh S. cerevisiae
AO1 AO2 AO3 AM1 AM2 AM3 EO1 EO2 EO3 EM1 EM2 EM3 Mikroba 3% 40,33 77,56 84,62 31,33 30,39 13,91 95,63 95,20 96,22 80,44 94,52 94,27 Mikroba 10% 33,39 78,74 84,86 37,49 37,03 17,01 97,23 95,19 95,40 82,47 94,27 96,09 Mikroba 17% 41,85 79,40 85,15 38,24 44,59 29,52 97,36 95,14 95,22 79,36 93,48 95,85
11
Rendemen Etanol
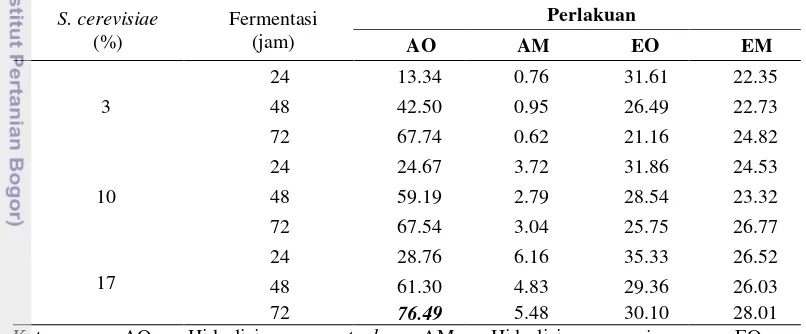
Secara keseluruhan proses bioetanol dapat dinilai dari rendemen etanol, baik terhadap kadar karbohidrat maupun terhadap berat kolang-kaling. Rendemen etanol yaitu efisiensi produksi total secara teoritis dengan memperhitungkan etanol yang dihasilkan terhadap bahan. Rendemen etanol tertinggi terhadap kadar karbohidrat dalam kolang-kaling yaitu pada metode hidrolisis AO dengan fermentasi S. cerevisiae 17% selama 72 jam (76.49%). Metode hidrolisis dan waktu fermentasi berpengaruh nyata terhadap rendemen etanol, tetapi tidak untuk konsentrasi S. cerevisiae (tingkat α = 95%) dan interaksi antara konsentrasi S. cerevisiae dan waktu fermentasi. Dengan uji lanjut Duncan, metode hidrolisis memberikan hasil bahwa metode hidrolisis asam-autoclave berbeda untuk semua metode hidrolisis lainnya, tetapi untuk hidrolisis enzim-microwave tidak berbeda nyata dengan enzim-autoclave. Pengaruh waktu fermentasi 24 jam berbeda nyata dengan 48 jam dan 72 jam, tetapi pengaruh waktu 48 jam tidak berbeda nyata dengan 72 jam.
Rendemen etanol terhadap berat serbuk kolang-kaling dihitung karena selama proses penelitian digunakan serbuk kolang-kaling, tanpa adanya ekstraksi pati. Dengan proses ekstraksi, hanya pati yang dipecah menjadi glukosa, sementara diperkirakan ada jenis karbohidrat lain yang dapat menghasilkan glukosa. Selain itu, pada penelitian pendahuluan, nilai kadar glukosa untuk ekstraksi pati lebih rendah dibandingkan kadar glukosa dari serbuk kolang-kaling.
Peningkatan konsentrasi S. cerevisiae dan waktu fermentasi untuk hidrolisis AO cenderung meningkatkan rendemen etanol, meskipun peningkatan konsentrasi
S. cerevisiae tidak berpengaruh nyata, yang bererbeda dengan hidrolisis lainnya. Hal tersebut dimungkinkan karena jumlah kadar glukosa yang tersedia dari hidrolisis asam-autoclave mencukupi. Perlakuan dengan nilai efisiensi fermentasi tertinggi di sini berbeda dengan perlakuan yang memiliki rendemen etanol tertinggi. Perbedaan proses perhitungan dapat mempengaruhi nilai-nilai tersebut, karena untuk efisiensi fermentasi memperhitungkan glukosa yang dimanfaatkan, sedangkan rendemen etanol memperhitungkan etanol yang dihasilkan. Kemungkinan lainnya untuk efisiensi fermentasi tertinggi, tidak semua glukosa Tabel 1 Rendemen etanol berdasarkan hasil etanol terhadap kadar karbohidrat
12
dikonversi menjadi etanol, tetapi lebih banyak digunakan untuk pertumbuhan sel
S. cerevisiae.
Rendemen etanol yang diperoleh dapat digunakan untuk menduga volume etanol yang dihasilkan dari setiap pohon. Dinas Kehutanan Provinsi Jawa Tengah (2010) menyebutkan bahwa tanaman aren dapat memproduksi sekitar 50 kg kolang-kaling dalam setiap panen. Massa kolang-kaling tersebut apabila dengan memperhitungkan kadar air 62.38% (b/b, kering tanur), pada rendemen tertinggi dapat menghasilkan etanol sekitar 8.28 l setiap pohon dalam sekali panen.
SIMPULAN DAN SARAN
Simpulan
Daging buah aren atau kolang-kaling berpotensi sebagai alternatif sumber bioetanol. Metode hidrolisis asam dengan pemanasan autoclave memberikan kadar glukosa tertinggi. Sedangkan hidrolisis asam dengan pemanasan microwave
menghasilkan kadar glukosa terendah, karena waktu pemanasan microwave ini terlalu singkat. Kadar glukosa yang dihasilkan tersebut mempengaruhi proses fermentasi dan kadar etanol yang dihasilkan.
Hidrolisis asam dengan pemanasan autoclave merupakan perlakuan terbaik dengan efisiensi hidrolisis tertinggi, sehingga menghasilkan rendemen etanol yang tinggi. Metode yang memiliki efisiensi fermentasi tertinggi berbeda dengan rendemen etanol tertinggi, karena efisiensi fermentasi diperhitungkan dari jumlah glukosa yang dimanfaatkan S. cerevisiae sedangkan rendemen etanol dari jumlah etanol yang dihasilkan. Kemungkinan untuk efisiensi fermentasi tertinggi, glukosa yang dikonversi menjadi etanol lebih sedikit, tetapi lebih banyak digunakan untuk pertumbuhan sel S. cerevisiae.
13
Saran
Penelitian mengenai bioetanol dari daging buah aren belum ada sebelumnya. Penelitian ini masih perlu diadakan penelitian lanjutan, terutama untuk penentuan waktu optimum dalam penggunaan microwave dan penggunaan jenis mikroorganisme lain. Penggunaan parameter lain juga diperlukan untuk menilai setiap proses, seperti pertimbangan limbah dan biaya.
DAFTAR PUSTAKA
Adinoyl EH, Oti E, Sanchez T, Majekodunmi OR, Solomon AO, Ikpeama A. 2012. Effect of variety and influence of starch-hydrolyzing enzyme and yeast on the yield of ethanol generated from sweetpotato flour and starches.
Adv Appl Sci Res. 3(5):2774-2778.
Alim KY. 2002. Mempelajari pembuatan dan daya terima es krim kolang-kaling [skripsi]. Bogor (ID): Institut Pertanian Bogor.
Choudhary R, Umagiliyage AL, Liang Y, Siddaramu T, Haddock J, Markevicius G. 2012. Microwave pretreatment for enzymatic saccharification of sweet sorghum bagasse. Biomass and Bioenergy. 39:218-226. doi:10.1016/j.biombioe.2012.01.006.
Demirbas T, Demirbas AH. 2010. Bioenergy, green energy, biomass and biofuels.
Energy Sources. Part A. 32:1067-1075.doi: 10.1080/15567030903058600. Dinas Kehutanan Provinsi Jawa Tengah. 2010. Budidaya dan pengembangan tanaman Aren [Internet]. [diunduh 2012 Mei 12]. Tersedia pada:
http://epetani.deptan.go.id/budidaya/budidaya-dan-pengembangan-tanaman-aren-3703.
Dodic S, Popov S, Dodic J, Rankovic J, Zavargo Z, Mucibacic RJ. 2009. Bioethanol production from thick juice as intermediate of sugar beet processing. Biomass and Bioenergy. 33:822-827. doi:10.1016/j.biombioe.2009.01.002.
Efendi DS. 2010. Prospek pengembangan tanaman aren (Arenga pinnata Merr) mendukung kebutuhan bioetanol di Indonesia. Perspektif. 9(1):36-46. El-Zawawy WK, Ibrahim MM, Abdel-Fattah YR, Soliman NA, Mahmoud MM.
2011. Acid and enzymes hydrolysis to convert pretreated lignocellulosic materials into glucose for ethanol production. Carbohydrate Polymers. 84:865-871. doi:10.1016/j.carbpol.2010.12.022.
Gomez FJD, Hernandez CC, Carrillo EP, Rooney WL, Saldivar SOS. 2011. Evaluation of bioethanol production from five different varieties of sweet and forage sorghums (Sorghum bicolor (L) Moench). Industrial Crops and Products. 33:611-616.doi:10.1016/j.indcrop.2010.12.022.
Gupta R, Sharma KK, Kuhad RC. 2009. Separate hydrolysis and fermentation (SHF) of Prosopis julifora, a wood substrate, for the production of cellulosic ethanol by Saccharomyces cerevisiae and Pichia stipitis-NCIM
3498. Bioresour Technol. 100:1214-1220.
14
Hashem M, Darwish SMI. 2010. Production of bioethanol and associated by-products from potato starch residue stream by Saccharomyces cerevisiae.
Biomass and Bioenergy. 34:953-959.doi:10.1016/j.biombioe.2010.02.003. Iranmahboob J, Nadim F, Monemi S. 2002. Optimizing acid-hydrolysis: a critical
step for production of ethanol from mixed wood chips. Biomass and Bioenergy. 22:401-404.
Jamai L, Ettayebi K, Yamani JE, Ettayebi M. 2007. Production of ethanol from starch by free and immobilized Candida tropicalis in the presence of α
-amylase. Bioresour Technol. 98:2765-2770.
doi:10.1016/j.biortech.2006.09.057.
Jiping P, Shujun W, Jinglin Y, Hongyan L, Jiugao Y, Wenyuan G. 2007. Comparative studies on morphological and crystalline properties of B-type and C-type starches by acid hydrolysis. Food Chem. 105: 989-995. doi:10.1016/j.foodchem.2007.04.053.
Kadokawa JI, Murakami MA, Takegawa A, Kaneko Y. 2009. Preparation of cellulose – starch composite gel and fibrous material from a mixture of the polysaccharides in ionic liquid. Carbohydrate Polymers. 75:180-183. doi:10.1016/j.carbpol.2008.07.021.
Kasavi C, Finore I, Lama L, Nicolaus B, Oliver SG, Oner ET, Kirdar B. 2012. Evaluation of industrial Saccharomyces cerevisiae strains for ethanol production from biomass. Biomass and Bioenergy. 45:230-238.
Kolusheva T, Marinova A. 2007. A study the optimal conditions for starch hydrolysis through thermostable α-amylase. Journal of the University of Chemical Technology and Metallurgy. 42 (1):93-96.
Muhaemin. 2012. Budidaya aren (Arenga saccharifera Labill. Syn. A. Pinnata
(Wurmb.) Merr) [Internet]. [diunduh 2012 September 27]. Tersedia pada: http://ditjenbun.deptan.go.id/budtanan/images/stories/pdf/budidaya_aren.p df.
Muljadi E, Billah M, Karaman N. 2012. Proses produksi bioetanol berbasis singkong. Di dalam: Muljadi E, Billah M, Karaman N, editor.
Implementasi Teknologi Informasi dalam pengembangan industri pangan, kimia dan manufaktur; 2009 Nopember 25; Surabaya, Indonesia. Surabaya
(ID): Fakultas Teknik Industri & LPPM UPN “Veteran” Jawa Timur;
[diunduh 2012 Agustus 27]. Tersedia pada:
http://eprints.upnjatim.ac.id/id/eprint/1358.
Naiola E. 2006. Karakterisasi enzim kasar glukoamilase dari Saccharomycopsis sp. [Characterization of crude glucoamylase from Saccharomycopsis sp.].
Berita Biologi. 8 (3):187-192.
Nguyen MH, Prince RGH. 1996. A simple rule for bioenergy conversion plant size optimisation: bioethanol from sugar cane and sweet sorghum. Biomass and Bioenergy.10(516):361-365.
Nikolic S, Mojovic L, Rakin M, Dusanka P, Pejin J. 2010. Ultrasound-assisted production of bioethanol by simultaneous saccharification and fermentation of corn meal. Food Chem. 122:216-222. doi:10.1016/j.foodchem.2010.02.063.
15 Nitayavardhana S, Shrestha P, Rasmussen ML, Lamsal BP, Leeuwen JHV, Khanal SK. 2009. Ultrasound improved ethanol fermentation from cassava chips in cassava-based ethanol plants. Bioresour Technol. 101:2741-2747. doi:10.1016/j.biortech.2009.10.075.
Putri LS, Sukandar D. 2008. Konversi pati ganyong (Canna edulis Ker.) menjadi bioetanol melalui hidrolisis asam dan fermentasi. Biodiversitas. 9 (2): 112-116.
Puturuhu F, Riry J, Ngingi AJ. 2011. Kondisi fisik lahan tanaman Aren (Arenga pinnata L.) di Desa Tuhaha Kecamatan Saparua Kabupaten Maluku Tengah. Jurnal Budidaya Pertanian. 7 (2):94-99.
Risnoyatiningsih S. 2011. Hydrolysis of starch Saccharides from sweet potatoes using enzyme (Hidrolisis pati ubi jalar kuning menjadi glukosa secara enzimatis). Jurnal Teknik Kimia. 5 (2):417-424.
Ruane J, Sonnino A, Agostini A. 2010. Bioenergy and the potential contribution of agricultural biotechnologies in developing countries. Biomass and Bioenergy. 34:1427-1439. doi:10.1016/j.biombioe.2010.04.011.
Saifuddin N, Hussain R. 2011. Microwave assisted bioethanol production from sago starch by co-culturing of ragi tapai and saccharomyces cerevisiae. J Math & Stat. 7(3):198-206.
Santos JRA, Lucena MS, Gusmao NB, Gouveia ER. 2012. Optimization of ethanol production by Saccharomyces cerevisiae UFPEDA 1238 in simultaneous saccharification and fermentation of delignified sugarcane bagasse. Industrial Crops and Products. 36:584-588. doi:10.1016/j.indcrop.2011.10.002.
Shanavas S, Padmaja G, Moorthy SN, Sajeev MS, Sheriff JT. 2011. Process optimization for bioethanol production from cassava starch using novel eco-friendly enzymes. Biomass and Bioenergy. 35:901-909. doi:10.1016/j.biombioe.2010.11.004.
Sharma V, Rausch KD, Graeber JV, Schmidt SJ, Buriak P, Tumbleson ME, Singh V. 2010. Effect of resistant starch on hydrolysis and fermentation of corn starch for ethanol. Appl Biochem Biotechnol. 160:800-811. doi 10.1007/s12010.009.8651.7.
Singh A, Bishnoi NR. 2012. Optimization of ethanol production from microwave alkali pretreated rice straw using statistical experimental designs by
Saccharomyces cerevisiae. Industrial Crops and Products. 37:334-341. doi:10.1016/j.indcrop.2011.12.033.
Stanley D, Bandara A, Fraser S, Chambers PJ, Stanley GA. 2010. The ethanol stress response and ethanol tolerance of Sacchaomyces cerevisiae. J Appl Microbiol. 109:13-14. doi:10.1111/j.1365-2672.2009.04657.x.
Su MY, Tzeng WS, Shyu YT. 2010. An analysis of feasibility of bioethanol from Taiwan sorghum liquor waste. Bioresour Technol 101: 6669-6675. doi:10.1016/j.biortech.2010.03.105.
Tibayrenc P, Belloy LP, Ghommidh C. 2011. Single-cell analysis of S. cerevisiae
growth recovery after a sublethal heat-stress applied during an alcoholic fermentation. J Ind Microbiol Biotechnol. 38:687-696. doi:10.1007/s10295-010-0814-6.
16
Zhang B. Dhital S. Haque E. Gidley MJ. 2012. Preparation and characterization of gelatinized granular starches from aqueous ethanol treatments.
17
RIWAYAT HIDUP
Penulis dilahirkan di Ciamis pada tanggal 12 Juli 1989 sebagai anak ketiga dari tiga bersaudara dalam keluarga Bapak Oom Daryono dan Ibu Entin Kartini. Jenjang pendidikan formal yang telah dilalui penulis adalah TK Aisyiah, kemudian dilanjutkan di SD Negeri XI Banjarsari pada tahun 1996-2002, SMP Negeri 1 Banjarsari pada tahun 2002-2005, serta SMA Negeri 1 Banjarsari dan lulus pada tahun 2008.
Pada tahun 2008 penulis diterima sebagai mahasiswa Institut Pertanian Bogor melalui jalur USMI (Undangan Seleksi Masuk IPB) dan mendapatkan mayor Teknologi Hasil Hutan. Selanjutnya pada tahun 2011 penulis memilih Bagian Kimia Hasil Hutan sebagai bidang keahlian.
Selama menuntut ilmu di IPB, penulis telah mengikuti beberapa kegiatan praktek lapang, antar lain Praktek Pengenalan Ekosistem Hutan (PPEH) pada bulan Juli 2010 jalur Cilacap dan Baturraden, Jawa Tengah, serta pada bulan Juli 2011 penulis melaksanakan Praktek Pengelolaan Hutan (PPH) di Gunung Walat, Sukabumi. Penulis juga melakukan Praktek Kerja Lapang di PT. Pindo Deli Pulp and Paper Mills, Karawang, Jawa Barat pada tanggal 12 April-12 Mei 2012. Penulis pernah mengikuti sejumlah organisasi kemahasiswaan yakni anggota Paguyuban Mahasiswa Galuh Ciamis (PMGC) tahun 2008-2012, pengurus PC Sylva IPB tahun 2009-2010, pengurus Himpunan Profesi Departemen Hasil Hutan (Himasiltan) tahun 2009-2011, serta menjadi panitia Kompak THH tahun 2010. Penulis juga pernah mengikuti lomba karya tulis ilmiah di bidang penelitian yang didanai oleh Dirjen Pendidikan Tinggi, Kementrian Nasional dan pernah juga mendapatkan beasiswa PPA tahun 2009-2012.