Isoterm Adsorpsi Ion Ni(II)) dalam Larutan oleh Biomassa Alga
Nannochloropsis sp yang Dimodifikasi dengan Silika-magnet
Buhani, Suharso, dan Albert Ferdinan Partogi
Jurusan Kimia, F MIPA Universitas Lampung
Jl. Prof. Soemantri Brojonegoro No. 1 Bandar Lampung 35145 Tel. +62 (721) 770422; Fax +62 (721) 770422; email: buhani_s@yahoo.co.id Abstrak. Adsorpsi ion Ni(II) pada material biomassa alga Nannochloropsis sp yang
dimodifikasi dengan teknik pelapisan silika-magnetit (Fe3O4) telah dilakukan. Material hibrida Nannochloropsis sp-silika (HAS) dan Nannochloropsis sp dengan silika-magnet (HASM) disintesis melalui proses sol-gel dan dikarakterisasi dengan spekrofotometer inframerah (IR). Proses adsorpsi dilakukan dengan metoda bacth dan kadar ion Ni(II) dianalisis dengan spektrofotometer serapan atom (SSA). Adsorpsi ion Ni(II) pada konsentrasi awal 0-400 mg L-1, pH 6, dan waktu interaksi selama 60 menit oleh HAS dan HASM dievaluasi menggunakan model isotherm adsorpsi Langmuir dan Freundlich. Pola isotherm adsorpsi ion Ni(II) pada HAS dan HASM cenderung mengikuti isotherm Langmuir dengan kapasitas adsorpsi ion Ni(II) masing-masing sebersar 36,875 dan 45,385 mg g-1. Kata kunci: Adsorpsi, Nannochloropsis sp, pelapisan silika-magnet, ion Ni(II)
PENDAHULUAN
Pemanfaatan alga sebagai adsorben logam berat masih belum optimal, padahal alga memiliki kemampuan yang besar untuk mengikat logam berat. Hal ini disebabkan oleh beberapa kendala seperti ukurannya kecil, berat jenis yang rendah, dan mudah rusak karena degradasi oleh mikroorganisme lain. Selain itu juga alga tidak dapat digunakan secara langsung dalam kolom adsorpsi, karena sangat lunak dan tidak berbentuk granular. Untuk mengatasi kelemahan tersebut maka berbagai upaya dilakukan antara lain dengan mengimmobilisasi biomassa alga menggunakan berbagai polimer pendukung. Immobilisasi biomassa alga dengan matriks pendukung silika telah dilakukan dan berhasil meningkatkan kapasitas adsorpsi terhadap ion logam. Selain itu telah dilakukan peningkatan selektivitas adsorpsi melalui teknik imprinting ionik pada biomassa Nannochloropsis sp.
Meskipun telah diperoleh material hasil modifikasi biomasa alga dengan kapasitas,
selektivitas adsopsi besar, dan stabil secara kimia, akan tetapi dalam penggunaanya sebagai material adsorben untuk adsorpsi kontinyu menimbulkan permasalahan karena terbentuk padatan tersuspensi (flocculant) yang menghambat proses pemisahan logam dari larutan, akibatnya proses adsorpsi lebih lambat dan menghasilkan produk samping berupa padatan tersuspensi, sehingga kurang ramah lingkungan. Untuk itu perlu dilakukan modifikasi mikroalga lebih lanjut dalam meningkatkan daya gunanya sebagai adsorben logam berat.
Peningkatan kualitas biomassa alga sebagai adsorben dapat dilakukan dengan pelapisan partikel magnetit (Fe3O4) pada silika sebagai matriks pendukung. Teknik pelapisan silika dengan magnet merupakan teknik yang ramah lingkungan, karena tidak membentuk produk yang mengandung kontaminasi seperti padatan tersuspensi, selain itu mempercepat proses pemisahan logam dari larutan karena adsorben memiliki sifat magnet. Dengan menggunakan teknik tersebut, maka akan
diperoleh adsorben yang memiliki kapasitas dan selektivitas besar terhadap ion logam target serta dapat memisahkan logam target dengan cepat.
Bertitik tolak dari uraian tersebut maka dilakukan sintesis dan karakterisasi biomassa alga Nannochloropsis sp yang dimodifikasi dengan teknik pelapisan silika-magnet. Kamampuan adsorpsi dari material tersebut terhadap ion logam diuji dengan menggunakan ion Ni(II) sebagai adsorbat. Data adsorpsi yang diperoleh dievaluasi menggunakan model isoterm adsorpsi Langmuir dan Freundlich.
METODE PENELITIAN ALAT DAN BAHAN
Alat-alat yang digunakan dalam penelitian ini adalah alat-alat gelas yang biasa digunakan di laboratorium. Selain itu dilengkapi dengan peralatan untuk adsorpsi seperti, pengaduk magnet, pH meter, sentrifugator, kertas saring Whatman No.42. Spektrofotometer IR (Prestige-21 Shimadzu) digunakan untuk identifikasi gugus fungsional material HAS dan HASM. Analisis kadar ion Ni(II) dengan SSA Model Perkins Elmer 3110.
Bahan-bahan yang digunakan dalam penelitian ini adalah biomassa alga
Nannochloropsis sp yang diperoleh dari
Balai Besar Budidaya Laut Lampung.
Bahan-bahan kimia meliputi:
Ni(NO3)26H2O p.a Merck, magnetit (Fe3O4), tetraetil orthosilikat (TEOS), NaOH, HCl, NH4OH, etanol, larutan buffer pH 4 dan 7, dan akuades.
PROSEDUR PENELITIAN SINTESIS HAS DAN HASM
Sintesis HAS dilakukan dengan mengikuti prosedur yang telah dilaporkan Buhani dkk.,. Untuk sintesis material HASM dilakukan dengan mencampurkan sebanyak 5 mL TEOS, 2,5 mL akuades, dan 100 mg Fe3O4 dimasukkan ke dalam gelas
plastik dan diaduk dengan pengaduk magnet selama 30 menit serta ditambahkan HCl 1 M hingga pH 2 (Larutan I). Dalam pembuatan larutan II, sebanyak 400 mg biomassa Nannochloropsis sp ditambahkan 5 mL etanol, kemudian diaduk dengan pengaduk magnet sampai homogen. Selanjutnya, kedua larutan dicampurkan dan diaduk dengan pengaduk magnet hingga membentuk gel. Gel yang terbentuk didiamkan selama 24 jam. Kemudian dicuci dengan akuades dan etanol (60:40) hingga pH ≈ 7. Setelah dicuci, dikeringkan di dalam oven pada suhu 40ºC selama 2-3 jam hingga mencapai berat konstan.
UJI ADSORPSI
Sebanyak 50 mg material HAS dan HASM masing-masing ditambahkan 20 mL larutan ion Ni(II) dengan variasi konsentrasi 0 - 400 mg L-1 dan diinteraksikan pada pH ≈ 6 selama 6 menit. Kemudian campuran tersebut dipisahkan dengan sentrifugasi. Filtrat yang dihasilkan, dianalisis dengan SSA untuk menentukan kadar ion Ni(II). Korelasi antara konsentrasi awal ion Ni(II) yang digunakan dalam proses adsorpsi terhadap jumlah logam teradsorpsi oleh HAS dan HASM ditentukan dengan menggunakan persamaan berikut ini:
q = (Co-Ca)V/W (1)
dimana q menyatakan jumlah ion logam teradsorpsi (mg g-1), Co dan Ca menyatakan
konsentrasi awal dan kesetimbangan dari ion logam (mg L-1), W adalah massa adsorben (g), V adalah volume larutan ion logam (L).
HASIL DAN PEMBAHASAN KARAKTERISASI MATERIAL
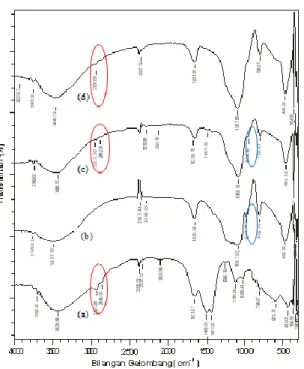
Pada Gambar 1c dan d dapat diamati spektra IR dari material HAS dan HASM menunjukkan pola serapan yang berasal dari gabungan spektra IR yang terdapat pada biomassa alga Nannochloropsis sp dan silika. Hal ini ditunjukkan dengan adanya serapan pada daerah bilangan gelombang
2931,80 cm-1 yang merupakan serapan vibrasi ulur -C-H dari (-CH2) alifatik yang berasal dari biomassa alga Nannochloropsis sp (Gambar 1a).
GAMBAR 1. Spektra IR a) alga, b) silika, c) HAS,
dan d) HASM
Lebih lanjut pada material HAS dan HASM (Gambar 1c dan d ) terdapat pita serapan yang berasal dari material silika, yaitu puncak serapan pada bilangan gelombang 1087,85 cm-1 yang merupakan serapan vibrasi asimetri atom O dari gugus Si-O-Si. Adanya gugus siloksan diperkuat dengan munculnya serapan pada 802,39 cm -1
yang menunjukkan vibrasi ulur simetris dari Si-O dan puncak pada 462,92 cm-1 dari vibrasi tekuk dari Si-O dari gugus siloksan (Si-O-Si). Pita serapan pada 964,41 cm-1 berasal vibrasi ulur Si-O dari silanol (Si-OH). Pada bilangan gelombang 3487,30 cm-1 muncul puncak serapan dengan pita lebar yang merupakan vibrasi ulur -OH dari gugus silanol (Si-OH) (Gambar 1b). Berdasarkan spektra IR yang terdapat pada material HAS dan HASM dapat dinyatakan bahwa hibridisasi biomassa alga Nannochloropsis sp dengan silika telah berhasil dilakukan.
ISOTERM ADSORPSI
Evaluasi isotherm adsorpsi pada penelitian ini dilakukan pendekatan korelasi antara jumlah ion Ni(II) yang teradsorpsi secara eksperimen dengan metode bacth dan jumlah ion Ni(II) yang teradsorpsi secara estimasi melalui persamaan isotherm adsorpsi yang digunakan yaitu model Langmuir (persamaan 2 ) dan Freundlich (persamaan 3) [4, 13] sebagai berikut.
e L e L m e C K C K q q 1 (2) e f e C n K q log 1log log (3) Dimana, qm dan qe masing-masing adalah
jumlah ion logam maksimum teradsorpsi dan jumlah ion logam dalam kesetimbangan (mg g-1), Ce adalah konsentrasi
kesetimbangan ion logam (mL g-1), n eksponen Freundlich adalah KL (L mol-1)
dan KF (mg g-1) masing-masing adalah
konstanta Langmuir dan Freundlich.
Lebih lanjut kedua parameter isotherm adsorpsi tersebut dievaluasi dengan menentukan root mean squared
error (RMSE) dan chi-square test (χ2) [14-15] dengan masing-masing formula sebagai berikut :
m i cal i i q q m RMSE 1 2 , exp , 2 1 (4)
m i i cal i i q q q 1 2 exp , , exp , 2 (5) dimana qi,exp and qi,cal masing-masingdiperoleh dari hasil eksperimen dan hasil estimasi melalui isotherm adsorpsi, m adalah jumlah pengamatan dalam percobaan isotherm adsorpsi yang dilakukan.
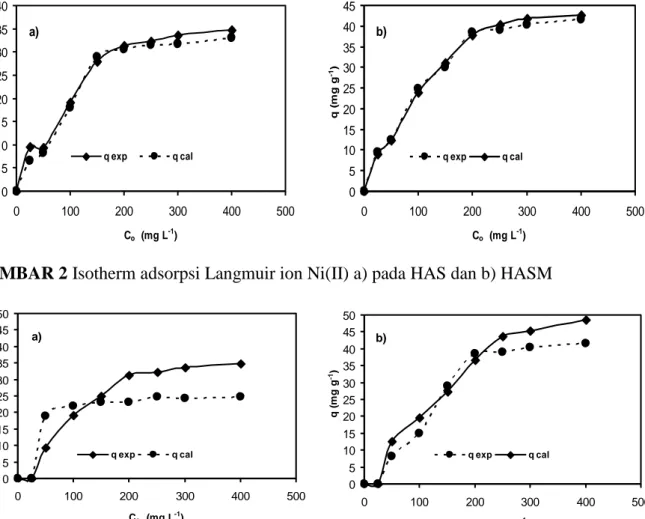
GAMBAR 2 Isotherm adsorpsi Langmuir ion Ni(II) a) pada HAS dan b) HASM
GAMBAR 3 Isotherm adsorpsi Freundlich ion Ni(II) a) pada HAS dan b) HASM
Pada Gambar 2 dapat dilihat pola isotherm adsorpsi ion Ni(II) oleh HAS dan HMS menunjukkan bahwa makin tinggi konsentrasi ion Ni(II) yang dipaparkan,
maka makin meningkat jumlah ion Ni(II) yang teradsorpsi. Selain itu jumlah logam teradsorpsi yang ditentukan secara eksperimen (qexp) dan
hasil estimasi yang
Tabel 1. Parameter adsorpsi ion Ni(II) oleh HAS dan HASM pada pH 6, waktu interaksi 60 Menit
Data pada Tabel 1 menunjukkan bahwa, kapasitas adsorpsi ion Ni(II) pada material HASM lebih besar dibandingkan dengan HAS. Hal ini dapat terjadi karena pada HASM, selain gugus aktif dari biomassa
Nannochloropsis sp dan silika (siloksan dan
silanol), maka terjadi peningkatan interaksi antara ion Ni(II) dengan HASM karena ada sifat magnet dari HASM yang berasal dari pelapisan magnet silika [17-18]. Adanya sifat magnet pada HASM menyebabkan interaksi antara ion Ni(II) dan HASM tidak saja terjadi melalui interaksi kimia tetapi juga melalui interaksi fisika yang melibatkan sifat magnet dari material adsorben dan ion logam sebagai adsorbat.
KESIMPULAN a) 0 5 10 15 20 25 30 35 40 0 100 200 300 400 500 Co (mg L-1) q ( m g g -1) q exp q cal b) 0 5 10 15 20 25 30 35 40 45 0 100 200 300 400 500 Co (mg L-1) q ( m g g -1) q exp q cal a) 0 5 10 15 20 25 30 35 40 45 50 0 100 200 300 400 500 Co (mg L -1 ) q ( m g g -1) q exp q cal b) 0 5 10 15 20 25 30 35 40 45 50 0 100 200 300 400 500 Co (mg L-1) q ( m g g -1) q exp q cal Parameter Langmuir Adsorben qm (mg g-1) KL x 10 -4 L mol-1 R2 RMSE χ2 HAS 36,875 10,596 0,996 1,676 1.364 HASM 45,385 4,727 0,988 1,060 0.233 Parameter Freundlich Adsorben n KF (mg g-1) R2 RMSE χ2 HAS 4,807 1,643 0,822 9,070 19,663 HASM 2,283 5,081 0,889 5,310 6,446
Pembuatan material biomassa alga
Nannochloropsis sp melalui modifikasi
dengan silika-magnet telah berhasil dilakukan dan diuji kemampuan adorpsinya terhadap ion Ni(II) dalam larutan. Material tersebut memiliki kapasitas adsorpsi lebih besar dibandingkan dengan material hibrida biomassa alga-silika dan cenderung mengikuti pola isotherm adsorpsi Langmuir.
UCAPAN TERIMA KASIH
Terima kasih kepada Direktorat Jendral Pendidikan Tingggi (DIKTI) Kementrian Pendidikan dan Kebudayaan RI atas didanainya penelitian ini melalui Hibah Kompetensi tahun 2013.
DAFTAR PUSTAKA
P.O. Harris and G.J. Ramelow. (1990). Binding of metal ions by particulate biomass derived from Chorella vulgaris and Scenedesmus quadricauda, Enviromental Science & Technologyl.
Vol. 24: 220-228.
B. Volesky and Z.R. Holan. (1995). Biosorption of heavy metals.
Biotechnology Progress. Vol.
11:235-250.
Buhani and Suharso. (2009).
Immobilization of Nannochloropsis sp biomass by sol-gel technique as adsorbent of metal ion Cu(II) from aqueous solution. Asian Journal of
Chemistry, Vol. 21(5): 3799-3808.
Buhani, Suharso and Sumadi. (2010). Adsorption kinetics and isotherm of Cd(II) ion on Nannochloropsis sp biomass imprinted ionic polymer.
Desalination, Vol. 259 :140-146.
Buhani, Suharso and Sumadi. (2012). Production of ionic imprinted polymer from Nannochloropsis sp biomass and its adsorption characteristics toward
Cu(II) ion in solutions. Asian Journal of Chemistry, Vol. 24(01): 133-140.
C. Jeon. (2011). Adsorption characteristic of copper ions using magnetically modified medicinal stones, Journal of
Industrial and Engineering Chemistry,
Vol. 17: 321-324.
Q. Peng, Y. Liu, G. Zeng, W. Xu, C. Yang, and J. Zhang. (2010). Biosorption of copper(II) immobilizing Saccharomyces
cerevisae on the surface of
chitosan-coated magnetic nanoparticle from aqueous solution. Journal of Hazardous
Materials, Vol. 177: 676-682.
Y. Lin, H. Chen, K. Lin, B. Chen, and C. Chiou. (2011). Application of magnetic particles modified with amino groups to adsorb cooper ions in aqueous solution.
J. Environt. Sci., 23: 44-50.
Y.C. Chang and D.H. Chen. (2005). Preparation and adsorption properties of monodisperse chitosan-bound Fe3O4 magnetic nanoparticles for removal of Cu(II) ions. Journal of Colloid and
Interface Science. Vol. 283: 446-451.
J. Hu, M.C. Lo, and G.H. Chen. (2004). Adsorption of Cr(VI) by magnetite nanoparticles, Water Science and Technology. Vol. 50: 139-146.
Y. Ren, M. Zhang, and D. Zhao. (2008). Synthesis and properties Cu(II) ion imprinted composite adsorbent for selective removal of copper,
Desalination, 228: 135-149.
A.F. Partogi. (2012). Modifikasi biomassa
Nannochloropsis sp dengan pelapisan
silika-magnetit sebagai adsorben ion Zn(II) dan Ni(II). Skripsi, Universitas Lampung.
A. Aklil, M. Mouflih, and S. Sebti. (2004). Removal of heavy metal ions from water by using calcined phosphate as new adsorbent. Journal of Hazardous Materials, Vol. A112: 183-190.
M. M. Montazer-Rahmati, P. Rabbani, A. Abdolali, and A.R. Keshtkar. (2011). Kinetics and Equilibrium Studies on Biosorption of Cadmium, Lead, and Nickel Ions from Aqueous Solution by Intact and Chemically Modified Brown Algae. Journal of Hazardous Materials, Vol. 185: 401-407.
N. Chen, Z. Zhang , C. Feng, M. Li, D. Zhu, and N. Sugiura. (2011). Studies on fluoride adsorption of iron-impregnated granular ceramics from aqueous solution. Materials Chemistry and Physics, Vol. 125: 293-298.
K. Vijayaraghavan, M. Sathishkumar, and R. Balasubramanian. (2011). Interaction of rare earth elements with a brown
marine alga in multi-componen solutions, Desalination, Vol. 265: 54-59. A.Z.M. Badruddoza, A.S.H. Tay, P.Y. Tan, K. Hidayat, and M.S. Uddin. (2011), Carboxymethyl-ß-cyclodextrin
conjugated magnetic nanoparticles as nano-adsorbents for removal of copper ions: Synthesis and adsorption studies,
Journal of Hazardous Materials, Vol.
185: 1177-1186.
I. Larraza, M. Lopez-Gonzales, T. Corrales, and G. Marcelo. (2012). Hybrid materials: Magnetite-Polyethylenimine-Montmorillonite, as magnetic adsorbent for Cr(VI) water treatment, Journal of
Colloid and Interface Science, Vol.