BAHAN DAN METODE PENELITIAN
Lokasi dan Waktu Penelitian
Penelitian ini dilaksanakan di Laboratorium Ilmu Nutrisi dan
Makanan Ternak Jl. Prof. A. Sofyan No. 3 Program Studi Magister Ilmu
Peternakan Fakultas Pertanian Universitas Sumatera. Penelitian ini dilakukan
pada bulan Mei 2016 sampai dengan Januari 2017.
Bahan dan Alat Penelitian
Bahan
Bahan yang digunakan pada penelitian ini antara lain:
bungkil inti sawit (BIS), Asam Asetat (CH3COOH) 1 %, enzim mannanase,
aquades dan bahan-bahan k i m i a untuk analisis laboratorium yang diperoleh
dari perusahaan komersil serta 25 ekor ayam broiler berumur 5 minggu yang
digunakan untukmengukur energi metabolis.
Alat
Alat yang digunakan antara lain timbangan digital, grinder, oven,
shaker water bath, centrifuge, vortex mixer, ayakan, autoclave, freezer,
gelas ukur, aluminium foil, tabung reaksi, labu Erlenmeyer, labu ukur,
pipet mikro, plastik tahan panas, plastik klip dan kandang metabolis ukuran
50 x 20 x 50 cm yang dilengkapi dengan penampung feses, tempat pakan dan air
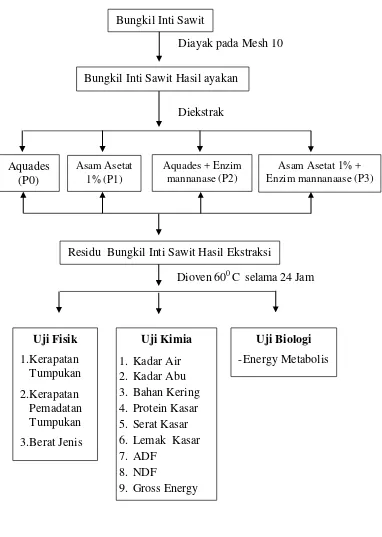
Skema Penelitian
Skema penelitian yang dilakukan adalah sebagai berikut :
Prosedur Penelitian
Persiapan Bungkil Inti Sawit
Bungkil inti sawit yang diperoleh dari industri dipisahkan menggunakan
ayakan No.10 mesh 9 (2 mm/0,787 inches). BIS yang diperoleh, selanjutnya
diproses sesuai perlakuan.
Ekstraksi Bungkil Inti Sawit
1. Ekstraksi Bungkil Inti Sawit Dengan Aquades
Bungkil inti sawit yang sudah diayak ditimbang sebanyak 50 g.
kemudian dituang ke dalam labu Erlenmeyer 500 ml ditambahkan aquades
sebanyak 500 ml. Perbandingan BIS dengan aquades adalah 1:10.
Larutan BIS dengan aquades dihomogenkan kemudian dibungkus dengan plastik
bening tahan panas. Disterilkan dengan autoclave pada suhu 1100 C selama 1 jam kemudian didinginkan sampai suhu 400 C kemudian campuran BIS dengan
aquades dicentrifuge pada suhu 150 C 4200 rpm selama 15 menit. Supernatant dan residu dipisahkan, dikoleksi dan disimpan difreezer pada suhu
50 C. Residu diovenkan pada suhu 600 C selama 24 jam. Residu kering ini menjadi bahan perlakuan P0.
2. Ekstraksi Bungkil Inti Sawit dengan Asam Asetat (CH3COOH)
a. Pembuatan Asam Asetat 1 %
Aquades 500 ml dimasukkan ke dalam labu ukur 1000 ml kemudian asam
asetat murni/glasial 10 ml dipipetkan ke dalam aquades 500 ml tersebut dengan
menggunakan pipet skala. Tambahkan aquadest sampai batas tanda tera kemudian
b. Ekstraksi Bungkil Inti Sawit Dengan Asam Asetat 1 %
Bungkil inti sawit yang sudah diayak ditimbang sebanyak 50 g.
kemudian dituang ke dalam labu Erlenmeyer 500 ml ditambahkan asam asetat 1%
sebanyak 500 ml. Perbandingan BIS dengan asam asetat 1% adalah 1:10.
Larutan BIS dengan asam asetat 1% dihomogenkan kemudian dibungkus dengan
plastik bening tahan panas. Disterilkan dengan autoclave pada suhu 1100 C selama 1 jam kemudian didinginkan sampai suhu 400 C kemudian campuran BIS dengan Asam Asetat 1% dicentrifuge pada suhu 150 C 4200 rpm selama 15 menit. Supernatant dan residu dipisahkan, dikoleksi dan disimpan difreezer suhu 50 C. Residu diovenkan pada suhu 600 C selama 24 jam. Residu kering ini menjadi bahan perlakuan P1.
3. Ekstraksi Bungkil Inti Sawit dengan Aquades Ditambah Enzim
Mannanase
Bungkil inti sawit yang sudah diayak ditimbang sebanyak 50 g,
kemudian dituang ke dalam labu Erlenmeyer 500 ml ditambahkan aquades
sebanyak 500 ml dan enzim mannanase sebanyak 83 µl. Perbandingan BIS
dengan aquadest adalah 1:10. Larutan diinkubasi dengan shaker water bath pada
suhu 600 C selama 72 jam kemudian didinginkan sampai suhu 400 C, kemudian campuran BIS dengan aquadest tambah enzim mannanase dicentrifuge pada suhu
150 C 4200 rpm selama 15 menit. Supernatant dan residu dipisahkan, dikoleksi dan disimpan difreezer suhu 50 C. Residu diovenkan pada suhu 600 C
4. Ekstraksi BIS dengan Asam Asetat 1% Ditambah Enzim Mannanase
Bungkil Inti sawit yang sudah diayak ditimbang sebanyak 50 g,
kemudian dituang ke dalam labu Erlenmayer 500 ml ditambahkan asam asetat 1%
sebanyak 500 ml dan enzim mannanase sebanyak 83 µl. Perbandingan BIS
dengan asam asetat 1 % adalah 1:10. Larutan diinkubasi dengan shaker water
bath pada suhu 600 C selama 72 jam kemudian didinginkan sampai suhu 400 C
kemudian campuran BIS dengan asam asetat tambah enzim mannanase
dicentrifuge pada suhu 150 C 4200 rpm selama 15 menit. Supernatant dan residu dipisahkan, dikoleksi dan disimpan difreezer suhu 50 C. Residu diovenkan pada suhu 600 C selama 24 jam. Residu ini menjadi bahan perlakuan P3.
Prosedur Uji Kualitas Fisik Pakan
1. Kerapatan Tumpukan (Khalil, 1999)
Kerapatan tumpukan diukur dengan menggunakan metode Khalil (1999).
Bahan dicurahkan ke dalam gelas ukur dengan menggunakan corong dan sendok
teh sampai volume 30 ml. Gelas ukur yang telah berisi bahan ditimbang.
Adapun perhitungan kerapatan tumpukan adalah dengan cara membagi berat
bahan dengan volume ruang yang ditempati. Kerapatan tumpukan dihitung
dengan rumus :
Kerapatan tumpukan = Berat Bahan (kg)
Volume Ruang (m3)
2. Kerapatan Pemadatan Tumpukan (Khalil, 1999)
Kerapatan pemadatan tumpukan diukur dengan menggunakan metode
khalil (1999). Pengukuran hampir sama dengan pengukuran kerapatan tumpukan,
menggoyang-goyangkan gelas ukur dengan tangan selama 10 menit.
Kerapatan pemadatan tumpukan dihitung dengan rumus:
Kerapatan pemadatan tumpukan = Berat bahan (kg)
Volume setelah pemadatan (m3)
3. Berat Jenis (Khalil,1999)
Berat jenis (kg/m3). Bahan dimasukan ke dalam galas ukur 100 ml dengan menggunakan sendok teh secara perlahan sampai volume 30 ml. Gelas ukur yang
sudah berisi bahan ditimbang. Aquadest sebanyak 50 ml dimasukan ke dalam
gelas ukur. Pengadukan menggunakan pengaduk mika dilakukan untuk
menghilangkan udara antar partikel. Sisa bahan yang menempel pada pengaduk
dimasukan dengan menyemprotkan aquades dan ditambahkan kedalam volume
awal. Pembacaan volume akhir dilakukan setelah konstan. Perubahan volume
aquadest merupakan volume bahan sesungguhnya. Pembacaan volume dilakukan
setelah volume air konstan. Berat jenis dihitung dengan rumus :
Berat Jenis = Berat Bahan (kg)
Perubahan volume Aquades (m3)
Prosedur Uji Kualitas Kimia Pakan
1. Kadar Air dan Bahan Kering (AOAC, 1995)
Banyaknya kadar air dalam suatu bahan pakan dapat diketahui bila bahan
pakan tersebut dipanaskan pada suhu 105⁰ C. Bahan kering dihitung sebagai
selisih antara 100% dengan persentase kadar air suatu bahan pakan yang
dipanaskan hingga ukurannya tetap.
Prosedur kerjanya, cawan porselin kosong dipanaskan dalam tanur
hingga 1100 C. Angkat cawan porselin dan dinginkan ke dalam desikator selama 30 menit lalu ditimbang. Timbang residu BIS hasil perlakuan seberat 2 g (A)
setelah itu masukan ke dalam cawan porselen (A) kemudian panaskan cawan yang
berisi residu BIS hasil perlakuan ke dalam oven 1100 C selama 2 jam (B). Angkat dan dinginkan ke dalam desikator selama 30 menit, lalu ditimbang (C)
dan dihitung ke dalam rumus :
Kadar Air = (A + B) – C X 100 %
B
Dan bahan kering dihitung dengan rumus :
Kadar bahan kering (BK) = 100 %- kadar air
2. Kadar Abu (AOAC, 1995)
Analisa kadar abu bertujuan untuk memisahkan bahan organik dan bahan
anorganik suatu bahan pakan. Kandungan abu ditentukan dengan cara
mengabukan atau membakar bahan pakan dalam tanur, pada suhu 400 - 6000 C sampai semua karbon hilang dari sampel, dengan suhu tinggi ini bahan organik
yang ada dalam bahan pakan akan terbakar dan sisanya merupakan abu yang
dianggap mewakili bagian inorganik makanan.
Prosedur kerjanya, cawan porselin kosong dipanaskan dalam tanur
pengabuan suhu 6000 C selama 2 jam, kemudian suhu tanur diturunkan hingga 1100 C. Cawan porselin kosong dalam tanur diangkat dan dinginkan dalam desikator selama 30 menit lalu timbang (A). kemudian masukan ke dalam cawan
porselin berisi residu BIS hasil perlakuan dalam tanur suhu 6000 C selama
Dihitung dengan rumus :
Kadar Abu = (C - A) X 100 %
B
3. Kadar Serat Kasar
Bahan dilarutkan dengan larutan H2SO4 1,25 % (setara 0,255 N) mendidih
selama 30 menit dan larutan NaOH 1,25 % (setara 0,313 N) mendidih selama
30 menit. Bagian yang tidak larut dinyatakan sebagai serat kasar.
Prosedur kerjanya, kertas Whatman no. 40 dipanaskan dalam oven pada
suhu 1100 C selama 1 jam. Diangkat dan dinginkan kedalam desikator selama 30 menit lalu ditimbang (A). Ditimbang sebanyak 2 g residu BIS hasil perlakuan
(B). Dieksatraksi lemaknya lalu dipindahkan kedalam becker glass 600 ml.
Ditambahkan 200 ml larutan H2SO4 1,25 % panas, dipasang di dalam alat
pereduksi dengan pendingin dibalik dan didihkan selama 30 menit.
Suspensi yang diperoleh disaring dengan menggunakan kertas Whatman
no. 41 dan pisahkan ke dalam beker glass 600 ml dan ditambahkan larutan NaOH
1,25 % panas. Dipasang kembali alat destruksi dengan pendingin terbalik,
didihkan kembali selama 30 menit.
Suspensi yang diperoleh kembali disaring dengan kertas whatman no 40
yang telah di oven dan telah diketahui bobotnya (A). Dibilas dengan akuades
panas hingga netral, dicuci dengan larutan K2SO4 10 % sebanyak 50 ml. Dibilas
kembali dengan akuades panas hingga netral kembali dan disiram alcohol 95 % 15
ml. Dikeringkan kertas residu berisi serat panaskan ke dalam oven pada suhu 1100 C selama 2 jam minimal. Kemudian diangkat dan dinginkan dalam desikator
Perhitungan dilakukan dengan rumus :
Kadar Serat (%) = (C - A) x 100 % B
4. Kadar Protein Kasar (AOAC, 1995)
Kadar protein diukur dengan menggunakan metoda Kjeldahl. Protein
rata-rata mengandung 16% Nitrogen, maka 100 % : 16 % = 6.25 harus dipakai untuk
mendapatkan nilai protein kasar (Protein kasar = N % x 6.25).
Prosedur kerjanya, ditimbang 0,3 gram residu BIS hasil perlakuan (A)
kemudian dimasukkan ke dalam tabung destruksi dan tambahkan 1,5 ml
katalisator, 1 ml H2O2 dan 10 ml H2SO4 pekat, kemudian dipanaskan secara
perlahan hingga suhu 4250 C pada unit alat destruksi dalam ruang asam sehingga cairan jernih, kemudian dinginkan dan tambahkan 25 ml aquades seacara perlahan
setelah itu tabung destruksi dengan perangkat alat destilasi dihubungkan,
ditambahkan larutan NaOH 40 % secara otomatis. Lakukan destilasi selama
4 menit hingga diperoleh destilat + 125 ml asam borat 4 %. Kemudian dititrasi
dengan larutan HCL 0,2 N hingga warna berubah dari hijau menjadi merah muda
atau jingga. Dihitung dengan rumus :
Kadar Nitrogen (%) = Y
14,01x N titran x100 x (ml titrasi sampel- ml titrasi blanko)x100 % Y (%) =
Mg Sampel
Kadar Protein (%) = % Nitrogen X angka Faktor
5. Kadar Lemak Kasar (AOAC, 1995)
Kandungan lemak suatu bahan pakan dapat ditentukan dengan metode
Selain mengandung lemak sesungguhnya, ekstrak eter juga mengandung waks
(lilin), asam organik, alkohol, dan pigmen, oleh karena itu fraksi eter untuk
menentukan lemak tidak sepenuhnya benar (Anggorodi, 1994).
Prosedur kerjanya, ditimbang residu BIS hasil perlakuan sebanyak 0,5-2 g
(A) dan kemudian masukan ke dalam cawan stainless homogenizer kemudian
tambah air sebanyak 0,6 ml aduk secara manual hingga merata, ditambahkan
10 ml methanol dan 20 ml chloroform kemudian diaduk dengan alat homogenizer
dengan kecepatan 1500 rpm selama 3 menit. Dibuka dan ditambahkan lagi 10 ml
methanol, aduk kembali dengan alat yang sama selama 1 menit.
Disaring dengan kertas saring top filter paper dan tamping dalam labu
terpisah. Hasil saringan ditambahkan 7,5 ml larutan NaCl 0,9 % selanjutnya
dikocok hingga homogen, diamkan hingga terbentuk lapisan sempurna.
Dipindahkan lapisan bawah (lemak dalam larutan chloroform) tamping dalam
botol asah evaporator, uapkan pelarut dengan alat evaporator. Lemak dipindahkan
ke dalam botol contoh yang telah diketahui botolnya, (B). Keringkan dengan oven
pengering suhu 410 C, kemudian diangkat dan didinginkan di desikator selama 30 menit lalu ditimbang. Dihitung dengan rumus
Kadar Lemak = (C - B) X 100 % A
7. Kandungan NDF (Metoda Van Soest & Robertson 1968).
Residu BIS hasil perlakuan ditimbang 1 g dan dimasukkan ke dalam gelas
piala 600 ml. Kemudian ditambahkan 100 ml larutan NDS (Neutral Detergent
Fiber). Setelah itu dipanaskan (ekstraksi) dengan pemanas listrik selama 1 jam
kertas saring yang telah diketahui beratnya (b gram) dengan bantuan pompa
vakum. Residu hasil penyaringan dibilas dengan 300 ml air panas ± 5 kali dan
terakhir dengan 25 ml aseton/alcohol 96 % ± 2 kali. Residu kemudian dikeringkan
dalam oven pada suhu 105º C selama 8 jam. Kemudian didinginkan di dalam
desikator selama 30 menit dan timbang (c gram). Persentase NDF dihitung dengan
menggunakan persamaan :
Kadar NDF = ADF X 100% % BK
8. Kandungan ADF (Metoda Van Soest & Robertson 1968).
Residu BIS hasil perlakuan ditimbang 1 g dan dimasukkan ke dalam gelas
piala 600 ml. Kemudian ditambahkan 100 ml larutan ADS (Acid Detergent
Fiber). Setelah itu dipanaskan (ekstraksi) dengan pemanas listrik selama 1 jam
dihitung mulai dari mendidih. Hasil ekstraksi disaring dengan menggunakan
kertas saring yang telah diketahui beratnya (b gram) dengan bantuan pompa
vakum. Residu hasil penyaringan dibilas dengan 300 ml air panas ± 5 kali dan
terakhir dengan 25 ml aseton/alcohol 96 % ± 2 kali. Residu kemudian dikeringkan
dalam oven pada suhu 105ºC selama 8 jam. Kemudian didinginkan didalam
desikator selama 30 menit dan timbang (c gram). Rumus perhitungan :
Kadar ADF = NDF X 100% % BK
9. Kandungan Energi Bruto
Residu BIS hasil perlakuan ditimbang 1 g kemudian dibakar dalam bomb
kalorimeter yang sudah diisi gas O2 dengan tekanan mencapai 25 - 30 atm.
Panas pembakaran akan menaikkan suhu air. Panas (kalor) yang dibutuhkan untuk
menaikan suhu 1 kg air sebanyak 10 C adalah 1 kilokalori.
Sampel dalam bentuk pellet ditimbang 0,5 –1 gram, kemudian dimasukkan
kedalam cawan bomb dan disentuhkan kawat platina sepanjang 10 cm pada
sampel dalam tabung bomb, terus diisi dengan oksigen sebanyak 25 atm.
Tabung bomb dimasukkan kedalam buchet yang sudah diisi air sebanyak 2 liter
kemudian ditulis, serta suhu distabilkan dengan memutar tombol pemutar selama
5 menit, setelah itu dicatat sebagai suhu awal.
Sampel dibakar dengan menekan tombol pemutar pada alat Parr Ignation,
biarkan temperatur naik sampai stabil (lebih kurang 5 menit), setelah itu suhu
dicatat sebagai suhu akhir, kemudian buka calorimeter dan keluarkan tabung
bomb dan buang oksigen dari bomb, lalu cuci bagian dalam tabung dan cawan
bomb dengan menyemprotkan aquadest dan beri beberapa tetes larutan methyl
orange. Titer dengan larutan Na2CO3 sampai berubah warna dan catat volume
titrasi yang dipakai lalu kawat yang dibakar diukur dengan sekala dari kawat yang
tidak terbakar. Persamaan yang dipakai :
(T2-T1) x 1325,605 GE =
A
Keterangan : A : Berat sampel
T1 : suhu konstan sebelum dibomb
Prosedur Uji Biologi (Energi Metabolis) (Sibbald, 1976)
Tahapan Persiapan Kandang Metabolis
Kandang metabolis sebelum digunakan dan peralatan pendukung lainnya
dibersihkan dan disterilisasikan terlebih dahulu dengan menggunakan desinfektan.
Lampu penerangan dipersiapkan. Lampu dinyalakan hanya pada malam hari.
Penentuan letak kandang dilakukan secara acak dan untuk memudahkan
pencatatan masing-masing kandang diberi tanda sesuai dengan perlakuan yang
diberikan.
Masa Istirahat Ayam
Sebelum ayam ditempatkan pada kandang metabolis, terlebih dahulu ayam
percobaan ditimbang bobot badannya. Ayam kemudian dipelihara seperti biasa
pada kandang metabolis selama 24 jam untuk proses adaptasi lingkungan.
Pemuasaan Ayam
Pemuasaan ayam yaitu penghentian pemberian pakan tanpa menghentikan
pemberian air minum yang bertujuan mengosongkan saluran pencernaan dari
sisa-sisa pakan sebelumnya. Pemuasaan ini dilakuan selama 24 jam.
Tahap Pelaksaaan Percobaan
1. Semua ayam ditimbang untuk mengetahui bobot ayam setelah pemuasaan.
Kemudian dikelompokkan sesuai rataan bobotnya dan ditentukan jumlah
ayam yang dikembangkan sebagai ulangan pengujian.
2. Mulai perlakuan ayam diberi makan dengan bahan percobaan secara loloh
paksa (force feeding) 35 gr/ ekor.
4. Seluruh ayam yang diuji 20 ekor yang diberi makan bahan percobaan
dan 5 ekor ayam yang dipuasakan ditampung ekskretanya selama 24 jam.
Setiap 3 jam sekali tempat penampungan ekskreta disemprot asam sulfat
H2SO4 0,01 N untuk mencegah penguapan nitrogen.
5. Ekskreta diangkat dan ditimbang bobot basahnya kemudian ditempatkan
dalam wadah khusus yang diberi nomor sesuai dengan ayamnya.
Kemudian seluruh sempel kotoran dikeringkan dioven dengan suhu 600 C selama 24 jam (Farrell, 1978).
6. Eksreta yang kering dibersihkan dari bulu dan kulit kaki ditimbang bobot
keringnya, kemudian dihaluskan dan dianalisis kandungan energi brutonya.
7. Perhitungan nilai energi metabolis (EM) dihitung dengan rumus
Sibbald (1995) dan Yamazaki (1986) yang disitasi oleh Sulistiyanto (2001).
E Intake – (E Excreta – E Excreta Unfeed)
TME=
Intake
Keterangan :
TME : True metabolizable energy (kkal/kg)
E Intake : ∑ konsumsi X gross energi bahan pakan (kkal/kg)
E Excreta : ∑ ekskreta X gross energi ekskreta (kkal/kg)
E Excreta Unfeed : ∑ ekskreta ayam dipuasakan X gross energy (kkal/kg)
Rancangan dan Analisis Data
Metode Penelitian
Metode penelitian yang digunakan adalah secara experimental dengan
menggunakan rancangan acak lengkap (RAL) dengan 4 perlakuan dan 5 ulangan
dengan setiap ekor ayam sebagai unit percobaan pada uji biologis
(energi metabolis). Perbandingan bungkil inti sawit dengan bahan pengekstrak
dalam setiap perlakuan adalah 1:10.
Perlakuan pada penelitian ini yaitu:
P0 = Bungkil Inti Sawit + Aquadest (Kontrol)
P1 = Bungkil Inti Sawit + Asam Asetat 1%
P2 = Bungkil Inti Sawit + Aquades + Enzim Mannanase 100U/l
P3 = Bungkil Inti Sawit + Asam Asetat 1 % + Enzim Mannanase 100U/l
Menurut Hanafiah (2003) model matematika percobaan yang digunakan
adalah : Yij = μ + τi + εij
Dimana:
Yij = nilai unit percobaan pada perlakuan uji ke-i, ulangan ke-j
µ = rataan umum
τi = pengaruh uji ke-i
εij = pengaruh galat percobaan
I = perlakuan
Peubah yang Diamati
Peubah yang diamati dalam penelitian berupa uji fisik
(kerapatan tumpukan, kerapatan pemadatan tumpukan, berat jenis),
uji kimia (kadar air, kadar abu, berat kering, protein kasar, serat kasar, lemak
kasar, gross energy, ADF dan NDF) uji biologi (energi metabolis).
Analisis Data
Data hasil pengukuran energi metabolis dan data sifat fisik dianalisis
ragam (Anova). Jika terdapat perbedaan yang nyata dilakukan uji lanjut Duncan
(Steel dan Torrie,1995). Analisis data dilakukan menurut prosedur SAS versi 9.1.3.
HASIL DAN PEMBAHASAN
Sifat Fisik Residu Bungkil Inti Sawit Hasil Perlakuan
Hasil uji sifat fisik residu bungkil inti sawit dari perlakuan penelitian yang
meliputi berat jenis, kerapatan tumpukan dan kerapatan pemadatan tumpukan
diperlihatkan pada Tabel 7.
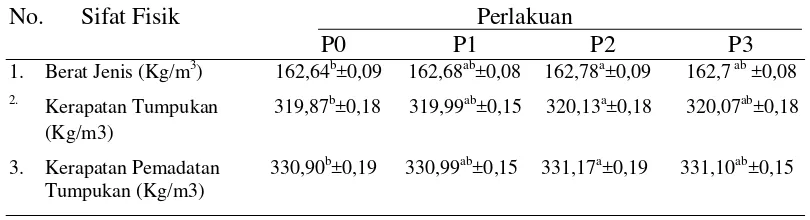
Tabel 7. Hasil uji kualitas sifat fisik residu BIS dari perlakuan penelitian
No. Sifat Fisik Perlakuan
Keterangan : P0 = BIS diekstrak dengan aquades P1 = BIS diekstrak dengan asam asetat
P2 = BIS diekstrak dengan aquades + enzim mannanase 100U/l P3 = BIS diekstrak dengan asam asetat + enzim mannanase 100U/l
Nilai rata-rata yang diikuti oleh superskrip yang berbeda dalam baris yang sama menunjukkan hasil yang berbeda nyata (P˂0,05).
Berdasarkan Tabel 7 di atas dapat diketahui bahwa karakteristik fisik dari
residu bungkil inti sawit hasil perlakuan adalah sebagai berikut :
Berat Jenis (BJ)
Berat jenis juga disebut berat spesifik (specific gravity),
merupakan perbandingan antara berat bahan terhadap volumenya,
satuannya adalah kg/m3. Berat jenis memegang peranan penting dalam berbagai proses pengolahan, penanganan dan penyimpanan. Berat jenis diukur dengan
menggunakan prinsip Hukum Archimedes, yaitu suatu benda di dalam fluida,
baik sebagian ataupun seluruhnya akan memperoleh gaya Archimedes sebesar
Hasil analisis ragam menunjukkan adanya pengaruh nyata perlakuan
ekstraksi bungkil inti sawit terhadap nilai berat jenis residu BIS hasil perlakuan
(P˂0,05) (Lampiran 11). Hasil uji lanjut menggunakan uji jarak berganda duncan
menunjukkan bahwa perlakuan P2 (bungkil inti sawit diekstrak dengan aquades
ditambah enzim mannanase 100U/l) mempunyai nilai berat jenis lebih tinggi atau
sama dengan perlakuan P3 (bungkil inti sawit diektraksi dengan asam asetat 1 %
ditambah enzim mannanase 100 u/l) dan perlakuan P1 (bungkil inti sawit
diekstrak dengan asam asetat 1 %) diantara perlakuan. Selanjutnya perlakuan P0
(bungkil inti sawit diekstrak dengan aquades) menunjukkan adanya pengaruh
yang nyata.
Nilai berat jenis yang berbeda dari residu BIS hasil perlakuan dikarenakan
adanya perbedaan kandungan nutrisi dan karakteristik permukaan partikel dari
residu BIS hasil perlakuan. Hal ini ditinjau dari berat rata-rata residu BIS hasil
perlakuan (Lampiran 4) dan hasil analisis proksimat dan uji Van Soest
(Lampiran 16) menunjukkan adanya perbedaan nilai rata-rata dari berat residu dan
nutrisi yang dikandung oleh masing-masing residu BIS hasil perlakuan.
Perhitungan korelasi berat jenis pada residu BIS hasil perlakuan dan
kandungan NDF (Lampiran 13) menunjukkan nilai R²= 0,928 (sangat
berhubungan). Dimana “y” sebagai berat jenis dan “x” sebagai kandungan NDF
dan persamaannya adalah y = - 0,0302x + 165,07. Hal ini menjelaskan bahwa
tinggi rendahnya nilai berat jenis residu BIS hasil perlakuan sangat berhubungan
dengan kandungan nutrisi yang dikandung oleh residu BIS hasil perlakuan.
Kandungan NDF mewakili komponen kimia residu BIS hasil perlakuan
kandungan NDF maka semakin tinggi nilai berat jenis residu BIS hasil perlakuan.
Hal ini sesuai dengan pendapat Khalil (1999) yang menyatakan bahwa adanya
variasi dalam nilai BJ dipengaruhi oleh kandungan nutrisi bahan, distribusi ukuran
partikel dan karakteristik permukaan partikel.
Sejalan dengan pendapat tersebut, Gautama (1998) menyatakan berat jenis
dipengaruhi oleh komposisi kimia pakan. Menurunnya nilai berat jenis disebabkan
ruang antar partikel bahan sudah terisi oleh aquades dalam pengukuran sehingga
nilai berat jenisnya rendah. Apabila partikel semakin kasar maka ukuran partikel
semakin besar dan kerapatan semakin menurun sehingga air lebih mudah mengisi
ruang antara partikel
Kerapatan Tumpukan
Kerapatan tumpukan adalah perbandingan antara berat bahan dengan
volume ruang yang ditempati dalam satuan kg/m3. Pengukuran kerapatan
tumpukan (bulk density) dilakukan untuk menentukan volume ruang pada suatu
bahan dengan berat jenis tertentu seperti dalam pengisian alat pencampur dan
elevator (Khalil, 1999).
Hasil analisis ragam menunjukkan adanya pengaruh nyata perlakuan
ekstraksi bungkil inti sawit terhadap nilai kerapatan tumpukan residu BIS hasil
perlakuan (P˂0,05) (Lampiran 9). Hasil uji lanjut menggunakan uji jarak berganda
duncan menunjukkan bahwa perlakuan P2 (bungkil inti sawit diekstrak dengan
aquades ditambah enzim mannanase 100U/l) mempunyai nilai kerapatan
tumpukan lebih tinggi atau sama dengan perlakuan P3 (bungkil inti sawit
diektraksi dengan asam asetat 1 % ditambah enzim mannanase 100 u/l) dan
perlakuan. Selanjutnya perlakuan P0 (bungkil inti sawit diekstrak dengan
aquades) menunjukkan adanya pengaruh yang nyata.
Perhitungan korelasi kerapatan tumpukan pada residu BIS hasil perlakuan
dan kandungan NDF (Lampiran 14) menunjukkan nilai R² = 0,9566
(sangat berhubungan). Dimana “y” sebagai kerapatan tumpukan dan “x” sebagai
kandungan NDF dan persamaannya adalah y = -0,0538x + 324,22. Hal ini
menjelaskan bahwa tinggi rendahnya nilai kerapatan tumpukan residu BIS hasil
perlakuan sangat berhubungan dengan kandungan nutrisi yang dikandung oleh
residu BIS hasil perlakuan. Kandungan NDF mewakili komponen kimia residu
BIS mempengaruhi besarnya nilai kerapatan tumpukan residu hasil perlakuan,
semakin rendah kandungan NDF maka semakin tinggi nilai kerapatan tumpukan
residu BIS hasil perlakuan.
Tingginya nilai kerapatan tumpukan yang dimiliki oleh perlakuan P2
(BIS diekstrak dengan aquades ditambah enzim mannanase 100U/l) disebabkan
tekstur residu BIS yang dihasilkan lebih halus dari pada perlakuan yang lainnya.
Hal ini akibat dari hasil proses ekstraksi dengan enzim mannanase yang
mendegradasi serat kasar bungkil inti sawit, sehingga kandungan serat kasar
semakin rendah dan tekstur substrat juga semakin halus. Nurcahaya (1999)
menyatakan bahwa semakin kecil ukuran partikel maka nilai kerapatan tumpukan
akan meningkat, karena terisinya rongga-rongga antar partikel.
Chang dan Lee (1985) berpendapat bahwa kerapatan tumpukan lebih
penting dari berat jenis bahan dalam hal pengeringan dan penyimpanan bahan
secara praktis. Kandungan nutrisi dan distribusi ukuran partikel diduga ikut
kadar lemak yang tinggi dan distribusi ukuran partikel kecil yang seragam
cenderung memiliki nilai kerapatan tumpukan yang rendah dan bahan tersebut
membutuhkan ruang yang lebih besar artinya bobot per satuan volume pada
keadaan curah lebih kecil.
Rataan kerapatan tumpukan hasil perlakuan dalam penelitian ini memiliki
nilai kisaran 319,867-320,133 kg/m3. Kolatac (1996) menyatakan bila suatu bahan
memiliki nilai kerapatan tumpukan kurang dari 450 kg/m3 membutuhkan lebih lama waktu untuk mengalir atau jatuh serta dapat ditimbang lebih teliti dengan
alat penakar otomatis, baik volumetrik maupun gravimetris.
Kerapatan Pemadatan Tumpukan
Kerapatan pemadatan tumpukan adalah perbandingan antara bahan
terhadap volume ruang yang ditempatinya setelah melalui proses pemadatan
(penggoyangan).
Hasil analisis ragam menunjukkan adanya pengaruh nyata perlakuan
ekstraksi bungkil inti sawit terhadap nilai kerapatan pemadatan tumpukan residu
BIS hasil perlakuan (P˂0,05) (Lampiran 10). Hasil uji lanjut menggunakan uji
jarak berganda duncan menunjukkan bahwa perlakuan P2 (bungkil inti sawit
diekstrak dengan aquades ditambah enzim mannanase 100U/l) mempunyai nilai
kerapatan pemadatan tumpukan lebih tinggi atau sama dengan perlakuan P3
(bungkil inti sawit diektraksi dengan asam asetat 1 % ditambah enzim mannanase
100 u/l) dan perlakuan P1 (bungkil inti sawit diekstrak dengan asam asetat 1 %)
diantara perlakuan. Selanjutnya perlakuan P0 (bungkil inti sawit diekstrak dengan
Perhitungan korelasi kerapatan pemadatan tumpukan pada residu BIS hasil
perlakuan dan kandungan NDF (Lampiran 15) menunjukkan nilai R² = 0,9603
(sangat berhubungan). Dimana “y” sebagai kerapatan pemadatan tumpukan dan
“x” sebagai kandungan NDF dan persamaannya adalah y = -0,0571x + 335,51.
Korelasi positif memiliki arti bahwa kandungan NDF mempengaruhi besarnya
nilai kerapatan pemadatan tumpukan dari residu BIS hasil perlakuan.
Nilai kerapatan pemadatan tumpukan yang semakin besar menunjukkan
bahwa kemampuan memadat substrat semakin tinggi. Sebaliknya, apabila nilai
kerapatan pemadatan tumpukan semakin kecil maka kemampuan memadat
substrat semakin rendah sehingga mengurangi efisiensi tempat penyimpanan.
Hal ini sesuai dengan pernyataan Rikmawati (2005) yang menyatakan bahwa
kerapatan pemadatan tumpukan yang tinggi berarti bahan memiliki kemampuan
memadat yang tinggi dibandingkan dengan bahan yang lain. Semakin rendah
kerapatan pemadatan tumpukan yang dihasilkan maka laju alir semakin menurun.
Sifat Kimia Residu Bungkil Inti Sawit Hasil Perlakuan
Bahan pakan adalah segala sesuatu yang dapat diberikan kepada ternak
baik berupa bahan organik maupun anorganik yang sebagian atau semuanya dapat
dicerna tanpa menggangu kesehatan ternak, sehingga bahan pakan yang diteliti
harus di analisis proksimat yaitu suatu metode analisis kimia untuk
mengidentifikasi kandungan nutrisi seperti protein, karbohidrat, lemak dan serat
pada bahan pakan. Hasil analisis kandungan nutrisi secara proksimat
dan Van Soest dari bahan penelitian residu bungkil inti sawit hasil ekstraksi asam
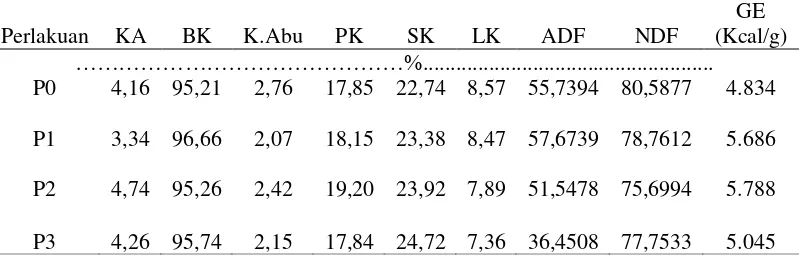
Tabel 8. Hasil analisis proksimat dan Van Soest residu dari proses ekstraksi bungkil inti sawit
Keterangan:P0=Ekstraksi menggunakan aquades; P1=Ekstraksi menggunakan asam asetat 1 %; P2=Ekstraksi menggunakan enzim mannanase 100U/l; P3=Ekstraksi menggunakan asam asetat 1% + enzim mannanase 100 U/l; KA=Kadar Air; BK=Bahan Kering;; K.Abu=Kadar Abu; PK=Protein Kasar; SK=Serat Kasar; LK=Lemak Kasar; ADF=Acid Detergent Fiber; NDF=Neutral Detergent Fiber; GE=Gross Energy.
Berdasarkan Tabel 8 dapat dilihat bahwa nilai kadar air residu bungkil inti
sawit hasil ekstraksi menunjukkan perbedaan diantara perlakuan, dimana nilai
kadar air tertinggi terdapat pada P2 yaitu 4,74% dan terendah pada perlakuan P1
yaitu 3,34 %. Hal ini dikarenakan adanya perbedaan bahan pengekstrak
dimasing-masing perlakuan. Perlakuan P2, BIS diekstrak dengan aquades
ditambah enzim mannanase sedangkan P1 dengan asam asetat 1%.
Residu yang dihasilkan dari proses ekstraksi dengan asam asetat memiliki
nilai kadar air yang lebih rendah dibanding residu yang diekstrak dengan aquades.
Hal ini sesuai dengan pendapat Endriadila (2014) yang menyatakan bahwa
perendaman partikel dalam asam asetat menyebabkan sebagian zat ekstraktif
terlarut serta mendegradasi polisakarida amorf (hemiselulosa) dan pati. Hal ini
menyebabkan sifat higroskopis partikel menurun karena hemiselulosa dan pati
merupakan polihidroksi. Penurunan sifat higroskopis menyebabkan kapasitas
pengikatan air rendah sehingga kadar air menurun.
Tabel di atas menunjukkan bahwa residu proses ekstraksi menunjukkan
kandungan protein kasar yang lebih tinggi dibandingkan dengan bungil inti sawit
tanpa perlakuan. Kandungan protein kasar BIS menunjukkan kadar 13,61%,
sedangkan residu BIS proses ekstraksi menunjukkan kadar 17,85% (P0),
18,15% (P1), 19,20 % (P2) dan 17,84 % (P3). Kandungan protein kasar tertinggi
berada pada perlakuan P2 (bungkil inti sawit diekstrak dengan aquades ditambah
enzim mannanase 100 U/l) dan terendah berada pada perlakuan P3 (bungkil inti
sawit diekstrak dengan asam asetat 1% ditambah enzim mannanase 100U/l).
Adanya peningkatan kandungan protein kasar pada residu BIS proses
ekstraksi dibanding BIS tanpa perlakuan menunjukkan bahwa proses ekstraksi
pada BIS mampu meningkatkan kandungan protein dan mengurangi faktor
pembatas dari BIS. Bungkil inti sawit memiliki struktur serat kasar sangat rumit
dan bersifat glikoprotein yaitu kemampuan mengikat protein di dalam serat.
Aritonang (1986) menyatakan bahwa struktur serat kasar pada bungkil inti sawit
sangat rumit sehingga mengikat protein di dalamnya dan struktur ini tahan
terhadap enzim pencernaan dan bakteri saluran pencernaan monogastrik.
Penggunaan autoclave pada proses ekstraksi mampu melarutkan
karbohidrat dan merenggangkan ikatan serat kasar. Sehingga, residu BIS proses
ekstraksi mengalami peningkatan kandungan protein kasar dari molekul protein
yang terbebaskan dari ikatannya dengan serat. Serta, peningkatan protein terkait
dengan penurunan komponen karbohidrat (gula) yang dimiliki oleh residu akibat
proses pemisahan (sentrifugasi) dalam proses ekstraksi.
Residu BIS proses ekstraksi menggunakan enzim mannanase 100 U/l (P2)
karena adanya penambahan enzim mannanase dalam proses ekstraksi BIS. Hal ini
sesuai dengan pendapat Jhonson (1990) berpendapat bahwa mannanase adalah
enzim pengurai mannan dan galaktomanan menjadi manosa dan galaktosa.
Enzim ini memotong secara acak rantai utama mannan dan hetero ß-D-mannan
menjadi gula terlarut yaitu manodekstrin dan manosa.
Dirujuk dari hasil reset “Biomaterial Baru Turunan BIS sebagai Imbuhan
Pakan untuk Ternak Unggas” (Tafsin et.al., 2017) (belum dipublikasikan)
menunjukkan bahwa penggunaan enzim B-mannanase menunjukkan komponen
mannose tertinggi dibandingkan perlakuan lainnya. Hasil paling rendah
ditunjukkan pada perlakuan menggunakan asam asetat 1%. Hasil tersebut
mengindikasikan bahwa komponen mannose yang terdeteksi sudah berupa
komponen yang relative sederhana (mendekati monosakarida).
Penggunaan autoclave, centrifuge dan aktifitas enzim mannanase
menghasilkan peningkatan molekul protein yang terbebaskan dari ikatan serat.
Sehingga residu BIS hasil perlakuan P2 memiliki kadar protein kasar yang tinggi
dalam penelitian ini.
Tinjauan terhadap kandungan serat kasar menunjukkan bahwa terjadi
penurunan yang relative kecil dari proses ekstraksi dibandingkan dengan BIS
tanpa perlakuan. Kandungan serat kasar pada BIS mencapai angka 24,47%,
sedangkan pada residu proses ekstraksi serkisar antara 22,74-24,72%.
Berdasarkan tabel di atas menunjukkan bahwa kandungan serat kasar tertinggi
berada pada perlakuan P3 (bungkil inti sait diekstrak dengan asam asetat 1%
ditambah enzim mannanase 100U/l) yaitu sebesar 24,72% dan yang terendah
sebesar 22,74%. Hasil tersebut mengindikasikan bahwa terjadi perombakan
komponen serat menjadi komponen yang lebih sederhana tetapi masih sulit
terlarut dengan proses ekstraksi dan menunjukkan penggunaan enzim mannanase
tidak efektif bila dikombinasikan dengan perlakuan asam asetat karena tidak
mampu menurunkan kadar serat kasar pada residu BIS.
Tinjauan lanjutan terhadap komponen serat dapat dilihat dari kandungan
ADF (Acid Detergent Fiber) dari analisis Van Soest. Kandungan ADF pada BIS
mencapai angka 50.74% sedangkan pada residu proses ekstraksi berkisar antara
36.45% – 57.67%. Kandungan ADF paling rendah ditunjukkan pada perlakuan
kombinasi asam asetat 1% dengan enzim b-mannannase yang menunjukkan nilai
sebesar 36.45%. Hasil tersebut menunjukkan bahwa penggunaan kombinasi
pelakuan asam asetat dengan enzim paling efektif dibandingkan perlakuan lainnya
dalam merombak komponen serat menjadi bahan yang terlarut dalam proses
ekstraksi.
Menurut Crampton dan Haris (1969) kenaikan nilai ADF lebih banyak
disebabkan komponen yang ada pada BIS yang tidak terdegradasi. Semakin tinggi
ADF, maka kualitaas daya cerna bahan pakan semakin rendah. Ditinjau dari nilai
kandungan ADF residu BIS hasil perlakuan maka perlakuan P3 memiliki
kandungan ADF terendah, tetapi kandungan protein kasar yang dimiliki P3
termasuk terendah dan kandungan serat kasar tertinggi diantara perlakuan.
Hasil tersebut diduga nilai nutrisi yang dimiliki P3 sudah terlarut pada proses
ekstraksi dengan kombinasi asam asetat dan enzim mannanase 100 u/l dan
kandungan ADF yang dimiliki oleh perlakuan P3 diduga komponen serat yang
Kandungan NDF tertinggi diperoleh pada perlakuan P0 yakni 80,59% dan
terendah pada perlakuan P2 yaitu 75,70%. Menurut Daud (1995) kandungan NDF
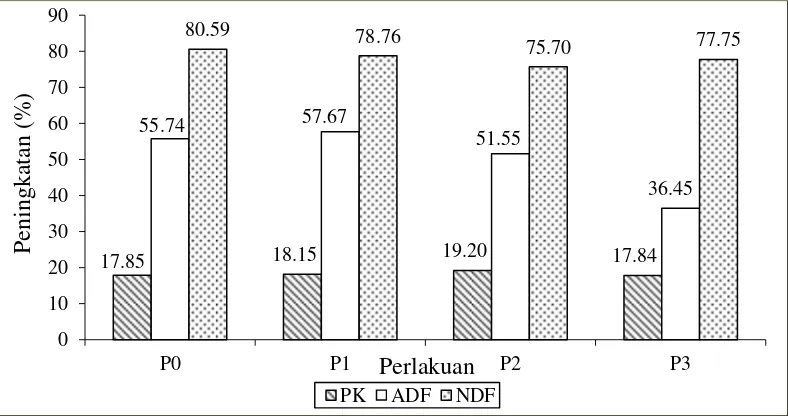
di atas 52% mengindikasikan bahwa tinggi akan komponen dinding sel. mannanase 100U/l. PK (Protein Kasar), ADF ((AcidDetergent Fiber), NDF (Neutral Detergent Fiber)
Gambar 2. Grafik nilai PK,ADF,NDF mewakili nilai uji kimia residu BIS hasil perlakuan
Kandungan lemak kasar residu BIS hasil penelitian berkisar 7,36-8,57%,
dengan lemak kasar tertinggi dihasilkan oleh perlakuan P0 (bungkil inti sawit
diekstrak dengan aquades) yaitu sebesar 8,57% dan nilai terendah berada pada
perlakuan P3 (bungkil inti sawit diekstrak dengan asam asetat ditambah enzim
mannanase) yaitu sebesar 7,36%. Hasil tersebut menunjukkan bahwa penggunaan
bahan pengekstrak yang berbeda akan menghasilkan nilai kandungan lemak kasar
yang berbeda pula. Menurut Bahri dan Rusdi (2008) menyatakan bahwa
kandungan lemak yang tinggi mempunyai kontribusi yang besar terhadap nilai
gross energy (GE) atau energi kasar suatu bahan. Hal ini berbeda dengan hasil
nilai GE pada residu BIS hasil perlakuan dalam penelitian ini.
Nilai gross energy tertinggi berada pada perlakuan P2 (bungkil inti sawit
diekstrak dengan aquades ditambah enzim mannanase) yaitu sebesar
5.788 kkal/kg dan nilai terendah berada pada perlakuan P0 (bungkil inti sawit
diekstrak dengan aquades) sebesar 4.834 kkal/kg. Hasil tersebut menunjukkan
bahwa kandungan lemak yang dikandung oleh perlakuan P0 bukan lemak murni,
sehingga tidak memberikan kontribusi pada nilai GE residu BIS perlakuan P0.
Anggorodi (1994) berpendapat bahwa lemak yang didapatkan dari analisis lemak
ini bukan lemak murni. Selain mengandung lemak sesungguhnya, ekstrak eter
juga mengandung waks (lilin), asam organik, alkohol, dan pigmen, oleh karena itu
fraksi eter untuk menentukan lemak tidak sepenuhnya benar.
Sifat Biologi (Energi Metabolis)
Energi merupakan nutrisi yang dijadikan sebagai pembatas dalam
penyusunan ransum ternak, merupakan faktor tunggal paling penting yang
dibutuhkan dalam ransum unggas guna menentukan nilai makanannya
(Tillman et al., 1998). Energi merupakan komponen yang dibutuhkan ternak
untuk proses metabolisme dalam tubuh (Parakkasi, 1990). Kebutuhan energi,
menurut Wahju (1978) dapat diartikan dengan jumlah energi yang tersedia dan
dapat memenuhi kebutuhan energi untuk pertumbuhan dan produksi.
Energi dipergunakan untuk pertumbuhan jaringan, produksi, aktivitas fisik,
protein, dan lemak (Scott et al.,1982). Energi metabolis adalah perbedaan
kandungan energi bruto ransum dengan energi bruto yang dikeluarkan melalui
ekskreta (Sibbald, 1980). Semakin sedikit energi yang dikeluarkan maka semakin
tinggi energi ransum yang diserap atau dicerna oleh tubuh, sehingga efisiensi
penggunaan energi ransum tinggi. Pengaruh perlakuan terhadap residu bungkil
inti sawit terhadap nilai energi metabolis dapat dilihat pada Tabel 9.
Tabel 9. Nilai energi metabolis residu bungkil inti sawit hasil perlakuan
Perlakuan Nilai energi metabolis (kkal/kg)
P0 2667,8b±56,331
P1 2897,1a±54,479 P2 2907,0a±46,965 P3 2689,9b±55,149
Keterangan: Superskrip yang berbeda pada kolom yang sama menunjukkan perbedaan yang sangat nyata (P<0,01).
Hasil analisis ragam menunjukkan adanya pengaruh yang sangat nyata dari
perlakuan ekstraksi bungkil inti sawit terhadap nilai energi metabolis residu BIS
hasil perlakuan (P˂0,01) (Lampiran 12). Hasil uji lanjut menggunakan uji jarak
berganda duncan menunjukkan bahwa perlakuan P2 (bungkil inti sawit diekstrak
dengan aquades ditambah enzim mannanase 100U/l) dan perlakuan P1
(bungkil inti sawit diekstrak dengan asam asetat 1 %) mempunyai nilai energi
metabolis lebih tinggi diantara perlakuan. Selanjutnya perlakuan P3 (bungkil inti
sawit diekstrak dengan asam asetat 1 % ditambah enzim mannanase 100 u/l) dan
perlakuan P0 (bungkil inti sawit diekstrak dengan aquades) menunjukkan adanya
pengaruh yang nyata. Nilai energi metabolisme yang berbeda dari residu BIS hasil
perlakuan dikarenakan adanya perbedaan kandungan nutrisi dan karakteristik fisik
Perbedaan nilai energi metabolis pada residu BIS proses ekstraksi
dipengaruhi oleh beberapa faktor, yang pertama adalah kandungan energi bahan
penyusun dalam residu BIS proses ekstraksi itu sendiri. Menurut Batal dan Dale
(2006) menyatakan bahwa energi bahan dipengaruhi oleh ketersediaan
karbohidrat, protein, lemak serta vitamin B komplek. Kerusakan pada komponen
nutrien tersebut akan menurunkan kandungan energi bahan tersebut. Hal ini sesuai
dengan lampiran 16 hasil analisis proksimat dan uji Van Soest residu BIS hasil
perlakuan. Berdasarkan lampiran tersebut kandungan nutrisi residu BIS hasil
perlakuan P2 (bungkil inti sawit diekstrak dengan aquades ditambah enzim
mannanase 100 u/l) memiliki kandungan nutrisi dan nilai energi yang terbaik
diantara perlakuan.
Faktor yang kedua yang mempengaruhi nilai energi metabolis pada ternak
unggas adalah kemampuan ternak untuk memetabolis ransum di dalam tubuhnya.
Faktor ini dipengaruhi oleh sifat fisik pakan, pH, enzim-enzim saluran
pencernaan, komposisi zat makanan, suhu lingkungan, dan fisiologis ternak
(Sibbald, 1989). Berdasarkan hasil uji sifat fisik (Tabel 7) dan analisis proksimat
dan uji Van Soest residu BIS hasil perlakuan (lampiran 16) yang terbaik dimiliki
oleh perlakuan P2 (bungkil inti sawit diekstrak dengan aquades ditambah enzim
mannanase 100 u/l)
Proses ekstraksi pada BIS dengan enzim sangat nyata meningkatkan nilai
energi metabolis residu BIS hasil perlakuan pada ayam broiler. Hal ini diduga
karena kandungan zat makanan dalam residu BIS hasil perlakuan mempunyai
daya cerna yang tinggi, karena banyak komponen yang mudah dicerna akibat dari
perubahan nutrisi yaitu meningkatnya kandungan protein kasar. Semakin tinggi
kandungan protein kasar bahan pakan, maka semakin tinggi energi metabolis.
Hal ini sesuai menurut Prabowo et al. (2002), perbedaan energi metabolis
disebabkan oleh perbedaan kandungan protein kasar dan serat kasar antar
perlakuan. Semakin tinggi protein kasar atau semakin rendah serat kasar,
maka semakin tinggi energi metabolis. Sebaliknya semakin rendah protein kasar
atau semakin tinggi serat kasar, maka semakin rendah energi metabolis.
Selain pengaruh dari tingginya kandungan serat kasar, tingginya
kandungan polisakarida mannan pada BIS diduga memiliki efek negatif pada
kecernaan pakan. Choct (2002) menjelaskan bahwa polisakarida mannan termasuk
dalam komponen bukan pati (NSP; non-starch polysaccharide). Kandungan NSP
yang tinggi dalam suatu bahan baku pakan akan bersifat antinutritif, dan
mempengaruhi penampilan ternak karena adanya gangguan pencernaan dan
absorpsi nutrisi. Sejalan dengan hal tersebut Leeson dan Summers (2001)
menyatakan bahwa pengaruh negatif dari NSP yaitu menurunkan energi tersedia
pada unggas, sehingga energi yang dapat dimetabolis menjadi lebih rendah.
Selanjutnya Lee et al. (2003) melaporkan bahwa penggunaan enzim mannanase
efektif untuk mengatasi hal tersebut.
Semakin rendah nilai faktor pembatas pada perlakuan P2 (BIS diekstrak
dengan aquades ditambah enzim mannanase 100 u/l) serta nilai sifat fisik yang
tinggi yang dimiliki oleh perlakuan P2 mendapat respon biologis positif pada
ternak karena diduga ayam mampu mencerna dan memanfaatkan komponen
nutrisi residu BIS hasil perlakuan P2 dengan baik, sehingga energi yang
KESIMPULAN DAN SARAN
Kesimpulan
1. Residu hasil ekstraksi menghasilkan nilai sifat fisik yang berbeda nyata. BIS
yang diekstrak dengan aquades ditambah enzim mannanase 100 u/l
menghasilkan nilai berat jenis, kerapatan tumpukan dan kerapatan pemadatan
tumpukan yang lebih besar dari antara perlakuan.
2. Residu bungkil inti sawit yang diekstrak dengan aquades ditambah enzim
mannanase 100 u/l mampu meningkatkan nilai protein kasar dan menurunkan
nilai NDF.
3. Residu proses ekstraksi bungkil inti sawit menghasilkan nilai energi metabolis
yang berbeda. BIS yang diekstrak dengan aquades ditambah enzim mannanase
atau yang diekstrak dengan asam asetat lebih besar nilai energi metabolisnya
dibanding dengan BIS yang diestrak dengan aquades atau yang diekstrak
kombinasi asam asetat ditambah enzim mannanase.
Saran
Residu bungkil inti sawit hasil ekstraksi aquades ditambah enzim
mannanase 100U/l dapat dijadikan sumber bahan pakan ternak unggas.
Penelitian lanjutan masih diperlukan agar diperoleh proses ekstraksi yang lebih