TINJAUAN PUSTAKA Tanah Sulfat Masam
Bahan sulfat masam terdiri atas tanah salin atau sedimen yang terdapat
besi sulfida (FeS2
Pirit (FeS
) di atas layer tanah dalam keadaan tergenang atau kondisi
anaerob. Akan tetapi, pirit menjadi teroksidasi menjadi asam sulfat. Asam sulfat
dihasilkan dari oksidasi pirit yang menyebabkan pH tanah berada pada tingkat
yang sangat bahaya, pada waktu derajat keasaman 3.0. Tanah menjadi racun,
termasuk meningkatkan aluminium, besi dan (dalam beberapa masalah) mangan
yang terlarut, dan kualitas unsur hara menjadi tidak tersedia (Bloomfield, 1972).
2
Jika tanah ini direklamasi, maka senyawa pirit akan terpapar udara
membentuk ferri hidroksida (Fe(OH)
) pada kondisi anaerob atau tergenang adalah senyawa yang
stabil dan tidak berbahaya, akan tetapi menjadi berbahaya jika kondisi tanah
berubah menjadi aerob. Senyawa pirit dalam kondisi aerob akan teroksidasi dan
menghasilkan senyawa beracun serta meningkatkan kemasaman tanah, yang
berbahaya bagi pertumbuhan tanaman. Ada dua keadaan yang menyebabkan pirit
berada dalam kondisi aerob yaitu apabila tanah pirit diangkat ke permukaan tanah
(misalnya pada waktu mengolah tanah, membuat saluran, atau membuat surjan)
dan jika permukaan air tanah turun (misalnya pada musim kemarau). Dent (1986)
dan Langenhoff (1986) melaporkan bahwa hasil oksidasi pirit, antara lain asam
sulfat dan hidroksida besi yang menyebabkan reaksi tanah sangat masam.
Senyawa yang terbentuk secara alamiah dapat mengalami reaksi penetralan
dengan terbentuknya senyawa jarosit yang berupa bercak-bercak karatan berwarna
kuning jerami.
sehingga tanah menjadi sangat masam (Wijaya-Adhi et al., 1992). Reaksi oksidasi
Produksi ferri sulfat dari ferro sulfat sangat besar karena proses pembentukannya
dipercepat oleh aktivitas bakteri Thiobacillus ferrooxidans (No. 2) dan pada
kondisi yang masam reaksi pirit dengan ferri sulfat (No. 3) berlangsung sangat
cepat. Ferri sulfat juga dapat terhidrolisis sehingga menambah kemasaman seperti
diperlihatkan reaksi berikut:
4
Fe2(SO4)3 + 6 H2O → 2 Fe(OH)3 + 3 H2SO
Hasil reaksi adalah dihasilkannya Fe
4
3+
koloidal dan asam sulfat yang terlarut
menjadi ion sulfat dan melimpahnya ion H+ yang mengakibatkan pH tanah turun
drastis dari awalnya netral-agak alkalis (pH 5,5-6,5) menjadi masam ekstrim (pH
1,3 sampai <3,5). Pada kondisi ini terjadi keracunan ion H+, Al3+, SO42- dan Fe2+
Dalam keadaan teroksidasi, pirit yang berubah menjadi sulfida besi
tersebut diikuti dengan peningkatan kemasaman tanah yang tajam yang akan
menghambat pertumbuhan tanaman dan menjadi racun bagi tanaman melalui
beberapa mekanisme antara lain: 1. Kerusakan sel tanaman akibat peningkatan ion
H
,
serta penurunan kesuburan tanah alami akibat hilangnya basa-basa tanah,
sehingga tanah mengalami kahat P, K, Ca dan Mg (Subagyo, 2006).
+
, 2. Peningkatan kelarutan Fe, Al, dan Mn yang bersifat toksik bagi tanaman, 3.
Terhambatnya pertumbuhan akar, serapan air dan abnormalitas faktor biotik
(Leiwakabessy, 1980).
Tanah sulfat masam telah diketahui sebagai tanah yang sulit untuk
mengelola hasil produksi pertanian karena tingkat kesuburannya yang sangat
rendah (Shamshuddin et al., 2014). Pengembagan pertanian di tanah sulfat masam
sering menghadapai beberapa permasalahan seperti rendahnya pH tanah dan fosfat
tersedia serta tingginya kandungan Fe (Purnomo et al., 2005). Pada keadaan ini,
manajemen yang sesuai sangat berguna untuk menahan potensi yang
membahayakan dari tanah sulfat masam dan dianggap bisa digunakan untuk
tujuan pertanian (Khan, 1994).
Alternatif pengelolaan yang dapat dilakukan adalah aplikasi bahan
pembenah tanah yang mempunyai efek pengapuran (liming effect), pencucian
sulfat masam (Noorsyamsi dan Sarwani, 1989), dan aplikasi pupuk yang sesuai
kaidah 4 T (Tepat Jenis, Dosis, Waktu, dan Metode). Khan et al. (2006)
melaporkan bahwa terak dasar telah digunakan di lahan pertanian sejak tahun
1985 dan tidak menciptakan efek berbahaya pada tanaman. Mereka menyarankan
bahwa terak dasar dapat diterapkan untuk mereklamasi kembali tanah sulfat
masam. Sebuah reklamasi dan praktek manajemen yang tepat dari tanah sulfat
masam diperlukan untuk mengurangi pencucian basa dari larutan tanah serta
untuk mengurangi defisiensi unsur hara (Jintaridth, 2006). Menurut Cook et al.
(2006) peningkatkan keasaman pada tanah sulfat masam dapat mengurangi basa
dan dapat membahayakan bagi lingkungan akuatik dan terestrial. Namun,
sebagian besar studi yang bertujuan untuk mereklamasi tanah sulfat masam
Kapur Dolomit
Ada banyak teknik tradisional dan modern yang dapat memperbaiki sifat
kimia tanah dari tanah sulfat asam. Salah satunya adalah aplikasi bahan kapur.
Kapur lebih sering sesuai untuk memperbaiki tanah masam karena kelarutannya
tinggi dalam jumlah sekitar 6,25-12,5 ton/ha. Penggunaan bahan kapur
bersama-sama dengan pupuk kimia, terutama nitrogen dan fosfor, dapat meningkatkan
produktivitas padi. Selain itu, aplikasi silikon (Si) dapat mengurangi toksisitas
aluminium untuk tanaman termasuk padi (Hara et al., 1999). Silikon
meningkatkan fotosintesis tanaman padi dan meningkatkan ketahanan tanaman
padi terhadap beberapa penyakit dan serangga yang merugikan tanaman padi
Bahan pembenah tanah bisa berupa dolomit yang merupakan salah satu
jenis kapur pertanian yang dapat meningkatkan pH, juga menambahkan
kandungan Ca dan Mg untuk menunjang pertumbuhan dan perkembangan
tanaman. Untuk meningkatkan pH pasang surut dari 4,5 menjadi 5,3 diperlukan
kapur sebanyak 2 ton/ha (Badan Litbang Pertanian, 2009). (Ma and Takahashi, 2002).
Selain itu dolomit banyak digunakan karena relatif murah dan mudah
didapat. Disamping itu bahan tersebut dapat memperbaiki sifat fisik tanah dan
kimia dengan tidak meninggalkan residu yang merugikan tanah. Apabila pH tanah
telah meningkat, maka kation Aluminium akan mengendap sebagai gibsit
sehingga tidak lagi merugikan tanaman (Safuan, 2002).
Para pakar yang telah banyak meneliti di daerah tropik menyatakan bahwa
untuk mendapatkan efisiensi pengapuran di daerah tropik basah dimana jumlah
diatas 6, tetapi cukup meniadakan atau menekan Al yang meracuni tanaman.
Prinsip pengapuran yang didasarkan pada Al-dd ternyata sangat efektif dalam
menunjang pertumbuhan tanaman. Prinsip ini terus berkembang hingga kemudian
ditentukan kebutuhan kapur berdasarkan kejenuhan Al
(Ragland and Coleman, 1959).
Secara umum pemberian kapur antara 0,5 ton sampai dengan 3,0 ton per
hektar sudah cukup memadai (Alihamsyah, 2003). Sedangkan beberapa peneliti
seperti Subiksa et al. (1990) dan Noor et al. (2010), menyatakan bahwa
pemberian bahan amelioran seperti pupuk organik, tanah mineral, zeolit, dolomit,
fosfat alam, pupuk kandang, kapur pertanian, abu sekam,
purun tikus (Eleocharis dulcis) dapat meningkatkan pH tanah dan basa-basa
tanah.
Pupuk dan Pemupukan
Pupuk merupakan suatu bahan yang diberikan pada tanaman baik secara
langsung maupun tidak langsung untuk mendorong pertumbuhan tanaman,
meningkatkan produksi atau memperbaiki kualitasnya sebagai akibat perbaikan
nutrisi tanaman (Leiwakabessy dan Sutandi, 2004). Pupuk dapat digolongkan
kedalam senyawa organik maupun anorganik yang dapat terdiri dari satu atau
lebih unsur hara.
Pemupukan telah menjadi komponen dari peningkatan teknik-teknik
budaya untuk sebagian besar tanaman sejak lebih dari 95 persen dari lahan yang
paling subur dari Nigeria barat selatan yang sering dibudidayakan. Kendala dan
ketersediaan nutrisi yang menyebabkan lahan berada di posisi bawah tingkat
potensial (Adepetu, 1986).
Cara terbaik untuk mencegah tanah menjadi miskin adalah dengan
mengembalikan yang tanaman telah ambil dan ini hanya dapat dicapai dengan
penggunaan pupuk anorganik (Roberts and Andrew, 1989). Dalam program
manajemen kesuburan tanah yang baik, waktu yang tepat dan pemupukan yang
baik diperlukan untuk mempertahankan tingkat produksi tanaman yang tinggi
(Harper, 1983).
Cooke (1972) melaporkan bahwa nutrisi utama yang dibutuhkan oleh
tanaman yang Nitrogen (N), Fosfor (P) dan Kalium (K). Pasokan yang tidak
memadai dari setiap nutrisi selama pertumbuhan tanaman diketahui memiliki
dampak negatif pada kemampuan reproduksi, pertumbuhan dan hasil tanaman
(Vine, 1953; Solubo, 1972) dan jumlah tambahan nutrisi dapat ditambahkan ke
tanah dalam bentuk pupuk anorganik untuk memperbaiki kekurangan pasokan
nutrisi ke tanaman (Dirk and Hargarty, 1984)
Bakteri Pereduksi Sulfat
.
Bakteri Pereduksi Sulfat (BPS) atau Sulphate Reduction Bacteria
merupakan salah satu mikrobia penting. Bakteri ini ditemukan hampir di semua
lingkungan di bumi: tanah, air tawar, air laut dan air payau, sumber air panas,
daerah geothermal; sumur minyak dan gas, cadangan sulfur, endapan lumpur,
selokan, besi berkarat, rumina kambing dan usus serangga (Postgate,1984).
Hidupnya obligat anaerob, namun dapat bertahan dalam waktu yang cukup lama
umumnya lebih suka berada dalam lingkungan yang agak basa (Jalaludin, 2005),
mereka dapat pula berkembang dalam lingkungan dengan rentang pH 5,5-8,5.
Kebanyakan tipe asimilasi bakteri pereduksi sulfat yang telah diisolasi dari
alam dan dijelaskan bahwa sejauh ini merupakan bakteri mesofilik, anaerob dan
tidak mampu membentuk spora. Kelompok yang termasuk bakteri ini merupakan
bakteri dari subdivisi delta dari genus proteobakteria. Data terbaru dari kategori
ini adalah Desulfovibrio. Berbagai jenis sel telah dijelaskan termasuk bentuk bulat
(coccus); oval atau batang lurus panjang; batang melengkung atau spiral; sel-sel
dengan vesikular gas; bergerak meluncur serta memiliki filamen multiseluler. Di
alam dikenal beragam bakteri yang memanfaatkan senyawa anorganik sebagai
elektron donor atau elektron akseptor dalam aktivitas metabolismenya, salah
satunya adalah bakteri pereduksi sulfat. Bakteri pereduksi sulfat memanfaatkan
ion sulfur dalam bentuk sulfat (SO42-), tiosulfat (S2O32-) dan sulfit (SO3
2-Dalam melakukan reduksi sulfat, BPS menggunakan sulfat sebagai sumber
energi yaitu sebagai akseptor elektron dan menggunakan bahan organik sebagai
sumber karbon (C). Karbon tersebut berperan sebagai donor elektron dalam
metabolisme juga merupakan bahan penyusun selnya (Groudev et al., 2001).
Sedangkan menurut Djurle (2004) menjelaskan bahwa BPS menggunakan donor
elekron H
) sebagai
akseptor elektron terminal dalam respirasi metabolismenya, yang kemudian
direduksi menjadi sulfida. Spesies bakteri pereduksi sulfat yang paling banyak
ditemukan adalah dalam sedimen laut karena kandungan sulfat cukup tinggi
(Widdel and Bak, 1992).
Reduksi sulfat dapat terjadi dalam kisaran nilai pH, tekanan, suhu dan kondisi
salinitas yang luas.
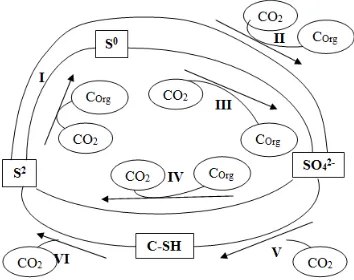
Gambar 1. Skema Beberapa Jalur Berbeda yang Terlibat dalam Siklus Sulfur Mikrobial (Sumber: Lens et.al., 2004)
Siklus sulfur merupakan salah satu proses biogeokimia utama di alam.
Terdapat empat jenis stok senyawa sulfur alamiah utama berdasarkan tingkat
oksidasinya dalam siklus sulfur, yaitu senyawa sulfida (S2-), sulfur elemental (S0),
sulfat (SO42-) dan sulfur-organik (C-SH) (Lens et.al., 2004). Gambar di atas
menunjukan jalur-jalur reaksi yang terlibat dalam siklus sulfur mikrobial. Perilaku
senyawa-senyawa sulfur di perairan dipengaruhi oleh sejumlah organisme
terutama mikroba. Jalur I, II, III, dan V melibatkan mikroba autotrof yang
menggunakan CO2 anorganik sebagai sumber karbon. Sedangkan jalur IV dan VI
melibatkan mikroba heterotrof yang menggunakan senyawa organik sebagai
Reaksi oksidasi senyawa sulfur terjadi pada jalur I, II, dan III, sedangkan
reaksi reduksi terjadi pada jalur IV dan VI. Oksidasi senyawa sulfur melibatkan
mikroorganisme kemoautotrof atau fotoautotrof, seperti bakteri dari genus
Thiobacillus dan bakteri-sulfur fotosintetik (Chlorobiaceae dan Chromatiaceae).
Dari semua kelompok bakteri pengoksidasi sulfat, hanya kelompok bakteri
thiobacillus yang mampu menghasilkan sulfat secara langsung tanpa
mengakumulasi sulfur dalam proses oksidasi H2S pada tekanan oksigen normal.
Kelompok bakteri lainnya mengakumulasi sulfur. Sulfur yang terakumulasi
tersebut akan dioksidasi lebih lanjut menjadi sulfat ketika suplai H2S menurun
atau hilang (Ehrlich and Newman, 2009).
Habitat pertumbuhan bakteri pereduksi sulfat cukup luas. Selain di lautan,
bakteri ini juga ditemukan di lahan sawah dan perairan darat. Mengingat bakteri
ini merupakan bakteri anaerob obligat, bakteri pereduksi sulfat lebih banyak
ditemukan pada lingkungan anoksik, terutama di bagian bawah sedimen.
Jorgensen (1982) melaporkan bahwa jumlah dan aktivitas bakteri pereduksi sulfat
meningkat dengan ketebalan lapisan sedimen. Namun demikian, ada kelompok
bakteri pereduksi sulfat yang mampu tumbuh pada kondisi oksik. Hal ini yang
menyebabkan ada keragaman bakteri yang tumbuh dalam sedimen. Risatti et al.
(1994) mengemukakan bahwa kelompok Desulfovibrio sp. lebih dominan di
bagian atas sedimen, sedangkan Desulfotomaculum sp. Banyak ditemukan pada
bagian bawah sedimen.
Di alam BPS sering berasosiasi dengan BPB (iron reduction bacteria)
dalam melaksanakan bioremediasi lingkungan. Keduanya dapat dijumpai di
sebagai akseptor elektron, bakteri pereduksi besi menggunakan besi (III) sebagai
akseptor elektron terminal (Luef et al., 2013).
Kemampuan isolat bakteri pereduksi sulfat juga beragam, namun efisiensi
reduksi sulfat semua isolat meningkat dengan peningkatkan nilai pH. Pada pH 6
efisiensi reduksi sulfat berkisar antara 74,75% sampai 91,79%. Kemampuan
terendah diperoleh isolat ICBB 8820, sedangkan isolat ICBB 8818 mempunyai
kemampuan mereduksi sulfat paling tinggi, yakni sebesar 91,79%. Penurunan pH
menurunkan kemampuan bakteri mereduksi sulfat. Pada pH 6, isolat ICBB 8820
mampu mereduksi sebesar 74,75%, berkurang menjadi 72,77% pada pH 4, dan
tidak mampu tumbuh pada pH 3. Sedangkan kemampuan reduksi isolat ICBB
8818 mencapai 91,79% pada pH 6, tetapi hanya sebesar 84,28% pada pH 3. Pada
pH 3 total sulfat yang tereduksi oleh 8 isolat yang mampu tumbuh berkisar antara