BAB II
TINJAUAN PUSTAKA 2.1 Air Minum
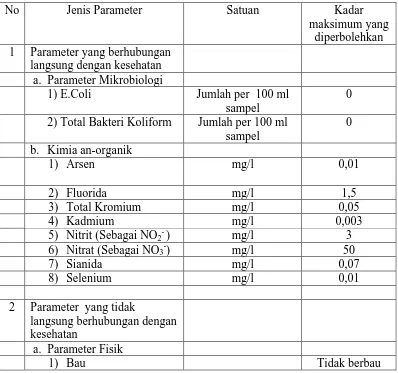
Air minum adalah air yang melalui proses pengolahan atau tanpa proses pengolahan yang memenuhi syarat kesehatan dan dapat langsung di minum (Kepmenkes, RI., 2002). Air minum yang baik dan aman untuk kesehatan jika memenuhi persyaratan fisika, mikrobiologis dan kimiawi sesuai dengan parameter yang ditentukan oleh Permenkes RI No.492/Menkes/Per/IV/2010 yang dapat di lihat pada Tabel 2.1
Tabel 2.1 Baku Mutu Air Minum Menurut Permenkes RI No.492/Menkes/Per/IV/2010
No Jenis Parameter Satuan Kadar
maksimum yang diperbolehkan 1 Parameter yang berhubungan
langsung dengan kesehatan a. Parameter Mikrobiologi
1) E.Coli Jumlah per 100 ml sampel
0 2) Total Bakteri Koliform Jumlah per 100 ml
sampel
0 b. Kimia an-organik
1) Arsen mg/l 0,01
a. Parameter Fisik
2) Warna TCU 15
b. Parameter Kimiawi
1) Aluminium mg/l 0,2
Dari Tabel 2.1 di atas diuraikan tentang kesadahan dalam air minum yang dikaitkan dengan adanya kalsium karbonat dan magnesium karbonat. Jika kesadahan dalam air minum rendah maka akan meningkatkan resiko terkena penyakit jantung (De Zuane, 1996).
2.2 Manfaat Mineral Dalam Air Minum
memenuhi syarat atau di proses melalui perusahaan air minum supaya memenuhi syarat (Kozisek, 2005; Fox, 1998; Silalahi, 2014).
Air minum menjadi salah satu sumber beberapa mineral karena terdapat secara alamiah atau ditambahkan. Ada beberapa mineral yang terdapat di dalam air minum dengan kadar potensial untuk menopang kesehatan yakni kalsium, magnesium, florida, selenium, kuprum, dan kalium. Kontribusi air minum sebagai sumber mineral yang diperlukan dibandingkan dengan kontribusi makanan lainnya berkisar 1-20 %. Mineral kalsium dan magnesium merupakan yang paling banyak yakni sampai 20% dari yang diperlukan tubuh berasal dari air minum. Tingkat penyerapan kalsium dari air minum yang mengandung kalsium yang tinggi sebanding dengan penyerapan kalsium dari susu. Air minum yang mengandung 300 mg kalsium per liter menyumbangkan kalsium yang setara dengan kalsium dari satu gelas susu (WHO, 2005; Olivares dan Uauy, 2005; Silalahi, 2014).
2.2.1 Kalsium
Kalsium merupakan mineral yang paling banyak terdapat di dalam tubuh yaitu 1,5 % - 2 % dari berat badan orang dewasa atau kurang lebih sebanyak 1 kg. Dari jumlah ini, 99% berada dalam jaringan keras yaitu tulang dan gigi. Di dalam cairan ekstraselular dan intraselular kalsium memegang peranan penting dalam mengatur fungsi sel seperti transmisi saraf, kontraksi otot, penggumpalan darah dan menjaga permeabilitas membran sel. Kalsium mengatur pekerjaan hormon-hormon dan faktor pertumbuhan (Almatsier, 2004).
menurun pada proses menua. Kemampuan absorpsi pada laki-laki lebih tinggi daripada perempuan pada semua golongan usia. Hal ini dikarenakan penyerapan mineral dari air minum dipengaruhi oleh kondisi fisiologis pencernaan dan komposisi makanan. Kalsium membutuhkan pH 6 agar dapat berada dalam keadaan terlarut (Almatsier, 2004; Kozisek, 2005).
2.2.2 Magnesium
Magnesium adalah kation nomor dua paling banyak setelah natrium di dalam cairan intraselular. Kurang lebih 60% dari 20-28 mg di dalam tubuh terdapat di dalam tulang dan gigi, 26% di dalam otot dan selebihnya di dalam jaringan lunak lainnya serta cairan tubuh. Magnesium memegang peranan penting dalam lebih dari tiga ratus jenis sistem enzim di dalam tubuh. Magnesium bertindak di dalam semua sel jaringan lunak sebagai katalisator dalam reaksi biologi termasuk reaksi yang berkaitan dengan metabolisme energi, karbohidrat, lipida, protein, dan asam nukleat serta dalam sintesis, degradasi, dan stabilitas bahan gen DNA. Sebagian besar reaksi ini terjadi dalam mitokondria sel (Almatsier, 2004).
2.3 Kesadahan
Kesadahan air berbeda di setiap tempat dan menggambarkan sifat lapisan tanah yang kontak dengan air. Secara umum, air permukaan lebih lunak dibandingkan dengan air tanah. Kesadahan disebabkan oleh logam atau kation bervalensi dua. Kalsium dan magnesium adalah ion mayor penyebab kesadahan, diikuti oleh besi, aluminium, mangan, stronsium dan zink sebagai komponen minor (Gray, 2008; De Zuane, 1996).
Tingkat kesadahan air digolongkan sebagai berikut : - lunak (soft) = 0 – 50 mg/l - sedikit keras (moderately hard) = 50 – 150 mg/l - keras (hard) = 150 – 300 mg/l
- sangat keras (very hard) = >300 mg/l (Gray, 2008; De Zuane, 1996). Kesadahan air dibedakan menjadi dua macam yaitu kesadahan sementara (temporary hardness) dan kesadahan permanen (permanent hardness). Kesadahan
Menurut Chandra (2006), metode yang dapat digunakan untuk menghilangkan kesadahan air antara lain :
1. Pemanasan
Pemanasan menyebabkan dikeluarkannya CO2 dari dalam air dan terbentuknya
endapan CaCO3
Ca(HCO3)2 + Panas CaCO3 + H2O + CO2
2. Penambahan Kapur
Penambahan kapur pada air yang sifat kesadahannya sementara dapat mengabsorbsi CO2 dan membentuk endapan CaCO3.
Ca(OH)2 + Ca(HCO3) 2CaCO3 + 2H2O
3. Penambahan natrium karbonat dapat menghilangkan kesadahan sementara dan permanen.
Na2CO3 + Ca(HCO3)2 2NaHCO3 + CaCO3
CaSO4 + Na2CO3 CaCO3 + Na2SO4
4. Proses pertukaran basa
2.4 Total Zat Terlarut
Di dalam air minum total zat terlarut (total dissolved solids) pada umumnya disebabkan oleh adanya garam inorganik dan zat organik. Adanya kontribusi ion karbonat, bikarbonat, klorida, sulfat, nitrat, natrium, kalium, kalsium, dan magnesium. Total zat terlarut dalam air akibat adanya kontak dengan batuan dan tanah, dan polusi di daerah perkotaan juga memberikan kontribusi (Gray, 2008; De Zuane, 1996).
Total zat terlarut dapat dihubungkan dengan kesadahan. Dimana total zat-zat terlarut dapat dihitung secara gravimetri dengan pengeringan dan pengukuran residu dalam mg/l. Metode lain dalam penentuan total zat terlarut yaitu dengan menggunakan konduktivitas (Gray, 2008; De Zuane, 1996).
2.5 Total Zat Padat
Total zat padat yaitu semua zat padat (total solids) yang terdapat di dalam air minum yang dapat dihitung dengan penguapan dan pengeringan pada suhu 103 – 1050C. Total zat padat 500 mg/l merupakan batas maksimal yang diinginkan (De Zuane, 1996).
2.6 Sumber-Sumber Air Yang Diolah Menjadi Air Minum 2.6.1 Air Hujan
2.6.2 Air Permukaan
Air permukaan meliputi badan-badan air seperti sungai, danau, telaga, waduk, dan rawa. Sebagian besar air permukaan berasal dari air hujan yang jatuh ke permukaan bumi (Chandra, 2006).
2.6.3 Air Tanah
Air tanah berasal dari air hujan yang jatuh ke permukaan bumi kemudian mengalami penyerapan ke dalam tanah dan proses filtrasi secara alami. Proses-proses yang telah dialami air hujan membuat air tanah menjadi lebih baik dan lebih murni dibandingkan air permukaan. Sebelum mencapai lapisan tempat air tanah, air hujan akan menembus beberapa lapisan tanah menyebabkan air mengandung zat-zat mineral dan menyebabkan terjadinya kesadahan pada air. Zat-zat mineral tersebut antara lain kalsium, magnesium, besi, dan mangan (Chandra, 2006).
2.7 Proses Pengolahan Air Minum 2.7.1 Klorinasi
Klorinasi dapat dilakukan dengan menggunakan gas klorin cair, larutan natrium hipoklorit atau butiran kalsium hipoklorit. Gas klorin cair dimasukkan ke dalam tabung bertekanan. Gas dikeluarkan dari tabung dan ditakar ke dalam air menggunakan klorinator yang sekaligus dapat mengendalikan dan mengukur laju alir gas (WHO, 2004).
untuk membentuk produk tidak terlarut yang dapat disingkirkan melalui filtrasi lanjut (WHO, 2004).
2.7.2 Ozonasi
Ozon adalah oksidasi yang kuat dan banyak kegunaannya dalam pengolahan air, termasuk oksidasi zat kimia organik. Ozon dapat digunakan sebagai desinfektan utama. Gas ozon (O3) dibentuk dengan melewatkan oksigen melalui
medan listrik bertegangan tinggi. Hasil udara kaya ozon dialirkan langsung ke dalam air dengan alat penghambur berpori pada dasar kolam penghubung. Pelarutan minimal 80 % ozon akan tercapai, sementara sisanya dalam bentuk gas akan keluar yang dialirkan menuju penghancur ozon dan keluar menuju atmosfer (WHO, 2004).
2.7.3 Filtrasi
Zat partikulat dapat disingkirkan dari air mentah melalui filter gravitasi cepat, horizontal, bertekanan, dan filter pasir lambat. Filtrasi pasir lambat pada dasarnya adalah proses biologis sedangkan lainnya adalah proses pengolahan fisik. Filter gravitasi cepat, horizontal, dan bertekanan dapat digunakan untuk filtrasi langsung air mentah tanpa pengolahan awal (WHO, 2004).
2.7.4 Aerasi
dalam tangki menara yang air nya dialirkan menuju semacam kincir air yang digerakkan oleh tiupan udara (WHO, 2004).
2.7.5 Koagulasi Kimiawi
Pengolahan berbasis koagulasi merupakan metode paling umum digunakan untuk mengolah air permukaan. Koagulan kimia biasanya garam aluminium atau besi dialirkan ke dalam air mentah dalam kondisi yang terkendali untuk membentuk hidroksida logam flokulen padat. Flok akan mengikat kontaminan yang melayang dan terlarut melalui mekanisme netralisasi muatan, adsorpsi, dan penangkapan. Efisiensi proses koagulasi bergantung pada mutu air mentah, koagulan yang digunakan, dan faktor operasional termasuk kondisi pencampuran, dosis koagulasi, dan pH (WHO, 2004).
2.7.6 Adsorpsi Karbon Teraktivasi
Karbon teraktivasi dihasilkan melalui termalisasi terkendali dari materi karbon terutama kayu, tempurung kelapa dan sayuran busuk. Aktivasi tersebut menghasilkan materi berpori yang luas (500-1500 m2/g) dan afinitas yang tinggi terhadap senyawa organik. Karbon teraktivasi digunakan untuk menyingkirkan pestisida dan zat kimia organik lain, senyawa berasa dan berbau, racun sianobakterial, dan karbon organik total (WHO, 2004).
2.7.7 Penukaran Ion
habis maka resin akan dibentuk kembali dengan menggunakan larutan natrium klorida (WHO, 2004).
2.7.8 Proses Membran
Proses membran yang paling signifikan dalam pengolahan air adalah osmosis balik (reverse osmosis), ultrafiltrasi, mikrofiltasi, dan nanofiltrasi. Proses ini biasanya digunakan untuk menghasilkan air dalam aplikasi industri, farmasi dan sekarang digunakan untuk pengolahan air minum (WHO, 2004).
Apabila dua larutan dipisahkan oleh membran semipermeabel, pelarut biasanya mengalir dari larutan berkonsentrasi rendah ke larutan berkonsentrasi tinggi. Namun, pelarut dapat dipaksa mengalir ke arah yang berlawanan dari konsentrasi tinggi ke konsentrasi rendah dengan menaikkan tekanan pada larutan berkonsentrasi tinggi. Selisih tekanan yang diperlukan disebut tekanan osmotik dan proses nya dikenal sebagai reverse osmosis (WHO, 2004).
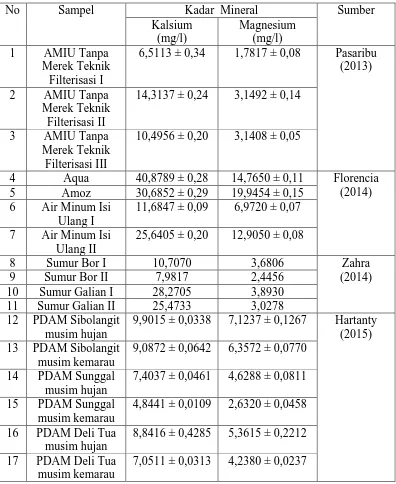
2.8 Kadar Kalsium Dan Magnesium Dalam Air Minum
Tabel 2.2 Kadar Kalsium dan Magnesium dalam Sampel 12 PDAM Sibolangit
musim hujan
9,9015 ± 0,0338 7,1237 ± 0,1267 Hartanty (2015) 13 PDAM Sibolangit
musim kemarau
2.9 Dampak Negatif Air Minum Yang Rendah Mineral dan Demineral
pipa distribusi. Penyerapan logam-logam toksis seperti Pb di dalam pencernaan akan meningkat jika mineral kalsium dan magnesium sangat rendah dalam air minum. Jika dalam makanan terdapat logam toksis Pb walaupun dalam jumlah sedikit, akan mudah diserap oleh tubuh apabila kadar kalsium dan magnesium rendah di dalam air minum. Akan tetapi apabila kalsium dan magnesium cukup dalam air minum maka penyerapan Pb, baik yang terdapat di dalam air minum dan makanan lainnya akan dihambat atau tidak terjadi (Fox, 1998; Kozisek, 2005; Silalahi, 2014).
Air minum bukanlah satu-satunya sumber mineral kalsium dan magnesium. Akan tetapi jika kandungan kalsium dan magnesium dalam air minum sangat rendah maka akan terjadi gangguan penyerapan kalsium dan magnesium yang terdapat di dalam makanan lainnya. Berdasarkan fakta ini maka WHO telah menganjurkan dan memberikan persyaratan mineral di dalam air minum, masing-masing dengan syarat minimal 20 mg kalsium dan 10 mg magnesium dalam satu liter air minum. Sedangkan menurut Depkes RI hanya menyatakan kandungan maksimal kalsium dan magnesium yang dianjurkan dalam air minum yaitu 75 mg/liter dan 30 mg/l dan tidak ada syarat minimal (WHO, 2005; Permenkes, RI., 1975; Silalahi, 2014).
2.10 Analisis Kalsium Dan Magnesium 2.10.1 Titrasi Kompleksometri
membentuk kompleks yang tidak stabil pada pH rendah. Oleh karena itu titrasi kalsium dan magnesium dengan EDTA dilakukan pada larutan buffer amonia pH 10 (Gandjar dan Rohman, 2007).
Untuk deteksi titik akhir titrasi digunakan indikator zat warna. Indikator zat warna ditambahkan pada larutan logam pada saat awal sebelum dilakukan titrasi dan akan membentuk kompleks berwarna. Pada saat titik akhir titrasi (ada sedikit kelebihan EDTA) maka kompleks indikator-logam akan pecah dan akan menghasilkan warna yang berbeda. Indikator yang dapat digunakan untuk titrasi kompleksometri adalah hitam eriokrom, mureksid, jingga pirokatekol, jingga xilenol, kalmagit, dan biru hidroksi naftol (Gandjar dan Rohman, 2007).
2.10.2 Spektrofotometri Serapan Atom
Metode spektrofotometri serapan atom didasarkan pada absorbsi cahaya oleh atom. Atom-atom akan menyerap cahaya pada panjang gelombang tertentu tergantung sifat unsurnya. Sebagai contoh kalsium menyerap cahaya pada panjang gelombang 422,7 nm dan magnesium pada panjang gelombang 285,2 nm. Cahaya pada panjang gelombang ini mempunyai cukup energi untuk mengubah tingkat elektronik suatu atom (Khopkar, 1985).
Keberhasilan analisis ini tergantung pada proses eksitasi dan cara memperoleh garis resonansi yang tepat. Oleh karena itu temperatur nyala yang digunakan harus sangat tinggi. Nyala yang digunakan berfungsi sebagai pembakar dan oksidator. Umumnya bahan bakar yang digunakan adalah propana, butana, hidrogen dan asetilen sedangkan oksidator nya adalah udara, oksigen, N2O, dan
2.11 Validasi Metode Analisis
Validasi metode analisis adalah suatu tindakan penilaian terhadap parameter tertentu berdasarkan percobaan laboratorium untuk membuktikan bahwa parameter tersebut memenuhi persyaratan untuk penggunaannya. Hal ini dilakukan untuk menjamin bahwa metode analisis akurat, spesifik, reprodusibel, dan tahan pada kisaran analit yang akan dianalisis (Harmita, 2004 ; Gandjar dan Rohman, 2007).
Beberapa parameter analisis yang harus dipertimbangkan dalama validasi metode analisis adalah sebagai berikut :
1. Kecermatan
Kecermatan (accuracy) dinyatakan sebagai persen perolehan kembali (recovery) analit yang ditambahkan. Untuk mencapai kecermatan yang tinggi dapat dilakukan dengan cara menggunakan peralatan yang telah dikalibrasi, menggunakan pereaksi dan pelarut yang baik, pengontrolan suhu, dan pelaksanaannya yang cermat serta taat asas sesuai prosedur (Harmita, 2004).
Kecermatan ditentukan dengan dua cara yaitu : - Metode simulasi (spiked-placebo recovery)
Dalam metode simulasi, sejumlah analit bahan murni ditambahkan ke dalam campuran bahan pembawa sediaan farmasi (plasebo) lalu campuran tersebut dianalisis dan hasilnya dibandingkan dengan kadar analit yang ditambahkan (kadar yang sebenarnya) (Harmita, 2004).
- Metode penambahan baku (standard addition method)
dianalisis lagi. Selisih kedua hasil dibandingkan dengan kadar sebenarnya (hasil yang diharapkan) (Harmita, 2004).
Dalam kedua metode tersebut, persen perolehan kembali dinyatakan sebagai rasio antara hasil yang diperoleh dengan hasil yang sebenarnya. Metode adisi dapat dilakukan dengan menambahkan sejumlah analit dengan konsentrasi tertentu pada sampel yang diperiksa lalu dianalisis dengan metode tersebut. Persen perolehan kembali ditentukan dengan menentukan berapa persen analit yang ditambahkan tadi dapat ditentukan (Harmita, 2004).
Persen perolehan kembali dapat dihitung dengan menggunakan rumus di bawah ini:
% Perolehan kembali = ��−��
��∗ � 100%
Keterangan :
CA = Kadar mineral dalam sampel sebelum penambahan baku
CF = Kadar mineral dalam sampel setelah penambahan baku
C*A = Kadar larutan baku yang ditambahkan (Harmita, 2004). 2. Keseksamaan
adalah keseksamaan metode jika dilakukan berulang kali oleh analis yang sama pada kondisi sama dan dalam interval waktu yang pendek (Harmita, 2004).
Menurut Harmita (2004), simpangan baku relatif dapat dihitung dengan menggunakan rumus berikut ini :
RSD = ×100%
X SD
Keterangan : X = kadar rata-rata sampel (mg/l) − SD = standar deviasi (mg/l)
Koefisien variasi meningkat dengan menurunnya kadar analit yang dianalisis. Pada kadar satu per sejuta (ppm) RSD nya adalah 16 % dan pada kadar part per billion (ppb) adalah 32 % (Harmita, 2004).
3. Batas Deteksi dan Batas Kuantitasi
Batas deteksi adalah jumlah analit terkecil dalam sampel yang dapat di deteksi dan memberikan respon signifikan dibandingkan dengan blangko. Batas kuantitasi merupakan parameter pada analisis dan diartikan sebagai kuantitas analit terkecil dalam sampel yang masih dapat memenuhi kriteria cermat dan seksama (Harmita, 2004).
Menurut Harmita (2004), batas deteksi (limit of detection, LOD) dan batas kuantitasi (limit of quantification, LOQ) dihitung dengan menggunakan rumus sebagai berikut:
Standar deviasi (��) = �∑(�−��)2
�−2
LOD = 3� (��)
�����
LOQ = 10� (��)