SKRIPSI
STUDI EKSTRAKSI PADA PROSES PEMBUATAN GELATIN TIPE B DARI KULIT SAPI
Oleh HASAN F24101107
2007
FAKULTAS TEKNOLOGI PERTANIAN INSTITUT PERTANIAN BOGOR
Hasan. F24101107. Studi Ekstraksi Pada Proses Pembuatan Gelatin Tipe B Dari Kulit Sapi. Dibawah bimbingan Dr. Ir. Sugiyono, M.App.Sc dan Ir. Irshan Zainudin,M.Si.
ABSTRAK
Gelatin merupakan molekul polipeptida dengan bobot molekul tinggi yang berasal dari kolagen yang merupakan komponen utama penyusun jaringan hewan (kulit, tulang, dan tendon). Gelatin umumnya digunakan sebagai bahan pengemulsi dan penstabil sistem emulsi mengingat kemampuannya dalam berikatan dengan air dan lemak. Produk pangan yang umumnya diproduksi dengan tambahan gelatin antara lain permen, es krim, jelly, dan daging kaleng. Kemampuan gelatin untuk meningkatkan nilai guna suatu produk dimanfaatkan oleh industri pangan, industri farmasi, kosmetika dan kimia. Industri farmasi umumnya menggunakan gelatin sebagai bahan baku dalam pembuatan kapsul sedangkan industri kimia menggunakan gelatin dalam pembuatan perekat (lem) dan film untuk fotografi
Salah satu proses penting dalam pembuatan gelatin adalah ekstraksi. Proses ekstraksi termasuk dalam proses utama dikarenakan selama proses ini berlangsung terjadi denaturasi serat kolagen menjadi gelatin. Semakin efektif dan efisien proses ekstraksi yang dilakukan maka akan semakin baik pula kualitas gelatin yang akan didapatkan. Oleh karena itu perlu dilakukan penelitian tentang hal-hal yang dapat memaksimalkan proses ekstraksi. Penelitian ini menggunakan metode perendaman (liming) bahan baku kulit sapi dalam kondisi basa. Hal ini didasarkan pada kondisi kulit yang dijadikan sebagai bahan baku. Kulit diperoleh dari sapi dewasa (2-3 tahun) dengan kondisi kolagen yang sudah tua (US Patent 5877287). Kolagen yang tua mempunyai susunan ikatan triple helix yang lebih rapat dan kompleks akibatnya membutuhkan basa agar proses hidrolisis kolagen menjadi gelatin lebih optimal. Penelitian ini bertujuan untuk mengetahui pengaruh perlakuan perbandingan kulit-air serta pemberian interval agitasi yang berbeda pada proses pembuatan gelatin tipe B dari kulit sapi menggunakan metode ekstraksi basa. Karakteristik produk gelatin hasil penelitian yang diukur antara lain; rendemen, kadar air, kadar abu, warna, kekuatan gel, viskositas, dan stabilitas emulsi.
Ekstraksi dilakukan pada 4 tingkat perbandingan kulit-air yaitu ; 1 :1, 1:2, 1:3, dan 1: 4 dengan interval agitasi di tiap 10, 20, dan 30 menit. Agitasi dilakukan dengan kecepatan putaran 50 rpm dan lama putaran 3 menit setiap kali berputar. Ekstraksi dilakukan dengan 5 tahap dengan suhu dan lama masing-masing: tahap I (55 OC, 5 jam), tahap II (65 OC, 4 jam), tahap III ( 75 OC, 3 jam), tahap IV (85 OC, 2 jam) , dan tahap V (95 OC, 1 jam). Pengamatan pengaruh kedua perlakuan (perbandingan kulit-air serta interval agitasi) terhadap beberapa parameter gelatin menunjukkan bahwa kedua perlakuan tidak memberikan pola kecenderungan tertentu. Dengan kata lain tidak ada tren khusus (naik atau turun) pada parameter yang diamati akibat dari peningkatan atau penurunan kuantitas perlakuan yang diberikan.
Kisaran nilai rendemen yang didapatkan dari penelitian ini adalah 6,46 – 13,11%,. Pengukuran warna gelatin hasil penelitian menggunakan chromameter
didapatkan kisaran notasi L 55,49-58,90 (cerah) dan notasi b 39,74-41,68 (kuning). Nilai kadar air gelatin hasil penelitian berada pada kisaran 8,82-12,74 % dengan nilai kadar abu berada pada kisaran 2,89-3,89 (% bk). Pengukuran nilai kekuatan gel, viskositas, dan stabilitas emulsi gelatin hasil penelitian didapatkan nilai masing-masing berada pada kisaran 115– 280 bloom, 5 – 18 cP dan 50,71-59,62%.
Mutu gelatin hasil penelitian jika dinilai berdasarkan United States Patent (1999), yang termasuk gelatin kualitas tinggi adalah sampel gelatin A1B2, A2B3, dan A4B1. Sampel gelatin yang termasuk gelatin kualitas sedang adalah A1B1, A1B3, A2B1, A2B2, A3B1, A3B2, A3B3, dan A4B2. Terdapat satu sampel yang termasuk gelatin kualitas rendah yaitu sampel A4B3. Penilaian ini menunjukkan bahwa sebagian besar sampel gelatin merupakan gelatin dengan kualitas sedang.
STUDI EKSTRAKSI PADA PROSES PEMBUATAN GELATIN TIPE B DARI KULIT SAPI
Skripsi
Sebagai syarat untuk memperoleh gelar SARJANA TEKNOLOGI PERTANIAN pada Departemen Ilmu dan Teknologi Pangan
Fakultas Teknologi Pertanian Institut Pertanian Bogor
Oleh HASAN F24101107
2007
FAKULTAS TEKNOLOGI PERTANIAN INSTITUT PERTANIAN BOGOR
STUDI EKSTRAKSI PADA PROSES PEMBUATAN GELATIN TIPE B DARI KULIT SAPI
Skripsi
Sebagai syarat untuk memperoleh gelar SARJANA TEKNOLOGI PERTANIAN pada Departemen Ilmu dan Teknologi Pangan
Fakultas Teknologi Pertanian Institut Pertanian Bogor
Oleh HASAN F24101107
Dilahirkan pada tanggal 14 Februari 1982 di Jakarta Tanggal Lulus : 27 Desember 2006
Menyetujui, Bogor , April 2007
Dr. Ir. Sugiyono, MApp.Sc Ir. Irshan Zainudin,M.Si Dosen Pembimbing I Dosen Pembimbing II
Dr. Dahrul Syah, MSc
RIWAYAT HIDUP
HASAN lahir di Jakarta, 14 Februari 1982. Penulis merupakan anak kelima dari sembilan bersaudara pasangan Bapak H. Abdul Hamid (alm) serta Ibu Hasanah. Pendidikan dari sekolah dasar hingga sekolah menengah umum diselesaikan di Jakarta yaitu SDN 05 Pagi Jakarta Utara, SLTPN 244 Jakarta Utara, dan SMUN 52 Jakarta Utara.
Tahun 2001 penulis diterima di Departemen Ilmu dan Teknologi Pangan, Institut Pertanian Bogor melalui UMPTN. Selama menempuh pendidikan, penulis aktif mengikuti organisasi kemahasiwaan di Badan Eksekutif Mahasiswa Tingkat Persiapan Bersama IPB (BEM TPB IPB 2001-2002), Pendiri UKM Klip (2002), Badan Pengawas HIMITEPA (2002-2003), staf divisi profesi HIMITEPA (2003-2004), menjadi asisten mata kuliah Pengawasan Mutu dan Mata Kuliah Pendidikan Agama Islam. Penulis menyelesaikan kuliah di IPB dengan skripsi berjudul ” Studi Ekstraksi Pada Proses Pembuatan Gelatin Tipe B Dari Kulit Sapi”
KATA PENGANTAR
Alhamdulillah, segala puji bagi Allah Ta’ala Rabb Semesta Alam atas nikmat Iman, nikmat Islam, dan nikmat sehat wal afiat sehingga penulis bisa merampungkan amanah besar ini. Shalawat serta salam penulis sampaikan pada Guru Besar dalam ilmu penghambaan pada sang Khalik, junjungan seluruh umat manusia, dialah Muhammad Rasulullah Sallallahu Alaihi Wassalam. Shalawat serta salam juga penulis sampaikan pada seluruh keluarga Beliau, Sahabat, Tabi’in serta seluruh umat manusia yang mengikuti ajarannya sampai hari akhir kelak.
Penulis ingin mengucapkan terima kasih sebesar-besarnya atas segala dukungan, arahan, dan doa sehingga skripsi ini akhirnya bisa diselesaikan. Terima kasih penulis sampaikan pada;
1. Almarhum Ayahanda dan Ibunda, serta semua Kakak serta Adikku anggota Keluarga Besar Hamid (Muliani, Abdullah, Nurbani,. Jihan, Husain, Rahmatiah, Muslim, dan Mei Muna). Semoga Allah Ta’alla selalu memberikan rasa kasih dan sayang diantara kita semua serta menjaga kita semua dari siksaan api neraka.
2. Bapak Dr. Ir Sugiyono, M.App Sc selaku dosen pembimbing pertama yang sudah dengan sabar memberikan arahan, dukungan, serta ilmu selama penulis menempuh studi di almamater ini. Semoga Allah membalas semua kebaikan Bapak dengan sesuatu yang lebih baik.
3. Bapak Ir. Irshan Zainuddin, Msi selaku dosen pembimbing kedua atas semua dukungan moril, motivasi, serta pembiayaan selama penulis menyelesaikan penelitian ini.
4. Bapak Dr. Ir. Djoko Hermanianto yang telah bersedia menjadi dosen penguji pada ujian skripsi penulis
5. Bapak Ir. Harianto Msi, Ir. Suharjito MSi, dan Bapak Ir. M. Jusuf Djafar MM selaku tim proyek penelitian gelatin BPPT.
6. Bapak Ir. Gigih Atmaji selaku Kepala Laboratorium Teknologi Agroindustri yang telah memberikan izin penggunaan Laboratorium.
7. Mbak Tuti, Mas Dedi, Mas Budi, Mas Sofyan, Kak Encep yang telah menemani dan membantu secara teknis penelitian di laboratorium.
8. Fajri Helmi “Adjie” (Hortikultura 41) yang banyak membantu dalam penyediaan fasilitas kepada penulis.
Semoga skripsi ini bisa bermanfaat bagi semua pihak.
Bogor, April 2007 Penulis
Hasan. F24101107. Studi Ekstraksi Pada Proses Pembuatan Gelatin Tipe B Dari Kulit Sapi. Dibawah bimbingan Dr. Ir. Sugiyono, M.App.Sc dan Ir. Irshan Zainudin,M.Si.
RINGKASAN
Penelitian ini bertujuan mempelajari pengaruh perlakuan perbandingan kulit-air sertal pemberian interval agitasi yang berbeda pada proses pembuatan gelatin tipe B dari kulit sapi menggunakan metode ekstraksi basa. Beberapa parameter yang diamati antara lain; rendemen, warna, kadar air, kadar abu, kekuatan gel, viskositas, dan stabilitas emulsi. Alat ekstraksi yang digunakan adalah ekstraktor yang didesain oleh Laboratorium Teknologi Agroindustri Badan Pengkajian dan Penerapan Teknologi (LTA-BPPT) Serpong.
Ekstraksi dilakukan pada 4 tingkat perbandingan kulit-air yaitu ; 1 :1, 1:2, 1:3, dan 1: 4 dengan interval agitasi di tiap 10, 20, dan 30 menit. Agitasi dilakukan dengan kecepatan putaran 50 rpm dan lama putaran 3 menit setiap kali berputar. Ekstraksi dilakukan dengan 5 tahap dengan suhu dan lama masing-masing: tahap I (55 OC, 5 jam), tahap II (65 OC, 4 jam), tahap III ( 75 OC, 3 jam), tahap IV (85 OC, 2 jam) , dan tahap V (95 OC, 1 jam).
Pengamatan pengaruh kedua perlakuan (perbandingan kulit-air serta interval agitasi) terhadap beberapa parameter gelatin menunjukkan bahwa kedua perlakuan tidak memberikan pola kecenderungan tertentu. Dengan kata lain tidak ada tren khusus (naik atau turun) pada parameter yang diamati akibat dari peningkatan atau penurunan kuantitas perlakuan yang diberikan.
Kisaran nilai rendemen yang didapatkan dari penelitian ini adalah 6,46 – 13,11%,. Pengukuran warna gelatin hasil penelitian menggunakan chromameter didapatkan kisaran notasi L 55,49-58,90 (cerah) dan notasi b 39,74-41,68 (kuning). Nilai kadar air gelatin hasil penelitian berada pada kisaran 8,82-12,74 % dengan nilai kadar abu berada pada kisaran 2,89-3,89 (% bk). Pengukuran nilai kekuatan gel, viskositas, dan stabilitas emulsi gelatin hasil penelitian didapatkan nilai masing-masing berada pada kisaran 115– 280 bloom, 5 – 18 cP dan 50,71-59,62%.
Mutu gelatin hasil penelitian jika dinilai berdasarkan United States Patent (1999), yang termasuk gelatin kualitas tinggi adalah sampel gelatin A1B2, A2B3,
dan A4B1. Sampel gelatin yang termasuk gelatin kualitas sedang adalah A1B1, A1B3, A2B1, A2B2, A3B1, A3B2, A3B3, dan A4B2. Terdapat satu sampel yang termasuk gelatin kualitas rendah yaitu sampel A4B3. Penilaian ini menunjukkan bahwa sebagian besar sampel gelatin merupakan gelatin dengan kualitas sedang.
DAFTAR ISI
Halaman
KATA PENGANTAR... i
DAFTAR ISI... iii
DAFTAR TABEL... v
DAFTAR GAMBAR... vi
DAFTAR LAMPIRAN ... vii
I. PENDAHULUAN... 1
A. LATAR BELAKANG... 1
B. TUJUAN PENELITIAN... 3
II. TINJAUAN PUSTAKA ... 4
A. KULIT... 4
B. KOLAGEN... 4
C. GELATIN... 6
D. PERUBAHAN KOLAGEN MENJADI GELATIN... 10
E. PERUBAHAN GELATIN MENJADI GEL ... 11
F. PROSES PEMBUATAN GELATIN ... 12
III. METODOLOGI ... 15
A. BAHAN DAN ALAT ... 15
B. WAKTU DAN TEMPAT ... 16
C. METODE PENELITIAN ... 16
IV. HASIL DAN PEMBAHASAN ... 22
A. PENELITIAN PENDAHULUAN ... 22
B. PENELITIAN UTAMA ... 23
1. Rendemen ... 23
2. Warna ... 24
3. Kadar Air Gelatin Kering... 28
4. Kadar Abu ... 30
5. Kekuatan Gel ... 31
6. Viskositas ... 34
V. KESIMPULAN DAN SARAN ... 38
A. KESIMPULAN ... 38
B. SARAN ... 38
DAFTAR PUSTAKA ... 39
DAFTAR TABEL
Halaman
Tabel 1. Data impor gelatin Indonesia tahun 1998 – 2005 ... 1
Tabel 2. Jumlah pemotongan sapi dan potensi kulit split ... 2
Tabel 3.Penyebaran kolagen dalam jaringan hewan mamalia ... 5
Tabel 4. Perbedaan sifat gelatin berdasarkan tipe ... 7
Tabel 5. Standar mutu gelatin berdasarkan Standar Nasional Indonesia No. 06-3735 tahun 1995 dan British Standard : 757 tahun 1975 ……….. 8
Tabel 6. Tahapan proses ekstraksi kolagen secara bertingkat dalam menghasilkan gelatin ... 13
Tabel 7. Suhu dan waktu yang digunakan di setiap tahap ekstraksi penelitian pendahuluan ... 16
DAFTAR GAMBAR
Halaman
Gambar 1. Susunan molekul tropokolagen pada fibril kolagen... 5
Gambar 2. Perubahan kolagen menjadi gelatin ... 11
Gambar 3. Ekstraktor ... 15
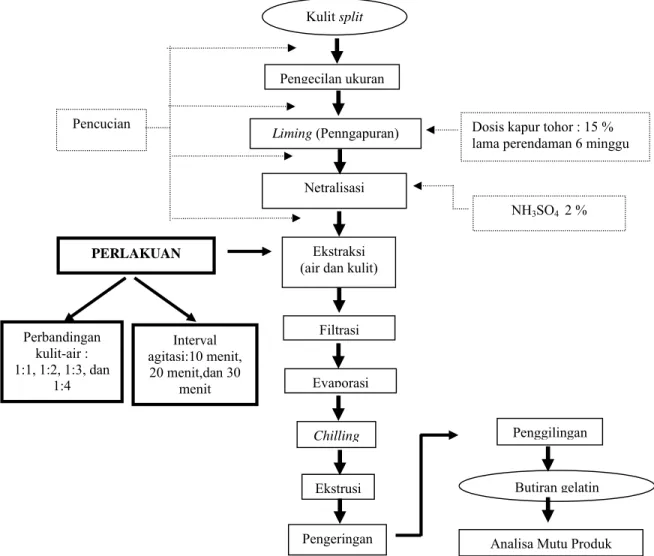
Gambar 4. Diagram alir proses pembuatan gelatin dari kulit split... 18
Gambar 5. Pengaruh perbandingan kulit-air dan interval agitasi terhadap rendemen gelatin sampel... 23
Gambar 6. Pengaruh perbandingan kulit-air dan interval agitasi terhadap notasi L sampel gelatin ... 25
Gambar 7. Pengaruh perbandingan kulit-air dan interval agitasi terhadap notasi b sampel gelatin ... 27
Gambar 8. Bubuk Sampel Gelatin ... 28
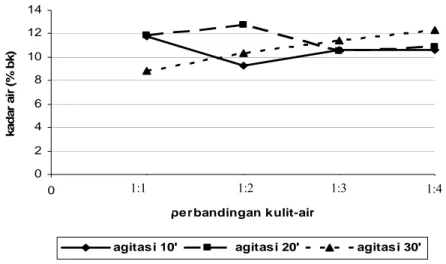
Gambar 9. Pengaruh perbandingan kulit-air dan interval agitasi terhadap kadar air sampel gelatin ... 29
Gambar 10. Pengaruh perbandingan kulit-air dan interval agitasi terhadap kadar abu sampel gelatin ... 31
Gambar 11. Pengaruh perbandingan kulit-air dan interval agitasi terhadap kekuatan gel sampel gelatin ... 33
Gambar 12. Pengaruh perbandingan kulit-air dan interval agitasi terhadap viskositas sampel gelatin ... 34
Gambar 13. Pengaruh perbandingan kulit-air dan interval agitasi terhadap stabilitas emulsi sampel gelatin ... 36
DAFTAR LAMPIRAN
Halaman
Lampiran 1. Nilai Rata-Rata Rendemen (%) Pada Setiap Perlakuan... 43
Lampiran 2. Diagram Kromatisitas ... 43
Lampiran 3. Nilai Rata-Rata Notasi L Pada Setiap Perlakuan... 44
Lampiran 4. Nilai Rata-Rata Notasi b Pada Setiap Perlakuan... 44
Lampiran 5. Nilai Rata-rata Kadar Air (%bk) Pada Setiap Perlakuan ... 44
Lampiran 6. Nilai Rata-Rata Kadar Abu (%) Pada Setiap Perlakuan... 45
Lampiran 7. Nilai Rata-Rata Kekuatan Gel (bloom) Pada Setiap Perlakuan ... 45
Lampiran 8. Nilai Rata-Rata Viskositas (cP) Pada Setiap Perlakuan... 45
Lampiran 9. Nilai Rata-Rata Stabilitas Emulsi (%) Pada Setiap Perlakuan... 46
I. PENDAHULUAN
A. LATAR BELAKANG
Gelatin merupakan molekul polipeptida dengan bobot molekul tinggi yang berasal dari kolagen yang merupakan komponen utama penyusun jaringan hewan (kulit, tulang, dan tendon). Gelatin umumnya digunakan sebagai bahan pengemulsi dan penstabil sistem emulsi mengingat kemampuannya dalam berikatan dengan air dan lemak. Produk pangan yang umumnya diproduksi dengan tambahan gelatin antara lain permen, es krim, jelly, dan daging kaleng. Kemampuan gelatin untuk meningkatkan nilai guna suatu produk dimanfaatkan oleh industri pangan, industri farmasi, kosmetika dan kimia. Industri farmasi umumnya menggunakan gelatin sebagai bahan baku dalam pembuatan kapsul sedangkan industri kimia menggunakan gelatin dalam pembuatan perekat (lem) dan film untuk fotografi.
Selama ini untuk menutupi kebutuhan gelatin dalam negeri, industri pangan mendapatkannya melalui impor dari negara-negara Eropa, China, dan Amerika. Mulai tahun 1998 sampai tahun 2001 jumlah impor gelatin cenderung meningkat. Pada tahun 2002 nilai impor menurun dan kembali meningkat pada tahun 2003. Data impor gelatin di Indonesia dapat dilihat pada Tabel 1.
Tabel 1. Data impor gelatin Indonesia tahun 1998 - 2005
Tahun Bobot (kg) Nilai (US $)
1998 1. 851. 328 6. 781. 735 1999 2. 371. 738 9. 059. 440 2000 3. 418. 383 10. 555. 489 2001 4. 291. 579 10. 749. 199 2002 2. 144. 372 6. 801. 882 2003 2. 145. 916 8. 001. 714 2004 2. 630. 692 8. 063. 802 Jan- Mei 2005 1. 213. 111 4. 215. 779 Sumber : BPS (2005)
Ketergantungan Indonesia terhadap gelatin impor setiap tahun pada dasarnya dapat dikurangi. Jumlah ketersediaan kulit di Indonesia cukup
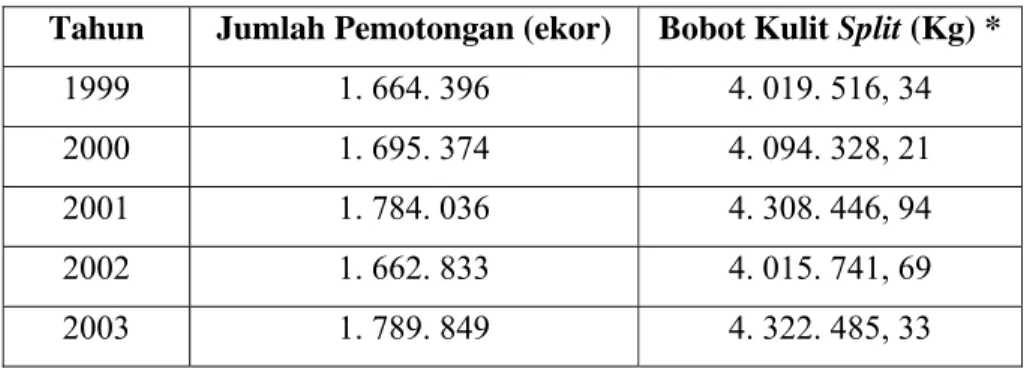
melimpah. Jumlah ini berasal dari industri penyamakan kulit yang ada di Indonesia. Industri penyamakan kulit menghasilkan limbah industri yang cukup besar, khususnya limbah yang tergolong pada kelompok kulit split. Kulit split adalah kulit yang telah mengalami proses splitting yaitu pembelahan kulit menjadi dua lapisan atau lebih untuk memperoleh tebal yang dikehendaki. Hasil samping kulit dari proses ini bisa mencapai sampai 11,5 % dari bahan baku kulit mentah yang diproses (BPS, 1998). Jumlah pemotongan sapi di Indonesia pada tahun 2003 sebesar 1.789.849, sehingga ketersediaan jumlah kulit split dari sapi potong di Indonesia tahun 2003 adalah sebesar 4.322.485,33 kg (BPS, 2003). Data pemotongan sapi dan potensi kulit split disajikan pada Tabel 2.
Tabel 2. Jumlah pemotongan sapi dan potensi kulit split
Tahun Jumlah Pemotongan (ekor) Bobot Kulit Split (Kg) *
1999 1. 664. 396 4. 019. 516, 34
2000 1. 695. 374 4. 094. 328, 21
2001 1. 784. 036 4. 308. 446, 94
2002 1. 662. 833 4. 015. 741, 69
2003 1. 789. 849 4. 322. 485, 33
Keterangan : * Data diperoleh dari bobot sapi (300 Kg) x 7 % x 11.5 % Sumber : Badan Pusat Statistik (2003)
Selain itu, ketergantungan terhadap impor gelatin dapat memberikan beberapa konsekuensi, antara lain harga gelatin impor yang beredar di pasaran menjadi relatif mahal serta status kehalalannya yang masih belum jelas. Lebih dari 80 % gelatin yang diproduksi di luar negeri adalah berasal dari daging babi dan ditegaskan oleh Glicksmann (1969) bahwa umumnya gelatin yang diproduksi oleh Amerika Serikat adalah dari daging babi yang dibekukan dan diproduksi secara asam.
Salah satu proses penting dalam pembuatan gelatin adalah ekstraksi. Proses ekstraksi termasuk dalam proses utama dikarenakan selama proses ini berlangsung terjadi denaturasi serat kolagen menjadi gelatin. Semakin efektif
dan efisien proses ekstraksi yang dilakukan maka akan semakin baik pula kualitas gelatin yang akan didapatkan. Oleh karena itu perlu dilakukan penelitian tentang hal-hal yang dapat memaksimalkan proses ekstraksi.
Penelitian ini menggunakan metode perendaman (liming) bahan baku kulit sapi dalam kondisi basa. Hal ini didasarkan pada kondisi kulit yang dijadikan sebagai bahan baku. Kulit diperoleh dari sapi dewasa (2-3 tahun) dengan kondisi kolagen yang sudah tua (US Patent 5877287). Kolagen yang tua mempunyai susunan ikatan triple helix yang lebih rapat dan kompleks akibatnya membutuhkan basa agar proses hidrolisis kolagen menjadi gelatin lebih optimal.
B. TUJUAN PENELITIAN
Penelitian ini bertujuan untuk mengetahui pengaruh perlakuan perbandingan kulit-air serta pemberian interval agitasi yang berbeda pada proses pembuatan gelatin tipe B dari kulit sapi menggunakan metode ekstraksi basa.
II. TINJAUAN PUSTAKA
A. KULIT (Hides)
Kulit merupakan hasil samping dari pemotongan hewan yang berupa organ tubuh bagian terluar yang dipisahkan dari tubuh pada saat proses pengulitan. Kulit tersebut merupakan bahan mentah kulit samak, berupa tenunan dari tubuh hewan yang terbentuk dari sel-sel hidup (Djojowidagdo, 1981). Kulit mentah dibedakan atas dua kelompok, yaitu kelompok kulit yang berasal dari hewan besar seperti sapi, kerbau, dan lain-lain, yang dalam istilah asing disebut hides, dan kelompok kulit yang berasal dari hewan kecil seperti kambing, kelinci, dan lain-lain yang dalam istilah asing disebut skins (Purnomo, 1985). Kulit hewan besar lebih banyak mengandung protein, lemak, dan khitin dibanding kulit hewan kecil (Akademi Teknologi Kulit, 1984).
Komposisi kimia kulit hewan segar terdiri atas 64 % air, 33% protein, 2 % lemak, 0.5% mineral, dan 0.5% substansi lain. Protein kulit sebesar 33% disusun oleh 29 % kolagen, 2% keratin, 0.3% elastin, 1% albumin, dan globulin serta 0.7% mucin dan mucoid (Sharphouse, 1978).
Komposisi kimia kulit hewan pada umumnya secara kimia dapat dibagi atas dua golongan, yaitu bagian non protein dan protein. Bagian non protein terdiri dari lipid, karbohidrat, enzim, vitamin dan mineral. Bagian protein dapat dibedakan dalam dua bentuk, yaitu protein yang berbentuk serat (fibrous protein) dan protein yang tidak berbentuk serat (globular protein). Protein yang tidak berbentuk serat adalah albumin dan globulin, sedangkan protein yang berbentuk serat adalah kolagen, elastin dan keratin (Purnomo, 1985).
B. KOLAGEN
Kolagen merupakan komponen struktural utama pada serat-serat jaringan pengikat, berwarna putih dan terdapat di dalam semua jaringan dan organ hewan dan berperan penting dalam penyusun bentuk tubuh. Pada mamalia, kolagen terdapat pada kulit, tendon, tulang rawan dan jaringan ikat
lainnya. Jumlahnya mencapai 30% dari jumlah protein total yang terdapat dalam hewan vertebrata dan invertebrata (Ward dan Courts, 1977). Kandungan kolagen di setiap bagian tubuh mamalia disajikan pada Tabel 3, dengan bagian kulit sebagai bagian yang mengandung kolagen tertinggi, mencapai 89% dibandingkan jenis jaringan lainnya.
Tabel 3. Penyebaran kolagen dalam jaringan hewan mamalia
Jenis jaringan Kolagen (%) Jenis jaringan Kolagen (%)
Kulit 89 Usus Besar 18
Tulang 24 Lambung 23
Tendon 85 Ginjal 5
Aorta 23 Hati 2
Otot 2
Sumber : Ward dan Courts (1977)
Unit dasar penyusun kolagen adalah tropokolagen yang diperkirakan terdiri atas tiga rantai heliks polipeptida (Gambar 1) yang saling mengelilingi (berpilin) satu sama lain membentuk sebuah coil (gulungan), memiliki panjang dan diameter, masing-masing 3.000 Ǻ dan 14 Ǻ (Glicksman, 1969).
Gambar 1. Susunan molekul tropokolagen pada fibril kolagen (Lehninger, 1993)
Disamping pelarut alkali, kolagen juga larut dalam pelarut asam, sehingga kedua pelarut ini dimungkinkan untuk digunakan dalam proses produksi gelatin (Bennion, 1980). Dibawah mikroskop, jaringan tersebut
tampak sebagai serat putih buram yang dikelilingi oleh protein lain dan mucopolysaccharida (Poppe, 1992). Perlakuan alkali dan asam menyebabkan kolagen mengembang dan menyebar. Pemanasan kolagen secara bertahap akan menyebabkan struktur rusak dan rantai-rantai akan terpisah. Bentuk konformasi larutan kolagen sangat sensitif terhadap perubahan temperatur yang dapat menghancurkan makromolekulnya (Wong, 1989).
C. GELATIN
Gelatin adalah protein dari kolagen kulit, membran, tulang dan bagian tubuh berkolagen lainnya. Jika gelatin mendapat perlakuan perendaman dalam air maka gelatin akan mengembang dan menjadi lunak, dan berangsur-angsur menyerap air 5-10 kali bobot gelatin. Gelatin larut dalam air panas dan jika didinginkan (48 OC ) akan membentuk gel (Anonim, 1978).
Menurut Carley (1982), gelatin merupakan senyawa turunan yang dihasilkan dari serabut kolagen jaringan penghubung yang dihidrolisis dengan asam atau basa. Ditambahkan oleh Imeson (1985), bahwa gelatin merupakan salah satu hidrokoloid yang dapat digunakan sebagai bahan pembentuk gel (gelifying agent), bahan pengental (thickening agent), atau bahan penstabil (stabilizer). Gelatin berbeda dengan hidrokoloid lainya karena pada umumnya hidrokoloid adalah merupakan polisakarida sedangkan gelatin sendiri adalah senyawa protein. Hal inilah yang menjadikan gelatin mempunyai kemampuan untuk reversibel.
Gelatin termasuk kedalam zat yang bersifat amfoter, mempunyai gugus asam (karboksil) dan gugus basa (amina). Gelatin mudah larut dalam gliserol, manitol, dan propilen. Gelatin tidak larut dalam alkohol, aseton, dan pelarut non polar lainnya (King di dalam Glicksmann, 1969).
Gelatin bukanlah merupakan protein lengkap. Hal ini disebabkan karena tidak adanya asam amino esensial triptofan. Namun gelatin mengandung sejumlah kecil asam amino yang jarang yaitu hidroksilisin. Secara kimiawi komposisi asam amino gelatin mamalia hampir tetap. Perbedaan karakteristik kimia yang terjadi adalah sebagai hasil perbedaan perlakuan pada tahap awal.
Gelatin hasil perlakuan basa (tipe B) dan perlakuan asam (tipe A) mengalami perbedaan hidrolisis gugus amida primer yang dibentuk.
Gelatin tipe A umumnya diperoleh dari bahan baku kulit babi atau ternak yang masih muda. Babi atau ternak yang masih muda mempunyai rantai triple helix yang lebih sederhana. Sedangkan gelatin tipe B umumnya diperoleh dari kulit atau tulang sapi dewasa karena kandungan kolagennya yang sudah tua. Kolagen yang tua mempunyai rantai triple helix yang lebih rapat dan kompleks sehingga umumnya digunakan basa saat perendaman agar hidrolisis kolagen menjadi gelatin lebih optimal. (US Patent 5877287). Perbedaan sifat gelatin berdasarkan tipenya dapat dilihat pada Tabel 4.
Tabel 4. Perbedaan sifat gelatin berdasarkan tipe
Sifat Tipe A Tipe B
Kekuatan gel ( bloom) 50,0 – 300,0 50,0 – 300,0
Viskositas (cP) 1,50 – 7,50 2,00 – 7,50
Kadar abu (%) 0,30 – 2,00 0,50 – 2,00
pH 3,80 – 6,00 5,00 – 7,10
Titik isoelektrik 7,00 – 9,00 4,70 – 5,40
Sumber : GMIA (2001)
Sifat fisik maupun kimia gelatin tergantung dari kualitas bahan baku, pH, keberadaan zat-zat organik, metode ekstraksi, suhu dan konsentrasi (Parker, 1982). Bentuk gelatin yang beredar di pasaran terdiri dari dua bentuk yaitu gelatin yang tidak memiliki rasa apapun (plain atau unflavoured) dan gelatin yang memiliki rasa tertentu (flavoured). Gelatin flavoured mengandung gelatin, gula asam sitrat, rasa tertentu dan warna (Gates, 1981)
Menurut Ward dan Courts (1977), gelatin larut dalam air minimal pada suhu 49°C, atau biasanya berada pada suhu 60°C sampai 70°C. Gelatin tidak larut dalam air dingin, tetapi hanya akan mengembang. Perendaman dalam air dingin menjadikan gelatin lunak dan berangsur-angsur menyerap air 5 sampai 10 kali bobotnya (King, 1969). Ketika gelatin dipanaskan pada suhu di atas titik lelehnya, gelatin akan mencair dan dapat kembali membentuk gel apabila didinginkan.
Titik leleh gelatin adalah antara 27°C hingga 34°C dan dapat meleleh di dalam mulut. Karakteristik di atas sangat diharapkan oleh berbagai industri
pangan (Poppe,1992). Winarno (1997) menambahkan saat pemanasan, daya tarik menarik antara molekul air berkurang sehingga memberikan energi bagi untuk mengatasi daya tarik menarik molekul yang larut pada air, dengan demikian daya larut molekul yang dilarutkan dalam air akan meningkat dengan meningkatnya suhu air.
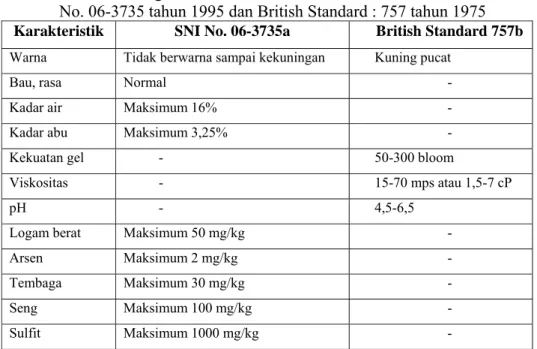
Warna gelatin tergantung pada bahan baku yang digunakan, metode pembuatan dan jumlah ekstraksi. Secara umum, warna gelatin tidak mempengaruhi kegunaannya (Glicksman,1969). Standar mutu gelatin disajikan pada Tabel 5.
Tabel 5. Standar mutu gelatin berdasarkan standar nasional Indonesia No. 06-3735 tahun 1995 dan British Standard : 757 tahun 1975
Karakteristik SNI No. 06-3735a British Standard 757b
Warna Tidak berwarna sampai kekuningan Kuning pucat
Bau, rasa Normal -
Kadar air Maksimum 16% -
Kadar abu Maksimum 3,25% -
Kekuatan gel - 50-300 bloom
Viskositas - 15-70 mps atau 1,5-7 cP
pH - 4,5-6,5
Logam berat Maksimum 50 mg/kg -
Arsen Maksimum 2 mg/kg -
Tembaga Maksimum 30 mg/kg -
Seng Maksimum 100 mg/kg -
Sulfit Maksimum 1000 mg/kg -
Sumber : a) Dewan Standarisasi Nasional (SNI 06.3735-1995)(1995) b) British Standard : 757 (1975)
United States Patent (1999) menggolongkan mutu gelatin menjadi tiga kelas berdasarkan kekuatan gelnya. Gelatin dengan kekuatan gel >240 bloom termasuk gelatin kualitas tinggi, gelatin dengan kekuatan gel 120-240 termasuk gelatin kualitas sedang, dan gelatin dengan kekuatan gel < 120 bloom termasuk gelatin kualitas rendah.
Menurut Fardiaz (1989), molekul-molekul gelatin mengandung tiga kelompok asam amino yang tinggi, yaitu sekitar sepertiganya terdiri dari residu asam amino glisin atau alanin, hampir seperempatnya terdiri atas asam amino
basa atau asam, dan seperempatnya lagi merupakan asam amino prolin dan hidroksiprolin. Proporsi yang tinggi dari residu polar ini membuat molekul gelatin mempunyai afinitas yang sangat tinggi terhadap air. Oleh karena proporsi yang tinggi dari residu prolin dan hidroksiprolin, molekul-molekul gelatin tidak mampu untuk berlilit membentuk coil helix seperti halnya pada kebanyakan molekul protein, sebaliknya molekul-molekul gelatin ini membentuk molekul yang panjang dan tipis, suatu sifat yang sangat menguntungkan dalam proses pembentukan gel.
Industri pangan dan non pangan menggunakan gelatin untuk berbagai tujuan. Jones (1977) mengemukakan beberapa kelebihan yang dimiliki oleh gelatin sehingga digunakan oleh banyak industri makanan. Kemampuan gelatin untuk memperhalus dan menimbulkan struktur gel yang kenyal digunakan oleh industri pangan sebagai bahan tambahan pada produk-produk olahan daging seperti sosis. Kemampuan lain yang dimiliki oleh gelatin adalah mampu menimbulkan tampilan yang lebih menarik karena adanya lapisan berwarna bening. Kemampuan gelatin ini dimanfaatkan oleh industri selai. Produk-produk selai juga memanfaatkan gelatin karena kemampuannya untuk melindungi produk dari sinar dan oksigen sehingga bisa lebih awet.
Berbagai produk permen dan coklat memanfaatkan gelatin untuk membuat produk permen dan coklat menjadi lebih lembut dan kenyal. Gelatin ditambahkan pada produk es krim karena kemampuannya yang mampu mencegah pembentukan kristal-kristal es yang besar sehingga tekstur es krim lebih lembut. Industri gelatin menggunakan gelatin sebagai bahan penjernih dan penyerap zat-zat yang dapat menyebabkan minuman menjadi berembun. Embun pada produk-produk minuman dapat menimbulkan kesan kotor pada wadahnya.
Industri non pangan khususnya farmasi menggunakan gelatin pada produk kapsul yang menjadikan kapsul menjadi lebih mudah ditelan. Produk lain di dunia farmasi yang menggunakan gelatin antara lain adalah obat tablet. Gelatin ditambahkan pada obat-obat berbentuk tablet karena kemampuannya untuk mengawetkan kandungan zat dalam obat tablet tersebut. Industri fotografi menggunakan gelatin yang sudah dicampur kristal perak halida untuk
melapisi lembaran film. Kristal perak halida menjadi lebih stabil terhadap sinar jika dilarutkan terlebih dahulu pada larutan gelatin.
D. PERUBAHAN KOLAGEN MENJADI GELATIN
Prinsip utama dalam transformasi kolagen menjadi gelatin adalah dengan cara mendenaturasi kolagen yang terlarut. Denaturasi menggunakan suhu (thermal) dapat dilakukan dengan cara memanaskan kolagen dalam kondisi netral atau sedikit asam pada suhu 40°C (Poppe, 1992). Menurut Johns dan Curts (1977), cara paling mudah mengubah kolagen menjadi gelatin adalah melalui proses denaturasi kolagen pada air bersuhu 40°C.
Kolagen akan terdisosiasi menjadi unit tropokolagen akibat kehilangan ikatan hidrogen dan ikatan hidrofobik yang membantu menstabilkan struktur helix pada kolagen. Langkah selanjutnya dalam hidrolisis kolagen adalah pemutusan ikatan intramolekul antara tiga rantai dalam struktur helix menjadi tiga rantai alpha, beta atau gamma.
Perbedaan bentuk utama antara alpha, beta dan gamma terletak pada bobot molekulnya. Bobot molekul struktur alpha antara 80.000-125.000. Untuk struktur beta bobot molekul antara 160.000-250.000 dan rantai gamma memiliki bobot molekul 240.000-375.000 (Poppe, 1992), sedangkan menurut Lehninger (1993), kolagen akan terputus jika terkena asam kuat dan basa kuat dan akan mengalami transformasi dari bentuk untaian tidak larut dan tidak tercerna menjadi gelatin dalam air panas.
Salah satu karakteristik serat kolagen adalah mengkerut/menciut ketika dipanaskan. Suhu pengerutan (Ts) berbeda untuk sumber kolagen dari spesies yang berbeda. Suhu pengerutan untuk kolagen dari kulit mamalia berkisar antara 60-65°C. Ketika kolagen dipanaskan dengan suhu diatas suhu pengerutannya (T>Ts), maka ikatan silang dari rantai triple helix pada kolagen akan terputus dalam jumlah yang sangat besar, sehingga struktur kolagen terpisah menjadi gulungan (coils) secara acak yang larut dalam air dan disebut sebagai gelatin (Belitz dan Grosch, 1999).
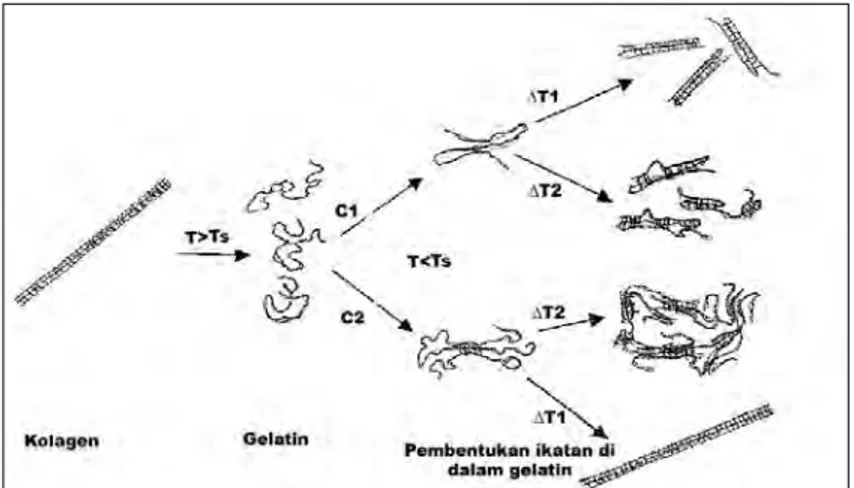
Berdasarkan konsentrasi dan suhu larutan gelatin, perubahan kolagen menjadi gelatin dan gelatin menjadi gel pada suhu rendah (cooling temperature) disajikan pada Gambar 2.
Gambar 2. Perubahan kolagen menjadi gelatin (Belitz dan Grosch, 1999) Pada saat konsentrasi rendah (C1), struktur intramolekuler gelatin akan membentuk untaian/ikatan-ikatan tunggal (single-strands). Pada saat konsentrasi tinggi (C2) dan proses pendinginan berjalan lambat (∆T1), struktur intramolekuler akan membentuk untaian/ikatan-ikatan seperti semula (pada kolagen), pada setiap konsentrasi tinggi dan proses berjalan cepat (∆T2), maka akan dihasilkan segmen-segmen helix dengan ikatan-ikatan secara acak pada setiap struktur gulungannya (coils) (Belitz dan Grosch, 1999).
E. PERUBAHAN GELATIN MENJADI GEL
Gelatin merupakan suatu hidrokoloid, yaitu suatu polimer larut dalam air yang mampu membentuk koloid, mengentalkan larutan atau membentuk gel dari larutan tersebut. Pembentukan gel merupakan suatu fenomena penggabungan atau pengikatan silang rantai-rantai polimer membentuk jalinan tiga dimensi yang kontinyu dan kaku yang tahan terhadap aliran di bawah tekanan. Pada waktu sol dari gelatin mendidih, konsistensinya menjadi lebih kental, dan selanjutnya akan terbentuk gel yang elastis. Pembentukan kristal, diperkirakan karena diagram sinar-X menunjukkan adanya bagian kristalin di
dalam sel gelatin. Molekul-molekul secara individu bergabung dalam lebih dari satu bentuk kristalin membentuk jalinan tiga dimensi yang menjerat cairan (Fardiaz, 1989).
Gaya untuk mengikat molekul-molekul gelatin di dalam gel ini tidak diketahui. Meskipun demikian, ikatan-ikatan hidrogen dan gaya van der waals diperkirakan sebagai pengikatnya, mengingat sifat gel yang mudah mencair dan membentuk gel kembali dengan adanya perubahan suhu (Fardiaz, 1989). E. PROSES PEMBUATAN GELATIN
Gelatin dapat dibuat dengan berbagai bahan baku antar lain kulit dan tulang sapi, kulit domba, kulit sapi, dan tulang (ossein). Tipe gelatin yang dihasilkan dibedakan menjadi dua tipe yaitu tipe A dan tipe B. Gelatin tipe A adalah gelatin yang dihasilkan melalui proses perendaman asam sedangkan gelatin tipe B berasal dari perendaman basa.
Proses utama pembuatan gelatin dibagi dalam tiga tahapan, yaitu persiapan bahan baku berupa penghilangan komponen non kolagen dengan atau tanpa pengurangan ikatan antara komponen kolagen, konversi kolagen menjadi gelatin, pemurnian dan perolehan gelatin dalam bentuk kering. Bahan baku (kulit atau tulang) awalnya dipotong-potong atau diberikan proses pengecilan ukuran. Pengecilan ukuran bahan baku diperlukan untuk memperluas permukaan bahan yang terendam dalam larutan sehingga proses ekstraksi dapat berlangsung lebih cepat dan sempurna (Hinterwaldner, 1977).
Proses pengapuran (liming) dilakukan untuk melunakkan kulit dan menghilangkan albumoid bagian luar seperti globulin, mukopolisakarida, albumin, karoten dan pigmen-pigmen (Glicksman, 1969). Menurut Hinterwaldner (1977), proses liming bertujuan untuk merusak atau memutuskan berbagai ikatan kimia yang masih ada dalam kolagen dan untuk menghilangkan atau mengurangi material lain yang tidak diinginkan, seperti protein lain dan karbohidrat. Selama proses liming, lemak dikonversi menjadi sabun-sabun basa yang terlarut.
Menurut Glicksman (1969), kapur untuk perendaman basa ditambahkan ke dalam air perendam dengan jumlah secukupnya berkisar antara 5 hingga 15
% dari bobot bahan sehingga terbentuk larutan kalsium hidroksida. Proses perendaman kulit dilakukan selama 3-12 minggu atau lebih tergantung pada jenis bahan baku, suhu liming, perlakuan sebelumnya dan kapur yang ditambahkan. Hinterwaldner (1977) menambahkan bahwa suhu proses liming tidak boleh lebih dari 20°C jika ingin menghindari jumlah kolagen yang hilang lebih banyak. Jika suhu liming terlalu rendah, maka proses liming akan berjalan lambat sehingga membutuhkan waktu perendaman yang lebih lama.
Proses liming yang tidak dilakukan dengan tepat dapat menyebabkan kelarutan kolagen dalam basa. Hal ini dapat menurunkan rendemen gelatin yang dihasilkan (Ward dan Courts, 1977). Hinterwaldner (1977) menyatakan bahwa gelatin diperoleh dari bahan setelah perlakuan liming. Bahan tersebut kemudian diekstraksi dengan air pada suhu tertentu. Proses ekstraksi multistage merupakan salah satu proses produksi gelatin yang penting.
Mutu gelatin yang diperoleh dipengaruhi oleh proses konversi (jenis bahan baku dan lama proses ekstraksi). Metode yang digunakan untuk pemutusan ikatan hidrogen dalam ekstraksi gelatin yaitu meningkatkan suhu hingga titik penyusutan dicapai dan merendam kolagen dalam larutan pemutus ikatan hidrogen pada suhu ruang. Proses ekstraksi dilakukan pada suhu 50 oC hingga 100 oC. Tahapan proses ekstraksi kolagen secara bertingkat menjadi gelatin disajikan pada Tabel 6.
Tabel 6. Tahapan proses ekstraksi kolagen secara bertingkat dalam menghasilkan gelatin
Ekstraksi Waktu (jam) Suhu (°OC) Rendemen (%)
1 4-9 55-65 5-10 2 4-9 65-75 3-6 3 4-6 75-85 3-6 4 4-6 85-95 2-4 5 2-4 95-100 1-2 Total 14-28 Sumber : Glicksman (1969)
Menurut Hinterwaldner (1977) ekstraksi pertama biasanya dilakukan pada suhu 50 oC sampai 60 oC, dimana untuk ekstraksi-ekstraksi selanjutnya suhu ekstraksi dinaikkan 5-10oC hingga ekstraksi terakhir suhunya mencapai titik didih air. Ekstraksi dilakukan pada bejana stainless steel dibuka tanpa
tutup. Gillespie (1960) menambahkan degradasi gelatin terjadi sangat lambat pada suhu 30-40°C, dengan peningkatan suhu (suhu di atas 40°C) akan meningkatkan degradasi dan reaksi berlangsung sangat cepat. Menurut The United Stated Patent (1993), total waktu ekstraksi pada keseluruhan ekstraksi biasanya dilakukan pada kisaran waktu 10 sampai 20 jam. Namun sebaiknya dilakukan pada waktu 16 jam atau kurang.
Cara yang digunakan untuk menghilangkan zat-zat lain yang tidak larut yang dapat mengurangi kemurnian gelatin adalah dengan melakukan penyaringan. Filtrasi atau penyaringan larutan koloidal dapat dilakukan dengan pemisahan secara kimiawi maupun pemisahan dengan penyaring. Pemisahan secara kimiawi tidak biasa digunakan karena prosesnya mahal dan dapat menyebabkan kerusakan kualitas larutan gelatin. Proses penyaringan lebih efisien dengan memperhatikan sifat fisiko kimia, endapan-endapan partikel dan suhu. Di bawah suhu 32°C gelatin membentuk gel rigid sehingga kekakuan meningkat dengan peningkatan kandungan padatan filtrasi dilakukan pada suhu tersebut atau di atasnya (Hinterwaldner, 1977).
Hinterwaldner (1977) menyatakan bahwa evaporasi gelatin harus memenuhi ketentuan seperti suhu evaporasi rendah (40-80 oC) , waktu kontak antara larutan gelatin dengan panas singkat dan mencegah pembentukan buih. Suhu yang digunakan harus di atas titik lelehnya dengan menggunakan vacuum.
Menurut Ward dan Courts (1977), proses pengeringan gelatin dapat dilakukan dengan spray maupun roller dryer. Suhu pengeringan dilakukan pada suhu 38 oC hingga 70 oC. Pengeringan merupakan proses yang dilakukan dengan tujuan untuk mengurangi air dalam larutan gelatin.
III. METODE PENELITIAN
A. BAHAN DAN ALAT
Bahan yang digunakan dalam penelitian ini adalah kulit sapi sisa (kulit split) hasil samping industri penyamakan kulit dari PT. Muhara Dwitunggal Laju yang berada di kecamatan Citeureup, Bogor. Bahan kimia yang digunakan antara lain kapur tohor (CaO) untuk proses liming, NH3SO4 untuk netralisasi dan bahan-bahan lain untuk prosedur analisa karakter mutu. Sebagai bahan pembanding pada analisa mutu gelatin digunakan gelatin komersial (impor) tipe B yang diperoleh dari toko Setia Guna di Bogor
Peralatan yang digunakan dibagi menjadi dua bagian yaitu : 1. Peralatan untuk produksi
Terdiri dari drum, alat pemotong kulit, mollen, ekstraktor (Gambar 3), filter vakum, evaporator vakum, chiller, alat ekstrusi, alat pengering, dan blender.
Gambar 3. Ekstraktor 2. Peralatan untuk analisa
Peralatan yang digunakan antara lain desikator, pH meter, chromameter tipe Minolta CR 300, viscometer, termometer, rheoner RE 3305, dan alat-alat lainnya yang digunakan pada prosedur analisa karakter mutu.
B. WAKTU DAN TEMPAT
Penelitian dilakukan pada bulan Maret 2005 hingga bulan Februari 2006. Penelitian dilakukan di Laboratorium Teknologi Agroindustri Badan Pengkajian dan Penerapan Teknologi (LTA-BPPT) yang terletak di kawasan Pusat Penelitian Ilmu Pengetahuan dan Teknologi (PUSPIPTEK), Serpong, Tangerang; dan PT. Muhara Dwitunggal Laju, Kecamatan Citeureup, Bogor. C. METODE PENELITIAN
1. Penelitian Pendahuluan
Aktivitas yang dilakukan pada penelitian pendahuluan adalah menentukan banyaknya tahap, waktu, serta suhu di tiap tahap ekstraksi. Dasar dari penentuan banyaknya tahap ekstraksi adalah pendapat Glicksman (1969) yang menyatakan bahwa proses ekstraksi kolagen menjadi gelatin dilakukan secara bertingkat. Ekstraksi yang dilakukan pada penelitian ini adalah dengan cara mencampur air dengan kulit sapi dengan perbandingan 1: 2. Campuran air dan kulit sapi dimasukkan dalam ekstraktor kemudian dipanaskan secara bertahap.
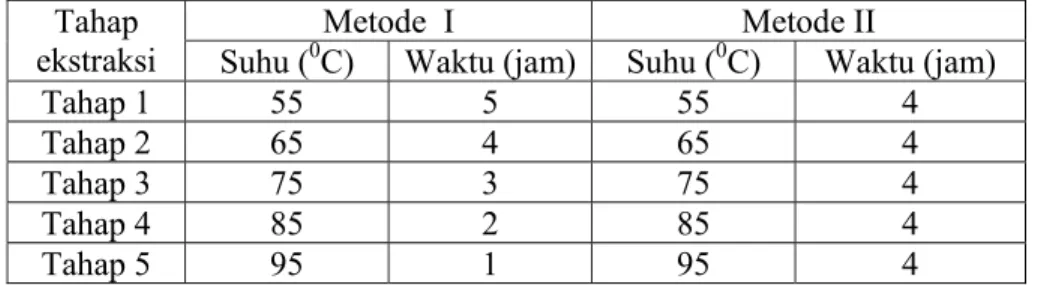
Ekstraksi dilakukan dengan menggunakan dua alternatif metode. Suhu dan waktu yang digunakan di setiap tahap ekstraksi dapat dilihat di Tabel 7.
Tabel 7. Suhu dan waktu yang digunakan di setiap tahap ekstraksi penelitian pendahuluan
Tahap ekstraksi
Metode I Metode II
Suhu (0C) Waktu (jam) Suhu (0C) Waktu (jam)
Tahap 1 55 5 55 4
Tahap 2 65 4 65 4
Tahap 3 75 3 75 4
Tahap 4 85 2 85 4
Tahap 5 95 1 95 4
Melalui dua alternatif metode ini dicari metode yang menghasilkan rendemen gelatin yang tertinggi. Pemberian agitasi dilakukan dengan menggunakan agitator yang digerakkan oleh motor.
2. Penelitian Utama
Aktivitas yang dilakukan pada penelitian utama adalah mengolah kulit sapi yang sudah disiapkan kemudian diproses hingga didapatkan bubuk gelatin kering. Langkah pertama dalam mengolah kulit sapi adalah melakukan pengecilan ukuran. Proses pengecilan ukuran (7 x 10 cm2) dilakukan untuk memudahkan proses pencucian dan perendaman kulit. Proses perendaman (liming) dilakukan agar serabut-serabut kolagen berubah menjadi serat-serat yang lebih kecil sehingga kulit menjadi longgar. Proses perendaman dilakukan selama enam minggu melalui perendaman kulit di dalam 300 % air. Hal ini berdasarkan penelitian yang telah dilakukan oleh Harijatmoko (2004), proses perendaman enam minggu dengan dosis kapur tohor 15 % dapat menghasilkan rendemen gelatin terbaik.
Langkah berikutnya adalah proses deliming yang dilakukan dengan cara merendam kulit selama tiga jam di dalam 300 % air dan amonium sulfat 2 % (persentase dihitung berdasarkan bobot kulit split basah yang telah dilakukan pengecilan ukuran). Proses deliming dilakukan untuk menghilangkan kapur yang telah terikat dengan kulit secara kimia dan untuk menghilangkan pembekuan akibat dari pengapuran.
Langkah selanjutnya adalah proses ekstraksi bertingkat. Berdasarkan hasil penelitian pendahuluan metode ekstraksi yang digunakan adalah metode pertama yang dilakukan dalam lima tahap dengan suhu dan waktu masing-masing; 55 OC - 5 jam, 65 OC - 4 jam, 75 OC - 3 jam, 85 OC - 2 jam, dan 95 OC - 1 jam. Ekstraksi dilakukan dengan empat perbedaan perbandingan kulit-air; 1:1, 1:2, 1:3, dan 1:4, serta tiga interval agitasi yang berbeda yaitu tiap 10 menit, 20 menit, dan 30 menit, dengan kecepatan serta lama berputar masing-masing 50 rpm dan 3 menit.
Filtrat diperoleh melalui filtrasi vakum secara bertahap dengan ukuran filter 150 mesh. Proses selanjutnya adalah proses pemekatan dengan evaporasi dengan menggunakan evaporator vakum pada suhu 57°OC dan tekanan -73 cmHg sampai kepekatannya mencapai kisaran 10 % dari volume semula. Filtrat yang telah pekat kemudian disimpan dalam
Pencucian
Chilling Filtrasi
Penggilingan
Butiran gelatin
Analisa Mutu Produk Pengeringan
Ekstrusi
Dosis kapur tohor : 15 % lama perendaman 6 minggu Netralisasi
Kulit split
Liming (Penngapuran) Pengecilan ukuran
Ekstraksi (air dan kulit) PERLAKUAN Perbandingan kulit-air : 1:1, 1:2, 1:3, dan 1:4 Interval agitasi:10 menit, 20 menit,dan 30 menit Evaporasi NH3SO4 2 %
Gambar 4. Diagram alir proses pembuatan gelatin dari kulit sapi
pendingin (chiller) selama 30 menit agar filtrat tersebut menjadi gel. Filtrat gelatin dalam bentuk gel diperlukan agar proses ekstrusi dapat dilakukan dengan baik. Proses ekstrusi dilakukan dengan alat ekstrusi hingga didapatkan gelatin dalam bentuk seperti mie. Gelatin yang telah diekstrusi kemudian dikeringkan dengan alat pengering tipe rak yang dilakukan pada 30 OC kemudian meningkat secara bertahap hingga suhu tertinggi 75°OC sampai diperoleh gelatin kering dengan kadar air kurang lebih 16 %. Selanjutnya dilakukan proses penggilingan (grinding) sehingga diperoleh gelatin kering dalam bentuk butiran–butiran halus. Parameter yang diukur antara lain; rendemen, kadar air, kadar abu, warna, kekuatan gel, viskositas, dan stabilitas emulsi. Diagram alir proses pembuatan gelatin dari kulit sapi disajikan pada Gambar 4.
Prosedur Analisa Karakter Mutu
1. Rendemen (Association of Offical Analytical Chemists, 1995)
Rendemen diperoleh dari perbandingan bobot kering gelatin (setelah dikurangi kadar air) yang dihasilkan dengan bobot kulit yang digunakan dengan rumus sebagai berikut:
Bobot kering gelatin
Rendemen (%) = x100% Bobot kulit yang digunakan
2. Warna (Soekarto, 1990)
Warna ditentukan menggunakan chromameter dengan sistem Hunter, yaitu dicirikan tiga notasi warna, yaitu L, a dan b (tetapi yang diamati pada penelitian ini hanya notasi L dan b). Notasi L merupakan notasi yang menyatakan tingkat kecerahan (light) dan memiliki nilai dari 0 (hitam) sampai 100 (putih). Notasi b menyatakan warna kromatik campuran biru-kuning, dengan nilai +b (positif) dari 0 sampai +70 untuk warna kuning dan nilai –b (negatif) dari 0 sampai -70 untuk warna biru. Sejumlah contoh gelatin hasil penelitian ditempatkan pada satu wadah yang merupakan bagian dari alat chromameter. Contoh ditempatkan pada wadah hingga menutupi semua permukaan dasar dari wadah tersebut. Contoh kemudian diukur menggunakan chromameter. Hasil pengukuran notasi warna gelatin akan tercetak dan menunjukkan nilai notasi L dan b dari gelatin hasil penelitian.
3. Kadar Air (Association of Offical Analytical Chemists, 1995)
Cawan porselen dikeringkan pada suhu 105 OC selama 1 jam, kemudian didinginkan dan ditimbang. Contoh yang akan ditentukan kadar airnya ditimbang sebanyak 5 gram. Cawan yang telah berisi contoh dimasukkan dalam oven bersuhu 105OC sampai bobotnya konstan (24 jam). Kadar air dihitung berdasarkan persamaan berikut :
B - A
Kadar air = x 100 % Bobot contoh basah
Keterangan : A = Bobot cawan + contoh kering (g) B = Bobot cawan + contoh basah (g)
4. Kadar Abu (Association of Offical Analytical Chemists, 1995)
Contoh yang telah diuapkan airnya dimasukkan ke dalam tanur bersuhu 600°C. Sebelumnya bobot cawan kering dan bobot contoh telah diketahui. Proses pembakaran dilakukan sampai semua bahan berubah menjadi abu ( sekitar 6 jam), kemudian hasilnya ditimbang.
A
Kadar abu = x 100 % B
Keterangan : A = Bobot contoh akhir (g) B = Bobot contoh awal (g) 5. Kekuatan Gel (British Standard 757,1975)
Contoh sebannyak 6,67 gram dilarutkan dalam aquades pada labu takar sampai mencapai volume 100 ml, kemudian larutan diambil sebanyak 10ml dan dipindahkan dalam gelas piala 25 ml dan didinginkan pada suhu 10°C dengan kisaran lama antara 15 hingga 19 jam. Selanjutnya hasilnya dianalisa menggunakan Voland Steven Texture Analyzer. Hasil dari pengukuran berupa grafik dan diamati tinggi kurva sebelum pecah serta berat beban yang tercatat pada alat saat contoh pecah. Kekuatan gel ditentukan dari grafik yang diperoleh. Rumus untuk menentukan kekuatannya adalah sebagai berikut :
A x B
Kekuatan gel (Bloom) = x 98,07 x 2,86 x 10-3 C
Keterangan : A = Tinggi kurva sebelum patah B = Bobot penekan (gram)
C = Luas permukaan penekan (cm2) 6. Viskositas (British Standard 757, 1975)
Contoh sebanyak 6,67 gram dilarutkan dalam aquades pada labu takar sampai mencapai volume 100 ml, kemudian dipanaskan pada suhu 60°C. Viskositasnya diukur dengan menggunakan spindle nomer 2 dan kecepatan putarnya 60 rpm. Viskositasnya (cP) adalah 5 (faktor konversi) dikalikan dengan angka hasil pengukuran.
7. Stabilitas Emulsi (Sathe dan Salunkhe, 1981)
Sebanyak 10 gram contoh disuspensikan dalam 100 ml aquades. Setelah itu ditambahkan air sampai 150 ml dan minyak jagung sebanyak 150 ml, kemudian diblender selama dua menit. Hasilnya dituang dalam tabung sentrifuse dan dipanaskan pada suhu 80°C selama 30 menit, selanjutnya didinginkan dan disentrifuse pada 1400 rpm selama 30 menit. Fase yang sudah tidak membentuk emulsi dipisahkan kemudian bahan ditimbang. Stabilitas emulsi dinyatakan sebagai campuran yang masih membentuk emulsi setelah mengalami pemanasan dan dihitung dengan menggunakan rumus:
Bobot fase yang tersisa
Stabilitas Emulsi (SE) = x 100 % Bobot total bahan emulsi
IV. HASIL DAN PEMBAHASAN
A. PENELITIAN PENDAHULUAN
Penelitian ini menggunakan bahan baku kulit sapi yang sebelumnya telah mengalami proses pengepressan (buang daging), perendaman, pengapuran (liming) dan pembelahan (splitting). Proses pembelahan ini merupakan pembelahan kulit menjadi dua lapisan atau lebih untuk mendapatkan tebal yang dikehendaki.
Setelah kulit sapi dinilai siap, kulit sapi kemudian diekstraksi dengan dua alternatif metode. Metode pertama ekstraksi dilakukan dengan suhu dan waktu masing-masing 55 OC - 5 jam, 65 OC – 4 jam, 75 OC – 3 jam, 85 OC – 2 jam, dan 95 OC – 1 jam. Metode ini menghabiskan waktu proses selama 15 jam. Metode kedua dilakukan dengan suhu dan waktu masing-masing 55 OC - 4 jam, 65 OC – 4 jam, 75 OC – 4 jam, dan 85 OC – 4 jam. Total waktu untuk metode kedua ini adalah 16 jam. Selama proses ekstraksi berlangsung, secara berkala diberikan agitasi menggunakan agitator yang disambungkan pada motor pemutar.
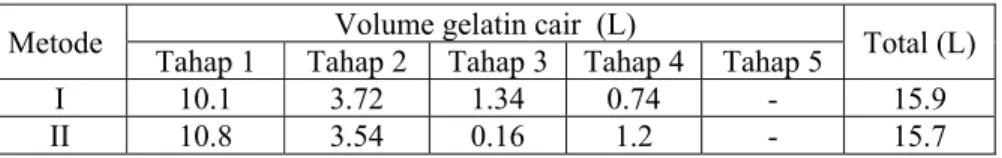
Hasil pengukuran pada volume filtrat ekstraksi menentukan metode mana yang dipilih sebagai metode ekstraksi pada penelitian utama. Dari dua proses ekstraksi dengan perbandingan kulit-air yang sama, volume filtrat yang lebih banyak diyakini memberikan rendemen yang lebih banyak. Tabel 8 menunjukkan bahwa metode pertama dengan volume filtrat sebanyak 15.9 L lebih memungkinkan untuk dipilih sebagai metode ekstraksi di penelitian utama dibandingkan dengan metode kedua yang hanya menghasilkan volume filtrat sebanyak 15.7 L.
Tabel 8. Volume filtrat ekstraksi pada penelitian pendahuluan
Metode Volume gelatin cair (L) Total (L)
Tahap 1 Tahap 2 Tahap 3 Tahap 4 Tahap 5
I 10.1 3.72 1.34 0.74 - 15.9
0 2 4 6 8 10 12 14 1 2 3 4 perbandingan kulit-air re nde m e n ( % )
agitasi 10' agitasi 20' agitasi 30'
B. PENELITIAN UTAMA
Informasi yang didapatkan dari penelitian pendahuluan kemudian dijadikan panduan untuk melakukan penelitian utama. Kulit sapi yang sudah disiapkan untuk bahan baku penelitian utama kemudian diproses sesuai dengan metode penelitian pendahuluan hingga didapatkan bubuk gelatin kering. Gelatin yang sudah didapatkan dari penelitian ini kemudian dianalisa beberapa karakteristiknya antara lain ; rendemen, warna (notasi L dan b), kadar air, kadar abu, kekuatan gel, viskositas, dan stabilitas emulsi.
1.Rendemen
Rendemen merupakan salah satu parameter untuk mengukur efisiensi dan efektifitas proses ekstraksi yang dilakukan. Kecenderungan naik turunnya nilai rendemen sampel gelatin hasil penelitian disajikan pada Gambar 5.
Gambar 5. Pengaruh perbandingan kulit-air dan interval agitasi terhadap rendemen gelatin sampel
Gambar 5 menunjukkan ekstraksi gelatin dengan interval agitasi setiap 10 dan 20 menit sekali mempunyai nilai rendemen yang semakin meningkat seiring dengan bertambahnya jumlah air yang ditambahkan. Dengan kata lain semakin banyak air yang ditambahkan, rendemen gelatin yang diperoleh semakin tinggi. Hal ini dikarenakan lebih banyak air yang
dapat mengikat ekstrak gelatin yang tertinggal dalam kapiler-kapiler kulit. Gaya adhesi kapiler-kapiler kulit dapat menyebabkan ekstrak gelatin tertinggal di dalamnya selama proses ekstraksi berlangsung (Handojo, 1995).
Namun peningkatan nilai rendemen ini tidak terjadi pada ekstraksi yang dilakukan dengan interval agitasi tiap 30 menit. Penambahan jumlah air tidak menambah jumlah rendemen gelatin. Terdapat nilai rendemen yang rendah dari dua sampel (lampiran 1). Nilai ini dipengaruhi oleh proses pembuatan gelatin selanjutnya yaitu proses pengeringan. Panas yang diberikan oleh alat pengering membuat sampel gelatin khususnya yang masih mempunyai kadar air yang masih tinggi mencair kembali. Gelatin yang mencair akhirnya masuk dan mengering di antara sela-sela kawat wadah. Gelatin yang mengering ini pada akhirnya sulit untuk diambil dan ditimbang.
Pengamatan pada pengaruh agitasi terhadap nilai rendemen menunjukkan bahwa perbedaan interval agitasi tidak memberikan kecenderungan khusus (naik atau turun) pada nilai rendemen. Tidak seperti yang diduga sebelumnya bahwa pemberian agitasi yang semakin sering memberikan nilai rendemen yang lebih tinggi. Hal ini diduga karena selama proses ekstraksi berlangsung, agitator sering mengalami bongkar pasang. Hal ini menyebabkan posisi agitator tidak persis sama dalam setiap proses ekstraksi. Posisi yang tidak persis sama ini mempengaruhi jumlah kulit yang ikut berputar bersama air sehingga mempengaruhi jumlah rendemen gelatin.
2. Warna
Warna memiliki peranan yang penting dalam komoditas pangan dan hasil pertanian lainnya. Karakteristik warna sangat penting sebagai daya tarik, tanda pengenal dan atribut mutu. Salah satu cara untuk mengukur warna adalah menggunakan alat yang disebut dengan chromameter. Pengukuran menggunakan alat ini menghasilkan tiga notasi yang biasa dikenal dengan notasi L, a, dan b. Angka-angka ini kemudian dibandingkan
53 54 55 56 57 58 59 60 1 2 3 4 perbandingan kulit-air n ila i n o ta s i L
agitasi 10' agitasi 20' agitasi 30'
dengan komponen-komponen warna dalam diagram uji warna seperti terdapat dalam Lampiran 2. Penelitian ini hanya mengukur notasi L dan notasi b. Notasi a tidak dilakukan pengukuran dikarenakan notasi ini menunjukkan spektrum warna hijau dan merah, dua warna yang tidak pernah ditemukan pada sampel gelatin pada umumnya.
Nilai L merupakan parameter yang menunjukkan cahaya pantul yang menghasilkan warna akromatik putih, abu-abu, dan hitam (Soekarto, 1990). Paramater ini memperlihatkan tingkat kecerahan (light) dari suatu bahan dengan kisaran dari 0 (hitam) sampai 100 (putih). Larutan encer gelatin kualitas tinggi tidak berwarna, sedangkan gelatin kualitas rendah memiliki warna coklat kejinggaan.
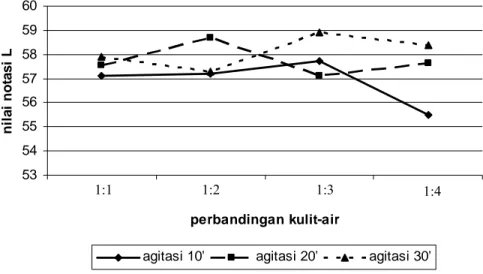
Kisaran rata-rata notasi L gelatin sampel yang didapatkan dari penelitian ini adalah 55,49 - 58,90, tidak jauh berbeda tingkat kecerahannya dengan notasi L pada gelatin komersial yang tercatat sebesar 56,36 (Lampiran 3). Pengaruh perbandingan kulit-air serta interval agitasi terhadap nilai rata-rata notasi L pada gelatin hasil penelitian ini dapat dilihat di Gambar 6. .
Gambar 6. Pengaruh perbandingan kulit-air dan interval agitasi terhadap notasi L sampel gelatin.
Hasil pengamatan menunjukkan bahwa perbandingan kulit-air dan interval agitasi tidak memberikan kecenderungan nilai naik atau turun pada tingkat kecerahan sampel gelatin. Perbandingan kulit-air yang semakin besar diharapkan dapat memberikan nilai kecerahan yang lebih baik dengan lebih banyaknya gelatin yang ikut terekstrak. Hal tersebut tidak terjadi pada empat tingkat perbandingan kulit-air yang dilakukan pada penelitian ini. Hal ini dimungkinkan terjadi karena selama proses ekstraksi berlangsung, bukan saja gelatin yang terekstrak namun juga zat-zat pengotor lain ikut pula terekstrak. Menurut Arthadana (2001) kejernihan warna gelatin tergantung pada kemampuan zat-zat pengotor yang ada untuk memancarkan cahaya, terutama keberadaan ion logam pada bahan dapat mempengaruhi warna gelatin yang dihasilkan. Semakin banyaknya air yang ditambahkan semakin besar peluang zat-zat pengotor ikut dalam filtrat gelatin.
Begitu pula dengan pengaruh agitasi pada tingkat kecerahan sampel gelatin. Proses agitasi yang diharapkan dapat membantu untuk mengektrak gelatin dengan lebih baik, ternyata mempunyai efek samping. Agitasi yang diberikan tidak saja mengekstrak gelatin, namun juga membuat komponen-komponen non kolagen ikut terekstrak sehingga mempengaruhi tingkat kecerahan. Semakin sering agitasi diberikan, peluang komponen-komponen non kolagen ikut serta dalam filtrat lebih besar. Banyaknya komponen-komponen non kolagen yang ikut terekstrak sangat dipengaruhi jumlah komponen-komponen tersebut dalam bahan baku kulit yang digunakan.
Notasi b menyatakan warna kromatik campuran biru dan kuning dengan nilai b positif sampai +60 untuk warna kuning dan nilai b negatif dari 0 sampai -60 untuk warna biru. Warna gelatin dapat dipengaruhi oleh bahan baku yang digunakan, metode pembuatan dan jumlah ekstraksi (Glicksman, 1969). Gelatin dari kulit babi mempunyai warna yang lebih cerah jika dibandingkan dengan gelatin dari tulang paupun kulit sapi. Larutan encer gelatin kualitas tinggi tidak berwarna, sedangkan gelatin kualitas rendah memiliki warna coklat kejinggaan.
38,5 39 39,5 40 40,5 41 41,5 42 1 2 3 4 perbandingan kulit-air n ila i n o ta s i b
agitasi 10' agitasi 20' agitasi 30'
Nilai rata-rata untuk notasi b yang didapatkan dari pengukuran gelatin hasil penelitian berkisar antara 39,74 sampai 41,68, semua menunjukkan nilai positif (Lampiran 4). Kisaran nilai tersebut menunjukkan bahwa warna gelatin hasil penelitian penelitian mengarah pada warna kuning.
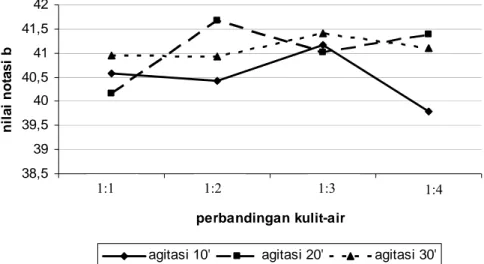
Kecenderungan naik turunnya nilai notasi b sampel gelatin hasil penelitian disajikan pada Gambar 7. Kedua perlakuan yaitu perbandingan kulit-air dan interval agitasi ternyata tidak memberikan pola tertentu pada nilai notasi b sampel gelatin. Adanya komponen-komponen non gelatin yang turut serta dalam filtrat mempengaruhi nilai notasi b. Perbandingan kulit-air yang semakin besar ternyata tidak selalu memberikan nilai notasi b yang selalu lebih tinggi (warna lebih kuning) seperti dugaan semula. Perbandingan kulit-air yang semakin besar juga dapat menurunkan nilai notasi b dikarenakan adanya komponen-komponen non gelatin dalam filtrat. Komponen ini memberikan peluang yang semakin besar terhadap terjadinya warna kuning yang semakin tua.
Gambar 7. Pengaruh perbandingan kulit-air dan interval agitasi terhadap notasi b sampel gelatin.
Agitasi yang diberikan tidak memberikan pengaruh khusus pada nilai notasi b. Kondisi fisik bahan baku kulit diduga menjadi penyebab hal ini terjadi. Kondisi fisik kulit yang terlalu lembek, menjadikan kulit tersebut
lebih mudah untuk terkoyak karena adanya agitasi. Kulit dengan kondisi yang terlalu lembek, semakin sering agitasi itu diberikan semakin banyak serpihan-serpihan kulit yang terkoyak dan bercampur dalam filtrat gelatin. Serpihan-serpihan ini menyebabkan warna kuning gelatin semakin tua.
Perbandingan warna sampel gelatin yang dihasilkan dari penelitian ini dibandingkan dengan gelatin komersial dapat dilihat di Gambar 8.
Gambar 8. Bubuk sampel gelatin Keterangan :
Dari atas : kiri-kanan : A1B1, A1B2, A1B3, A1B4, A2B1, A2B2, A2B3, A2B4, A3B1, A3B2, A3B3, A3B4, Komersial, A4B1, A4B2, A4B3, A4B4.
3. Kadar Air
Kadar air diketahui sebagai persentase air yang terikat oleh suatu bahan terhadap berat kering setelah dioven. Kandungan air suatu bahan menentukan penampakan, tekstur, dan kemampuan bahan tersebut terhadap kerusakan yang disebabkan oleh mikroba yang dinyatakan dengan aw, yaitu jumlah air bebas yang dapat dimanfaatkan oleh mikroba untuk pertumbuhannya. Air pada suatu bahan dapat digolongkan menjadi beberapa macam dengan karakteristiknya masing-masing.
Air bebas merupakan air yang secara fisik terikat dalam jaringan matriks bahan seperti membran, kapiler, serat dan lain-lain. Air tipe ini cenderung mudah diuapkan. Air bebas juga dapat dimanfaatkan untuk
0 2 4 6 8 10 12 14 0 1 2 3 4 perbandingan kulit-air k a da r a ir ( % bk )
agitasi 10' agitasi 20' agitasi 30'
pertumbuhan mikroba dan media bagi reaksi-reaksi kimiawi. Selain air bebas, ditemukan juga jenis air terikat (bound water), air tipe ini sulit diuapkan dan dipisahkan karena terikat kuat dengan komponen lain dalam bahan tersebut. Air yang terikat secara fisis adalah bagian air yang terdapat dalam tenunan bahan karena adanya ikatan-ikatan garis. Air yang terikat secara kimia terdiri dari bagian air yang terdapat dalam bahan dan terikat dalam susunan kimia (Setijahartini, 1985).
Kadar air sampel gelatin penelitian ini berkisar antara 8,82 % (bk) hingga 12,74 % (bk) (Lampiran 5). Nilai ini lebih rendah dibandingkan dengan nilai kadar air gelatin gelatin komersial yaitu 15,20 %. Nilai tersebut secara keseluruhan masih memenuhi standar yang telah ditetapkan oleh Dewan Standar Indonesia (1995), yaitu <16 %.
Gambar 9 menunjukkan bahwa perbandingan kulit-air tidak memberikan pengaruh yang jelas pada nilai kadar air gelatin. Hanya ekstraksi sampel gelatin pada agitasi setiap 30 menit sekali yang menunjukkan nilai kadar air yang semakin meningkat seiring dengan penambahan jumlah air. Menurut Clarks dan Courts (1977), rantai asam amino berikatan dengan rantai asam amino lainnya secara acak dengan menjerat air di dalam ikatan tersebut sehingga kadar air di dalam gelatin menjadi lebih tinggi. Dengan kata lain, semakin banyak molekul gelatin yang dapat terekstrak semakin besar jumlah air yang dapat terikat.
Gambar 9. Pengaruh perbandingan kulit-air dan interval agitasi terhadap kadar air sampel gelatin
Perlakuan agitasi juga tidak memberikan kecenderungan tertentu pada nilai kadar air sampel gelatin. Molekul-molekul gelatin dalam kulit seharusnya dapat terekstrak lebih optimal dengan semakin seringnya diberikan agitasi. Namun dari penelitian ini, hal tersebut tidak sepenuhnya terjadi.
Nilai kadar air sampel gelatin hasil penelitian yang cenderung naik turun ini diduga dipengaruhi oleh proses evaporasi dan pengeringan yang dilakukan. Rendahnya efisiensi kedua alat mempengaruhi nilai kadar air sampel gelatin yang didapatkan. Pada saat proses evaporasi dan pengeringan jumlah air yang teruapkan tidak dapat ditetapkan dengan tepat dikarenakan keterbatasan kerja alat.
4. Kadar Abu
Kadar abu suatu bahan dapat menunjukkan kemurnian suatu bahan. Metode pembuatan dan bahan kimia pendukung (non organik) yang digunakan selama proses pembuatan gelatin akan mempengaruhi kadar abu di dalam gelatin. Metode pembuatan gelatin melalui proses basa akan meninggalkan residu berupa mineral-mineral tertentu sesuai dengan bahan kimia yang digunakan.
Air digunakan sebagai pengekstrak dalam proses ekstraksi gelatin. Sampai titik tertentu semakin banyak air yang digunakan maka semakin banyak molekul gelatin yang dapat terekstrak. Namun semakin banyak air yang digunakan dapat juga meningkatkan jumlah mineral yang ikut dalam filtrat. Agitasi pada dasarnya ditujukan untuk menambah jumlah molekul gelatin yang dapat terekstrak. Namun pada pelaksanaannya, agitasi bisa juga menambah jumlah mineral yang terekstrak dari kulit. Semakin sering agitasi itu diberikan (interval semakin kecil), kemungkinan mineral yang terekstrak juga semakin besar.
Gelatin yang diperoleh pada penelitian ini mempunyai kadar abu berkisar antara 2,89-3,89 (% bk) (Lampiran 6). Perbandingan air yang semakin besar tidak selalu memberikan nilai kadar abu yang lebih tinggi. Hal ini dipengaruhi oleh proses perendaman (liming) dan proses netralisasi yang
0 0.5 1 1.5 2 2.5 3 3.5 4 4.5 0 1 2 3 4 perbandingan kulit-air k a da r a bu ( % bk )
agitasi 10' agitasi 20' agitasi 30'
dilakukan. Perbandingan air yang lebih sedikit namun menghasilkan nilai kadar abu yang lebih tinggi diduga disebabkan karena kulit yang digunakan terendam selama proses liming berada di posisi terbawah sehingga lebih banyak kapur yang masuk dalam kapiler-kapiler kulit. Proses netralisasi yang tidak sempurna juga turut serta mempengaruhi pengukuran nilai kadar abu ini. Pengaruh perbandingan kulit-air terhadap nilai kadar abu sample gelatin dapat dilihat di Gambar 10.
Gambar 10. Pengaruh perbandingan kulit-air dan interval agitasi terhadap kadar abu sampel gelatin
Agitasi yang semakin sering diberikan, namun memberikan nilai kadar abu yang lebih sedikit bisa dikarenakan jumlah mineral yang terdapat pada sampel yang digunakan memang sedikit. Optimalisasi proses perendaman (liming) dan netralisasi menjadi hal yang menentukan.
5. Kekuatan Gel
Sifat gelatin yang sering dimanfaatkan oleh industri pangan adalah kemampuannya untuk membentuk gel yang reversible. Sifat ini yang membedakan gelatin dengan gel hidrokoloid lainnya seperti pektin yang bersifat irreversible. Kekuatan gel merupakan sebuah satuan yang
0 50 100 150 200 250 300 1 2 3 4 perbandingan kulit-air ke ku at a n g e l ( b lo o m )
agitasi 10' agitasi 20' agitasi 30'
menunjukkan tingkat kekuatan formasi yang terbentuk jika diberi beban tertentu.
Menurut Glicksman (1969) formasi gel terbentuk karena adanya ikatan hidrogen pada struktur molekulnya sehingga terbentuk formasi semikoloid gel dengan air. Hal ini sangat dipengaruhi oleh susunan asam amino pada gelatin. Stanby (1977) juga menyebutkan bahwa kekuatan gel gelatin dipengaruhi oleh kondisi asam amino penyusunnya terutama panjang rantai asam aminonya.
Beberapa hal yang dapat mempengaruhi nilai kekuatan gel dari gelatin antara lain pH, senyawa elektrolit dan non elektrolitnya. Pendapat lain disampaikan oleh King (1969) yang menyebutkan bahwa kekuatan gel dapat dipengaruhi oleh pH, keberadaan asam, basa, panas, dan enzim proteolitik. Hal-hal tersebut dapat mempengaruhi pembentukan gel.
Pengukuran nilai kekuatan gel dari gelatin sampel menghasilkan kisaran kekuatan gel antara 72,5 sampai 225 Bloom, masih lebih rendah jika dibandingkan dengan kekuatan gel dari gelatin komersial yang terukur sebesar 205 Bloom (Lampiran 7). Namun nilai gelatin sampel tersebut masih memenuhi kriteria berdasarkan British Standar yang memberikan kisaran kekuatan gel gelatin antara 50 hingga 300 Bloom. Kekuatan gel sampel gelatin dengan perbandingan air 1:3 dan 1:4 cenderung mempunyai nilai yang rendah (Gambar 11).
Gambar 11. Pengaruh perbandingan kulit-air dan interval agitasi terhadap kekuatan gel sampel gelatin
Selama proses ekstraksi berlangsung terjadi hidrolisis kolagen menjadi gelatin oleh air. Semakin banyak air yang ditambahkan maka diharapkan semakin banyak kolagen yang dapat terhidrolisis menjadi gelatin kemudian terekstrak. Jumlah gelatin yang terekstrak ini menentukan kekuatan gel dari sampel gelatin kering. Gambar 11 menunjukkan pengaruh jumlah air yang ditambahkan dengan nilai kekuatan gel sampel gelatin.
Dari gambar terlihat bahwa semakin banyak air yang ditambahkan tidak selalu menghasilkan nilai kekuatan gel yang lebih tinggi. Hal ini bisa disebabkan oleh mineral yang terdapat dalam sampel tersebut. Mineral-mineral terebut dapat saja menghambat hidrolisis kolagen menjadi gelatin. Hal ini mengurangi jumlah gelatin yang terekstrak, dengan sendirinya kekuatan gel menurun.
Gelatin dalam filtrat hasil ekstraksi diyakini bertambah jumlahnya jika ditambahkan proses agitasi dalam proses ekstraksi. Semakin sering agitasi diberikan diharapkan semakin besar nilai kekuatan gel sampel gelatin. Hal ini terjadi pada sampel-sampel gelatin hasil penelitian yang didapatkan dari ekstraksi menggunakan perbandingan kulit-air 1 :3 dan 1 :4. Namun pemberian agitasi yang semakin sering ternyata tidak selalu memberikan nilai kekuatan gel yang lebih tinggi. Hal ini terjadi pada ekstraksi yang dilakukan dengan tingkat perbandingan 1: 1 dan 1:2.
Ada sampel dimana saat diberikan agitasi yang lebih banyak (interval lebih sempit) didapatkan nilai kekuatan gel yang lebih rendah. Hal ini terjadi karena sampel-sampel tersebut mempunyai nilai kadar abu yang lebih tinggi dibandingkan sampel yang diberikan agitasi lebih sedikit pada perbandingan kulit-air yang sama. Hal inilah yang menyebabkan kecenderungan nilai kekuatan gel sampel gelatin perbandingan 1 :1 dan 1: 2 mengalami naik turun. United States Patent (1999) menggolongkan mutu gelatin menjadi tiga kelas berdasarkan kekuatan gelnya. Gelatin dengan kekuatan gel >240 bloom termasuk gelatin kualitas tinggi, gelatin dengan kekuatan gel 120-240 termasuk gelatin kualitas sedang, dan gelatin dengan kekuatan gel < 120 bloom termasuk gelatin kualitas rendah.