Abstrak—Pengendalian pH merupakan proses titrasi antara asam dan basa. Proses titrasi asam dan basa adalah gabungan dari dua model, yaitu model statik dan model dinamik. Model statik dibentuk dari hukum kesetimbangan muatan ion berdasarkan reaksi invarian, sedangkan model dinamik dipengaruhi oleh tempat terjadinya reaksi antara asam dan basa. Penelitian ini bertujuan untuk mendesain proses pengendalian titrasi asam-basa reaksi invariant. Sebagai pemodelan reaksinya adalah asam lemah H2
θ
S dengan basa kuat NaOH. Tempat terjadinya pengamatan adalah unit pengolah limbah gas, khususnya di bagian Observation Bassin. Sistem kendalinya menggunakan pengendalian Adaptive controljenis Model Refference Adaptive Control dikarenakan respon sistem proses titrasi asam-basa yang nonlinier. Parameter proses (a1,a2,b1,b2) diestimasi menggunakan Least Square Method, parameter proses dan parameter plant referensi (Ym) digunakan untuk menala PID Pengendali menggunakan algoritma Minimum Variance. Dari hasil simulasi baik open loop dan closed loop, perbedaan nilai pH yang dihasilkan olehAdaptive controladalah 0.00015, untuk laju aliran basa berbeda sekitar 1.34125x10-6
Kata Kunci—kontrol adaptif, variansi minimum, pH, PID . Nilai error untuk adaptive control baik pada uji setpoint dan noise sebesar 0.0003 sedangkan untuk PID pengendali sebesar 0.0004.
I. PENDAHULUAN
ndustri-industri eksplorasi minyak dan gas yang terdapat di daerah Jawa Timur sangat memperhatikan proses pengolahan limbah, dikarenakan unsur sulfur termasuk gas keluaran dari proses di industri yang berbahaya bagi makhluk hidup dan membuat karat atau korosi pada material unit-unit produksi pada industri tersebut. Untuk mengurangi dampak yang diakibatkan oleh gas sulfur tersebut, maka dilakukanlah sebuah penanganan agar kadar surfur menjadi netral. Salah satunya adalah dengan proses penetralan.
Umumnya sering ditemui pada proses penetralan pH di industri dilakukan secara manual oleh operator dengan cara buka tutup katup kendali secara manual. Terkadang jenis pengendali yang digunakan tergolong pengendali tradisional.Pengendali biasa tidak bisa mengikuti perubahan-perubahan yang terjadi saat proses sedang berlangsung karena memiliki parameter yang tetap. Oleh karena itu, diperlukan pengendalian yang secara sendiri dapat menyesuaikan parameter saat proses sedang berlangsung.
Dalam hal ini, pengendali yang digunakan untuk mengendalikan proses penetralan pH adalah jenis adaptif dengan metode minimum variance. Penggunaan metode ini digunakan dengan maksud untuk dapat mengatasi karakteristik pH yang nonlinier dengan menggunakan
minimum variance sebagai estimator.
II. METODOLOGIPENELITIAN
A. Pemodelan Plant
1. Pemodelan Statik Proses Pencampuran
Reaksi disosiasi asam lemah dan basa kuat yang terjadi dapat dijabarkan seperti berikut:
𝐻𝐻2𝑆𝑆+ 2𝐻𝐻2𝑂𝑂 → 𝑆𝑆𝑂𝑂2+ 3𝐻𝐻2 (1)
Berdasarkan reaksi kesetimbangan pada persamaan (1), karena gas hasil dari proses di scrubber tersebut masih bersifat asam lemah, maka perlu ditambahkan larutan NaOH sebagai penetral, sehingga reaksi kesetimbangannya seperti di bawah ini:
𝑆𝑆𝑂𝑂2+ 3𝐻𝐻2+ 2𝑁𝑁𝑁𝑁𝑂𝑂𝐻𝐻 → 𝑁𝑁𝑁𝑁2𝑆𝑆+𝐻𝐻2𝑂𝑂 (2)
Berdasarkan eksperimen [1], reaksi kimia yang terjadi pada sistem adalah: 𝐾𝐾𝑁𝑁1=[𝐻𝐻𝑆𝑆 −][𝐻𝐻+] [𝐻𝐻2𝑆𝑆] (3) 𝐾𝐾𝑁𝑁2=[𝑆𝑆 2−][𝐻𝐻+] [𝐻𝐻𝑆𝑆−] (4)
Pemodelan kesetimbangan kimia dilakukan dengan konsep dari reaksi invarian [2]. Pada sistem ini, ada dua reaksi invariant yang melibatkan aliran input, yaitu:
𝑊𝑊𝑁𝑁 = [𝐻𝐻+]−[𝑂𝑂𝐻𝐻−]−[𝐻𝐻𝑆𝑆−]−2[𝑆𝑆2−] (5) 𝑊𝑊𝑏𝑏 = [𝐻𝐻2𝑆𝑆] + [𝐻𝐻𝑆𝑆−] + [𝑆𝑆2−] (6)
Dengan: 𝑊𝑊𝑁𝑁 adalah jumlah konsentrasi relasi ion hidrogen (Molar)
𝑊𝑊𝑏𝑏adalah jumlah konsentrasi ion sulfida (Molar)
Persamaan (5) dan (6) di atas merupakan reaksi invarian saat proses berlangsung. Penggabungan kedua persamaan tersebut dengan persamaan (3), (4) dan (5) akan didapatkan pemodelan persamaan statik plant.
𝑥𝑥𝑏𝑏 𝐾𝐾𝑁𝑁1 [𝐻𝐻+]+2𝐾𝐾[𝐻𝐻𝑁𝑁1+∙𝐾𝐾]2𝑁𝑁2 1 +𝐾𝐾𝑁𝑁1 [𝐻𝐻+]+ 𝐾𝐾𝑁𝑁1∙𝐾𝐾𝑁𝑁2 [𝐻𝐻+]2 +𝑥𝑥𝑁𝑁+[𝐾𝐾𝐻𝐻𝑤𝑤+]−[𝐻𝐻+] = 0 (7)
Dengan mendefinisikan model state-space nonlinier, dimana: 𝑥𝑥=�𝑊𝑊𝑁𝑁 𝑊𝑊𝑏𝑏� 𝑦𝑦=𝑝𝑝𝐻𝐻 Dengan 𝑥𝑥𝑁𝑁 =𝑊𝑊𝑁𝑁
𝑥𝑥
𝑏𝑏=
𝑊𝑊
𝑏𝑏Dengan mengubah persamaan (7) menjadi bentuk polinomial, maka persamaan tersebut akan menjadi seperti di bawah ini.
Perancangan Sistem Pengandalian pH dengan Metode Adaptive
Control Menggunakan Minimum Variance pada Unit
Pengolahan Limbah Gas di PT HESS (Indonesia-Pangkah) Ltd.
Nursinggih Wahyuni, Hendra Cordova
Jurusan Teknik Fisika, Fakultas Teknologi Industri, Institut Teknologi
Sepuluh Nopember (ITS)
Jl. Arief Rahman Hakim, Surabaya 60111
: [email protected]
𝑥𝑥𝑏𝑏� 𝐾𝐾𝑁𝑁1 �𝐻𝐻+�+2𝐾𝐾𝑁𝑁�𝐻𝐻1+∙𝐾𝐾𝑁𝑁�22 1+�𝐻𝐻𝐾𝐾𝑁𝑁+1�+𝐾𝐾𝑁𝑁1∙𝐾𝐾𝑁𝑁2 �𝐻𝐻+�2 �[𝐻𝐻+] +𝑥𝑥 𝑁𝑁[𝐻𝐻+] +𝐾𝐾𝑤𝑤−[𝐻𝐻+]2 (8) 𝑥𝑥𝑏𝑏∙ 𝐾𝐾𝑁𝑁1+𝑥𝑥𝑏𝑏2𝐾𝐾[𝑁𝑁𝐻𝐻1+∙𝐾𝐾]𝑁𝑁2+𝑥𝑥𝑁𝑁[𝐻𝐻+] +𝑥𝑥𝑁𝑁∙ 𝐾𝐾𝑁𝑁1+𝑥𝑥𝑁𝑁 𝐾𝐾𝑁𝑁1∙𝐾𝐾𝑁𝑁2 [𝐻𝐻+] + 𝐾𝐾𝑤𝑤+𝐾𝐾𝑁𝑁[𝐻𝐻1∙𝐾𝐾+]𝑤𝑤+ 𝐾𝐾𝑁𝑁1∙𝐾𝐾𝑁𝑁2∙𝐾𝐾𝑤𝑤 [𝐻𝐻+]2 −[𝐻𝐻+]2− 𝐾𝐾𝑁𝑁1∙[𝐻𝐻+]− 𝐾𝐾𝑁𝑁1∙ 𝐾𝐾𝑁𝑁2= 0 (9) 𝑥𝑥𝑏𝑏𝐾𝐾𝑁𝑁1[𝐻𝐻+]2+𝑥𝑥𝑏𝑏2𝐾𝐾𝑁𝑁1∙ 𝐾𝐾𝑁𝑁2[𝐻𝐻+] +𝑥𝑥𝑁𝑁[𝐻𝐻+]3+ 𝑥𝑥𝑁𝑁𝐾𝐾𝑁𝑁1[𝐻𝐻+]2+𝑥𝑥𝑁𝑁𝐾𝐾𝑁𝑁1∙ 𝐾𝐾𝑁𝑁2[𝐻𝐻+] +𝐾𝐾𝑤𝑤[𝐻𝐻+]2+𝐾𝐾𝑤𝑤𝐾𝐾𝑁𝑁1[𝐻𝐻+] + 𝐾𝐾𝑤𝑤𝐾𝐾𝑁𝑁1𝐾𝐾𝑁𝑁2−[𝐻𝐻+]4− 𝐾𝐾𝑁𝑁1[𝐻𝐻+]3− 𝐾𝐾𝑁𝑁1𝐾𝐾𝑁𝑁2[𝐻𝐻+]2= 0 (10) [𝐻𝐻+]4+ (𝐾𝐾 𝑁𝑁1− 𝑥𝑥𝑁𝑁)[𝐻𝐻+]3+ (𝐾𝐾𝑁𝑁1𝐾𝐾𝑁𝑁2− 𝐾𝐾𝑁𝑁1𝑥𝑥𝑁𝑁− 𝐾𝐾𝑁𝑁1𝑥𝑥𝑏𝑏− 𝐾𝐾𝑤𝑤𝐻𝐻+2+−𝐾𝐾𝑁𝑁1𝐾𝐾𝑁𝑁2𝑥𝑥𝑁𝑁−2𝐾𝐾𝑁𝑁1𝐾𝐾𝑁𝑁2𝑥𝑥𝑏𝑏−𝐾𝐾𝑤𝑤𝐾𝐾𝑁𝑁1𝐻𝐻+−𝐾𝐾𝑤𝑤𝐾𝐾𝑁𝑁 1𝐾𝐾𝑁𝑁2=0 (11) Konsentrasi ion hidrogen [H+
2. Pemodelan Dinamik Proses Pencampuran
] dari penyelesaian persamaan (11) dapat digunakan untuk mengetahui proses statik dari plant.
Proses dinamik digunakan untuk mendapatkan nilai konsentrasi xa (asam) dan xb (basa) saat proses berlangsung. Proses dinamik juga digunakan dalam pemodelan sistem dimana pemodelan yang didapatkan adalah model nonlinier. Untuk proses dinamik yang terjadi pada plant dapat diturunkan dari komponen material balance untuk reaksi invariant, sebagai berikut :
𝑉𝑉𝑑𝑑𝑊𝑊𝑑𝑑𝑑𝑑𝑁𝑁 =𝑞𝑞1(𝑊𝑊𝑁𝑁1− 𝑊𝑊𝑁𝑁3) +𝑞𝑞2(𝑊𝑊𝑁𝑁2− 𝑊𝑊𝑁𝑁3) (13)
𝑉𝑉𝑑𝑑𝑊𝑊𝑑𝑑𝑑𝑑𝑏𝑏=𝑞𝑞1(𝑊𝑊𝑏𝑏1− 𝑊𝑊𝑏𝑏3) +𝑞𝑞2(𝑊𝑊𝑏𝑏2− 𝑊𝑊𝑏𝑏3) (14)
dimana:
𝑞𝑞1: laju aliran asam (L/s), 𝑞𝑞2: laju aliran basa (L/s), 𝑊𝑊𝑁𝑁: reasi invariant asam (Molar), 𝑊𝑊𝑏𝑏: reaksi invariant basa (Molar), 𝑉𝑉 : volume dari campuran (L).
Setelah mengetahui nilai xa dan xb, selanjutnya dilakukan proses identifikasi. Pada proses identifikasi ini, akan didapatkan nilai dari estimator 𝜃𝜃 (a1, a2, b1, dan b2
Berdasakan persamaan di atas, maka persamaan sistem orde-2 untuk plant adalah:
𝐺𝐺(𝑧𝑧) =𝑧𝑧20,2848−1,592𝑧𝑧 −𝑧𝑧+ 2,955 (16)2,955
). Pendekatan yang digunakan dalam pengerjaan Tugas Akhir ini adalah sistem orde-2 dengan menggunakan persamaan dalam bentuk diskrit seperti berikut.
𝐺𝐺(𝑧𝑧) =𝑧𝑧2𝑏𝑏1+𝑧𝑧𝑁𝑁𝑚𝑚−1+𝑏𝑏2𝑧𝑧𝑚𝑚−2+⋯+𝑏𝑏𝑚𝑚𝑧𝑧𝑚𝑚−𝑀𝑀
1𝑧𝑧𝑛𝑛−1+𝑁𝑁2𝑧𝑧𝑛𝑛−2+⋯+𝑁𝑁𝑛𝑛𝑧𝑧𝑛𝑛−𝑁𝑁 (15)
B. Pemodelan Matematik Elemen Pengendalian
1. Perhitungan Gain Transmitter
Transmitter atau sensor pH yang digunakan adalah jenis elektrode. Sensor ini terdiri dari 2 elektroda, elektroda pertama digunakan untuk pengukuran dan elektrode lainnya sebagai referensi. Kedua elektroda ini dipisahkan oleh partisi yang terbuat dari gelas padat. Hubungan pH dengan ion hidrogen dapat dirumuskan dengan Persamaan 3.17. Perubahan konsentrasi ion hidrogen tersebut kemudian dikonversikan kedalam sinyal keluaran listrik oleh elektroda
gelas pH sensor dengan range pengukuran pH = 0 – 14 dan sinyal keluaran 4 – 20 mA, sehingga diperoleh gain sensor/ transmitter pH :
𝐾𝐾𝑝𝑝𝐻𝐻 =𝑠𝑠𝑝𝑝𝑁𝑁𝑛𝑛𝑠𝑠𝑝𝑝𝑁𝑁𝑛𝑛𝑣𝑣𝑁𝑁𝑘𝑘𝑣𝑣𝑁𝑁𝑏𝑏𝑘𝑘𝑘𝑘𝑘𝑘𝑘𝑘𝑘𝑘𝑘𝑘𝑁𝑁𝑘𝑘𝑁𝑁𝑛𝑛𝑑𝑑𝑘𝑘𝑘𝑘𝑘𝑘𝑘𝑘𝑘𝑘𝑘𝑘 (17𝑁𝑁) 𝐾𝐾𝑝𝑝𝐻𝐻 =20mA14−−4mA0 =87 (17𝑏𝑏) 𝐺𝐺𝑝𝑝𝐻𝐻 =𝜏𝜏(𝑠𝑠𝐾𝐾) + 1 (17𝑝𝑝𝐻𝐻 𝑐𝑐)
Karena media pengiriman merupakan sinyal elektrik maka konstanta waktu yang terjadi sangat kecil dan dapat diabaikan. Maka fungsi alih transmitter adalah 𝐾𝐾𝑝𝑝𝐻𝐻 =8
7.
Diketahui bahwa keluaran dari sensor pH berupa nilai arus antara 4 mA sampai dengan 20 mA. Nilai ini harus dikonversi terlebih dahulu menjadi nilai tegangan. Setelah konversi dari arus menjadi tegangan kemudian sinyal ini dimasukkan ke dalam ADC (Analog to Digital Converter). Diasumsikan bahwa resolusi dari ADC ini sangat tinggi serta kecepatan konversi yang tinggi pula. Jika proses ini berlangsung sangat cepat dapat diasumsikan bahwa proses konversi adalah dari nilai arus menjadi nilai pH kembali. Sehingga nilai gain dari transmiter ini adalah sama dengan 1,143.
2. Perhitungan Gain Pompa Diafragma
Pada tugas akhir ini aktuator yang digunakan adalah pompa diafragma. Pompa ini digunakan untuk mengatur laju aliran NaOH. Untuk mendapatkan fungsi transfer pompa, maka terlebih dahulu harus menghitung nilai gain dengan menggunakan persamaan seperti berikut ini.
𝐺𝐺𝑝𝑝=𝑠𝑠𝑝𝑝𝑁𝑁𝑛𝑛𝑘𝑘𝑘𝑘𝑘𝑘𝑘𝑘𝑁𝑁𝑘𝑘𝑁𝑁𝑛𝑛𝑠𝑠𝑝𝑝𝑁𝑁𝑛𝑛𝑚𝑚𝑁𝑁𝑠𝑠𝑘𝑘𝑘𝑘𝑁𝑁𝑛𝑛 (18)
Data di lapangan diperoleh data sebagai berikut:
1. Laju aliran maksimum : 200 lph = 0,056 liter/detik 2. Laju aliran minimum : 0 lph (ini diambil berdasarkan
nilai terkecil dari range kontrol kapasitas pompa yaitu 0%-100%)
3. Tekanan maksimum : 14 bar = 203,052841 psi 4. Tekanan minimum : 1,5 bar = 21,755662 psi Sehingga nilai gain pompa sebesar:
𝐺𝐺𝑝𝑝=181.2972 = 0,0003090.056
Time constant pompa dapat dicari dengan menggunakan persamaan:
𝜏𝜏𝑝𝑝 =𝜏𝜏(∆𝑉𝑉+𝑅𝑅) (19) 𝜏𝜏𝑝𝑝 merupakan konstanta waktu pompa, 𝜏𝜏 merupakan time
stroke, ΔV adalah fraksi perubahan posisi stem pada posisi normal dan R adalah perubahan dari konstanta waktu inherent pada stroking time yang bernilai 0,03 untuk jenis diafragma. Mengacu pada penelitian sebelumnya [3], nilai 𝜏𝜏 =1,733.
∆𝑉𝑉=𝑄𝑄𝑚𝑚𝑁𝑁𝑥𝑥𝑄𝑄− 𝑄𝑄𝑚𝑚𝑣𝑣 𝑛𝑛
𝑚𝑚𝑁𝑁𝑥𝑥 =
0,056−0 0,056 = 1
𝜏𝜏𝑝𝑝= 1,733(1 + 0,03) = 1,785
Jadi, bentuk persamaan matematis pompa diafragma adalah:
𝐺𝐺=𝜏𝜏 𝐺𝐺𝑝𝑝
𝑝𝑝𝑠𝑠+ 1 =
0.000309 1,785 𝑠𝑠+ 1
Sehingga dari pemodelan komponen-komponen di atas didapatkan model closed loop seperti berikut
.
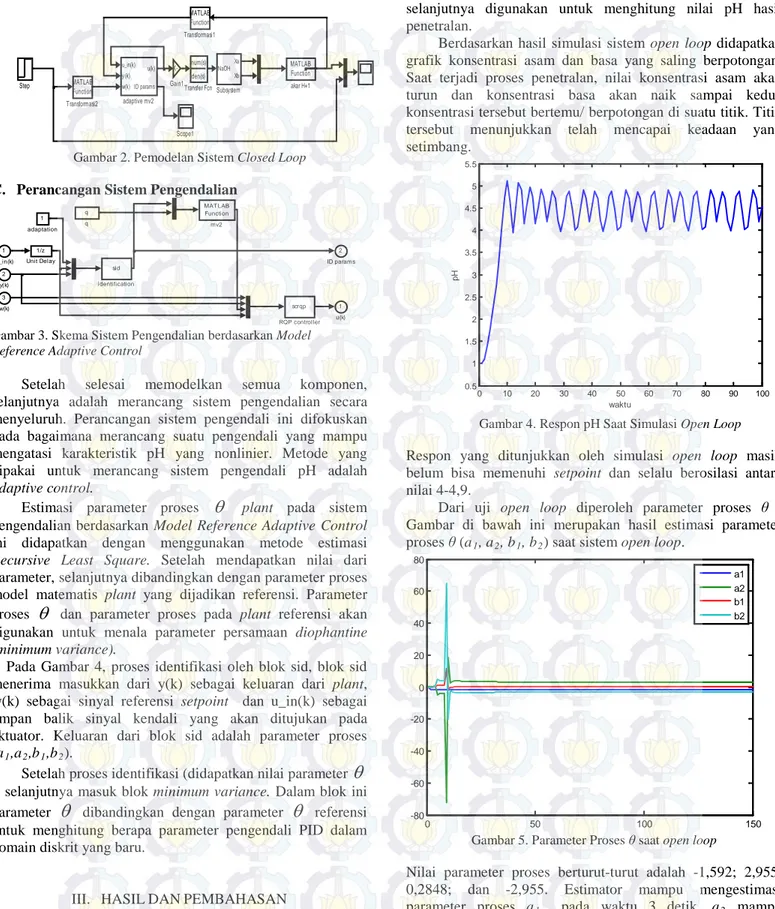
Gambar 2. Pemodelan Sistem Closed Loop
C. Perancangan Sistem Pengendalian
Gambar 3. Skema Sistem Pengendalian berdasarkan Model
Reference Adaptive Control
Setelah selesai memodelkan semua komponen, selanjutnya adalah merancang sistem pengendalian secara menyeluruh. Perancangan sistem pengendali ini difokuskan pada bagaimana merancang suatu pengendali yang mampu mengatasi karakteristik pH yang nonlinier. Metode yang dipakai untuk merancang sistem pengendali pH adalah adaptive control.
Estimasi parameter proses
θ
plant pada sistem pengendalian berdasarkan Model Reference Adaptive Control ini didapatkan dengan menggunakan metode estimasi Recursive Least Square. Setelah mendapatkan nilai dari parameter, selanjutnya dibandingkan dengan parameter proses model matematis plant yang dijadikan referensi. Parameter prosesθ
dan parameter proses pada plant referensi akan digunakan untuk menala parameter persamaan diophantine (minimum variance).Pada Gambar 4, proses identifikasi oleh blok sid, blok sid menerima masukkan dari y(k) sebagai keluaran dari plant, w(k) sebagai sinyal referensi setpoint dan u_in(k) sebagai umpan balik sinyal kendali yang akan ditujukan pada aktuator. Keluaran dari blok sid adalah parameter proses (a1,a2,b1,b2
θ
).Setelah proses identifikasi (didapatkan nilai parameter ), selanjutnya masuk blok minimum variance. Dalam blok ini parameter
θ
dibandingkan dengan parameterθ
referensi untuk menghitung berapa parameter pengendali PID dalam domain diskrit yang baru.III. HASILDANPEMBAHASAN
A. Hasil Simulasi Open Loop
Pada sistem open loop tersebut terdapat proses dinamik yang dirancang sesuai dengan Persamaan (5) dan (6). Sedangkan model statik merupakan model plant penetralan pH berdasarkan reaksi invarian yang terdapat pada persamaan (7) untuk mengetahui konsentrasi larutan asam dan basa yang
selanjutnya digunakan untuk menghitung nilai pH hasil penetralan.
Berdasarkan hasil simulasi sistem open loop didapatkan grafik konsentrasi asam dan basa yang saling berpotongan. Saat terjadi proses penetralan, nilai konsentrasi asam akan turun dan konsentrasi basa akan naik sampai kedua konsentrasi tersebut bertemu/ berpotongan di suatu titik. Titik tersebut menunjukkan telah mencapai keadaan yang setimbang.
Gambar 4. Respon pH Saat Simulasi Open Loop
Respon yang ditunjukkan oleh simulasi open loop masih belum bisa memenuhi setpoint dan selalu berosilasi antara nilai 4-4,9.
Dari uji open loop diperoleh parameter proses θ . Gambar di bawah ini merupakan hasil estimasi parameter proses θ (a1, a2, b1, b2
Gambar 5. Parameter Proses θsaat open loop
Nilai parameter proses berturut-turut adalah -1,592; 2,955; 0,2848; dan -2,955. Estimator mampu mengestimasi parameter proses a
) saat sistem open loop.
1 pada waktu 3 detik, a2 mampu
mengestimasi pada waktu 31 detik, parameter b1 mampu
mengestimasi proses pada waktu 17 detik, dan parameter b2
B. Hasil Simulasi Closed Loop
mampu mengestimasi pada waktu 29 detik.
Pada simulasi closed loop dilakukan beberapa pengujian, di antaranya pengujian setpoint 7 dan uji terhadap noise.
MATLAB Function akar H+1 u_in(k) y (k) w(k) u(k) ID params adaptive mv2 MATLAB Function Transformasi2 MATLAB Function Transformasi1 num(s) den(s) Transfer Fcn NaOH Xa Xb Subsystem Step Scope1 -K-Gain1 2 ID params 1 u(k) q q MATLAB Function mv2 sid identification 1 adaptation 1/z Unit Delay scrqp RQP controller 3 w(k) 2 y(k) 1 u_in(k) 0 10 20 30 40 50 60 70 80 90 100 0.5 1 1.5 2 2.5 3 3.5 4 4.5 5 5.5 pH waktu 0 50 100 150 -80 -60 -40 -20 0 20 40 60 80 a1 a2 b1 b2
Gambar 6. Respon sistem closed loop saat uji setpoint Berdasarkan gambar di atas, telah didapatkan bentuk kurva penetralan pH berbentuk S yang mengikuti perubahan nilai setpoint. Namun seperti terlihat pada gambar di atas, nilai pH yang dihasilkan oleh simulasi closed loop masih belum sesuai setpoint.
Berdasarkan Gambar 6 di atas terlihat bahwa sistem tidak memiliki dead time, maximum overshoot, dan peak time. Sedangkan waktu yang dibutuhkan untuk mencapai keadaan steady sebesar 38 detik.
Dari simulasi closed loop tersebut didapatkan parameter proses θ yang baru, yaitu , yaitu a1= -0,4966, a2= 0,05993,
b1= -0,002998, dan b2
Gambar 7. Parameter Proses θ
Berdasarkan gambar di atas, terlihat terjadi perubahan parameter proses θ antara sebelum dan sesudah ditambah sinyal kendali. Pada simulasi gambar di atas dapat dilihat bahwa estimator sudah mampu mengestimasi parameter proses a
= -0,05993.
1 pada waktu 2 detik, a2 pada waktu 4 detik, b1 pada
waktu 4 detik, dan b2
Gambar 8. Perubahan Laju Aliran Basa saat uji setpoint
Berdasarkan gambar perubahan laju aliran basa, dimana terlihat bahwa laju aliran basa yang dikeluarkan melalui pompa terus berubah sampai sistem mencapai keadaan steady, setelah mencapai keadaan steady maka laju aliran basa dipetahankan tetap yaitu 3,0484x10
mampu mengestimasi pada waktu 4 detik. Dibandingkan dengan hasil estimasi pada saat open loop, dapat diketahui bahwa pada saat closed loop waktu yang dibutuhkan sistem unruk mengestimasi masing-masing parameter proses membutuhkan waktu lebih cepat jika dibandingkan dengan pada saat open loop.
-6.
Pada waktu diberi gangguan, parameter proses mengalami perubahan, baik nilai maupun waktu. Perubahan parameter proses (a1,a2,b1,b2). Berdasarkan gambar,
parameter proses selalu berubah secara signifikan ketika sistem belum mencapai keadaan steady. Lain halnya ketika sistem mencapai keadaan steady, parameter proses tetap mengalami perubahan tetapi tidak terlalu signifikan dibandingkan ketika sistem belum mencapai keadaan steady. Parameter proses pada keadaan steady adalah a1= -0.4006,
a2= -0.2591, b1= -0.0045, dan b2
Gambar 8. Parameter Proses saat Diberi Gangguan = 0.2591.
Pada waktu diberi gangguan, parameter proses mengalami perubahan, baik nilai maupun waktu. Berdasarkan Gambar 8 di atas dapat diketahui lamanya waktu estimator untuk mengestimasi masing-masing parameter proses, yaitu untuk a1 membutuhkan waktu selama 2 detik, a2 selama 24
detik, b1 selama 14 detik, dan b2
0 10 20 30 40 50 60 70 80 0 1 2 3 4 5 6 7 8 respon pH setpoint
selama 32 detik. Dengan adanya perubahan yang terjadi pada parameter proses saat diberi gangguan, secara langsung juga berakibat pada perubahan laju aliran basa dan respon pH terhadap setpoint. Laju aliran basa yang dihasilkan melalui pompa terus 0 5 10 15 20 25 30 35 40 45 50 -0.5 -0.4 -0.3 -0.2 -0.1 0 0.1 0.2 a1 a2 b1 b2 0 50 100 150 200 250 0 0.5 1 1.5 2 2.5 3 3.5x 10 -6 laj u al ir an waktu 0 10 20 30 40 50 60 -0.8 -0.6 -0.4 -0.2 0 0.2 0.4 0.6 a1 a2 b1 b2
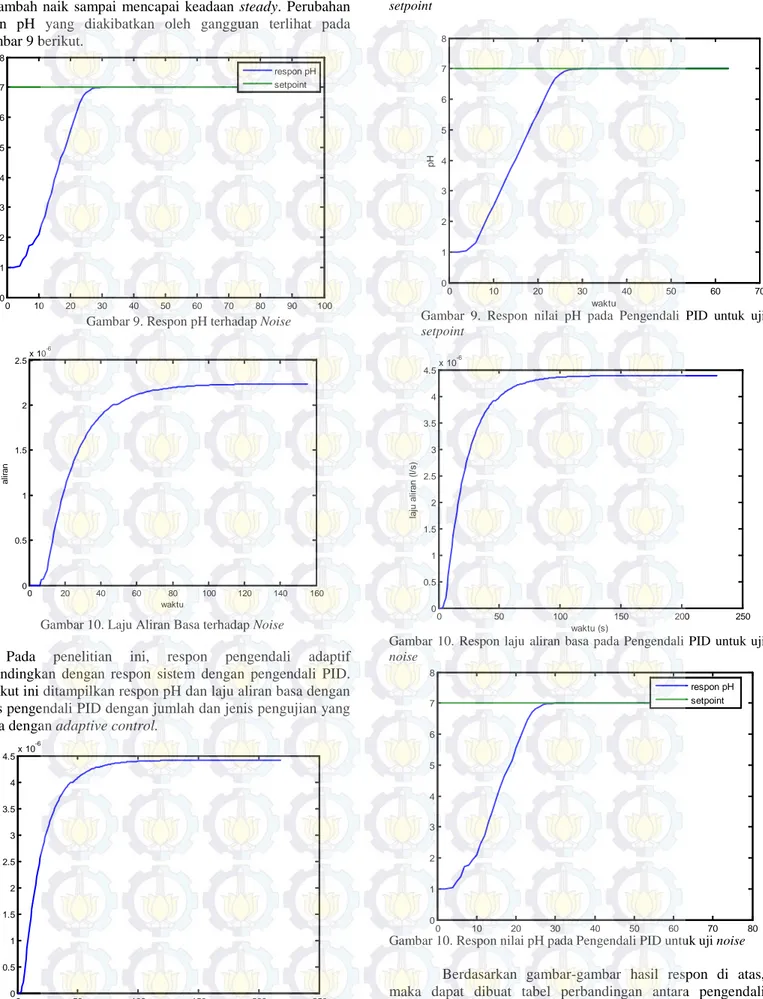
bertambah naik sampai mencapai keadaan steady. Perubahan respn pH yang diakibatkan oleh gangguan terlihat pada Gambar 9 berikut.
Gambar 9. Respon pH terhadap Noise
Gambar 10. Laju Aliran Basa terhadap Noise
Pada penelitian ini, respon pengendali adaptif dibandingkan dengan respon sistem dengan pengendali PID. Berikut ini ditampilkan respon pH dan laju aliran basa dengan jenis pengendali PID dengan jumlah dan jenis pengujian yang sama dengan adaptive control.
Gambar 8. Respon laju aliran basa pada pengendali PID untuk uji
setpoint
Gambar 9. Respon nilai pH pada Pengendali PID untuk uji
setpoint
Gambar 10. Respon laju aliran basa pada Pengendali PID untuk uji
noise
Gambar 10. Respon nilai pH pada Pengendali PID untuk uji noise
Berdasarkan gambar-gambar hasil respon di atas, maka dapat dibuat tabel perbandingan antara pengendali adaptif dan pengendali PID seperti pada Tabel 1 di bawah ini.
0 10 20 30 40 50 60 70 80 90 100 0 1 2 3 4 5 6 7 8 respon pH setpoint 0 20 40 60 80 100 120 140 160 0 0.5 1 1.5 2 2.5x 10 -6 al ir an waktu 0 50 100 150 200 250 0 0.5 1 1.5 2 2.5 3 3.5 4 4.5x 10 -6 laj u al ir an bas a ( lit er /det ik ) waktu (detik) 0 10 20 30 40 50 60 70 0 1 2 3 4 5 6 7 8 pH waktu 0 50 100 150 200 250 0 0.5 1 1.5 2 2.5 3 3.5 4 4.5x 10 -6 laj u al ir an ( l/ s ) waktu (s) 0 10 20 30 40 50 60 70 80 0 1 2 3 4 5 6 7 8 respon pH setpoint
Tabel 1
Perbandingan Nilai Respon antara Adaptive control dengan
Pengendali PID Jenis Uji Bagian yang diamati Adaptive control Pengendali PID Setpoint Laju aliran basa 3,0484 x10-6 4,4143x10-6 Nilai respon pH 7,0003 7,0004 Settling time 38 detik 37 detik error 0,0003 0,0004 Noise Laju aliran basa 3,0235 x10-4 4,3884x10 Nilai respon pH -6 7,0003 7,0004 Settling time 37detik 37detik error 0,0003 0,0004
C. Pembahasan
Pada sistem pengendalian secara adaptif dapat diketahui bahwa terdapat perubahan nilai parameter proses θ terhadap setiap pemberian uji. Perubahan yang dialami oleh parameter proses juga meliputi waktu yang diperlukan untuk mengestimasi nilai parameter. Perubahan nilai parameter proses θ mempunyai pengaruh terhadap respon nilai pH dan laju aliran basa yang diberikan saat terjadi proses penetralan. Pada saat simulasi open loop terlihat bahwa nilai parameter proses besar, gambar respon nilai pH berfluktuatif dan tidak konstan sehingga menyebabkan sistem tidak stabil. Waktu yang diperlukan oleh pengendali untuk mengestimasi masing-masing parameter juga membutuhkan waktu yang lama jika dibandingkan dengan waktu estimasi saat sistem closed loop. Salah satu yang menjadi penyebab respon sistem open loop tidak stabil adalah karena pada sistem open loop tersebut belum dipasang pengendali (kontroler). Tujuan dari pengendali adalah mengurangi gangguan dan menstabilkan proses. Hal ini memaksa identifikasi parameter proses menjadi lebih sulit.
Waktu simulasi closed loop, sistem sudah ditambahkan pengendali (kontroler) sehingga respon yang dihasilkan sudah stabil dan mendekati setpoint yang telah ditetapkan. Nilai dan waktu parameter proses menyesuaikan terhadap perubahan sistem yang terjadi, sehingga pada sistem closed loop nilai paramater proses yang dihasilkan lebih kecil daripada saat sistem open loop, baik pada saat uji setpoint dan uji gangguan. Perubahan nilai parameter proses menyesuaikan terhadap nilai setpoint yang telah ditetapkan sistem, sehingga menjaga sistem tetap stabil terhadap setpoint. Identifikasi proses pada kontrol adaptif berlangsung pada waktu yang tidak terbatas. Sehingga tidak diasumsikan estimasi parameter konstan.
Berdasarkan pada simulasi yang telah dilakukan, pada grafik respon pH terdapat delay time (waktu tunda) saat akan mencapai setpoint. Adanya delay time tersebut disebabkan oleh time constant (konstanta waktu) yang terdapat pada pemodelan di aktuator (pompa). Akibat adanya delay time tersebut menyebabkan adanya keterlambatan sistem menghasilkan respon beberapa detik untuk mencapai setpoint.
KESIMPULAN DAN SARAN
1. Kesimpulan
Dari analisa data dan pembahasan pengujian kehandalan sistem pengendalian yang telah dirancang, dapat disimpulkan bahwa:
• Pengendalian pH dengan Adaptive control dan pengendali PID untuk sistem closed loop memiliki keunggulan beberapa keunggulan jika dibandingkan dengan pengendali PID. Perbedaan nilai pH yang dihasilkan oleh Adaptive control lebih kecil 0,00015. Untuk laju aliran basa berbeda sekitar 1,34125x10-6. Dan nilai error untuk adaptive control baik pada uji setpoint dan noise sebesar 0,0003 sedangkan untuk pengendali PID sebesar 0,0004.
2. Saran
Saran yang dapat diberikan dalam penelitian ini adalah dapat ditemukan metode lain dari pengendali adaptif yang dapat bekerja lebih baik dalam meminimumkan nilai error dari minimum variance.
UCAPAN TERIMA KASIH
Penulis mengucapkan terimak kasih kepada PT HESS (Indonesia-Pangkah) Ltd yang telah membantu dan memberikan kesempatan bagi penulis untuk mengambil data. Ucapan terima kasih juga penulis sampaikan kepada PT Angkasa Pura II (BUMN) yang telah memberikan bantuan beasiswa.
DAFTARPUSTAKA
[1] D. Mamrosh, C. Beitler, dan K. Fisher. Consider improved scrubbing designs for acid gases. Trimeric Corp: Texas [2] Gustafsson& Waller. Dynamic Modeling and Reaction
Invariant Control Of pH. Chemical Engineering Science Vol. 38 No. 3 (1983) pp 389-398.
[3] Operahadi Jaya Dwi Putera. 2007. Perancangan Sistem Pengendalian pH pada Sistem Pengolahan Limbah Berbasis Adaptive control dengan Variant Forgetting Factor. Institut Teknologi Sepuluh Nopember: Surabaya