dy/igsb/2007/kinetika reaksi nonkatalitik gas-cair/halaman 1 dari 9 halaman Reaksi heterogen fluida-fluida meliputi:
1. Reaksi gas-cair (G/L) 2. Reaksi cair-cair
Beberapa alasan dilangsungkannya reaksi G/L:
1. Mendapatkan produk akhir yang bernilai lebih tinggi, misalnya: CO2 (g) + 2 NaOH (l) Na2CO3 + H2O
SO3 (g) + H2O (l) H2SO4
2. Menghilangkan zat yang tidak dikehendaki, atau me-recovery zat yang dikehendaki. Untuk menjabarkan persamaan kecepatan reaksinya, diperlukan:
1. Persamaan kecepatan keseluruhan (overall), yang terdiri atas 2 komponen, yaitu: a) Kecepatan perpindahan massa (difusi)
b) Kecepatan reaksi kimia.
2. Kelarutan gas dalam cairan/larutan (equilibrium solubility)
3. Sistem pengontakan fluida.
Tujuannya: menghasilkan luas bidang atau permukaan kontak antarfluida yang cukup besar. Untuk sistem G/L, mode pengontakan yang pada umumnya dilakukan adalah semibatch dan
counter-current.
Tinjauan sistem reaksi G/L secara umum:
A (g→l) + b B (l) R (s atau l atau g) dengan:
♦ A berada pada fase gas, tetapi terlarut dalam cairan, dengan hubungan kelarutan yang dinyatakan melalui Hukum Henry:
pAi = HA.CAi .… (1)
Keterangan: pAi ≡ tekanan parsial A di antarmuka [=] Pa
CAi ≡ konsentrasi A di antarmuka [=] mol/m3 cairan
HA ≡ konstanta Henry untuk zat A [=] Pa.m3 cairan/mol
♦ B berada dalam fase cair, dan tidak dapat memasuki fase gas.
♦ Reaksi hanya berlangsung dalam fase cair, dengan dua kemungkinan tempat berlangsungnya reaksi: ♣ Dekat dengan antar muka (dalam film cairan), atau
♣ Di dalam cairan (fase bulk)
KINETIKA REAKSI NONKATALITIK
FLUIDA-FLUIDA (GAS-CAIR)
dy/igsb/2007/kinetika reaksi nonkatalitik gas-cair/halaman 2 dari 9 halaman Beberapa harga HA gas yang melarut dalam air [Pa.m3/mol]:
Gas T = 20oC T = 60oC N2 1,45.105 2,16.105 H2 1,23.105 1,34.105 CO 0,96.105 1,48.105 O2 0,74.105 1,13.105 CO2 2600 6300 NH3 0,020 0,096
Berdasarkan tabel di samping, terlihat bahwa harga HA semakin besar dengan
semakin besarnya suhu (T).
HA yang semakin besar berarti pula bahwa
kelarutan gas di dalam larutan menjadi semakin kecil.
Jika HA besar, maka : ♣ Gas A sukar larut dalam cairan
♣ Tahanan film gas yang mengontrol Jika HA kecil, maka : ♣ Gas A mudah larut dalam cairan
♣ Tahanan film cairan yang mengontrol/menentukan. Beberapa cara untuk menyatakan –rA:
dt dN S 1 '' rA =− A − , dt dN V 1 r A l l A =− − , dt dN V 1 '' '' r A r A =− − sehingga: r”” Vr = rl Vl = r” S r”” = fl rl = a r” di mana: r V S a= dan r l l V V f =
Keterangan: Vr ≡ volume reaktor (kontaktor)
Vl ≡ volume cairan dalam reaktor
S ≡ luas bidang antarmuka gas-cairan fl ≡ fraksi volume cairan dalam reaktor
a ≡ luas bidang antarmuka gas-cairan spesifik Dua tahanan seri: ♣ Tahanan film gas
♣ Tahanan film cairan
Kecepatan perpindahan massa A dari gas ke cairan:
Pada film gas: -rA” = kAg (pA – pAi) atau: -rA”” = kAg a (pA – pAi) .… (2)
Pada film cairan: -rA” = kAl (CAi – CA) atau: -rA”” = kAl a (CAi – CA) .… (3)
Satuan: s . Pa . kontaktor m mol a . kAg ≡ 3 s . Pa . m mol kAg ≡ 2 s . kontaktor m cairan m a . kAl ≡ 3 3 s . m cairan m kAl ≡ 3 2
Karena pAi dan CAi merupakan besaran-besaran yang tak terukur, maka persamaan-persamaan (1),
(2), dan (3) harus saling disubstitusikan sehingga menghasilkan:
a . k H a . k 1 C H p '' '' r Al A Ag A A A A + − = − .… (4)
Persamaan (4) merupakan persamaan kecepatan reaksi intrinsik A yang didasarkan pada tiap satuan volume reaktor, jika hanya terjadi perpindahan massa saja. Secara visual terlihat bahwa sebenarnya
dy/igsb/2007/kinetika reaksi nonkatalitik gas-cair/halaman 3 dari 9 halaman persamaan (4) merupakan persamaan kecepatan difusi A dari fase gas ke fase cairan, melewati lapisan film antarmuka gas-cairan.
a . k
1 Ag
merupakan tahanan lapisan gas (gas film resistance)
a . k
H Al
A merupakan tahanan lapisan cairan (liquid film resistance)
PERSAMAAN KECEPATAN BERDASARKAN
PERPINDAHAN MASSA DAN REAKSI
Tempat atau lokasi berlangsungnya reaksi (lihat gambar di samping):
♦ Sebuah zone sempit di dalam film cairan (jika reaksi cepat),
atau
♦ Film cairan dan fase bulk cairan (jika reaksi lambat)
Faktor-faktor yang menentukan persamaan kecepatannya: ♦ Harga-harga relatif antara k, kg, dan kl
♦ Perbandingan komposisi reaktan ⎟⎟
⎠ ⎞ ⎜⎜ ⎝ ⎛ B A C p ♦ Harga konstanta Henry (HA)
Delapan kasus yang akan ditinjau:
Kasus A : Reaksi sangat cepat (instantaneous), CB rendah
Kasus B : Reaksi sangat cepat (instantaneous), CB tinggi
Kasus C : Reaksi cepat, CB rendah
Kasus D : Reaksi cepat, CB tinggi
Kasus E dan F : Kecepatan reaksi sedang/menengah (dalam film cairan dan fase cairan) Kasus G : Reaksi lambat, ada tahanan melalui film
Kasus H : Reaksi sangat lambat, tidak ada tahanan perpindahan massa Persamaan umum untuk kecepatan reaksi gas-cair:
A l B A Al A Ag A p f C k H E a k H a k 1 1 ' ' ' ' r + + = − .... (5) dengan: a k 1 Ag
≡ tahanan kecepatan melalui film gas E
a k
H Al
A ≡ tahanan kecepatan melalui film cairan
l B A f C k H
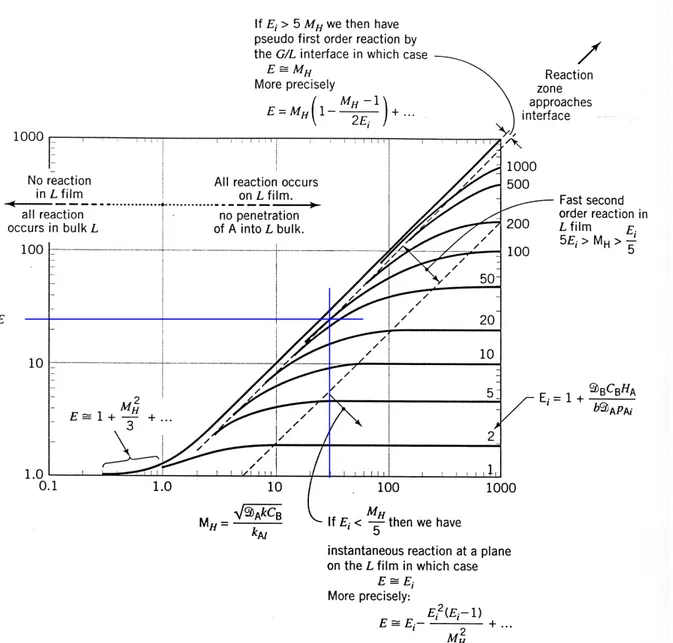
dy/igsb/2007/kinetika reaksi nonkatalitik gas-cair/halaman 4 dari 9 halaman E menyatakan liquid film enhancement factor, yakni:
massa n perpindaha tan kecepa kimia reaksi dengan massa n perpindaha tan kecepa E= .... (6)
Gambar di atas merupakan representasi grafis dari faktor E yang merupakan fungsi dari Ei dan
MH (untuk beberapa kasus yang ditinjau).
Harga E: ≥ 1
Harga E ditentukan oleh:
♦ Ei (enhancement factor untuk reaksi yang berlangsung sangat cepat (infinitely fast reaction)) Ai A A B B i p D b H C D 1 E = + .... (7)
♦ MH2 (parameter konversi film) atau MH (angka atau bilangan Hatta)
Al B A H k C k D M = .... (8)
Keterangan: DA ≡ koefisien difusi A
DB ≡ koefisien difusi B
dy/igsb/2007/kinetika reaksi nonkatalitik gas-cair/halaman 5 dari 9 halaman k ≡ konstanta kecepatan reaksi (berbasis orde-dua)
kAl ≡ koefisien perpindahan massa A di fase cair
b ≡ perbandingan koefisien stoikiometri B (reaktan cair) terhadap A (reaktan gas)
Kasus A
♦ Penentu kecepatan: perpindahan massa (A dan B) ♦ Reaksi berlangsung pada sebuah bidang reaksi
(reaction plane) di dalam film cairan
♦ Seluruh gas A habis bereaksi pada bidang reaksi tersebut. Dengan kata lain, tidak ada A yang berdifusi ke fase cairan bulk.
♦ Perubahan besarnya pA atau CB akan menggeser
letak bidang reaksi. ♦ Pada steady state:
b " r " r B A =− − .... (9) dengan:
(
)
(
)
x x 0 C k p p k " r 0 Ai Al Ai A Ag A = − = − − .... (10)(
)
x x x 0 C k " r 0 0 B Bl B = − − − .... (11)Koefisien distribusi: pAi =HA CAi (Hukum Henry) .... (1)
Rasio koefisien perpindahan massa A dan B:
Bl Al 0 Bl 0 Al Bl Al D D x D x D k k = = .... (12)
Eliminasi harga-harga x, x0, pAi, dan CAi pada kombinasi persamaan-persamaan (1), (9), (10),
(11), dan (12) menghasilkan: Al Ag A A A B Al Bl A A k 1 k H 1 H p b C D D dt dN S 1 " r + + = − = − ⎟ ⎠ ⎞ ⎜ ⎝ ⎛ > B Bl A Ag C b k p k : karena .... (13)
Kasus B
♦ Konsentrasi B (CB) tinggi atau berlebihan
dibandingkan dengan stoikiometri, sehingga bidang reaksi bergeser ke antarmuka film dan gas A habis bereaksi di antarmuka tersebut.
♦ Penentu kecepatan reaksi: perpindahan massa A saja (ada tahanan melalui film gas)
Bl B A Ag C b k p k ≤ sehingga: A Ag A A k p dt dN S 1 " r =− = − .... (14)
dy/igsb/2007/kinetika reaksi nonkatalitik gas-cair/halaman 6 dari 9 halaman
Kasus C
♦ Bidang reaksi pada kasus A sekarang tersebar ke dalam sebuah zone reaksi (ada A dan B di dalamnya); diasumsikan terjadi fast second order reaction.
♦ Reaksi berlangsung cukup cepat, sehingga keseluruhan zone reaksi berada di dalam film cairan, dan tidak ada gas A yang berdifusi ke fase cairan.
♦ Karena k (konstanta kecepatan reaksi) besar (atau, tahanan kecepatan melalui fase cairan dapat diabaikan), maka:
A Al A Ag A p E a k H a k 1 1 '' '' r + = − .... (15)
Kasus D
♦ CB >> CA, maka CB dapat dianggap
konstan (CB ≈ CB0); diasumsikan terjadi pseudo first order reaction.
♦ Jika CB makin besar, maka kecepatan
reaksi menjadi makin besar, sehingga zone reaksi akan bergeser ke arah antarmuka film. ♦ Persamaan kecepatannya: A B A A Ag A p C k D a H a k 1 1 ' ' ' ' r + = − .... (16)
Kasus E dan F
♦ Reaksi berlangsung cukup lambat (terjadi di film cairan dan fase cairan bulk)
♦ Persamaan kecepatannya: A l B A Al A Ag A p f C k H E a k H a k 1 1 ' ' '' r + + = − .... (17)
dy/igsb/2007/kinetika reaksi nonkatalitik gas-cair/halaman 7 dari 9 halaman
Kasus G
♦ Reaksi berlangsung lambat dan berlangsung seluruhnya di fase cairan
bulk. ♦ Persamaan kecepatannya: A l B A Al A Ag A p f C k H a k H a k 1 1 '' '' r + + = − .... (18)
Kasus H
♦ Reaksi berlangsung sangat lambat
dibandingkan dengan perpindahan massa, sehingga tahanan perpindahan massa dapat diabaikan.
♦ Komposisi A dan B dalam cairan: seragam
♦ Persamaan kecepatannya menjadi:
B A l B A A l A p C k f C C H f k ' ' ' ' r = = − .... (19)
ANGKA ATAU BILANGAN HATTA (M
H)
MH merupakan suatu angka atau bilangan tak berdimensi yang mengindikasikan suatu reaksi
berlangsung cepat atau lambat, dalam sistem reaksi nonkatalitik gas-cair. ♦ Fokus peninjauan: pada satuan luas permukaan antarmuka gas-cairan. ♦ Asumsi: tahanan kecepatan melalui fase gas dapat diabaikan.
♦ Definisikan parameter konversi film (yang merupakan kuadrat dari bilangan Hatta): film the through transport l diffusiona imum max film the in conversion possible imum max MH2 = .... (20)
♦ Jika kecepatan reaksi kimia diasumsikan berorde-dua:
Ai 0 Al 0 B Ai 2 H C x D x C C k M = .... (21) Karena: 0 Al Al x D k = .... (22) maka: 2 Al Al B 2 H k D C k M = .... (23)
Jika M
H>> 1:
dy/igsb/2007/kinetika reaksi nonkatalitik gas-cair/halaman 8 dari 9 halaman ♦ Luas permukaan berperan sebagai faktor penentu kecepatan
♦ Jika MH sangat besar, maka reaktor harus dilengkapi dengan pengadukan, untuk memperluas
antarmuka film gas dengan cairan (atau, memperluas bidang kontak G/L)
Jika M
H<< 1:
♦ Tidak ada reaksi yang berlangsung dalam film cairan (dengan kata lain, keseluruhan reaksi berlangsung dalam fase cairan bulk); reaksi berlangsung sangat lambat
♦ Volume cairan bulk berperan sebagai faktor penentu kecepatan ♦ Jika MH sangat kecil, maka diperlukan volume cairan yang besar.
Penggolongan yang lain untuk MH:
MH > 2 : reaksi berlangsung dalam film cairan (kasus A, B, C, dan D)
0,02 < MH < 2 : keadaan intermediet/antara (kasus E, F, dan G)
MH < 0,02 : reaksi berlangsung sangat lambat dan terjadi dalam fase cairan bulk (kasus H)
CONTOH SOAL
Gas A digelembungkan melalui sebuah tangki yang berisi cairan B, dan berlangsung reaksi sbb: A (g → l) + 2 B (l) R (l)
dengan: -rA = k CA CB2 (reaksi berorde-tiga, k = 106 m6/mol2.jam)
Untuk sistem ini: kAg a = 0,01 mol/jam.m3.Pa
kAl a = 20 jam-1
DAl = DBl = 10-6 m2/jam
fl = 0,98
HA = 105 Pa.m3/mol (kelarutan A dalam B sangat kecil)
a = 20 m2/m3
Jika pA = 5 x 103 Pa dan CB = 100 mol/m3, maka tentukan:
a) lokasi tahanan-tahanan terhadap kecepatan reaksi (berapa % tahanan yang melalui film gas, melalui film cairan, dan melalui fase cairan bulk)
b) tempat terbentuknya zone reaksi (reaksi berlangsung di mana) c) besarnya kecepatan reaksi (dalam mol/m3.jam)
Penyelesaian:
Untuk reaksi yang bukan berorde-dua, reaksi dalam soal ini (yang berorde-tiga) diselesaikan dengan pendekatan orde-dua, sehingga: k CA CB2 ⇒ (k CB) CA CB
Berdasarkan persamaan umum untuk kecepatan reaksi gas-cair: A l B A Al A Ag A p f C k H E a k H a k 1 1 ' ' '' r + + = −
maka, mula-mula harga Ei dan MH harus dievaluasi lebih dahulu (dengan menebak pAi = pA): 100 1 100 10 10 k C k D M 2 6 6 Al 2 B A H = = = −
( )
(
)
3 5 5 Ai A A B B pertama tebakan i 10 10 x 5 2 10 x 100 1 p D b H C D 1 E = + = + =Karena (Ei) tebakan pertama > 5 MH, maka untuk tebakan-tebakan pAi lain yang lebih kecil, akan
dy/igsb/2007/kinetika reaksi nonkatalitik gas-cair/halaman 9 dari 9 halaman merupakan reaksi orde-satu semu (pseudo first-order) dan berlangsung dalam film cairan, dengan: E = MH = 100 sehingga: A l B A Al A Ag A p f C k H E a k H a k 1 1 ' ' '' r + + = − reaktor m . jam / mol 33 ) 98 , 0 ( ) 100 ( ) 10 ( 10 ) 100 ( ) 20 ( 10 01 , 0 1 10 x 5 '' '' r 3 2 6 5 5 3 A = + + = − 2/3 1/3 ≈ 0
Jadi: (a) 2/3 tahanan berada di film gas, dan 1/3 berada di film cairan (b) Zone reaksi berada di dalam film cairan
(c) Reaksi berlangsung menurut orde-satu semu, pada antarmuka (d) Kecepatan reaksinya, -rA”” = 33 mol/jam.m3
Catatan: Setiap kali menyelesaikan sebuah soal, selalulah mengecek satuan yang bersesuaian.
LATIHAN SOAL
(1) Pada tekanan tinggi, CO2 diabsorpsi dengan larutan NaOH di dalam sebuah kolom packing.
Reaksi yang terjadi: CO2 + 2 NaOH Na2CO3 + H2O
(A) (B) dengan: -rA = k CA CB (reaksi orde-dua)
(a) Hitunglah kecepatan absorpsi,
(b) hitunglah tahanan kecepatan yang mengontrol, dan (c) apakah yang terjadi di dalam film cairan
pada sebuah lokasi di dalam kolom dengan: pA = 105 Pa dan CB = 500 mol/m3.
Data: kAg a = 10-4 mol/m2.s.Pa HA = 25000 Pa.m3/mol
kAl = 1 x 10-4 m/s DA = 1,8 x 10-9 m2/s
a = 100 m-1 D
B = 3,06 x 10-9 m2/s k = 10 m3/mol.s fl = 0,1
(2) Gas A terabsorp dan bereaksi dengan cairan B, menurut persamaan:
A (g → l) + 2 B (l) R (l), dengan: -rA = k CA CB (reaksi orde-dua)
di dalam sebuah kolom packing, dengan:
kAg a = 0,1 mol/jam.m2 reaktor.Pa HA = 105 Pa.m3 cairan/mol
kAl a = 100 m3 cairan/m3 reaktor.jam DA = DB = 10-6 m2/jam
a = 100 m2/m3 reaktor fl = 0,01 m3 cairan/m3 reaktor
k = 10 m3 cairan /mol.jam
Pada titik atau lokasi dalam kolom di mana pA = 100 Pa dan CB = 100 mol/m3 cairan:
(a) Hitunglah kecepatan reaksi (dalam mol/jam.m3 reaktor)
(b) Tentukan lokasi tahanan-tahanan utama terhadap kecepatan reaksinya (tahanan melalui film gas, tahanan melalui film cairan, dan tahanan melalui cairan bulk)
PUSTAKA
Pustaka rujukan untuk materi kuliah ini:
1. Levenspiel, O., 1999, Chemical Reaction Engineering, 3rd ed., New York; John Wiley & Sons, Inc., Chapter 23.
2. Missen, R. W., Mims, C. A., and Saville, B. A., 1999, Introduction to Chemical Reaction Engineering and Kinetics, New York: John Wiley & Sons, Inc., Chapter 9.