1. INDEKS MASSA TUBUH
Berat badan ditentukan oleh keseimbangan kalori yang
dikonsumsi dalam makanan dengan kalori yang dikeluarkan untuk
kebutuhan istirahat fungsi seluler dan pekerjaan fisik (Kernan dkk,
2013).
Obesitas meningkatkan risiko stroke dengan beberapa
mekanisme seperti diabetes melitus, hipertensi, aterosklerosis, atrial
fibrilasi, dan obstructive sleep apnea. Hasil akhir dapat berupa
aterosklerosis yang progresif dan atau tromboembolisme yang dapat
menimbulkan oklusi atau ruptur arteri (Kernan dkk, 2013).
Indeks Massa Tubuh yaitu suatu pengukuran antropometrik
sederhana dimana berat badan dibagi dengan kuadrat tinggi badan,
yang merupakan suatu alat screening untuk overweight dan obesitas
yang paling sering digunakan. Indeks Massa Tubuh sering digunakan
karena berkaitan erat dengan kadar lemak tubuh. Pengukurannya
relatif mudah dan murah serta merupakan suatu metode yang non
invasif untuk menilai status gizi seseorang (Duncan dkk, 2009 ;
Bigaard dkk, 2005).
Indeks Massa Tubuh merupakan metode pengukuran yang
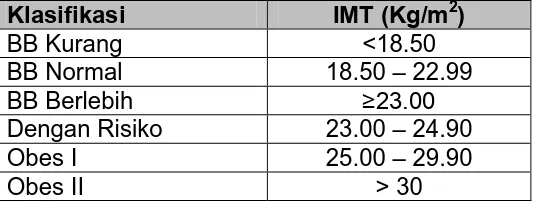
menilai massa lemak tubuh (Tabel 1) (Konsensus Pengendalian dan
Pencegahan Diabetes Mellitus Tipe 2 di Indonesia. 2011.
Perkumpulan Endokrinologi Indonesia). Indeks Massa Tubuh
menghasilkan suatu pengukuran total lemak tubuh yang lebih akurat
bila dibandingkan dengan pengukuran berat badan saja (NHLBI,
2002).
Indeks Massa Tubuh dapat dinilai dari hasil berat badan (BB)
dalam kilogram (kg) dibagi dengan kuadrat tinggi badan (TB) dalam
meter (m). Dapat disederhanakan dalam rumus berikut (NHLBI, 2002;
Konsensus Pengendalian dan Pencegahan Diabetes Mellitus Tipe 2 di
Indonesia. 2011. Perkumpulan Endokrinologi Indonesia) :
Tabel 1. Klasifikasi IMT berdasarkan WHO dalam The Asia-Pacific Perspective : Redifining Obesity and Its Treatment
Klasifikasi IMT (Kg/m2)
BB Kurang <18.50
BB Normal 18.50 – 22.99
BB Berlebih ≥23.00
Dengan Risiko 23.00 – 24.90
Obes I 25.00 – 29.90
Obes II > 30
Dikutip dari : Konsensus Pengendalian dan Pencegahan Diabetes Mellitus Tipe 2 di Indonesia. 2011. Perkumpulan Endokrinologi Indonesia
IMT = BB = (kg)
2. ALIRAN DARAH OTAK
Aliran darah otak, adalah suplai darah ke otak dalam waktu
tertentu. Jumlah aliran darah ke otak biasanya dinyatakan dalam
cc/menit/100 gram jaringan otak. Pada orang dewasa, normal CBF
adalah 750 cc/menit atau 15% dari curah jantung. Hal ini sama
dengan 50 – 54 cc darah per 100 gram jaringan otak/menit. Aliran
darah otak diatur untuk memenuhi tuntutan metabolisme otak. Terlalu
banyak darah (hiperemia) dapat menyebabkan peningkatan tekanan
intrakranial/ ICP), yang dapat menekan dan
merusak jaringan otak. Terlalu sedikit darah yang mengalir (iskemik)
bila aliran darah ke otak di bawah 18 – 20 cc/100 gram jaringan
otak/menit, dan kematian jaringan terjadi jika aliran darah di bawah 8
– 10 cc/100 gram jaringan otak/menit. Dalam jaringan otak, kaskade
biokimia yang dikenal sebagai kaskade iskemik dipicu saat jaringan
menjadi iskemik, yang berpotensi mengakibatkan kerusakan dan
kematian sel-sel otak (Modul Neurovaskular PERDOSSI, 2009).
Aliran darah ke otak ditentukan oleh sejumlah faktor, seperti
viskositas darah, dilatasi pembuluh darah, dan tekanan aliran darah
ke otak, yang dikenal sebagai tekanan perfusi serebral, yang
ditentukan oleh tekanan darah tubuh. Pembuluh darah serebral
mampu mengubah aliran darah dengan mengubah diameter
pembuluh darah yang disebut autoregulasi, yaitu pembuluh darah
bila tekanan darah sistemik diturunkan. Arteriol juga berkonstriksi dan
berdilatasi terhadap konsentrasi kimia yang berbeda. Sebagai contoh,
pembuluh darah berdilatasi bila kadar karbondioksida lebih tinggi
dalam darah (Modul Neurovaskular PERDOSSI, 2009).
Cerebral Blood Flow tergantung pada nilai tekanan perfusi
serebral (Cerebral Perfusion Pressure / CPP) dan resistensi
serebrovaskular (Cerebrovascular Resistance / CVR) :
Komponen CPP ditentukan oleh tekanan darah sistematik (Mean
Arterial Blood Pressure / MABP) dikurangi dengan ICP, sedangkan
komponen CVR ditentukan oleh beberapa faktor, yaitu :
1. Tonus pembuluh darah otak
2. Struktur dinding pembuluh darah
3. Viskositas darah yang melewati pembuluh darah otak
2.1 Anatomi Pembuluh Darah Otak
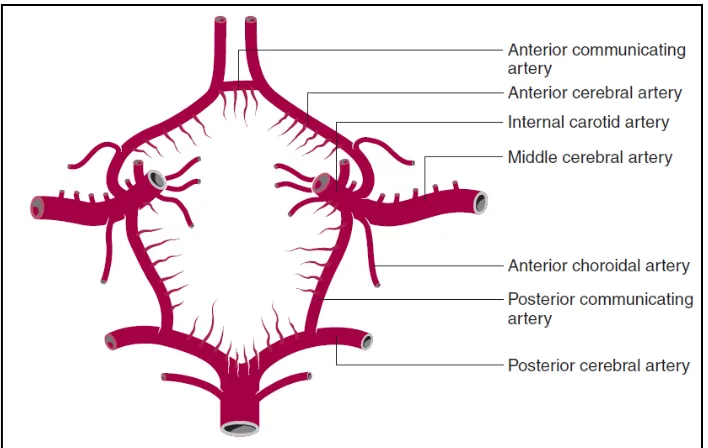
Sirkulasi darah ke otak ada sirkulasi anterior dan sirkulasi
posterior. Sirkulasi anterior adalah arteri karotis komunis dengan
cabang distalnya yaitu arteri karotis internal, arteri serebri media
dan arteri serebri anterior. Sirkulasi posterior adalah arteri
vertebrobasilar yang berasal dari arteri vertebralis kanan dan kiri
dan kemudian bersatu menjadi arteri basilaris dan seluruh
percabangannya termasuk cabang akhirnya yaitu arteri serebri
CBF = CPP = MABP – ICP
posterior kanan dan kiri (Gambar 1) (Modul Neurovaskular
PERDOSSI, 2009).
Ada tiga sirkulasi yang membentuk sirkulus Willisi di otak.
Ketiga sirkulasi tersebut adalah : 1) sirkulasi anterior terdiri dari
arteri serebri media, arteri serebri anterior dan arteri komunikans
anterior yang menghubungkan kedua arteri serebri anterior, 2)
sirkulasi posterior yang terdiri dari arteri serebri posterior, dan 3)
arteri komunikans posterior yang menghubungkan arteri serebri
media dengan arteri serebri posterior. Kegunaan dari sirkulus
Willisi ini adalah untuk proteksi terjaminnya pasokan darah ke
otak, apabila terjadi sumbatan di salah satu cabang. Contohnya
bila terjadi sumbatan parsial pada proksimal dari arteri serebri
anterior kanan, maka arteri serebri kanan ini akan menerima
darah dari arteri karotis komunis lewat arteri serebri anterior kiri
dan arteri komunikans anterior (Modul Neurovaskular PERDOSSI,
Gambar 1. Sirkulus Willisi.
Dikutip dari : Williams P.L.Gray’s Anatomy : The Anatomical Basis of Medicine and Surgery. Ed 40th. British Edition. 2008
Arteri serebri anterior memperdarahi daerah medial hemisfer
serebri, lobus frontal bagian superior dan lobus parietal bagian
superior. Arteri serebri media memperdarahi daerah frontal
inferior, parietal inferolateral dan lobus temporal bagian lateral.
Arteri serebri posterior memperdarahi lobus oksipital dan lobus
temporal bagian medial (Modul Neurovaskular PERDOSSI, 2009).
Batang otak diperdarahi secara eksklusif dari sirkulasi
posterior. Medula oblongata menerima darah dari arteri vertebralis
melalui arteri perforating medial dan lateral, sedangkan pons dan
midbrain (mesensefalon) menerima darah dari arteri basilaris
lewat cabangnya yaitu arteri perforating lateral dan medial (Modul
Serebelum mendapat darah dari tiga pembuluh darah
serebelar, yaitu : 1) arteri serebelar posterior inferior (Posterior
Inferior Cerebellar Artery / PICA) yang merupakan akhir dari
cabang arteri vertebralis, 2) arteri serebelar anterior inferior
(Anterior Inferior Cerebellar Artery / AICA) yang merupakan
cabang pertama dari arteri basilaris, dan 3) arteri serebelar
superior (Superior Cerebellar Artery / SCA) yang merupakan
cabang akhir dari arteri basilaris (Modul Neurovaskular
PERDOSSI, 2009).
Basal ganglia diperdarahi oleh arteri lentikulostriata kecil
percabangan dari arteri serebri media. Talamus diperdarahi oleh
arteri perforating thalamogeniculata yang merupakan cabang dari
arteri serebri posterior. Genu kapsula internal diperdarahi oleh
arteri lenticulostriata anteromedial atau disebut juga rekuren arteri
Heubneur (Modul Neurovaskular PERDOSSI, 2009).
3. STROKE 3.1 Definisi
Stroke adalah suatu episode disfungsi neurologi akut yang
disebabkan oleh iskemik atau perdarahan berlangsung 24 jam atau
meninggal, tapi tidak memiliki bukti yang cukup untuk
Stroke iskemik adalah episode disfungsi neurologis yang
disebabkan infark fokal serebral, spinal dan infark retinal. Dimana
infark Susunan Saraf Pusat (SSP) adalah kematian sel pada otak,
medulla spinalis, atau sel retina akibat iskemia, berdasarkan :
• Patologi, imaging atau bukti objektif dari injury fokal iskemik
pada serebral, medula spinalis atau retina pada suatu
distribusi vaskular tertentu.
• Atau bukti klinis dari injury fokal iskemik pada serebral,
medula spinalis atau retina berdasarkan simptom yang
bertahan ≥ 24 jam atau meninggal dan etiologis lainnya telah
dieksklusikan (Sacco dkk,2013).
Stroke hemoragik adalah disfungsi neurologis yang
berkembang cepat yang disebabkan oleh kumpulan darah
setempat pada parenkim otak atau sistem ventrikular yang tidak
disebabkan oleh trauma (Sacco dkk,2013).
3.2 Epidemiologi
Insidens terjadinya stroke di Amerika Serikat lebih dari
700.000 jiwa per tahun, dimana 20% darinya akan mati pada
tahun pertama. Jumlah ini akan meningkat menjadi 1 juta jiwa per
tahun pada tahun 2050. Secara internasional insidens global dari
Di Indonesia, data nasional epidemiologi stroke belum ada.
Tetapi dari data sporadik di rumah sakit terlihat adanya tren
kenaikan angka morbiditas stroke, yang sering dengan semakin
panjangnya life expentancy dan gaya hidup yang berubah (Modul
Neurovaskular PERDOSSI, 2009).
Dari hasil Survei Kesehatan Rumah Tangga (SKRT) di
Indonesia dilaporkan bahwa proporsi stroke di rumah sakit antara
tahun 1984 sampai dengan tahun 1986 meningkat, yaitu 0,72 per
100 penderita pada tahun 1984 dan naik menjadi 0,89 per 100
penderita pada tahun 1985 dan 0,96 per 100 penderita pada
tahun 1986. Sedangkan di Jogyakarta pada penelitian Lamsudin
dkk (1998) dilaporkan bahwa proporsi morbiditas stroke di rumah
sakit di Jogyakarta tahun 1991 menunjukkan kecenderungan
meningkat hampir 2 kali lipat (1,79 per 100 penderita)
dibandingkan dengan laporan penelitian sebelumnya pada tahun
1989 (0,96 per 100 penderita) (Sjahrir, 2003).
Dari studi rumah sakit yang dilakukan di Medan pada tahun
2001, ternyata pada 12 rumah sakit di Medan dirawat 1.263 kasus
stroke yang terdiri dari 821 stroke iskemik dan 442 stroke
hemoragik, dimana meninggal sebanyak 201 orang (15,91%)
terdiri dari 98 orang (11,93%) stroke iskemik dan 103 orang
3.3 Faktor Risiko
Penelitian prospektif stroke telah mengidentifikasi berbagai
faktor-faktor yang dipertimbangkan sebagai faktor risiko yang kuat
terhadap timbulnya stroke. Faktor risiko timbulnya stroke,
diantaranya (Sjahrir, 2003; Nasution, 2007; Howard dkk, 2009) :
1. Faktor risiko yang tidak dapat dimodifikasi
a. Umur
b. Jenis kelamin
c. Ras dan suku bangsa
d. Faktor keturunan
e. Berat badan lahir rendah
2. Faktor risiko yang dapat dimodifikasi
a. Perilaku
1. Merokok
2. Diet tidak sehat : lemak, garam berlebihan, asam urat,
kolesterol, kurang asupan buah
3. Alkoholik
4. Obat-obatan : narkoba (kokain), anti koagulansia, anti
platelet, amfetamin, pil kontrasepsi
5. Kurang gerak badan
b. Fisiologis
1. Penyakit hipertensi
3. Diabetes melitus
4. Infeksi/ lues, arthritis, traumatik, AIDS, lupus
5. Gangguan ginjal
6. Kegemukan (obesitas)
7. Polisitemia, viskositas darah meninggi & penyakit
perdarahan
8. Kelainan anatomi pembuluh darah
9. Stenosis karotis asimtomatik
3.4 Klasifikasi
Dasar klasifikasi yang berbeda-beda diperlukan, sebab
setiap jenis stroke mempunyai cara pengobatan, preventif dan
prognosis yang berbeda, walaupun patogenesisnya serupa
(Misbach dkk, 2011).
3.4.1 Berdasarkan patologi anatomi dan penyebabnya
1. Stroke iskemik
a. TIA
b. Thrombosis serebri
c. Emboli serebri
2. Stroke hemoragik
a. Perdarahan intraserebral
3.4.2 Berdasarkan stadium / pertimbangan waktu
1. TIA
2. Stroke in evolution
3. Completed stroke
3.4.3 Berdasarkan jenis tipe pembuluh darah
1. Sistem karotis
2. Sistem vertebro-basiler
3.4.4 Berdasarkan tipe infark (Sjahrir, 2003)
1. Total Anterior Circulation Infarction
2. Partial Anterior Circulation Infarction
3. Posterior Circulation Infarction
4. Lacunar Infarction
3.4.5 Klasifikasi stroke iskemik berdasarkan kriteria kelompok
peneliti TOAST (Trial of Org 10172 in Acute Stroke
Treatment) (Sjahrir, 2003) :
1. Aterosklerosis arteri besar (embolus/trombosis)
2. Kardioembolisme (risiko tinggi/risiko sedang)
3. Oklusi pembuluh darah kecil (lakunar)
4. Stroke akibat dari penyebab lain yang menentukan
a. Non-aterosklerosis Vaskulopati
• Non inflamasi
• Inflamasi non infeksi
b. Kelainan Hematologi atau Koagulasi
5. Stroke akibat dari penyebab lain yang tidak dapat
ditentukan
3.5 Patofisiologi
Pada level makroskopik, stroke iskemik paling sering
disebabkan oleh emboli dari ekstrakranial atau trombosis di
intrakranial, tetapi dapat juga disebabkan oleh berkurangnya aliran
darah ke otak. Pada level seluler, setiap proses yang
mengganggu aliran darah ke otak dapat mencetuskan suatu
kaskade iskemik, yang akan mengakibatkan kematian sel-sel otak
dan infark otak (Becker dkk, 2010).
Secara umum daerah regional otak yang iskemik terdiri dari
bagian inti (core) dengan tingkat iskemik terberat dan berlokasi di
sentral. Daerah ini akan menjadi nekrotik dalam waktu singkat jika
tidak ada reperfusi. Di luar daerah core iskemik terdapat daerah
penumbra iskemik. Sel-sel otak dan jaringan pendukungnya belum
mati, akan tetapi sangat berkurang fungsi-fungsinya dan
menyebabkan juga defisit neurologis. Tingkat iskemiknya makin
ke perifer makin ringan. Daerah penumbra iskemik, diluarnya
dapat dikelilingi oleh suatu daerah hiperemik akibat adanya aliran
darah kolateral (luxury perfusion area). Daerah penumbra iskemik
inilah yang menjadi sasaran terapi stroke iskemik akut supaya
tergantung pada faktor waktu dan jika tidak terjadi reperfusi,
daerah penumbra dapat berangsur-angsur mengalami kematian
(Misbach, 2007).
Iskemik otak mengakibatkan perubahan dari sel neuron otak
secara bertahap, yaitu (Sjahrir, 2003) :
1. Tahap 1
a. Penurunan aliran darah
b. Pengurangan O2
c. Kegagalan energi
d. Terminal depolarisasi dan kegagalan homeostasis ion
2. Tahap 2
a. Eksitoksisitas dan kegagalan homeostasis ion
b. Spreading depresion
3. Tahap 3 : Inflamasi
4. Tahap 4 : Apoptosis
4. HIPERTENSI
4.1 Klasifikasi Tekanan Darah
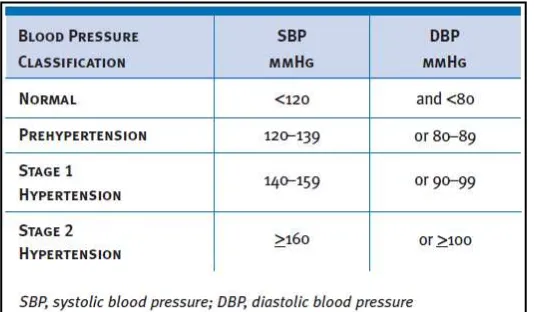
Tabel 2 menunjukkan klasifikasi tekanan darah untuk orang
dewasa ≥18 tahun. Klasifikasi ini berdasarkan rata-rata dari dua
atau lebih pengukuran, saat duduk, tekanan darah dibaca pada
Tabel 2. Klasifikasi tekanan darah pada dewasa.
Dikutip dari The Sevent Report of the Joint National Committee on Prevention, Detection, Evaluation, and Treatment of High Blood Pressure (JNC 7). 2004
4.2 Epidemiologi
Di Indonesia masalah hipertensi cenderung meningkat. Hasil
SKRT tahun 2001 menunjukkan bahwa 8,3% penduduk menderita
hipertensi dan meningkat menjadi 27,5% pada tahun 2004.
Kelompok Kerja Serebrokardiovaskuler FK UNPAD/RSHS tahun
1999, menemukan prevalensi hipertensi sebesar 17,6%, dan
MONICA Jakarta tahun 2000 melaporkan prevalensi hipertensi di
daerah urban adalah 31,7%. Sementara untuk daerah rural
(Sukabumi) FKUI menemukan prevalensi sebesar 38,7%. Hasil
SKRT 1995, 2001 dan 2004 menunjukkan penyakit kardiovaskuler
merupakan penyakit nomor satu penyebab kematian di Indonesia
dan sekitar 20–35% dari kematian tersebut disebabkan oleh
4.3 Patofisiologi
Patofisiologi hipertensi sangat kompleks, diantaranya adalah
mekanisme output jantung dan resistensi perifer, sistem renin
angiotensin, sistem saraf simpatik, remodeling vaskular, arterial
stiffness, dan disfungsi endotel (Beevers dkk, 2001; Oparil dkk,
2003).
5. DIABETES MELITUS 5.1 Definisi
Menurut American Diabetes Association (ADA) tahun 2010,
DM merupakan suatu kelompok penyakit metabolik dengan
karakteristik hiperglikemia yang terjadi karena kelainan sekresi
insulin, kerja insulin, atau kedua-duanya (Konsensus DM tipe 2
Indonesia 2011, PERKENI).
5.2 Epidemiologi
Berbagai penelitian epidemiologi menunjukkan adanya
kecenderungan peningkatan angka insidensi dan prevalensi DM
tipe 2 di berbagai penjuru dunia. World Health Organization
memprediksi adanya peningkatan jumlah penyandang diabetes
yang cukup besar pada tahun-tahun mendatang. World Health
Organization memprediksi kenaikan jumlah penyandang DM di
Indonesia dari 8,4 juta pada tahun 2000 menjadi sekitar 21,3 juta
pada tahun 2030. Senada dengan WHO, International Diabetes
penyandang DM dari 7,0 juta pada tahun 2009 menjadi 12,0 juta
pada tahun 2030. Meskipun terdapat perbedaan angka prevalensi,
laporan keduanya menunjukkan adanya peningkatan jumlah
penyandang DM sebanyak 2-3 kali lipat pada tahun 2030
(Konsensus DM tipe 2 Indonesia 2011, PERKENI).
Laporan dari hasil penilitian di berbagai daerah di Indonesia
yang dilakukan pada dekade 1980-an menunjukkan sebaran
prevalensi DM tipe 2 antara 0,8% di Tanah Toraja, sampai 6,1%
yang didapatkan di Manado. Hasil penelitian pada rentang tahun
1980-2000 menunjukkan peningkatan prevalensi yang sangat
tajam. Sebagai contoh, pada penelitian di Jakarta (daerah urban),
prevalensi DM dari 1,7% pada tahun 1982 naik menjadi 5,7%
pada tahun 1993 dan meroket lagi menjadi 12,8% pada tahun
2001 (Konsensus DM tipe 2 Indonesia 2011, PERKENI).
Berdasarkan data Badan Pusat Statistik Indonesia tahun
2003, diperkirakan penduduk Indonesia yang berusia di atas 20
tahun sebanyak 133 juta jiwa. Dengan prevalensi DM sebesar
14,7% pada daerah urban dan 7,2%, pada daerah rural, maka
diperkirakan pada tahun 2003 terdapat sejumlah 8,2 juta
penyandang diabetes di daerah urban dan 5,5 juta di daerah rural.
Selanjutnya, berdasarkan pola pertambahan penduduk,
diperkirakan pada tahun 2030 nanti akan ada 194 juta penduduk
pada urban (14,7%) dan rural (7,2%) maka diperkirakan terdapat
12 juta penyandang diabetes di daerah urban dan 8,1 juta di
daerah rural (Konsensus DM tipe 2 Indonesia 2011, PERKENI).
Laporan hasil Riset Kesehatan Dasar tahun 2007 oleh
Departemen Kesehatan, menunjukkan bahwa prevalensi DM di
daerah urban Indonesia untuk usia diatas 15 tahun sebesar 5,7%.
Prevalensi terkecil terdapat di Propinsi Papua sebesar 1,7%, dan
terbesar di Propinsi Maluku Utara dan Kalimantan Barat yang
mencapai 11,1%. Sedangkan prevalensi toleransi glukosa
terganggu (TGT), berkisar antara 4,0% di Propinsi Jambi sampai
21,8% di Propinsi Papua Barat (Konsensus DM tipe 2 Indonesia
2011, PERKENI).
5.3 Klasifikasi
Klasifikasi DM dapat dilihat pada Tabel 3 (Konsensus DM
tipe 2 Indonesia 2011, PERKENI).
Tabel 3. Klasifikasi etiologis DM.
5.4 Patofisiologi Diabetes Melitus Tipe 2
Diabetes melitus Tipe 2 ditandai dengan resistensi insulin
perifer dan inadekuat sekresi insulin oleh sel beta pankreas.
Resistensi insulin, berkaitkan dengan peningkatan kadar asam
lemak bebas dan sitokin proinflamasi dalam plasma,
menyebabkan penurunan transportasi glukosa ke dalam sel-sel
otot, peningkatan produksi glukosa hepatik dan peningkatan
pemecahan lemak (Kaku, 2010; D’Adamo dkk, 2011).
5.5 Diagnosis
Diagnosis DM ditegakkan atas dasar pemeriksaan kadar
glukosa darah. Diagnosis tidak dapat ditegakkan atas dasar
adanya glukosuria. Guna penentuan diagnosis DM, pemeriksaan
glukosa darah yang dianjurkan adalah pemeriksaan glukosa
secara enzimatik dengan bahan darah plasma vena. Penggunaan
bahan darah utuh (wholeblood), vena, ataupun angka kriteria
diagnostik yang berbeda sesuai pembakuan oleh WHO.
Sedangkan untuk tujuan pemantauan hasil pengobatan dapat
dilakukan dengan menggunakan pemeriksaan glukosa darah
kapiler dengan glukometer (Konsensus DM tipe 2 Indonesia 2011,
PERKENI).
Berbagai keluhan dapat ditemukan pada penyandang
keluhan klasik DM seperti di bawah ini (Konsensus DM tipe 2
Indonesia 2011, PERKENI) :
- Keluhan klasik DM berupa: poliuria, polidipsia, polifagia, dan penurunan berat badan yang tidak dapat dijelaskan sebabnya
- Keluhan lain dapat berupa: lemah badan, kesemutan, gatal, mata kabur, dan disfungsi ereksi pada pria, serta pruritus
vulvae pada wanita
Diagnosis DM dapat ditegakkan melalui tiga cara (Konsensus DM
tipe 2 Indonesia 2011, PERKENI) :
1. Jika keluhan klasik ditemukan, maka pemeriksaan glukosa
plasma sewaktu >200 mg/dL sudah cukup untuk menegakkan
diagnosis DM
2. Pemeriksaan glukosa plasma puasa ≥ 126 mg/dL dengan
adanya keluhan klasik.
3. Tes Toleransi Glukosa Oral (TTGO). Meskipun TTGO dengan
beban 75 g glukosa lebih sensitif dan spesifik dibanding
dengan pemeriksaan glukosa plasma puasa, namun
pemeriksaan ini memiliki keterbatasan tersendiri. Tes
Toleransi Glukosa Oral sulit untuk dilakukan berulang-ulang
dan dalam praktek sangat jarang dilakukan karena
Langkah-langkah diagnostik DM dan gangguan toleransi
glukosa dapat dilihat pada Bagan 1. Kriteria diagnosis DM untuk
dewasa tidak hamil dapat dilihat pada Tabel 4. Apabila hasil
pemeriksaan tidak memenuhi kriteria normal atau DM, bergantung
pada hasil yang diperoleh, maka dapat digolongkan ke dalam
kelompok Toleransi Glukosa Terganggu (TGT) atau Glukosa
Darah Puasa Terganggu (GDPT) (Konsensus DM tipe 2 Indonesia
2011, PERKENI).
1. Toleransi Glukosa Terganggu (TGT) : Diagnosis TGT
ditegakkan bila setelah pemeriksaan TTGO didapatkan
glukosa plasma 2 jam setelah beban antara 140 – 199 mg/dL
(7,8-11,0 mmol/L).
2. Glukosa Darah Puasa Terganggu (GDPT) : Diagnosis GDPT
ditegakkan bila setelah pemeriksaan glukosa plasma puasa
didapatkan antara 100 – 125 mg/dL (5,6 – 6,9 mmol/L) dan
pemeriksaan TTGO gula darah 2 jam < 140 mg/dL.
Tabel 4. Kriteria diagnosis DM.
Bagan 1. Langkah-langkah diagnostik DM dan gangguan toleransi glukosa.
Dikutip dari : Konsensus Pengendalian dan Pencegahan Diabetes Melitus Tipe 2 di Indonesia 2011. PERKENI
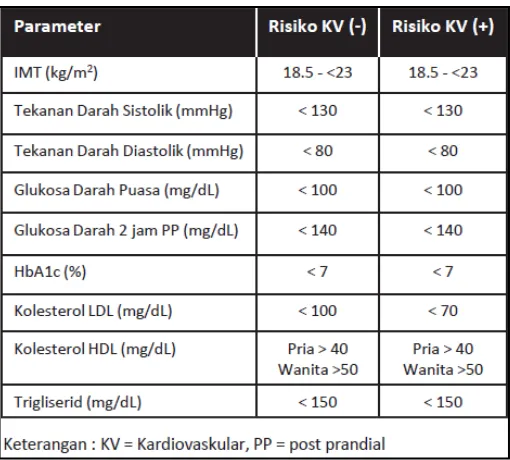
5.6 Kriteria Pengendalian DM
Untuk dapat mencegah terjadinya komplikasi kronik,
diperlukan pengendalian DM yang baik yang merupakan sasaran
terapi. Diabetes terkendali baik, apabila kadar glukosa darah
mencapai kadar yang diharapkan serta kadar lipid dan A1C juga
mencapai kadar yang diharapkan. Demikian pula status gizi dan
tekanan darah. Kriteria keberhasilan pengendalian DM dapat
dilihat pada Tabel 5 (Konsensus DM tipe 2 Indonesia 2011,
Tabel 5. Target pengendalian DM.
Dikutip dari : Konsensus Pengendalian dan Pencegahan Diabetes Melitus Tipe 2 di Indonesia 2011. PERKENI
6. TRANSCRANIAL DOPPLER
Transcranial doppler merupakan suatu alat diagnostik yang
non-invasif yang dapat digunakan untuk mengevaluasi karakteristik aliran
darah pembuluh darah intraserebral melalui regio tulang kranium yang
tipis. Suatu transduser dari gelombang yang digetarkan memancarkan
gelombang-gelombang dan kemudian menerima pemantulannya dari
permukaan sel darah merah di dalam pembuluh darah intrakranial.
Informasi ini akan dianalisa oleh suatu komputer untuk menghasilkan
output numerik dan visual, yang berguna untuk menilai karakteristik
aliran dalam pembuluh darah (Sarkar dkk, 2007). Transcranial doppler
pertama sekali diperkenalkan oleh Aaslid dkk pada tahun 1982,
ultrasound. Untuk dapat mentransmisikan melewati tulang kranium
digunakan transducer dengan frekuensi rendah yaitu probe dengan
frekuensi 2 MHz (Demirkaya dkk, 2008).
Pemeriksaan TCD berdasarkan pada prinsip dasar yang sama
seperti doppler ekstrakranial. Suatu sinyal dipancarkan dari probe dan
dipantulkan ke objek yang bergerak (sel darah merah), dan frekuensi
dari sinyal yang dipantulkan dialihkan dalam proporsi langsung ke
kecepatan (velocity) dari objek yang bergerak (prinsip Doppler). Bila
pembuluh darah sempit, apapun penyebabnya, kecepatan aliran
darah meningkat agar darah dapat melewati lumen pembuluh darah
yang sempit tadi. Peningkatan kecepatan itu dideteksi oleh TCD.
Kecepatan juga meningkat bila ada peningkatan aliran darah
sehubungan dengan kontribusi kolateral terhadap teritori vaskular
yang lain atau suplai darah ke suatu arterio-venous malformation
(AVM) yang besar (Alexandrov dkk, 2004).
Ketepatan interpretasi data TCD bergantung pada pengetahuan,
skill dan pengalaman teknisi dan interpreter. Pemahaman terhadap
anatomi dan fisiologi sirkulasi serebral diperlukan untuk evaluasi yang
tepat (Kassab dkk, 2007).
Transcranial Doppler merupakan suatu prosedur diagnostik yang
canggih dan modern yang dapat memberikan visualisasi perubahan
hemodinamik (autoregulasi) pada arteri serebral sewaktu dan
fisiologik ataupun patofisiologik. Transcranial Doppler merupakan
metode yang sangat sensitif dan spesifik untuk penilaian cepat
hemodinamik sirkulasi serebrovaskular. Gangguan hemodinamik
memperberat autoregulasi arteri dalam otak dan mengganggu
perkembangan sirkulasi kolateral dan aliran kompensasinya.
Hemodinamik sirkulasi serebrovaskular yang dinilai adalah MFV dan
PI (Dikanovic dkk, 2005).
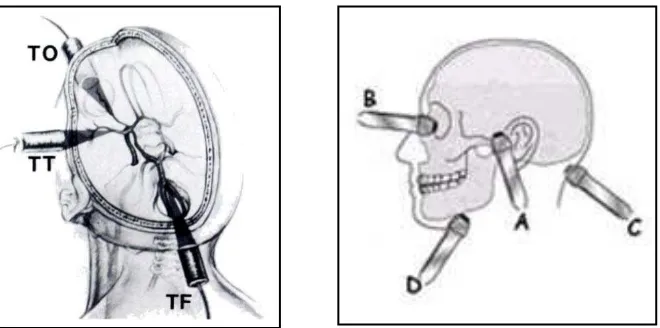
6.1 Pencarian Window
Probe daripada TCD diletakkan di atas ‘acoustic windows’
yang berbeda sesuai dengan spesifik area di tulang kranium yang
tipis. Pemeriksaan TCD yang lengkap terdiri dari 4 pendekatan
untuk mengakses arteri intrakranial sebagai berikut, yaitu (1)
Transtemporal, (2) Transorbital, (3) Suboccipital (transforaminal),
dan (4) Submandibular. Window transtemporal (temporal)
digunakan untuk insonasi arteri serebri media, arteri serebri
anterior, arteri serebri posterior dan bagian terminal dari arteri
karotid interna. Window transorbital (orbita) memberi akses pada
insonasi arteri oftalmika, juga arteri karotid interna pada level
siphon. Window transforaminal (oksipital) untuk insonasi arteri
vertebralis dan arteri basilaris. Yang terakhir window
submandibular memberikan insonasi distal dari arteri karotid
Gambar 2. Posisi transducer pada transcranial sonographic. TO, transorbital; TT, transtemporal; TF, transforaminal.
Dikutip dari : Lupetin AR, Davis DA, Beckman I, Dash N. Transcranial Doppler. Radiographics 1995; 15:179-191
6.2 Identifikasi Arteri
Untuk pemeriksaan TCD diagnostik, digunakan kecepatan
3-5 seconds sweep yang dapat memberikan gambaran detail dari
waveform (bentuk gelombang) dan spektrum. Untuk
memperpendek waktu yang diperlukan untuk mencari window dan
mengidentifikasi segmen arterial yang berbeda-beda dengan
single-gate spectral TCD, pemeriksaan harus dimulai dengan
power maksimum dan pengaturan gate (misalnya power 100%,
gate 10-15 mm) untuk pendekatan transtemporal dan suboccipital.
Meskipun rekomendasi ini tampaknya melanggar peraturan
pemakaian power ultrasound ‘as low as reasonably achievable’,
namun memberikan waktu yang diperlukan untuk mencari window
sehingga mengurangi paparan pasien terhadap energi ultrasound
secara keseluruhan (Kassab dkk, 2007).
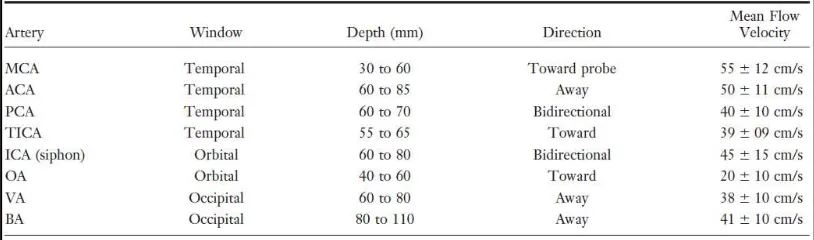
6.3 Indeks TCD
Perbedaan rata-rata kedalaman, arah aliran dan rata-rata
flow velocity dihubungkan dengan usia yang normal telah
ditetapkan pada setiap arteri. Pengukuran TCD dipengaruhi oleh
faktor fisiologik dan patologik serta obat-obat vasoaktif (Tabel 6
dan Tabel 7) (Kassab dkk, 2007).
Nilai sistolik, diastolik dan nilai rata-rata digunakan untuk
mendeskripsikan tekanan, aliran dan kecepatan aliran pada
sistem arterial. Dari nilai-nilai ini, nilai rata-rata memiliki signifikan
fisiologis yang tertinggi karena ia tidak bergantung pada faktor
kardiovaskular sentral seperti denyut jantung, kontraktilitas,
resistensi perifer total dan komplians aorta dibandingkan dengan
nilai sistolik dan diastolik. Selanjutnya nilai rata-rata kecepatan
lebih berkorelasi dengan perfusi dibandingkan dengan nilai peak
(Lupetin dkk, 1995).
Saat ini TCD dapat menunjukkan Gosling’s pulsatility index
yang didapat dari persamaan sebagai berikut :
dimana V = CBFV, yang diperoleh dari TCD. Pada vaskulatur
serebral, PI dapat menunjukkan tingginya resistensi pembuluh
darah perifer, yang seiring dengan peningatan ICP. Peningkatan
ICP mempengaruhi waveform TCD, menunjukkan dengan
meningkatnya PI dan selanjutnya bila ICP terus menekan perfusi,
terjadi penurunan pada CBFV. Pulsatility digambarkan dengan
bentuk dari waveform spektral dan normal bila Vs>Vd, abnormal
atau spiked (Vs>>Vd), atau menurun (Vd>50%Vs). Pulsatility
index dianggap normal bila nilainya 0,8 – 1,2. Peningkatan PI>1,2
biasanya terjadi karena peningkatan resistensi perifer serebral,
sekunder terhadap peningkatan tekanan intrakranial atau
hipokapnia, meskipun pada beberapa kasus bisa disebabkan oleh
abnormalitas kardiak, seperti insufisiensi aorta atau bradikardia.
Penurunan PI<0,8 tipikalnya ditunjukkan oleh pembuluh darah
yang mensuplai suatu AVM, dikarenakan penurunan resistensi
perifer atau downstream hingga high-grade stenoses, dikarenakan
aliran darah yang rendah (Lupetin dkk, 1995).
Resistance Index merupakan estimasi lain dari resistensi
vaskular, dimana resistensi vaskular yang rendah berhubungan
dengan peningkatan FVd, dan resistensi vaskular yang tinggi
dikarakteristikkan dengan penurunan FVd. Resistance Index of
Pourcelot didapat dari persamaan :
Baik PI maupun RI dipengaruhi oleh sejumlah faktor, termasuk
tekanan arterial sistemik, resistensi distal terhadap aliran, ICP,
vascular compliance, dan CO2, membatasi nilai diagnostiknya di
praktek klinis. Namun, hal ini mungkin memiliki peran kualitatif
dalam menilai perubahan dalam resistensi terhadap aliran pada
area spesifik dari sirkulasi serebral. Penting untuk diingat bahwa
TCD hanya mengukur kecepatan darah serebral dan aliran (flow).
Hubungan antara keduanya adalah sebagai berikut :
diameter
Oleh karenanya, bila flow masih konstan, sementara diameter
menurun, Flow Velocity (FV) akan meningkat (Alexandrov dkk,
2004).
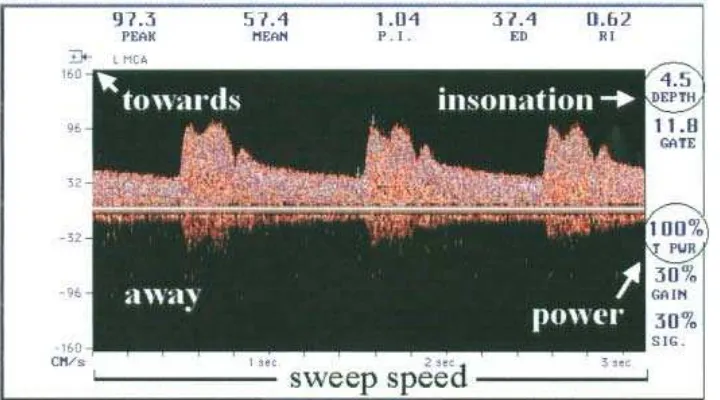
Gambar 3. Tampilan pulsed-wave spectral waveform. Identifikasi arah aliran, skala kecepatan (velocity), kedalaman insonasi (depth), kecepatan sweep dan pengaturan power. Panah kecil menunjukkan pengukuran cardiac cycle untuk menghitung peak, mean dan end-diastolic (ED) flow velocities. PI, pulsality index; RI, resistance index.
Tabel 6. Nilai normal hasil pengukuran TCD pada setiap arteri.
Dikutip dari : Kassab M.Y., Majid A., Farooq M.U., Azhary H., Hershey L.A., Bednarczyk E.M., et al. 2007. Transcranial Doppler : An Introduction for Primary Care Physicians. J Am Board Fam Med;20:65-71
Tabel 7. Efek dari berbagai status fisiologik pada flow velocity
TCD
Dikutip dari : Kassab M.Y., Majid A., Farooq M.U., Azhary H., Hershey L.A., Bednarczyk E.M., et al. 2007. Transcranial Doppler : An Introduction for Primary Care Physicians. J Am Board Fam Med;20:65-71
6.4 Aplikasi Klinis TCD
The American Academy of Neurology mempublikasikan
guidelines aplikasi klinis TCD untuk para klinisi, untuk penyakit
sickle cell, intracranial vasospasm, oklusi dan stenosis arteri,
pada Patent Foramen Ovale (PFO), evaluasi brain death,
autoregulasi serebral (Kassab dkk, 2007).
A. Oklusi dan stenosis arteri
Pengukuran TCD berkorelasi dengan stenosis yang
dapat meningkatkan FV pada tempat stenosisnya (Kassab
dkk, 2007).
- Penurunan FV bagian distal dari tempat sumbatan
- Penurunan FV bagian proksimal dan peningkatan PI bagian proksimal tempat penyumbatan
- Peningkatan FV dan atau aliran balik pada pembuluh darah kolateral
Pada kasus oklusi total, seharusnya tidak ada sinyal
aliran dari tempat penyumbatan. Peningkatan velocity dan
atau aliran balik pada pembuluh darah kolateral dapat juga
ditemukan. Pembuluh darah lain pada window yang sama
harus dapat ditembus insonasi. Penurunan flow velocity darah
bagian proksimal ke tempat oklusi dapat juga terlihat (Kassab
dkk, 2007).
Gambaran aliran utama yang dihubungkan dengan
adanya oklusi secara langsung yang dapat dinilai dengan TCD
ialah suatu gelombang abnormal yang terletak pada lokasi
Jika suatu clot menyebabkan obstruksi komplit untuk
aliran darah, kemudian tidak ada perubahan frekuensi yang
terjadi sehingga tidak ada signal doppler yang dapat
terdeteksi, hal ini disebut sebagai tidak ada aliran darah
(absent). Akan tetapi aliran darah yang tidak ada secara
komplit pada letak clot tersebut cenderung jarang terjadi
karena pergerakan darah yang terdapat di sekitar clot sering
menghasilkan suara bunyi di sekitar garis dasar yang sering
disebut sebagai “minimal flow”. Aliran bergaung (reverberating
flow) merupakan suatu bentuk lain dari aliran minimal dan
kadang-kadang dapat dideteksi di bagian proksimal dari clot.
Bentuk lain dari aliran minimal juga dapat terlihat pada tempat
clot dimana aliran sistolik intensitas rendah dapat ditemukan
berkaitan dengan tahanan tinggi dengan tanpa adanya aliran
darah selama diastol. Dibagian distal dari clot, arteri akan
sepenuhnya mengalami vasodilatasi dan aliran darah akan
muncul, signal arteri ini memiliki pulsatility index, kecepatan
dan intensitas yang rendah. Hal ini disebut dengan istilah
“blunted flow” dan jika sedikit lebih berat disebut “dampened
flow”. kecepatan meningkat berkaitan dengan penyempitan
pembuluh darah, aliran darah tetap terbatas sehingga signal
yang timbul memiliki intensitas yang rendah. Dalam keadaan
dasar) dan kadang-kadang bruit juga dapat terdeteksi. Akan
tetapi bentuk gelombang ini tidak khas untuk stenosis dan
dapat ditemukan juga untuk spasme arteri yang berhubungan
dengan perdarahan subarakhnoid atau perdarahan
intraserebral ringan sampai sedang (Gambar 4) (Syme, 2006).
Signal TCD yang terlihat pada arteri yang lebih besar
pada bagian proksimal dari clot bervariasi tergantung dari
ukuran obstruksi di bagian distal dan dekatnya dengan clot.
Dengan oklusi cabang distal yang kecil, pembuluh darah
utama yang memberi nutrisi dapat terlihat normal secara
khusus dengan sirkulasi kolateral yang baik. Ketika oklusi
yang lebih besar terjadi, signal juga dapat menjadi
“dampened” dengan pengurangan intensitas, kecepatan dan
PI yang sangat kecil. Dengan adanya obstruksi yang lebih
berat di bagian distal, signal pada pembuluh darah nutrisi
(feeding vessel) yang ukurannya lebih besar menunjukkan
gambaran kasar “blunting” yang lebih jauh lagi (Gambar 4)
dengan perubahan yang kecil dalam intensitas tetapi
penurunan yang lebih jauh lagi dalam kecepatan dan
pulsatility. Penurunan pulsatility sepertinya berkaitan dengan
dilatasi bagian proksimal arteri dan mencerminkan elastisitas
dari arteri ini serta ketersediaan cabang-cabang pembuluh
melalui proksimal arteri berkaitan dengan oklusi tersebut
(Syme, 2006).
Transcranial doppler memiliki positive predictive value
yang tinggi >80% sehingga membuat TCD dijadikan sebagai
alat yang dapat menilai kejadian serebrovaskular pada pasien
dengan risiko stroke. Transcranial doppler juga dapat
digunakan untuk mengetahui efektivitas penanganan
trombolitik pada pasien stroke (Kassab dkk, 2007).
B. Menilai autoregulasi serebrovaskular
Autoregulasi serebral adalah kemampuan untuk
mempertahankan aliran darah serebral meskipun menit ke
menit berbeda rata-rata perfusi serebral. Pada status fisiologis
orang normal, hal ini dapat dicapai dengan kontrol arteriolar
melalui resistensi vaskular serebral perifer. Seseorang dengan
autoregulasi serebral yang terganggu memiliki gejala klinis
seperti nyeri kepala, dizziness, sinkop (Kassab dkk, 2007).
Pengukuran FV dan PI sebelum dan selama minum
obat-obatan atau manipulasi mekanikal autoregulasi dan
tekanan darah sistemik dapat digunakan untuk memonitor
reaktivitas vaskularisasi intrakranial. Breath holding dan
pemakaian acetazolamid adalah yang terbanyak digunakan
untuk memanipulasi autoregulasi serebral. Tehnik
asimptomatik stenosis arteri karotid internal yang diindikasikan
untuk bedah endarterectomy. Data terbaru menunjukkan TCD
dapat menilai gangguan autoregulasi peningkatan risiko stroke
iskemik pada pasien dengan stenosis karotid yang berat
(>70%). Transcranial doppler juga dapat menilai risiko
potensial iskemik serebral pada pasien dengan stenosis
karotid yang akan menjalani tindakan anastesi dan
pembedahan (Kassab dkk, 2007).
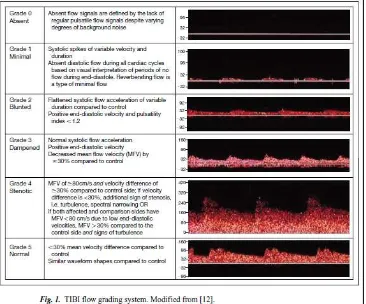
Gambar 4 : TIBI flow grading system
Dikutip dari : Mikulik R., Alexandrov A.V.2006. Acute Stroke: Therapeutic Transcranial Doppler Sonography. Handbook on Neurovascular
7. HUBUNGAN INDEKS MASSA TUBUH DENGAN KECEPATAN ALIRAN DARAH PADA PENDERITA STROKE ISKEMIK, HIPERTENSI DAN DM TIPE 2
Obesitas ditandai dengan lemak tubuh yang berlebih sehingga
menyebabkan masalah kesehatan. Baru-baru ini, rekomendasi the
National Cholesterol Education Program Adult Treatment Panel III
(NCEP-ATPIII) dan the Seventh Report of the Joint National
Committee on Prevention, Detection, Evaluation, and Treatment of
High Blood Pressure (JNC 7) untuk mengidentifikasi dan mengobati
orang dewasa dengan sindrom metabolik menekankan perlunya
pengobatan agresif untuk mengurangi risiko yang berkaitan dengan
penyakit kardiovaskular (Smith dkk, 2012).
Jaringan adiposa tidak lagi dilihat sebagai sebuah repositori pasif
untuk penyimpanan triasilgliserol dan menjadi sumber asam lemak
bebas (Free Fatty Acids / FFAs). Pre-adiposit berkembang menjadi
adiposit matur. Adiposit matur merupakan organ parakrin dan endokrin
aktif yang mensekresi sejumlah mediator untuk proses metabolisme.
Senyawa yang mempengaruhi adipogenesis diantaranya lipoprotein
lipase, cholesterol ester transfer protein, angiotensinogen, faktor
komplemen, interleukin-6 (IL-6), prostaglandin, Tumor Necrosis
Factor-α (TNF-α), dan Nitric Oxide (NO) (Smith dkk, 2012).
Jaringan adiposa diakui sebagai sumber yang kaya mediator
vaskular, resistensi insulin dan aterogenesis. Yang termasuk
adipositokin pro-inflamasi atau adipokin diantaranya TNF-α, IL-6,
leptin, Plasminogen Activator Inhibitor-1 (PAI-1), angiotensinogen,
resistin, dan C-Reactive Protein (CRP) (Gambar 5). Di sisi lain, NO
dan adiponektin memberikan perlindungan terhadap inflamasi dan
resistensi insulin yang berkaitan dengan obesitas (obesity-linked
insulin resistance) (Gambar 5) (Smith dkk, 2012).
Gambar 5. Adipokin Anti- dan Pro-Inflamatori. Jaringan adiposa kaya akan mediator pro-inflamator seperti TNF-α, IL-6, leptin, PAI-1, angiotensinogen, resistin dan CRP, yang memicu disfungsi endotel, resistensi insulin dan akhirnya aterosklerosis. Produksi adiposit lain seperti NO dan adiponektin merupakan proteksi, tetapi kemampuan ini menurun bila terjadi obesitas.
Diunduh dari : Smith, M., M., Minson, C., T., 2012. Obesity and Adipokines : Effect on Sympathetic Overactivity. J Physiol. 590(8);1787-1801
Aterosklerosis adalah proses inflamasi yang dimulai dengan
disfungsi endotel. Disfungsi endotel ditandai dengan
vasokonstriksi. Nitric oxide mempertahankan vasodilatasi endotel dan
melawan efek vasokonstriktor seperti Endotelin (ET)-1 dan
Angiotensin II (ANG II). Nitric oxide menginhibisi leukosit serta aktivasi
dan agregasi trombosit, bersama dengan prostasiklin, membantu
menjaga endotelium sebagai barrier non-trombotik. Respon terhadap
pemicu inflamasi seperti Vascular Cell Adhesion Molecule-1 (VCAM-1)
dan Intercellular Adhesion Molecule-1 (ICAM-1), yang mengakibatkan
adhesi endotel dan permeabilitas meningkat sehingga leukosit masuk
dan ekspresi adhesi molekul di endotelium. Adiposit menghasilkan
Monocyte Chemoattractant Protein-1 (MCP-1) yang dapat membantu
perpindahan leukosit. Fagositosis dari partikel Low-Density Lipoprotein
(LDL) teroksidasi oleh monosit menimbulkan pembentukan sel-sel
busa (foam cells) dan pembentukan plak dan fatty streaks serta
proliferasi sel otot polos. Dengan demikian disfungsi endotel
merupakan gambaran utama berbagai tahapan aterogenesis, dari
perkembangan awal aterosklerotik dari fatty streaks hingga plak
ateromatous, plak yang rentan dan mudah ruptur, vasospasm,
pembentukan trombus, dan akhirnya oklusi pembuluh darah dan infark
(Smith dkk, 2012).
Levi dkk (2001) dalam penelitiannya menyatakan bahwa
penyebab terbanyak stroke iskemik adalah oklusi arteri besar, yang
berhubungan dengan trombosis dan emboli. Dan menurut Seo dkk
dan peningkatan RI pada penderita stroke iskemik diakibatkan oleh
kekakuan (stiffness), dilatasi dan lika-liku arteri.
Brown dkk (2008) dalam penelitiannya menyatakan bahwa
disfungsi vaskular akibat terganggunya sintesis oksida nitrit (nitric
oxide synthase-dependent) di pembuluh darah otak cenderung
menurunkan aliran darah otak serta meningkatkan risiko komplikasi
STROKE
massa tubuh, serta lingkar pinggang dan panggul.
Brown dkk (2008) dalam penelitiannya menyatakan bahwa disfungsi vaskular akibat terganggunya sintesis oksida nitrit (nitric oxide
synthase-dependent) di pada pasien dengan diabetes tipe 2.
Tekanan darah merupakan tekanan perfusi yang secara langsung mempengaruhi aliran darah serebral. Menurut penelitian Zhang dkk (2006) terhadap subyek dengan hipertensi awal (<5 tahun) dan hipertensi kronik (≥5 tahun) yang berusia 42 – 73 tahun mendapati pengaruh hipertensi terhadap aliran darah otak yaitu bahwa aliran darah di arteri serebri media berkorelasi positif terhadap tekanan darah sistolik dan sedikit berkorelasi negatif pada arteri karotis komunis. Seo dkk (2009) dalam
penelitiannya terhadap 38 orang penderita stroke iskemik dan 10 orang penderita Transient Ischemic blood flow velocity pada arteri
9. Kerangka Konsep