Titik Didih, Mendidih dan Titik Didih Normal dalam Kimia
Fisika
A. Perbedaan dari titi didih, mendidih dan titik didih normal
Titik didih adalah suhu (temperatur) dimana tekanan uap sebuah zat cair sama dengan tekanan external yang dialami oleh cairan. Titik didih suatu zat adalah suhu yang tekanan uap jenuhnya sama dengan tekanan di atas permukaan zat cair. Titik Didih suatu zat cair dipengaruhi oleh tekanan udara, artinya makin besar tekanan udara makin besar pula titik didih zat cair tersebut. Sebuah cairan di dalam vacuum akan memiliki titik didih yang rendah dibandingkan jika cairan itu berada di dalam tekanan atmosphere. Cairan yang berada di dalam tekanan tinggi akan memiliki titik didih lebih tinggi jika dibandingkan dari titik didihnya di dalam tekanan atmosphere.
Titik Didih Cairan adalah suhu di mana Point fase cair dan uap berada dalam kesetimbangan dengan satu sama lain pada tekanan tertentu. Oleh karena itu, titik didih adalah suhu dimana tekanan uap cairan sama dengan tekanan diterapkan pada cairan. Titik didih pada tekanan 1 atmosfer disebut titik didih normal. Untuk substansi murni pada tekanan P tertentu, fase stabil adalah fase uap pada temperatur tepat di atas titik didih dan fase cair pada temperatur langsung di bawah titik didih. Garis kesetimbangan cair-uap pada diagram fase zat murni memberikan titik didih sebagai fungsi dari tekanan. Atau, baris ini memberikan tekanan uap cairan sebagai fungsi temperatur.
Titik didih normal (juga disebut titik didih atmospheris) dari sebuah cairan merupakan kasus istimewa dimana tekanan uap cairan sama dengan tekanan atmospher di permukaan laut, satu atmosphere. Pada suhu ini, tekanan uap cairan bisa mengatasi tekanan atmospher dan membentuk gelembung di dalam massa cair. Pada saat ini (per 1982) Standar Titik Didih yang ditetapkan oleh IUPAC adalah suhu dimana pendidihan terjadi pada tekanan 1 bar.Pada tekanan dan temperatur udara standar(76 cmHg, 25 °C) titik didih air sebesar 100 °C.
menuju permukaan bebas cairan. Selama bergerak naik tersebut gelembung uap akan memindahkan sebagian panas ke cairan sekitarnya. Karena gerak gelembung dan juga gerakan cairan itu sendiri yang menyebabkan besarnya laju perpindahan panas pada proses pendidihan. Pendidihan selalu membutuhkan panas dari sekitarnya. Atau dengan kata lain proses pendidihan menyerap panas dari sekitarnya. Contohnya adalah proses pendidihan di evaporator pada suatu lemari pendingin atau pendingin ruang. Udara yang melewati evaporator akan menjadi dingin karena diambil panasnya untuk mendidihkan refrigeran (’freon’).
B. Kenaikan Titik Didih
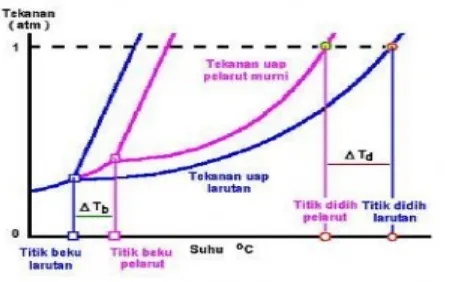
Hasil eksperimen Roult menunjukan bahwa Kenaikan titik didih larutan akan semakin besar apabila konsentrasi (molal) dari zat terlarut semakin besar. Titik didih larutan akan lebih tinggi dari titik didih pelarut murni. Hal ini juga diikuti dengan penurunan titik beku pelarut murni, atau titik beku larutan lebih kecil dibandingkan titik beku pelarutnya. Hasil eksperimen ini disederhanakan dalam Gambar 11.4.
Gambar 11.4. Diagram tekanan dan suhu untuk titik didih dan titik beku dari pelarut dan larutan
Roult menyederhanakan ke dalam persamaan
Tb = kb . m
Tb = kenaikan titik didih larutan
kb = tetapan kenaikan titik didih molal pelarut (kenaikan titik didih untuk 1 mol zat dalam 1000 gram pelarut)
Perubahan titik didih atau ΔTb merupakan selisih dari titik didih larutan dengan titik didih pelarutnya, seperti persamaan : ΔTb = Tb – Tbº.
Hal yang berpengaruh pada kenaikan titik didih adalah harga kb dari zat pelarut. Kenaikan tidak dipengaruhi oleh jenis zat yang terlarut, tapi oleh jumlah partikel/mol terlarut khususnya yang terkait dengan proses ionisasinya.
Untuk zat terlarut yang bersifat elektrolit persamaan untuk kenaikan titik didik harus dikalikan dengan faktor ionisasi larutan, sehingga persamaannya menjadi :
dimana
n = jumlah ion-ion dalam larutan
α = derajat ionisasi
Contoh jumlah ion untuk beberapa elektrolit:
HCl → H+ + Cl-, jumlah n = 2
H2SO4 → 2 H+ + SO42-, jumlah n = 3
H3PO4 → 3 H+ + PO43-, jumlah n = 4
Agar mudah dimengerti kita ambil perhitungan kenaikan titik didih untuk zat non-elektrolit dan non non-elektrolit sebagai perbandingannya.
Sebuah larutan gula C6H12O6 dengan konsentrasi sebesar 0.1 molal, jika pelarutnya air dengan harga kb = 0.52 °C/molal. Tentukan titik didih larutan tersebut.
Larutan gula tidak mengalami ionisasi sehingga,
C6H12O6 → C6H12O6
0.1 molal → 0.1 mola
ΔTb = kb . m
ΔTb = 0.052oC
Diketahui titik didih air adalah 100°C, maka titik didih larutan adalah
ΔTb = Tb – Tb0
Tb = 100 + 0.052
Tb = 100.052
C. Aplikasi Kegunaan dari Titik Didih dalam Pertambangan 1. Proses Operasi di dalam Kilang Minyak
Minyak mentah yang baru dipompakan ke luar dari tanah dan belum diproses umumnya tidak begitu bermanfaat. Agar dapat dimanfaatkan secara optimal, minyak mentah tersebut harus diproses terlebih dahulu di dalam kilang minyak.
Minyak mentah merupakan campuran yang amat kompleks yang tersusun dari berbagai senyawa hidrokarbon. Di dalam kilang minyak tersebut, minyak mentah akan mengalami sejumlah proses yang akan memurnikan dan mengubah struktur dan komposisinya sehingga diperoleh produk yang bermanfaat.
Secara garis besar, proses yang berlangsung di dalam kilang minyak dapat digolongkan menjadi 5 bagian, yaitu:
a. Proses Distilasi, yaitu proses penyulingan berdasarkan perbedaan titik didih; Proses ini berlangsung di Kolom Distilasi Atmosferik dan Kolom Destilasi Vakum.
b. Proses Konversi, yaitu proses untuk mengubah ukuran dan struktur senyawa hidrokarbon. Termasuk dalam proses ini adalah:
1. Dekomposisi dengan cara perengkahan termal dan katalis (thermal and catalytic cracking)
2. Unifikasi melalui proses alkilasi dan polimerisasi
3. Alterasi melalui proses isomerisasi dan catalytic reforming
c. Proses Pengolahan (treatment). Proses ini dimaksudkan untuk menyiapkan fraksi-fraksi hidrokarbon untuk diolah lebih lanjut, juga untuk diolah menjadi produk akhir.
d. Formulasi dan Pencampuran (Blending), yaitu proses pencampuran fraksi-fraksi hidrokarbon dan penambahan bahan aditif untuk mendapatkan produk akhir dengan spesikasi tertentu.
e. Proses-proses lainnya, antara lain meliputi: pengolahan limbah, proses penghilangan air asin (sour-water stripping), proses pemerolehan kembali sulfur (sulphur recovery), proses pemanasan, proses pendinginan, proses pembuatan hidrogen, dan proses-proses pendukung lainnya.
Tahap awal proses pengilangan berupa proses distilasi (penyulingan) yang berlangsung di dalam Kolom Distilasi Atmosferik dan Kolom Distilasi Vacuum. Di kedua unit proses ini minyak mentah disuling menjadi fraksi-fraksinya, yaitu gas, distilat ringan (seperti minyak bensin), distilat menengah (seperti minyak tanah, minyak solar), minyak bakar (gas oil), dan residu. Pemisahan fraksi tersebut didasarkan pada titik didihnya.
Kolom distilasi berupa bejana tekan silindris yang tinggi (sekitar 40 m) dan di dalamnya terdapat tray-tray yang berfungsi memisahkan dan mengumpulkan fluida panas yang menguap ke atas. Fraksi hidrokarbon berat mengumpul di bagian bawah kolom, sementara fraksi-fraksi yang lebih ringan akan mengumpul di bagian-bagian kolom yang lebih atas.