BAB II
TINJAUAN PUSTAKA
2.1. Anatomi dan Histologi Paru
Sistem pernafasan tumbuh dari dinding depan foregut, dan epitel laring, trakea, bronkus dan
alveoli berasal dari endoderm. Komponen tulang rawan, otot dan jaringan konektif berasal dari
mesoderm. Setelah fase pseudoglandular (5-16 minggu) dan kanalikular (16-26 minggu), sel
epitel kubus yang melapisi bronkiolus berubah menjadi tipis berupa sel gepeng yang disebut sel
epitel alveolar tipe I, yang langsung berhubungan dengan kapiler pembuluh darah dan limfe.
Sebelum bayi lahir, paru akan terisi cairan dengan sedikit protein, mukus dan surfaktan yang
dihasilkan oleh sel epitel alveolar tipe II. Cairan akan teresorbsi sesaat setelah pernafasan
dimulai kecuali surfaktan yang menjaga alveoli tidak kolaps.11
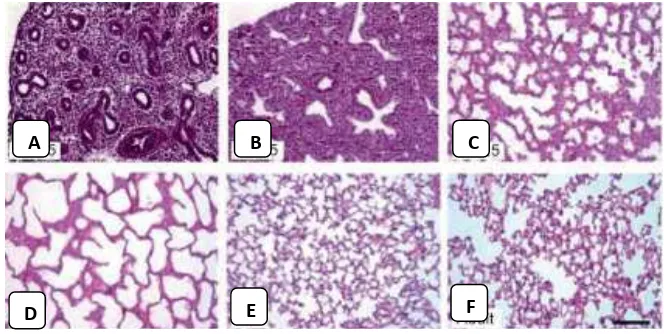
Gambar 2.1 . Histologi paru tikus pada tahap perkembangan embrional. Perkembangan mulai dari fase pseudoglandular (A) berlanjut ke fase canalicular (B) dan
akhirnya fase terminal sac (C dan D). Selanjutnya terjadi alveolarisasi dengan terbentuk banyak
septa-septa (E). Akhirnya terbentuk struktur mirip sarang lebah yang matur dengan alveoli
disekeliling saluran alveolar seperti yang terlihat pada struktur paru dewasa (F) 12 D
C B
A
Bronkus utama kanan lebih lebar, lebih pendek dan lebih vertikal dibandingkan yang kiri,
dengan ukuran panjang sekitar 1 inchi (2,5cm), berjalan langsung ke akar paru setinggi T5.
Sebelum bergabung dengan paru melalui hilus, bronkus utama kanan memberikan cabang ke
lobus atas paru. Bronkus utama kiri mempunyai panjang hampir 2 inchi (5cm), berbeda dengan
yang kanan, saluran ini tidak memberikan cabang sampai memasuki hilus paru setinggi T6.
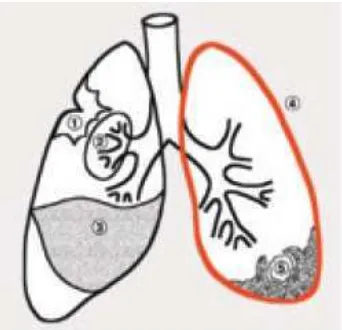
Kedua paru masing-masing mempunyai bentuk seperti kerucut dengan apeks yang tumpul
kira-kira setinggi sternum dan iga pertama, sedangkan dasar yang konkaf berada di atas diafragma.
Paru kanan sedikit lebih besar daripada paru kiri, terbagi atas tiga lobus, yaitu atas, tengah dan
bawah, yang dipisahkan oleh fissura obliqua dan horizontal. Paru kiri hanya terdiri dari dua buah
lobus yang dipisahkan oleh fissura obliqua.13
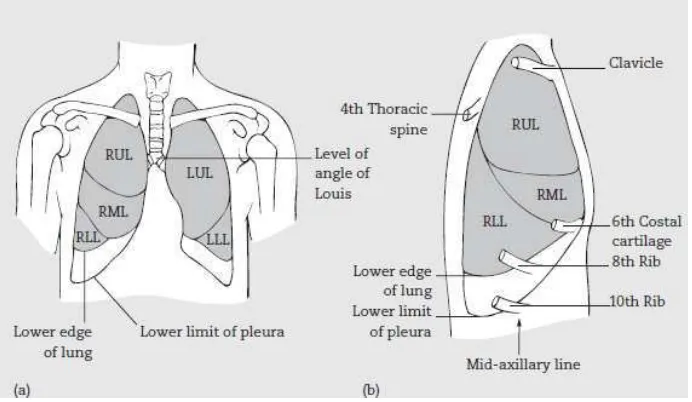
Gambar 2.2. Anatomi paru14
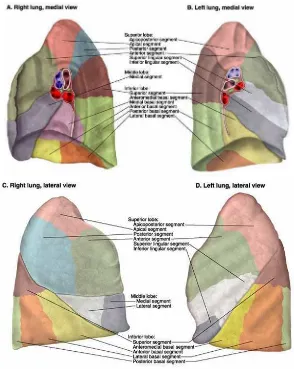
Tiap lobus masing-masing paru terbagi atas sejumlah segmen bronkopulmonar, yang disuplai
dengan bagian puncak berada di hilus dan basis pada permukaan paru. Penamaan tiap segmen
bronkopulmonar berasal dari bronkus segmental yang mensuplainya. Mengetahui dengan baik
struktur anatomi bronchial tree, merupakan pengetahuan dasar yang harus dimiliki dalam
radiologi paru dan sangat membantu dalam interpretasi bronkoskopi maupun tindakan reseksi
segmen paru.13
2.2. Kanker paru
2.2.1. Epidemiologi
Kanker paru merupakan keganasan yang paling banyak terdiagnosa di Amerika Serikat pada
tahun 2010. Tercatat 222.520 kasus terdiagnosa pada tahun tersebut. Kematian akibat penyakit
ini juga cukup tinggi, sekitar 157.300 kematian pada tahun 2010. Umur rata-rata saat
terdiagnosis adalah 71 tahun dan ketahanan hidup lima tahun adalah 16,4%. Menurut data SEER
17, insidensi kanker paru dan bronkus adalah 62,5 per 100.000 orang pertahun dari 2003-2007.1
Sedangkan menurut data Kementerian Kesehatan RI berdasarkan data Sistem Informasi Rumah
Sakit (SIRS) tahun 2007 kasus kanker bronchus dan paru pada pasien rawat inap sebesar 5,8%
dari seluruh jenis kanker.16
Data yang didapatkan antara tahun 2003 dan 2007, diperkirakan 14% kasus kanker paru
merupakan small cell carcinoma, dan setelah dilakukan konfirmasi ulang pada pemeriksaan
histologis didapati 85% merupakan non small cell carcinoma.1
2.2.2 Etiologi dan Faktor Risiko
1) Asap rokok.
Faktor risiko terpenting pada kanker paru adalah merokok tembakau, yang telah lama
dikemukakan melalui penelitian di berbagai institusi oleh berbagai kelompok peneliti. Terdapat
hubungan yang bermakna antara risiko kanker paru dengan durasi merokok, banyaknya rokok
yang dihisap perhari, derajat inhalasi dan umur awal merokok. 1,17,18 Tipe dari rokok juga turut
Lingkungan asap rokok yang terbentuk akibat ekshalasi asap rokok para perokok serta asap yang
berasal dari hasil pembakaran tembakau juga menjadi faktor risiko penting. Asap yang berasal
dari hasil pembakaran tembakau diketahui mempunyai komposisi karsinogenik yang lebih tinggi
dibandingkan asap hasil ekshalasi. Penelitian membuktikan bahwa perokok pasif meningkatkan
risiko untuk mendapatkan kanker paru. 1,17
Kecenderungan umur muda dalam menderita kanker paru juga cukup mendapat perhatian, selain
berperannya faktor genetik, hal lain adalah adanya paparan yang berlangsung dini dan
bertahun-tahun terhadap seorang anak, dapat berupa paparan asap rokok, bahan kimia tertentu dan
lain-lain. Penelitian membuktikan bahwa perokok pasif meningkatkan risiko untuk mendapatkan
kanker paru. 1,17 Isu lain yang saat ini marak dibicarakan adalah thirdhand smoke (THS), yaitu
risiko pada orang yang tidak merokok, terutama pada anak-anak yang selalu kontak dengan
permukaan benda-benda yang terkontaminasi dengan residu dan partikel asap rokok. Zat yang
terhirup berupa reaksi di atmosfer oleh O3, nitrous acid (HONO), NOx dengan residu asap rokok
yang melekat pada permukaan perabot, dinding, kulit, pakaian; keseluruhan merupakan sumber
polutan yang terhirup selama bertahun-tahun. 19
2)Paparan di tempat kerja
Beberapa paparan bahan tertentu yang berkaitan dengan pekerjaan diduga juga menjadi faktor
risiko untuk kanker paru, yaitu paparan terhadap asbestos, beberapa logam (nikel, arsenik,
cadmium, timah hitam), silika, dan radiasi terionisasi.17
Beberapa paparan bahan yang jarang didapati juga meningkatkan risiko kanker paru antara lain
3)Radon
Radon (222Rn) suatu gas radioaktif tidak bewarna, tidak berbau, terbentuk akibat pengrusakan
uranium alami yang didapati pada bebatuan dan tanah sekitar pemukiman dan pertambangan
bawah tanah. Diperkirakan bahwa paparan akibat Radon menjadi penyebab kanker paru nomor
dua terbanyak pada negara maju.17,18
4)Diet
Beberapa penelitian telah dilakukan untuk membuktikan adanya hubungan antara berbagai
macam diet makanan dengan risiko terjadinya kanker paru. Penelitian menemukan bahwa tidak
dijumpai hubungan antara risiko kanker paru dengan asupan lemak dan kolesterol. Asupan buah
dan sayuran telah lama diyakini dapat mengurangi risiko kanker paru, tetapi penelitian
menunjukkan bahwa efek proteksi dari buah dan sayuran belum terbukti secara bermakna.
Demikian juga dengan hubungan antara kanker paru dan konsumsi alkohol, hingga kini belum
ada hasil penelitian menunjukkan adanya hubungan yang bermakna.17
Adanya sinergisme yang terjadi pada paparan dua atau lebih agen secara simultan, akan lebih
meningkatkan terjadinya risiko kanker paru yang lebih besar. Merokok dengan bahan tembakau
akan menjadi faktor risiko kanker paru jika berada dalam lingkungan yang juga mendukung
terjadinya interaksi dengan agen eksogen lain, misalnya asbestos, radiasi terioniasasi, arsenik,
silika dan faktor makanan.17
5) Status sosioekonomi
Sejumlah kecil penelitian telah dilakukan untuk melihat hubungan antara kanker paru dengan
tingkat pendidikan dan jenis pekerjaan turut mempengaruhi risiko terjadinya kanker paru.
Demikian juga hasil penelitian di Kanada terhadap responden pria menunjukkan hasil yang
sama. Terlihat perbedaan mendasar pada status merokok pada dua kelompok masyarakat, yaitu
pada masyarakat dengan tingkat pendidikan yang rendah dan status pekerjaan tanpa keahlian
yang cukup maka cenderung lebih sering merokok dibandingkan dengan kelompok masyarakat
dengan kelas sosial dan pendidikan lebih tinggi.17
6)Mutasi gen p53 supresor tumor
Penelitian menunjukkan bahwa mutasi gen p53 supresor tumor ditemukan secara bermakna pada
tumor dari subyek yang terpapar asap rokok tembakau dibanding subyek yang tidak terpapar.17
7)Jenis kelamin dan ras
Sementara penelitian sebelumnya telah menemukan bahwa terdapat perbedaan antara risiko
kanker paru antara pria dan wanita perokok, maka beberapa penelitian terkini justru tidak
mendukung hasil sebelumnya, yaitu efek karsinogenik rokok pada paru didapati sama pada pria
dan wanita.1
Kanker paru dijumpai meningkat pada etnis kulit hitam dibandingkan dengan etnuis lainnya di
Amerika Serikat, dan hal ini disebabkan tingginya konsumsi tembakau pada etnis tersebut. Tidak
ada bukti yang kuat mengenai perbedaan etnis dengan kecenderungan untuk karsinogenesis paru
akibat tembakau. 1
8)Virus
Virus juga terbukti memainkan peran penting dalam proses timbulnya kanker paru. Large cell
mempunyai hubungan dengan perkembangan kanker paru. Terdapat perbedaan geografis untuk
keterlibatan virus ini, di Jerman virus HPV terdeteksi sebanyak 4,2%, sedangkan di daerah
tertentu di Asia didapati sebanyak 80%.18
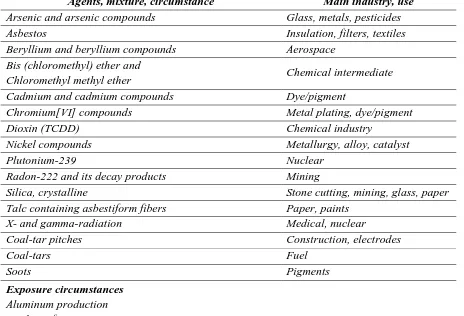
Tabel 2.1. Agen-agen di tempat kerja yang diakui sebagai karsinogen paru oleh International Agency for Research on Cancer (IARC)1
Agents, mixture, circumstance Main industry, use
Arsenic and arsenic compounds Glass, metals, pesticides
Asbestos Insulation, filters, textiles
Beryllium and beryllium compounds Aerospace Bis (chloromethyl) ether and
Chloromethyl methyl ether Chemical intermediate
Cadmium and cadmium compounds Dye/pigment
Chromium[VI] compounds Metal plating, dye/pigment
Dioxin (TCDD) Chemical industry
Nickel compounds Metallurgy, alloy, catalyst
Plutonium-239 Nuclear
Radon-222 and its decay products Mining
Silica, crystalline Stone cutting, mining, glass, paper Talc containing asbestiform fibers Paper, paints
X- and gamma-radiation Medical, nuclear
Coal-tar pitches Construction, electrodes
Haematite mining (underground) with exposure to radon Iron and steel founding
2.2.3. Biologi Molekuler Kanker Paru
Saat ini telah diketahui bahwa proses karsinogenesis paru merupakan proses tahapan multipel
yang melibatkan perubahan genetik yang saling berkesinambungan, terjadi pada sel epitel
bronkus hingga mencapai transformasi menjadi sel kanker. Beberapa pembuktian penelitian juga
menunjukkan bahwa abnormalitas genetik juga telah dijumpai pada tampilan sel-sel bronkus
normal, tidak hanya penderita kanker paru, tetapi pada individu tanpa penyakit kronis dan
mantan perokok, sebagai akibat efek genotoksis asap rokok tembakau.20
Tabel 2.2. Frekuensi perubahan molekuler pada kanker paru20
Alteration Small cell lung cancer Non small cell lung cancer
Receptor tyrosine kinases c-kit 70% EGFR overexpression: 90% (SCC); 50% (ADC) HER2/neu: 30% (ADC) MET point mutations (rare) MET overexpression: 25%
RAS point mutations - 10–30% (ADC)
MYC family amplification 65% high level 50% low level
p53 inactivation 75–100% 50%
Rb inactivation 90% 15–30%
p16INK4A inactivation 0–10% 30–40%
FHIT inactivation 80% 50–70%
3p, 9p, 13q, 17p allelic loss 90% 70%
Bcl2 overexpression 75–90% 30%
SCC=squamous cell carcinoma; ADC=adenocarcinoma;
EGFR=epidermal growth factor receptor; Rb=retinoblastoma gene; FHIT=Fragile histidine triad.
Berdasarkan asal histologinya, diketahui ketiga tipe kanker paru yaitu small cell carcinoma,
selanjutnya berkemampuan untuk berdiferensiasi menjadi sel silia dan sel mukus, yang dapat
tumbuh menjadi adenocarcinoma sentral, dan kemungkinan besar juga menjadi sel
neuroendokrin pada bronkiolus terminal. Unit respirasi terminal yang terdiri dari kompartemen
perifer bronkiolus dan alveolus, tumbuh menjadi adenocarcinoma perifer, dan berasal dari sel
puncaputatif yang berkemampuan untuk memperbaharui diri dan berproliferasi, yaitu sel punca
bronkoalveolar, lebih dikenal sebagai Clara cell (mengekspresikan CC10) dan type-II
pneumonocytes (mengekspresikan surfaktan dan TTF-1). Kanker paru pada non perokok tumbuh dari kompartemen perifer oleh suatu karsinogen eksogenus yang belum dapat diidentifikasi,
seperti yang ditemukan pada perokok pasif.21
2.2.4. Klasifikasi Kanker Paru
Menurut klasifikasi WHO 2004, secara histologi kanker paru terbaggi atas tumor epitel ganas,
tumor mesenkim, tumor limfoproliferatif, dan tumor lainnya.22
Klasifikasi ini merupakan sistem standar dalam mengklasifikasikan morfologi kanker paru
sekaligus yang pertama mempertimbangkan parameter genetik dalam mengkarakteristikkan
setiap subtipe. Beberapa entiti campuran menjadi lebih jelas, seperti combined small cell
carcinoma yang mempunyai proporsi non-small cells; adeno squamous carcinoma (adenocarcinoma dan squamous cell carcinoma); atau carcinosarcoma. Demikian juga
adenocarcinoma yang juga mempunyai tipe campuran berdasarkan pola pertumbuhannya. Keragaman dari kanker paru menimbulkan masalah dalam evaluasi diagnostik. Entiti campuran,
heterogenitas tumor dan terjadinya transisi fenotip pada subtipe tumor menunjukkan
ketidakstabilan genetik yang meningkat, yang juga bertanggungjawab atas meningkatnya
Tabel 2.3. Klasifikasi WHO 2004 untuk tumor epitel paru malignan1
Klasifikasi ini selanjutnya sangat berperan dalam konsistensi terapi, karena berdasarkan pada
penelitian epidemiologi dan biologi. Berdasarkan hal tersebut pula maka kanker paru dapat
dikatagorikan atas empat katagori besar, yaitu: Squamous cell carcinoma (25% - 40%),
Klasifikasi kanker paru melalui pemeriksaan sitologi diatas dapat dikelompokkan sebagai
berikut:
Tabel 2.4. Klasifikasi Sitologi Kanker Paru Primer dan Tumor Lainnya24
Squamous carcinoma
Solid carcinoma with mucin formation Papillary carcinoma
Atypical carcinoid (well-differentiated neuroendocrine carcinoma) Large-cell carcinoma with endocrine differentiation
Rare carcinomas
Secara sitologi, klasifikasi kanker paru dikelompokkan pada 5 kelompok utama sebagai berikut:
1) Karsinoma dengan tampilan dominan diferensiasi skuamus, dikelompokkan pada squamous
bronkus atau alveoli, diklasifikasikan sebagai adenocarcinoma bronkogenik dengan berbagai
tipe atau sebagai bronchoalveolar carcinoma; 3) Karsinoma yang terdiri atas sel-sel kecil tidak
terdiferensiasi, menyerupai sel basal dari epitel bronkus, termasuk dalam kelompok small cell
carcinoma atau squamous cell carcinoma; 4) Karsinoma yang terdiri dari sel-sel besar yang tidak berdiferensiasi atau berdiferensiasi buruk, beberapa dapat menunjukkan diferensiasi
kelenjar atau skuamus atau bahkan gambaran endokrin; 5) Karsinoma tipe yang jarang, termasuk
tumor dengan gambaran endokrin. 2
Hal terpenting dalam penegakan diagnosis kanker paru dengan sediaan sitologi adalah
menegakkan diagnosa yang akurat antara small cell carcinoma dan diferensiasinya dengan tumor
lainnya yaitu NSCC. Pembedaan ini penting karena berhubungan dengan penatalaksanaan terapi;
small cell carcinoma sangat responsif terhadap iradiasi dan kemoterapi yang merupakan pilihan terapinya; sedangkan kanker paru lainnya (kecuali limfoma malignan) terbaik diterapi dengan
pembedahan.24
Para pakar molekuler, radiologi, histomorfologi dan klinisi telah merumuskan klasifikasi baru
interdisiplin untuk adenocarcinoma paru melalui suatu konsensus dari International Agency for
the Study of Lung Cancer (IASLC) dan American Thoracic Society (ATS), serta European Respiratory Society (ERS) pada tahun 2011. Klasifikasi baru ini didasarkan pada prinsip pembedaan histomorfologi tidak hanya antara subtipe dengan prognosis yang berbeda, tetapi
juga defek genetik dan respon terapi. Pada klasifikasi ini, preinvasive lesions (atypical
Tabel 2.5. Klasifikasi multidisiplin dari karsinoma paru oleh International Association for the Study of Lung Cancer, American Thoracic Society and European
Respiratory Society 201125
2.2.4.1. Small Cell Carcinoma
Small cell carcinoma merupakan tumor epitel ganas dengan agresifitas yang tinggi, pertumbuhan yang cepat dan metastasis luas sehingga sangat jarang diterapi dengan pembedahan. Tumor ini
dapat menginduksi endocrine paraneoplastic syndromes karena dapat memproduksi secara aktif
berbagai variasi yang luas dari hormon-hormon polipeptida, termasuk adrenocorticotropin
(ACTH), antidiuretic hormone, parathormone, calcitonin, dan gonadotropins. Sindroma klinis yang ditimbulkan termasuk, Cushing's syndrome, retensi air, hipo dan hiperkalsemia,
dan serebelar. Hal ini menjadi perhatian penting saat pasien menunjukkan gejala endocrine
paraneoplastic syndromes, maka perlu dipikirkan adanya tumor ganas, dan sitologi memegang peran penting untuk mengevaluasi hal tersebut. Berkaitan dengan hal diatas, maka diyakini
bahwa small cell carcinoma merupakan bagian dari tumor-tumor neuroendokrin.24
Klasifikasi sebelumnya memberikan terminologi tumor ini sebagai oat cell carcinoma, small cell
anaplastic carcinoma, undifferentiated small cell carcinoma, intermediate cell type, dan mixed small cell/large cell carcinom, dan selanjutnya terminologi ini tidak digunakan lagi.22
Gambaran klinis. Tumor ini hampir keseluruhan diderita oleh perokok, dengan proporsi perempuan lebih banyak dibanding laki-laki, dijumpai hampir lebih dari setengah kasus. Secara
umum SCLC respon terhadap kemoterapi sehingga harus benar-benar dibedakan dengan jenis
non small cell lung carcinoma.26
Staging tumor. Pengelompokan staging tumor pada SCLC lebih sering memakai limited disease dan extensive disease dibandingkan dengan sistem TNM, walaupun penyesuaian data pada
sistem TNM telah dilakukan, dikarenakan SCLC merupakan tumor high-grade dengan
penyebaran yang cepat. Pada limited disease (30%-40% pasien), tumor terbatas pada ipsilateral
hemithorax dan dalam port radioterapi tunggal (sesuai sebagian untuk TNM stadium sampai I
hingga IIIB). Sedangkan pada extensive disease (60%-70% pasien), ditemukan bukti metastasis
diluar dari ipsilateral hemithorax.26
Makroskopis tumor. Tumor mempunyai gambaran tipikal berupa masa di perihilar bewarna putih kecoklatan, lunak, gembur dan menunjukkan nekrosis yang ekstensif dan sering melibatkan
dan membentuk gambaran melingkar serta sering melibatkan limfatik. Sebanyak hampir 5%
small cell carcinoma tampak berupa lesi koin di perifer.22,26
Sitologi. Gambaran sitologi menunjukkan kelompokan sel dengan kohesi rendah, tidak teratur atau tersebar, juga tampak sel-sel individual tumor tersusun dalam pola linier.22 Pada pembesaran
rendah, sel-sel tumor sering dimisinterpretasikan dengan limfosit.24 Pada kelompokan sel dengan
kohesifitas lebih erat tampak gambaran nuclear moulding. Mitosis sangat mudah dijumpai.
Masing- masing sel tumor mempunyai rasio inti/ sitoplasma yang meningkat dengan pinggiran
inti tidak teratur. Pada sediaan sitologi yang baik akan tampak sebaran halus kromatin inti yang
memberikan gambaran klasik berupa “salt and pepper”, sedangkan pada sediaan yang jelek
tampak gambaran inti berkromatin biru gelap tanpa struktur yang jelas. Penonjolan anak inti
jarang bahkan tidak dijumpai. Gambaran serpihan-serpihan kromatin inti sering dijumpai pada
sediaan hapus disebabkan kerapuhan inti sel kanker, terutama pada biopsi aspirasi dan sikatan
bronkus. Latar belakang hapusan biasanya mengandung badan-badan apoptotik dan sebaran
debris nekrotik. 22,24
Histopatologi. Ukuran sel tumor biasanya lebih kecil dari ukuran tiga buah limfosit. Sel tumor mempunyai bentuk inti bulat, oval, atau spindel, kromatin inti bergranul halus dengan sitoplasma
sedikit. Batas sel biasanya tidak jelas, dan inti molding merupakan gambaran yang lazim
dijumpai. Gambaran lain yang penting untuk penegakkan diagnosa adalah tidak dijumpainya
anak inti, walaupun pada sel-sel tumor berukuran besar dapat juga dijumpai anak inti yang
menonjol. Mitosis sangat mudah dijumpai, rata-rata sekitar 60 mitosis persepuluh lapangan
neuroendokrin dapat dijumpai, yaitu berupa pola sarang, trabekula, palisading perifer dan
formasi roset, walaupun pola lembaran yang sama sekali tidak menyerupai pola tumor
neuroendokrin sering juga dijumpai. Kombinasi SCLC dijumpai kurang dari 3%, biasanya
berupa squamous cell, adenocarcinoma, or large cell carcinoma; dapat ditemukan walaupun
jarang berupa spindle cell atau giant cell carcinoma.24,26
Pewarnaan khusus dan imunohistokimia. Secara umum SCLC terwarnai dengan sitokeratin (termasuk CK7) dan EMA. Sekitar 90% SCLC mengekspresikan TTF-1, dan 90% SCLC juga
mengekspresikan positif untuk satu atau lebih penanda neuroendokrin,, serta kurang dari 10%
dari SCLC mengekspresikan negatif penanda neuroendokrin.26
Diagnosis molekuler. Delesi dari kromosom 3p merupakan temuan konsisten pada SCLC dan daerah ini mencakup rapuhnya fragile histidine triad gene (FHIT) yang berlokasi di 3p14.2.
Sekitar 20% SCLC menunjukkan mutasi pada gen Rb, dan sekitar 70%-95% SCLC
menunjukkan ekspresi positif Bcl-2. Selain itu SCLC menunjukkan mutasi p53 yang paling
tinggi dari seluruh kanker paru, sehingga tampilan pewarnaan p53 yang kuat pada inti di hampir
10%-20% sel tumor mengindikasikan adanya suatu mutasi dari p53.26
Small cell carcinoma terkadang sulit dibedakan dari SCC varian small cell atau adenocarcinoma yang mempunyai ukuran sel yang relatif kecil-kecil. Gambaran yang paling membantu untuk
membedakannya adalah tekstur kromatin yang halus,, anak inti tidak menonjol, nuclear
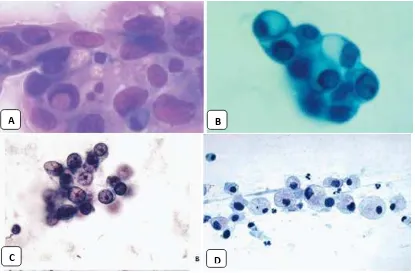
Gambar 2.4. Small cell carcinoma
Gambaran sitologi (A) dan histopatologi (B dan C) tampak sel-sel dengan sitoplasma sedikit, inti
moulding dengan kromatin bergranul halus tanpa anak inti. Mitosis sering dijumpai.21 Pada gambar C tampak sel-sel tumor yang mirip dengan limfosit, tetapi mempunyai ukuran 2 kali
besar limfosit.24
2.2.4.2. Non Small Cell Carcinoma (NSCC)
Terminologi NSCC secara umum diberikan pada berbagai tipe karsinoma bronkogenik, yaitu
tumor yang berasal dari epitel pelapis bronkus, yang meliputi adenocarcinoma, SCC dan large
cell carcinoma tidak terdeferensiasi. Pemisahan antara small cell carcinoma dan NSCC didasarkan pada perbedaan terapi penanganan pada keduanya.27
1) Adenocarcinoma
Adenocarcinoma paru merupakan tumor ganas epitel dengan diferensiasi kelenjar atau produksi musin, menunjukkan struktur asiner, papiler, bronkoalveolar atau solid dengan gambaran
produksi musin atau campuran dari keseluruhan struktur.28
Makroskopis tumor. Tumor berupa masa tunggal atau nodular dengan berbagai ukuran, timbul pada sentra hilus ataupun perihilus di bronkus. Tumor bewarna coklat keabu-abuan, padat
dengan beberapa area nekrosis. Tumor dapat bertumbuh dengan salahsatu dari enam pola
pertumbuhan, meliputi pola: 1) Perifer, terjadi retraksi desmoplastik dari pleura diatasnya
menimbulkan gambaran pengkerutan tanpa jaringan parut; 2) Endobronchial adenocarcinoma;
3) Pneumonia-like consolidation, berhubungan dengan pola papillary; 4) Visceral pleural-based,
pseudomesotheliomatous carcinoma; 5) Adenokarsinoma yang tumbuh di latarbelakang yang mendasari fibrosis dan 6) Diffuse bilateral lung disease. Penetrasi pleura menyebabkan
penyebaran ke arah rongga pleura, efusi pleura dan kadang-kadang invasi pada dinding dada.26
Gambar 2.5. Pola pertumbuhan makroskopik adenocarcinoma28
Pola 1: tipe tersering: adenocarcinoma perifer dengan pembentukan fibrosis desmoplastik meretraksi pleura diatasnya. Pola 2: adenocarcinoma sentral atau endobronkial. Pola 3: diffuse
pneumonia-like, terjadi konsolidasi yang sering berhubungan dengan pertumbuhan bronkoalveolar atau papiler. Pola 4: penebalan pleura yang difus, terjadi pada
pseudomesotheliomatous carcinoma.
Sitologi. Diagnosa adenocarcinoma pada sitologi didasarkan pada kombinasi dari ciri individual sel serta pola kelompokan sel. Sel-sel adenocarcinoma dapat terlihat tunggal atau berupa
gambaran morula tiga dimensi, berstruktur asiner, pseudopapiler, papiler sejati dengan
jelas satu sama lain. Gambaran sitoplasma bervariasi tapi biasanya dijumpai dalam jumlah
banyak dengan tipikal bewarna kebiruan dan lebih translusen jika dibandingkan dengan
squamous cell carcinoma. Umumnya sitoplasma bewarna homogen atau bergranul halus dan beberapa tampak adanya vakuola kecil-kecil yang samar dalam jumlah banyak. Pada beberapa
kasus dapat dijumpai vakuola berisi musin pada sitoplasma sehingga mendesak inti ke pinggir
menunjukkan gambaran signet-ring cell. Inti biasanya berbentuk bulat hingga oval, tunggal,
eksentrik dan relatif berkontur licin, dengan kromatin bergranul halus dan tersebar merata pada
tumor dengan diferensiasi baik, selanjutnya akan tampak kasar dan bergumpal serta
hiperkromatik pada yang berdiferensiasi buruk. Anak inti umumnya menonjol dengan
karakteristik tunggal, besar, dengan kontur bervariasi mulai dari bulat dan licin hingga ireguler.
Beberapa studi menunjukkan keterkaitan antara pleomorfisme pada gambaran sitologi dengan
grading histologi tumor , dan sebagian dengan besarnya tumor. Morishita et al menyimpulkan
bahwa sel-sel bronchoalveolar carcinoma mempunyai diameter kurang dari 2cm serta relatif
kecil dan bulat hingga oval jika dibandingkan dengan sel-sel adenocarcinoma (yang invasif )
berukuran kecil.28,29
Sediaan dari sikatan bronkus mempunyai nilai penting dalam mendapatkan sampel kecil dari
adenocarcinoma. Pada sediaan yang adekuat, sel-sel tumor ditemukan lebih banyak dibandingkan dari aspirat atau bilasan bronkus. Sel-sel umumnya tampak berupa kelompokan
papiler, atau lembaran yang terdiri dari sel-sel besar berbentuk bulat atau poligonal. Pada
adenocarcinoma yang memproduksi mukus, tampak vakuola mukus yang besar menekan inti, memberikan gambaran seperti sel goblet. Beberapa sel tumor menyerupai sel bronkus bersilia
menonjol dan sering multipel, dan yang paling terpenting adalah ketiadaan silia. Kanker bersilia
sangat jarang dijumpai.24
Gambar 2.6. Sitologi adenocarcinoma24
A. Inti sel ganas berbentuk oval dengan membran inti licin, terkadang tampak kromatin yang
tersebar dengan anak inti kecil dan pseudoinklusi inti yang besar. B. Sekelompok sel tumor dari
sputum penderita karsinoma bronkoalveolar tipe musinos. Sel mempunyai inti relatif kecil dan
samar dengan pinggir licin, kromatin halus dan anak inti tidak menonjol. Rasio inti-sitoplasma
rendah dengan vakuola musin menempati hampir keseluruhan sitoplasma.(pewarnaan
Papanicolaou). C. Sekelompok sel-sel tumor yang saling bertumpangtindih, dengan sitoplasma pucat dan sedikit, inti relatif besar, kromatin halus dan anak inti menonjol. D. Sel kanker dengan
sitoplasma banyak dan bervakuola mirip dengan histiosit, tetapi dapat dibedakan berdasarkan
abnormalitas inti termasuk anak inti yang menonjol.
Histopatologi. Sejak sistem klasifikasi adenokarsinoma yang baru diberlakukan oleh International Association for the Study of Lung Cancer, American Thoracic Society, dan
A B
European Respiratory Society (IASLC/ATS/ERS), komponen micropapillary ditetapkan sebagai
subtipe baru, ditambahkan dengan subtipe lainnya yaitu lepidic, acinar, papillary, dan solid
yang sebelumnya telah ditetapkan oleh klasifikasi World Health Organization (WHO) 2004.30
Subtipe histolologi mayor berupa:
1) Subtipe acinar: asini dan tubulus dibentuk oleh sel-sel kuboid dan kolumnar menyerupai
kelenjar bronkus dengan produksi musin;26
2) Subtipe papillary: tumor soliter berbentuk papiler yang dibatasi sel-sel atipik, dengan inti
membesar, hiperkromatik, anak inti menonjol dan mitosis yang cukup mudah dijumpai. Papila
sering menunjukkan pola percabangan sekunder dan tersier menggantikan struktur paru.
Beberapa kasus menunjukkan adanya psammoma bodies, dan pada kasus yang sangat jarang
tampak psammoma bodies dikelilingi oleh sel-sel tumor. Pola pertumbuhan papiler harus
dibedakan dengan tumor lain yang bermetastasis;24,26,29
3) Subtipe micropapillary. Dikatakan suatu komponen mikropapiler adalah jika ditemukan
pertumbuhan sel tumor dengan pola papiler tetapi tanpa adanya fibrovascular cores, dan
terapung dalam ruangan alveolar. Gambaran ini sering disebut dengan aerogenous
micropapillary component (AMPC).Komponen mikropapiler yang ada pada karsinoma paru ini berbeda dengan komponen mikropapiler yang ada pada keganasan organ lain, misalnya payudara
atau kandung kemih, yaitu invasi komponen mikropapiler berada di dalam stroma, sehingga
sering disebut dengan stromal invasive micropapillary component (SMPC). Walau demikian
SMPC ini dapat juga ditemukan pada karsinoma paru walaupun jarang, dan diketahui adanya
4) Subtipe lepidic. Pada pola ini menunjukkan pertumbuhan sel tumor sepanjang struktur
alveolar tanpa dijumpai stroma, pembuluh darah atau invasi pleura. Pola pertumbuhan ini
dibedakan atas varian musinus dan non musinus. Pada varian non musinus tampak pelebaran
septa disertai sklerosis, juga ditandai dengan adanya sel Clara dan atau sel tipe II yang
mengalami diferensiasi. Sel Clara merupakan sel kolumnar dengan tonjolan sitoplasma bewarna
eosinofilik pucat. Sel tipe II merupakan sel kuboidal atau dome-shaped dengan sitoplasma
bervakuola halus, jernih hingga berbusa. Sel-sel tampak berupa gambaran seperti bola tanpa
moulding interseluler. Terkadang tampak gambaran struktur papiler. Inti bentuk bulat hingga oval dengan kromatin halus tersebar, dengan anak inti dapat dijumpai walau tidak menonjol.Sel
kadang-kadang menunjukkan vakuola berisi sekret. Varian musinus ditandai dengan sel-sel
kolumnar tinggi dengan inti di basal dan sitoplasma pucat, yang terkadang menyerupai sel
goblet, dengan banyaknya musin intrasitoplasma yang bervariasi. Gambaran khas adalah adanya
kolam musin disekeliling ruang alveolar.26,28,29
5) Subtipe solid. Pada pola ini tidak dijumpai papil, tubulus dan asini, hanya tampak lembaran
yang terdiri sel-sel poligonal dengan paling sedikit dijumpai lima sel positif musin pada setiap
dua lapangan pandang besar. Beberapa varian dapat dijumpai pada subtipe ini antara lain colloid,
fetal dan enteric. Fetal adenocarcinoma, disebut juga well differentiated fetal adenocarcinoma, pulmonary adenocarcinoma of fetal type, pulmonary endodermal tumour resembling fetal lung.
Tipe ini merupakan varian adenocarcinoma yang terdiri dari elemen kelenjar dengan tubulus
berisi glycogen-rich dengan sel-sel tak bersilia, mirip dengan tubulus pada paru fetus. Adanya
dijumpai gambaran morula berbentuk bulat yang terdiri dari sel-sel bentuk poligonal dengan
sitoplasma banyak bergranul halus eosinofilik. 26,28
Colloid (mucinous) adenocarcinoma, disebut demikian karena adanya kesamaan dengan saluran cerna, berupa kolam musin yang berisi pulau-pulau sel-sel epitel tumor, terkadang tampak
terapung dan beberapa dengan gambaran well differentiated.28
Pada varian enteric, termasuk di dalamnya signet ring adenocarcinoma paru, berupa gambaran
asiner yang fokal bercampur dengan subtipe histologis lain dari adenocarcinoma terdiri atas
sel-sel tumor dengan sitoplasma bervakuola yang banyak berisi musin dan inti terdorong ke pinggir.
Pemeriksaan yang cermat sangat penting dilakukan untuk menyingkirkan kemungkinan
metastasis terutama dari saluran cerna.26,28
Varian lainnya adalah clear cell adenocarcinoma paru, berupa pola yang fokal dan sangat jarang
menjadi komponen mayor dari tumor paru. Pada kasus seperti ini penting untuk menyingkirkan
Gambar 2.7 Gambaran mikroskopis komponen mikropapiler pada adenokarsinoma paru31 A. Komponen mikropapiler berupa sel tumor yang terapung dalam ruang alveolar (AMPC). B.
Komponen mikropapiler dalam stroma (SMPC). A dan B pembesaran 100xx, C dan D
pembesaran 400x.(pewarnaan dengan hematoxyllin-eosin (HE))
Pewarnaan khusus dan imunohistokimia. Produksi musin dapat diketahui dengan pewarnaan mucicarmine, PAS, atau Alcian blue stains. Sel-sel tumor pssitif terwarnai dengan penanda
epitel CAM5.2, pancytokeratin AE1/AE3, epithelial membrane antigen (EMA),
carcinoembryonic antigen (CEA), Leu-M1, Ber-Ep4, dan B72.3/BRST-3/TAG-72.
Adenokarsinoma biasanya mengekspresikan CK7 lebih sering dibanding CK20. Penanda TTF-1
diekspresikan pada sekitar 75%--95% adenokarsinoma paru.7,26
Selanjutnya adanya komponen predominan mikropapiler pada adenokarsinoma paru
menunjukkan peningkatan insidensi metastasis kelenjar getah bening dan prognosis yang buruk.
Adanya komponen mikropapiler di stroma (stromal micropapillary component/ SMPC) pada
adenokarsinoma paru sangat jarang ditemui, dan dihubungkan dengan prognosis yang buruk. 31
Sistem grading yang menggabungkan antara persentase antara pola solid dengan derajat atipia
inti pada sitologi merupakan prediktor independen terhadap ketahanan hidup pasien penderita
adenokarsinoma paru.30,32
Gambar 2.8. Gambaran histopatologi subtipe adenokarsinoma paru33
A. Lepidic (non musinus). B. Lepidic (musinos). C. Acinar. D. Papillary. E. Micropapillary.
E. Solid (pewarnaan hematoxyllin-eosin, (HE) dengan pembesaran 100x)
Para pakar molekuler, radiologi, histomorfologi dan klinisi telah merumuskan klasifikasi baru
interdisiplin untuk adenocarcinoma paru melalui suatu konsensus dari International Agency for
Respiratory Society (ERS) pada tahun 2011. Klasifikasi baru ini didasarkan pada prinsip pembedaan histomorfologi tidak hanya antara subtipe dengan prognosis yang berbeda, tetapi
juga defek genetik dan respon terapi. Pada klasifikasi ini, preinvasive lesions (atypical
adenomatous hyperplasia, adenocarcinoma in situ (AIS), dan minimally invasive adenocarcinoma (MIA) mempunyai prognosis yang sangat baik.18
Penelitian sebelumnya meneliti penggunaan klasifikasi baru dari IASLC/ATS/ERS terhadap
pasien yang sebelumnya telah diketahui prognostiknya dan karakteristik tumor yang diderita
masing-masing pasien menunjukkan adanya korelasi dengan ketahan hidup 5 tahun. Klasifikasi
baru ini diyakini tidak hanya memberikan kepentingan terhadap perawatan pasien , tetapi juga
untuk seleksi dan pengelompokkan pasien yang lebih baik untuk penelitian klinis dan
molekuler.34
2) Squamous cell carcinoma (SCC)
Squamous cell carcinoma merupakan tumor epitel ganas yang menunjukkan keratinisasi dan atau jembatan interseluler yang berasal dari epitel bronkus.Tumor ini jugadikenal dengan karsinoma
epidermoid. Klasifikasi WHO membagi tumor ini atas Squamous cell carcinoma, Papillary
carcinoma, Clear cell carcinoma, Small cell carcinoma, dan Basaloid carcinoma.35
Lebih dari 90% SCC diderita oleh perokok,pada pria dan wanita diatas 50 tahun.Arsen juga
diketahui mempunyai hubungan dengan timbulnya SCC. Lokasi tumor ini didapati pada bagian
Diagnosis melalui pemeriksaan sitologi sputum atau sekresi bronkus dapat ditegakkan dengan
cepat dan akurat, walaupun tumor tidak terlihat pada pemeriksaan bronkoskopi. Sel kanker
skuamus tampak menyerupai epitel sel skuamus, tetapi berbeda pada beberapa gambaran, yaitu:
a) Sel kanker skuamus bervariasi dalam bentuk dan besar, yang ditemukan pada latarbelakang
peradangan dan nekrosis, bahkan dapat dijumpai gambaran bizzare. Sel kanker berbentuk spindel
dan tadpole cukup sering dijumpai dan hal ini menjadi karakteristik tumor ini.; b) Sitoplasma sel
tumor memproduksi keratin yang tampak berupa warna jingga terang atau kuning pada
pewarnaan Papanicolaou yang dapat terlihat pada pembesaran kecil. Pada sel yang mengalami
kariolisis maka warna jingga atau kuning tampak memudar, tampak berupa batas samar inti atau
bahkan inti tidak tampak sama sekali. Pada keadaan sel tanpa inti, keberadaan ghost cells ini
pada sputum atau spesimen bronkus mengindikasikan, walau tidak sepenuhnya, adanya
keganasan; c) Abnormalitas inti yang khas berupa hiperkromatik tidak selalu dijumpai pada
semua SCC. Beberapa sel kanker mempunyai inti yang pucat, terutama pada yang keratinizing
dan sel yang mengalami nekrotik dan selanjutnya kariolisis; d) Gambaran fagositosis sel kanker
oleh sel kanker, tampak berupa multinucleated squamous cancer yang jarang dijumpai, yaitu
Tabel 2.6. Perbedaan gambaran sitologi SCC pada spesimen sputum, sikatan bronkus dan aspirasi biopsi transbronkial24
Gambaran Sitologi Sputum Sikatan bronkus dan aspirasi biopsi transbronkial
Gambaran sel kanker
Gambaran sitologi non keratinizing SCC atau epidermoid berbeda dalam hal warna sitoplasma,
yaitu bewarna basofilik, atau amfofilik dan lebih transparan, dengan sitoplasma tidak sebanyak
keratinizing SCC. Inti hiperkromatik dengan kromatin kasar dan anak inti dapat terlihat.24
Gambaran sitologi SCC varian small cell berupa sel-sel berukuran kecil jika dibandingkan
dengan sel-sel yang biasa dijumpai pada SCC. Gambaran pada varian ini dapat dibedakan
dengan small cell carcinoma berdasarkan kromatin inti yang lebih kasar, anak inti yang lebih
menonjol dan batas sel yang jelas.2
Gambaran sitologi SCC varian basaloid, adalah berupa sel-sel yang membentuk palisading
Gambar 2.9. Sitologi SCC24
Sediaan sputum (A) dan bronkus (B) menunjukkan sel kanker dengan latar belakang peradangan.
Sel mempunyai bentuk dan besar bervariasi dengan sitoplasma eosinofilik padat, relatif
membesar, inti hiperkromatik. Tampak sel kanker berbentuk spindel dan elongasi pada (B), dan
sel tadpole pada (C). “Ghost” cells pada bilasan bronkus mengindikasikan suatu SCC (D)
.
Sebagian besar SCC dapat dibedakan dengan adenocarcinoma berdasarkan ciri masing-masing
tipe, yaitu adanya keratinisasi, musin ataupun struktur kelenjar, tetapi pembedaan ini menjadi
lebih sulit pada poorly differentiated SCC. Secara umum kromatin inti lebih bertekstur pada
adenocarcinoma, dan lebih kasar pada SCC. Sitoplasma lebih tipis dan bervakuola pada adenocarcinoma dan lebih padat pada SCC. Histokimia untuk mengenali musin (mucicarmine dan periodic acid-Schiff-D) dan imunohistokimia p63 dapat membantu membedakan hal
tersebut. Walaupun pada SCC terkadang didapati sebagian kecil musin intra sel, tetapi
A B
didapatinya musin dalam jumlah banyak akan mengarahkan pada diagnosa adenocarcinoma,
sedangkan p63 merupakan tipikal untuk SCC. Kemungkinan didapatinya kedua komponen ini
dapat dijumpai, misalnya pada adenosquamous carcinoma. Jika masih didapati kesulitan untuk
membedakan hal tersebut, maka interpretasi berupa “Non–small cell carcinoma” lebih
dianjurkan.2
3) Large Cell Carcinoma
Large cell carcinoma merupakan NSCC yang tidak terdiferensiasi, tanpa gambaran sitologi dan struktur dari small cell carcinoma dan kelenjar atau diferensiasi skuamus. Large cell carcinoma
sebelumnya dikenal dengan large cell anaplastic carcinoma dan large cell undifferentiated
carcinoma. Sedangkan terminologi large cell neuroendocrine carcinoma (LNEC) dideskripsikan pada tahun 1991, basaloid carcinoma pada tahun 1992, dan large cell carcinoma
serta LNEC dikenal sebagai dua entitas yang berbeda pada klasifikasi WHO di tahun 1999.36
Large cell carcinoma tidak mempunyai gambaran sitologi yang spesifik. Umumnya membentuk gambaran agregasi sel-sel yang cukup banyak, sangat sedikit dijumpai gambaran yang tersebar.
Pinggir membran sel umumnya tidak berbatas jelas, sehingga sel-sel tampak berpola sinsisium
yang berserakan. Inti sel bervariasi , mulai dari bulat hingga sangat ireguler, dengan sebaran
kromatin inti yang tidak teratur. Anak inti umumnya sangat menonjol. Sitoplasma bewarna
basofilik, biasanya sangat sedikit dengan rasio inti sitoplasma meningkat. Gambaran sitologi
LNEC menunjukkan palisade inti dan moulding, dan hal ini dapat dibedakan dengan small cell
sel-sel, dapat dijumpai gambaran palisade inti pada pinggir kelompokan. Gambaran sitologi
lymphoepithelioma-like carcinomas menunjukkan lembaran sel-sel berpola sinsisium dengan kohesifitas erat, dengan sel bentuk spindel, inti besar dan soliter dengan anak inti sangat besar,
bercampur dengan sejumlah besar limfosit.29,36
Gambar 2.10. Large cell carcinoma36
A. Spesimen dari sikatan bronkus, tampak sel-sel ganas denganstruktur berkelompok dengan
kohesifitas rendah. Inti mempunyai membran tebal dan ireguler, kromatin kasar dan
berkelompok serta anak inti ireguler dan menonjol. Pewarnaan Papanicolaou. B. Large cell
carcinoma perifer dengan fokus nekrosis di tengah bewarna putih kekuningan, jaringan ikat di tengah dan pigmentasi. C Histopatologi: sel tumor yang besar dengan sitoplasma banyak dan inti
membesar, kromatin vesikuler dan anak inti menonjol. Tidak dijumpai diferensiasi kelenjar dan
skuamus.
Gambaran histopatologi large cell carcinoma, sesuai dengan definisinya, menggambarkan
diferensiasi yang buruk. Diagnosis ini ditegakkan setelah menyingkirkan adanya gambaran SCC,
adenocarcinoma dan small cell carcinoma, yaitu berupa lembaran atau sarang-sarang yang berisi sel-sel besar berbentuk poligonal, dengan inti vesikuler dan anak inti menonjol dan sitoplasma
dalam jumlah sedang.36
2.2.5. Gejala dan Diagnostik Kanker Paru
Penderita kanker paru mengalami sesak nafas yang progresif, batuk, nyeri dada, suara serak atau
kehilangan suara, hemoptisis (terutama pada SCC). Pnemonia yang biasanya sering residif
merupakan profil umum yang dijumpai pada paseien kanker paru. Adenocarcinoma merupakan
lebih sering tanpa gejala jika dibanding dengan tipe NSCC lainnya, dan sering ditemukan
insidental pada saat dilakukan foto ronsen toraks. Penderita small cell carcinoma berbeda dalam
banyak hal dengan NSCC, berupa gejala yang timbul akibat metastasis jauh. Sekitar 10% pasien
small cell carcinoma menderita sindroma vena kava superior. Stridor dan hemoptisis jarang dijumpai pada penderita small cell carcinoma, sebaliknya gejala akibat meluasnya penyakit
sering ditemukan, seperti kehilangan berat badan, nyeri abdomen akibat keterlibatan hepar,
adrenal dan pankreas serta nyeri akibat metastase ke tulang. Metastasis ke otak dijumpai pada
Tabel 2.7. Penanda tumor pada serum penderita kanker paru (kiri) dan tehnik pencitraan dalam menentukan stadium kanker paru37
2.2.6. Stadium dan Tingkatan Kanker Paru
Penentuan stadium dan tingkatan tumor paru primer berdasarkan pada besar,lokasi dan jauhnya
invasi lokal. CT Scann lebih akurat dibandingkan foto toraks dalam mengevaluasi hal di atas, dan
biasanya digunakan sebagai pemeriksaan utama setelah seseorang didiagnosa menderita kanker
paru. CT Scann maupun MRI, keduanya bermanfaat dalam mengkonfirmasi invasi pada rongga
dada secara umum ataupun pada medistinum, tetapi tidak akurat untuk membedakan gambaran
anatomi secara lebih terperinci serta invasi halus.38
Stadium pada small cell carcinoma dapat dibedakan atas dua stadium, sebagai berikut:1) Limited
kontralateral, atau supraklavikular, (b) Penderita small cell carcinoma dengan metastasis ke
kelenjar getah bening mediastinum kontralateral dan supraklavikular dengann prognosis lebih
baik dibandingkan metastasis ke organ jauh, (c) Penderita small cell carcinoma dengan efusi
pleura ipsilateral (benigna ataupun maligna), 2) Extensive stage, yaitu seluruh penderita yang
tidak dapat dimasukkan dalam katagori limited stage.22
Tabel. 2.8. Stadium dan Tingkatan Kanker Paru1
Stadium pada NSCC pada tabel 2.8 diatas mengacu pada sistem TNM, yaitu
temuan laboratorium, radiologi sampel jaringan, sedangkan stadium histopatologi mencakup data
tumor yang telah direseksi seperti tingkatan histologi, batas tumor dan invasi limfovaskuler.37
Metastasis jauh (M1) dilaporkan terjadi sebesar 11-36% pada penderita NSCC.38
2.2.7. Penatalaksanaan Terapi
Seperti telah diketahui sebelumnya bahwa penataksanaan terapi untuk small cell carcinoma
adalah terapi sistemik, disebabkan kecenderungan tumor ini untuk bermetastase, sehingga
penatalaksanaan terapi yang akan dibicarakan dibawah ini adalah untuk NSCC yang meliputi
beberapa standar terapi tergantung pada stadium tumor .
Terapi standar untuk NSCC stadium dini adalah pembedahan, umumnya berupa lobektomi atau
pnemonektomi. Mayoritas penderita yag memang telah mempunyai profil kesehatan yang buruk,
misalnya perokok berat, dengan berujung pada penyakit paru dan kardioveskular, menjadikan
operasi sebagai kontraindikasi, baik relatif maupun absolut. Berkenaan dengan hal tersebut
beberapa penelitian dilakukan untuk mencari alternatif terapi selain operasi pada
keadaan-keadaan seperti di atas, yaitu sebagai berikut: 1) Radiasi sinar eksternal dengan fraksionasi
konvensional atau terapi radiasi stereotaktik tubuh; 2) Brachytherapi; 3) Ablasi radioterapi; 4)
Krioterapi; 5) Elektrokauter; 6) Terapi laser; 7) Terapi fotodinamik.39
Penatalaksanaan terapi untuk NSCC dikelompokkan berdasarkan stadium tumor menganut pada
1)Stadium IA-IIB
Reseksi bedah merupakan terapi dengan peluang terbaik pada penderita stadium dini I-II
NSCC, berdasarkan bukti beberapa seri penelitian yang telah dilakukan. Penderita NSCC
stadium IIB(T3, N0), dengan adanya invasi dinding dada harus menjalani reseksi disusul
dengan kemoterapi. Pasien yang menjalani reseksi komplit satdium IIA dan IIB diterapi
dengan Cisplatin sebagai terapi ajuvandikombinasi dengan Vinorelbine atau Etoposide.40
2)Stadium IIIA
Pada stadium IIIA, jika didapati N2 sebelum operasi, maka terapi berupa kemoradioterapi
dengan regimen bertahap Cisplatin dan Vinblastine diikuti dengan radiasi, dan kemungkinan
reseksi operasi. Jika didapati N2 setelah operasi, maka terapi selanjutnya adalah kemoterapi
bertahap diikuti dengan radiasi. Pada (T4, N0-N1) dengan invasi langsung ke jantung,,
esofagus, pembuluh darah besar, nervus recurrent laryngeal, corpus vertebra atau karina,
maka diterapi dengan kemoradiasi secara bersamaan.40
3)Stadium IIIB
Reseksi tidak dapat dilakukan pada (T4, N2-3). Pada pasien dengan status performa baik,
maka direkomendasikan terapi radiasi bersamaan dengan Cisplatin, sedangkan pada status
performa yang buruk maka cukup terapi radiasi saja.40
4)Stadium IV
Pasien NSCC stadium IV yang diketahui sebelum operasi akan memiliki pilihan terapi yang
pleurodesis, catheter drainage, dan pericardial window disusul dengan terapi sistemik. Pasien
dengan metastasis ke otak yang terisolasi (M1b) menunjukkan perbaikan dengan reseksi dan
radiasi seluruh otak.40
Saat ini berbagai terapi target terus dikembangkan berdasarkan pada sifat biologi molekuler
tumor, seperti mutasi pada K-Ras, EGFR, dan ALK .40
2.2.8. Prognosis
Prognosis kanker paru meningkat tajam ketika kanker direseksi pada tahap dini.40 Pengamatan
rata-rata ketahanan hidup pasien penderita NSCC per stadium, menunjukkan SCC lebih baik
secara bermakna dibandingkan adenocarcinoma. Lebih dari 80% penderita SCC pada stadium
reseksi 1(T1 N0 M0) hidup selama lima tahun setelah didiagnosa, dibandingkan dengan
npenderita adenocarcinoma pada stadium yang sama hanya sebanyak 70%.35
2.3. Pemeriksaan Diagnostik dengan Bronkoskopi
2.3.1. Bronkoskopi
Bronkoskopi merupakan prosedur medis untuk memeriksa bronkus atau percabangan paru-paru
untuk tujuan diagnostik dan terapetik. Alat yang digunakan dalam prosedur ini disebut
bronkoskop, yaitu sejenis endoskop, yang merupakan instrumen untuk pemeriksaan organ dalam
yaitu Bronkoskopi Kaku (Rigid) dan fiber optic bronchoscopy/ Bronkoskopi Serat Optik Lentur.
(BSOL). 41,42
Berbagai penelitian yang dilakukan menggunakan prosedur ini menunjukkan bahwa bronkoskopi
merupakan prosedur yang aman dengan tingkat kematian sangat rendah berkisar dari 0% hingga
1%. Saat ini bahkan bronkoskopi dapat dilakukan dengan aman pada pasien penderita infark
miokard dengan syarat pasien tidak mengelami iskemia pada selama prosedur berlangsung.
Walaupun demikian komplikasi dapat terjadi selama maupun sesudah prosedur dilakukan.43
A. Bronkoskopi rigid
Bronkoskopi rigid merupakan alat yang berbentuk tabung lurus terbuat dari bahan stainless steel.
Panjang dan lebar bervariasi, tetapi bronkoskopi untuk dewasa biasanya berukuran panjang 40
cm dan diameter berkisar 9-13,5 mm, tebal dinding bronkoskop berkisar 2-3 mm. Tindakan ini
harus dilakukan oleh bronchoscopist yang berpengalaman di ruang operasi dengan penderita di
bawah anestesi umum. Bronkoskopi rigid diindikasikan pada penderita dengan obstruksi saluran
nafas besar yang tidak memungkinkan untuk penggunaan FOB. Indikasi umum lainnya adalah:
1) Mengeluarkan benda asing dari saluran trakeobronkial; 2) Mengontrol dan penanganan batuk
darah masif; 3) Penanganan obstruksi saluran nafas akibat neoplasma; 4) Penanganan stenosis
Gambar 2.11. Bronkoskopi kaku (rigid)46
B. Bronkoskopi serat optik lentur (BSOL)
BSOL pertama kali diperkenalkan oleh S. Ikeda pada tahun 1964. Sejak saat itu BSOL menjadi
alat diagnostik dan terapetik penting dalam penatalaksanaan penyakit di rongga dada dan
selanjutnya berkembang sebagai suatu prosedur diagnostik invasif paru.43 Saat ini BSOL diakui
sebagai standar emas dalam mendeteksi dan mendiagnosis kelainan pada trakeobronkial dengan
adanya visualisasi langsung pada lumen jalan nafas.47
Sejak bronkoskopi diperkenalkan lebih hampir 100 tahun yang lalu, pengembangan terus
dilakukan untuk melimitasi kemampuan dalam memastikan lokasi nodul, masa, infiltrat dari paru
maupun nodus limfatikus, untuk pengambilan jaringan yang tepat dan menghindari intervensi
bedah yang tidak perlu.48
Saat ini penggunaan bronkoskop telah dikembangkan dengan berbagai teknik pengambilan
spesimen dalam pemeriksaan sitologi maupun histopatologi, yaitu dengan bronchoalveolar
Tehnik pengambilan spesimen tersebut adalah berupa:
1) Bilasan bronkus (bronchial washing). Prosedur ini berupa tindakan membilas daerah bronkus dan cabang-cabangnya dengan bantuan kateter atau fasilitas suction yang ada pada
bronkoskop. Bilasan bronkus dilakukan dengan menggunakan cairan salin atau ringer yang
dialirkan melalui saluran yang ada pada bronkoskop ke dalam bronkus yang dijumpai
kelainan dan disedot kembali. Jumlah cairan yang dialirkan 3-5 ml dan dapat diulang
beberapa kali. Sekret yang diperoleh dilakukanpemeriksaan sitologi cairan bronkus.4,50
2) Sikatan bronkus (bronchial brushing). Spesimen diperoleh dengan menggunakan kateter, sikat dan jarum, sampel yang didapat selanjutnya diperiksa secara sitologi.4,50
3) Bronchoalveolar Lavage (BAL). BAL bertujuan untuk mengambil spesimen yang terletak
pada ujung saluran nafas (alveolus). Cairan salin atau ringer dimasukkan ke ujung scope
bronkoskop kemudian disedot. Tindakan ini diulang beberapa kali sampai didapat sampel
100-300 ml untuk mendapatkan material yang cukup dari alveolus. Sampel yang didapat
selanjutnya akan dilakukan pemeriksaan mikrobiologi dan sitologi.4,50
4) Biopsi endobronkial. Biopsi dapat dilakukan dengan menggunakan forcep, yang terletak pada ujung bronkoskop dekat dengan bidang visual lesi. Sampel yang didapat selanjutnya
akan dilakukan pemeriksaan histopatologi.4,50
5) Transbronchial Needle Aspiration (TBNA). Prosedur ini merupakan tindakan invasif
minimal yang bertujuan untuk menegakkan diagnosis dan stage bronchogenik carcinoma
dengan cara mengambil sampel kelenjar limfe mediastinum dengan menggunakan jarum atau
forcep, yaitu dengan menembus trakeobronkus menggunakan jarum atau forcep menembus lesi/kelainan yang menekan trakeobronkial (trakea, bronkus utama, karina dan karina dua).
American Thoracic Society (ATS) membuat suatu sistem pemetaan untuk mengetahui lokasi kelenjar lymph.Untuk mengambil sampel pada tempat yang letaknya perifer, TBNA
dilakukan dengan panduan fluroskopi untuk menentukan lokasinya.50
6) Biopsi paru transbronkial. Prosedur ini merupakan cara yang paling aman untuk mendapatkan biopsi dari parenkim paru. Prosedur ini sangat membantu untuk menegakkan
diagnosis.50
Gambar 2.12. Bronkoskopi serat optik lentur (BSOL)51
Tindakan umumnya dilakukan menggunakan sedasi atau dengan pembiusan lokal. Bronkoskop
dimasukkan melalui hidung, ke orofaring, melewati pita suara hingga ke trakea dan mencapai
bronkus segmentalis.
2.3.2. Pemeriksaan Sitologi dari Sikatan Bronkus
Penggunaan metode sitologi dalam menegakkan diagnosa keganasan pada saluran nafas telah
diakui sebagai salah satu aplikasi yang paling berhasil. Penggunaan BSOL menjadikan metode
populer, karena mempermudah pencapaian pada kelainan di saluran nafas, sehingga menjadikan
sitologi sebagai alat prosedur dan diagnostik lini pertama.3
Sikatan bronkus dilakukan untuk memperoleh spesimen analisa mikrobiologi atau untuk
mendiagnosa adanya keganasan. Konfirmasi diagnosis dalam menegakkan keganasan pada paru
dan penyakit endotrakeal adalah sekitar 50%-90%. Secara keseluruhan sensitifitas dilaporkan
sebesar 65% sedangkan spesifisitas sebesar 98%. Penelitian juga menunjukkan bahwa sikatan
bronkus lebih efektif dalam prosedur dan pembiayaan serta lebih aman jika dibandingkan dengan
prosedur bilasan atau biopsi. Sikatan bronkus distal atau sikatan transbronkial biasanya
dilakukan menggunakan panduan fluroskopi untuk menghindarkan perlukaan pleura uang dapat
berpotensi menimbulkan pneumotoraks.4
Beberapa penelitian dilakukan untuk melihat prosedur terbaik untuk mengklasifikasikan NSCC
pada biopsi halus dan sitologi, yang meliputi histopatologi biopsi, sitologi, imunohistokimia, dan
pemeriksaan mutasi EFGR. Hasilnya membuktikan bahwa sitologi merupakan modalitas terkuat
karena pada sejumlah besar kasus dapat menggambarkan klasifikasi yang lebih spesifik yang
tidak dimungkinkan pada pemeriksaan histopatologi atau imunohistokimia. Penelitian ini juga
menyimpulkan keuntungan pembuatan blok sediaan dari spesimen sitologi dari efusi pleura dan
biopsi aspirasi transbronkial, untuk selanjutnya dapat dilakukan pemeriksaan imunohistokimia
atau penelitian molekuler.52
Keterbatasan utama dari metode persiapan spesimen pada pemeriksaan sitologi adalah kualitas
sediaan yang bervariasi akibat adanya kontaminasi oleh darah, debris seluler dan mukus, yang
Beberapa penelitian memperoleh hasil bahwa sensitifitas diagnostik dari sediaan sitologi yang
berasal dari sikatan bronkus dilaporkan cukup bervariasi di berbagai institusi, yaitu antara
62-78%.53
Selain itu selularitas aspirat (dengan limfosit maupun sel epitel bronkial), keragaman entiti akibat
saling bertumpang tindihnya gambaran sitomorfologi dan kelangkaan material pada sediaan turut
mempengaruhi interpretasi pembacaan sediaan.54
Tehnik liquid-based Pap cytological test (LPT) yang digunakan telah dibuktikan bermanfaat dan
telah disetujui oleh Food and Drug Administration (FDA) pada tahun 1999. Penelitian ini
membuktikan bahwa penggunaan kombinasi metode LPT dan Pap smear meningkatkan
sensitifitas dan spesifisitas dibandingkan dengan hanya metode Pap smear saja, sehingga
disimpulkan bahwa LPT merupakan tehnik yang mudah dan luas penggunaannya dalam
meningkatkan kemampuan diagnosis kanker paru. 53
Selain itu sikatan bronkus memungkinkan sel-sel epitel bronkus normal ikut terbawa pada saat
penyikatan, sehingga umumnya selularitas pada sediaan cukup banyak, tetapi memerlukan
Gambar 2.13. Perbandingan sitologi adenocarcinoma metode Pap dengan metode LPT53
A. Slaid yang menggunakan metode Pap smear. B. Slaid pada pasien yang sama dipreparasi
dengan metode LPT, menunjukkan latarbelakang yang lebih bersih. Kelompokan kecilsel
kanker tersusun dalam struktur asiner. (Pewarnaan Papanicolaou, 400x)
Pemeriksaan sitologi yang optimal pada berbagai tipe kanker paru adalah dengan menggunakan
metode pewarnaan Papanicolaou. Walau demikian air-dried, methanol-fixed smears, pewarnaan
dengan Diff-Quik atau pewarnaan hematologi lainnya lazim digunakan terutama pada sediaan
sitologi aspirasi perkutaneus. Pada metode pewarnaan ini, umumnya diagnosa kanker dapat
ditegakkan, tetapi perbedaan antara tipe tumor satu dengan lainnya kurang jelas terlihat.
Sitoplasma bewarna kebiruan yang akan mengaburkan evaluasi dari struktur inti; berbeda dengan
pewarnaan Papanicolaou yang sangat berkualitas dalam mewarnai sitoplasma keratin.24
2.3.3. Pemeriksaan Imunositokimia
Imunositokimia dapat dilakukan pada hampir seluruh sediaan sitologi, termasuk aspirasi jarum
halus, cairan serosa, Pap smears, serta sediaan sikatan dan bilasan. Jika sampel yang didapatkan
adekuat, maka dianjurkan untuk membuat cell block untuk sediaan ideal imunositokimia, tetapi
biasanya sampel yang didapati minimal, ataupun dari cytocentrifuge. Umumnya kebutuhan
melakukan imunositokimia timbul setelah melakukan pembacaan slaid yang diwarnai dengan
Papanicolaou. Preparasi dengan penyaringan tidak dianjurkan pada imunositokimia, karena filter dapat mengabsorbsi reagent imunologik dan kromogen, yang dapat menyebabkan tidak
munculnya pewarnaan. Fiksasi dengan 95% isopropyl alcohol, buffered formalin,
formol-acetone, atau campuran dari alkohol dan formalin memberikan hasil yang baik pada imunositokimia. Spesimen air-dried tidak dianjurkan pada imunositokimia penanda sitoplasma
dan inti. Seperti halnya sediaan jaringan, fiksasi sitologi yang terlalu lama dengan formalin;
minggu hingga bulan; dapat menimbulkan hilangnya antigenisitas sediaan, sebaliknya fiksasi
yang lama menggunakan alcohol-base fi xatives, tidak terlalu menimbulkan masalah.55
2.4. Thyroid Transcription Factor-1 (TTF-1)
Thyroid transcription factor-1 (TTF-1) merupakan 38-kDa homeodomain yang mengandung DNA-binding protein dari Nkx-2 gene family, yang diekspresikan pada tiroid, paru dan beberapa
area pada diencephalon. Pada masa embriogenesis, ekspresi lokal TTF-1 muncul dari endoderm
pada fase awal kehidupan. Pada penelitian eksperimental pada tikus, didapati TTF-1 tertampil
pada daerah dimana tiroid dan paru akan terbentuk, dan memainkan peran penting pada
diferensiasi sel dan morfogenesis tiroid dan paru.56,57
Terdapat tiga macam thyroid-specific transcription factor yaitu: 1) NKX2-1 (disebut juga TTF1,
TITF1, T/EBP, atau NKX2.1); 2) FOXE1 (disebut juga TTF2 atau TITF2); 3) PAX8.
Keseluruhannya merupakan anggota dari homeodomain, forkhead box, dan paired box family of
NKX2-1 juga diekspresikan pada paru primordial dan ventral forebrain, sedangkan PAX8 pada perkembangan ginjal,, dan FOXE1 ditampilkan pada dasar foregut dan ektoderm kraniofaringeal.
Pada tahap lanjut FOXE1 ditampilkan pada palatum sekunder, choana dan folikel rambut. Pada
tikus percobaan tanpa gen NKX2-1, terjadi defek berupa hipoplastik paru yang buruk, defek
hipotalamus dan agenesis pituitary. Tikus tanpa gen Foxe1 mengalami cleft plate. Variasi defek
dari gen NKX2-1 adalah Brain-Thyroid-Lung syndrome, dengan gambaran khas benign
hereditary chorea, congenital hypothyroidism, dan penyakit pernafasan. Mutasi gen FOXE1 bertanggungjawab terhadap sindroma kongenital berupa hypothyroidism dysgenesis, cleft plate,
dan rambut meruncing.57,58
Gambar 2.14. Regulator molekuler dalam morfogenesis paru57
TTF-1 diekspresikan pada primordia paru (lu) dan tiroid (th) pada embrio tikus 10 hari57
TTF-1 juga diketahui sebagai faktor transkripsi terpenting pada perkembangan jalan nafas perifer
adenocarcinoma perifer. Pada jaringan dewasa, distribusi TTF-1 sangat minimal, hanya pada jalan nafas perifer dan sel epitel tiroid.21
Penelitian yang dilakukan Abutaily dkk untuk menilai pewarnaan imunohistokimia dalam
membedakan malignant mesothelioma dan adenocarcinoma paru telah diuji secara berulang
dengan menggunakan beberapa antibodi, dengan tujuan meningkatkan sensitifitas dan
spesifisitas diagnostik serta menentukan panel antibodi yang efektif. Penelitian menyimpulkan
bahwa E-cadherin menunjukkan sensitifitas sebesar 100% untuk adenocarcinoma paru, dan
TTF-1 menunjukkan spesifisitas sebesar 100% untuk adenocarcinoma paru. Aplikasi kedua
antibodi ini cukup adekuat untuk menegakkan diagnosis adenocarcinoma paru sebesar 69% dan
diagnosa mesothelioma sebesar 78%. Tumor-tumor yang menunjukkan reaktifitas terhadap
kedua antibodi diatas, tidak satupun berasal dari mesotel, tetapi pada tumor primer paru
menunjukkkan suatu adenocarcinoma paru. Hal ini menunjukkan bahwa TTF-1 merupakan
penanda spesifik untuk tumor primer paru.59
Penelitian lain yang meneliti hubungan antara ekspresi dari TTF-1 pada histopatologi jaringan
paru dengan kelangsungan hidup pasien penderita adenocarcinoma paru primer, menunjukkan
TTF-1 terekspresi positif kuat dan berkorelasi dengan ketahanan hidup pasien penderita
adenocarcinoma paru primer.9
Penelitian oleh Myong mendapatkan bahwa tampilan TTF-1 meningkat bermakna pada wanita
dibanding pria, dan cenderung meningkat pada yang tidak merokok dibanding perokok. Hasil ini
tampaknya sesuai dengan epidemiologi yang tercatat selama ini bahwa prevalensi
Penelitian ini juga mendapatkan bahwa seluruh kasus SCC tidak imunoreaktif terhadap TTF-1,
sejalan dengan hasil penelitian-penelitian sebelumnya, yang membuktikan bahwa TTF-1 tidak
terlibat pada diferensiasi sel skuamus. 56
Gambar. 2.15. Tampilan TTF-1 pada Sitologi55
A.Sitologi dari aspirasi jarum halus dari tumor paru perifer menggunakan pewarnaan
Papanicolaou pada seorang wanita berumur 71 tahun, yang diduga sutau SCC. B. Inti sel tumor
posistif terwarnai denga TTF-1, sehingga diagnosa ditegakkan sebagai adenocarcinoma
Penelitian oleh Stenhouse dkk menyimpulkan bahwa pewarnaan positif dari TTF-1 berguna
dalam diagnosis diferensial adenocarcinoma paru jika sebelumnya telah menyingkirkan tumor
tiroid dan tumor neuroendokrin yang dapat mengekspresikan TTF-1. Penelitian juga
menyimpulkan bahwa TTF-1 dapat menjadi penanda keturunan untuk tumor yang timbul dari
saluran napas perifer atau epitel alveolar dan tidak memiliki relevansi prognostik. Penelitian ini
mendapatkan bahwa TTF-1 terwarnai positif pada adenocarcinoma sebanyak 75%, sesuai
dengan penelitian sebelumnya yaitu TTF-1 positif berkisar antara 72%-80%. Pewarnaan TTF-1
hampir seluruhnya tertampil negatif pada adenocarcinoma tipe mucinous, sedangkan pada
atypical adenomatous hyperplasia dan poorly differentiated pewarnaan dengan TTF-1 tertampil kuat.7
Gambar 2.16. Tampilan TTF-1 pada sediaan histopatologi7
(A).Gambaran invasif dari kelenjar pada adenocarcinoma menunjukkan TTF-1 terwarnai positif
kuat. (B). Pola solid pada adenocarcinoma yang berdiferensiasi buruk menunjukkan pewarnaan
positif dengan tingkatan lebih kuat. (C). Pewarnaan positif yang banyak pada non-mucinous
bronchioloalveolar carcinoma. (D). TTF-1 tertampil positif kuat pada adenomatous hyperplasia. (E) Alveolar pneumocytes dan epitel bronkiolar positif terwarnai dengan TTF-1. Pada
bronkiolus TTF-1 tertampil lebih kuat dibanding epitel. (F) TTF-1 tertampil negatif pada epitel
bronkial sentral.
A B
C D