ke dalam 50 mL bufer fosfat pH 7.2. Campuran tersebut disaring dan filtratnya diencerkan sebanyak 10 kali. Setelah itu, filtrat dibaca absorbansnya dengan spektrofotometer UV/Vis pada panjang gelombang maksimum 222 nm. Absorbans yang diperoleh digunakan untuk menentukan konsentrasi ibuprofen dengan bantuan kurva standar.
Uji Disolusi Secara In Vitro (Depkes 1995) Uji disolusi mikrokapsul dilakukan menggunakan alat disolusi tipe 2 (tipe dayung). Sebanyak 200 mg mikrokapsul ditimbang dan dimasukkan ke dalam chamber disolusi. Uji disolusi dilakukan dalam media simulasi cairan usus (larutan bufer fosfat pH 7.2) selama 6 jam pada suhu (37 0.5) C dengan kecepatan pengadukan 100 rpm. Volume media disolusi yang digunakan sebanyak 900 mL. Pengambilan alikuot dilakukan setiap 15 menit dengan volume setiap kali pengambilan 10 mL. Setiap kali pengambilan alikuot, volume media yang terambil digantikan dengan larutan media yang baru dengan volume dan suhu yang sama. Konsentrasi ibuprofen dalam larutan alikuot diukur menggunakan spektrofotometer UV pada λmaks. Data yang diperoleh dibuat
kurva hubungan antara persen pelepasan ibuprofen dan waktu disolusi, serta dikaji kinetika pelepasannya.
Morfologi Mikrokapsul
Pengamatan morfologi mikrokapsul dilakukan terhadap mikrokapsul kosong dan yang terisi ibuprofen menggunakan mikroskop dan SEM.
HASIL DAN PEMBAHASAN
Poli(asam laktat) (PLA)
PLA disintesis menggunakan metode polikondensasi secara langsung dengan suhu tinggi. Metode ini merupakan metode yang paling sederhana dibandingkan dengan metode pembuatan PLA lainnya (Gonzales et al. 1999). Pada tahap awal pembentukan PLA, monomer asam laktat dipanaskan terlebih dahulu di dalam reaktor sintesis PLA pada suhu 120oC. Hal ini bertujuan melepaskan air dan sekaligus terjadinya depolimerisasi pembentukan dimer asam laktat. Kemudian suhu dinaikkan menjadi 150oC selama 24 jam untuk mempercepat reaksi polimerisasi (Kemala 2010).
Gambar 1 Reaksi pembentukan PLA (Kaitian et al. 1996).
Reaksi pembentukan PLA merupakan reaksi yang dapat balik (Gambar 1). Oleh karena itu, molekul air yang dihasilkan harus langsung dipindahkan atau dihilangkan dengan menggunakan pompa vakum. Adanya molekul air akan menurunkan laju polimerisasi sehingga PLA yang dihasilkan memiliki bobot molekul yang lebih rendah. (Kaitian et al. 1995).
PLA hasil sintesis berwarna kuning kecoklatan (Gambar 2). PLA ini diduga merupakan PLA dalam bentuk rasemiknya (D,L-PLA). Menurut Dutkiewicz et al. (2003), sintesis PLA pada suhu lebih dari 140°C akan menghasilkan PLA dalam bentuk rasemiknya. D,L-PLA lebih bersifat amorf dibandingkan L-PLA, oleh sebab itu penggunaan D,L-PLA lebih disukai dalam sistem penghantaran obat, karena mudah terdegradasi dan lebih mampu untuk mendispersikan obat secara homogen dalam matriks polimer (Gunatilake dan Adhikari 2003).
Gambar 2 PLA hasil sintesis Bobot Molekul PLA
Tinggi rendahnya bobot molekul PLA yang dihasilkan dipengaruhi oleh penggunaan suhu pemanasan dan lamanya waktu polimerisasi yang optimal. Hal tersebut disebabkan oleh sifat PLA yang mudah terdegradasi oleh lingkungan maupun oleh reaksi hidrolisis dan enzimatik karena adanya ikatan ester dan gugus hidroksil pada rantai ujungnya. Penggunaan suhu yang terlalu tinggi dan waktu polimerisasi yang terlalu lama akan menurunkan bobot molekul dari PLA yang terbentuk. Panas yang dihasilkan pada sistem reaktor sintesis karena suhu yang terlalu tinggi akan menghidrolisis polimer PLA yang terbentuk, sehingga polimer tersebut akan kembali ke bentuk monomernya. Hal ini dikarenakan oleh reaksi polimerisasi yang bersifat dapat balik. Apabila dalam keadaan tersebut proses polimerisasi
n CH3 O HC C O Pemanasan H2O CH3 O H HC C O OH
+
masih dilanjutkan, polimer tersebut akan terdegradasi dan hangus (Kaitian et al. 1995). Pelarut etil asetat digunakan pada pengukuran bobot molekul PLA karena bersifat nonpolar, tidak beracun, dan tidak higroskopis. PLA hasil sintesis memiliki bobot molekul sebesar 8239.50 g mol-1 (Lampiran 2) dengan rendemen sebesar 58.8404%. PLA dengan bobot molekul rendah (kurang dari 10.000 g mol-1 dapat dibuat menggunakan metode polikondensasi langsung (Vroman dan Tighzert 2009).
Mikroenkapsulasi Ibuprofen Menggunakan Paduan Lilin Lebah-PLA
Mikrokapsul paduan lilin lebah dan PLA dibuat melalui proses pencampuran fisika yaitu tidak membentuk ikatan kovalen antara komponen-komponennya. Interaksi yang terjadi adalah ikatan van der Waals, ikatan hidrogen atau interaksi dipol-dipol (Rabek 1980). Metode yang digunakan untuk membuat mikrokapsul pada penelitian ini yaitu metode emulsifikasi obat dalam larutan polimer organik dan media dispersi air (o/w) (Birnbaum dan Brannon-Peppas 2004). Metode emulsi-penguapan pelarut cocok untuk membuat mikrokapsul obat dari poliester biodegaradabel seperti PLA (Dubey et al. 2009). Metode ini memiliki beberapa keuntungan yaitu dilakukan pada suhu ruang dan menghasilkan mikrokapsul yang memiliki mekanisme pelepasan material yang dikungkung secara optimal karena material yang dikungkung terdispersi secara homogen pada matriks polimer sehingga dianggap ideal untuk sistem pengantaran obat (Obeidat 2009). Proses pada metode ini dilakukan dengan melarutkan polimer dalam pelarut volatil yang tidak dapat campur dengan fase cair (o/w emulsi) (Venkatesan et al. 2009). Fase organik yang digunakan pada penelitian ini adalah diklorometana. Selain diklorometana, dapat juga digunakan kloroform, tetapi membutuhkan waktu yang lebih lama untuk menguap dibandingkan dengan diklorometana. Kloroform menguap pada suhu 61°C, sedangkan diklorometana menguap pada suhu 39 °C. Mikrokapsul akan lebih cepat terbentuk ketika menggunakan diklorometana (Kemala et al. 2010). Yeo dan Park (2004) mengatakan bahwa diklorometana lebih mudah larut dalam air dibandingkan kloroform. Kelarutan yang tinggi dalam air akan membuat transfer massa antara fase dispersi dan fase pendispersi relatif cepat sehingga pengendapan polimer lebih
cepat. Pengemulsi yang digunakan dalam penelitian ini adalah gelatin yang memiliki kemampuan mengadsorpsi pada antarmuka Gugus hidrofil dari gelatin akan berikatan dengan molekul air sedangkan gugus lipofilnya akan berikatan dengan diklometana sehingga emulsi lebih stabil. Pendispersian ke dalam air berfungsi untuk menguapkan diklorometana dari emulsi dan mikrokapsul yang terbentuk akan mengendap. Mikrokapsul yang didapatkan selanjutnya didekantasi dan dibilas beberapa kali dengan akuades panas untuk menghilangkan sisa-sisa gelatin yang menempel pada mikrokapsul.
Mikrokapsul ibuprofen yang dihasilkan memiliki bentuk visual seperti serbuk, halus, kering, dan berwarna putih (Gambar 3).
Gambar 3 Mikrokapsul ibuprofen tersalut paduan lilin lebah-PLA.
Campuran dikatakan homogen jika tidak terlihat lagi perbedaan antara komponen-komponen penyusunnya, baik dalam bentuk, ukuran, maupun warna karena semua komponennya telah tercampur secara merata (Rosida 2007). Kemala et al. (2012) mengatakan bahwa pencampuran dua atau lebih cairan menghasilkan campuran homogen, maka dapat dikatakan kompartibel, Pada penelitian ini dapat disimpulkan bahwa campuran PLA dan lilin lebah adalah kompartibel.
Panjang Gelombang Maksimum dan Kurva Standar
Pelarut yang digunakan dalam pembuatan larutan ibuprofen adalah bufer fosfat pH 7.2. Nilai pH bufer tersebut dipilih untuk menyesuaikan dengan pH usus dan biasa digunakan sebagai media disolusi tablet ibuprofen (Depkes 1995).
Penentuan λmaks dilakukan pada daerah
ultraviolet karena ibuprofen memiliki struktur ikatan terkonjugasi. Pengukuran sampel pada λmaks karena memiliki perubahan serapan
untuk setiap satuan konsentrasi paling besar. Dengan demikian akan didapatkan kepekaan dan sensitivitas pengukuran yang maksimum (Sutrisna 2005). Panjang gelombang maksimum (λmaks) yang diperoleh yaitu 222
nm (Lampiran 3). Nilai λmaks larutan ibuprofen
yang diperoleh tersebut sesuai dengan literatur, yaitu 222 nm (Depkes 1995). Linearitas menunjukkan kemampuan suatu metode analisis untuk memperoleh hasil pengujian yang sesuai dengan konsentrasi analit dalam contoh pada kisaran konsentrasi tertentu (AOAC 2002). Linearitas suatu metode analisis adalah ukuran yang menunjukkan tingkat kesesuaian atau korelasi antara kadar analit dan respons detektor, dinyatakan sebagai koefisien korelasi (R2) (Depkes 2001).
Persamaan regresi linear untuk kurva standar adalah y = 0.0451x + 0.0082 dengan nilai r sebesar 0.9998 (Lampiran 4). Menurut AOAC (2002) nilai ini memenuhi syarat yang ditetapkan, yaitu 0.9900. Nilai koefisien korelasi yang tinggi menunjukkan hubungan yang linear antara sinyal detektor yang terukur dan jumlah ibuprofen dalam contoh.
Efisiensi Enkapsulasi Ibuprofen Efisiensi enkapsulasi merupakan parameter yang digunakan untuk menentukan keberhasilan proses enkapsulasi. Parameter ini menunjukkan berapa persen senyawa ibuprofen yang berhasil disalut dalam mikrokapsul. Semakin tinggi efisiensi ibuprofen dalam mikrokapsul maka semakin banyak ibuprofen yang tersalut didalam paduan.
Gambar 4 Efisiensi enkapsulasi mikrokapsul ibuprofen dengan konsentrasi gelatin = 1%; = 1.5%; = 2%.
Hasil uji efisiensi menunjukkan peningkatan efisiensi enkapsulasi dengan bertambahnya perbandingan PLA terhadap lilin lebah (Gambar 4). Efisiensi enkapsulasi
terendah dihasilkan oleh mikrokapsul AG1
sebesar 51.50% dan efisiensi enkapsulasi tertinggi oleh mikrokapsul DG3 yaitu sebesar
84.21%. Perbedaan hasil ini dipengaruhi oleh nisbah massa paduan. Pada mikrokapsul AG1,
lilin lebah yang digunakan lebih banyak dibandingkan mikrokapsul DG3. Lilin lebah
merupakan lemak hewan yang terdiri dari senyawa campuran alkana, alkena, monoester, diester, monohidroksiester, dan asam lemak. Monoester dari alkohol C24-C34 merupakan
komponen terbanyak yaitu sekitar 40% (Jackson dan Eller 2006). Lilin lebah memiliki bobot molekul sekitar 868 g mol-1. Lilin lebah yang lebih banyak pada paduan menyebabkan komponen paduan dengan bobot molekul rendah bertambah sehingga akan lebih sulit untuk mengungkung ibuprofen. Hal ini sesuai dengan pernyataan Kim et al.(2003) yaitu efisiensi mikrokapsul berbeda pada penggunaan berat molekul polimer berbeda, semakin tinggi berat molekul polimer maka semakin tinggi efisiensi yang dihasilkan.
Selain itu, jenis dan konsentrasi pengemulsi juga merupakan faktor yang memberikan pengaruh terhadap efisiensi enkapsulasi. Ranjha et al. (2010) melaporkan bahwa tween 20 memberikan efisiensi enkapsulasi lebih tinggi dibandingkan gelatin. Hal ini dipengaruhi oleh nilai keseimbangan hidrofilik lipofilik (HLB) tween 20 yang lebih besar dibandingkan gelatin. HLB yang lebih besar dapat menurunkan tegangan antar muka lebih baik lagi sehingga dispersi emulsi dalam media pendispersi semakin meningkat. Konsentrasi pengemulsi juga memberikan pengaruh yang cukup besar. Hal ini berkesesuaian dengan hasil yang diperoleh. Pada nisbah paduan 6:4, 8:2 dan 9:1, dapat dilihat bahwa dengan meningkatnya konsentrasi gelatin maka efisiensi enkapsulasi juga meningkat. Namun, tidak demikian untuk nisbah paduan 7:3. Hal ini mungkin disebabkan oleh faktor kecepatan pengadukan yang tidak homogen atau waktu dispersi yang tidak seragam. Data perhitungan efisiensi enkapsulasi untuk semua formula mikrokapsul dapat dilihat pada Lampiran 5.
Morfologi Mikrokapsul Hasil Efisiensi Enkapsulasi
Morfologi mikrokapsul paduan lilin lebah-PLA diamati dengan menggunakan mikroskop (Gambar 5) dan SEM (Gambar 6).
AG(9:1) BG(8:2) CG(7:3) DG(6:4) Nisbah paduan lilin lebah:PLA
(a) (b)
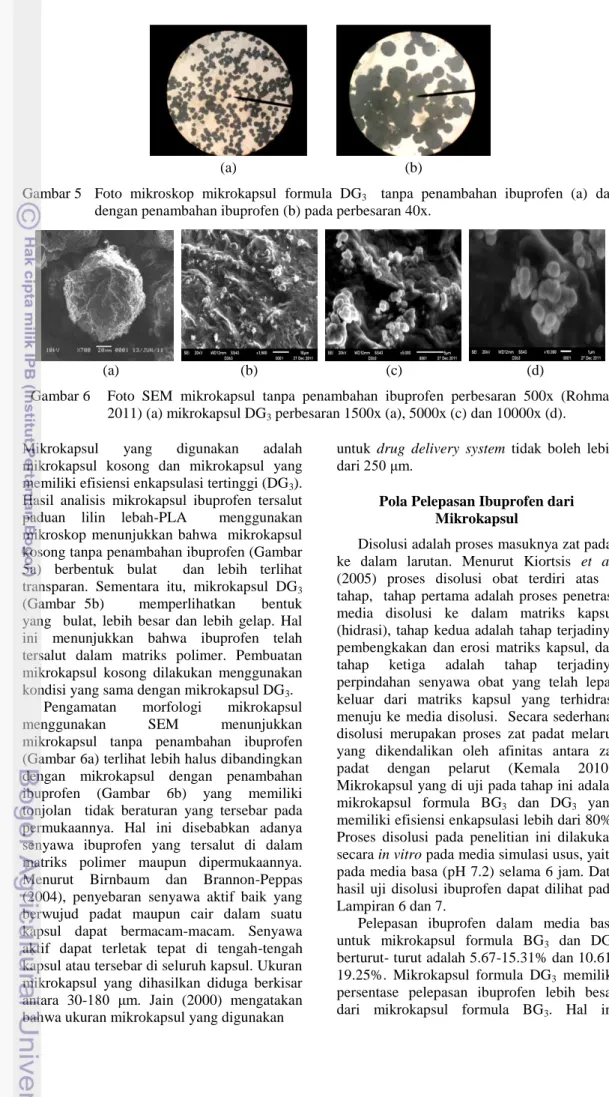
Gambar 5 Foto mikroskop mikrokapsul formula DG3 tanpa penambahan ibuprofen (a) dan
dengan penambahan ibuprofen (b) pada perbesaran 40x.
(a) (b) (c) (d)
Gambar 6 Foto SEM mikrokapsul tanpa penambahan ibuprofen perbesaran 500x (Rohman 2011) (a) mikrokapsul DG3 perbesaran 1500x (a), 5000x (c) dan 10000x (d).
Mikrokapsul yang digunakan adalah mikrokapsul kosong dan mikrokapsul yang memiliki efisiensi enkapsulasi tertinggi (DG3).
Hasil analisis mikrokapsul ibuprofen tersalut paduan lilin lebah-PLA menggunakan mikroskop menunjukkan bahwa mikrokapsul kosong tanpa penambahan ibuprofen (Gambar 5a) berbentuk bulat dan lebih terlihat transparan. Sementara itu, mikrokapsul DG3
(Gambar 5b) memperlihatkan bentuk yang bulat, lebih besar dan lebih gelap. Hal ini menunjukkan bahwa ibuprofen telah tersalut dalam matriks polimer. Pembuatan mikrokapsul kosong dilakukan menggunakan kondisi yang sama dengan mikrokapsul DG3.
Pengamatan morfologi mikrokapsul menggunakan SEM menunjukkan mikrokapsul tanpa penambahan ibuprofen (Gambar 6a) terlihat lebih halus dibandingkan dengan mikrokapsul dengan penambahan ibuprofen (Gambar 6b) yang memiliki tonjolan tidak beraturan yang tersebar pada permukaannya. Hal ini disebabkan adanya senyawa ibuprofen yang tersalut di dalam matriks polimer maupun dipermukaannya. Menurut Birnbaum dan Brannon-Peppas (2004), penyebaran senyawa aktif baik yang berwujud padat maupun cair dalam suatu kapsul dapat bermacam-macam. Senyawa aktif dapat terletak tepat di tengah-tengah kapsul atau tersebar di seluruh kapsul. Ukuran mikrokapsul yang dihasilkan diduga berkisar antara 30-180 μm. Jain (2000) mengatakan bahwa ukuran mikrokapsul yang digunakan
untuk drug delivery system tidak boleh lebih dari 250 μm.
Pola Pelepasan Ibuprofen dari Mikrokapsul
Disolusi adalah proses masuknya zat padat
ke dalam larutan. Menurut Kiortsis et al. (2005) proses disolusi obat terdiri atas 3
tahap, tahap pertama adalah proses penetrasi media disolusi ke dalam matriks kapsul (hidrasi), tahap kedua adalah tahap terjadinya pembengkakan dan erosi matriks kapsul, dan tahap ketiga adalah tahap terjadinya perpindahan senyawa obat yang telah lepas keluar dari matriks kapsul yang terhidrasi menuju ke media disolusi. Secara sederhana, disolusi merupakan proses zat padat melarut yang dikendalikan oleh afinitas antara zat padat dengan pelarut (Kemala 2010). Mikrokapsul yang di uji pada tahap ini adalah mikrokapsul formula BG3 dan DG3 yang
memiliki efisiensi enkapsulasi lebih dari 80%. Proses disolusi pada penelitian ini dilakukan secara in vitro pada media simulasi usus, yaitu pada media basa (pH 7.2) selama 6 jam. Data hasil uji disolusi ibuprofen dapat dilihat pada Lampiran 6 dan 7.
Pelepasan ibuprofen dalam media basa untuk mikrokapsul formula BG3 dan DG3
berturut- turut adalah 5.67-15.31% dan 10.61-19.25%. Mikrokapsul formula DG3 memiliki
persentase pelepasan ibuprofen lebih besar dari mikrokapsul formula BG3. Hal ini
disebabkan mikrokapsul formula DG3
memiliki efisiensi enkapsulasi lebih tinggi dari mikrokapsul formula BG3, yang berarti
kandungan ibuprofen dalam mikrokapsul formula DG3 lebih banyak daripada
kandungan ibuprofen dalam mikrokapsul formula BG3. Kandungan ibuprofen yang
lebih banyak dalam mikrokapsul formula DG3
akan menghasilkan lebih banyak pori atau lubang pada mikrokapsul, oleh karena itu ketika senyawa obat lepas dari matriks polimer, maka pori-pori pada matriks polimer akan semakin banyak sehingga meningkatkan laju pelepasan senyawa obat (Cardinal 1984). Faktor lainnyayang dapat mempengaruhi laju pelepasan adalah ukuran dari mikrokapsul. Semakin kecil ukuran mikrokapsul, maka pelepasan senyawa inti dari matriks polimer akan semakin cepat. Hal ini dikarenakan luas permukaannya yang semakin besar. Hubungan antara persentase pelepasan ibuprofen dengan waktu ditunjukkan pada Gambar 7.
Gambar 7 Pelepasan ibuprofen dari mikrokapsul formula BG3(i)
dan DG3(ii) terhadap waktu
(menit).
Profil disolusi untuk kedua formula menunjukkan adanya initial burst release pada menit ke-15 yaitu 5.67% untuk mikrokapsul formula BG3 dan 10.61 % untuk
mikrokapsul formula DG3. Initial burst
release terjadi karena adanya obat yang tersalut pada permukaan. Pelepasan ibuprofen meningkat secara bertahap hingga mencapai waktu pelepasan maksimum yaitu pada menit ke-225. Hal ini berarti bahwa mikrokapsul yang dihasilkan telah memenuhi tujuan dalam
penelitian ini yaitu memperlama waktu pelepasan ibuprofen, yang mana waktu eliminasi ibuprofen komersial pada umumnya adalah 2 jam.
Kinetika Pelepasan Ibuprofen Kinetika pelepasan obat digunakan untuk mengetahui laju pelepasan obat dan mekanismenya berdasarkan model yang sesuai. Umumnya kinetika pelepasan obat terkendali mengikuti orde ke nol atau ke satu (Singhvi dan Singh 2011). Mekanisme pelepasan ibuprofen dapat ditentukan dengan melihat nilai koefisien korelasi (R2) tertinggi yang dihasilkan oleh model kinetika untuk sistem penghantaran obat lepas terkendali. Penentuan model kinetika ini dilakukan dengan menggunakan software KinetDS 3.0 rev 2010.
Mekanisme pelepasan ibuprofen dari mikrokapsul formula BG3 dan DG3 mengikuti
model kinetika orde ke-0 berdasarkan nilai R2 yang diperoleh (Tabel 2). Pada Lampiran 6 dan 7, dapat dilihat bahwa persentase pelepasan ibuprofen pada formula BG3 dan
DG3 meningkat namun tidak terlalu signifikan
dengan bertambahnya waktu disolusi. Hal ini dipengaruhi oleh sifat dari matriks mikrokapsul yang mampu menahan laju pelepasan ibuprofen sehingga persentase ibuprofen yang dilepaskan setiap 15 menit tidak terlalu besar. Selain itu, adanya sinyal yang terukur dari media disolusi menandakan bahwa permukaan mikrokapsul telah mengalami pengikisan. Hubungan antara persentase ibuprofen dengan waktu tersebut kemudian diplot kedalam kurva dan mengikuti model kinetika orde ke-0 dengan nilai R2 untuk formula BG3 dan DG3 sebesar 0.9929
dan 0.9868%. Laju pelepasan ibuprofen terjadi secara bertahap dari menit ke-15 hingga menit ke-225 (Gambar 7). Setelah menit ke-225, laju pelepasan ibuprofen tidak lagi mengalami kenaikan melainkan turun secara perlahan-lahan. Hal ini berarti konsentrasi obat telah menurun. Selanjutnya kurva menjadi cenderung turun karena telah terjadinya kesetimbangan antara media dan cairan dalam mikrokapsul sehingga laju
Tabel 2 Parameter pelepasan ibuprofen dari mikrokapsul
Formula Orde ke-0 Orde ke-1 Hickson-Crowell
R2 K R2 K R2 K
HC
BG3 0.9929 0.0485 0.9746 0.0049 0.9841 0.0035