BAB VI PEMBAHASAN
6.1 Penyiapan Bahan
Hasil determinasi tumbuhan yang dilakukan di LIPI-UPT Balai Konservasi Tumbuhan Kebun Raya ”Eka Karya” Bedugul Bali menunjukkan bahwa tumbuhan bungur yang dikumpulkan dari Jalan Hang Tuah, Denpasar pada Desember, 2010 merupakan spesies Lagerstroemia speciosa Pers. yang selanjutnya digunakan sebagai sampel di dalam penelitian. Kulit batang yang digunakan terlebih dahulu dibersihkan dari kotoran, selanjutnya dipotong untuk mempercepat proses pengeringan. Sampel tersebut kemudian dikeringkan tanpa terkena sinar matahari secara langsung, namun sirkulasi udaranya baik. Paparan sinar matahari secara langsung pada suhu tinggi dapat merusak dan menyebabkan terdegradasinya senyawa kimia dalam sampel yang dianalisis.
Sampel yang telah kering selanjutnya dihaluskan dengan menggunakan blender kemudian diayak sampai berbentuk serbuk berwarna cokelat sebanyak ±1500 g. Sampel yang berbentuk serbuk bertujuan untuk memperbesar luas permukaan sehingga memudahkan tertariknya komponen-komponen kimia yang terdapat dalam bahan. Serbuk sampel yang digunakan juga diukur kadar airnya sebagai standarisasi sampel.
Metode yang digunakan untuk pengukuran kadar air adalah secara termogravimetri dengan menggunakan oven pengering. Pengeringan adalah suatu metode untuk mengeluarkan atau menghilangkan sebagian air dari suatu bahan
dengan cara menguapkan air tersebut menggunakan energi panas. Umumnya kandungan air bahan tersebut dikurangi agar mikroba tidak dapat tumbuh lagi di dalamnya (Underwood, 2002)
Prinsip dari metode oven pengering adalah bahwa air yang terkandung dalam suatu bahan akan menguap bila bahan tersebut dipanaskan pada suhu 105o C selama waktu tertentu. Perbedaan antara berat sebelum dan sesudah dipanaskan adalah kadar air yang terkandung dalam bahan tersebut (Underwood, 2002). Setelah dilakukan perhitungan dengan menggunakan metode tersebut, didapatkan kadar air pada sampel yang digunakan yaitu sebesar 10,27%. Cara perhitungan kadar air dapat dilihat pada Lampiran 5. Besarnya kadar air pada sampel ini sedikit melebihi standar yang ditentukan dalam Farmakope Indonesia yang menyatakan bahwa kadar air standar pada suatu simplisia bahan obat yaitu sebesar 10% (Depkes RI, 1995).
6.2 Ekstraksi Kulit Batang Bungur
penguap putar vakum (rotary vacuum evaporator) tersebut diperoleh ekstrak etanol (crude extract) yang berwarna cokelat sebanyak 21,88 g. Terhadap ekstrak etanol kemudian dilakukan uji senyawa tanin dan uji hipoglikemik.
6.2.1 Uji senyawa tanin ekstrak etanol
Ekstrak etanol yang diperoleh selanjutnya diuji kandungan senyawa taninnya dengan menggunakan pereaksi FeCl3, larutan gelatin dan air brom. Hasil
uji fitokimia tersebut menunjukkan bahwa pada ekstrak etanol terdapat senyawa tanin. Hal ini diperlihatkan dengan perubahan warna yang terjadi dari cokelat menjadi hijau dengan FeCl3, terbentuknya endapan dengan gelatin, dan
terdapatnya endapan dengan air brom. 6.2.2 Uji hipoglikemik ekstrak etanol
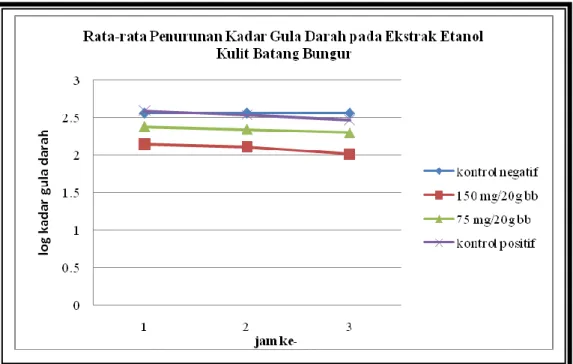
berbeda-beda. Tiga puluh menit kemudian mencit diberikan pembebanan glukosa monihidrat. Sampel darah selanjutnya diambil pada jam ke 1, 2, dan 3 setelah pembebanan glukosa monohidrat yang kemudian diukur kadar gula darahnya (Aman, 2007). Profil efek perlakuan yang diberikan terhadap kadar gula darah mencit yang diinduksi dengan aloksan dapat dilihat pada Gambar 6.1.
Gambar 6.1 Grafik Rata-Rata Penurunan Log Kadar Gula Darah pada Ekstrak Etanol Kulit Batang Bungur
Keterangan: Kontrol negatif = diberi 0,5 mL aquades
Uji dosis I (150 mg/20 g bb) = diberi 0,5 mL ekstrak etanol kulit batang bungur
Uji dosis II (75 mg/20 g bb) = diberi 0,5 mL ekstrak etanol kulit batang bungur
Kontrol positif = diberi 0,5 mL glibenklamid (dosis 3 mg/20 g bb)
menurunkan kadar gula darah lebih baik dibandingkan pada dosis II. Untuk memastikan pengamatan, data yang diperoleh selanjutnya dianalisis statistik menggunakan SPSS 15.0 for windows. Uji statistik yang dilakukan adalah uji normalitas, uji homogenitas, dan uji Kruskal-wallis.
6.2.2.1 Uji normalitas data
Data perubahan kadar gula darah mencit pada kontrol negatif, uji dosis I, uji dosis II, dan kontrol positif diuji normalitasnya dengan menggunakan uji Kolmogorov-Smirnov test. Hasilnya menunjukkan data tidak terdistribusi normal dengan nilai p=0,000 (p<0,05) yang dapat dilihat pada Lampiran 11.
6.2.2.2 Uji homogenitas data
Data perubahan kadar gula darah mencit pada kontrol negatif, uji dosis I, uji dosis II, dan kontrol positif diuji homogenitasnya. Hasilnya menunjukkan data tidak homogen dengan nilai p = 0,000 (p<0,05) yang dapat dilihat pada Lampiran 11.
6.2.2.3 Uji Kruskal Wallis
Tabel 6.1
Analisis Kruskal Wallis Setelah Perlakuan Antar Kelompok
Kelompok N Rerata p interpretasi
Kontrol negatif 18 63,50 0,000 Berbeda nyata Dosis 150 mg/20 g bb 18 16,03 0,000 Berbeda nyata Dosis 75 mg/20 g bb 18 39,42 0,000 Berbeda nyata Kontrol positif 18 27,06 0,000 Berbeda nyata
Berdasarkan tabel tersebut, terlihat bahwa keempat kelompok perlakuan memiliki perbedaan yang sangat nyata p=0,000 (p<0,005) setelah diberi perlakuan. Hasil ini menyatakan bahwa kontrol negatif memiliki nilai perubahan kadar gula darah dan efek yang berbeda dari ketiga kelompok lainnya. Berdasarkan hal tersebut, uji dosis 150 mg/20 g bb memiliki nilai perubahan kadar gula darah terendah dan berbeda nyata dengan dosis 75 mg/20 g bb dan kontrol positif (tablet glibenklamid). Maka dapat dinyatakan, bahwa ekstrak etanol kulit batang bungur memiliki efek hipoglikemik terhadap darah mencit yang diinduksi aloksan.
kulit bungur dosis I lebih efektif dalam menurunkan kadar gula darah mencit yang diinduksi dengan aloksan dibandingkan ekstrak etanol kulit bungur dosis II dengan tablet glibenklamid sebagai kontrol positif.
6.3 Partisi
Ekstrak etanol kulit batang bungur yang positif mengandung tanin dan memiliki efek hipoglikemik ini selanjutnya dipisahkan tahap awal dengan cara partisi. Sebanyak 20 g ekstrak etanol dilarutkan dalam air : etanol (7:3). Setelah ekstrak ini melarut kemudian dievaporasi untuk menghilangkan etanolnya sehingga diperoleh ekstrak air. Ekstrak air ini selanjutnya dipartisi berturut-turut dengan menggunakan n-heksana, dan aseton. Partisi ini dilakukan untuk menarik senyawa-senyawa yang bersifat non polar dengan menggunakan n-heksana, semi polar dengan aseton dan senyawa polar diharapkan terdapat pada airnya.
6.3.1 Uji senyawa tanin ekstrak aseton
Ketiga hasil partisi ini kemudian diuji kandungan senyawa taninnya dengan menggunakan pereaksi FeCl3, larutan gelatin dan air brom. Dilihat dari
perubahan yang terjadi dengan ketiga pereaksi tersebut, hanya ekstrak aseton yang positif mengandung senyawa tanin. Dengan FeCl3 ekstrak aseton menunjukkan
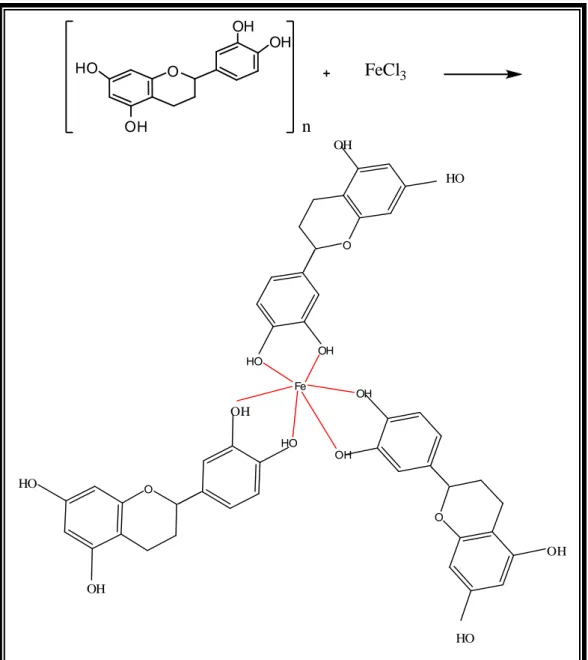
nonlogam (Effendy, 2007). Persamaan Reaksi antara senyawaan tanin dengan FeCl3 dilihat pada Gambar 6.2.
Gambar 6.2 Reaksi antara Tanin dengan FeCl3
Terbentuknya endapan setelah ditambahkan larutan gelatin yang menyatakan bahwa pada ekstrak aseton kulit batang bungur positif mengandung tanin. Semua tanin menimbulkan endapan sedikit atau banyak jika ditambahkan
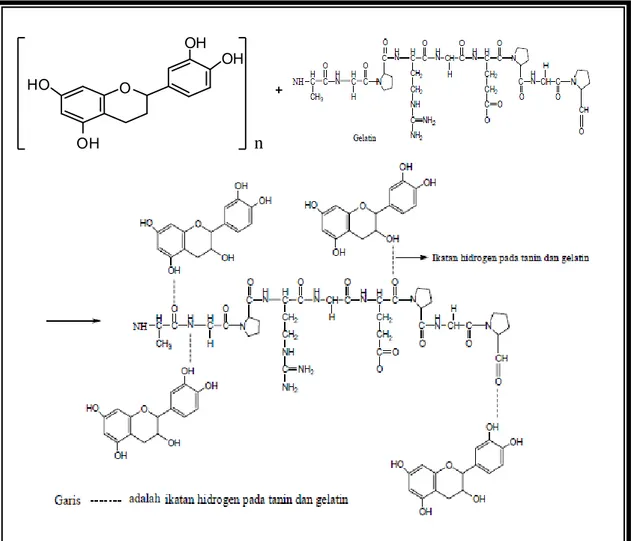
dengan gelatin (Harborne, 1995). Gelatin merupakan protein alami yang memberikan sifat penstabil dan pengental bagi media yang berbasiskan air, mengandung asam amino yaitu dengan kandungan glisin (27%), prolin (16%) dan hidroxiprolin (14%), sehingga terbentuknya senyawa tanin protein dikarenakan adanya ikatan hidrogen antara tanin dan protein pada gelatin sehingga terbentuk endapan putih (Leemensand, 1991). Reaksi antara tanin dengan gelatin ditunjukkan Gambar 6.3.
Gambar 6.3 Reaksi antara Tanin dan Gelatin
OH
HO O
OH OH
Terbentuknya endapan setelah ditambahkan air brom yang menyatakan bahwa pada ekstrak aseton kulit batang bungur positif mengandung tanin.
6.3.2 Uji efek hipoglikemik ekstrak aseton
Proses pengerjaan uji efek hipoglikemik ekstrak aseton kulit batang bungur ini sama dengan proses pengerjaan uji efek hipoglikemik ekstrak etanol yaitu dengan menggunakan empat kelompok perlakuan yaitu kontrol negatif, uji dosis I (150 mg/ 20 g bb), uji dosis II (75 mg/20 g bb), dan kontrol positif dengan masing menggunakan enam kali ulangan. Setiap mencit pada masing-masing kelompok mula-mula dibuat menjadi diabetes dengan menyuntikkan aloksan secara intra peritoneal pada abdomen perutnya. Setelah semua mencit menjadi diabet yaitu ditandai dengan kadar gula darah di atas 160 mg/dL, mencit lalu dipuasakan selama 18 jam kemudian diberikan masing-masing perlakuan yang berbeda-beda sesuai kelompoknya. Tiga puluh menit kemudian, mencit diberikan pembebanan glukosa monohidrat. Mencit diukur kadar gula darahnya pada jam ke-1, 2, dan 3 setelah pembebanan glukosa monohidrat.
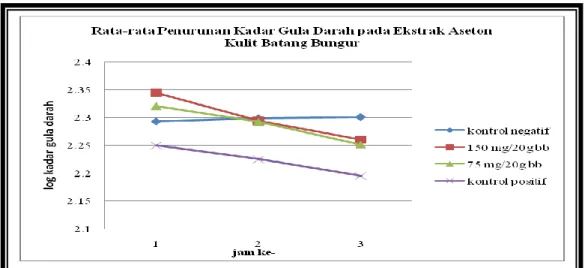
Gambar 6.4 Grafik Rata-Rata Penurunan Log Kadar Gula Darah pada Ekstrak aseton Kulit Batang Bungur
Keterangan: Kontrol negatif = diberi 0,5 mL aquades
Uji dosis I (150 mg/20 g bb) = diberi 0,5 mL ekstrak aseton kulit batang bungur
Uji dosis II (75 mg/20 g bb) = diberi 0,5 mL ekstrak aseton kulit batang bungur
Kontrol positif = diberi 0,5 mL glibenklamid (dosis 3 mg/20 g bb)
6.3.2.1 Uji normalitas data
Data perubahan kadar gula darah mencit pada kontrol negatif, uji dosis I, uji dosis II, dan kontrol positif diuji normalitasnya dengan menggunakan uji Kolmogorov-Smirnov test. Hasilnya menunjukkan data terdistribusi normal dengan nilai p=0,215 (p>0,05) yang dapat dilihat pada Lampiran 12.
6.3.2.2 Uji homogenitas data
Data perubahan kadar gula darah mencit pada kontrol negatif, uji dosis I, uji dosis II, dan kontrol positif diuji homogenitasnya. Hasilnya menunjukkan data tidak homogen dengan nilai p = 0,000 (p<0,05) yang dapat dilihat pada Lampiran 12.
6.3.2.3 Uji ANOVA
Berdasarkan uji analisis dengan ANOVA menghasilkan nilai F = 16,594 dan nilai p = 0,000 (p<0,05). Hasil ini menyatakan bahwa perubahan kadar gula darah keempat kelompok memiliki perbedaan yang sangat nyata setelah diberikan masing-masing perlakuan yang dapat dilihat pada Lampiran 12. Untuk mengetahui kelompok yang berbeda dengan kelompok kontrol perlu dilakukan uji lanjut dengan Tamhane test.
6.3.2.4 Uji Tamhane
Tabel 6.2
Analisis Tamhane Setelah Perlakuan Antar Kelompok
Kelompok Beda
rerata
P interpretasi Kontrol negatif dan dosis I 0,249 0,000 Berbeda nyata Kontrol negatif dan uji dosis II 0,185 0,000 Berbeda nyata Kontrol positif dan uji dosis I 0,089 0,285 Tidak berbeda
nyata
Kontrol positif dan uji dosis II 0,026 0,965 Tidak berbeda nyata
Kontrol negatif dan kontrol positif 0,159 0,000 Berbeda nyata Uji dosis I dan uji dosis II 0,063 0,744 Tidak berbeda
nyata
Berdasarkan tabel tersebut, terlihat bahwa kontrol negatif memiliki perbedaan yang nyata (p<0,05) terhadap uji dosis I, uji dosis II, dan kontrol positif. Hasil ini menyatakan bahwa kontrol negatif memiliki nilai perubahan kadar gula darah dan efek yang berbeda dari ketiga kelompok lainnya. Kontrol positif memiliki efek yang tidak berbeda nyata terhadap uji dosis I dan uji dosis II serta uji dosis I dan uji dosis II yang tidak memiliki perbedaan nyata. Maka dapat dinyatakan bahwa ekstrak aseton kulit batang bungur memiliki efek hipoglikemik terhadap darah mencit yang diinduksi aloksan.
Ekstrak kulit batang bungur yang positif tanin mampu memberikan efek hipoglikemik terhadap darah mencit yang diinduksi aloksan, hal ini juga diperkuat dengan hasil uji hipoglikemik ekstrak daun bungur yang mengandung senyawa flavonoid memiliki efek hipoglikemik terhadap darah mencit yang diinduksi aloksan sebanding dengan kontrol positif yaitu glibenklamid (Indradewi, 2011), berdasarkan penelitian Astiti (1990) penggunaan air rebusan daun Bungur (Lagerstroemia speciosa Pers.) dengan kepekatan 10% dan 20% yang diberikan secara oral pada kelinci mampu menurunkan kadar gula darah sebesar 85,97% dan 96,27% dibandingkan dengan tolbutamid 250 mg/kg b.b. Hayashi (2001) telah meneliti tentang elagitanin pada fraksi aseton daun bungur yang dapat menurunkan kadar glukosa darah.
menghambat asupan glukosa dan laju peningkatan glukosa darah tidak terlalu tinggi (Dalimartha, 2005)
6.4 Pemisahan dan Pemurnian Senyawa Tanin
Sebelum dilakukan proses pemisahan menggunakan teknik kromatografi kolom, fase gerak yang akan digunakan dipilih berdasarkan pendekatan pencarian eluen pada kromatografi lapis tipis (KLT). Pemilihan jenis eluen yang terbaik dilakukan dengan mencoba berbagai campuran pelarut yang berbeda polaritasnya untuk dapat memisahkan komponen-komponen yang terdapat pada ekstrak aseton dengan jarak resolusi yang baik. Noda hasil pemisahan dilihat dibawah lampu UV pada panjang gelombang 254 nm dan 365 nm untuk dilihat pola pemisahannya.
Hasil pencarian eluen terbaik dengan kromatografi lapis tipis menunjukkan bahwa campuran eluen etanol:petroleumbenzene:kloroform (1:3:1) memberikan pola noda yang paling baik. Sehingga campuran pelarut tersebut dipilih sebagai fase gerak dalam proses pemisahan dengan kromatografi kolom.
kelompok fraksi yaitu fraksi 1 (F1), F2, F3, F4 selanjutnya keempat fraksi tersebut diuji golongan senyawa taninnya dan dilanjutkan dengan uji kemurniannya dengan metode KLT menggunakan berbagai campuran eluen yang berbeda-beda polaritasnya. Dari hasil uji fitokimia, fraksi 2 (F2) yang positif mengandung tanin adalah F2 dan selanjutnya diuji kemurniannya.
6.4.1 Uji Kemurnian
Hasil uji kemurnian dengan lima (5) jenis eluen, fraksi 2 (F2) tetap memberikan noda tunggal. Hal ini menunjukkan bahwa fraksi 2 relatif murni secara KLT dan selanjutnya fraksi 2 (F2) yaitu isolat positif tanin diidentikasi dengan spektrofotometer UV-Vis dan IR.
6.5 Identifikasi Senyawa Tanin Fraksi 2
Isolat (F2) diukur menggunakan spektrofotometer ultraviolet-tampak dan inframerah.
6.5.1 Spektrofotometer ultraviolet-tampak
yang terjadi pada λ 430 nm adalah transisi π→π* akibat adanya ikatan rangkap terkonjugasi C=C yang diperkuat munculnya gugus C=C pada inframerah pada bilangan gelombang 1458,18 cm-1. Tanin mengandung sistem aromatik yang terkonjugasi oleh karena itu menunjukkan pita serapan yang kuat pada daerah ultraviolet dan tampak (Kopkar, 1990; Harborne, 1987).
6.5.2 Spektrofotometer inframerah
Identifikasi isolat positif tanin (F2) menggunakan spektrofotometri inframerah dilakukan dengan cara sejumlah isolat yang berupa padatan dibuat pellet KBr kemudian diamati spektrumnya pada alat IR Prestige-21 Shimadzu. Berdasarkan spektrum inframerah yang dihasilkan maka data bilangan gelombang, bentuk pita, intensitas, dan penempatan gugus-gugus terkait pada isolat (F2) dipaparkan pada Tabel 6.3.
Tabel 6.3
Data Bilangan Gelombang dan Kemungkinan Gugus Fungsinya
Bilangan Gelombang (cm-1) Bentuk pita Intensitas Penempatan gugus Isolat pustaka
3425,58 3750-3000 Lebar sedang ν O-H bebas
3095,00 3150-3010 Tajam sedang ν CH aromatik
2854,65 3000-2700 Tajam sedang ν CH alifatik
1705,07 1850-1700 Tajam kuat ν C=O
1234,44 1260-1000 Lebar lemah γ O-H
1458,18 1500-1400 tajam kuat ν C=C
aromatik
1373,32 1475-1300 Tajam kuat ν CH alifatik
1049,28 1300-1000 Tajam sedang γ C-O alkohol
810,10 900-700 Tajam lemah γ CH aromatik
Identifikasi dengan spektrofotometer inframerah terhadap fraksi 2 (isolat) menunjukkan serapan melebar pada daerah bilangan gelombang 3425,58 cm-1 yang diduga adalah serapan uluran dari gugus OH bebas dan didukung dengan adanya serapan sedang pada daerah bilangan gelombang 1234,44 cm-1 yang menunjukkan adanya gugus fungsi tekukan OH dan pada bilangan gelombang 1049,28 cm-1 menunjukkan adanya tekukan C-O alkohol. Serapan pita tajam dengan intensitas sedang pada daerah bilangan gelombang 3095,00 cm-1 yang diduga menunjukkan adanya gugus fungsi uluran CH aromatik yang didukung oleh adanya serapan pada bilangan gelombang 810,10 cm-1 yang menunjukkan adanya gugus fungsi tekukan CH aromatik.
Adanya pita tajam dengan intensitas sedang pada bilangan gelombang 2854,65 cm-1 diduga menunjukkan adanya gugus uluran C-H alifatik yang didukung oleh adanya serapan pada bilangan gelombang 1373,32 cm-1 yang menunjukkan adanya gugus fungsi tekukan C-H alifatik.
Serapan pita yang tajam dengan intensitas kuat pada daerah bilangan gelombang 1705,07 cm-1 yang diduga menunjukkan adanya gugus uluran C=O. Adanya serapan pita yang tajam dengan intensitas kuat pada bilangan gelombang 1458,18 cm-1 yang diduga menunjukkan adanya gugus uluran C=C aromatik yang didukung dengan adanya serapan pada bilangan gelombang 617,22 cm-1 yang menunjukkan adanya gugus tekukan C=C.