PENGARUH SUHU DAN WAKTU EKSTRAKSI
TERHADAP KARAKTERISTIK PEKTIN YANG DIISOLASI
DARI POLONG KEDELAI
FAHRANI NISRINA HABIBATI
DEPARTEMEN ILMU DAN TEKNOLOGI PANGAN FAKULTAS TEKNOLOGI PERTANIAN
INSTITUT PERTANIAN BOGOR 2017
PERNYATAAN MENGENAI SKRIPSI DAN SUMBER
INFORMASI SERTA PELIMPAHAN HAK CIPTA
Dengan ini saya menyatakan bahwa skripsi berjudul Pengaruh Suhu dan Waktu Ekstraksi terhadap Karakteristik Pektin yang Diisolasi dari Polong Kedelai adalah benar karya saya dengan arahan dan komisi pembimbing dan belum diajukan dalam bentuk apa pun kepada perguruan tinggi mana pun. Sumber informasi yang berasal dari penulis lain telah disebutkan dalam teks dan dicantumkan dalam Daftar Pustaka di bagian akhir skripsi ini.
Dengan ini saya melimpahkan hak cipta dari skripsi saya kepada Institut Pertanian Bogor.
Bogor, Maret 2017
Fahrani Nisrina Habibati
ABSTRAK
FAHRANI NISRINA HABIBATI. Pengaruh Suhu dan Waktu Ekstraksi terhadap Karakteristik Pektin yang Diisolasi dari Polong Kedelai. Dibimbing oleh BUDIATMAN SATIAWIHARDJA dan NUGRAHA EDHI SUYATMA.
Polong kedelai (Glycine max (L.) Merril sebagai hasil samping produksi kedelai masih memiliki banyak manfaat. Tidak seperti ampas kedelai, limbah ini belum banyak dimanfaatkan. Selain nilai gizi, polong kedelai masih mengandung sejumlah pektin. Sejauh ini kebutuhan terhadap pektin di Indonesia terpenuhi dari hasil impor, padahal sumber pektin seperti pektin dari limbah konsumsi kedelai ini berpotensi menjadi alternatif sumber pektin. Sedikitnya literatur tentang pektin polong kedelai menjadikan perlu dilakukannya penelitian lebih lanjut. Penelitian ini bertujuan untuk mengetahui pengaruh suhu dan waktu ekstraksi terhadap kualitas pektin yang dihasilkan polong kedelai edamame serta mencari kombinasi yang tepat untuk memperoleh hasil yang terbaik. Rancangan percobaan dilakukan dengan Rancangan Acak Kelompok (RAK) dua faktor dan dua taraf perlakuan, yaitu faktor suhu (80°C dan 95°C) dan waktu pemanasan (30 dan 60 menit). Pektin polong kedelai di ekstraksi dengan menggunakan asam klorida. Berdasarkan metode Bayes pektin terbaik yang dihasilkan adalah pektin hasil ekstraksi suhu 95°C selama 60 menit. Pektin yang dihasilkan dari kombinasi proses tersebut diketahui mengandung pektin sebesar 5.16%, 14.80% air, 8.02% abu, 1867.4 mg bobot ekivalen, 3.74% kadar metoksil, 30.41% kadar asam galakturonat, 68.99% derajat esterifikasi, dan viskositas tertentu sebesar 10.5 mpa.s. Sementara pektin komersial yang didapat dari CV. Nura Jaya menghasilkan 7.57% air, 18.66% abu, 49829.9 mg bobot ekivalen, 3.70% kadar metoksil, 21.37% kadar asam galakturonat, 98.30% derajat esterifikasi, dan viskositas tertentu sebesar 4133.3 mpa.s. Pektin hasil penelitian belum memiliki mutu yang lebih baik dari parameter kadar air, bobot ekivalen, derajat esterifikasi, dan viskositas tertentu.
ABSTRACT
FAHRANI NISRINA HABIBATI. The Effects of Temperature and Extraction Time on Characterization of Soybean Pods Pectin. Supervised by BUDIATMAN SATIAWIHARDJA and NUGRAHA EDHI SUYATMA.
Edamame soybean pods (Glycine max (L.) Merrill as a result of the production side of edamame still has many benefits. Unlike soybean hull, waste of soybean pod has not been widely used. Beside nutritional value, soybean pod contains a number of pectin. Indonesia still fulfill the needs of pectin by import. Whereas, the source of pectin such as pectin from waste soybean has the potential to be alternative source of pectin. Since there is very little literature on pectin soybean pod it is necessary to do research for it. This research was aimed to determine the effect of temperature and extraction time on the quality of pectin produced soybean pods and to find the right combination to get the best results. The experimental design was done with Randomized Design method group for two treatment and two factor; temperature (80°C and 95°C) and extraction time (30 and 60 minutes). Pectin soybean pod was extracted using hydrochloric acid. Based on Bayes method, the best pectin was produced in extraction temperature of 95 ° C for 60 minutes. Pectin which was produced from the best combination process contains 5.16% yield, 14.80% moisture, 8.02% ash, 1867.4 mg equivalent weight, 3.74% methoxyl content, 30.41% galacturonic acid, 68.99% degree of esterification, and apparent viscosity 10.5 mpa.s. Whereas, commercial pectin from CV. Nura Jaya contains 7.57% moisture, 18.66% ash, 49829.9 mg equivalent weight, 3.70% methoxyl content, 21.37% galacturonic acid, 98.30% degree of esterification, and apparent viscosity 4133.3 mpa.s. Pectin from this research yet has better quality value related to moisture content, equivalent weight, degree of esterification and apparent viscosity.
PENGARUH SUHU DAN WAKTU EKSTRAKSI
TERHADAP KARAKTERISTIK PEKTIN YANG DIISOLASI
DARI POLONG KEDELAI
FAHRANI NISRINA HABIBATI
Skripsi
sebagai salah satu syarat untuk memperoleh gelar Sarjana Teknologi Pertanian
pada
Departemen Ilmu dan Teknologi Pangan
DEPARTEMEN ILMU DAN TEKNOLOGI PANGAN FAKULTAS TEKNOLOGI PERTANIAN
INSTITUT PERTANIAN BOGOR BOGOR
Judul Skripsi: Pengaruh Suhu dan Waktu Ekstraksi terhadap Karakteristik Pektin yang Diisolasi dari Polong Kedelai
Nama : Fahrani Nisrina Habibati
NIM : F24120033
Disetujui oleh
Dr Ir Budiatman Satiawihardja MSc Dr. Nugraha Edhi Suyatma STP DEA
Pembimbing 1 Pembimbing 2
Diketahui oleh
Dr Ir Feri Kusnandar, MSc Ketua departemen
PRAKATA
Puji dan syukur penulis panjatkan kepada Allah SWT atas berkat dan rahmat-Nya penelitian serta penulisan karya ilmiah ini dapat diselesaikan. Penelitian ini dilakukan pada bulan September hingga Januari 2016 di laboratorium SEAFAST, Institut Pertanian Bogor dan beberapa laboratorium analisis di Departemen Ilmu dan Teknologi Pangan IPB. Pada penelitian ini, penulis melakukan ekstraksi pektin dari sumber polong kedelai dan melakukan analisis karakteristiknya yang dibandingkan dengan pektin komersial. Penelitian ini berjudul “Pengaruh Suhu dan Waktu Ekstraksi terhadap Karakteristik Pektin yang Diisolasi dari Polong Kedelai”
Terima kasih penulis ucapkan kepada Dr. Ir. Budiatman Satiawihardja MSc dan Dr. Nugraha Edhi Suyatma STP DEA selaku pembimbing atas bimbingan, arahan, dan pembelajaran yang telah diberikan selama masa studi penulis di Institut Pertanian Bogor serta kepada Dr. Ir. Feri Kusnandar MSc selaku penguji atas masukan dan arahannya dalam penyempurnaan karya tulis ini. Terima kasih juga penulis sampaikan kepada kedua orang tua, Bapak Farkhani Koesnindar dan Ibu Farida Handayani, Fahry Adam atas dukungan, kesabaran dan doa selama penulis menyelesaikan penelitian dan penulisan karya ilmiah ini, juga kepada rekan-rekan satu bimbingan: Ratu, Astrie, Nabhiela, Lidya, Shabrina atas bantuannya dalam mengerjakan penelitian dan penyusunan skripsi ini. Penulis juga menyampaikan terima kasih kepada teman-teman ITP49, teman-teman IAAS, teman-teman TPB, teman-teman asrama A4, teman-teman kosan Cibanteng Proyek, teman-teman OPPO Campus Club atas dukungannya sehingga penulis dapat menyelesaikan studi di IPB. Secara khusus, penulis juga menyampaikan terima kasih kepada Soraya, Bunga, Erka, Raudhah, Nevvi, Adan, Ivan, Ega, Kevin, Eric, Aufar, Hesti, Reni, Dinny, Tyo, Goklas, Maskun, Dewo, Radit, Wiysha, Ayida, Annisa, Danifan serta teman-teman lainnya atas dukungan dan bantuannya selama penulis menyelesaikan karya ilmiah ini. Semoga karya ilmiah ini bermanfaat.
Bogor, Maret 2017
DAFTAR ISI
DAFTAR TABEL vi DAFTAR GAMBAR vi DAFTAR LAMPIRAN vi PENDAHULUAN 1 Latar Belakang 1 Perumusan Masalah 1 Tujuan Penelitian 2 Manfaat Penelitian 2 TINJAUAN PUSTAKA 2 Kedelai 2 Pektin 2Struktur dan Komposisi Kimia Pektin 4
Sifat Pektin 4
Aplikasi Pektin 5
METODE 6
Waktu dan Tempat Penelitian 6
Bahan 6
Alat 6
Prosedur Penelitian 6
Prosedur Analisis Data 8
HASIL DAN PEMBAHASAN 11
Karakteristik Pektin 11 Rendemen 11 Kadar Air 12 Kadar Abu 13 Bobot Ekivalen 14 Kadar Metoksil 15
Kadar Asam Galakturonat 16
Derajat Esterifikasi 17
Perlakuan terbaik 19 SIMPULAN 21 SARAN 21 DAFTAR PUSTAKA 22 LAMPIRAN 25
DAFTAR TABEL
Penentuan bobot karakteristik mutu pektin 19
Penentuan karakteristik pektin polong kedelai dengan metode Bayes 20 Perbandingan pektin polong kedelai hasil penelitian dengan pektin 20
DAFTAR GAMBAR
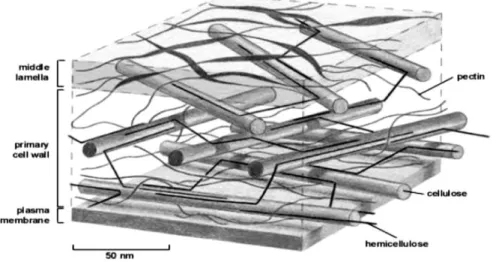
Struktur Dinding Sel Tanaman 3
Struktur Kimia Asam Poligalakturonat 4
Diagram alir ekstraksi pektin 7
Hubungan perlakuan suhu (80°C dan 95°C) dan waktu (30 dan 60 menit)
ekstraksi terhadap rendemen pektin polong kedelai 12
Hubungan perlakuan suhu (80°C dan 95°C) dan waktu (30 dan 60 menit)
ekstraksi terhadap kadar air pektin polong kedelai 13
Hubungan perlakuan suhu (80°C dan 95°C) dan waktu (30 dan 60 menit)
ekstraksi terhadap kadar abu pektin polong kedelai 14
Hubungan perlakuan suhu (80°C dan 95°C) dan waktu (30 dan 60 menit) ekstraksi terhadap bobot ekivalen pektin polong kedelai 15 Hubungan perlakuan suhu (80°C dan 95°C) dan waktu (30 dan 60 menit)
ekstraksi terhadap kadar metoksil pektin polong kedelai 16 Hubungan perlakuan suhu (80°C dan 95°C) dan waktu (30 dan 60 menit)
ekstraksi terhadap kadar galakturonat pektin polong kedelai 17 Hubungan perlakuan suhu (80°C dan 95°C) dan waktu (30 dan 60 menit)
ekstraksi terhadap kadar galakturonat pektin polong kedelai 18 Hubungan perlakuan suhu (80°C dan 95°C) dan waktu (30 dan 60 menit)
ekstraksi terhadap apparent viscosity pektin polong kedelai 19
DAFTAR LAMPIRAN
Dokumentasi proses produksi polong kedelai 25
Dokumentasi pektin kering polong kedelai 26
Hasil uji statistik analisis bobot ekivalen 26
Hasil uji statistik analisis kadar metoksil 27
Hasil uji statistik analisis kadar galakturonat 27
Hasil uji statistik analisis derajat esterifikasi 28
1
PENDAHULUAN
Latar BelakangPektin biasanya banyak terdapat pada limbah pertanian salah satunya pada kulit. Di Indonesia, pektin masih merupakan barang impor dan belum cukup terkenal. Pada tahun 2007, Indonesia mengimpor pektin sebesar 136.334 kg dan meningkat pada tahun 2008 menjadi 670.410 kg (BPS 2010).
Indonesia memiliki berbagai jenis kacang salah satunya adalah yang sedang banyak dikembangkan yaitu edamame (Glycine max L). Edamame memiliki nilai jual lebih tinggi dibandingkan dengan kacang kedelai biasa. Jepang adalah produsen komersial edamame terbesar, hampir 105.000 miliar pada tahun 1988 (MAFF 1990) sekaligus importir terbesar sebanyak lebih dari 33.000 miliar pada tahun 1989 (JTA 1989). Taiwan memasok lebih dari 99% jumlah impor produk edamame beku Jepang. Negara-negara lain yang juga telah menghasilkan edamame dalam jumlah besar adalah Argentina, Australia, Israel, Mongolia, Selandia Baru, Taiwan dan Thailand. Sementara dengan skala lebih kecil diproduksi oleh; Bhutan, Brazil, Inggris, Chile, Prancis, Jerman, Indonesia, Malaysia, Nepal, Filipina, Singapura, dan Sri Lanka (Wang et al. 1979). Menurut Rukmana (1996), beberapa varietas kedelai edamame beradaptasi dengan baik di Indonesia dengan potensi hasil polong segar sekitar 5-12 ton/hektar.
Sentra produksi edamame di Indonesia terdapat di daerah Jember (Jawa Timur), Wonogiri (Jawa Tengah) dan Ciawi-Bogor (Jawa Barat). Sekitar 65% dari total produksi edamame oleh PT Mitratani Dua Tujuh diekspor ke Jepang. Indonesia berada pada urutan ke empat yang paling besar mengekspor edamame ke Jepang setelah China, Taiwan dan Thailand. Hal ini masih menunjukkan bahwa Indonesia memiliki potensi pasar yang terbuka luas untuk mengekspor komoditas edamame ke Jepang. Berdasarkan hasil penelitian, preferensi konsumen Indonesia dalam pembelian edamame kemasan dipengaruhi oleh variabel produk dan promosi, sedangkan harga edamame dan distribusi tidak memiliki pengaruh nyata (Poerwanto 2014).
Kedelai biasa maupun edamame biasa dikonsumsi tanpa polongnya. Polong kedelai adalah 2/3 bagian dari total kedelai utuh. Polong kedelai saat ini belum banyak dimanfaatkan, padahal berdasarkan penelitian Wheeler (1990) polong kedelai masih memiliki zat yang baik untuk tubuh seperti protein 3-5%, karbohidrat 42-60%, serta serat kasar 30%.
Polong kedelai mengandung pektin yang belum diketahui kadarnya. Penelitian ini dilakukan untuk mengidentifikasi banyaknya pektin yang tersedia pada polong kedelai beserta karakteristik lainnya dibandingkan dengan pektin komersial.
Perumusan Masalah
Pemanfaatan polong kedelai belum banyak dilakukan. Padahal, polong kedelai masih memiliki kandungan gizi dan non-gizi termasuk kandungan pektin. Selain itu, pektin dengan sumber berbeda mungkin memiliki kondisi yang berbeda untuk mencapai karakteristik pektin yang terbaik. Oleh karena itu diperlukan
2
kajian/ penelitian tentang karakteristik pektin yang terkandung dalam polong kedelai yaitu jenis kedelai edamame.
Tujuan Penelitian
Secara umum penelitian ini dilakukan untuk mentukan kondisi proses pembuatan pektin dari bahan baku polong kacang kedelai. Secara khusus penelitian ini bertujuan untuk mempelajari karakteristik sifat kimia dan fisik untuk mendapatkan pektin terbaik dari ekstraksi pektin polong kedelai jenis edamame dengan perlakuan waktu dan suhu dibandingkan dengan standar mutu pektin komersial.
Manfaat Penelitian
Penelitian ini diharapkan dapat bermanfaat sebagai referensi industri dan akademisi dalam mencari alternatif sumber pektin dan referensi kondisi proses untuk menghasilkan pektin. Selain itu, pengembangan pektin polong kedelai jenis edamame juga dapat bermanfaat dalam meningkatkan varietas kedelai dan nilai tambahnya.
TINJAUAN PUSTAKA
Kedelai
Kedelai Glycine max (L.) Merrill merupakan tanaman pangan berupa semak yang tumbuh tegak. Kedelai merupakan salah satu tanaman budidaya dengan kandungan nutrisi yang tinggi, diantaranya megandung protein 30-50% (Richard et
al 1984). Selain itu kedelai segar juga mengandung 63% kadar air, 11.7% pati,
19.6% lemak (Stevenson 2007), 6% serat kasar (Duke 1986). Salah satu jenis kedelai yang saat ini banyak dikonsumsi adalah kedelai edamame yaitu kedelai yang dipanen ketika benih pada tahap R6 belum matang dan telah mencapai 80 sampai 90% lebar dari polongnya (Konovsky et al. 1992). Kedelai edamame dikonsumsi sebagai sayuran hampir di setiap negara yang memproduksi kedelai. Kelebihan kedelai edamame dibandingkan dengan kedelai biasa adalah memiliki cita rasa yang manis, polongnya berukuran besar, dan umur panennya pendek antara 50-60 hari setelah tanam (Rukmana 1996). Penanaman kedelai edamame dimulai pada bulan November dan produksi berakhir dengan panen terakhir pada bulan Juli.
Pektin
Menurut Andarwulan et al. (2011), serat merupakan total karbohidrat yang tidak dapat dicerna yang terdapat dalam bahan pangan. Pada umumnya, serat terdiri dari bahan penyusun dinding sel, yaitu selulosa, hemiselulosa, lignin, pektin, dan gom. Serat ada yang bersifat larut dan ada yang tidak larut dalam air. Selulosa,
3
lignin dan hemiselulosa termasuk serat yang tidak dapat larut, sedangkan pektin dan gom termasuk serat yang dapat larut. Berdasarkan fungsinya di dalam tanaman, serat dibagi menjadi tiga fraksi utama, yaitu (a) poliskarida struktural yang terdapat pada dinding sel tumbuhan, yaitu selulosa, hemiselulosa dan substansi pektat; (b) non-polisakarida struktural yang sebagian besar terdiri dari lignin; dan (c) polisakarida non-struktural, yaitu gom dan agar-agar.
Pektin adalah substansi alami yang terdapat pada sebagian besar tanaman pangan. Selain sebagai elemen struktural pada pertumbuhan jaringan dan
komponen utama dari lamella tengah pada tanaman, pektin juga berperan sebagai perekat dan menjaga stabilitas jaringan dan sel (Herbstreith dan Fox, 2005 dalam Hariyati, 2006). Gambar 1 menunjukkan keberadaan senyawa pektin pada dinding sel tanaman.
Pektin tersusun atas asam pektat, asam pektinat dan protopektin (Hanum dkk 2012) yang dijelaskan sebagai berikut:
1) Asam Pektat
Asam pektat adalah senyawa asam galakturonat yang bersifat koloid dan pada dasarnya bebas dari kandungan metil ester (Hanum dkk 2012). Asam pektat merupakan senyawa pektin dengan gugus karboksil yang tidak teresterifikasi pada asam galakturonat. Asam pektat bersifat tidak larut dalam air dan tidak membentuk gel. Namun, jika membentuk garam, asam pektat disebut pektat dan dapat larut dalam air (Perina 2007).
2) Asam Pektinat
Asam pektinat adalah asam poligalakturonat yang bersifat koloid dan mengandung sejumlah metil ester (Hanum dkk 2012). Pektin memiliki derajat netralisasi yang berbeda-beda. Pektinat yang mengandung metil ester yang cukup yaitu lebih dari 50% dari seluruh karboksil disebut pektin. Pektin ini terdispersi dalam air dan dapat membentuk garam yang disebut garam pektinat. Dalam bentuk garam ini, pektin berfungsi dalam pembuatan jeli dengan keberadaan gula dan asam (Perina 2007).
4
3) Protopektin
Protopektin merupakan senyawa-senyawa pektin yang terdapat pada tanaman yang masih muda atau pada buah–buahan yang belum matang. Protopektin tidak larut dalam air. Namun, jika dipanaskan dalam air yang mengandung asam, maka protopektin dapat diubah menjadi pektin dan terdispersi dalam air. Protopektin akan menjadi pektin yang larut dengan adanya hidrolisis asam, secara enzimatis dan secara fisis oleh pemanasan. Hasil dari hidrolisis adalah asam pektinat (Perina 2007).
Kadar substansi pektat dapat ditentukan berdasarkan metode spektrofotometri dan gravimetri. Pada metode spektrofotometri penetapan didasarkan atas reaksi antara O-hidroksi difenil dengan anhidrogalakturonat yang menghasilkan warna yang dapat diukur pada panjang gelombang 520 nm. Sementara dengan metode gravimetri pektin yang telah diekstrak dari contoh disaponifikasi dengan alkali dan diendapkan sebagai kalsium pektat dengan menambahkan kalsium klorida dalam suasana asam. Endapan kalsium pektat dicuci sampai bebas klorida, kemudian dikeringkan dan ditimbang bobotnya (Andarwulan
et al. 2011).
Struktur dan Komposisi Kimia Pektin
Substansi pektat atau pektin merupakan poligalakturonat dengan rantai linear yang terdiri dari unit asam α-D-galakturonat yang dihubungkan dengan ikatan α-(1,4)-glikosida. Grup karboksil dari asam poligalakturonat sebagian teresterifikasi oleh grup metil dan sebagian atau seluruhnya dinetralkan oleh satu atau lebih jenis basa (Andarwulan et al. 2011). Gugus karboksil sebagian teresterifikasi dengan metanol dan sebagian gugus alkohol sekunder terasetilasi (Herbstreith dan Fox 2005 dalam Hariyati 2006). Gambar 2 di bawah ini menunjukkan struktur kimia unit asam poligalakturonat.
Gambar 2 Struktur Kimia Asam Poligalakturonat
Sifat Pektin
Pektin merupakan zat berbentuk serbuk kasar hingga halus yang berwarna putih, kekuningan, kelabu atau kecoklatan dan banyak terdapat pada buah-buahan dan sayuran matang. Gliksman (1969) dalam Hariyati (2006) menyatakan bahwa pektin kering yang telah dimurnikan berupa kristal yang berwarna putih dengan kelarutan yang berbeda-beda sesuai dengan kandungan metoksilnya. Kualitas pektin dikatakan tinggi jika mampu membentuk gel yang kuat, yang didapat dari semakin tinggi kadar metoksil dan semakin panjangnya rantai galakturonat.
5
Menurut Vaclavic dan Christian (2008), pektin dapat dibedakan menjadi dua golongan berdasarkan banyaknya gugus karboksil yang mengalami esterifikasi, yaitu: 1) High Methoxyl Pectin (HMP), yaitu pektin yang mengandung gugus metoksil sekurang-kurangnya 7-8%. HMP mengandung 50-58% gugus karboksil yang teresterifikasi. HMP hanya dapat membentuk gel dengan gula dan asam pada kadar gula 60-65%, oleh karena itu HMP dapat dimanfaatkan dalam pembuatan jeli; 2) Low Methoxyl Pectin (LMP), yaitu pektin yang mengandung gugus metoksil kurang dari 7% (biasanya 3-5%). Pada LMP, hanya 20-40% gugus karboksil yang teresterifikasi. LMP dapat membentuk gel pada kadar gula 10-20% dan dengan ion bivalen yaitu kalsium.
Kualitas pektin komersial ditentukan oleh sifat-sifat fisik pektin. Sifat fisik tersebut diantaranya warna dan cita rasa yang cocok, kelarutan, derajat gel, kecepatan membeku, serta tidak mengandung bahan atau zat berbahaya bagi kesehatan. Sifat fisik tersebut dipengaruhi oleh sifat kimia pektin (Hariyati 2006).
Grade pektin merupakan indikasi penting yang menggambarkan mutu
pektin. Grade pektin didefinisikan sebagai jumlah gula yang dibutuhkan oleh satu bagian pektin untuk membentuk gel yang diinginkan pada kondisi yang sesuai. Pektin yang mempunyai grade pektin 100 berarti dapat membentuk gel yang baik dengan 100 g gula. Penentuan grade pektin biasanya menggunakan metode
International Food Technologist (IFT) yaitu dengan membuat gel dengan
konsentrasi gula 65% pada pH 2.2-2.4. Gel kemudian disimpan selama 18-24 jam dan kemudian diuji dengan alat Ridgelimeter. Selain grade pektin, dalam standardisasi pektin sering digunakan istilah setting time. Setting time adalah waktu yang diperlukan untuk terbentuknya gel sejak bahan-bahan pembentuk gel ditambahkan. Kecepatan pembentuk gel ditentukan oleh mutu gel (Widiastuti 2015).
Aplikasi Pektin
Pektin digunakan secara luas sebagai komponen fungsional pada industri makanan karena kemampuannya membentuk gel encer dan menstabilkan protein (May 1990). Pektin dapat digunakan sebagai stabilizer dan pengental pada minuman sari buah, pemberi tekstur yang baik pada roti dan keju, serta bahan pokok pembuatan jeli, jam, dan marmalade (Herbstreith dan Fox 2005). Penambahan pektin pada makanan juga dapat memengaruhi proses metabolisme dan pencernaan khususnya pada adsorpsi glukosa dan kolesterol (Baker 1994).
Pektin dalam pemanfaatannya digolongkan sebagai food additive dan ditemukan secara alami pada tanaman maka Food and Drug Administration (FDA) menggolongkannya sebagai bahan tambahan makanan yang aman (Perina 2007).
6
METODE
Waktu dan Tempat Penelitian
Penelitian ini dilaksanakan di Laboratorium Kimia dan Mikrobiologi SEAFAST, Institut Pertanian Bogor. Penelitian dimulai pada bulan September 2016 sampai Februari 2017.
Bahan
Bahan baku yang digunakan adalah kedelai utuh jenis edamame yang diproduksi oleh PT Mitra Tani 27 Jember diperoleh di Lotte Mart di Bogor dan pektin komersial yang dibeli dari CV. Nura Jaya. Bahan kimia yang dipakai dalam ekstraksi pektin antara lain HCl 0.05 N dan 2-propanol. Bahan untuk analisis adalah HCl 0.2 N, NaOH 0.1 N, NaOH 0.25 N, phenol red, etanol 96%, aquades, NaCl, asam phtalate.
Alat
Alat yang digunakan diantaranya blender, cabinet dryer, oven, ayakan 20 mesh, tanur, tray, gelas ukur, gelas piala, magnetic stirrer, buret, hot plate,
centrifuge Hermile Z 383 K, cawan petri, cawan porselen, cawan aluminium,
baskom, thermometer, pH meter, viscometer Brookfield dan alat-alat laboratorium lainnya.
Prosedur Penelitian
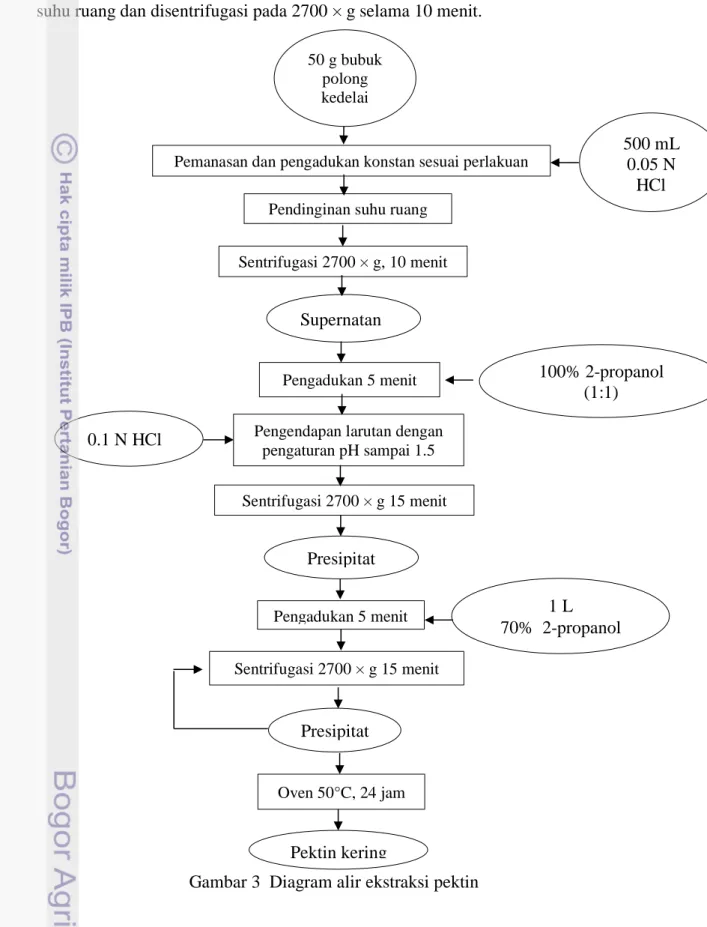
Penelitian ini dilakukan dengan melalui tiga tahapan penelitian yaitu pemisahan polong kedelai, ekstraksi pektin, dan isolasi pektin. Diagram alir ekstraksi pektin dapat dilihat pada Gambar 3.
Pemisahan polong kedelai
Polong pada kedelai dipisahkan manual setelah mengalami tahapan perebusan pada air selama 5 menit. Hal ini dilakukan untuk menyesuaikan cara konsumsi kedelai rebus. Polong kedelai yang telah dipisahkan kemudian di-blender dengan tambahan air 2 kali bobot polong lalu dikeringkan dalam oven 60oC selama 5-7 jam.
Ekstraksi pektin
Sebanyak 50 gram bubuk kasar polong kedelai yang telah dipisahkan dari kedelai dilarutkan menggunakan 500 mL 0.05 M HCl pada suhu dan waktu sesuai perlakuan dengan pengadukan konstan (Monsoor dan Proctor 2001). Pada kondisi ini pH larutan menjadi 1.5. Menurut Fardiaz (1984), ekstraksi pada pH 1.5 memberikan jumlah rendemen pektin kulit jeruk tertinggi. Kondisi panas dan asam
7
menyebabkan terjadi perubahan senyawa pektin yang disebabkan oleh proses hidrolisis protopektin. Proses tersebut menyebabkan protopektin berubah menjadi pektinat (pektin). Apabila proses hidrolisis dilanjutkan senyawa pektin akan perubah menjadi asam pektat (Tuhuloula, 2013). Hasil ekstraksi didinginkan pada suhu ruang dan disentrifugasi pada 2700 × g selama 10 menit.
Gambar 3 Diagram alir ekstraksi pektin
Pemanasan dan pengadukan konstan sesuai perlakuan Pendinginan suhu ruang
Sentrifugasi 2700 × g, 10 menit
Pengendapan larutan dengan pengaturan pH sampai 1.5 Supernatan Pengadukan 5 menit 0.1 N HCl 100% 2-propanol (1:1) Sentrifugasi 2700 × g 15 menit Pengadukan 5 menit 1 L 70% 2-propanol Sentrifugasi 2700 × g 15 menit Presipitat 500 mL 0.05 N HCl Presipitat 50 g bubuk polong kedelai Oven 50°C, 24 jam Pektin kering
8
Isolasi Pektin
Supernatan dipisahkan dan dilarutkan dalam 2-propanol 100% dengan perbandingan 1:1. Proses ini dapat dinamakan dehidrasi pektin. Proses dehidrasi pektin merupakan suatu proses pemisahan pektin dari larutannya. Pektin adalah koloid hidrofilik yang bermuatan negatif (dari gugus karboksil bebas yang terionisasi) dan tidak mempunyai titik isoelektrik seperti kebanyakan koloidal hidrofilik. Penambahan alkohol dapat mengganggu stabilitas larutan pektin sehingga pektin akan terkoagulasi (Rouse 1977). Larutan diaduk selama 5 menit kemudian di sentrifugasi kembali selama 15 menit pada 2700 × g. Suspensi ini tidak boleh dibiarkan lebih dari 4 jam karena akan membentuk lapisan. Endapan dikumpulkan dan dicuci dengan 2-propanol 70% dengan perbandingan 1:3, diaduk selama 10 menit lalu dilakukan sentrifugasi kembali selama 15 menit. Pencucian dilakukan untuk menghilangkan residu klorida. Endapan yang didapat setelah sentrifugasi merupakan pektin basah yang kemudian dikeringkan dalam oven 50 oC selama 24 jam. Pengeringan dengan suhu rendah bertujuan meminimalkan degradasi pektin.
Prosedur Analisis Data Rendemen
Perhitungan rendemen dilakukan dengan menimbang pektin kering yang dihasilkan kemudian dibagi dengan bobot bahan baku yang telah dikeringkan.
Perhitungan :
Rendemen (%) = Bobot pektin (gram)
Bobot bobot kering bahan baku (gram)x 100
Kadar Air (SNI 01-2891-1992)
Kadar air menyatakan kandungan air yang terdapat dalam pektin. Pektin komersial biasanya memiliki kadar air 8%. Kadar air dipengaruhi oleh proses pemurnian pektin baik dengan penguapan maupun pada saat pengeringan. Pengukuran kadar air dilakukan dengan menimbang sampel sebanyak 5 g setelah cawan aluminium dikeringkan di dalam oven selama 15 menit lalu didinginkan dalam desikator. Cawan yang sudah berisi sampel dikeringkan pada oven suhu 105oC selama 3 jam. Cawan didinginkan kemudian ditimbang.
Perhitungan:
Kadar Air (% b.k) = W −(W1 − W2) W1 − W2 x 100
Keterangan : W = bobot contoh
W1 = bobot contoh + cawan kering W2 = bobot cawan kosong
9
Kadar Abu (SNI 01-2891-1992)
Kadar abu menyatakan banyaknya abu setelah pembakaran. Kadar abu menunjukkan masih ada komponen organik yang tertinggal dalam pektin. Semakin kecil kadar abu maka kemurnian pektin semakin baik. Pektin dengan mutu terbaik memiliki kadar abu 0%. Prosedur analisis kadar abu yaitu dengan mengeringkan cawan porselin kosong di dalam oven bersuhu 105oC selama 15 menit dan didinginkan dalam desikator. Cawan kemudian ditimbang dan dicatat bobotnya. Sebanyak 1.5 g contoh ditimbang kemudian dipanaskan didalam tanur listrik pada suhu maksimum 550oC sampai pengabuan sempurna. Cawan didinginkan di dalam desikator dan kemudian ditimbang.
Perhitungan:
Kadar Abu (% b.k) = W1−W2
W x 100
Keterangan : W = bobot contoh
W1= bobot contoh + cawan diabukan W2= bobot cawan kosong
Bobot Ekivalen
Bobot Ekivalen menyatakan banyaknya kandungan karboksil yang tidak teresterifikasi dalam rantai poligalakturonat pektin. Nilai bobot ekivalen ditentukan berdasarkan reaksi penyabunan gugus karboksil oleh NaOH dimana bobot ekivalen akan berbanding terbalik dengan banyaknya volume NaOH yang digunakan untuk bereaksi dengan gugus karboksil. Semakin kecil bobot ekivalen maka kandungan metoksilnya semakin tinggi.
Pektin sebanyak 0.5 gram dibasahi dengan 5 ml etanol 96% dan dilarutkan dalam 100 ml akuades yang berisi 1 gram NaCl. Pemberian garam digunakan untuk mempertajam titik akhir. Larutan hasil campuran tersebut dititrasi perlahan-lahan dengan NaOH 0.1 N dengan indikator fenol merah sampai terjadi perubahan menjadi merah kekuningan (pH 7.5) yang bertahan 30 detik. Indikator fenol merah memiliki pH 6.8-8.2 (Haryadi 1990). Titrasi dilakukan perlahan untuk menghindari deesterifikasi. Bobot ekivalen dihitung dengan rumus (Ranganna 1977):
Perhitungan:
Bobot ekivalen (mg) = Bobot sampel (g) x 1000 Volume NaOH (ml)x N NaOH
Kadar Metoksil
Kadar metoksil adalah faktor penting dalam mengontrol setting time, sensitivitas kation polivalen, dan kegunaan pada gel, film dan serat pada pektin (Ranganna 1977). Berdasarkan kandungan metoksilnya, pektin dapat dibagi menjadi dua golongan yaitu pektin berkadar metoksil tinggi (HMP), dan pektin berkadar metoksil rendah (LMP). Pektin bermetoksil tinggi mempunyai kandungan metoksil minimal 7%, sedangkan pektin bermetoksil rendah mempunyai kandungan pektin maksimal 7% (Hariyati, 2006). Kadar metoksil menyatakan banyaknya gugus metil yang teresterifikasi. Kadar metoksil berpengaruh terhadap
10
kemampuan pembentukan gel yang baik. Semakin besar kandungan metoksil maka kemampuan pembentukan gel akan semakin besar.
Larutan netral dari penentuan BE ditambah 25 ml larutan NaOH 0.25 N dan dikocok serta dibiarkan selama 30 menit dalam keadaan tertutup. Selanjutnya ditambahkan 25 ml HCl 0.25 N dan dititrasi dengan larutan NaOH 0.1 N dengan indikator fenol merah sampai titik akhir. Penambahan HCl ini sebanding dengan ekivalen pada basa yang ditambahkan (Ranganna 1977).
Perhitungan:
Kadar metoksil (%) = Volume NaOH x N NaOH x 3.1 Bobot sampel (g)
Kadar Asam Galakturonat
Pektin yang berupa poligalakturonat yang teresterifikasi sebagian mengandung 10% atau lebih kandungan organik seperti arabinosa, galaktosa dan mungkin gula. Penentuan kadar asam galakturonat penting untuk menentukan kemurnian pektin, derajat esterifikasi, dan untuk mengevaluasi karakteristik fisik dari pektin (Ranganna 1977). Semakin besar kadar asam galakturonat maka pektin akan semakin murni karena semakin kecil kandungan organiknya.
Kadar galakturonat dihitung dari mek (miliekivalen) NaOH yang diperoleh dari penentuan bobot ekivalen dan kandungan metoksil (Meilina 2003).
Perhitungan:
Kadar asam galakturonat (%) = mek (BE+KM) x 176 x 100 Bobot sampel (mg)
Nilai 176 didapat dari bobot molekul galakturonat.
Derajat Esterifikasi
Derajat esterifikasi adalah jumlah asam D-galakturonat teresterifikasi per jumlah total asam anhidrogalakturonat dikali 100. Derajat esterifikasi menentukan sifat-sifat pektin terutama kelarutan dan pembentukan gel. Derajat esterifikasi dihitung dari kadar metoksil dan kadar galakturonat yang diperoleh (Meilina 2003).
Perhitungan:
Derajat esterifikasi (%) = kadar metoksil x 176 x 100 kadar galakturonat x 31
Viskositas Tertentu (Apparent Viscosity)
Serbuk pektin ditimbang sebanyak 3 gram dan dilarutkan dalam 250 ml pelarut akuades kemudian dilakukan pengadukan konstan selama 4 jam pada suhu kamar. Larutan kemudian dipindahkan kedalam tabung gelas dan diukur menggunakan viskometer brookfield dengan spindel no. 1 dengan speed 60 selama 1 menit. Pada pektin komersial, kekentalan pektin berbeda sehingga spindel dan
speed yang digunakan berbeda yaitu spindel no. 2 dengan speed 6. Tuas lalu ditekan
dan dibaca angka yang tertera pada viskometer. Viskositas didapat dengan mengalikan faktor konversi dengan angka yang terbaca.
11
Rancangan Percobaan
Faktor perbandingan formulasi pelapis edibel berbasis pektin terdiri atas dua faktor perlakuan. Faktor pertama yaitu suhu ekstraksi (T) yang terdiri dari dua taraf yaitu 80oC dan 95oC. Faktor kedua yaitu waktu ekstraksi yang terdiri dari dua taraf yaitu 30 menit dan 60 menit. Masing-masing faktor menggunakan rancangan acak kelompok sebagai rancangan percobaannya. Model linier yang tepat untuk rancangan acak kelompok adalah:
Yij(t) = µ + Kj + P(t) + εi(t) dimana:
i = 1, 2, ...n; dan t = 1, 2, ...n
Yi(t) = nilai pengamatan pada baris ke-i, kolom ke-j yang mendapat perlakuan ke-t.
µ = nilai rata-rata umum
Ki = pengaruh kelompok ke-i P(t) = pengaruh perlakuan ke-t
ei(t) = pengaruh galat pada kelompok ke-i, yang memperoleh perlakuan ke-t
Data diolah menggunakan uji parametrik analisis keragaman (ANOVA). Tidak dilakukan uji lanjut karna taraf kurang dari 3. Penentuan perlakuan terbaik dilakukan dengan pembobotan terhadap parameter sesuai tingkat kepentingannya (metode Bayes). Pemberian bobot ini dilakukan berdasarkan penilaian dari ahli yang banyak mengetahui tentang pektin dan aplikasinya.
HASIL DAN PEMBAHASAN
Karakteristik Pektin Rendemen
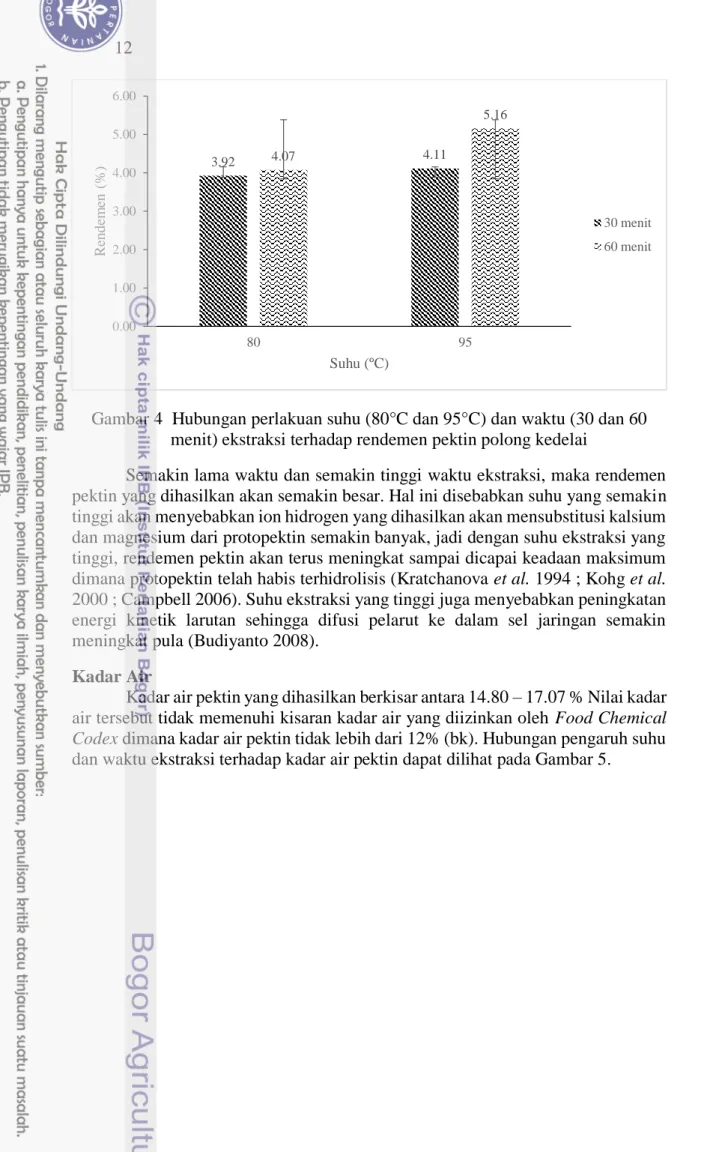
Rendemen pektin yang dihasilkan dari berbagai perlakuan berkisar antara 3.92 – 5.16 % (bk). Grafik hubungan perlakuan suhu dan waktu ekstraksi terhadap rendemen pektin yang dihasilkan pada Gambar 4.
12
Gambar 4 Hubungan perlakuan suhu (80°C dan 95°C) dan waktu (30 dan 60 menit) ekstraksi terhadap rendemen pektin polong kedelai
Semakin lama waktu dan semakin tinggi waktu ekstraksi, maka rendemen pektin yang dihasilkan akan semakin besar. Hal ini disebabkan suhu yang semakin tinggi akan menyebabkan ion hidrogen yang dihasilkan akan mensubstitusi kalsium dan magnesium dari protopektin semakin banyak, jadi dengan suhu ekstraksi yang tinggi, rendemen pektin akan terus meningkat sampai dicapai keadaan maksimum dimana protopektin telah habis terhidrolisis (Kratchanova et al. 1994 ; Kohg et al. 2000 ; Campbell 2006). Suhu ekstraksi yang tinggi juga menyebabkan peningkatan energi kinetik larutan sehingga difusi pelarut ke dalam sel jaringan semakin meningkat pula (Budiyanto 2008).
Kadar Air
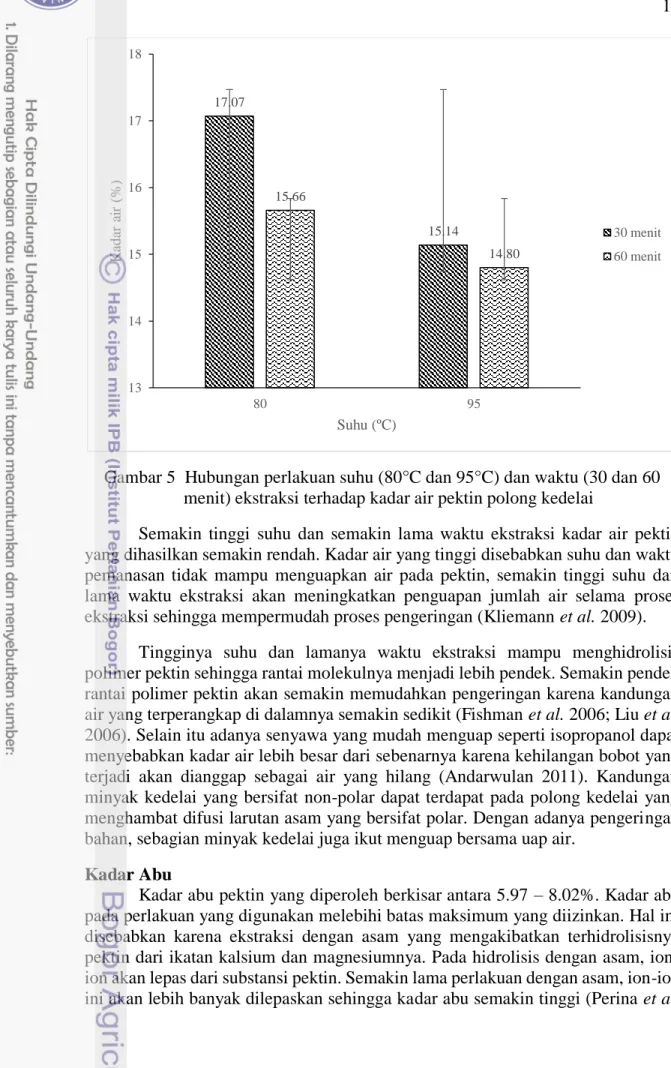
Kadar air pektin yang dihasilkan berkisar antara 14.80 – 17.07 % Nilai kadar
air tersebut tidak memenuhi kisaran kadar air yang diizinkan oleh Food Chemical
Codex dimana kadar air pektin tidak lebih dari 12% (bk). Hubungan pengaruh suhu
dan waktu ekstraksi terhadap kadar air pektin dapat dilihat pada Gambar 5.
3.92 4.07 4.11 5.16 0.00 1.00 2.00 3.00 4.00 5.00 6.00 80 95 R en de m en ( % ) Suhu (ºC) 30 menit 60 menit
13
Gambar 5 Hubungan perlakuan suhu (80°C dan 95°C) dan waktu (30 dan 60 menit) ekstraksi terhadap kadar air pektin polong kedelai
Semakin tinggi suhu dan semakin lama waktu ekstraksi kadar air pektin yang dihasilkan semakin rendah. Kadar air yang tinggi disebabkan suhu dan waktu pemanasan tidak mampu menguapkan air pada pektin, semakin tinggi suhu dan lama waktu ekstraksi akan meningkatkan penguapan jumlah air selama proses ekstraksi sehingga mempermudah proses pengeringan (Kliemann et al. 2009).
Tingginya suhu dan lamanya waktu ekstraksi mampu menghidrolisis polimer pektin sehingga rantai molekulnya menjadi lebih pendek. Semakin pendek rantai polimer pektin akan semakin memudahkan pengeringan karena kandungan air yang terperangkap di dalamnya semakin sedikit (Fishman et al. 2006; Liu et al. 2006). Selain itu adanya senyawa yang mudah menguap seperti isopropanol dapat menyebabkan kadar air lebih besar dari sebenarnya karena kehilangan bobot yang terjadi akan dianggap sebagai air yang hilang (Andarwulan 2011). Kandungan minyak kedelai yang bersifat non-polar dapat terdapat pada polong kedelai yang menghambat difusi larutan asam yang bersifat polar. Dengan adanya pengeringan bahan, sebagian minyak kedelai juga ikut menguap bersama uap air.
Kadar Abu
Kadar abu pektin yang diperoleh berkisar antara 5.97 – 8.02%. Kadar abu
pada perlakuan yang digunakan melebihi batas maksimum yang diizinkan. Hal ini disebabkan karena ekstraksi dengan asam yang mengakibatkan terhidrolisisnya pektin dari ikatan kalsium dan magnesiumnya. Pada hidrolisis dengan asam, ion-ion akan lepas dari substansi pektin. Semakin lama perlakuan dengan asam, ion-ion-ion-ion ini akan lebih banyak dilepaskan sehingga kadar abu semakin tinggi (Perina et al.
17.07 15.14 15.66 14.80 13 14 15 16 17 18 80 95 K ada r ai r (% ) Suhu (ºC) 30 menit 60 menit
14
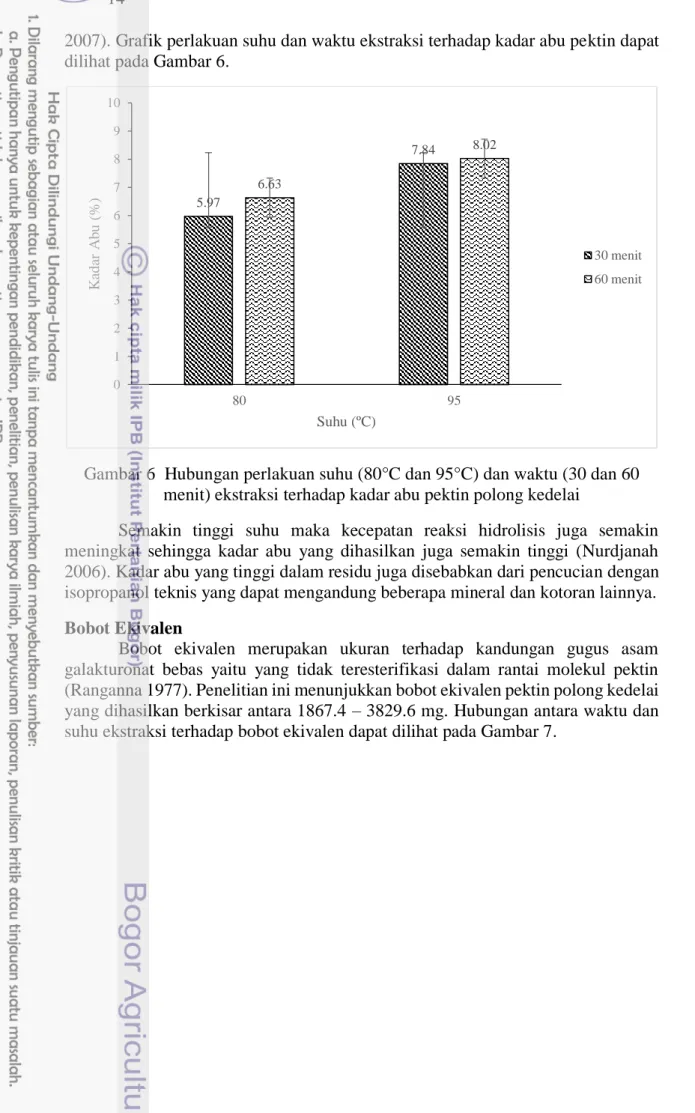
2007). Grafik perlakuan suhu dan waktu ekstraksi terhadap kadar abu pektin dapat dilihat pada Gambar 6.
Gambar 6 Hubungan perlakuan suhu (80°C dan 95°C) dan waktu (30 dan 60 menit) ekstraksi terhadap kadar abu pektin polong kedelai
Semakin tinggi suhu maka kecepatan reaksi hidrolisis juga semakin meningkat sehingga kadar abu yang dihasilkan juga semakin tinggi (Nurdjanah 2006). Kadar abu yang tinggi dalam residu juga disebabkan dari pencucian dengan isopropanol teknis yang dapat mengandung beberapa mineral dan kotoran lainnya.
Bobot Ekivalen
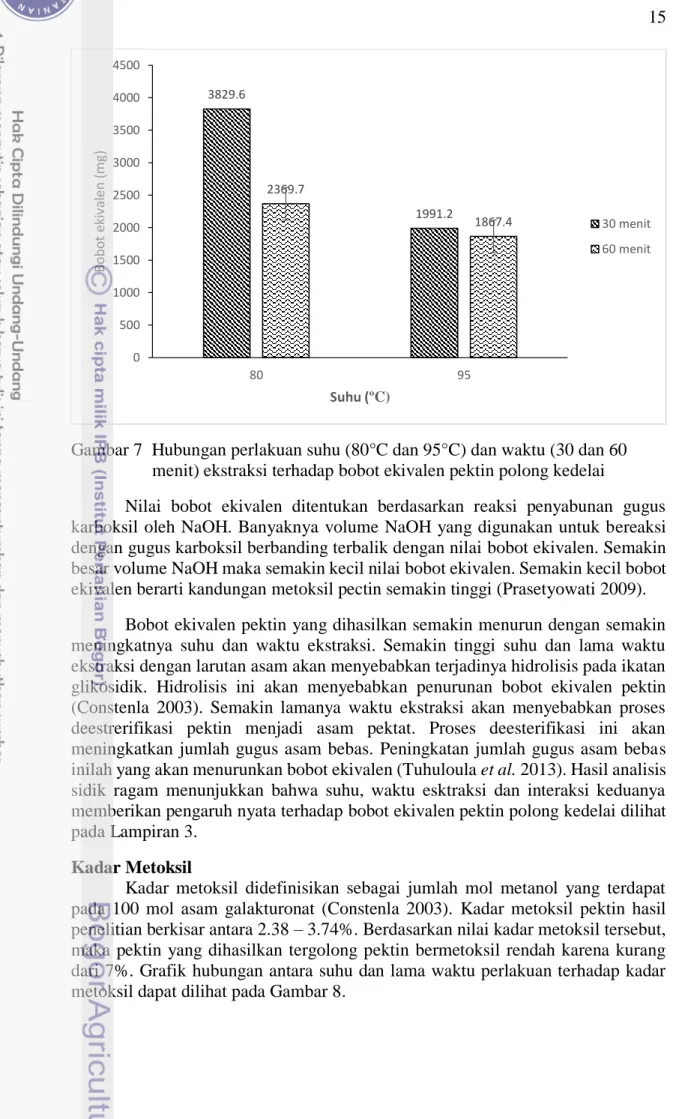
Bobot ekivalen merupakan ukuran terhadap kandungan gugus asam galakturonat bebas yaitu yang tidak teresterifikasi dalam rantai molekul pektin (Ranganna 1977). Penelitian ini menunjukkan bobot ekivalen pektin polong kedelai yang dihasilkan berkisar antara 1867.4 – 3829.6 mg. Hubungan antara waktu dan suhu ekstraksi terhadap bobot ekivalen dapat dilihat pada Gambar 7.
5.97 7.84 6.63 8.02 0 1 2 3 4 5 6 7 8 9 10 80 95 K ada r A b u (% ) Suhu (ºC) 30 menit 60 menit
15
Gambar 7 Hubungan perlakuan suhu (80°C dan 95°C) dan waktu (30 dan 60 menit) ekstraksi terhadap bobot ekivalen pektin polong kedelai
Nilai bobot ekivalen ditentukan berdasarkan reaksi penyabunan gugus karboksil oleh NaOH. Banyaknya volume NaOH yang digunakan untuk bereaksi dengan gugus karboksil berbanding terbalik dengan nilai bobot ekivalen. Semakin besar volume NaOH maka semakin kecil nilai bobot ekivalen. Semakin kecil bobot ekivalen berarti kandungan metoksil pectin semakin tinggi (Prasetyowati 2009).
Bobot ekivalen pektin yang dihasilkan semakin menurun dengan semakin meningkatnya suhu dan waktu ekstraksi. Semakin tinggi suhu dan lama waktu ekstraksi dengan larutan asam akan menyebabkan terjadinya hidrolisis pada ikatan glikosidik. Hidrolisis ini akan menyebabkan penurunan bobot ekivalen pektin (Constenla 2003). Semakin lamanya waktu ekstraksi akan menyebabkan proses deestrerifikasi pektin menjadi asam pektat. Proses deesterifikasi ini akan meningkatkan jumlah gugus asam bebas. Peningkatan jumlah gugus asam bebas inilah yang akan menurunkan bobot ekivalen (Tuhuloula et al. 2013). Hasil analisis sidik ragam menunjukkan bahwa suhu, waktu esktraksi dan interaksi keduanya memberikan pengaruh nyata terhadap bobot ekivalen pektin polong kedelai dilihat pada Lampiran 3.
Kadar Metoksil
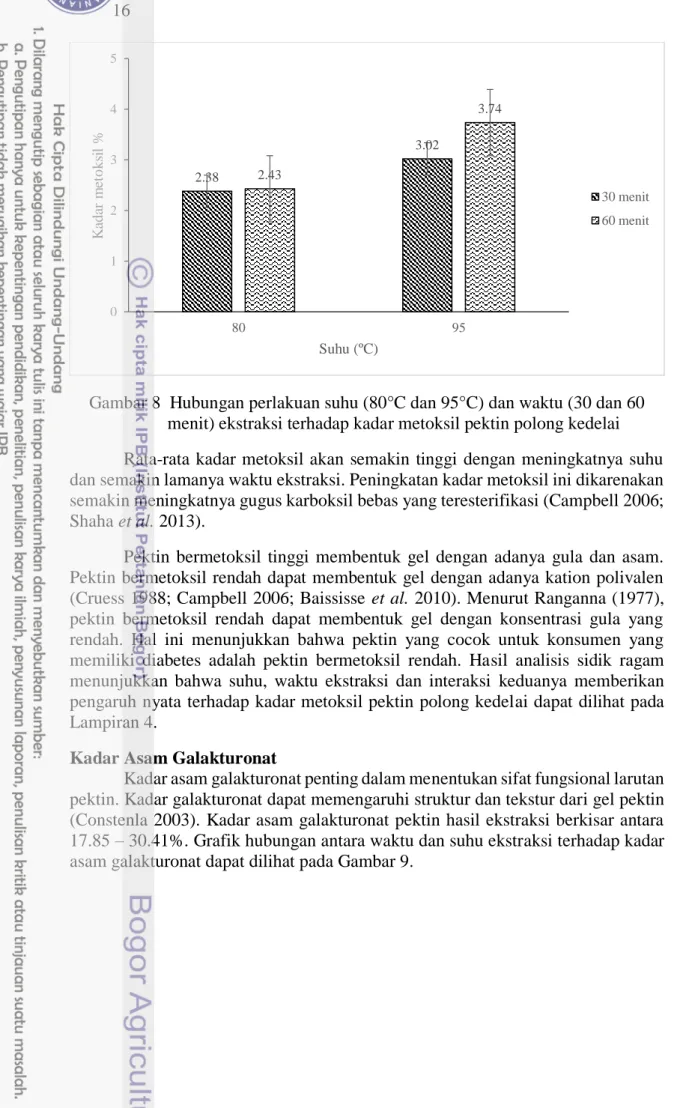
Kadar metoksil didefinisikan sebagai jumlah mol metanol yang terdapat pada 100 mol asam galakturonat (Constenla 2003). Kadar metoksil pektin hasil penelitian berkisar antara 2.38 – 3.74%. Berdasarkan nilai kadar metoksil tersebut, maka pektin yang dihasilkan tergolong pektin bermetoksil rendah karena kurang dari 7%. Grafik hubungan antara suhu dan lama waktu perlakuan terhadap kadar metoksil dapat dilihat pada Gambar 8.
3829.6 1991.2 2369.7 1867.4 0 500 1000 1500 2000 2500 3000 3500 4000 4500 80 95 B o b o t ek iv al en (mg ) Suhu (ºC) 30 menit 60 menit
16
Gambar 8 Hubungan perlakuan suhu (80°C dan 95°C) dan waktu (30 dan 60 menit) ekstraksi terhadap kadar metoksil pektin polong kedelai
Rata-rata kadar metoksil akan semakin tinggi dengan meningkatnya suhu dan semakin lamanya waktu ekstraksi. Peningkatan kadar metoksil ini dikarenakan semakin meningkatnya gugus karboksil bebas yang teresterifikasi (Campbell 2006; Shaha et al. 2013).
Pektin bermetoksil tinggi membentuk gel dengan adanya gula dan asam. Pektin bermetoksil rendah dapat membentuk gel dengan adanya kation polivalen (Cruess 1988; Campbell 2006; Baississe et al. 2010). Menurut Ranganna (1977), pektin bermetoksil rendah dapat membentuk gel dengan konsentrasi gula yang rendah. Hal ini menunjukkan bahwa pektin yang cocok untuk konsumen yang memiliki diabetes adalah pektin bermetoksil rendah. Hasil analisis sidik ragam menunjukkan bahwa suhu, waktu ekstraksi dan interaksi keduanya memberikan pengaruh nyata terhadap kadar metoksil pektin polong kedelai dapat dilihat pada Lampiran 4.
Kadar Asam Galakturonat
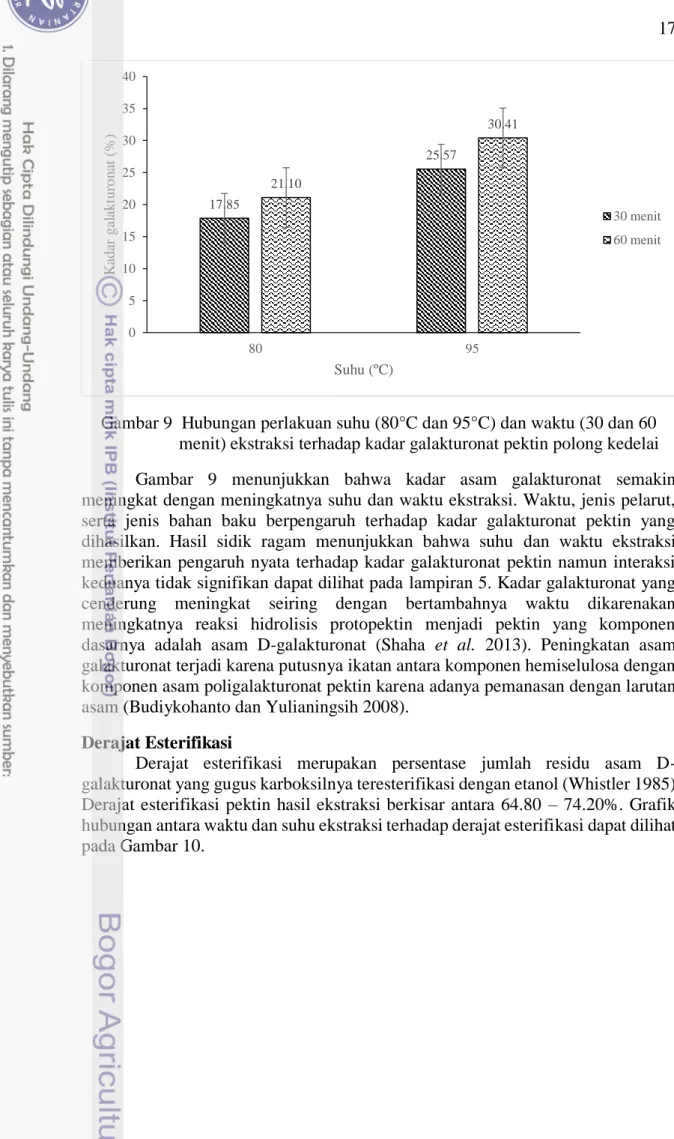
Kadar asam galakturonat penting dalam menentukan sifat fungsional larutan pektin. Kadar galakturonat dapat memengaruhi struktur dan tekstur dari gel pektin (Constenla 2003). Kadar asam galakturonat pektin hasil ekstraksi berkisar antara 17.85 – 30.41%. Grafik hubungan antara waktu dan suhu ekstraksi terhadap kadar asam galakturonat dapat dilihat pada Gambar 9.
2.38 3.02 2.43 3.74 0 1 2 3 4 5 80 95 K ada r m et o ks il % Suhu (ºC) 30 menit 60 menit
17
Gambar 9 Hubungan perlakuan suhu (80°C dan 95°C) dan waktu (30 dan 60 menit) ekstraksi terhadap kadar galakturonat pektin polong kedelai
Gambar 9 menunjukkan bahwa kadar asam galakturonat semakin meningkat dengan meningkatnya suhu dan waktu ekstraksi. Waktu, jenis pelarut, serta jenis bahan baku berpengaruh terhadap kadar galakturonat pektin yang dihasilkan. Hasil sidik ragam menunjukkan bahwa suhu dan waktu ekstraksi memberikan pengaruh nyata terhadap kadar galakturonat pektin namun interaksi keduanya tidak signifikan dapat dilihat pada lampiran 5. Kadar galakturonat yang cenderung meningkat seiring dengan bertambahnya waktu dikarenakan meningkatnya reaksi hidrolisis protopektin menjadi pektin yang komponen dasarnya adalah asam D-galakturonat (Shaha et al. 2013). Peningkatan asam galakturonat terjadi karena putusnya ikatan antara komponen hemiselulosa dengan komponen asam poligalakturonat pektin karena adanya pemanasan dengan larutan asam (Budiykohanto dan Yulianingsih 2008).
Derajat Esterifikasi
Derajat esterifikasi merupakan persentase jumlah residu asam D-galakturonat yang gugus karboksilnya teresterifikasi dengan etanol (Whistler 1985). Derajat esterifikasi pektin hasil ekstraksi berkisar antara 64.80 – 74.20%. Grafik hubungan antara waktu dan suhu ekstraksi terhadap derajat esterifikasi dapat dilihat pada Gambar 10. 17.85 25.57 21.10 30.41 0 5 10 15 20 25 30 35 40 80 95 K ada r ga la kt ur o n at ( % ) Suhu (ºC) 30 menit 60 menit
18
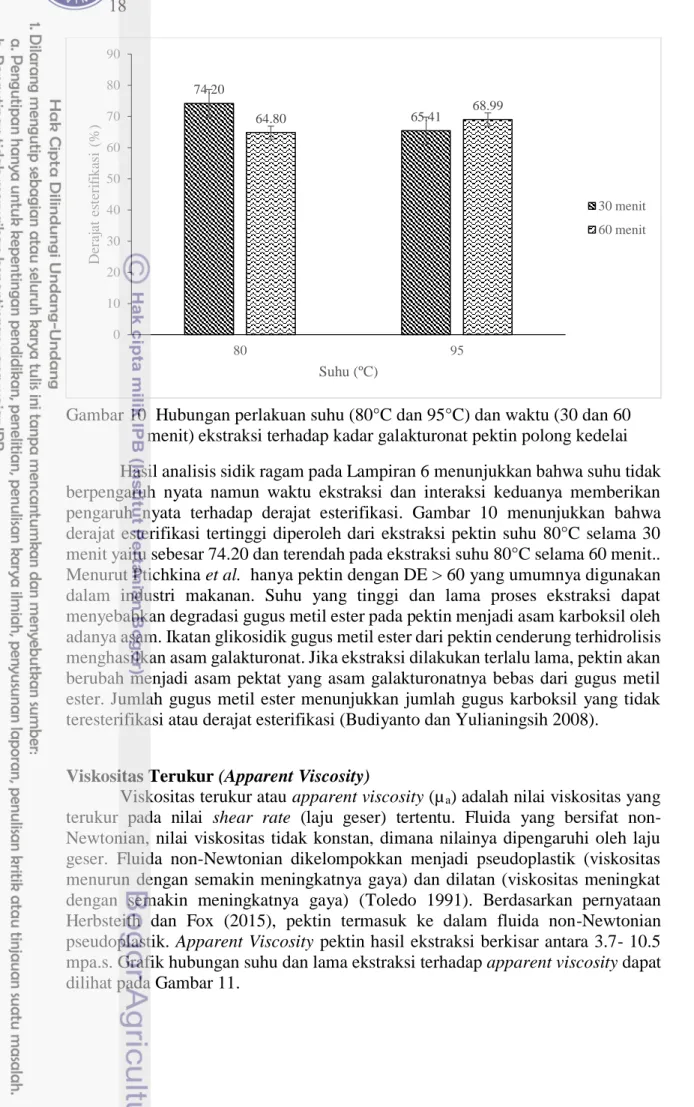
Gambar 10 Hubungan perlakuan suhu (80°C dan 95°C) dan waktu (30 dan 60 menit) ekstraksi terhadap kadar galakturonat pektin polong kedelai
Hasil analisis sidik ragam pada Lampiran 6 menunjukkan bahwa suhu tidak berpengaruh nyata namun waktu ekstraksi dan interaksi keduanya memberikan pengaruh nyata terhadap derajat esterifikasi. Gambar 10 menunjukkan bahwa derajat esterifikasi tertinggi diperoleh dari ekstraksi pektin suhu 80°C selama 30 menit yaitu sebesar 74.20 dan terendah pada ekstraksi suhu 80°C selama 60 menit.. Menurut Ptichkina et al. hanya pektin dengan DE > 60 yang umumnya digunakan dalam industri makanan. Suhu yang tinggi dan lama proses ekstraksi dapat menyebabkan degradasi gugus metil ester pada pektin menjadi asam karboksil oleh adanya asam. Ikatan glikosidik gugus metil ester dari pektin cenderung terhidrolisis menghasilkan asam galakturonat. Jika ekstraksi dilakukan terlalu lama, pektin akan berubah menjadi asam pektat yang asam galakturonatnya bebas dari gugus metil ester. Jumlah gugus metil ester menunjukkan jumlah gugus karboksil yang tidak teresterifikasi atau derajat esterifikasi (Budiyanto dan Yulianingsih 2008).
Viskositas Terukur (Apparent Viscosity)
Viskositas terukur atau apparent viscosity (µa) adalah nilai viskositas yang terukur pada nilai shear rate (laju geser) tertentu. Fluida yang bersifat non-Newtonian, nilai viskositas tidak konstan, dimana nilainya dipengaruhi oleh laju geser. Fluida non-Newtonian dikelompokkan menjadi pseudoplastik (viskositas menurun dengan semakin meningkatnya gaya) dan dilatan (viskositas meningkat dengan semakin meningkatnya gaya) (Toledo 1991). Berdasarkan pernyataan Herbsteith dan Fox (2015), pektin termasuk ke dalam fluida non-Newtonian pseudoplastik. Apparent Viscosity pektin hasil ekstraksi berkisar antara 3.7- 10.5 mpa.s. Grafik hubungan suhu dan lama ekstraksi terhadap apparent viscosity dapat dilihat pada Gambar 11.
74.20 65.41 64.80 68.99 0 10 20 30 40 50 60 70 80 90 80 95 D er aj at e st er if ika si ( % ) Suhu (ºC) 30 menit 60 menit
19
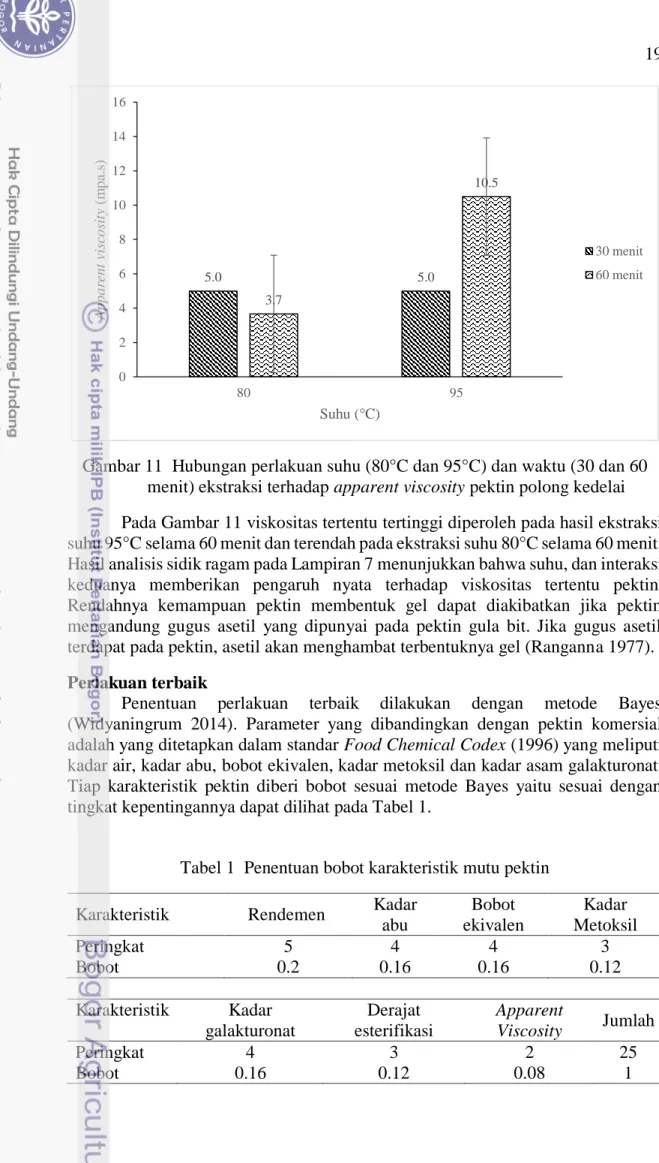
Gambar 11 Hubungan perlakuan suhu (80°C dan 95°C) dan waktu (30 dan 60 menit) ekstraksi terhadap apparent viscosity pektin polong kedelai
Pada Gambar 11 viskositas tertentu tertinggi diperoleh pada hasil ekstraksi suhu 95°C selama 60 menit dan terendah pada ekstraksi suhu 80°C selama 60 menit. Hasil analisis sidik ragam pada Lampiran 7 menunjukkan bahwa suhu, dan interaksi keduanya memberikan pengaruh nyata terhadap viskositas tertentu pektin. Rendahnya kemampuan pektin membentuk gel dapat diakibatkan jika pektin mengandung gugus asetil yang dipunyai pada pektin gula bit. Jika gugus asetil terdapat pada pektin, asetil akan menghambat terbentuknya gel (Ranganna 1977).
Perlakuan terbaik
Penentuan perlakuan terbaik dilakukan dengan metode Bayes (Widyaningrum 2014). Parameter yang dibandingkan dengan pektin komersial adalah yang ditetapkan dalam standar Food Chemical Codex (1996) yang meliputi kadar air, kadar abu, bobot ekivalen, kadar metoksil dan kadar asam galakturonat. Tiap karakteristik pektin diberi bobot sesuai metode Bayes yaitu sesuai dengan tingkat kepentingannya dapat dilihat pada Tabel 1.
Tabel 1 Penentuan bobot karakteristik mutu pektin
Karakteristik Rendemen Kadar
abu Bobot ekivalen Kadar Metoksil Peringkat 5 4 4 3 Bobot 0.2 0.16 0.16 0.12 Karakteristik Kadar galakturonat Derajat esterifikasi Apparent Viscosity Jumlah Peringkat 4 3 2 25 Bobot 0.16 0.12 0.08 1 5.0 5.0 3.7 10.5 0 2 4 6 8 10 12 14 16 80 95 A ppar ent vis cos it y (m pa .s ) Suhu (°C) 30 menit 60 menit
20
Nilai tiap parameter mutu pektin diurutkan dari yang terkecil sampai yang terbesar. Perlakuan yang diberi nilai 9 yaitu mutu pektin yang tertinggi diantaranya; rendemen tertinggi, kadar abu terendah, bobot ekivalen tertinggi, kadar metoksil tertinggi, kadar galakturonat tertinggi, derajat esterifikasi tertinggi dan viskositas tertinggi. Sebaliknya, mutu pektin yang terendah diberi nilai 1.
Nilai tiap karakteristik yang diberikan pada langkah tersebut dikalikan dengan bobot karakteristik tersebut. Hasil perhitungan untuk tiap karakteristik mutu pektin dijumlahkan sehingga diperoleh nilai total. Pektin yang memiliki nilai total tertinggi adalah pektin terbaik. Pernentuan metode Bayes dapat dilihat pada Tabel 2.
Tabel 2 Penentuan karakteristik pektin polong kedelai dengan metode Bayes
Perlakua n Rendemen Kadar abu Bobot ekivalen Kadar Metoksil Kadar galakturonat 80°C 30 menit 1 1 4 1 1 80°C 60 menit 2 2 3 2 2 95°C 30 menit 3 3 2 3 3 95°C 60 menit 4 4 1 4 4
Karakteristik Derajat esterifikasi Apparent
Viscosity Nilai Peringkat
80°C 30 menit 4 2 1.92 4
80°C 60 menit 1 1 1.96 3
95°C 30 menit 2 2 2.64 2
95°C 60 menit 3 3 3.32 1
Dari hasil analisa diperoleh hasil terbaik pada perlakuan 95°C selama 60 menit dibandingkan dengan kondisi proses lainnya.
Tabel 3 Perbandingan pektin polong kedelai hasil penelitian dengan pektin komersial
Parameter Nilai standar
(Food Chemical Codex) Pektin hasil penelitian (95°C 60 menit) Pektin komersial (CV. Nura Jaya) Kadar air (%) 12 14.80 7.57 Kadar abu (%) 1 8.02 18.66 Bobot ekivalen (mg) - 1867.4 49825.9 Kadar metoksil (%) 7 3.74 3.70 Kadar galakturonat (%) 65 (bk) 30.41 21.37 Derajat esterifikasi (%) - 68.99 98.30 Apparent Viscosity (mpa.s) - 10.5 (spindle No. 1 speed 60) 4133.3 (spindle No. 2 speed 6)
21
SIMPULAN
Limbah konsumsi kedelai yang berupa polong dapat dimanfaatkan sebagai bahan baku pembuatan pektin. Rendemen pektin yang dihasilkan dalam penelitian berkisar antara 3.92-5.16 %. Rendemen tertinggi diperoleh pada ekstraksi suhu 90°C selama 60 menit. Kadar air yang dihasilkan lebih dari 12 % yaitu sekitar 14.80-17.07 %. Kadar air terendah diperoleh pada ekstraksi suhu 95°C selama 60 menit. Kadar abu yang dihasilkan lebih dari 1 % yaitu berkisar antar 5.97-8.02 %. Kadar abu terendah diperoleh pada ekstraksi suhu 80°C selama 30 menit. Bobot ekivalen pektin yang dihasilkan berkisar antara 1867.3773-3829.5701. Bobot ekivalen tertinggi diperoleh pada suhu 80°C selama 30 menit.
Pektin yang dihasilkan dalam penelitian termasuk dalam pektin bermetoksil rendah dengan kadar metoksil berkisar antara 2,.38-3.74%. Kadar galakturonat yang dihasilkan berkisar antara 17.85-30.41%. Derajat esterifikasi yang dihasilkan berkisar antara 64.80-74.20. Viskositas tertentu larutan pektin yang dihasilkan berkisar antara 3.7-10.5 mpa.s. Viskositas tertentu terbesar diperoleh pada larutan pektin yang diekstrak pada suhu 95°C selama 60 menit.
Berdasarkan hasil penelitian dengan metode Bayes kondisi ekstraksi pektin yang terbaik adalah perlakuan pada suhu 95°C selama 60 menit. Namun ekstraksi pektin terbaik masih belum memiliki mutu yang lebih baik dari pektin komersial dari kriteria kadar air, bobot ekivalen, derajat esterifikasi, dan viskositas tertentu. Pektin polong kedelai pada penelitian tidak sepenuhnya bisa dibandingkan dengan pektin komersial. Pektin pada polong kedelai berfungsi sebagai gelling agent, sementara pektin komersial berfungsi sebagai thickener.
SARAN
Pengembangan lebih lanjut proses ekstraksi pektin polong kedelai dapat
dilakukan terhadap kondisi proses lainnya, seperti pH, blanching saat proses pendahuluan, lama proses pencampuran sehingga dapat diperoleh kombinasi proses yang menghasilkan karakteristik terbaik untuk menjadi alternatif pektin komersial yang lebih baik. Selain itu juga dapat dilakukan pengeringan polong kedelai tanpa penghancuran terlebih dahulu agar air tidak menjadi faktor penambah adanya mineral-mineral yang akan mengganggu proses analisis. Pektin komersial yang digunakan juga harus memiliki fungsi yang sama dengan pektin yang dianalisis agar dapat dibandingkan.
22
DAFTAR PUSTAKA
Andarwulan N, Kusnandar F, Herawati D. 2011. Analisis Pangan. Jakarta (ID): Dian Rakyat.
Baississe S, Hanachi G, Djamel F, Adel L. 2010. Comparasion of structure and emulsifiying activity of pectin extracted from apple pomace and apricot pulp. World Journal of Dairy & Food Sciences. 5(1): 79-84.
Baker RA. 1994. Pectin. Carbohydrate Polymer. 12: 133-138.
Budiyanto A, Yulianingsih. 2008. Pengaruh suhu dan waktu ekstraksi terhadap karakter pektin dari ampas jeruk siam (Citrus nobilis L). Jurnal Pascapanen
5(2): 37-44.
[BPS] Badan Pusat Statistik. 2010. Statistik Perdagangan Ekspor Impor Indonesia. Didalam Elvianto DD. Ekstraksi Pektin dari Labu Siam. Malang (ID): Institut Teknologi Nasional Malang.
Campbell M. 2006. Extraction of Pectin from Watermelon Rind. Oklahoma (US): Oklahoma State University Stillwater.
Constenla, Lozano. 2003. Kinetic model of pektin demethylation. Latin American
Applied Research. 33, Hal 91-96.
Cruess. 1988; Campbell 2006; Baississe et al., 2010. Cruess, W.V. 1988.
Commercially Fruits and Vegetable Products. New York (US): McGraw
HillBook Co.
Duke JA, Atchley AA. 1986. Handbook of proximate analysis tables of higher
plants. Boca Raton (FL): CRC Press.
Fardiaz D. 1984. Pemanfaatan Limbah Jeruk Sebagai Bahan Pembuat Pektin. Bogor (ID): Institut Pertanian. Bogor.
Fishman et al. 2006. Characterization of pectin, flash-extracted from orange albedo by microwave heating under pressure. Carbohydrate Research. 323, 126 – 138.
Food Chemical Codex. 1996. Pectins. [Internet]. [diunduh pada 2017 Feb 8]. Tersedia pada: http://arjournals.annualreviews.org/doi/abs/10.1146/ annurev.bi.20.070151.000435.
Gliksman. 1969 di dalam Hariyati 2006. Gum Technology in the Food Industry. New York (US): Academic Press.
23
Hanum F, IMD Kaban, MA Tarigan. 2012. Ekstraksi pektin dari kulit buah pisang raja (Musa sapientum). Jurnal Teknik Kimia USU. Vol. 1 No. 2.
Hariyati MN. 2006. Ekstraksi dan karakterisasi pektin dari limbah proses pengolahan jeruk Pontianak [skripsi]. Bogor (ID): Institut Pertanian Bogor.
Haryadi W. 1990. Ilmu Kimia Analitik Dasar. Jakarta (ID): Gramedia.
Herbstreith, Fox. 2005 di dalam Hariyati, 2006. http://www.herbstreithfox.de /pektin/forschung und entwicklung /forschung_entwicklung04a.htm
Herbstreith, Fox. 2015. Technical application laboratory. [Internet]. [diunduh
pada 30 Maret 2017]. Tersedia pada:
http://www.herbstreith-fox.de/fileadmin/tmpl/pdf/awtinfo/AWT_praxisrelevante_Rheometrie_e.p df
[JTA] Japan Tariff Association. 1989. Japan exports and imports. Tokyo [JP].
Kliemann E, de Limas KN, Amante ER, Prudencio ES, Teofi RF, Ferriera MMC, Amboni RDMC. 2009. Optimisation of pectin acid extraction from passion fruit peel using response surface methodology. International Journal of
Food Science and Technology. 44: 476-483.
Kohg Z, Lin ZD, Lin CST. 2000. Study on the extraction of pectin from apple pomace with microwave. Journal Zhengzhon Grain Colloids. 21 (2) 11-15.
Konovsky J, Lumpkin TA, Shanmugasundaram S, Tsou TSC. 1992. Edamame: the
vegetable soybean. Taiwan (CN): Asian Vegetable Research and
Development Center.
Kratchanova M, Panchev I, Pavlova E, and Shtereva L. 1994. Extraction of pectin from fruits materials pretreated in an electromagnetic field of super high frequency. Carbohydrate Polymers. 25. 141 - 144.
Liu Y, Shi J, Langrish TAG. 2006. Water-based extraction of pectin from flavedo and albedo of orange peels. Chemical Engineering Journal. 120: 126-138.
May CD. 1990. Industrial pectins: sources, production, and application. Carbohydrate
Polymer. 12: 79-84.
[MAFF] Ministry of Agriculture, Forestry, and Fisheries (MAFF). 1990. Statistical
Handbook. Tokyo (JP): Norinsuisansho.
Meilina H, Sailah I. 2003. Produksi pektin dari kulit jeruk lemon (Citrus medica). Prosiding Simposium Nasional Polimer V.
Monsoor M, Proctor A. 2001. Preparation and functional properties of soy hull pectin. Journal of the American Oil Chemist Society. 78: 709-713.
24
Nurdjanah, Usmiati 2006. Ekstraksi dan karakterisasi pektin dari kulit labu kuning.
Jurnal Penelitian Pascapanen Pertanian. 3(1): 13-23.
Perina, Satiruiani, ES Felycia, H Herman. 2007. Ekstraksi pektin dari berbagai macam kulit jeruk. Widya Teknik. Vol. 6 No. 1 : 1-10.
Poerwanto. 2014. Preferensi konsumen terhadap konsumsi edamame di Kabupaten Jember. Jurnal Ilmiah INOVASI. Vol. 14 No.1 Hal. 53-64.
Prasetyowati, Sari KP, Pesantri H. 2009. Ekstraksi pektin dari kulit mangga. Jurnal
Teknik Kimia. No.4 Vol. 16.
Ranganna S. 1977. Manual of Analysis of Fruit and Vegetable Products. New Delhi (IND): McGraw Hill.
Richard JD, JG Louis, Henry. 1984. Soybeans Crop Production. Englewood Cliffs (NJ): Practice Hall. Inc.
Rukmana R, Yuniarsih Y. 1996. Kedelai: Budidaya dan Pascapanen. Yogyakarta (ID): Kanisius.
Shaha, Ranajit K, Nayagi AP, Punichelvana, Asrul A. 2013. Optimized extraction condition and characterization of pectin from kaffir lime. Research Journal
of Agriculture and Forestry Sciences. vol.1(2): 1-11.
SNI 01-2891-1992. Analisis Kadar Air.
SNI 01-2891-1992. Analisis Kadar Abu.
Stevenson DG, Jane J, Inglett GE. 2007. Structures and physicochemical properties of starch from immature seeds of soybean varieties (Glycine max (L.) Merr) exhibiting normal, low-linolenic, or low-saturated fatty acid oil profiles at maturity. Carbohydrate Polymers. 70: 149-159.
Toledo RT. 1991. Fundamentals of Food Process Engineering. New York (US): Van Nonstrand Reinhold.
Tuhuloula Abubakar, Lestari B. Etha NF. 2013. Karakterisasi pektin dengan memanfaatkan limbah kulit pisang menggunakan metode ekstraksi. Jurnal
Konversi. Vol. 2 No. 1. Universitas Lambung Mangkurat.
Vaclavik VA, EW Christian. 2008. Essentials of Food Science. New York (US) Springer Science Business Media.
Wang HL, Mustakas GC, Wolf WJ, Wang LC, Hesseltine CW, Bagley EB. 1979. Soybeans as human food-unprocessed and simply processed. Department
Agriculture. Utilization Rpt. 5.
Wheeler RM, Mackowiak CL, Sager J C. 1990. Proximate Composition of Seed
25
(CO2) Concentrations. The Bionetics Corp. Florida (US): Kennedy Space
Center.
Whistler RL, Daniel JR. 1985. Carbohydrates. New York (US): Marcel Dekker.
Widiastuti DR. 2015. Ekstraksi pektin kulit jeruk bali dengan microwave assisted
extraction dan aplikasinya sebagai edible film [Skripsi]. Semarang(ID):
Universitas Negeri Semarang.
Widyaningrum, Luthfi M, Nugroho WA. 2014. Ekstraksi dan karakterisasi pektin dari buah pandan laut. Jurnal Keteknikan Pertanian Tropis dan Biosistem. Vol. 2 No. 2. 89-96.
LAMPIRAN
Lampiran 1 Dokumentasi proses produksi polong kedelai
Penimbangan polong kedelai Polong kedelai hasil pengeringan
Pemisahan larutan pektin
Larutan pektin polong kedelai dibandingkan dengan komersial
26
Proses isolasi pektin dengan
centrifuge Z 383 K
Hasil pengeringan pektin pada oven 50°C selama 24 jam
Lampiran 2 Dokumentasi pektin kering polong kedelai
Perlakuan 95°C 30 menit (kiri); Perlakuan 95°C 60 menit (kanan)
Perlakuan 80°C 30 menit (kiri) Perlakuan 80°C 60 menit (kanan)
Lampiran 3 Hasil uji statistik analisis bobot ekivalen
Tests of Between-Subjects Effects
Dependent Variable: BE Source Type III Sum of Squares df Mean Square F Sig . Corrected Model 7328790. 571a 3 2442930. 190 5920.1 66 .00 0 Intercept 7587146 4.399 1 7587146 4.399 18386 5.936 .00 0 Suhu 4109114. 182 1 4109114. 182 9957.9 75 .00 0
27 Waktu 1881074. 596 1 1881074. 596 4558.5 72 .00 0 Suhu * Waktu 1338601. 794 1 1338601. 794 3243.9 50 .00 0 Error 3301.165 8 412.646 Total 8320355 6.135 12 Corrected Total 7332091. 736 11
a. R Squared = 1.000 (Adjusted R Squared = .999)
Lampiran 4 Hasil uji statistik analisis kadar metoksil
Tests of Between-Subjects Effects
Dependent Variable: Metoksil
Source Type III Sum of Squares df Mean Square F Sig . Corrected Model 3.549 a 3 1.183 66.9 01 .00 0 Intercept 97.234 1 97.234 549 8.050 .00 0 Suhu 2.704 1 2.704 152. 886 .00 0 Waktu .505 1 .505 28.5 74 .00 1 Suhu * Waktu .340 1 .340 19.2 44 .00 2 Error .141 8 .018 Total 100.925 12 Corrected Total 3.691 11
a. R Squared = .962 (Adjusted R Squared = .947)
Lampiran 5 Hasil uji statistik analisis kadar galakturonat
Tests of Between-Subjects Effects
Dependent Variable: Galakturonat
Source Type III Sum of Squares df Mean Square F Sig .
28 Corrected Model 268.203 a 3 89.401 143.8 60 .00 0 Intercept 6759.268 1 6759.26 8 1087 6.681 .00 0 Suhu 217.350 1 217.350 349.7 48 .00 0 Waktu 48.975 1 48.975 78.80 8 .00 0 Suhu * Waktu 1.878 1 1.878 3.022 .12 0 Error 4.972 8 .621 Total 7032.442 12 Corrected Total 273.174 11
a. R Squared = .982 (Adjusted R Squared = .975)
Lampiran 6 Hasil uji statistik analisis derajat esterifikasi
Tests of Between-Subjects Effects
Dependent Variable: DE Source Type III Sum of Squares df Mean Square F Sig . Corrected Model 167.631 a 3 55.877 53.89 7 .00 0 Intercept 56058.94 8 1 56058.9 48 5407 2.200 .00 0 Suhu 15.801 1 15.801 15.24 1 .00 5 Waktu 25.391 1 25.391 24.49 1 .00 1 Suhu * Waktu 126.439 1 126.439 121.9 58 .00 0 Error 8.294 8 1.037 Total 56234.87 3 12 Corrected Total 175.925 11
29
Lampiran 7 Hasil uji statistik analisis viskositas tertentu
Tests of Between-Subjects Effects
Dependent Variable: Viskositas
Source Type III Sum of Squares df Mean Square F Sig . Corrected Model 83.063 a 3 27.688 332. 250 .00 0 Intercept 438.021 1 438.021 525 6.250 .00 0 Suhu 35.021 1 35.021 420. 250 .00 0 Waktu 13.021 1 13.021 156. 250 .00 0 Suhu * Waktu 35.021 1 35.021 420. 250 .00 0 Error .667 8 .083 Total 521.750 12 Corrected Total 83.729 11
30
RIWAYAT HIDUP
Penulis dilahirkan di Jakarta pada 25 Februari 1994, merupakan anak ke-2 dari dua bersaudara Bapak Farkhani Koesnindar dan Ibu Farida Handayani. Penulis menyelesaikan pendidikan dasar pada tahun 2006 di SD Islam Darussalam Bekasi, kemudian melanjutkan ke jenjang menengah pertama di SMP Islam Darussalam Bekasi. Penulis menyelesaikan pendidikan menengah atas di SMAN 31 Jakarta dan melanjutkan studi di Program Studi Teknologi Pangan, Departemen Ilmu dan Teknologi Pangan, Fakultas Teknologi Pertanian, Institut Pertanian Bogor dan diterima melalui jalur Seleksi Nasional Perguruan Tinggi Negeri jalur undangan (SNMPTN Undangan).
Selama menempuh pendidikan di IPB, penulis aktif di beberapa kepanitiaan, organisasi mahasiswa serta komunitas, di antaranya adalah; International
Association of Students in Agricultural and related Sciences (IAAS) sebagai
anggota departemen external (2012-2013), delegasi IPB di National Congress IAAS XII 2014, ketua departemen science and technology (2015), badan pengawas (2015-2016); relawan Earth Hour Bogor (2012-2014); anggota kepanitiaan Olimpiade Mahasiswa IPB (OMI) 2014; anggota DDD Lomba Cepat Tepat Ilmu Pangan 2013; ketua divisi DDD Foodival 2014; Liaison Officer IUFRO forum kehutanan; serta Campus Ambassador di OPPO Campus Club (2015-2017). Penulis menyelesaikan studi Strata-1 di Institut Pertanian Bogor dengan judul karya ilmiah “Pengaruh Suhu dan Waktu Ekstraksi terhadap Karakteristik Pektin yang Diisolasi dari Polong Kedelai” di bawah bimbingan Dr. Ir. Budiatman Satiawihardja MSc dan Dr. Nugraha Edhi Suyatma STP DEA.