LAPORAN PRAKTEK KERJA PROFESI APOTEKER FARMASI INDUSTRI
DI PT. MARTINA BERTO, Tbk. DAN PT. KALBE FARMA, Tbk. (25 APRIL - 30 APRIL 2016)
AIR HANDLING UNIT (AHU) DI PT. KALBE FARMA, Tbk.
OLEH :
VIVI FITRIYANTI S N211 15 776
PROGRAM STUDI PROFESI APOTEKER FAKULTAS FARMASI
UNIVERSITAS HASANUDDIN MAKASSAR
BAB I PENDAHULUAN I.1 Latar Belakang
Industri farmasi sebagai unit usaha yang menunjang kesehatan masyarakat serta bertindak sebagai penghasil obat yang dituntuk untuk dapat menghasilkan obat yang harus memenuhi persyaratan khasialt (efficacy), keamanan (safety), dan mutu (quality) yang berkewajiban dan bertanggung jawab sosial untuk memproduksi obat, kosmetik maupun makanan minuman yang bermutu tinggi, berkhasiat dan terjamin keamanannya.
Berdasarkan hal tersebut, industri farmasi di Indonesia perlu memberikan jaminan mutu terhadap produk yang dihasilkan. Jaminan mutu suatu produk obat jadi, tidak hanya sekedar lulus dari serangkaian pengujian, namun hal terpenting yaitu mutu harus di terapkan dan dijaga pada disetiap proses produksi dari awal hingga akhir. Langkah utama untuk menjamin mutu dari suatu produk obat yang dihasilkan adalah dengan menerapkan Cara Pembuatan Obat yag Baik (CPOB). Penerapan CPOB dalam industri farmasi bertujuan untuk mengatur dan memastikan mutu obat yang diproduksi secara konsisten sehingga produk yang dihasilkan memenuhi persyaratan mutu yang ditetapkan (Kementrian Kesehatan RI, 2010).
Oleh karena itu, pemerintah membuat kebijakan melalui Keputusan Menteri Kesehatan No. 43/MENKES/II/1988 tentang Pedoman Cara Pembuatan Obat yang Baik (CPOB), sehingga setiap industri farmasi wajib menerapkan CPOB dalam upaya pengendalian, pengadaan, distribusi dan pemantapan obat yang menyeluruh dan terpadu. Guna mengontrol agar produk yang beredar di masyarakat merupakan obat yang terjamin mutunya dan aman digunakan oleh mayarakat.
Dalam rangka membina generasi baru khususnya tenaga Apoteker berasaskan penerapan CPOB dan CPKB di bidang industri, maka PT.
Kalbe Farma Tbk. dan PT Martina Berto Tbk. membuka kesempatan bagi calon Apoteker untuk melaksanakan PKPA agar dapat menggali ilmu farmasi industri melalui kegiatan tersebut.
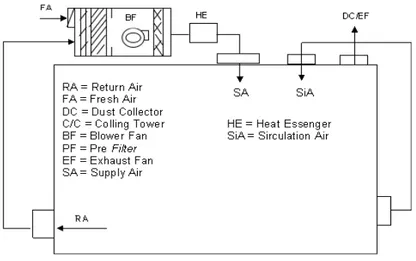
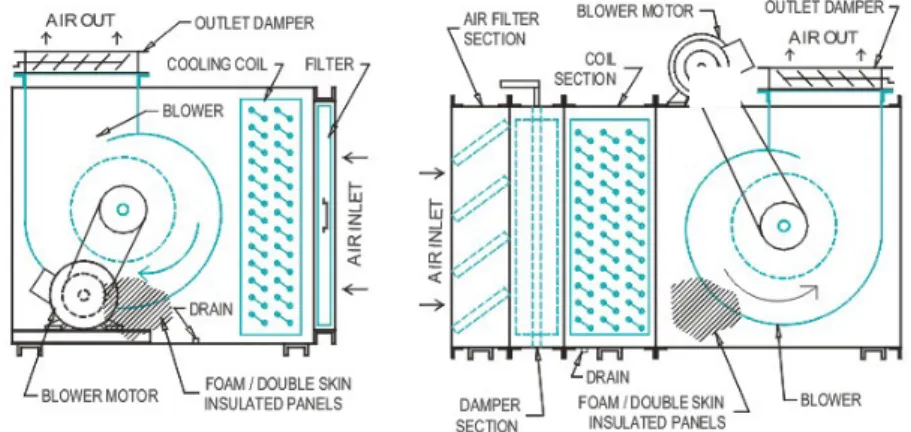
Salah satu aspek dalam penerapan CPOB yang perlu diperhatikan yaitu Sistem/Unit Pengaturan Udara (AHU) untuk menjamin dihasilkannya produk-poduk yang bermutu tinggi. AHU merupakan seperangkat alat yang dapat mengontrol suhu, kelembapan, aliran udara, jumlah pergantian udara, dan sebagainya, di ruang produksi sesuai dengan persyaratan ruangan yang telah ditentukan. Pengaturan AHU sangat penting untuk menunjang keberhasilan proses produksi hingga dihasilkan produk-produk yang bermutu tinggi.
I.2 Tujuan
Adapun tujuan dari kegiatan PKPA farmasi industri yang dilaksanakan di PT. Kalbe Farma, Tbk dan PT Martina Berto Tbk adalah :
a. Memperoleh pengetahuan dan wawasan mengenai penerapan segala aspek CPOB di PT. Kalbe Farma, Tbk dan penerapan CPKB di PT Martina Berto, Tbk.
b. Mengetahui penerapan CPOB terkait Sistem Pengaturan Udara (Air Handling Unit) di PT. Kalbe Farma Tbk.
BAB II TINJAUAN UMUM II.1 PT. Martina Berto, Tbk
II.1.1 Visi dan Misi
Visi dari PT. Martina Berto, Tbk adalah menjadi perusahaan perawatan kecantikan dan spa yang terkemuka di dunia dengan produk yang bernuansa ketimuran dan alami, melalui pemanfaatan teknologi modern, penelitian dan pengembangan sebagai sarana peningkatan nilai tambah bagi konsumen dan pemangku kepentingan lainnya (PT. Martina Berto, 2015)
Untuk mewujudkan visi yang telah ditetapkan, maka misi dari PT. Martina Berto, Tbk adalah :
1. Mengembangkan, memproduksi dan memasarkan produk perawatan kecantikan dan spa yang bernuansa ketimuran dan alami dengan standar mutu internasional guna memenuhi kebutuhan konsumen diberbagai segmen pasar dari premium, menengah atas, menengah dan menengah-bawah dalam suatu portofolio yang sehat dan setiap merek mampu mencapai posisi 3 besar di Indonesia di setiap segmen pasar yang dimasukinya.
2. Menyediakan layanan yang prima kepada semua pelanggan dalam porsi yang seimbang, termasuk konsumen dan para penyalur produk. 3. Mempertahankan kondisi keuangan yang sehat dan pertumbuhan
bisnis.
4. Merekrut, melatih dan mempertahankan tenaga kerja yang kompoten dan produktif sebagai bagian dari aset perseroan
5. Memanfaatkan metode operasi, sistem dan teknologi yang efisien dan efektif di seluruh unit dan fungsi usaha
6. Menerapkan “Good Corporate Governance” secara konsisten demi kepentingan para pemangku kepentingan (stakeholders)
7. Memberikan tingkat keuntungan yang wajar kepada para pemegang saham.
8. Mengembangkan pasar internasional kosmetika, produk spa dan herbal dengan fokus jangka menengah di kawasan Asia Pacific dan fokus jangka panjang di pasar global dengan produk dan merek pilihan
II.2.2. Lokasi
Saat ini PT. Martina Berto Tbk, memiliki dua pabrik dengan lokasi yang berbeda yaitu : (PT. Martina Berto, 2015)
1. Martina Berto Plant I, terletak di Kawasan Industri Pulogadung , didirikan pada tahun 1986 dengan luas area 10.245 m2.
2. Martina Berto Plant II, terletak di Gunung Putri didirikan pada tahun 1994 dengan luas area 10.629 m2.
Berdasarkan pada rencana pengembangan yang telah ditetapkan oleh perusahaan, masing-masing pabrik mempunyai fokus produksi tertentu. Martina Berto Plant I fokus pada produksi produk kosmetik, perawatan tubuh dan kulit. Sedangkan Martina Berto Plant II fokus pada produksi jamu dan makanan kesehatan. Selain dua pabrik PT. Matina Berto Tbk, juga mempunyai kebun budidaya tanaman dan penelitian yang terletak di Sawangan dan Cikarang. Kebun koleksi tanaman obat dan kosmetik seluas 0,7 hektar terletak di Sawangan dan kebun pengembangan dan produksi tanaman obat dan kosmetik seluas 10 hektar terletak di Cikarang.
II.2.3. Produk
Perseroan dan anak perusahaan memiliki fasilitas produksi yang terbagi ke dalam empat kategori, yaitu :
1. Kosmetik cair, termasuk didalamnya cairan pembersih muka, pelembab, toner, alas bedak, body splash cologne, hair spray, dan produk cair lainnya.
2. Kosmetik kering, termasuk didalamnya eye shadow, blush on, loose powder dan compact powder.
3. Kosmetik semi padat, termasuk didalamnya lipstik, creamy foundation, dan lain-lain
4. Obat tradisional termasuk didalamnya masker, mangir, lulur, dan teh herbal
Selain pembagian kategori produk berdasarkan proses produksi, Perseroan membagi produ-produk yang dimilikinya berdasarkan kategori produk, yaitu : colour cosmetic, skin care, body care, hair care, jamu (obat tradisional) dan lain-lain.
Produk kosmetik PT. Martina Berto Tbk antara lain : 1. Belia
a. Preparat wangi-wangian - mist cologne
b. Preparat make up
- lipstik, compact powder 2. Caring Colour
a. Preparat Make Up
- lip colour, liquid foundation, loose powder, dual action cake, cheek cake, lipstik, BB cream
b. Preparat mata
- eye shadow, eye candy 3. Biokos
Preparat perawatan : - skin care for all age 4. Cempaka Cosmetic
a. Skin care
b. Make up base
- Alas bedak, cream pemutih, bedak tabur, two way cake UV, whitening, foundation, bedak padat, compact powder, face powder
c. Decorative :
- mascara, beauty kit 5. Dewi Sri Spa
Preparat untuk kebersihan badan : levender oil, green tea, lemon oil, VCO, javanese rose, dan lain-lain
6. Mirabella
a. Preparat make up
- Lipstik, lip gloss, lip perfection b. Eye make up
- Eye liner, eye brow pencil, eyeliner liquid pen, eyeshadow
c. Make up base : cleansing milk, face tonic, foundation stick, blush on 7. PAC
a. Make up base
- Make up remover, brush cleaner, lipstick, blush on, foundation, lip gloss, lipstick pencil, liner, lip colour
b. Preparat mata :
- Liquid eyeliner, eyeshadow, mascara 8. Sari Ayu
a. Preparat make up
- Lipstik, alas bedak, blush on, lip gloss, bedak tabur, cleansing, penyegar
b. Preparat mata
- Eye brow, eye make-up, eyeshadow c. Preparat untuk perawatan :
- Facial foam acne, cream masker jerawat, body lotion, dan lain-lain
d. Hair Care : Sariayu Hijab Conditioner, Sariayu Hijab Shampoo Sachet
e. Jamu : Kaplet jerawat, kaplet susut perut, dan lain-lain. 9. Rudy hadisuwarno
a. Aloe Cream 250 ml
b. Hairlossdefense Shampoo Ginseng 200 ml
c. Hairlossdefense Hair Mask Ginseng 50 ml dan 200 ml d. Sariayu Hijab Conditioner
e. Anti Dundruff Serum f. Creambath Ginseng UVF
g. Damagefense Conditioner Sunflower h. Damagefense Hair Tonic Sunflower
i. Damagefense Shampoo Sunflower 100 ml dan 200 ml j. Dandrufdefense Hair Tonic Tea Tree Oil 100 ml dan 225 ml k. Dandrufdefense Shampoo Tea Tree Oil 200 ml
l. Hair Growth Serum
j. Hair Intenxive Repair Serum k. Hair Spray Aerosol Strong 250 ml l. Hair Spray Non Aerosol Strong 200 ml II.2.4. Sertifikat
Pada tahun 1996 PT Martina Berto menjadi pabrik kosmetik pertama di Indonesia yang memperoleh sertifikat ISO 9001 : 2008 (Sistem Manajemen Mutu), perusahaan ini menjadi satu-satunya pendiri Global Compact PBB dari Asia (PT. Martina Berto, 2015).
1. Perusahaan ini juga mendapatkan sertifikat ISO 14001 : 2004 dan sertifikat GMP: CPKB (Cara Produksi kosmetika Yang Baik) dan CPOTB (Cara Produksi Obat Tradisional Yang Baik) pada tahun 2000. 2. Halal Award 2015 diterima oleh brand Sariayu Martha Tilaar yang
terpilih sebagai Halal Top Brand 2015 untuk kategori kosmetik.
3. Pada tahun 2015 juga sertifikat Ecocert diberikan untuk brand Solusi Martha Tilaar Organic Renewage yang menjadi kosmetik pertama dari
Indonesia yang berbahan aktif dengan sertifikasi Ecocert, yaitu minyak biji anggur dan ekstrak kayu manis.
II.2.5. Penerapan CPKB 1. Sistem Manajemen Mutu
Perusahaan hendaknya memahami sistem penjaminan mutu termasuk Cara Pembuatan Kosmetik yang Baik (CPKB), dan dilengkapi dengan personil yang handal, bangunan, peralatan dan fasilitas yang sesuai serta cukup dalam mencapai sasaran mutu yang telah ditetapkan. Penjaminan Mutu mencakup semua hal yang dapat mempengaruhi mutu produk, baik secara individu maupun kolektif. Hal ini terkait pada semua aktivitas perusahaan secara total untuk memastikan bahwa produk yang dihasilkan sesuai dengan persyaratan mutu yang telah ditetapkan (PT. Martina Berto, 2015).
Secara struktur organisasi kedudukan QA dan QC sejajar tetapi dalam pelaksanaannya sistem manajemen mutu pada PT. Martina Berto semua dirilis oleh QA. Penjaminan mutu pada PT. Martina Berto mencakup semua hal yang dapat mempengaruhi mutu produk, baik secara individu maupun kolektif. Hal ini terkait pada semua aktivitas perusahaan secara total untuk memastikan bahwa produk yang dihasilkan sesuai dengan persyaratan mutu yang telah ditetapkan (PT. Martina Berto, 2015).
Pelaksanaan sistem mutu telah menjamin bahwa apabila diperlukan, dilakukan pengambilan contoh bahan awal, produk antara dan produk jadi, serta dilakukan pengujian terhadapnya untuk menentukan diluluskan atau ditolak, yang didasarkan atas hasil uji yang berkaitan dengan mutu (PT. Martina Berto, 2015).
2. Personalia
Personalia yang bekerja di PT. Martina Berto mempunyai pengetahuan, pengalaman, ketrampilan dan kemampuan yang sesuai dengan tugas dan fungsinya, dan tersedia dalam jumlah yang cukup.
Mereka harus dalam keadaan sehat dan mampu menangani tugas yang dibebankan kepadanya
Organisasi, Kualifikasi dan Tanggung jawab pada PT. Martina Berto yakni:
1) Dalam struktur organisasi perusahaan, bagian produksi dan pengawasan mutu hendaklah dipimpin oleh orang yang berbeda dan tidak ada keterkaitan tanggung jawab satu sama lain.
2) Kepala bagian produksi harus memperoleh pelatihan yang memadai dan berpengalaman dalam pembuatan kosmetik. Ia harus mempunyai kewenangan dan tanggung jawab dalam manajemen produksi yang meliputi semua pelaksanaan kegiatan, peralatan, personalia produksi, area produksi dan pencatatan.
3) Kepala bagian jaminan mutu harus memperoleh pelatihan yang memadai dan berpengalaman dalam bidang pengawasan mutu. Ia harus diberi kewenangan penuh dan tanggung jawab dalam semua tugas pengawasan mutu meliputi penyusunan, verifikasi dan penerapan semua prosedur pengawasan mutu.
3. Bangunan dan Fasilitas
Bangunan dan fasilitas pada PT. Martina Berto dipilih pada lokasi yang sesuai, dirancang, dibangun, dan dipelihara sesuai standar, yaitu sebagai berikut:
1) Tidak menyebabkan kontaminasi dari lingkungan sekitar dan hama. 2) Tersedia ruang ganti pakaian dan fasilitasnya. Toilet terpisah dari area
produksi guna mencegah terjadinya kontaminasi.
3) Permukaan dinding dan langit-langit halus dan rata serta mudah dirawat dan dibersihkan. Lantai di area pengolahan mempunyai permukaan yang mudah dibersihkan dan disanitasi.
4) Area gudang mempunyai luas yang memadai dengan penerangan yang sesuai, diatur dan diberi perlengkapan sedemikian rupa sehingga memungkinkan penyimpanan bahan dan produk dalam keadaan kering, bersih dan rapi.
4. Peralatan
Peralatan yang terdapat pada PT. Martina Berto didesain dan ditempatkan sesuai dengan produk yang dibuat:
1) Rancang Bangun
a. Permukaan peralatan yang bersentuhan dengan bahan yang diolah tidak bereaksi atau menyerap bahan.
b. Peralatan tidak menimbutkan akibat yang merugikan terhadap produk misalnya melalui tetesan oli, kebocoran katub atau melalui modifikasi atau adaptasi yang tidak salah/tidak tepat.
c. Peralatan mudah dibersihkan. 2) Pemasangan dan Penempatan
a. Peralatan/mesin ditempatkan sedemikian rupa sehingga tidak menyebabkan kemacetan aliran proses produksi dan diberi penandaan yang jelas untuk menjamin tidak terjadi campur baur antar produk.
b. Saluran air, uap, udara bertekanan atau hampa udara, dipasang sedemikian rupa sehingga mudah dicapai selama kegiatan berlangsung. Saluran ini diberi label atau tanda yang jelas sehingga mudah dikenali.
c. Sistem-sistem penunjang seperti sistem pemanasan, ventilasi, pengatur suhu udara, air (air minum, air murni, air suling), uap, udara bertekanan dan gas berfungsi dengan baik sesuai dengan tujuannya dan dapat di identifikasi.
3) Pemeliharaan
a. Peralatan untuk menimbang mengukur, menguji dan mencatat dipelihara dan dikalibrasi secara berkala. Semua catatan pemeliharaan dan kalibrasi disimpan.
b. Petunjuk cara pembersihan peralatan ditulis secara rinci dan jelas diletakkan pada tempat yang mudah dilihat dengan jelas.
Sanitasi dan higiene dilaksanakan untuk mencegah terjadinya kontaminasi terhadap produk yang diolah. Pelaksanaan sanitasi dan higiene mencakup personalia, bangunan, mesin-mesin dan peralatan serta bahan awal.
1) Personalia
a. Personalia harus dalam keadaan sehat untuk melaksanakan tugas yang dibebankan kepadanya, dilakukan pemeriksaan kesehatan secara teratur untuk semua personil bagian produksi yang terkait dengan proses pembuatan.
b. Semua personil harus melaksanakan higiene perorangan.
c. Setiap personil yang pada suatu ketika mengidap penyakit atau menderita luka terbuka atau yang dapat merugikan kualitas tidak diperkenankan menangani bahan baku, bahan pengemas, bahan dalam proses dan produk jadi.
d. Semua personil yang diizinkan masuk ke area produksi harus melaksanakan higiene perorangan termasuk mengenakan pakaian kerja yang memadai.
2) Bangunan
a. Tersedia wastafel dan toilet dengan ventilasi yang baik yang terpisah dari area produksi.
b. Tersedia loker di lokasi yang tepat untuk tempat ganti pakaian dan menyimpan pakaian serta barang-barang lain milik karyawan.
3) Peralatan dan Perlengkapan
a. Peralatan / perlengkapan harus dijaga dalam keadaan bersih. b. Pembersihan dengan cara basah atau vakum lebih dianjurkan.
Udara bertekanan dan sikat digunakan dengan hati-hati dan sedapat mungkin dihindari karena menambah risiko pencemaran produk.
c. Prosedur tetap pembersihan dan sanitasi mesin-mesin telah diikuti dengan konsisten.
Pada PT. Martina Berto metode pembersihan yang biasa digunakan yaitu bahan pembersih etanol 70% dan untuk higiene
perorangan dengan menggunakan masker, sarung tangan, baju dan sepatu kerja saat melakukan produksi.
6. Produksi
Pada setiap proses produksi pada PT. Martina Berto dilakukan pengawasan mutu yang mengacu kepada sistem Quality Assurance di mulai dari bahan baku, bahan setengah jadi, produk jadi, hingga pengiriman ke distributor.
1) Air untuk Produksi
a. Peralatan untuk memproduksi air dan sistem pemasokannya telah dapat memasok air yang berkualitas. Sistem pemasokan air disanitasi sesuai Prosedur Tetap yang telah ditetapkan oleh perusahaan.
b. Air yang digunakan untuk produksi sekurang-kurangnya berkualitas air minum. Mutu air yang meliputi parameter kimiawi dan mikrobilologi telah dipantau secara berkala, sesuai prosedur tertulis dan setiap ada kelainan akan segera ditindak lanjuti dengan tindakan koreksi.
c. Pada PT. Martina Berto air yang digunakan pada proses produksi adalah purified water.
2) Verifikasi Material (Bahan)
a. Semua pasokan bahan awal (bahan baku dan bahan pengemas) diperiksa dan diverifikasi mengenai pemenuhannya terhadap spesifikasi yang telah ditetapkan dan dapat ditelusuri sampai dengan produk jadinya.
b. Contoh bahan awal diperiksa secara fisik mengenai pemenuhannya terhadap spesifikasi ditetapkan, dan dinyatakan lulus sebelum digunakan.
c. Semua bahan harus bersih dan telah diperiksa kemasannya terhadap kemungkinan terjadinya kebocoran, lubang atau terpapar. 3) Pencatatan Bahan
a. Semua bahan memiliki catatan yang lengkap mengenai nama bahan yang tertera pada label dan pada bukti penerimaan, tanggal penerimaan, nama pemasok, nomor batch dan jumlah.
b. Setiap penerimaan dan penyerahan bahan awal dicatat dan diperiksa secara teliti kebenaran identitasnya.
4) Material Ditolak (Reject)
Pasokan bahan yang tidak memenuhi spesifikasi akan ditandai, dipisah dan segera diproses lebih lanjut sesuai Prosedur Tetap.
5) Sistem Pemberian Nomor Bets
a. Setiap produk antara, produk ruahan, dan produk akhir diberi nomor identitas produksi (nomor bets) yang dapat memungkinkan penelusuran kembali riwayat produk untuk produk yang sama guna menghindari kebingungan / kekacauan.
b. Catatan pemberian nomor bets disimpan 6) Penimbangan dan Pengukuran
a. Penimbangan dilakukan di tempat tertentu menggunakan peralatan yang telah dikalibrasi.
b. Semua pelaksanaan penimbangan dan pengukuran akan dicatat dan dilakukan pemeriksaan ulang oleh petugas yang berbeda. 7) Prosedur dan Pengolahan
a. Semua bahan awal harus lulus uji sesuai spesifikasi yang ditetapkan.
b. Semua prosedur pembuatan harus dilaksanakan sesuai prosedur tetap tertulis.
c. Semua pengawasan selama proses yang diwajibkan harus dilaksanakan dan dicatat.
d. Produk ruahan harus diberi penandaan sampai dinyatakan lulus oleh Bagian Pengawasan Mutu.
e. Hasil akhir proses produksi dicatat. 8) Produk Kering
Penanganan bahan dan produk kering memerlukan perhatian khusus dan bila perlu dilengkapi dengan sistem pengendali debu, atau sistem hampa udara sentral atau cara lain yang sesuai.
Penanganan bahan-bahan yang kering sering menimbulkan masalah: kontaminasi silang, kontaminasi udara dan masalah kesehatan bagi personil akibat debu pada saat pengolahan maupun
pengemasan sehingga memerlukan perhatian khusus. Kontaminasi silang, kontaminasi udara dan kemungkinan timbulnya masalah bagi kesehatan personil dapat dikurangi dengan :
a. Menggunakan sistem pengendalian debu, penyedot debu diruang timbang, ruang pencampuran, ruang pengisian dan pengemasan. b. Sistem penghisap debu yang efektif dipasang dengan letak lubang
pembuangan yang tepat untuk mencegah pencemaran terhadap produk atau proses lain.
c. Mesin pencampur, pengayak dan pengisian dilengkapi dengan sistem pengendalian debu.
d. Ruangan tertutup, terpisah dengan area proses basah. e. Menggunakan ruang antara (air lock).
f. Peralatan pelindung keselamatan bagi personil. 9) Produk Basah
a. Cairan, krim, dan lotion harus diproduksi sedemikian rupa untuk mencegahdari kontaminasi mikroba dan kontaminasi lainnya.
b. Penggunaan sistem produksi dan transfer secara tertutup. Sistem produksi secara tertutup adalah sistem pengolahan dimana semua bahan baku dicampur secara tertutup melalui proses pemindahan dengan udara bertekanan. Proses pencampuran berada dalam tangki yang tertutup, pemindahan dan pengisian produk dilakukan melalui sistem perpipaan yang tertutup untuk menjamin agar produk tidak tercemar.
10) Pelabelan dan Pengemasan
a. Lini pengemasan hendaklah diperiksa sebelum dioperasikan. Peralatan harus bersih dan berfungsi baik. Semua bahan dan produk jadi dari kegiatan pengemasan sebelumnya harus dipindahkan.
b. Selama proses pelabelan dan pengemasan berlangsung, akan diambil contoh secara acak dan diperiksa.
c. Sisa label dan bahan pengemas dikembalikan ke gudang dan dicatat. Bahan pengemas yang ditolak, dicatat dan diproses lebih lanjut sesuai dengan Prosedur Tetap.
Semua produk jadi dikarantina terlebih dahulu. Setelah dinyatakan lulus uji oleh bagian Pengawasan Mutu, barulah dimasukkan ke gudang produk jadi. Selanjutnya produk dapat didistribusikan.
7. Pengawasan Mutu
Pengawasan mutu merupakan semua upaya pemeriksaan dan pengujian yang dilakukan sebelum, selama dan setelah pembuatan kosmetik untuk menjamin agar kosmetik yang diproduksi senantiasa memenuhi persyaratan yang telah ditetapkan. Bila belum tersedia fasilitas uji, dapat dilakukan pengujian dengan menunjuk laboratorium yang terakreditasi. Untuk menjamin kebebasan dalam menetapkan keputusannya, maka Bagian Pengawasan Mutu merupakan bagian yang terpisah dari bagian produksi.
Pengawasan mutu pada PT.Martina Berto dilakukan oleh QC secara menyeluruh mulai dari incoming material, in process control, dan outgoing product. Proses pemeriksaan yang dilakukan QC mengacu pada standar yang telah ditetapkan yakni farmakope Indonesia, BP, dan USP.
Pengawasan mutu meliputi:
1) Pengambilan contoh (sampling), pemeriksaan dan pengujian terhadap bahan awal produk dalam proses, produk antara, produk ruahan dan produk jadi sesuai spesifikasi yang ditetapkan. Pengambilan contoh hendaklah dilakukan oleh tenaga yang terlatih dan diberi kewenangan untuk tugas tersebut, guna menjamin contoh yang diambil senantiasa sesuai dengan indentitas dan kualitas bets yang diterima.
2) Program pemantauan lingkungan, tinjauan terhadap dokumentasi bets, program pemantauan contoh pertinggal, pemantauan mutu produk di peredaran, penelitian stabilitas dan menetapkan spesifikasi bahan awal dan produk jadi agar senantiasa memenuhi standar yang ditetapkan.
A. Pengolahan Ulang
a) Metoda pengolahan ulang dievaluasi untuk menjamin agar pengolahan ulang tidak mempengaruhi mutu produk.
b) Pengujian tambahan dilakukan terhadap produk jadi hasil pengolahan ulang.
B. Produk Kembalian
a) Produk kembalian diidentifikasi dan disimpan terpisah di tempat yang dialokasikan untuk itu atau diberi pembatas yang dapat dipindah-pindah misalnya pembatas dari bahan pita, rantai atau tali.
b) Semua produk kembalian diuji kembali apabila perlu, disamping evaluasi fisik sebelum diluluskan untuk diedarkan kembali c) Produk kembalian yang tidak memenuhi syarat spesifikasi akan
ditolak.
d) Produk yang ditolak dimusnahkan sesuai Prosedur Tetap. e) Catatan produk kembalian dipelihara.
8. Dokumentasi
Dokumentasi adalah catatan tertulis tentang formula, prosedur, perintah dan catatan tertulis lainnya yang berhubungan dengan proses pembuatan kosmetik. Dokumen yang telah kadaluarsa dimusnahkan setiap 5 tahun sekali, dan soft copyannya disimpan sebagai arsip perusahaan.
1) Bila terjadi atau ditemukan suatu kekeliruan dalam dokumen hendaknya dilakukan pembetulan sedemikian rupa sehingga naskah aslinya harus tetap terdokumentasi.
2) Dokumen hendaklah diberi tanggal dan disahkan.
3) Salinan dokumen hendaklah diberikan kepada pihak-pihak yang terkait dan pendistribusiannya dicatat.
4) Semua dokumen hendaknya direvisi dan diperbaharui secara berkala, dokumen yang sudah tidak berlaku segera ditarik kembali dari pihak-pihak terkait untuk diamankan.
Audit Internal pada PT. Martina Berto terdiri dari kegiatan penilaian dan pengujian seluruh atau sebagian dari aspek produksi dan pengendalian mutu dengan tujuan untuk meningkatkan sistem mutu. Audit Internal dapat dilakukan oleh pihak luar, atau auditor profesional atau tim internal yang dirancang oleh manajemen untuk keperluan ini yang diaudit oleh BPOM satu kali setiap dua tahun. Pelaksanaan Audit Internal dapat diperluas sampai ke tingkat pemasok dan kontraktor, bila perlu. Laporan harus dibuat pada saat selesainya tiap kegiatan Audit Internal dan di dokumentasikan dengan baik. Sedangkan Pada inspeksi diri dilakukan sekali setahun oleh QA.
10.Penyimpanan
Ketentuan tentang penyimpanan meliputi area penyimpanan serta penanganan dan pengawasan persediaan.
1) Area Penyimpanan
a. Area penyimpanan hendaknya cukup luas untuk memungkinkan penyimpanan yang memadai dari berbagai kategori baik bahan maupun produk, seperti bahan awal, produk antara, ruahan dan produk jadi, produk yang dikarantina, dan produk yang lulus uji, ditolak, dikembalikan atau ditarik dari peredaran.
b. Area penyimpanan hendaknya dirancang atau disesuaikan untuk menjaminkondisi penyimpanan yang baik, bersih, kering dan dirawat dengan baik. Bila diperlukan area dengan kondisi khusus (suhu dan kelembaban)hendaknya disediakan, diperiksa dan dipantau fungsinya.
c. Area penyimpanan untuk produk karantina hendaknya diberi batas secara jelas.
2) Penanganan dan Pengawasan Persediaan Penerimaan Produk
a. Pada saat penerimaan, barang dokumen hendaknya diperiksa dan dilakukan verifikasi fisik dengan bantuan keterangan pada label yang meliputi tipe barang dan jumlahnya.
b. Barang kiriman harus diperiksa dengan teliti terhadap kemungkinan terjadinya kerusakan dan atau cacat. Hendaknya ada Catatan Pertingga luntuk setiap penerimaan barang.
Pengawasan
a. Catatan-catatan harus dipelihara meliputi semua catatan penerimaan dan catatan pengeluaran produk.
b. Pengawasan hendaknya meliputi pengamatan prinsip rotasi barang (FlFO).
c. Semua label dan wadah produk tidak boleh diubah, dirusak atau diganti.
11. Kontrak Produksi dan Pengujian
Pelaksanaan kontrak produksi dan pengujian hendaknya secara jelas dijabarkan, disepakati dan diawasi, agar tidak terjadi kesalah pahaman atau salah dalam penafsiran di kemudian hari, yang dapat berakibat tidak memuaskannya mutu produk atau pekerjaan. Dalam hal kontrak pengujian, keputusan akhir terhadap hasil pengujian suatu produk, tetap merupakan tanggung jawab pemberi kontrak. Penerima kontrak hanya bertanggung jawab terhadap pelaksanaan pengujian sampai diperoleh hasil pengujian.
12.Penanganan Keluhan dan Penarikan Produk 1) Penanganan Keluhan
a. Hendaknya ditentukan Personil yang bertanggung jawab untuk menangani keluhan dan menentukan upaya pengatasannnya. Bila orang yang ditunjuk berbeda dengan personil yang diberi kewenangan untuk menangani hal tersebut, yang bersangkutan hendaknya diberi arahan untuk waspada terhadap kasus-kasus keluhan, investigasi atau penarikan kembali (recall).
b. Harus ada prosedur tertulis yang menerangkan tindakan yang harusdiambil, termasuk perlunya tindakan penarikan kembali (recall), bila kasus keluhan yang terjadi meliputi kerusakan produk. c. Bila kerusakan produk ditemukan atau diduga terjadi dalam suatu bets, hendaknya dipertimbangkan kemungkinan terjadinya kasus serupa pada bets lain. Khususnya bets lain yang mungkin mengandung produk proses ulang dari bets yang bermasalah hendaknya diselidiki.
d. Apabila terjadi kegagalan produk dan kerusakan produk yang menjurus kepada terganggunya keamanan produk, Instansi yang berwenang hendaknya diberitahu.
2) Penarikan Produk
a. Hendaknya dibuat sistem penarikan kembali dari peredaran terhadap produk yang diketahui atau diduga bermasalah.
b. Hendaknya ditunjuk Personil yang bertanggung jawab atas pelaksanaan dan koordinasi penarikan kembali produk termasuk personil lain dalam jumlah yang cukup.
c. Keefektifan pengaturan penarikan kembali produk hendaknya dievaluasi dari waktu ke waktu.
d. Hendaklah dibuat instruksi tertulis yang menjamin bahwa produk yang ditarik kembali disimpan dengan baik pada daerah yang terpisah sambil menanti keputusan selanjutnya.
II.2 Kalbe Farma
II.2.1 Visi dan Misi Perusahaan
Visi PT. Kalbe Farma, Tbk adalah “Menjadi perusahaan Indonesia terbaik dalam bidang kesehatan yang didorong oleh inovasif, merek dagang yang kuat dan menejemen yang unggul.”
Misi PT. Kalbe Farma, Tbk.menetapkan misi perusahaan yang dilaksanakan secara berkesinambungan. Misi PT. Kalbe Farma, Tbk. terfokus pada tiga elemen utama, yaitu: (“To Improve Health For A Better
Life”), “Meningkatkan kesehatan untuk kehidupan yang lebih baik” dengan tujuan sebagai berikut :
1. Mengembangkan, memproduksi, dan memasarkan produk perawatan kecantikan dan spa yang bernuansa ketimuran dan alami dengan standar mutu internasional.
2. Menyediakan layanan prima kepada pelanggan dalam porsi yang seimbang, termasuk konsumen dan para penyalur produk.
3. Mempertahankan kondisi keuangan yang sehat dan pertumbuhan bisnis.
4. Merekrut, melatih, dan mempertahankan tenaga kerja yang kompeten dan produktif sebagai bagian dari aset Perseroan.
5. Memanfaatkan metode operasi, sistem, dan teknologi yang efisien dan efektif di seluruh unit dan fungsi usaha.
6. Menerapkan “Good Corporate Governance” secara konsisten demi kepentingan para pemangku kepentingan.
7. Memberikan tingkat keuntungan yang wajar kepada para pemegang saham.
8. Mengembangkan pasar internasional kosmetika, produk spa, dan herbal dengan fokus jangka menengah di kawasan Asia Pasifik dan fokus jangka panjang di pasar global.
Dalam mencapai visi dan misi kalbe mempunyai motto: “The Scientific Pursuit of Health for a Better Life” (Mengabdikan ilmu untuk kesehatan dan kesejahteraan). Visi dan misi tersebut dilaksanakan dengan melakukan juga nilai inti PT. Kalbe Farma, Tbk. yaitu dengan memberikan pelayanan terbaik kepada pelanggan (giving the best to customers), gigih untuk mencapai yang terbaik (striving for exellence), kerja sama yang kokoh (strong team work), inovasi (innovation), integritas (integrity), dan lincah (agillity).
Selain itu, PT Kalbe Farma, Tbk. juga membuat suatu core value (nilai inti) yang berfungsi menunjang penerapan visi dan misi yaitu berupa Kalbe Panca Sradha dan dijadikan landasan oleh seluruh karyawan dalam menjalankan kinerja sehari-hari (Fatmawati, 2014) :
2. Mindfulness is the foundation of our action (Kesadaran penuh adalah dasar setiap tindakan kami)
3. Innovation is the key to our success (Inovasi adalah kunci keberhasilan kami)
4. Strive to be the best (Bertekad untuk menjadi yang terbaik)
5. Interconnectedness is a universal way of life (Saling keterkaitan adalah panduan hidup kami)
Gambar 1. Logo PT. Kalbe Farma, Tbk.
II.2.2 Sertifikasi c-GMP dan CPOB terkini serta penghargaan PT. Kalbe Farma Tbk
Pada tahun 2001 mendapatkan sertifikat ISO 9001:2000 dari Lloyds Register Quality Assurance, pada tahun 2012 PT. Kalbe Farma, Tbk juga telah mendapatkan sertifikat CPOB (Cara Pembuatan Obat yang Baik) dari Badan Pengawasan Obat dan Makanan untuk sediaan tablet biasa dan salut non Antibiotika; tablet biasa dan salut antibiotika non β-laktam; suspensi kering oral non antibiotika; serta suspensi kering oral antibiotika non β-laktam dan pada bulan Januari 2014, PT. Kalbe Farma, Tbk telah mendapatkan sertifikat ISO 14001:2004. Selanjutnya, mendapatkan sertifikat ISO 9001:2008 pada tahun. dari Lloyds Register Quality Assurance. Selain itu juga mendapatkan sertifikat OHSAS 18001:2007 pada April 2014 (Fatmawati, 2014).
Saat ini, Kalbe adalah salah satu perusahaan farmasi terbesar di Asia Tenggara yangsahamnya telah dicatat di bursa efek dengan nilai kapitalisasi pasar di atas US$ 1 miliar dan penjualan melebihi Rp 7 triliun. II.2.3 Produk-produk
Terdapat tiga jenis produk kesehatan yang ditawarkan oleh Kalbe yaitu obat bebas, produk nutrisi dan produk minuman energi. Produk obat bebas ditujukan untuk keluarga yang diperkirakan memiliki keterbatasan untuk memperoleh layanan kesehatan profesional. Sedangkan, produk nutrisi yang ditawarkan adalah produk-produk yang digunakan untuk mendukung kesehatan dengan sasaran pasar masyarakat di semua kelompok usia, seperti susu bayi dan anak-anak, ibu hamil dan menyusui, beberapa kebutuhan khusus kaum manula serta biskuit dan sereal bayi. Produk minuman energi yang ditawarkan didominasi oleh Extra Joss® dengan sasaran konsumen adalah kaum pekerja.
Beberapa merek yang menjadi pemimpin masing-masing kategori produk adalah Promag® dan Waisan® (obat sakit maag), Neo-Entrostop® (anti-diare), Woods®, Komix®, Mextril® , dan Mixadin® (obat batuk), Procold® dan Mixagrip® (obat flu), Fatigon®, Cerebrovit® dan Cerebrofort® (multivitamin).
Produk nutrisi Kalbe telah memperoleh posisi pasar yang kuat di Industri. Beberapa produk nutrisi andalan Kalbe adalah Prenagen® (nutrisi kehamilan), Milna® (biskuit dan sereal bayi), BMT®, Chil Mil®, Chil Kid®, Chil School® (susu bayi dan balita). Selain itu, Kalbe menyediakan special clinical food, Diabetasol® yang telah mendominasi pasar. Awalnya produk ini diproduksi dengan perjanjian subkontrak dengan pihak ketiga, sekarang diproduksi oleh pabrik baru Kalbe Morinaga yang mulai beroperasi pada April 2007.
b. Devisi Obat Resep
Kalbe memiliki produk dalam beragam kategori terapi yang terdiri dari obat-obatan berlisensi, generik bermerek dan generik yang berjumlah lebih dari 280 jenis obat. Pada saat ini, Kalbe merupakan produsen obat resep terbesar di Indonesia. Pada tahun 2007, Kalbe memperkenalkan lebih dari 30 produk obat resep baru. Selama ini, Kalbe mengandalkan inovasi dalam riset dan pengembangan untuk memproduksi produk obat generik bermerek juga menjalin aliansi
strategis dengan produsen farmasi dengan reputasi internasional untuk produk yang masih dilindungi paten.
Sejak tahun 2004, Kalbe melakukan teknik baru dalam pengembangan produk, dengan dibentuknya Innogene Kalbiotech yang bergerak di bidang riset bioteknologi. Setelah dua tahun beroperasi, Kalbe memperkenalkan produk pertamanya yaitu Kalsolac®, obat dalam bentuk cairan steril yang digunakan pada fase pemulihan pasca-bedah jantung dan cidera otak traumatis. Untuk fase pemulihan pasca-bedah jantung, obat ini dipasarkan di Indonesia dengan merek Totilac®. Untuk indikasi cidera otak traumatis dilakukan pengujian pada hewan di Amerika Serikat pada tahun 2007 seiring dengan pengurusan paten. Produk lain yang siap dipasarkan adalah TheraCIM®, antikanker antibodi monoklonal yang digunakan untuk mengobati kanker otak serta kanker hidung dan tenggorokan. Kalbe Vision yang khusus bergerak dalam pengembangan dan pemasaran produk perawatan mata yang inovatif juga telah memperkenalkan solusi menyeluruh untuk tindakan operasi katarak.
c. Devisi distribusi dan kemasan.
Bisnis distribusi dan kemasan Kalbe Grup telah berangsur-angsur mengalami perubahan orientasi dan skala bisnisnya. Sehingga, tidak hanya memenuhi kebutuhan internal Grup. Divisi Distribusi Kalbe mengelola 40 pusat distribusi di seluruh Indonesia, mencakup lebih dari 1 juta outlet. Kalbe telah dipercaya untuk menangani distribusi produk-produk prinsipal non-afiliasi meliputi produsen farmasi, produk kesehatan serta diagnostik dan instrumen medis dan bahan baku kimia. Pada tahun 2007, Divisi distribusi melakukan upaya peningkatan pelayanan dan diversifikasi bisnis dengan membentuk Klinik Mitrasana di Kawasan Industri Jababeka 2, sebuah fasilitas kesehatan ekonomis yang terdiri dari klinik, farmasi, laboratorium dan mini market. Divisi kemasan Kalbe menyediakan berbagai jenis kemasan dari bahan fleksibel dan kertas bagi produsen obat, kosmetik, nutrisi dan produk kesahatan lain di Indonesia.
II.2.5 Penerapan Aspek CPOB
CPOB merupakan pedoman yang sangat penting tidak hanya bagi industri farmasi dan regulator, tetapi juga bagi konsumen dalam memenuhi kebutuhannya akan pengobatan yang aman, berkhasiat dan berkualitas.
PT. Kalbe Farma, Tbk senantiasa mengembangkan diri melalui inovasi, nama dagang yang kuat, dan manajemen yang unggul. Hal tersebut dilakukan agar PT. Kalbe Farma, Tbk. untuk menjadi perusahaan perawatan kesehatan terbaik. PT. Kalbe Farma, Tbk. memiliki komitmen membantu masyarakat mewujudkan kesehatan dan kehidupan yang lebih baik. Dalam mewujudkan komitmennya, berbagai hal telah dilakukan, salah satunya melalui penerapan Cara Pembuatan Obat yang Baik (CPOB) dalam setiap aspek pembuatan obat di PT. Kalbe Farma, Tbk
PT. Kalbe Farma, Tbk menerapkan CPOB 2012, yaitu sebagai berikut (BPOM, 2014; Kalbe Farma, 2016; Fatmawati, 2014):
a. Manajemen Sistem Mutu
Manajemen Mutu berfungsi untuk menjamin pembuatan obat agar sesuai dengan tujuan penggunaannya, memenuhi syarat izin edar dan bermutu. Konsep dasar manajemen mutu adalah pengawasan mutu, CPOB dan pemastian mutu yang terkait.
Kegiatan manajemen mutu di PT. Kalbe Farma, Tbk telah memenuhi CPOB. Bagian dari manajemen mutu di PT. Kalbe Farma, Tbk adalah Quality Operation, dimana pada bagian ini terdapat Quality Assurance (pemastian mutu) dan Quality Control (pengawasan mutu). Pemastian mutu adalah keseluruhan pengaturan yang dibuat dengan tujuan untuk memastikan bahwa obat yang dihasilkan telah memenuhi mutu yang sesuai dengan tujuan penggunaannya. Pengawasan mutu bertugas untuk mengontrol kualitas dari bahan awal (bahan baku dan bahan. kemas) hingga ke produk jadi yang siap dipasarkan. Pemeriksaan yang dilakukan meliputi pemeriksaan fisik, kimia, dan mikrobiologi.
Pemastian mutu ini telah dipastikan dengan pelaksanaan CPOB untuk menghindarkan atau meminimalkan resiko yang tidak dapat dideteksi melalui serangkaian tes misalnya kontaminasi dan tercemarnya produk. Pelaksanaan CPOB itu sendiri dipastikan dengan melakukan pengawasan mutu. Pengawasan mutu ini meliputi berbagai macam aspek seperti produk yang sesuai standar, bangunan dan fasilitas yang memadai, dan sebagainya.
b. Personalia
Dalam suatu industri farmasi, personil yang terlibat dalam industri tersebut harus memenuhi persyaratan, baik secara kuantitas maupun kualitas. CPOB mensyaratkan jumlah personil yang memadai dan terkualifikasi untuk melaksanakan semua tugas. Setiap personil harus memiliki kesehatan mental dan fisik yang baik sehingga mampu melaksanakan tugasnya secara professional. Sikap dan kesadaran tinggi setiap personil juga diperlukan dalam mewujudkan pelaksanaan CPOB.
PT. Kalbe Farma, Tbk menggunakan tenaga kerja yang terlatih secara teknis dalam jumlah yang memadai untuk melaksanakan kegiatan produksi dan pengawasan mutu sesuai dengan prosedur dan spesifikasi yang telah ditentukan secara efektif dan efisien. Masing-masing bagian produksi, RnD, QA, dan QC dipimpin oleh seorang apoteker dan diberi wewenang penuh dan saranan cukup yang diperlukan untuk dapat melaksanakan tugasnya secara efektif.
Peningkatan kesadaran dan pemahaman karyawan terhadap CPOB di PT. Kalbe Farma, Tbk. dilakukan melalui program pelatihan Kualitas Lima Aspek (KUA LIMA) yang meliputi K3 (Kesehatan dan Keselamatan Kerja), dan 5R (Ringkas, Rapi, Resik, Rawat, Rajin). Aspek KUA LIMA meliputi produk, manusia, bahan dan peralatan, metode, serta lingkungan kerja. Uraian lima aspek dalam KUA LIMA adalah:
b. Sumber daya manusia yang selalu mengutamakan kualitas c. Peralatan, bahan, dan teknologi yang memadai
Untuk menjamin kepuasan terhadap semua pelanggan, baik internal maupun eksternal PT. Kalbe Farma Tbk. melakukan berbagai upaya antara lain dengan menerapkan Kalbe Service Exellence (KSE). Setiap karyawan harus melaksanakan sebelas perilaku KSE, yaitu senyum tulus, wajah hangat dan bersemangat, pelanggan adalah orang penting, dengarkan kebutuhannya, menyebut namanya, bahasa tubuh positif, membicarakan yang diminati pelanggan, bahasa yang halus dan tepat, memberitahukan proses yang sudah/sedang/akan dikerjakan, pengetahuan akan produk, serta tampil dengan rapi.
c. Bangunan dan Fasilitas
PT. Kalbe Farma, Tbk. berlokasi di Kawasan Industri Delta Silicon, Jalan MH. Thamrin blok A3-1, Lippo Cikarang, Bekasi. Bangunannya memiliki luas total 41.027 m2 yang berdiri di atas lahan seluas 105.130 m2, terdiri dari gedung kantor, gedung produksi, teknik, gudang dan sarana pendukung seperti pengolahan limbah, lapangan parkir, koperasi serta kantin. Sedangkan untuk gedung pemasarannya terpisah, yaitu terletak di Gedung Enseval, Jalan Letjen Suprapto, Cempaka Putih, Jakarta.
Lokasi pabrik terletak cukup jauh dari pemukiman penduduk. Hal tersebut bertujuan untuk meminimalisasi resiko pencemaran, baik dari pabrik ke lingkungan maupun dari lingkungan ke pabrik. Gedung dilengkapi dengan sarana dan prasarana yang ditujukan untuk mencegah terjadinya kontaminasi yang berasal dari udara, tanah, air, maupun dari kegiatan di sekitarnya, seperti debu dari industri lain, rembesan air, serangga, binatang pengerat, dan sebagainya. PT. Kalbe Farma, Tbk. Memiliki instalasi pengolahan limbah sebagai upaya pencegahan terjadinya pencemaran terhadap lingkungan. Pengolahan limbah pabrik ini bekerja sama dengan pihak luar.
Ruang produksi di PT. Kalbe Farma, Tbk, dicat dengan cat epoxy dengan tujuan agar mudah dibersihkan. Ruangan dibuat melengkung (tidak memiliki sudut) agar tidak menjadi tempat berkumpulnya debu. Jendela dibuat miring dengan maksud agar mudah dibersihkan dan juga tidak menjadi tempat berkumpulnya debu. Ruangan dalam produksi dibagi menjadi 3 area yang memiliki tekanan udara yang berbeda. Tujuan dari pembedaan tekanan ini untuk mencegah terjadinya kontaminasi silang. Penutup fitting lampu, titik ventilasi, dan instalasi lainnya dibuat rata dengan langit-langit sehingga meminimalkan adanya celah yang dapat menahan debu. Sarana-sarana penunjang produksi, seperti Heating, Ventilating, and Air Conditioning (HVAC), pipa saluran air, Air Handling Unit (AHU), kabel listrik diletakkan di ruangan khusus di antara setiap lantai ruangan produksi yang disebut mezzanine. Beberapa ruangan juga dilengkapi dengan pengumpul debu (dust collector) untuk mengendalikan jumlah partikel sesuai dengan kelas ruangan masing-masing.
PT. Kalbe Farma Tbk. memiliki bangunan dengan ukuran, rancang bangun, konstruksi, dan tata letak yang secara umum telah memadai sesuai dengan persyaratan CPOB. Hal ini dilakukan dalam rangka menunjang pelaksanaan kerja, pembersihan, dan pemeliharaannya. Rancang bangun dan tata letak ruang produksi PT. Kalbe Farma, Tbk. dibagi menjadi beberapa kelompok sehingga kegiatan-kegiatan dapat berlangsung tanpa harus berhubungan dengan daerah luar. Ruang ganti pakaian berhubungan langsung dengan area produksi dan dipisahkan oleh pintu yang hanya dapat diakses dengan menggunakan kartu akses karyawan.
Gedung kantor PT. Kalbe Farma, Tbk. terdiri dari 4 lantai sebagai berikut:
a. Lantai 1 meliputi bagian Departemen Human Resource Development, Departemen Personal General Affair, Departemen Process Development, Departemen Akuntansi, Departemen
Pembelian, ruang perpustakaan, dan kantin.
b. Lantai 1½ meliputi Departemen Perencanaan Produksi dan Pengendalian Persediaan Pusat, Departemen Veteriner, serta Departemen Teknologi Informasi, Departemen Group Process Improvement.
c. Lantai 2 meliputi Departemen Keuangan dan Pemasaran, Departemen Quality System, dan Direksi.
d. Lantai 3 meliputi Departemen Research and Development yang terdiri dari bagian Formulation dan Analytical Development, Departemen Pemastian Mutu (Quality Assurance), Departemen Pengawasan Mutu (Quality Control) dengan laboratorium pengawasan mutu.
e. Lantai 4 meliputi ruangan pilot plant Departemen Research and Development.
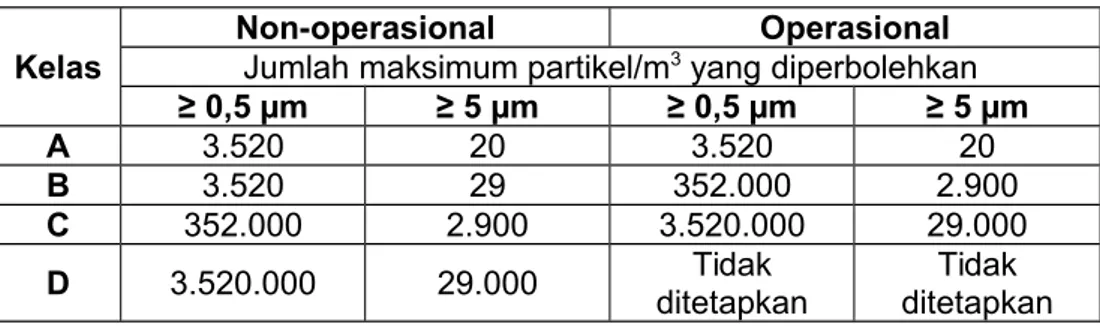
Bangunan pada PT. Kalbe Farma, Tbk. menerapkan sistem line (jalur produksi). Satu line mencakup semua tahap pengolahan sampai dengan pengemasan produk sehingga kontaminasi silang dapat dihindari. Ruang produksi di PT. Kalbe Farma, Tbk. diklasifikasikan sesuai dengan ASEAN GMP, yaitu kelas I dan II (white area), kelas III (grey area), dan kelas IV (black area). Apabila dikaitkan dengan CPOB, kelas black area merupakan kelas E, kelas grey area merupakan kelas C (untuk produksi steril), D (untuk produksi non-steril), dan kelas white area merupakan kelas A, B (produksi steril). Sebagai penghubung antara kelas ruangan yang satu dengan yang lain disediakan ruang antara atau ruang buffer dan loker karyawan. Setiap kelas ruangan memiliki persyaratan jumlah partikel dan jumlah mikroba tertentu, serta tekanan udara yang berbeda untuk mencegah terjadinya kontaminasi silang. Pengaturan perbedaan tekanan udara ini dilakukan dengan membedakan volume udara yang dimasukkan ke dalam ruangan oleh AHU. White area memiliki tekanan udara paling
tinggi dan black area memiliki tekanan udara yang paling rendah, sedangkan tekanan udara di grey area berada diantaranya.
Lantai dasar meliputi ruang produksi line 9, gudang alkohol, departemen teknik, dan ruang loker karyawan. Lantai 1 meliputi ruang produksi line 1, line 2, line 4, line 5, gudang bahan baku dan wadah, gudang kemas, dan gudang obat jadi. Lantai 2 meliputi ruang produksi line 6, line 7, line 8A, dan line 8B. Tiap lantai dalam gedung produksi dipisahkan dengan mezanine, yaitu ruang khusus untuk penempatan fasilitas utility seperti penyedot udara, pipa–pipa (steam pipe, aquademin pipe, water pipe, compressed air pipe), kabel listrik dan lain-lain.
Pergerakan barang dan manusia diatur dalam lalu lintas yang berbeda untuk mencegah kemungkinan terjadinya kontaminasi silang. Penghubung antar ruang atau kelas yang berbeda adalah ruang buffer atau ruang antara, sedangkan untuk barang digunakan penghubung berupa kotak penghubung (pass box). Khusus perpindahan antara grey area dengan white area terdapat air lock yang dilengkapi air shower. Setiap ruang produksi memiliki koridor sebagai lalu lintas umum karyawan atau bahan. Pada area produksi terdapat ruang staging yang digunakan sebagai tempat penyimpanan kemasan dan bahan baku. Selain itu, terdapat pula ruang work in process (WIP) untuk staging produk ruahan dan produk antara.
1) Black area
Area ini meliputi ruang kepala bagian, ruang kepala seksi (kasie), ruang pengemas sekunder, koridor yang menghubungkan gudang obat jadi dan ruang pengemas sekunder, ruang ganti pakaian black dengan pakaian grey, dan ruang buffer black. Perlengkapan yang digunakan berupa baju dan celana kerja berwarna putih (untuk bagian produksi), penutup kepala, dan sandal karet. Area ini memiliki tekanan udara yang paling rendah.
Area ini meliputi gudang timbang, koridor penghubung gudang timbang-ruang proses produksi, ruang proses produksi, ruang pengemasan primer, dan ruang buffer grey. Perlengkapan yang digunakan yaitu overall dengan penutup kepala, masker, sarung tangan (untuk yang bersentuhan langsung dengan produk), ear protector (untuk operator yang bekerja dengan mesin dengan kebisingan yang tinggi), dan sepatu grey. Jika memakai sandal maka harus mengenakan shoes cover disposable yang terbuat dari plastik. Area ini dilengkapi dengan Medium filter dengan kapasitas 95% untuk menyaring udara sehingga jumlah partikel, ukuran partikel, dan jumlah bakteri sesuai dengan persyaratan Tekanan di ruang ini lebih besar dibanding black area.
3) White area
Area ini hanya terdapat di line 6, yang khusus memproduksi sediaan steril. Yang termasuk dalam area ini yaitu : ruang buffer white, ruang ganti pakaian, ruang air shower, dan ruang filling. Perlengkapan yang digunakan yaitu overall dengan penutup kepala (bebas serat), sarung tangan, masker, goggle, dan sepatu white. Area ini dilengkapi dengan HEPA filter dengan kapasitas 99,99% untuk menyaring udara sehingga jumlah partikel, ukuran partikel, dan jumlah bakteri sesuai dengan persyaratan. Tekanan udara di area ini paling besar dibanding area yang lain.
d. Peralatan
Peralatan yang digunakan untuk produksi di PT. Kalbe Farma, Tbk. memiliki rancang-bangun dan konstruksi yang kuat, ukuran yang memadai, serta ditempatkan pada posisi yang tepat. Masing-masing alat diberi penandaan agar memudahkan dalam identifikasinya. Pemasangan dan penempatan peralatan diatur sedemikian rupa sehingga proses produksi dapat berjalan secara efektif dan efisien. Bahan yang digunakan untuk peralatan selama proses produksi sebagian besar adalah baja tahan karat (stainless steel). Peralatan
yang digunakan selalu dirawat secara berkala agar tetap berfungsi dengan baik dan konsisten serta mencegah terjadinya pencemaran yang dapat merubah identitas dan mutu atau kemurnian produk.
Peralatan yang digunakan pada tiap line produksi disesuaikan dengan produk yang dihasilkan dan ukuran bets dari masing-masing produk. Penempatan peralatan produksi dilakukan mengikuti alur proses kerja sehingga produksi dapat dilaksanakan dengan efektif dan efisien. Pemisahan peralatan dilakukan untuk menghindari kontaminasi silang antara produk satu dengan produk yang lain. Pencegahan terhadap kontaminasi debu yang dihasilkan pada saat proses produksi dilakukan dengan menggunakan pengumpul debu. Peralatan juga diberi penandaan status penggunaan alat tersebut untuk menghindari kesalahan penggunaan alat.
Tiap mesin diletakkan dalam ruang sesuai dengan proses yang sedang berlangsung. Bila terdapat lebih dari satu alat dalam satu ruangan maka peralatan diletakkan tidak berdekatan agar proses kerja dilakukan dengan leluasa dan mencegah terjadinya kontaminasi silang dan pencampuran antar bahan maupun produk ruahan.
Keakuratan peralatan selalu dijaga dengan melakukan validasi, kalibrasi, dan kualifikasi secara teratur oleh Departemen Pemastian Mutu bekerja sama dengan lembaga metrologi setempat. Peralatan dan mesin baru harus melalui tahapan kualifikasi terlebih dahulu, yaitu kualifikasi instalasi, kualifikasi operasi dan kualifikasi kinerja. Pada peralatan lama dilakukan kualifikasi secara periodik, yaitu setiap 3 tahun. Kalibrasi dilakukan pada periode tertentu yang sudah ditetapkan dan tercatat dalam Jadwal Kalibrasi Alat. Kalibrasi dilakukan terhadap peralatan yang digunakan untuk menimbang, mengukur, dan menguji. Sertifikat Penerimaan dikeluarkan untuk mesin yang telah melewati tahapan-tahapan tersebut dan menyatakan bahwa mesin tersebut telah memenuhi syarat.
Pemeliharaan peralatan menjadi tanggung jawab Departemen Produksi dan Departemen Teknik, yaitu Bagian Perencanaan Perawatan. Bagian ini melakukan perawatan pencegahan yang meliputi pengecekan, penggantian bagian-bagian dari mesin yang rusak, pembersihan, dan lubrikasi mesin secara periodik. Kegiatan perawatan dan pencegahan dilakukan dengan mempertimbangkan jadwal produksi sehingga tidak mengganggu jalannya proses produksi. Umumnya kegiatan ini dilakukan setiap bulan.
PT. Kalbe Farma, Tbk. memiliki ± 2200 peralatan dan mesin untuk keperluan produksi, sarana pendukung, maupun sarana In Process Control (IPC) di laboratorium. Beberapa mesin yang dimiliki PT. Kalbe Farma, Tbk. misalnya : Turbo Mixer Heidolph RZR 2051 Control; mesin granulasi Diosna P400; mesin pengeringan FBDT-6 NIRO & Haag; mesin pengayakan Quadro Comill dan Ronchi; pencampur massa Zanchetta; mesin cetak Fette, Killian RX 45; mesin blistering Uhlmann UPS 1070 dan Medik-55; mesin stripping Siebler Type 90. Sedangkan beberapa contoh peralatannya, yaitu timbangan analitik Sauter Type 414; alat pengukur disolusi Hanson-72; alat pengukur RH ruangan „Slinger ; alat penangas air Memmert W-350; mikroskop Leitz- Dialux-‟ 20.
e. Sanitasi dan Higiene
Tingkat sanitasi dan higiene yang tinggi harus dijaga pada setiap aspek pembuatan obat. Ruang lingkup sanitasi dan higiene, meliputi personalia, bangunan, peralatan dan perlengkapan, bahan produksi serta wadahnya, dan hal- hal lainnya yang dapat menjadi sumber pencemaran produk. Oleh karena itu, diperlukan suatu program sanitasi dan higiene yang menyeluruh dan terpadu. Prosedur sanitasi dan hygiene harus divalidasi, serta dievaluasi secara berkala untuk selalu memastikan bahwa hasilnya efektif dan memenuhi persyaratan.
Setiap personil PT. Kalbe Farma, Tbk. harus menjalani pemeriksaan kesehatan, baik sebelum diterima menjadi karyawan
maupun selama bekerja. Karyawan yang bertugas sebagai pemeriksa visual diharuskan menjalani pemeriksaan mata secara berkala untuk memastikan fungsi mata masih bekerja secara optimal. Tiap karyawan yang mengidap suatu penyakit yang dapat merugikan kualitas produk dilarang menangani bahan baku, bahan pengemas, bahan yang sedang dalam proses, dan obat jadi sampai karyawan tersebut dinyatakan telah sembuh.
Setiap personil tidak diperbolehkan makan dan merokok di dalam gedung produksi maupun kantor, khususnya di daerah yang berhubungan dengan produk, seperti daerah produksi dan gudang. Toilet, tempat cuci tangan, kotak P3K, dan ruang minum (pantry) yang terpisah dari ruang kerja dan ruang produksi. Hal ini merupakan salah satu bentuk sarana penunjang pelaksanaan sanitasi dan higiene. Kantin dan koperasi ditempatkan dalam lokasi yang strategis, namun tidak berhubungan langsung dengan kantor maupun area produksi.
Pada setiap grey area bagian produksi terdapat ruang pencucian untuk mencuci alat-alat yang telah selesai digunakan untuk proses produksi. Sanitasi line 5 dilakukan setialat kan digunakan. Sanitasi ruangan line 5 di fogging 1 bulan sekali. Peralatan line 6 ada yang disterilisasi, tidak hanya sanitasi. Sanitasi ruangan di line 6 dilakukan 24 jam sekali dengan cara fogging selama 4 jam. Sanitasi peralatan dilakukan setiap terjadi pergantian jenis produk. Pembersihan rutin juga dilakukan pada alat yang sudah lama tidak digunakan. Peralatan yang dapat dipindahkan dicuci di ruang pencucian pada grey area, sedangkan peralatan yang tidak dapat dipindahkan dicuci di ruangan tempat peralatan tersebut berada. Ruangan tersebut telah dilengkapi dengan saluran khusus untuk pembuangan limbah dari pencucian alat. Pembersihan alat dan mesin tersebut dilakukan berdasarkan prosedur tetap yang telah ditetapkan oleh Pemastian Mutu.
Semua ruang di line produksi memiliki status tertentu yang diwujudkan dalam bentuk tulisan yang ditempelkan pada pintu
ruangan, meliputi label ”TELAH DIBERSIHKAN”, ”SEDANG PROSES”, atau ”UNTUK DIBERSIHKAN”. Hanya ruang dengan label ”TELAH DIBERSIHKAN” yang dapat digunakan untuk proses produksi. Sedangkan, label untuk alat/mesin meliputi label ”SIAP PAKAI”, ”SEDANG PROSES”, ”UNTUK DIBERSIHKAN”, atau ”SEDANG RUSAK”. Hanya alat berlabel ”SIAP PAKAI” saja yang dapat digunakan untuk proses produksi.
Pada black area pakaian yang digunakan terdiri dari baju dan celana berwarna putih yang dilengkapi dengan penutup kepala dan sandal karet. Untuk masuk ke grey area ataupun white area, karyawan melalui ruang penyangga di mana tekanan udara di ruang buffer lebih kecil daripada ruang produksi sehingga mencegah adanya kontaminasi. Perlengkapan yang digunakan selama berada di grey area berupa baju terusan yang dilengkapi dengan penutup kepala yang dirangkap pada baju black area, masker, dan sepatu khusus dengan bagian depan tertutup atau menggunakan penutup sepatu (shoes cover). Sarung tangan digunakan jika bersentuhan langsung dengan produk, sedangkan penutup telinga digunakan untuk operator yang bekerja dengan mesin-mesin yang mengeluarkan bunyi bising. Khusus grey area pada line 6 baju terusan yang digunakan berwarna merah muda, sedangkan pada line lainnya berwarna putih. Pada white area, personel yang diperbolehkan masuk ke ruangan white area hanyalah personel yang telah terkualifikasi. Personal yang akan masuk ke white area harus mengganti baju grey area dengan baju white area dengan baju terusan bebas serat dengan penutup kepala, sarung tangan, masker, penutup mata, dan sepatu khusus. Pakaian kotor di simpan terpisah dalam wadah tertutup dan di cuci secara berkala dua kali dalam seminggu. Peraturan ini berlaku untuk semua orang, termasuk pimpinan dan tamu pabrik.
Departemen Produksi bertanggung jawab untuk memproduksi produk sesuai dengan target dan JPB (Jadwal Produksi Bulanan) yang ditetapkan bersama dengan Departemen Perencanaan Produksi dan Pengendalian Persediaan. Proses produksi dilaksanakan berdasarkan Prosedur Pengolahan Induk (PPI) yang disusun oleh R&D dan Process Development dan dikeluarkan oleh Departemen Perencanaan Produksi dan Pengendalian Persediaan. Formula dan proses yang digunakan telah tervalidasi melalui beberapa tahap, seperti percobaan pada skala laboratorium dan produksi, pravalidasi, dan validasi. Penggunaan PPI bertujuan untuk memberikan jaminan bahwa produk senantiasa dibuat melalui prosedur yang tetap dan tervalidasi sehingga kualitas produk selalu terjaga. Selain itu, penggunaan PPI juga ditujukan untuk memudahkan penelusuran pada proses produksinya jika ditemukan masalah pada suatu produk. Semua proses produksi dikerjakan sesuai dengan PPI dan bila ada perubahan dalam proses dilaporkan dalam Deviation Report (DR) di dalam Catatan Produksi Bets (CPB). Untuk produk yang telah rilis, pengolahan ulang produk dilakukan melalui pengajuan Formulir Usulan Pengolahan Ulang (FUPU) dengan persetujuan dari QA.
Pencegahan terjadinya pencemaran silang dan pencampuran bahan diupayakan melalui pembagian proses produksi dalam line produksi. Proses dikerjakan dalam ruang yang terpisah sesuai dengan tahapan proses dan terdapat ruang penyangga di antara kelas yang berbeda. Setiap line produksi mempunyai ruang timbang yang terpisah. Hal ini dimaksudkan untuk mencegah pencemaran di ruang timbang. Setiap line juga dilengkapi dengan AHU, pengumpul debu, dan pengaturan tekanan dalam upaya pencegahan pencemaran, baik kimia maupun mikroba. Selain itu, terdapat persyaratan penggunaan pakaian yang berbeda-beda pada tiap kelas.
Kontrol selama proses oleh bagian produksi dilakukan untuk menjamin kualitas produk . Kontrol ini dilakukan melalui pemeriksaan
terhadap parameter- parameter kritis kualitas produk. Laboratorium kontrol selama proses terletak di setiap line produksi dan dilengkapi dengan alat penguji semua sediaan yang diproduksi. Kontrol selama proses bertujuan mendeteksi langsung penyimpangan yang terjadi sehingga solusi dapat segera diupayakan. Kontrol proses ini mengikuti Prosedur Pengolahan Induk (PPI), meliputi jenis uji yang dilakukan, banyaknya sampel yang diambil, frekuensi pengambilan sampel, titik-titik pengambilan sampel, dan batas-batas yang masih memenuhi syarat untuk setiap spesifikasi uji yang dilakukan. Pengawasan mutu produk antara dan produk jadi juga dilakukan oleh Departemen Pengawasan Mutu. Produk antara boleh di kemas hanya jika sudah dinyatakan memenuhi persyaratan dan dirilis oleh Departemen Pengawasan Mutu.
Pada proses pengemasan produk PT. Kalbe Farma, Tbk. dapat dilakukan secara manual maupun otomatis. Hal ini disesuaikan dengan mesin yang digunakan pada masing-masing line produksi. Setelah produk dikemas, kemudian dilakukan pemeriksaan oleh Bagian Penjaminan Mutu untuk menentukan apakah produk dapat dirilis atau tidak. Jika hasil pemeriksaan menunjukkan hasil bahwa produk tidak dapat dirilis, akan dilakukan tindakan lebih lanjut, baik berupa pengolahan ulang, rilis dengan perubahan spesifikasi, ataupun pemusnahan. Pengolahan ulang untuk produk yang belum dirilis bisa dilakukan bila ada pengajuan Deviation Report yang disetujui oleh Departemen Produksi, R&D, dan Pemastian Mutu. Pengolahan ulang produk yang telah rilis dilakukan melalui pengajuan Formulir Usulan Pengolahan Ulang dengan persetujuan dari Departemen Pemastian Mutu.
Produk jadi, baik yang dalam status karantina maupun rilis, disimpan di gudang obat jadi yang terhubung langsung dari ruang produksi sesuai dengan kondisi penyimpanan yang tertera pada label
klaim. Contoh pertinggal (retained sample) dan PPI dikirim ke bagian Evaluasi Catatan Bets.
Apoteker memegang peranan penting dalam proses produksi. Seorang apoteker yang menjadi manajer produksi bertanggung jawab terhadap pelaksanaan pembuatan obat. Obat dibuat sesuai Cara Pembuatan Obat yang Baik dan memenuhi spesifikasi kualitas yang ditetapkan dalam batas waktu dan biaya yang telah ditentukan. Apoteker yang menjadi supervisor produksi akan mengatur dan memastikan obat dibuat menurut prosedur pembuatan yang telah ditentukan dan sesuai jadwal; memeriksa catatan pengolahan batch telah diisi dengan benar; serta membimbing karyawan dalam bidang teknis dan mengatur ketertiban atau disiplin karyawan.
Secara umum, line-line di bagian produksi dibedakan menjadi dua, yaitu Dedicated line (line 1, 2, 4, dan 9) dan non-dedicated line / General line (line 5, 6, 7, 8A, dan 8B). Dedicated line adalah line-line yang memproduksi obat dalam jumlah item yang sedikit tetapi dengan kapasitas batch atau batch size yang besar. Sedangkan yang dimaksud dengan General line adalah line yang memproduksi obat dalam jumlah item yang relatif banyak, namun dengan kapasitas batch atau batch size yang kecil (Anonim, 2010).
a. Line 1
Line ini memproduksi 1 item produk yaitu tablet Promag® dan dipimpin oleh seorang manajer produksi dan seorang Supervisor. Gambar 10 menjelaskan proses pembuatan tablet Promag®
b. Line ini memproduksi kaplet film coating, tablet inti dan tablet hisap (misal: Neo-entrostop®, Xon-Ce®, Neuralgin RX®, dan Pronicy®). Selain itu, line 2 juga menangani pengemasan produk Medik 55®. Line ini dipimpin oleh seorang manajer dan seorang Supervisor. c. Line 4
Line ini memproduksi Procold® untuk kebutuhan lokal dan ekspor, Neuralgin OTC dan produksi Medik 55® non kemas. Line ini dipimpin oleh seorang manajer dan seorang Supervisor.
d. Line 5
Line ini memproduksi sediaan cair oral sirup dan suspensi seperti Cerebrofort® dan Woods®. Line ini dipimpin oleh seorang Supervisor.
e. Line 6
Line ini khusus memproduksi sediaan cair steril (injeksi) non β-lactam, seperti Rantin®, Ulsikur®, Kalmethasone®, dan Sterile Water for Injection. Line ini dipimpin oleh seorang manajer.
f. Line 7
Line ini memproduksi sediaan semi padat topikal seperti krim, semi solid seperti jeli, dan salep serta sediaan suppositoria dan ovula. Contoh produknya adalah Bioplacenton®, Mycoral®, dan Kaltrofen®. Line ini dipimpin oleh seorang Supervisor.
g. Line 8
Line ini banyak memproduksi item obat tetapi dengan batch size kecil. Produk yang dihasilkan merupakan produk solid ethical. Line ini dibagi menjadi 2, yaitu line 8A yang menangani proses pembuatan produk dan line 8B menangani pengemasan primer dan sekunder produk yang dihasilkan dari line 8A. Line ini dipimpin oleh dua orang manajer produksi yang masing-masing bertugas di line 8A dan line 8B dan 1 orang Supervisor.
h. Line 9
Line ini khusus memprodusi liquid non oral seperti Kalpanax tincture® dan menangani labelling finished goods. Line ini dipimpin oleh seorang Supervisor.
g. Pengawasan mutu
Pelaksanaa pengawasan mutu di PT. Kalbe Farma, Tbk. dilakukan oleh bagian Pengawasan Mutu (QC) yang berada di bawah
departemen Quality Operation (QO). Pengawasan mutu bertujuan untuk memastikan bahwa tiap obat yang dibuat senantiasa memenuhi persyaratan mutu yang sesuai dengan tujuan penggunaannya. Sesuai dengan yang tertera pada CPOB pula, bagian ini sebaiknya independen dan terpisah dari produksi.
Tugas utama bagian pengawasan Mutu adalah mengontrol kualitas dari bahan awal (bahan baku dan bahan kemas) sejak masuk ke gudang hingga menjadi produk jadi yang siap dipasarkan. Pemeriksaan di bagian Pengawasan Mutu meliputi pemeriksaan bahan baku, produk ruahan, produk jadi, dan bahan kemas. Pemeriksaan yang dilakukan berupa pemeriksaan fisik, kimia, dan mikrobiologi. Bagian ini bertanggung jawab dalam menganalisa semua bahan baku dan produk jadi menggunakan metode analisis yang telah disusun oleh bagian Analytical Development, departemen R&D. Selain itu, bagian Pengawasan Mutu juga melakukan pemeriksaan bahan kemas dan wadah menggunakan metode analisis tertentu yang ditetapkan oleh bagian Packaging Development.
Kalibrasi peralatan dan validasi metode analisis dilakukan sesuai jadwal untuk menjamin agar peralatan dan metode analisa yang digunakan memberikan hasil pengukuran yang tepat. Peralatan yang digunakan untuk analisis selalu dalam keadaan terkalibrasi. Jika ada alat yang belum dikalibrasi, alat tersebut tidak boleh digunakan. Pada setiap alat ditempel label yang menandakan kondisi alat, tanggal kalibrasi terakhir, dan tanggal kalibrasi selanjutnya. Dengan adanya label tersebut, dapat dicegah penggunaan alat yang tidak terkalibrasi. Prosedur Tetap (protap) disediakan untuk semua alat di Laboratorium Pengawasan Mutu dan diletakkan di dekat alat untuk memudahkan operator atau personel lain dalam menggunakan alat yang bersangkutan.
Alat pelindung diri (APD) disediakan untuk keselamatan personil, seperti masker, kaca mata pelindung, sarung tangan, dan pembasuh
mata. Baku pembanding disimpan dalam kondisi yang sesuai. Pada wadahnya terdapat label informasi mengenai nama zat, nama penyalur, kadar, tanggal bahan datang, dan jenis stok. Hal ini telah sesuai dengan aturan CPOB.
Ruang laboratorium untuk pemeriksaan di bagian Pengawasan Mutu telah sesuai dengan aturan CPOB, seperti persyaratan spesifikasi ruangan, desain ruangan, dan tempat pembuangan limbah. Laboratorium memiliki letak yang terpisah dengan ruang produksi. Ruang laboratorium mikrobiologi juga terpisah dari ruang laboratorium lainnya. Pada laboratorium ini disediakan peralatan yang ditujukan untuk pengujian mutu obat.
h. Inspeksi Diri, Audit Mutu, dan Audit Persetujuan Pemasok
Untuk menilai kesesuaian seluruh aspek produksi dan pengendalian mutu dalam industri farmasi dengan ketentuan CPOB serta mengevaluasi dan menentukan tindakan apa yang harus diambil sebagai langkah korektif jika terjadi suatu penyimpangan, maka diperlukan adanya langkah mandiri dari industri tersebut, yaitu dengan melaksanakan inspeksi diri dan audit mutu. CPOB mensyaratkan agar kegiatan ini dilakukan secara teratur.
PT. Kalbe Farma, Tbk. telah melaksanakan program inspeksi diri melalui Departemen Pemastian Mutu. Inspeksi tersebut mencakup kesesuaian dengan sistem atau regulasi yang berlaku dan penilaian aspek produksi melalui inspeksi proses yang dilakukan secara berkala. Pelaksanaan inspeksi diri di PT. Kalbe Farma, Tbk. diwujudkan dalam bentuk audit internal yang dilakukan secara rutin. Audit internal dilakukan dua kali dalam setahun oleh suatu tim internal PT. Kalbe Farma, Tbk. yang telah terlatih dan tersertifikasi. Pelaporannya meliputi hasil audit, penilaian dan kesimpulan, serta usulan tindakan perbaikan. Berdasarkan laporan audit, manajemen perusahaan akan mengevaluasi dan mengambil tindakan perbaikan yang diperlukan.