i
LAPORAN AKHIR TAHUN
PENELITIAN STRATEGI NASIONAL INSTITUSI
MINI LABORATORIUM IPAL SEBAGAI PROTOTIPE PADA
PENGOLAHAN LIMBAH LABORATORIUM KIMIA SEBAGAI
UPAYA PADA PELESTARIAN LINGKUNGAN
Tahun ke - 2 dari rencana 3 tahun
Dr. Nuniek Herdyastuti, M.Si (NIDN 0010117004) Prof. Dr. Sari Edi Cahyaningrum, M.Si (NIDN 0029127002)
Rusmini, M.Si (NIDN 0012067905)
UNIVERSITAS NEGERI SURABAYA
NOPEMBER – 2018
iii Ringkasan
Laboratorium disebutkan sebagai salah satu sumber penghasil limbah baik padat, gas atau cair. Limbah merupakan buangan bahan kimia yang telah dipakai, bahan baku kedaluarsa, atau produk proses di laboratorium seperti sisa spesimen. Limbah organik atau anorganik dengan konsentrasi dan kualitas tertentu dapat berdampak negatif terhadap lingkungan terutama bagi kesehatan manusia sehingga perlu dilakukan penanganan terhadap limbah. Intensitas kegiatan laboratorium di Jurusan Kimia sangat tinggi baik untuk kegiatan praktikum maupun penelitian bagi mahasiswa maupun dosen. Selama ini pembuangan sisa kegiatan praktikum belum dilakukan dengan sebagaimana mestinya dikarenakan Jurusan Kimia belum mempunyai tempat pembuangan apalagi sistem pengolahan limbah laboratorium. Limbah laboratorium yang berupa bahan organik dan anorganik (logam-logam berat) tersebut apabila terakumulasi maka dapat membahayakan lingkungan di sekitar Jurusan Kimia seperti tanah, air dan tanaman. Tanah yang ada disekitar Jurusan Kimia selama ini merupakan lahan terbuka yang ditanami dengan beraneka tanaman hias atau tanaman yang dapat dikonsumsi seperti buah dan sayur. Seperti diketahui bahwa FMIPA telah mencanangkan diri sebagai kampus konservasi, yang berarti FMIPA sangat peduli dan berupaya pada perlindungan dan pengelolaan terhadap lingkungan dan sumber daya alam.
Berdasarkan kenyataan tersebut maka perlu dilakukan penanganan terhadap pengolahan limbah sehingga dapat mengurangi pencemaran serta dapat menjaga kelestarian lingkungan sekitar. Penelitian ini direncanakan selama tiga tahun, pada Tahun – 1 dilakukan untuk mengetahui distribusi dampak cemaran limbah laboratorium pada tanah, air dan tanaman yang ada di sekitar Jurusan Kimia. Selanjutnya pada Tahun – 2 akan dilakukan pengolahan hasil pembuangan laboratorium melalui treatment adsorbsi pada skala laboratorium. Pada Tahun – 3 akan dibuat suatu prototipe yang akan digunakan untuk uji limbah dengan cara adsorbsi dan hasil pengolahan limbah akan dianalisis sebagai buangan yang bersih sehingga ke depan dapat digunakan untuk kepentingan biota yang ada di sekitarnya. Penanganan limbah dilakukan dengan memisahkan limbah organik dan anorganik dan dilakukan treatment dengan menggunakan adsorben. Pada Tahun – 2 ini limbah yang dianalisis adalah logam yang sangat dominan di dalam buangan yaitu Cu dan Pb serta dilakukan optimasi untuk menentukan kondisi optimum meliputi massa adsorben dan waktu interaksi adsorben dan logam. Dibuat sebuah rancangan prototipe inkubator dalam bentuk gambar yang siap untuk digunakan pada Tahun – 3.
Diharapkan dari penelitian Tahun – 2 ini akan diketahui jenis adsorben terbaik yang dapat digunakan untuk menangani limbah di laboratorium, mendapatkan kondisi optimum serta membuat suatu rancangan prototipe untuk pengolahan limbah skala laboratorium . Penelitian ini mempunyai kontribusi dengan memberikan masukan kepada pimpinan di FMIPA maupun Unesa tentang penggunaan laboratorium dan arti penting penanganan limbah baik yang ada di jurusan Kimia maupun di jurusan lain yang berkaitan dengan laboratorium.
iv PRAKATA
Dengan mengucap syukur kehadlirat Allah s.w.t, atas segala Rahmad dan Kemurahan-Nya penulis dapat menyeleaikan penelitian dengan laporan akhir yang berjudul “Mini laboratorium IPAL sebagai prototipe pada pengolahan limbah laboratorium kimia sebagai upaya pada pelestarian lingkungan”. Penelitian ini dibagi dalam tiga tahapan, yaitu pada tahap pertama (Tahun – 1) dilakukan untuk mengetahui analisis cemaran logam dan non logam laboratorium dominan yang berbahaya yang ditimbulkan dari sisa bungan kegiatan praktikum di laboratorium Jurusan Kimia. Selanjutnya pada Tahun – 2 akan dilakukan pengolahan hasil pembuangan laboratorium melalui metode adsorbsi serta mencari kondisi optimum untuk pengolahan limbah. Pada Tahun – 3 akan dilakukan pembuatan prototipe inkubator untuk melakukan treatment adsorbsi pada skala laboratorium.
Penelitian ini memperoleh dana dari Proyek Peningkatan Kualitas Sumber Daya Manusia Direktorat Pembinaan Penelitian Dan Pengabdian Kepada Masyarakat Kementerian Riset, Teknologi dan Pendidikan Tinggi Tahun Anggaran 2017 melalui program penelitian Strategis Nasional Institusi. Untuk itu kami mengucapkan terima kasih kepada : Ketua DRPM, Rektor UNESA, Ketua Lembaga Penelitian dan Pengabdian UNESA, Ketua Jurusan Kimia UNESA, serta rekan-rekan laboran di laboratorium Jurusan Kimia yang telah membantu penelitian ini. Harapan kami semoga penelitian ini dapat membawa manfaat bagi peneliti sendiri khususnya dan dapat memberikan informasi bagi rekan-rekan peneliti lainnya.
Surabaya, Nopember 2018
v DAFTAR ISI Halaman HALAMAN JUDUL i LEMBAR PENGESAHAN ... ii RINGKASAN ... iii PRAKATA ... iv DAFTAR ISI ... v DAFTAR TABEL ... vi
DAFTAR GAMBAR ... vii
DAFTAR LAMPIRAN ... viii
BAB I PENDAHULUAN ... 1
1.1 Latar Belakang ... 1
1.2 Rumusan Masalah ... 2
BAB II TINJAUAN PUSTAKA ... 4
2.1 Pengertian limbah laboratorium ... 4
2.2 Macam-macam limbah laboratorium ... 4
2.3 Cemaran logam berbahaya ... 6
2.4 Cara pengolahan limbah laboratorium ... 21
2.5 Langkah-langkah mengurangi limbah laboratorium ... 27
BAB III TUJUAN DAN MANFAAT PENELITIAN ... 30
BAB IV METODE PENELITIAN BAB V HASIL DAN PEMBAHASAN 5.1 Identifikasi limbah di laboratorium 5.2 Senyawa logam-logam berat sisa pembuangan kegiatan praktikum 5.3 Senyawa non logam sisa pembuangan kegiatan praktikum 5.4 Akibat yang ditimbulkan dari pembuangan laboratorium BAB VI RENCANA TAHAPAN SELANJUTNYA ... ... ... ... ... ... ... 31 35 34 36 47 50 54 BAB VII SIMPULAN DAN SARAN ... 55
DAFTAR PUSTAKA ... 56
1 BAB I
PENDAHULUAN
1.1 Latar Belakang
Jurusan Kimia merupakan salah satu jurusan yang ada di Fakultas Matematika dan Ilmu Pengetahuan Alam Universitas Negeri Surabaya. Hampir semua jurusan Kimia yang ada dimanapun selalu identik dengan keberadaan laboratorium didalamnya. Hal ini dikarenakan beberapa mata kuliah Kimia tidak dapat hanya dijelaskan secara teoritis tetapi harus dilakukan secara praktis di dalam laboratorium. Selain itu pada kegiatan praktek di laboratorium dapat memberikan keterampilan motorik dan memberikan nilai lebih bagi lulusan Kimia. Untuk menunjang kegiatan praktek di laboratorium tersebut Jurusan Kimia FMIPA – UNESA menyediakan sembilan laboratorium, yaitu : laboratorium Kimia Dasar, Kimia Sekolah, Kimia Fisika, Kimia Analitik, Anorganik, Komputasi, Organik, Biokimia dan Instrumen.
Laboratorium disebutkan sebagai salah satu sumber penghasil limbah baik padat, gas atau cair. Limbah merupakan buangan bahan kimia yang telah dipakai, bahan baku kedaluarsa, atau produk proses di laboratorium seperti sisa spesimen. Limbah organik atau anorganik dengan konsentrasi dan kualitas tertentu dapat berdampak negatif terhadap lingkungan terutama bagi kesehatan manusia sehingga perlu dilakukan penanganan terhadap limbah. Intensitas kegiatan laboratorium di Jurusan Kimia sangat tinggi baik untuk kegiatan praktikum maupun penelitian bagi mahasiswa maupun dosen. Selama ini pembuangan sisa kegiatan praktikum belum dilakukan dengan sebagaimana mestinya dikarenakan Jurusan Kimia belum mempunyai tempat pembuangan apalagi sistem pengolahan limbah laboratorium. Hal ini kemungkinan tidak hanya terjadi di Jurusan kimia tetapi juga di jurusan lainnya yang sangat rentan dengan pembuangan limbah laboratorium.
Berdasarkan hasil penelitian pada Tahun - 1 telah diperoleh data bahwa banyak logam-logam berat yang berbahaya seperti Ag, Cd, Cr, Cu, Pb, Mg, Fe, dan Hg yang ditemukan pada sisa pembuangan kegiatan laboratorium. Beberapa pelarut organik yang bearacun seperti metanol, asetaldehid, fenilhidrazin dan fenol juga ditemukan dalam konsentrasi yang cukup tinggi. Berdasarkan hasil penelitian yang telah dilakukan tersebut maka perlu dilakukan penanganan terhadap pengolahan limbah sehingga dapat mengurangi pencemaran serta dapat menjaga kelestarian lingkungan sekitar. Keberadaan logam dapat dikurangi dengan menambahkan adsorben seperti karbon aktif atau bentonit. Bentonit dalam ilmu mineralogi tergolong ke dalam kelompok besar tanah lempung,
2 merupakan batu yang terbentuk dari abu vulkanik dan mengandung mineral montmorillonit. Ada dua jenis batu bentonite yaitu Bentonit Na dan Bentonit Ca yang masing-masing memiliki fungsi yang berbeda. Selain bentonite juga dapat digunakan arang aktif. Dalam proses penjernihan air, arang aktif selain mengadsorpsi logam-logam seperti besi, tembaga. nikel, juga dapat menghilangkan bau, warna dan rasa yang terdapat dalam larutan atau buangan air. Di beberapa negara arang aktif dilaporkan telah digunakan sebagai penyerap residu pestisida pada proses penjernihan air untuk mendapatkan air minum yang bebas pestisida (Gerard dan Barthelemy, 2003 dalam Gani, 2007). Bentonit dan arang aktif merupakan adsorben yang banyak digunakan karena mudah diperoleh dan harganya tidak mahal. Beberapa metode lain juga telah dilakukan untuk melakukan adsorbsi logam berat, seperti yang dilakukan oleh Deng, et al (2017) dengan menggunakan membran karboksimetil kitosan dan silikon dioksida yang mampu menyerap Cr (VI). Yasemin and Zeki (2006) mengatakan bahwa sawdust of walnut merupakan adsoben yang baik bagi ion-ion logam dalam cairan. Senyawa turunan lignin juga mampu mengadsorpsi logam berat seperti Pb2+ , Cd2+ , Hg2+, Ni2+ dan Cu2+ (Liu et al, 2013 and Berrima et al. 2016). Untuk mendapatkan kondisi yang terbaik maka perlu dilakukan optimasi baik terhadap pemilihan adsorben, pengukuran terhadap suhu, pH dan massa adosorben yang digunakan.
Pada Tahun – 2 akan dilakukan pengolahan hasil pembuangan laboratorium melalui treatment adsorbsi pada skala laboratorium dengan menggunakan dua adsorben yaitu bentonit dan karbon aktif. Untuk memperoleh hasil yang diharapkan maka akan dilakukan optimasi terhadap adsorben dan limbah yang digunakan serta waktu interaksi antara limbah dengan adsorben. Hasil tersebut diharapkan dapat dimanfaatkan untuk penerapan pada tahun ketiga dengan menggunakan prototipe yang telah dirancang.
Penelitian yang direncanakan dalam waktu tiga tahun dilakukan sebagai upaya untuk mengatasi permasalahan limbah sebagai hasil samping kegiatan praktikum dan penelitian di laboratorium kimia FMIPA – UNESA. Penanganan limbah yang dilakukan dengan memisahkan limbah organik dan anorganik dan dilakukan treatment dengan menggunakan adsorben diharapkan dapat mengatasi persoalan pembuangan limbah yang ada di laboratorium Kimia.
1.2 Permasalahan yang diangkat pada penelitian ini adalah :
3 a. Berapakah kondisi optimum yang diperoleh meliputi massa adorben, waktu
interaksi adsorben dan limbah serta konsentrasi limbah.
b. Berapakah kapasitas adsorbsi yang diperoleh dan bagaimana karakteristik adsorben meliputi analisis gugus fungsi, morfologi dan ukuran pori adsorben. c. Bagaimana kemampuan atau efektifitas adorben terhadap pengolahan limbah
4 BAB II
TINJAUAN PUSTAKA
2.1 Pengertian limbah laboratorium
Limbah adalah buangan yang dihasilkan dari suatu proses produksi baik industri maupun domestik (rumah tangga) yang kehadirannya pada suatu saat dan tempat tertentu tidak dikehendaki lingkungannya karena tidak mempunyai nilai ekonomi. Limbah mengandung bahan pencemar yang bersifat racun dan bahaya yang dikenal dengan limbah B3 (bahan beracun dan berbahaya). Limbah Laboratorium adalah buangan yang berasal dari laboratorium, dalam hal ini khususnya adalah laboratorium kimia. Limbah ini dapat berasal dari bahan kimia, peralatan untuk pekerjaan laboratorium dan lain-lain. Limbah laboratorium ini mempunyai resiko berbahaya bagi lingkungan dan mahluk hidup. Bila ditinjau secara kimiawi,limbah ini terdiri dari bahan kimia senyawa organik dan senyawa anorganik.
Tingkat bahaya keracunan yang ditimbulkan oleh limbah tergantung pada jenis dan karakteristik limbah. Karakterist ik limba h dipengaruhi oleh ukuran partikel (mikro), sifatnya dinamis, penyebarannya luas dan berdampak panjang atau lama. Sedangkan kualit as limbah dipengaruhi o leh vo lu me limbah, kandungan bahan pencemar dan frekuensi pembuangan limbah.
Sebagai limbah kehadirannya cukup mengkhawatirkan terutama yang bersumber dari laboratorium kimia dikarenakan bahan beracun dan berbahaya banyak digunakan di laboratorium kimia. Beracun dan berbahaya dari limbah ditunjukkan oleh sifat fisik dan kimia bahan itu sendiri, baik dari jumlah maupun kualitasnya. Beberapa kriteria berbahaya dan beracun telah ditetapkan antara lain mudah terbakar, mudah meledak, korosif, oksidator dan reduktor, iritasi bukan radioaktif, mutagenik, patogenik, mudah membusuk dan lain-lain. Dalam jumlah tertentu dengan kadar tertentu, kehadirannya dapat merusakkan kesehatan bahkan mematikan manusia atau kehidupan lainnya sehingga perlu ditetapkan batas-batas yang diperkenankan dalam lingkungan pada waktu tertentu.
2.2 Macam-macam limbah laboratorium
Berdasarkan wujudnya limbah dibagi menjadi 3 bagian yaitu: 1. Limbah padat
Limbah padat adalah hasil buangan laboratorium berupa padatan, lumpur, bubur yang berasal dari sisa kegiatan laboratorium.
5 2. Limbah cair
Limbah cair adalah sisa dari suatu hasil usaha atau kegiatan yang berwujud cair. Jenis-jenis limbah cair dapat digolongkan berdasarkan pada:
a. Sifat Fisika dan Sifat Agregat
Keasaman sebagai salah satu contoh sifat limbah dapat diukur dengan menggunakan metoda Titrimetrik
b. Parameter Logam, contohnya Arsenik (As) dengan metoda SSA
c. Anorganik non Metalik contohnya Amonia (NH3-N) dengan metoda Biru Indofenol d. Organik Agregat contohnya Biological Oxygen Demand (BOD)
e. Mikroorganisme contohnya E Coli dengan metoda MPN
Sifat Khusus contohnya Asam Borat (H3BO3) dengan metoda Titrimetrik f. Air Laut contohnya Tembaga (Cu) dengan metoda SPR-IDA-SSA 3. Limbah gas
Polusi udara adalah tercemarnya udara oleh berberapa partikulat zat (limbah) yang mengandung partikel (asap dan jelaga), hidrokarbon, sulfur dioksida, nitrogen oksida, ozon (asap kabut fotokimiawi), karbon monoksida dan timah.
Secara alamiah udara mengandung unsur kimia seperti O2, N2, NO2, CO2, H2 dan lain-lain. Penambahan gas ke dalam udara melampaui kandungan alami akibat kegiatan manusia akan menurunkan kualitas udara. Zat pencemar melalui udara diklasifikasikan menjadi dua bagian yaitu partikel dan gas.
Ada pula limbah yang disebut dengan limbah B3 (Bahan Berbahaya dan Beracun). Suatu limbah digolongkan sebagai limbah B3 bila mengandung bahan berbahaya atau beracun yang sifat dan konsentrasinya, baik langsung maupun tidak langsung, dapat merusak atau mencemarkan lingkungan hidup atau membahayakan kesehatan manusia. Yang termasuk limbah B3 antara lain adalah bahan baku yang berbahaya dan beracun yang tidak digunakan lagi karena rusak, sisa kemasan, tumpahan, sisa proses, dan oli bekas kapal yang memerlukan penanganan dan pengolahan khusus. Macam-macam limbah B3 diantaranya adalah : (1) Limbah mudah meledak, (2) limbah mudah terbakar, (3) limbah reaktif, (4) limbah beracun, (5) limbah penyebab infeksi dan (6) limbah yang bersifat korosif
6 2.3 Cemaran Logam Berbahaya
A. Perak
Logam perak (Ag) mempunyai sifat yang mengkilap, sangat mudah dibentuk dan ditempa, memiliki daya hantar listrik dan panas yang tinggi, serta tahan terhadap korosi. Oleh karena itu, logam perak banyak digunakan secara luas sebagai bahan konduktor listrik dan panas, serta sebagai perhiasan. Selain itu logam perak juga bersifat fotosensitif (peka terhadap cahaya) sehingga sering dipakai sebagai bahan dalam proses fotografi, baik fotografi hitam putih maupun proses radiologi rumah sakit. Dalam proses fotografi unsur Ag sebagai garam AgBr diemulsikan dalam gelatin yang digunakan pada pembuatan film. Film dibuat dengan cara melapiskan emulsi tersebut pada plastik atau kertas sehingga terbentuk kristal AgBr. Film kristal AgBr di dalam kamera jika dikenai sinar maka akan membentuk gambar. Gambar atau bayangan ini harus diubah menjadi gambar yang terlihat dengan mencelupkan film ke dalam larutan pengembang. Bagian film yang tak terkena sinar dapat membentuk bayangan hitam sehingga harus dihilangkan untuk mendapatkan gambar yang bagus. Agar dalam proses penghilangan ini tidak melarutkan AgBr yang telah membentuk bayangan, maka bayangan tersebut harus diikat terlebih dahulu menjadi gambar yang permanen (fixed) dengan cara melekatkan Ag pada film melalui proses fixing. Fixing merupakan tahapan dalam proses fotografi dimana perak akan dipindahkan dari film ke dalam larutan pencuci yaitu larutan Na2S2O3 yang terbentuk sebagai kompleks [Ag(S2O3)23-]. Senyawa kompleks tersebut akan terbuang bersama air pencucian menjadi air limbah (Shereve, 1967). Limbah yang mengandung perak sangat berbahaya bila langsung dibuang ke lingkungan. Perak selain termasuk logam berat, juga merupakan logam beracun yang dapat menimbulkan gangguan kesehatan manusia. Urutan toksisitas Ag adalah sebagai berikut : Hg2+ > Cd2+ > Ag+ > Ni2+ > Pb2+ > As3+ > Cr2+ > Sn2+ > Zn2+ (Darmono, 2001). Pencemaran lingkungan oleh ion Ag(I) menyebabkannya masuk ke dalam rantai makanan, kemudian apabila manusia mengkonsumsi makanan yang telah terkontaminasi ion Ag(I) maka akan terjadi akumulasi Ag dalam tubuh. Akumulasi perak pada tubuh manusia dapat mengakibatkan pigmentis yang disebut Argyria. Mengingat bahaya yang ditimbulkanya maka batas maksimum untuk perak yang diperbolehkan dalam air limbah sangat kecil. Berdasarkan Peraturan Menteri Energi dan Sumber Daya Mineral Republik Indonesia No.45 tahun 2006 tentang baku mutu TCLP (Toxicity Characteristic Leaching Prosedure) pencemar dalam limbah untuk penentuan karakteristik sifat racun, kandungan perak (Ag) yang diperbolehkan sebesar 5,0 mg/L (Anonim,2006). Mengingat rendahnya batas tersebut maka penanganan terhadap limbah perak untuk menghilangkan
7 atau menurunkan konsentrasi perak harus dilakukan sehingga memenuhi syarat untuk dibuang ke lingkungan. Karena logam perak merupakan logam yang bernilai ekonomis tinggi, maka pengolahan limbah yang mengandung perak sebaiknya menggunakan metode yang dapat menghilangkan logam Ag sekaligus dapat mengubahnya menjadi logam perak murni yang dapat digunakan untuk berbagai keperluan. Beberapa metode penanganan limbah perak (Ag) yang telah dikenal antara lain elektrolisis, pengendapan kimia, adsorpsi dan fotoreduksi. Metode elektrolisis untuk pengambilan perak dari limbah pencuci film melalui metode pengendapan elektrolitik, menunjukkan hasil yang efektif, praktis, dan memberikan hasil dengan kemurnian tinggi, tetapi prosesnya relatif mahal. Metode pengendapan juga cukup efektif, namun memerlukan pereaksi kimia yang mahal, dan dapat menyebabkan pencemaran lanjutan. Metode penanganan ion Ag yang lain adalah adsorpsi. Metode ini selain sederhana dan murah juga efektif, tetapi adsorben yang telah jenuh dengan ion logam dapat menjadi limbah padat yang juga berbahaya.
B. Timbal
Karakteristik dan Sifat Timbal
Timbal (Pb) merupakan salah satu jenis logam berat yang sering juga disebut dengan istilah timah hitam. Timbal memiliki titik lebur yang rendah, mudah dibentuk, memiliki sifat kimia yang aktif sehingga biasa digunakan untuk melapisi logam agar tidak timbul perkaratan. Timbal adalah logam yang lunak berwarna abu-abu kebiruan mengkilat dan memiliki bilangan oksidasi +2 (Sunarya, 2007).
8 Timbal mempunyai nomor atom 82 dengan berat atom 207,20. Titik leleh timbale adalah 1740 C dan memiliki massa jenis 11,34 g/cm3 (Widowati, 2008). Palar (2008) mengungkapkan bahwa logam Pb pada suhu 500-600 C dapat menguap dan membentuk oksigen di udara dalam bentuk timbal oksida (PbO). Beberapa sifat fisika yang dimiliki timbal ditunjukkan seperti pada Tabel 2.1
Tabel 2.1 Sifat-sifat fisika Timbal (Pb)
Sifat Fisika Timbal Keterangan
Nomor atom 82
Densitas (g/cm3) 11,34
Titik lebur (C) 327,46
Titik didih (C) 1.749
Kalor peleburan (kJ/mol) 4,77
Kalor penguapan (kJ/mol) 179,5
Kapasitas pada 25C (J/mol.K) 26,65 Konduktivitas termal pada 300K (W/m K) 35,5 Ekspansi termal 25C (µm/ m K) 28,9
Kekerasan (skala Brinell=Mpa) 38,6
Timbal merupakan salah satu logam berat yang sangat berbahaya bagi makhluk hidup karena bersifat karsinogenik, dapat menyebabkan mutasi, terurai dalam jangka waktu lama dan toksisistasnya tidak berubah (Brass & Strauss, 1981). Pb dapat mencemari udara, air, tanah, tumbuhan, hewan, bahkan manusia. Masuknya Pb ke tubuh manusia dapat melalui makanan dari tumbuhan yang biasa dikonsumsi manusia seperti padi, teh dan sayur-sayuran. Logam Pb terdapat di perairan baik secara alamiah maupun sebagai dampak dari aktivitas manusia. Logam ini masuk ke perairan melalui pengkristalan Pb di udara dengan bantuan air hujan. Selain itu, proses korofikasi dari batuan mineral juga merupakan salah satu jalur masuknya sumber Pb ke perairan (Palar, 1994). Timbal secara alami terdapat sebagai timbal sulfida, timbal karbonat, timbal sulfat dan timbal klorofosfat (Faust & Aly, 1981). Kandungan Pb dari beberapa batuan kerak bumi sangat beragam. Batuan eruptif seperti granit dan riolit memiliki kandungan Pb kurang lebih 200 ppm. Timbal (Pb) merupakan logam yang bersifat neurotoksin yang dapat masuk dan terakumulasi dalam tubuh manusia ataupun hewan, sehingga bahayanya terhadap tubuh semakin meningkat (Kusnoputranto, 2006). Menurut Underwood dan Shuttle (1999), Pb biasanya dianggap sebagai racun yang bersifat akumulatif dan akumulasinya tergantung levelnya. Hal itu
9 menunjukkan bahwa terdapat pengaruh pada ternak jika terdapat pada jumlah di atas batas ambang. Lebih lanjut Underwood dan Shuttle (1999) mencantumkan batas ambang untuk ternak unggas dalam pakannya, yaitu: batas ambang normal sebesar 1 – 10 ppm, batas ambang tinggi sebesar 20 – 200 ppm dan batas ambang toksik sebesar lebih dari 200 ppm. Timbal (Pb) menurut Lu (1995) dapat diserap dari usus dengan sistem transport aktif. Transport aktif melibatkan carrier untuk memindahkan molekul melalui membran berdasarkan perbedaan kadar atau jika molekul tersebut merupakan ion.
Pada saat terjadi perbedaan muatan transport, maka terjadi pengikatan dan membutuhkan energi untuk metabolisme (Rahde, 1991).
Toksisitas Logam Timbal
Berdasarkan toksisitasnya, logam berat digolongkan ke dalam tiga golongan, yaitu: 1. Hg, Cd, Pb, As, Cu dan Zn yang mempunyai sifat toksik yang tinggi,
2. Cr, Ni dan Co yang mempunyai sifat toksik menengah 3. Mn dan Fe yang mempunyai sifat toksik rendah (Connel and Miller, 1995)
Toksisitas logam berat sangat dipengaruhi oleh faktor fisika, kimia dan biologi lingkungan. Beberapa kasus kondisi lingkungan tersebut dapat mengubah laju absorbsi logam dan mengubah kondisi fisiologis yang mengakibatkan berbahayanya pengaruh logam. Akumulasi logam berat Pb pada tubuh manusia yang terjadi secara terus menerus dapat mengakibatkan anemia, kemandulan, penyakit ginjal, kerusakan syaraf dan kematian. Timbal dalam bentuk anorganik dan organik memiliki toksitas yang sama pada
manusia. Misalnya pada bentuk organik seperti tetraetil-timbal dan tetrametiltimbal (TEL dan TML). Timbal dalam tubuh dapat menghambat aktivitas kerja enzim. Namun yang paling berbahaya adalah toksitas timbal yang disebabkan oleh gangguan absorbsi kalsium (Ca). Hal ini menyebabkan terjadinya penarikan deposit timbal dari tulang tersebut (Darmono, 2001). Timbal adalah logam toksik yang bersifat kumulatif sehingga mekanisme toksitasnya dibedakan menurut beberapa organ yang dipengaruhinya, yaitu sebagai berikut :
a) Sistem hemopoeitik: timbal akan mengahambat sistem pembentukan hemoglobin sehingga menyebabkan anemia
b) Sistem saraf pusat dan tepi: dapat menyebabkan gangguan enselfalopati dan gejala gangguan saraf perifer
10 c) Sistem ginjal : dapat menyebabkan aminoasiduria, fostfaturia, gluksoria, nefropati,
fibrosis dan atrofi glomerular
d) Sistem gastro-intestinal: dapat menyebabkan kolik dan konstipasi
e) Sistem kardiovaskular: menyebabkan peningkatan permeabelitas kapiler pembuluh darah
f) Sistem reproduksi: dapat menyebabkan kematian janin pada wanita dan hipospermi dan teratospermia (Darmono, 2001).
g) Di perairan, timbal ditemukan dalam bentuk terlarut dan tersuspensi. Kelarutan timbal cukup rendah sehingga kadar timbal dalam air relatif sedikit. Bahan bakar yang mengandung timbal juga memberikan kontribusi yang berarti bagi keberadaan timbal dalam air (Effendi, 2003).
Timbal (Pb) Pada Tanaman
Kerusakan karena pencemaran dapat terjadi karena adanya akumulasi bahan toksik dalam tubuh tumbuhan, perubahan pH, peningkatan atau penurunan aktivitas enzim, rendahnya kandungan asam askorbat di daun, tertekannya fotosintesis, peningkatan respirasi, produksi bahan kering rendah, perubahan permeabilitas, terganggunya keseimbangan air dan penurunan kesuburannya dalam waktu yang lama. Gangguan metabolisme berkembang menjadi kerusakan kronis dengan konsekuensi tak beraturan. Tumbuhan akan berkurang produktivitasnya dan kualitas hasilnya juga rendah (Sitompul dan Guritno, 1995). Beberapa penelitian menunjukkan bahwa pencemaran mengakibatkan menurunnya pertumbuhan dan produksi tanaman serta diikuti dengan gejala yang tampak (visible symptoms). Kerusakan tanaman karena pencemaran berawal dari tingkat biokimia (gangguan proses fotosintesis, respirasi, serta biosintesis protein dan lemak), selanjutnya tingkat ultrastruktural (disorganisasi sel membran), kemudian tingkat sel (dinding sel, mesofil, pecahnya inti sel) dan diakhiri dengan terlihatnya gejala pada jaringan daun seperti klorosis dan nekrosis (Malhotra and Khan, 1984 dalam Treshow, 1989).
Menurut Lepp (1981) timbal (Pb), yang diserap oleh tanaman akan memberikan efek buruk apabila kepekatannya berlebihan. Pengaruh yang ditimbulkan antara lain dengan adanya penurunan pertumbuhan dan produktivitas tanaman serta kematian. Penurunan pertumbuhan dan produktivitas pada banyak kasus menyebabkan tanaman menjadi kerdil dan klorosis. Kepekaan logam berat pada daun memperlihatkan batas toksisitas terhadap tanaman yang berbeda-beda. Toksisitas timah hitam menyebabkan suatu mekanisme yang melibatkan klorofil. Pelepasan timah hitam ke dalam sitoplasma akan menghambat dua enzim yaitu Asam Delta Amino Levulenat Dehidratase (ALAD) dan
11 Profobilinogenase yang terlibat dalam biogenesis klorofil. Penelitian Sembiring dan Sulistyawati (2006), menunjukkan terjadi penurunan kadar klorofil pada daun Swietenia macrophylla yang terjadi bersamaan dengan peningkatan kadar Pb. Perubahan kandungan klorofil akibat meningkatnya konsentrasi Pb terkait dengan rusaknya struktur kloroplas. Pembentukan struktur kloroplas sangat dipengaruhi oleh nutrisi mineral seperti Mg dan Fe. Masuknya logam berat secara berlebihan dalam tumbuhan, misalnya logam berat Pb akan mengurangi asupan Mg dan Fe sehingga menyebabkan perubahan pada volume
dan jumlah kloroplas (Kovacs, 1992).
C. Merkuri
Merkuri (Hg) adalah logam berat berbentuk cair, berwarna putih perak, serta mudah menguap pada suhu ruangan. Merkuri (Hg) dapat larut dalam asam sulfat atau asam nitrit, tetapi tahan terhadap basa. Hg memiliki titik didih 356,6ºC. Hg mudah membentuk alloy amalgama dengan logam lainnya, seperti emas (Au), perak (Ag), platinum (Pt), dan tin (Sn). Garam merkuri yang penting antara lain HgC12 yang bersifat sangat toksik. Hg2C12 digunakan dalam bidang kesehatan, Hg(ONC)2 digunakan sebagai bahan detonator yang eksplosif, sedangkan HgS digunakan pigmen cat berwarna merah terang dan bahan antiseptik (Widowati dkk, 2008). Berbagai produk yang mengandung Hg diantaranya adalah bola lampu, penambal gigi, dan termometer. Hg di gunakan dalam kegiatan penambang emas, produksi gas klor dan soda kaustik, serta dalam industri pulp, kertas dan baterai. Merkuri dengan klor, belerang, atau oksigen akan membentuk garam yang digunakan dalam pembuatan krim pemutih dan krim antiseptik. Logam tersebut digunakan secara luas untuk mengekstrak emas (Au) dari bijihnya. Ketika Hg dicampur dengan bijih emas, Hg akan membentuk amalgama dengan emas (Au) dan perak (Ag). Amalgama tersebut harus dibakar untuk menguapkan merkuri guna menangkap dan memisahkan butir-butir emas dari butir-butir-butir-butir batuan. Hg bersifat sangat toksik sehingga penggunaan Hg dalam berbagai industri sebaiknya dikurangi, termasuk dalam industri farmasai, kedokteran gigi, industri pertanian, industri baterai, dan lampu fluorecence (Widowati et al, 2008).
Merkuri anorganik adalah logam murni yang berbentuk cair pada suhu kamar 25ºC, sehingga mudah menguap. Uap merkuri dapat menimbulkan efek samping yang sangat merugikan bagi kesehatan. Di antara sesama senyawa merkuri anorganik, uap logam merkuri (Hg), merupakan yang paling berbahaya. Ini disebabkan karena uap merkuri tidak terlihat dan sangat mudah akan terhisap seiring kegiatan pernafasan yang dilakukan (Palar, 2008). Pada saat terpapar oleh logam merkuri sekitar 80% dari logam merkuri akan terserap oleh
12 alveoli paru-paru dan jalur-jalur pernafasan untuk kemudian ditrasfer ke dalam darah. Dalam darah akan mengalami proses oksidasi, yang dilakukan oleh enzim hidrogen peroksida katalese sehingga berubah menjadi ion Hg2+. Ion merkuri ini selanjutnya dibawa ke seluruh tubuh bersama dengan peredaran darah. Logam ini juga terserap dan akan menumpuk pada ginjal dan hati. Namun demikian penumpukan yang terjadi pada organ ginjal dan hati masih dapat dikeluarkan bersama urine dan sebagian akan menumpuk pada empedu. (Palar, 2008). Contoh senyawa-senyawa merkuri organik adalah senyawa alkil-merkuri, sekitar 80% dari peristiwa keracunan merkuri bersumber dari senyawa-senyawa alkil-merkuri. Beberapa senyawa alkil-merkuri yang banyak digunakan terutama di kawasan negara negara sedang berkembang metil merkuri khlorida (CH3HgCl) dan etil khlorida (C2H5HgCl). Senyawa-senyawa tersebut di gunakan sebagai pestisida dalam bidang pertanian. Beberapa bentuk senyawa alkil-merkuri lainnya cukup banyak digunakan sebagai katalis dalam industri kimia. (Palar, 2008). Keracunan yang bersumber dari senyawa ini adalah melalui pernafasan. Peristiwa keracunan melalui jalur pernafasan tersebut lebih disebabkan karena senyawa senyawa alkil-merkuri terutama yang mempunyi rantai pendek sangat mudah menguap. Uap merkuri yang masuk bersama jalur pernapasan akan mengisi ruang-ruang dari paru-paru dan berikatan dengan darah. Di samping itu, senyawa organik merkuri lainnya seperti metil merkuri, juga merupakan penyebab keracunan merkuri yang besar, lebih dari 95% metil merkuri yang masuk ke dalam tubuh akan ditranportasi dalam sel darah merah utuk diedarkan keseluruh jaringan tubuh. Sejumlah kecil lainnya terakumulasi dalam plasma protein. Akumulasi paling tinggi ditemukan pada bagian cortex dan cerellum yaitu merupakan bagian-bagian dari organ otak. Lebih lanjut hanya sekitar 10% dari merkuri tersebut yang ditemukan dalam sel otak. (Palar, 2008).
Pencemaran Merkuri (Hg)
Sumber pencemaran Hg yaitu dari kegiatan alam dan industri. Secara almiah, pencemaran Hg berasal dari kegiatan gunung api atau rembesan air tanah yang melewati deposit Hg. Keberadaan Hg dari alam dan masuk ke suatu tatanan lingkungan tidak akan menimbulkan efek (Widowati et, al 2008). Salah satu penyebab pencemaran lingkungan oleh Hg adalah pembuangan tailing pengolahan emas yang diolah secara amalgamasi, di mana Hg mengalami perlakuan tertentu berupa putaran, tumbukan, atau gesekan, sehingga sebagian Hg akan membentuk almagam dengan logam-logam (Au, Ag, Pt) dan sebagian hilang dalam proses (Herman, 2006 dalam Widowati et al, 2008). Tersebarnya logam berat Hg di tanah, perairan ataupun udara bisa melalui berbagai jalur, seperti pembuangan
13 limbah industri secara langsung, baik limbah padat maupun limbah cair yang dibuang ke tanah, udara, dan air. Dapat di lihat pada Gambar. 2.2 proses yang terjadi bila logam berat masuk ke lingkungan laut (EPA, 1973 Destiany, 2007 dalam Yuniar, 2009).
Gambar 2.2 Proses masuknya logam berat ke lingkungan laut
Menurut Widowati et, al (2008) Logam merkuri (Hg) pada kerak bumi sebesar 0.08 mg/kg banyak tertimbun di daerah penambangan. Di alam, merkuri (Hg) ditemukan dalam bentuk unsur merkuri (Hgº), merkuri monovalen (Hg+1), dan bivalen (Hg+2). Apabila
Zat Pencemar Masuk ke ekosistem laut Dipekatkan oleh Proses Biologis Diserap oleh ikan Avertebrata Diserap oleh plankton nabati
Diserap oleh rumput laut dan tumbuhan
Plankton hewani
14 masuk ke dalam perairan, merkuri mudah berikatan dengan klor yang ada dalam air laut dan membentuk ikatan HgCl. Dalam bentuk tersebut, Hg mudah masuk ke dalam plankton dan bisa berpindah ke biota laut lain. Merkuri anorganik (HgCl) akan berubah menjadi merkuri organik metil merkuri (CH3Hg) oleh peran mikroorganisme yang terjadi pada sedimen di dasar perairan, merkuri dapat pula bersenyawa dengan karbon berbentuk senyawa organo-merkuri. Senyawa organomerkuri yang paling umum adalah metil merkuri yang dihasilkan oleh mikroorganisme dalam air dan tanah. Mikroorganisme kemudian termakan oleh ikan sehingga konsentrasi merkuri dalam ikan meningkat.
Pengaruh merkuri terhadap kesehatan manusia dapat diurai sebagai berikut: a. Pengaruh terhadap fisiologis.
Pengaruh toksisitas merkuri terutama pada Sistem Saluran Pencernaan (SSP) dan ginjal terutama akibat merkuri terakumulasi. Jangka waktu, intensitas dan jalur paparan serta bentuk merkuri sangat berpengaruh terhadap sistem yang dipengaruhi. Orgam utama yang terkena pada paparan kronik oleh elemen merkuri dan organomerkuri adalah SSP. Sedangkan garam merkuri akan berpengaruh terhadap kerusakan ginjal. Keracunan akut oleh elemen merkuri yan terhisap mempunyai efek terhadap system pernafasan sedang garam merkuri yang tertelan akan berpengaruh terhadap SSP, efek terhapap sistem cardiovaskuler merupakan efek sekunder.
b. Pengaruh terhadap sistem syaraf.
Merkuri yang berpengaruh terhadap system syaraf merupakan akibat pemajanan uap elemen merkuri dan metil merkuri karena senyawanya ini mampu menembus blood brain barrier dan dapat mengakibatkan kerusakan otak yang irreversible sehingga mengakibatkan kelumpuhan permanen. Metil merkuri yang masuk ke dalam saluran pencernaan akan memperlambat SSP yang mungkin tidak dirasakan pada pemajanan setelah beberapa bulan sebagai gejala pertama sering tidak spesifik seperti malas, pandangan kabur atau pendengaran hilang (ketulian)
c. Pengaruh terhadap ginjal.
Apabila terjadi akumulasi pada ginjal yang mengakibatkan oleh masuknya garam inorganik atau phenylmercury SSP akan menyebabkan naiknya permiabilitas epitel tubulus sehingga akan menurunkan kemampuan fungsi ginjal (disfungsi ginjal). Pajanan melalui uap merkuri atau garam merkuri melalui saluran pernafasan juga mengakibatkan kegagalan ginjal karena terjadi proteinuria atau nephrotik sindrom dan tubular nekrosis akut.
15
Terutama pad bayi dan ibu yang terpajan oleh metil merkuri dari hasil studi membuktikan ada kaitan yang signifikan bayi yang dilahirkan dari ibu yang makan gandum yang diberi fungisida, maka bayi yang dilahirkan mengalami gangguan kerusakan otak yaitu retardasi mental, tuli, penciutan lapangan pandang, microcephaly,
cerebral palsy, ataxia, buta dan gangguan menelan.
D. Kadmium
Logam Kadmium (Cd) merupakan logam yang bernomor atom 48 dan massa atom 112,41. Logam ini termasuk dalam logam transisi pada periode V dalam tabel periodik. Logam Cd dikenal sebagai unsur chalcophile, jadi cenderung ditemukan dalam deposit sulfida (Manahan, 2001). Di perairan umumnya Cd hadir dalam bentuk ion-ionnya yang terhidrasi, garam-garam klorida, terkomplekskan dengan ligan anorganik atau membentuk kompleks dengan ligan organik (Weiner,2008).
Pada umumnya di air permukaan, baik Cd terlarut maupun partikulatnya secara rutin dapat terdeteksi. Koefisien distribusi Cd partikulat/Cd terlarut pada perairan sungai di dunia berkisar dari 104 sampai 105. Fluks input antropogenik secara global per tahun jauh melebihi emisi Cd dari sumber alamiahnya seperti kegiatan gunung berapi, Windborne soil particles, garam-garam dari laut dan partikel biogenik sampai dengan satu tingkatan magnitude (Csuros and Csuros,2002). Diperkirakan 1.000 ton Cd dilepaskan per tahun ke atmosfer dari smelters dan pabrik-pabrik yang mengolah Cd. Pelepasan Cd ke dalam perairan alamiah sebagian besar berasal dari industri galvanik, sumber lain polusi Cd adalah industri batrei, pupuk dan fungisida yang mengandung Cd dan Zn juga merupakan sumber potensial polusi kedua logam ini (Allen et al., 1998).
Kadmium (Cd) merupakan logam yang bersifat kronis dan pada manusia biasanya terakumulasi dalam ginjal. Keracunan Cd dalam waktu yang lama membahayakan kesehatan paru-paru, tulang, hati, kelenjar reproduksi dan ginjal. Logam ini juga bersifat neurotoksin yang menimbulkan dampak rusaknya indera penciuman (Anwar,1996).
E. Tembaga (Cu)
Tembaga yang dilambangkan Cu adalah logam dengan nomor atom 29, massa atom 63,546, titik lebur 1083 °C, titik didih 2310 °C, jari atom 1,173 A° dan
jari-16 jari ion Cu2+ 0,96 A°. Tembaga adalah logam transisi (golongan I B) yang berwarna kemerahan, mudah regang dan mudah ditempa. Tembaga bersifat racun bagi makhluk hidup. Pencemaran logam berat meningkat sejalan dengan perkembangan industri. Pencemaran logam berat di lingkungan dikarenakan tingkat keracunannya yang sangat tinggi dalam seluruh aspek kehidupan makhluk hidup. Pada konsentrasi yang sedemikian rendah saja efek ion logam berat dapat berpengaruh langsung hingga terakumulasi pada rantai makanan. Logam berat dapat mengganggu kehidupan biota dalam lingkungan dan akhirnya berpengaruh terhadap kesehatan manusia (Suhendrayatna, 2001). Logam Cu dapat masuk ke dalam semua strata lingkungan, apakah itu pada strata perairan, tanah ataupun udara (lapisan atmosfer). Tembaga yang masuk ke dalam strata lingkungan dapat datang dari bermacam-macam sumber. Tetapi sumber–sumber masukan logam Cu ke dalam strata lingkungan yang umum dan diduga paling banyak adalah dari kegiatan-kegiatan perindustrian, kegiatan rumah tangga dan dari pembakaran serta mobilitas bahan-bahan bakar (Palar, 1994). Logam Cu yang masuk ke dalam tatanan lingkungan perairan dapat terjadi secara alamiah maupun sebagai efek samping dari kegiatan manusia. Secara alamiah Cu masuk ke dalam perairan dari peristiwa erosi, pengikisan batuan ataupun dari atmosfer yang dibawa turun oleh air hujan. Sedangkan dari aktifitas manusia seperti kegiatan industri, pertambangan Cu, maupun industri galangan kapal beserta kegiatan di pelabuhan merupakan salah satu jalur yang mempercepat terjadinya peningkatan kelarutan Cu dalam perairan (Palar, 1994).
Logam Cu termasuk logam berat essensial, jadi meskipun beracun tetapi sangat dibutuhkan manusia dalam jumlah yang kecil. Toksisitas yang dimiliki Cu baru akan bekerja bila telah masuk ke dalam tubuh organisme dalam jumlah yang besar atau melebihi nilai toleransi organisme terkait (Palar, 1994). Connel dan Miller (1995) menyatakan bahwa Cu merupakan logam essensial yang jika berada dalam konsentrasi rendah dapat merangsang pertumbuhan organisme sedangkan dalam konsetrasi yang tinggi dapat 11 menjadi penghambat. Selanjutnya oleh Palar (1994) dinyatakan bahwa biota perairan sangat peka terhadap kelebihan Cu dalam perairan sebagai tempat hidupnya. Konsentrasi Cu terlarut yang mencapai 0,01 ppm akan menyebabkan kematian bagi fitoplankton. Dalam tenggang waktu 96 jam biota yang tergolong dalam Mollusca akan mengalami kematian bila Cu yang terlarut dalam badan air berada pada kisaran 0,16 sampai 0,5 ppm. Tembaga adalah logam yang secara jelas mengalami proses akumulasi dalam tubuh hewan seiring dengan pertambahan umurnya, dan ginjal
17 merupakan bagian tubuh ikan yang paling banyak terdapat akumulasi Tembaga. Paparan Tembaga dalam waktu yang lama pada manusia akan menyebabkan terjadinya akumulasi bahan-bahan kimia dalam tubuh manusia yang dalam periode waktu tertentu akan menyebabkan munculnya efek yang merugikan kesehatan penduduk (Widowati, 2008). Gejala yang timbul pada manusia yang keracunan Cu akut adalah mual, muntah, sakit perut, hemolisis, netrofisis, kejang, dan akhirnya mati.Pada keracunan kronis, Cu tertimbun dalam hati dan menyebabkan hemolisis. Hemolisis terjadi karena tertimbunnya H2O2 dalam sel darah merah sehingga terjadi oksidasi dari lapisan sel yang mengakibatkan sel menjadi pecah. Defisiensi suhu dapat menyebabkan anemia dan pertumbuhan terhambat (Darmono, 2005).
F. Kromium (Cr)
Kromium atau dilambangkan Cr merupakan unsur kimia golongan 6 (VIB) dari tabel periodik. Merupakan logam baja abu-abu yang keras yang mengkilat dan digunakan dalam paduan untuk meningkatkan kekuatan dan ketahanan terhadap korosi. Kromium ditemukan tahun 1797 oleh kimiawan Perancis Nicolas-Louis Vauquelin dan diisolasi sebagai logam setahun kemudian; kromium dinamai berdasarkan senyawa warna-warninya tersebut. Warna hijau zamrud, serpentin, dan krom mika, warna merah ruby adalah karena terdapatnya sejumlah kecil kromium. Nama kromium sendiri berasal dari Chromos (bahasa Yunani) yang berarti "warna". Kromium adalah elemen yang relatif melimpah di kerak bumi; kromium dalam bentuk logam bebas tidak pernah ditemukan di alam. Kebanyakan bijih terdiri dari mineral kromit dengan formula ideal FeCr2O4. Kromium merupakan logam putih, keras, berkilau, rapuh dan sangat tahan terhadap reagen korosif biasa ; resistensi ini sangat berguna untuk digunakan secara luas sebagai lapisan pelindung. Pada suhu tinggi kromium bersatu langsung dengan halogen atau dengan sulfur, silikon, boron, nitrogen karbon atau oksigen. Kromium alami terdiri campuran empat isotop stabil, yaitu kromium-52 (83,76%), kromium-53 (9,55%), kromium-50 (4,31%) dan kromium-54 (2,38%). Kromium merupakan logam paramagnetik dan berada dalam dua bentuk yaitu : tubuh berpusat kubik (alpha) dan heksagonal - padat (beta). Pada suhu kamar, kromium secara perlahan larut dalam klorida dan asam sulfat encer. Mempunyai bilangan oksidasi yang umum +6, +3 dan +2 yang sering ditemukan sebagai ion kromat, Cr2O4- dan dikromat Cr2O72-. Ion-ion tersebut membentuk serangkaian garam yang penting dalam industri seperti Na2CrO4 atau Na2Cr2O7 yang digunakan dalam penyamakan kulit, pelapisan permukaan logam
18 atau katalis. Senyawa kromium lain dengan oksigen yang dapat membentuk kromium oksida atau oksida kromat, Cr2O3 merupakan bubuk hijau yang digunakan secara luas sebagai pigmen (Guignet yang hijau), serta ketahanan terhadap reaksi dan panas.
Logam berat kromium (Cr) diketahui berbahaya bagi kesehatan manusia. Kromium merupakan logam transisi golongan VI B yang dapat memiliki tingkat valensi yang bervariasi antara -2 dan +6 (Bramandita, 2009). Pada kadar yang rendah, kromium tergolong logam esensial bagi manusia yang berguna terutama dalam metabolisme karbohidrat karena bersama-sama dengan insulin menjaga kadar gula darah. Kekurangan kromium dapat mengganggu metabolisme karbohidrat, lemak dan protein serta mengganggu pertumbuhan (Kusnoputranto,1996 dalam Bramandita, 2009). Namun, kromium pada jumlah yang tinggi dapat menyebabkan reaksi alergi, peradangan, keracunan, kerusakan organ tubuh, penyakit kanker bahkan kematian (King, 1994 dalam Bramandita, 2009).
Kromium banyak digunakan oleh berbagai macam industri, salah satunya adalah industri tekstil. Industri tekstil merupakan industri yang mengolah serat menjadi bahan pakaian dengan kromium sebagai zat pengoksidasi pada proses penyempurnaan tekstil. Karena itu pula limbah cair dari industri tekstil mengandung kromium dengan konsentrasi tinggi. Limbah tersebut dapat membahayakan lingkungan karena kromium, terutama kromium heksavalen merupakan jenis bahan berbahaya dan beracun (B3) (Wahyuadi, 2004 dalam Bramandita, 2009). Dalam lingkungan hidup, kromium ditemukan dalam bentuk kromium logam, bivalen, trivalen dan heksavalen. Kromium logam memilki massa jenis (20C) sebesar 7,19 g/cm3 , titik leleh sebesar 1875C, titik didih sebesar 2658C dan tergolong logam yang mengkilap, keras serta tahan karat sehingga sering digunakan sebagai pelindung logam lain.
Logam kromium larut dalam asam klorida encer atau pekat. Jika tidak terkena udara, akan terbentuk ion-ion kromium (II) atau kromium bivalen. Kromium bivalen termasuk senyawa pereduksi kuat. Dengan adanya oksigen dari atmosfer, kromium sebagian atau seluruhnya menjadi teroksidasi ke dalam trivalen. Dalam bentuk heksavalen, kromium terdapat sebagai CrO4- dan Cr2O72-, sedangkan bentuk trivalen terdapat sebagai Cr3+, [Cr(OH)]2+, [Cr(OH)2] + dan [Cr(OH)4] - (Clesceri, et al., 1998 dalam Bramandita, 2009).
Dalam sistem biologis, kromium trivalen termasuk logam esensial bagi manusia (Massaro, 1997 dalam Bramandita, 2009). Dalam dosis 20 - 50 µg per 100 g
19 bobot badan, kromium memiliki fungsi yang baik dalam metabolisme karbohidrat, metabolisme lipid, sintesis protein dan metabolisme asam nukleat (Mertz, 1987 dalam Bramandita, 2009). Dalam metabolisme karbohidrat, kromium memiliki fungsi mempengaruhi kemampuan reseptor insulin dalam berinteraksi dengan insulin sehingga insulin dapat aktif bekerja mengatur kadar gula darah. Insulin yang aktif akan meningkatkan pengambilan glukosa yang kemudian terolah menjadi lemak. Dalam sintesis protein, keberadaan kromium mempengaruhi pembentukan asam amino glisin, serin dan metionin. Peranan kromium dalam metabolisme asam nukleat mampu berikatan dengan asam nukleat, dapat melindungi RNA dari denaturasi oleh panas dan dapat menjaga struktur tertier asam nukleat. Kekurangan kromium trivalen dalam tubuh dapat menyebabkan penurunan kerja hormon insulin yang kemudian dapat menimbulkan penyakit diabetes melitus, hiperglisemia dan glukosoria yang menyebabkan penurunan bobot badan, kadar asam lemak tinggi, gangguan proses pernafasan dan kelainan pada metabolisme nitrogen (King, 1994 dalam Bramandita, 2009).
Selain digolongkan sebagai logam esensial, kromium juga digolongkan dalam kelompok logam berat dengan sifat sangat beracun dan dalam kelompok senyawa yang karsinogen terhadap manusia. Keracunan oleh kromium menyebabkan gangguan kesehatan yang tidak dapat pulih dalam waktu singkat.
Dampak Pencemaran Kromium
Kromium termasuk dalam jenis logam berat yang sangat toksik. Sehingga keberadaan senyawa kromium dilingkungan harus mendapat perhatian yang serius. Kromium merupakan ion logam yang bersifat racun baik bagi manusia maupun bagi kehidupan mahluk hidup lainnya (ikan). Studi epidemiologi yang dilakukan oleh Baetjer, et al. (EPA, 1984) menunjukkan bahwa senyawa Cr (VI) sangat reponsif terhadap neoplasia saluran pernafasan. Senyawa ini juga dapat menyebabkan kanker lokal pada organ tubuh tikus dan kelinci yang terpapar senyawa kromium. Senyawa Cr (VI) dapat menyebabkan terjadinya mutagen yang pada akhirnya berpengaruh langsung pada asam deoksiribo nukleat (DNA) sehingga sel mahluk hidup akan berubah (Sukenjah, 2006). Hasil penelitian Jalius (2008) menunjukkan terjadi perbedaan metabolisme ion Cr3+ dan Cr6+. Perbedaan tersebut tergantung pada jenis atau spesies hewan yang dimasuki oleh ion logam tersebut. Tingkat keracunan lebih kuat ion-ion Cr6+ dibandingkan dengan ion-ion Cr3+. Logam Cr yang masuk ke dalam tubuh akan
20 ikut dalam proses fisiologis atau metabolisme tubuh. Logam Cr akan berintraksi dengan bermacam-macam unsur biologis yang terdapat dalam tubuh. Interaksi yang terjadi antara Cr dengan unsur-unsur biologis tubuh, dapat menyebabkan terganggunya fungsi-fungsi tertentu yang bekerja dalam proses metabolisme tubuh. Senyawa-senyawa yang mempunyai berat molekul rendah, seperti yang terdapat dalam sel darah rendah dapat melarutkan Cr dan seterusnya ikut terbawa ke seluruh tubuh bersama peredaran darah. Senyawa-senyawa ligan penting yang terdapat dalam tubuh juga mengubah Cr menjadi bentuk yang mudah terdifusi sehingga dapat masuk ke dalam jaringan. Di antara ligan-ligan tersebut adalah piropaspat, metionin, serin, glisin, leusin, lisin dan prolin. Terhadap piropospat, logam Cr mempunyai affinitas yang besar sekali. Affinitas Cr yang besar ini akan menjadi sangat berbahaya karena piropospat merupakan salah satu faktor biologis yang sangat penting dalam tubuh. Ion-ion Cr3+ yang masuk ke dalam tubuh akan bereaksi dengan protein dan secara lambat membentuk suatu ikatan kompleks yang sangat stabil. Selain itu Cr dapat mengkatalisis suksinat dalam enzim sitokrom reduktase, sehingga dapat mempengaruhi pertumbuhan dan beberapa reaksi biokimia lainnya dalam tubuh. Cr dengan kosentrasi sebesar 0,001 M dapat merangsang perubahan asetat menjadi CO2, kolesterol dan asam lemak (Palar, 2004 dalam Jalius, 2008). Ion-ion Cr6+ dalam proses metabolisme tubuh akan menghalangi atau mampu menghambat kerja dari enzim benzopiren hidroksilase. Penghambatan kerja enzim tersebut dapat mengakibatkan perubahan kemampuan pertumbuhan sel-sel, sehingga menjadi tumbuh secara tidak terkontrol yang dikenal sebagai sel-sel kanker
(Palar, 2004 dalam Jalius,2008).
Menurut Sukenjah (2006) kromium dapat menyebabkan gangguan pada kesehatan manusia baik secara akut maupun secara kronis. Paparan dengan konsentrasi yang lebih tinggi melalui pernafasan (pada manusia) dapat menyebabkan gangguan pada hati, ginjal, saluran pencernaan dan sistem kekebalan tubuh. Pada manusia kromium dapat mengakibatkan gangguan pada sistem reproduksi, gangguan hamil dan cacat pada bayi. EFA telah menggolongkan kromium (VI) sebagai zat karsinogenik kelompok A, yaitu kelompok yang paling berpotensi menimbulkan kanker. Secara umum efek yang pada dapat ditimbulkan oleh paparan kromium adalah sebagai berikut :
Efek fisiologis
Kromium mempunyai fungsi sebagai pengatur glukosa dalam darah, asupan harian kromium untuk manusia dewasa berkisar antara 50 sampai 200 µg per hari. Senyawa
21 kromium bersifat oksidator kuat sehingga apabila terkena paparan kromium dapat menyebabkan iritasi dan korosi. Organ tubuh yang menjadi sasaran pengaruh kromium adalah paru-paru, ginjal, hati, kulit dan sistem kekebalan tubuh. Efek senyawa kromium pada kulit dapat menyebabkan sensitasi dan iritasi pada kulit bahkan dapat menyebabkan eksim pada kulit. Efek pada sistem pernafasan disebabkan karena terhirupnya senyawa kromium sehingga mengakibatkan iritasi saluran pernafasan dan dapat menyebabkan sensitasi pada paru-paru bahkan kanker paru-paru. Efek pada ginjal, menunjukkan kerusakan pada saluran ginjal yang terkena paparan kromium sebesar (20 µg/m3). Hal ini setelah dilakukan studi pada pekerja yang terpapar kromium. Pada paparan yang lebih tinggi dapat mengakibatkan matinya sel ginjal. Efek pada hati dari paparan senyawa kromium dapat menyebabkan kerusakan pada hati. Suatu studi menunjukkan bahwa 20% pekerja yang terkena paparan kromium mengalami kerusakan pada hati dan ginjal. Efek karsinogenik, telah dilakukan studi epidemiologi yang menunjukkan bahwa pekerja yang terpapar kromium dalam jangka waktu yang lama mengalami kanker paru-paru. Efek pada sistem reproduksi menunjukkan data bahwa kromium dapat mempengaruhi organ reproduksi dan efek tetratogenik (perkembangan tidak normal dari sel selama kehamilan yang menyebabkan kerusakan pada embrio) pada hewan.
2.4 Cara pengolahan limbah laboratorium
Setiap limbah mempunyai cara pengolaham tersendiri tergantung dari jenisnya. Berikut adalah cara pengolahan limbah berdasarkan jenisnya.
A. Pengolahan Limbah Padat Penimbunan Terbuka
Terdapat dua cara penimbunan sampah yang umum dikenal, yaitu metode penimbunan terbuka (open dumping) dan metode sanitary landfill. Di lahan penimbunan terbuka, berbagai hama dan kuman penyebab penyakit dapat berkembang biak. Gas metan yang dihasilkan oleh pembusukan sampah organik dapat menyebar ke udara sekitar dan menimbulkan bau busuk serta mudah terbakar. Cairan yang tercampur dengan sampah dapat merembes ke tanah dan mencemari tanah serta air.
Sanitary Landfill
Pada metode sanitary landfill, sampah ditimbun dalam lubang yang dialasi lapisan lempung dan lembaran plastik untuk mencegah perembesan limbah ke tanah. Pada landfill
22 yang lebih modern, biasanya dibuat sistem Iapisan ganda (plastik – lempung – plastik – lempung) dan pipa-pipa saluran untuk mengumpulkan cairan serta gas metan yang terbentuk dari proses pembusukan sampah. Gas tersebut kemudian dapat digunakan untuk menghasilkan listrik.
Insinerasi
Insinerasi adalah pembakaran sampah/limbah padat menggunakan suatu alat yang disebut insinerator. Kelebihan dari proses insinerasi adalah volume sampah berkurang sangat banyak (bisa mencapai 90 %). Selain itu, proses insinerasi menghasilkan panas yang dapat dimanfaatkan untuk menghasilkan listrik atau untuk pemanas ruangan.
B. Pengolahan Limbah Pada Fasa Cair (Water Phase Treatment)
Sistem pengelolaan air limbah yang diterapkan harus memenuhi persyaratan berikut: Tidak mengakibatkan kontaminasi terhadap sumber air minum Tidak mengakibatkan pencemaran air permukaan
Tidak menimbulkan pencemaran pada flora dan fauna yang hidup di air di dalam penggunaannya sehari-hari
Tidak dihinggapi oleh vektor atau serangga yang mengakibatkan penyakit Tidak terbuka dan harus tertutup
Tidak menimbulkan bau atau aroma tidak sedap Pengolahan limbah cair dapat dilakukan dengan 3 cara, yaitu: 1. Pengolahan secara Fisika
Penyaringan (screening) merupakan cara yang efisien dan murah untuk menyisihkan bahan tersuspensi yang berukuran besar. Bahan tersuspensi yang mudah mengendap dapat disisihkan secara mudah dengan proses pengendapan.
2. Pengolahan secara Kimia
Pengolahan air buangan secara kimia biasanya dilakukan untuk menghilangkan partikel-partikel yang tidak mudah mengendap (koloid), logam-logam berat, senyawa fosfor, dan zat organik beracun; dengan membubuhkan bahan kimia tertentu yang diperlukan. 3. Pengolahan secara Biologi
Semua air buangan yang biodegradable dapat diolah secara biologi. Sebagai pengolahan sekunder, pengolahan secara biologi dipandang sebagai pengolahan yang paling murah dan efisien.
23 Proses Pengolahan dengan Pertumbuhan Tersuspensi ( Suspended Growth Treatment Processes – SGTP )
Pada pengolahan tersuspensi (SGTP), proses dilakukan oleh biomassa (mikroorganisme) yang tersuspensi dalam limbah cair. Beberapa proses pengolahan tersuspensi adalah sebagai berikut:
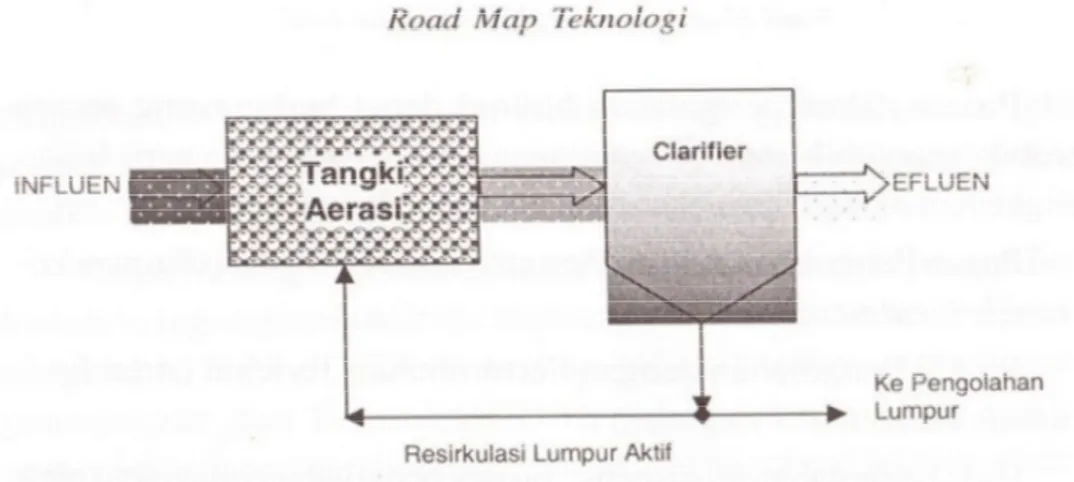
Activated Sludge (Pengolahan Lumpur Aktif)
Pada proses ini memanfaatkan mikroorganisme untuk menguraikan polutan, baik dalam suasana aerobik (dengan aerasi) maupun anaerobik (tanpa aerasi). Activated Sludgedigunakan pada pengolahan limbah cair domistik dan limbah cair industri yang memiliki kandungan zat organik yang tinggi (Lancester, 2002). Diagram Activated Sludge dapat ditunjukkan pada Gambar 2.3. Reaksi penguraian zat organik oleh mikroorganisme berlangsung pada lumpur aktif dalam tangki aerasi, yang berasal dari lumpur yang diresirkulasi dari clarifier dan dicampur dengan influen limbah cair yang disebut mixed liquor suspended solid (MLSS). Udara dialirkan pada tangki aerasi untuk memberikan oksigen pada proses serabik. Kelemahan proses ini memerlukan lahan yang luas dan menimbulkan polutan baru. Untuk mengurangi ActivatedSludgekonvensional dikembangkan Sequential Batch Reactor (SBR) dan
Contact Stabilization System. Sequential Batch Reactor (SBR)
Merupakan mudifikasi dari proses Activated sludgedengan mengubah aliran (inflow) dan aerasi kontinu menjadi batch (diskrit). SBR menggabungkan tangki ekualisasi, tangki aerasi, dan tangki sedimentasi sekunder (clarifier) menjadi satu reaktor. Operasi SBR dikontrol melalui suatu sistem monitoring dan kontroling yang terdiri atas komputer, programable logical controlling (PLC), dan alat-alat ukur (DO meter, pH meter untuk memonitor kondisi operasi. Diagram Activated Sludge dapat ditunjukkan pada Gambar 2.3
24 Gambar 2.3 Diagram Activated sludge
Prinsip kerja SBR adalah :
Limbah cair dialirkan kedalam tangki dan diaduk (mixing). Pada tahap ini berlangsung reaksi anaerobik.
Udara dialirkan kedalam tangki untuk mensuplai oksigen yang diperlukan dalam proses oksidasi. Pada tahap ini berlangsung reaksi aerobik.
Limbah cair berpisah menjadi dua fase yaitu fase padat (lumpur aktif/actived sludge) dan fase cair (air jernih/supernatant).
Air jernih dikeluarkan dari tangki dan siklus kerja kembali ke No.1
Gambar 2.4 Prinsip kerja Sequential Batch Reactor Contact Stabilization System (Nelleman, 2009)
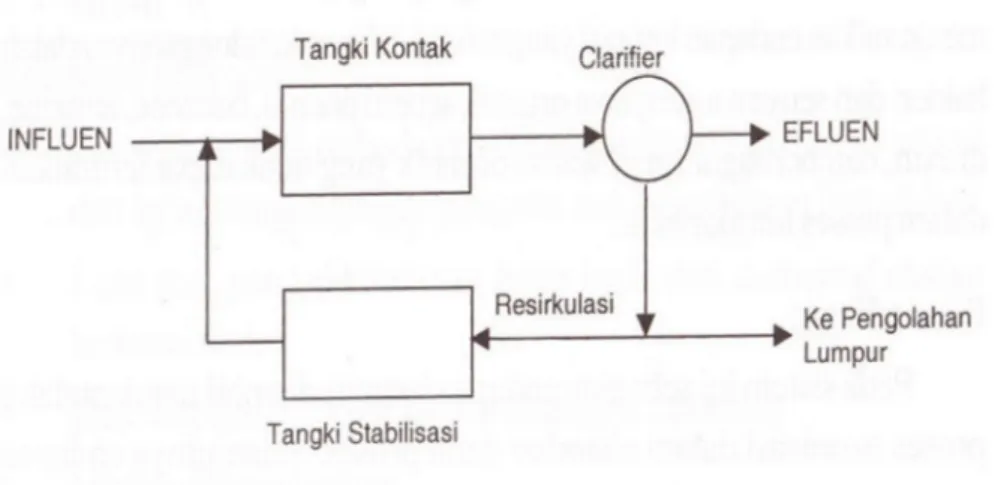
25 Contact Stabilization Systemmerupakan modifikasi dari proses actived sludge yang memanfaatkan proses biosorption. Biosorption adalah proses pengikatan polutan oleh biomassa dalam reaktor. Diagram Contact Stabilization System dapat ditunjukkan pada Gambar 2.5.
Gambar 2.5 Diagram proses control stabilization Upflow Anaerobic Sludge Bed (UASB)
Merupakan teknologi pengolahan yang umumnya digunakan dalam pengolahan limbah cair secara anaerobik. Pada teknologi ini, limbah cair dialirkan dari bawah ke atas (upflow). Melalui sludge bed. Proses ini didapatkan air jernih dan gas hasil proses anaerobik yang dapat dimanfaatkan. UASB digunakan untuk pengolahan limbah cair industri pengolahan makanan, minuman, pulp dan kertas, tekstil, kimia, dan petrokimia. Diagram Upflow Anaerobic Sludge Bed dapat ditunjukkan pada Gambar 2.7.
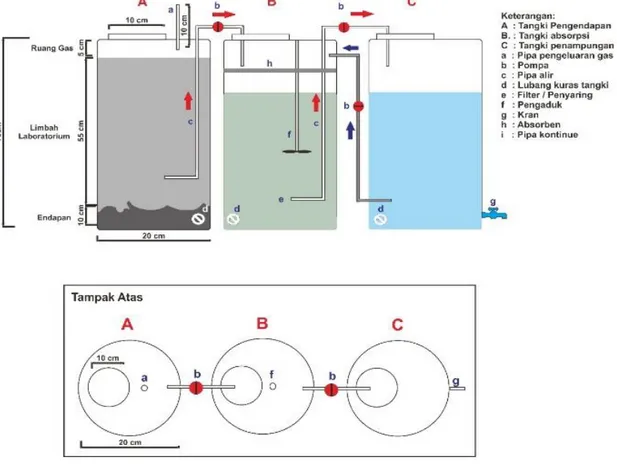
26 Salah satu bentuk prototipe pada pengolahan limbah yang dapat digunakan juga seperti pada Gambar 2.7 yaitu dengan penambahan adsorben pada bak pengolahan yang mengandung limbah kemudian air yang telah dipisahkan dari proses pengolahan tersebut dapat digunakan untuk kehidupan biota yang ada disekitarnya.
Gambar 2.7 Hasil rancangan prototipe pengolahan limbah dengan penambahan adsorben
2.5 Langkah-langkah mengurangi limbah laboratorium
Langkah-langkah yang dapat diolakukan untuk mengiurangi limbah dari laboratorium adalah sebagai berikut.
1. Menggunakan bahan kimia seperlunya
2. Melakukan reaksi kimia yang menghasilkan gas-gas beracun di lemari asam 3. Menggunakan alat dengan hati-hati sehingga tidak timbul kerusakan
27 Prinsip Pengolahan limbah B3
Limbah yang tidak saling cocok, disimpan dalam kemasan berbeda.
Jumlah pengisian volume limbah harus mempertimbangkan terjadinya pengembangan volume, pembentukan gas atau kenaikan tekanan selama penyimpanan.
Ganti kemasan yang mengalami kerusakan permanen (korosi atau bocor) dengan kemasan lain.
Kemasan yang telah berisi limbah ditandai sesuai dengan ketentuan yang berlaku. Kegiatan pengemasan, penyimpanan dan pengumpulan harus dilaporkan sebagai bagian
pengelolaan limbah.
2.6 Karbon aktif
Karbon aktif atau dikenal juga dengan arang aktif merupakan material amorf berkarbon yang memiliki luas permukaan yang besar yang dibangun oleh struktur pori internalnya melalui proses karbonisasi dan aktivasi. Karbon aktif mengandung 85-95% karbon, dihasilkan dari bahan-bahan yang mengandung karbon dengan pemanasan pada suhu tinggi. Ketika pemanasan berlangsung, diusahakan agar tidak terjadi kebocoran udara di dalam ruangan pemanasan sehingga bahan yang mengandung karbon tersebut hanya terkarbonisasi
dan tidak teroksidasi. Biasanya pengaktifan hanya bertujuan untuk memperbesar luas
permukaannya saja, namun beberapa usaha juga berkaitan dengan meningkatkan kemampuan adsorpsi karbon aktif itu sendiri.
Karbon aktif adalah suatu bahan padat yang berpori dan merupakan hasil pembakaran dari bahan yang mengandung karbon melalui proses pirolisis. Sebagian dari pori-porinya masih tertutup hidrokarbon, tar, dan senyawa organik lain. Komponennya terdiri dari karbon terikat (fixed carbon), abu, air, nitrogen, dan sulfur. Karbon aktif adalah karbon padat yang memiliki luas permukaan yang cukup tinggi berkisar antara 100 sampai dengan 2000 m2/g. Bahkan ada peneliti yang mengklaim luas permukaan karbon aktif yang dikembangkan memiliki luas permukaan melebihi 3000 m2/g. Bisa dibayangkan dalam setiap gram zat ini mengandung luas permukaan puluhan kali luasan lapangan sepak bola. Hal ini dikarenakan zat ini memiliki pori – pori yang sangat kompleks yang berkisar dari ukuran mikro dibawah 20 Aº. Sehingga luas permukaan disini lebih dimaksudkan luas permukaan internal yang diakibatkan dari adanya pori – pori yang berukuran sangat kecil. Karena memiliki luas permukaan yang sangat besar, maka karbon aktif sangat cocok digunakan untuk aplikasi yang membutuhkan luas kontak yang besar seperti pada bidang adsorpsi (penyerapan), dan pada bidang reaksi dan katalisis. Pada
28
prinsipnya bahan dasar pembuat karbon aktif haruslah mengandung unsur karbon yang besar. Dewasa ini karbon aktif yang berasal dari biomasa banyak dikembangkan para peneliti karena bersumber dari bahan yang terbarukan dan lebih murah. Beberapa karbon aktif dapat dibuat dari limbah biomasa seperti kulit kacang-kacangan, limbah padat pengepresan biji – bijiaan, ampas, kulit buah dan lain sebagainya. Karbon aktif berwarna hitam, tidak berbau, tidak berasa dan mempunyai daya serap besar. Karbon aktif mengalami perlakuan khusus berupa proses aktivasi baik secara fisika maupun secara kimia. Aktivasi tersebut menyebabkan pori-pori yang terdapat pada struktur molekulnya terbuka lebar sehingga daya serapnya akan semakin besar untuk menyerap bahan yang berfase cair maupun berfase gas (Sembiring dkk, 2003).
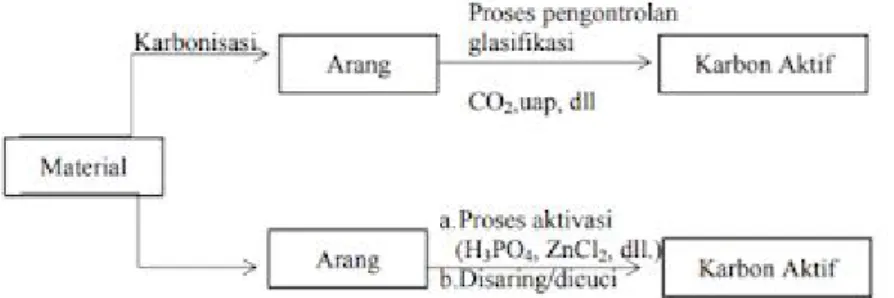
Proses pembuatan arang aktif dapat dibagi menjadi dua jenis yaitu pengaktifan secara fisika dan secara kimia (Gambar 2.8). Pengaktifan secara fisika pada dasarnya dilakukan dengan cara memanaskan bahan baku pada suhu yang cukup tinggi (600 – 900ºC) pada kondisi oksigen yang rendah dan suhu tinggi tersebut dialirkan media pengaktif seperti uap air dan CO2. Sedangkan pada pengaktifan kimiawi, bahan baku sebelum dipanaskan dicampur dengan bahan kimia tertentu seperti KOH, NaOH, K2CO3 dan lain sebagainya.
Arang aktif tidak hanya mengandung atom karbon saja, tetapi juga mengandung sejumlah kecil oksigen dan hidrogen yang terikat secara kimia dalam bentuk gugus-gugus fungsi yang bervariasi, misalnya gugus karbonil (CO), karboksil (COO), fenol, lakton, dan beberapa gugus eter. Oksigen pada permukaan arang aktif, kadang-kadang berasal dari bahan baku atau dapat juga terjadi pada proses aktivasi dengan uap (H2O) atau udara. Keadaan ini biasanya dapat menyebabkan arang bersifat asam atau basa. Pada umumnya bahan baku arang aktif mengandung komponen mineral.
29 Arang aktif mempunyai struktur berupa jaringan berpilin dari lapisan-lapisan karbon yang tidak sempurna, yang dihubungsilangkan oleh suatu jembatan alifatik. Luas permukaan, dimensi dan distribusi atom-atom karbon penyusun struktur arang aktif sangat tergantung pada bahan baku, kondisi karbonasi dan proses aktivasinya (Kyotani, 2000). Susunan atom-atom karbon pada arang aktif terdiri atas pelat-pelat heksagonal.
Arang aktif dapat digunakan dalam berbagai bidang, antara lain industri, kesehatan, lingkungan dan pertanian. Di bidang industri hampir 70 % menggunakan arang aktif (Harris, 1999). Penggunaan utama dari arang aktif diantaranya adalah untuk pemurnian larutan, seperti industri gula, sirop, air minum, sayuran, lemak, minyak, minuman alkohol, bahan kimia dan farmasi; penyerap gas beracun pada masker; penghilang bau pada sistem alat pendingin; penyerap emisi uap bahan bakar pada otomotif serta sebagai filter rokok (Austin, 1984; Harris, 1999). Arang aktif juga telah digunakan sebagai bahan tambahan dalam produk untuk pemeliharaan kebersihan dan kehalusan kulit dan rambut, antara lain sabun, lulur dan sampo. Di bidang kesehatan arang aktif digunakan dalam penanganan keracunan eksternal dan terapi diare sekretonik (Muthschler, 1986). Pada keracunan secara oral, untuk menghindari penyerapan sejumlah racun yang masih ada dalam saluran cerna dapat dilakukan dengan pemberian adsorben. Di bidang lingkungan, arang aktif digunakan sebagai adsorben terhadap logam Hg, Pb, Cd, Ni, Cu dalam limbah cair industri radiator, pelapisan nikel dan pelapisan tembaga (Kadirvelu et al., 2001). Kemampuan arang aktif sebagai penghilang logam tersebut dipengaruhi oleh pH dan konsentrasi karbon. Kenaikan kadar karbon menaikkan persen adsorpsi arang aktif terhadap ion logam. Benerapa bentuk arang aktif yang telah banyak diproduksi seperti pada Gambar 2.9
30 2.7 Bentonit
Bentonit dalam ilmu mineralogi tergolong ke dalam kelompok besar tanah lempung. Potensi endapan bentonit di Indonesia cukup besar dan tersebar di beberapa lokasi, yaitu di Pulau Jawa dan Sumatera dengan jumlah cadangan lebih dari 380 juta ton. Bentonit terbentuk dari transformasi hidrotermal abu vulkanik (Gambar 2.10), dimana mayoritas komponennya tergolong ke dalam kelas mineral smektit (struktur lembaran), yaitu montmorillonit. Mineral lain yang tergolong ke dalam smektit adalah hektorit, saponit, beidelit dan nontronit. Smektit adalah mineral yang terdiri dari tiga lapis struktur aluminium silikat hidrat, yaitu dua lembar silika tetrahedral dan satu lembar alumina oktahedral. Pada montmorillonit, lembaran yang berbentuk tetrahedral merupakan kombinasi dari silika tetrahedron yang terdiri dari atom Si dikelilingi oleh ion oksigen pada keempat ujung-ujungnya, sedangkan untuk lembaran yang berbentuk oktahedral, merupakan kombinasi dari alumina oktahedron. Alumina oktahedron terdiri dari atom Al yang dikelilingi oleh hidroksi (dapat berupa ion aluminium, magnesium, besi dan atom lainnya). Lapisan silika tersebut bermuatan sedikit negatif yang dikompensasi dengan keberadaan kation di antara lapisannya yang dapat tertukar. Pada umumnya adalah Ca+, Mg2+ dan atau Na+. Inilah karakteristik penting pada bentonit yang mempengaruhi kegunaan dan sifatnya. Selain montmorillonit, komponen yang umumnya ditemukan dalam bentonit adalah kaolin, felspar, kristoballit, illit, kuarsa, dan kalsit.
31 Berdasarkan kandungan mayoritas kation di dalam strukturnya, bentonit dibagi dua yaitu : Natrium Bentonit (Na-bentonit) ; Bentonit dengan kandungan natrium sebagai kation utama yang dapat ditukar (dikenal dengan istilah exchangeable cation), mampu mengalami pengembangan volume hingga beberapa kali bila kontak dengan air (dikenal dengan istilah swelling), membentuk koloid, bernilai viskositas tinggi, dan mampu mengikat air. Karakteristik tersebut membuat natrium bentonit dapat diaplikasikan pada bidang konstruksi dan teknik sipil, pengeboran minyak dan gas, serta pengecoran logam. Deposit terbesar dari natural Na-bentonit adalah yang ditemukan di negara bagian Wyoming, Amerika Serikat. (ii) Kalsium Bentonit (Ca-bentonit) ; Bentonit dengan kandungan kalsium sebagai kation utamanya yang dapat ditukar, memiliki kemampuan pengembangan volume yang rendah di dalam air. Sebagian besar deposit bentonit yang ditemukan merupakan Ca-bentonit dan sebagian lagi adalah campuran antara Ca-bentonit dan Na-bentonit.
Ada dua jenis bentonit yang dipakai dalam industri, yaitu Sodium (Na) bentonit dan Ca-bentonit. Na-bentonit dimanfaatkan sebagai bahan perekat, pengisi (filler), lumpur bor, sesuai sifatnya mampu membentuk suspensi kental setelah bercampur dengan air. Sedangkan Ca-bentonit banyak dipakai sebagai bahan penyerap. Untuk lumpur pemboran, bentonit bersaing dengan jenis lempung lain, yaitu atapulgit, sepiolit dan lempung lain yang telah diaktifkan. Dengan penambahan zat kimia pada kondisi tertentu, Ca-bentonit dapat dimanfaatkan sebagai bahan lumpur bor setelah melalui pertukaran ion, sehingga terjadi perubahan menjadi Na-bentonit dan diharapkan terjadi peningkatan sifat reologi dari suspensi mineral tersebut Agar mencapai persyaratan sebagai bahan lumpur sesuai dengan spesifikasi standar, perlu ada penambahan polimer. Hal itu dapat dilakukan melalui aktivasi bentonit untuk bahan lumpur bor.
Sifat bentonit yang perlu diperhatikan sehubungan dengan pemanfaatannya adalah :
Komposisi dan jenis mineral yang dikandung dalam bentonit, antara lain monmorillonit, kaolinit, illit, kwarsa, plagioklas, kristobalit, dan lainnya.
Komposisi kimia, yaitu unsur-unsur kimia yang terkandung antara lain, SiO2, Al2O3, CaO, MgO, Na2O, Fe2O3 H2O dll.
Sifat teknologi.
Sifat pertukaran ion; sifat ini antara lain, sifat pemucatan, adhesi, sifat penyerapan dan sifat lainnya.