BAB 2
TINJAUAN PUSTAKA
2.1. Morfologi tumbuhan sirsak
Sirsak (Annona muricata L) berupa tumbuhan atau potion yang berbatang utama berukuran kecil dan rendah. Daunnya berbentuk bulat telur agak tebal dan pada permukaan bagian atas yang halus berwarna hijau tua sedang pada bagian bawahnya mempunyai warna lebih muda. Tumbuhan ini dapat tumbuh di sembarang tempat. Tetapi untuk memperoleh hasil buah yang banyak dan besar-besar, maka yang paling balk ditanam di daerah yang tanahnya cukup mengandung air. Di Indonesia, sirsak tumbuh dengan baik pada daerah yang mempuyai ketinggian kurang dari 1000 meter di atas permukaan laut. Nama Sirsak itu sendiri sebenarnya berasal dari bahasa Belanda Zuurzak yang kuranglebih berarti kantung yang asam. Buah Sirsak yang sudah masak lebih berasa asam daripada manis. Pengembangbiakan sirsak yang paling baik adalah melalui okulasi dan akan menghasilkan buah pada usia 4 tahunan setelah ditanam. (Thomas, A. N. S, 1992).
Adapun kandungan dari buah sirsak adalah sebagai berikut: kaya vitamin C buah sirsak dari 67,5% daging buah,20% kulit buah,8,5% biji buah dan 4% inti buah. Setelah air, kandungan gizi yang terbanyak dalam sirsak adalah karbohidrat. Salah satu jenis karbohidrat yang terdapat dalam buah sirsak adalah gula pereduksi (glukosa dan fruktosa) dengan kadar 81,9 – 93,6 persen dari kandungan gula total. Buah sirsak mengandung sangat sedikit lemak (0,3 g/100 g), sehingga sangat baik untuk kesehatan. Rasa asam pada sirsak berasal dari asam organik non volatil terutama asam malat asam sitrat dan asam isositrat. Vitamin yang paling dominan pada buah sirsak adalah vitamin C, yaitu sekitar 20 mg per 100 gram daging buah. Kebutuhan vitamin C per orang per hari (yaitu 60 mg), telah dapat dipenuhi dengan hanya mengkonsumsi 300 gram daging buah sirsak. Kandungan vitamin C yang cukup tinggi pada sirsak merupakan anti oksidan yang sangat baik untuk meningkatkan daya tahan tubuh dalam memperlambat proses penuaan (tetap awet muda). Mineral yang cukup dominant adalah fosfor dan kalsium masing-masing
sebesar 27 dan 14 mg/100 g. kedua mineral tersebut penting untuk pembentukan massa tulang, sehingga berguna untuk membentuk tulang yang kuat serta menghambat osteoporosis.
Keunggulan sirsak terletak pada kadar sodium (natrium) yang rendah (14 mg/100 g) tetapi tinggi potasium (kalium), yaitu 278 mg/l00 g. Perbandingan kalium dan natrium yang tinggi sangat menguntungkan dalam rangka pencegahan penyakit hipertensi. Selain komponen gizi, buah sirsak juga sangat kaya akan komponen non gizi. Salah satu diantaranya adalah mengandung banyak serat pangan (dietary fiber), yaitu mencapai 3,3 g/100 g daging buah.
Konsumsi 100 g daging buah dapat memenuhi 13 persen kebutuhan serat pangan sehari. Buah sirsak merupakan buah yang kaya akan senyawa fitokimia, sehingga dapat dipastikan bahwa buah tersebut sangat banyak manfaat bagi kesehatan. Senyawa fitokimia tersebut dipastikan memiliki khasiat bagi kesehatan, walaupun belum semuanya terbukti secara ilmiah. Berbagai manfaat sirsak untuk terapi antara lain pengobatan batu empedu, antisembelit, asam urat, dan meningkatkan selera makan. Selain itu, kandungan seratnya juga berfungsi untuk memperlancar pencernaan, terutama untuk pengobatan sembelit (susah buang air besar). Sari buah (jus) sirsak di dalam sistem pencernaan akan meningkatkan selera makan. Kegunaan lain dari sari buah ini adalah untuk pengobatan pinggang pegal dan nyeri, penyakit wasir (ambeien), batu empedu, dan lain-lain. (Oleh: Prof. DR. Made Astawan, Ahli Teknologi Pangan dan Gizi)
2.1.1 Sistematika tumbuhan Sirsak adalah sebagai berikut :
Kingdom : Plantae Divisi : Spermatophyta Class : Dicotyledoneae Ordo : Ranales Family : Annonaceae Genus : Annona
Spesies : Annona muricata L. Nama daerah : Sirsak
2.1.2 Manfaat Tumbuhan Sirsak
Kulit batang tumbuhan sirsak ini berkhasiat sebagai obat mencret dan obat bisul, buah dan biji masak berkhasiat sebagai obat cacing. Buah sirsak juga berfungsi untuk memperlancar pencernaan. (Khomsan, A. 2009)
2.2. Senyawa Flavonoida
Senyawa flavonoida sebenarnya terdapat pada semua bagian tumbuhan termasuk daun, akar, kayu, kulit, tepung sari, bunga, buah, dan biji. Kebanyakan flavonoida ini berada di dalam tumbuh – tumbuhan kecuali alga. Namun ada juga flavonoida yang terdapat dalam hewan, misalnya dalam kelenjar bau berang – berang dan sekresi lebah. Dalam sayap kupu – kupu dengan anggapan bahwa flavonoida berasal dari tumbuh – tumbuhan yang menjadi makanan hewan tersebut dan tidak dibiosintesis di dalam tubuh mereka. Penyebaran jenis flavonoida pada golongan tumbuhan yang tersebar yaitu angiospermae, klorofita, fungi, briofita (Markham, 1988).
2.2.1. Struktur dasar senyawa flavonoida
Senyawa flavonoida adalah senyawa yang mengandung C15 terdiri atas dua inti fenolat yang dihubungkan dengan tiga satuan karbon. Struktur dasar flavonoida dapat digambarkan sebagai berikut :
C C C
A B
Kerangka dasar senyawa flavonoida
Cincin A adalah karakteristik phloroglusinol atau bentuk resorsinol tersubstitusi
O C3 OH HO C6
O
C
3HO
C
6Namun sering terhidroksilasi lebih lanjut : O C3 OH HO HO C6 A OCH3 O C3 OCH3 H3CO H3CO C6 A
Cincin B adalah karakteristik 4-, 3,4-, 3,4,5- terhidroksilasi
C3 (A) C6 R R' R'' B R = R’ = H, R’ = OH R = H, R’ = R” = OH R = R’ = R” = OH (juga, R = R’ = R” = H) (Sastrohamidjojo, 1996).
2.2.2. Klasifikasi senyawa Flavonoida
Flavonoida mengandung sistem aromatik yang terkonjugasi sehingga menunjukkan pita serapan kuat pada daerah spektrum sinar ultraviolet dan spectrum sinar tampak, umumnya dalam tumbuhan terikat pada gula yang disebut dengan glikosida
(Harbone, 1996).
Menurut Robinson (1995), flavonoida dapat dikelompokkan berdasarkan keragaman pada rantai C3 yaitu :
1.Flavonol
Flavonol paling sering terdapat sebagai glikosida, biasanya 3-glikosida, dan aglikon flavonol yang umum yaitu kamferol, kuersetin, dan mirisetin yang berkhasiat sebagai antioksidan dan antiimflamasi. Flavonol lain yang terdapat di alam bebas kebanyakan merupakan variasi struktur sederhana dari flavonol. Larutan flavonol dalam suasana basa dioksidasi oleh udara tetapi tidak begitu cepat sehingga penggunaan basa pada pengerjaannya masih dapat dilakukan.
2. Flavon
Flavon berbeda dengan flavonol dimana pada flavon tidak terdapat gugusan 3-hidroksi. Hal ini mempunyai serapan UV-nya, gerakan kromatografi, serta reaksi warnanya. Flavon terdapat juga sebagai glikosidanya lebih sedikit daripada jenis glikosida pada flavonol. Flavon yang paling umum dijumpai adalah apigenin dan luteolin. Luteolin merupakan zat warna yang pertama kali dipakai di Eropa. Jenis yang paling umum adalah 7-glukosida dan terdapat juga flavon yang terikat pada gula melalui ikatan karbon-karbon. Contohnya luteolin 8-C-glikosida. Flavon dianggap sebagai induk dalam nomenklatur kelompok senyawa flavonoida.
O O OH flavonol HO HO OH
O O flavon OH OH 1 2 3 4 10 5 6 7 8 9 1' 2' 3' 4' 5' 6' 3. Isoflavon
Isoflavon merupakan isomer flavon, tetapi jumlahnya sangat sedikit dan sebagai fitoaleksin yaitu senyawa pelindung yang terbentuk dalam tumbuhan sebagai pertahanan terhadap serangan penyakit. Isoflavon sukar dicirikan karena reaksinya tidak khas dengan pereaksi warna manapun. Beberapa isoflavon (misalnya daidzein) memberikan warna biru muda cemerlang dengan sinar UV bila diuapi amonia, tetapi kebanyakan yang lain tampak sebagai bercak lembayung yang pudar dengan amonia berubah menjadi coklat.
O O OH OH HO Struktur Isoflavon 4. Flavanon
Flavanon terdistribusi luas di alam. Flavanon terdapat di dalam kayu, daun dan bunga. Flavanon glikosida merupakan konstituen utama dari tanaman genus prenus dan buah jeruk ; dua glikosida yang paling lazim adalah neringenin dan hesperitin, terdapat dalam buah anggur dan jeruk.
O
O
Struktur Flavanon
5. Flavanonol
Senyawa ini berkhasiat sebagai antioksidan dan hanya terdapat sedikit sekali jika dibandingkan dengan flavonoida lain. Sebagian besar senyawa ini diabaikan karena konsentrasinya rendah dan tidak berwarna.
O
O
OH Struktur Flavanonol
6. Katekin
Katekin terdapat pada seluruh dunia tumbuhan, terutama pada tumbuhan berkayu. Senyawa ini mudah diperoleh dalam jumlah besar dari ekstrak kental Uncaria gambir
dan daun teh kering yang mengandung kira-kira 30% senyawa ini. Katekin berkhasiat sebagai antioksidan. O HO OH OH OH OH Struktur Katekin
7. Leukoantosianidin
Leukoantosianidin merupakan senyawa tan warna, terutama terdapat pada tumbuhan berkayu. Senyawa ini jarang terdapat sebagai glikosida, contohnya melaksidin, apiferol.
O
OH
HO OH
Struktur Leukoantosianidin
8. Antosianin
Antosianin merupakan pewarna yang paling penting dan paling tersebar luas dalam tumbuhan. Pigmen yng berwarna kuat dan larut dalam air ini adalah penyebab hampir semua warna merah jambu, merah marak , ungu, dan biru dalam daun, bunga, dan buah pada tumbuhan tinggi. Secara kimia semua antosianin merupakan turunan suatu struktur aromatik tunggal yaitu sianidin, dan semuanya terbentuk dari pigmen sianidin ini dengan penambahan atau pengurangan gugus hidroksil atau dengan metilasi atau glikosilasi.
O
OH Struktur Antosianin
9.Khalkon
Khalkon adalah pigmen fenol kuning yang berwarna coklat kuat dengan sinar UV bila dikromatografi kertas. Aglikon flavon dapat dibedakan dari glikosidanya, karena hanya pigmen dalam bentuk glikosida yang dapat bergerak pada kromatografi kertas dalam pengembang air (Harborne, 1996).
O
Struktur Khalkon
10. Auron
Auron berupa pigmen kuning emas yang terdapat dalam bunga tertentu dan briofita. Dalam larutan basa senyawa ini berwarna merah ros dan tampak pada kromatografi kertas berupa bercak kuning, dengan sinar ultraviolet warna kuning kuat berubah menjadi merah jingga bila diberi uap amonia (Robinson, 1995).
HC O
O
Struktur Auron
Prazat utama flavonoida sendiri sudah diketahui tanpa keraguan sebagai hasil dari banyak percobaan, tetapi masih banyak pertanyaan yang belum terjawab mengenai jalur rinci yang diikuti. Sering teramati bahwa dalam spesies tumbuhan tertentu semua flavoida yang berbeda-beda mempunyai pola hidroksilasi cincin yang sama, perberbeda-bedaan hanya terdapat asetilasi, glikosilasi, dan struktur bagian C-3. Pengamatan ini menunjukkan bahwa terdapat senyawa antara C-15 yang umum diubah menjadi berbagai senyawa flavonoida setelah pola hidroksilasi cincin terbentuk.
Akan tetapi, tampaknya berbagai gugus hidroksil ini sesungguhnya dimasukkan pada tahap yang berlainan dalam sintesis. Misalnya, jika hidroksil-7 harus terdapat pada produk akhir (misalnya sianidin), gugus ini harus terdapat pada cincin A kalkon. Pemasukan gugus hidroksil-3 ke dalam molekul yang sudah mengandung hidroksil-4 dapat terjadi bahkan pada tahap akhir jalur, dan jika telah ditambahkan tidak dapat dihilangkan. Hidroksil-3 ini terjadi dalam sistem bebas sel. Gugus hidroksil-2 yang tidak begitu lazim sering kali ditambahkan pada tahap flavonol dan jika telah ditambahkan biasanya tidak dihilangkan. Hidroksil-3 yang menjadi ciri flavonol dan antosianidin tampaknya juga ditambahkan pada tahap flavanonol. Hidroksilase-3
adalah oksigenase mikrosom, tetapi hidriksilasi-3 dikatalisis oleh enzim yamg larut. Pada flavonoida C-glikosida, gula terikat pada atom karbon flavonoida dan dalam hal ini gula tersebut terikat langsung pada inti benzene dengan suatu ikatan karbon-karbon yang tahan asam (Robinson,1995).
Menurut Harborne (1996), dikenal sekitar sepuluh kelas flavonoida dimana semua flavonoida, menurut strukturnya, merupakan turunan senyawa induk flavon dan semuanya mempunyai sejumlah sifat yang sama yakni:
Golongan flavonoida Penyebaran Ciri khas Antosianin Proantosianidin Flavonol Flavon Biflavonil
Khalkon dan auron
pigmen bunga merah marak, dan biru juga dalam daun dan jaringan lain.
terutama tan warna, dalam daun tumbuhan berkayu.
Terutamako-pigmen tanwarna dalam bunga sianik dan asianik; tersebar luas dalam daun.
seperti flavonol
tanwarna; hampir seluruhnya terbatas pada gimnospermae.
pigmen bunga kuning,
kadang-larut dalam air, λmaks 515-545 nm, bergerak dengan BAA pada kertas.
menghasilkan antosianidin (warna dapat diekstraksi dengan amil alkohol) bila jaringan dipanaskan dalam HCl 2M selama setengah
jam. Setelah hidrolisis, berupa bercak
kuning mirip pada kromatogram Forestal bila disinari dengan sinar UV;maksimal spektrum pada 330-350 nm.
Setelah hidrolisis, berupa bercak coklat redup pada kromatogram forestal; maksimal spektrum pada 330-350nm
Pada kromatogram BAA berupa bercak redup dengan Rf tinggi. Dengan amonia berwarna merah
Flavanon
Isoflavon
Glikoflavon
jaringan lain
tanwarna; dalam daun dan buah ( terutama dalam Citrus ) tanwarna; sering kali dalam akar; hanya terdapat dalam satu suku,Leguminosae
Seperti Flavonol
Berwarna merah kuat dengan Mg/HCl; kadang-kadang sangat pahit.
Bergerak pada kertas dengan pengembang air; tak ada uji warna yang khas
Mengandung gula yang terikat melalui ikatan C-C; bergerak dengan pengembang air, tidak seperti flavon biasa.
2.2.3. Sifat kelarutan Flavonoida
Aglikon flavonoida adalah polifenol dan karena itu mempunyai sifat kimia senyawa fenol, yaitu bersifat agak asam sehingga dapat larut dalam basa. Tetapi harus diingat, bila dibiarkan dalam larutan basa, dan di samping itu terdapat oksigen, banyak yang akan terurai. Karena mempunyai sejumlah gugus hidroksi, atau suatu gula, flavonoida merupakan senyawa polar, maka umumnya flavonoida cukup larut dalam pelarut polar seperti Etanol (EtOH), Metanol (MeOH), Butanol (BuOH), Aseton, Dimetilsulfoksida (DMSO), Dimetilformamida (DMF), Air dan lain-lain. Adanya gula yang terikat pada flavonoida (bentuk yang umum ditemukan) cenderung menyebabkan flavonoida lebih mudah larut dalam air dan dengan demikian campuran pelarut yang disebut diatas dengan air merupakan pelarut yang lebih baik untuk glikosida. Sebaliknya, aglikon yang kurang polar seperti isoflavon, flavanon dan flavon serta flavonol yang termetoksilasa cenderung lebih mudah larut dalam pelarut seperti Eter dan Kloroform (Markham, 1988).
2.3. Teknik Pemisahan
2.3.1 Ekstraksi
Ekstraksi dapat dilakukan dengan metoda maserasi, perkolasi, dan sokletasi. Sebelum ekstraksi dilakukan, biasanya serbuk tumbuhan dikeringkan lalu dihaluskan dengan derajat kehalusan tertentu, kemudian diekstraksi dengan salah satu cara di atas. Ekstraksi dengan metoda sokletasi dapat dilakukan secara bertingkat dengan berbagai pelarut berdasarkan kepolarannya, misalnya : n–heksana, eter, benzena, kloroform, etil asetat, etanol, metanol, dan air.
Ekstraksi dianggap selesai bila tetesan ekstrak yang terakhir memberikan reaksi negatif. Untuk mendapatkan larutan ekstrak yang pekat biasanya pelarut ekstrak diuapkan dengan menggunakan alat rotary evaporator. (Harborne, 1987 )
2.3.2. Kromatografi
Ada beberapa cara dalam mengelompokkan teknik kromatografi. Kebanyakan berdasarkan pada macam fasa yang digunakan (fasa gerak-fasa diam), misalnya kromatografi gas dan kromatografi cairan. Cara pengelompokan lainnya berdasarkan mekanisme yang membuat distribusi fasa. Disini metoda kromatografi sebagian dikelompokkan berdasarkan macam fasa yang digunakan dan sebagian lain berdasarkan pada mekanisme pada distribusi fasa.
Kromatografi cairan-padat atau kromatografi serapan, ditemukan oleh Tswett dan dikenalkan kembali oleh Khun dan Lederer pada 1931, telah digunakan sangat luas untuk analisis organik dan biokima. Pada umumnya sebagai isi kolom adalah silika gel atau alumina, yang mempunyai angka banding luas permukaan terhadap volume sangat besar.
Kromatografi cairan-cairan atau kromatografi partisi, dikenalkan oleh Martin dan Synge pada 1941, dan kemudian mendapatkan hadiah Nobel untuk itu. Fasa diam terdiri atas lapisan tipis cairan yang melapisi permukaan dari padatan inert yang berpori-pori.
Kromatografi gas-padat, digunakan sebelum tahun 1800 untuk memurnikan gas. Pada waktu dulu teknik ini tidak berkembang karena keterbatasannya yang sama seperti halnya kromatografi cairan-padat, tetapi penelitian lebih lanjut dengan macam fasa padat baru memperluas penggunaan teknik ini.
Kromatografi gas-cairan merupakan metoda pemisahan yang sangat efisien dan serba guna. Teknik ini telah menyebabkan revolusi dalam kimia Organik sejak dikenalkan pertama kali oleh James dan martin pada 1052. Hambatan yang paling utama adalah bahan cuplikan harus mempunyai tekanan uap paling tidak beberapa torr pada suhu kolom. Sistem ini sangat baik sehingga dapat dikatakan sebagai metoda pilihan dalam kromatografi karena dapat memisahkan dengan cepat dan peka. (Sudjadi, 1986 ).
2.3.2.1. Kromatografi Lapisan Tipis
Kromatografi lapisan tipis (KLT) dapat dipakai dengan dua tujuan. Yang pertama, dipakai selayaknya sebagai metode untuk mencapai hasil kualitatif, kuantitatif, dan preparative.Kedua dipkai untuk menjajaki sistem pelarut dan sistem penyangga yang akan dipakai dalam kromatografi kolom atau kromatografi cair kinerja tinggi.
Pada hakikatnya Kromatografi lapisan tipis melibatkan dua sifat fase : sifat fasa diam atau sifat lapisan dan sifat fase gerak atau campuran pelarut pengembang .Fasa diam dapat berupa serbuk halus yang berfungsi sebagai permukaan penyerap (kromatografi cair padat ) atau berfungsi sebagai penyangga untuk lapisan zat cair (kromatografi cair-cair).Fasa diam pada KLT sering disebut penyerap, walaupun sering berfungsi sebagai penyangga untuk lapisan zat cair di dalam sistem kromatogarafi cair-cair . Hampir segala macam serbuk dapat dipakai sebagai penyerap pada KLT , yaitu : silika gel (asam silikat). Alumina (aluminium oksida),kiselgur (tanah diatome), dan selulosa. Fasa gerak dapat berupa hampir segala macam pelarut atau campuran pelarut (Sudjadi, 1986).
2.3.2.2. Kromatografi Kolom
Kolom kromatografi atau tabung untuk pengaliran karena gaya tarik bumi (gravitasi) atau sistem bertekanan rendah biasanya terbuat dari kaca yang dilengkapi dengan keran jenis tertentu pada
bagian bawahnya untuk mengatur aliran pelarut. Ukuran keseluruhan kolom sungguh beragam, tetapi biasanya panjangnya sekurang –kurangnya 10 kali garis tengah dalamnya dan mungkin saja sampai 100 kali.
Pada kromatografi kolom, campuran yang akan dipisahkan diletakkan berupa pita pada bagian atas kolom penyerap yang berada dalam tabung kaca, tabung logam atau bahkan tabung plastik. Pelarut (fasa gerak ) dibiarkan mengalir melalui kolom karena aliran yang disebabkan oleh gaya berat atau didorong oleh tekanan. Pita senyawa linarut bergerak melalui kolom dengan laju yang berbeda, memisah dan dikumpulkan berupa fraksi ketika keluar dari alas kolom (Gritter , 1991).
2.3.2.3. Harga Rf (Retension Factor)
Mengidentifikasi noda – noda dalam lapisan tipis lazim menggunakan harga Rf yang diidentifikasi sebagai perbandingan antara jarak perambatan suatu zat dengan jarak perambatan pelarut yang dihitung dari titik penotolan pelarut zat. Jarak yang ditempuh oleh tiap bercak dari titik penotolan diukur dari pusat bercak. Untuk mengidentifikasi suatu senyawa, maka harga Rf senyawa tersebut dapat dibandingkan dengan harga Rf senyawa pembanding (Sastrohamidjojo, 1991). penotolan titik dari pelarut peramba Jarak penotolan titik dari bercak n perambat Jarak Rf tan a = 2.4. Teknik Spektroskopi
Teknik spektroskopi adalah salah satu teknik analisis kimia – fisika yang mengamati tentang interaksi atom atau molekul dengan radiasi elektronagnetik. Ada dua macam instrument pada teknik spekstroskopi yaitu spectrometer dan spektrofotometer. Instrumen yang memakai monokromator celah tetap pada bidang focus disebut sebagai spectrometer. Apabila spectrometer tersebut dilengkapi dengan detektor yang bersifat fotoelektrik maka disebut spektrofotometer (Muldja, 1995).
atom hidrogen. Kombinasinya dan data kadang-kadang menentukan struktur yang lengkap dari molekul yang tidak diketahui (Pavia, 1986).
Walaupun spektrum infra – merah merupakan kekhasan sebuah molekul secara menyeluruh, gugus atom tertentu memberikan penambahan pita-pita pada kerapatan tertentu, ataupun didekatnya, apapun bangun molekul selebihnya. Keberlakuan seperti itulah yang memungkinkan kimiawan memperoleh informasi tentang struktur yang berguna serta mendapatkan acuan bagi peta umum frekuensi gugus yang khas (Silverstain , 1986).
2.4.1. Spektrometri ultra violet
Serapan molekul di dalam derah ultra ungu dan terlihat dari spektrum bergantung pada struktur ultra elektronik dari molekul. Penyerapan sejumlah energi, menghasilkan percepatan dari elektron dalam orbital tingkat dasar ke orbital yang berenergi lebih tinggi di dalam keadaan tereksitasi (Silverstein, 1986).
Spektrum Flavonoida biasanya ditentukan dalam larutan dengan pelarut Metanol (MeOH) atau Etanol (EtOH). Spektrum khas terdiri atas dua maksima pada rentang 240-285 nm (pita II) dan 300-550 nm (pita I). Kedudukan yang tepat dan kekuatan nisbi maksima tersebut memberikan informasi yang berharga mengenai sifat flavonoida dan pola oksigenasinya. Ciri khas spektrum tersebut ialah kekuatan nisbi yang rendah pada pita I dalam dihidroflavon, dihidroflavonol, dan isoflavon serta kedudukan pita I pada spektrum khalkon, auron dan antosianin yang terdapat pada panjang gelombang yang tinggi.
Ciri spektrum golongan flavonoida utama dapat ditunjukkan sebagai berikut :
λ maksimum utama (nm) λ maksimum tambahan (nm) (dengan intensitas nisbi) Jenis flavonoida 475-560 390-430 365-390 350-390 ± 275 (55%) 240-270 (32%) 240-260 (30%) ± 300 (40%) Antosianin Auron Kalkol Flavonol
250-270 330-350 300-350 275-295 ± 225 310-330 ± 300 (40%) tidak ada tidak ada 310-330 (30%) 310-330 (30%) 310-330 (25%) Flavonol
Flavon dan biflavonil Flavon dan biflavonil Flavanon dan flavononol Flavonon dan flavononon Isoflavon
2.4.2. Spektrofotometri Infra Merah (FT - IR)
Cahaya tampak terdiri dari beberapa range frekuensi elektromagnetik yang berbeda dimana setiap frekuensi bias dilihat sebagai warna yang berbeda. Radiasi infra merah juga mengandung beberapa range frekuensi tetapi tidak dapat dilihat oleh mata. Pengukuran pada spectrum infra merah dilakukan pada daerah cahaya infra merah tengah (mid infrared) yaitu pada panjang gelombang 2.5 – 50 μm atau bilangan gelombang 4000 – 200 cm -1. energi yang dihasilkan oleh radiasi ini akan menyebabkan vibrasi atau getaran pada molekul. Pita absorbsi inframerah sangat khas dan spesifik untuk setiap tipe ikatan kimia atau gugus fungsi. Metoda ini sangat berguna mengidentifikasi senyawa organik dan organometalik. (Dachriyanus, 2004)
Spekrum infra merah suatu molekul adalah hasil transisi antara tingkat energi getaran yang berlainan. Pancaran infra merah yang kerapatannya kurang dari 100 cm-1 (panjang gelombang lebih daripada 100 µm) diserap oleh sebuah molekul organik dan diubah menjadi putaran energi molekul. (Silverstein, 1986).
2.4.3. Spektrofotometri Resonansi Magnetik Inti Proton (1H-NMR)
Spektrometri Resonansi Magnetik Inti (Nuclear Magnetic Rresonance, NMR ) merupakan alat yang berguna pada penentuan struktur molekul organik. Teknik ini memberikan informasi mengenai berbagai jenis atom hidrogen dalam molekul. Struktur NMR memberikan informasi mengenai lingkungan kimia atom hydrogen, jumlah atom hydrogen dalam setiap lingkungan dan
2.4.3.1. Penggunaan chemical shifts (pergeseran kimia)
Posisi sinyal memberikan informasi yang berguna tentang gugus masing-masing atom hidrogen. Pergeseran kimia yang penting untuk masing-masing gugus pada metilpropanoat adalah:
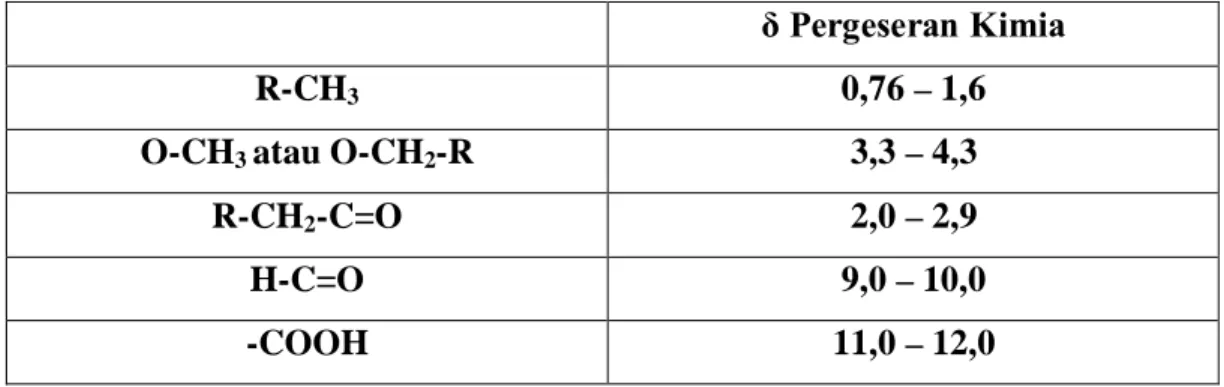
Tabel Pergeseran Kimia Beberapa Proton.
δ Pergeseran Kimia
R-CH3 0,76 – 1,6
O-CH3 atau O-CH2-R 3,3 – 4,3
R-CH2-C=O 2,0 – 2,9
H-C=O 9,0 – 10,0
-COOH 11,0 – 12,0
Keterangan :
“R” adalah gugus alkil. Pergeseran kimia ditunjukkan dalam range. Posisi yang tepat tergantung pada bagian gugus yang melekat padanya didalam molekul.
(Dachriyanus, 2004)
Pergeseran kimia adalah pengukuran medan dalam keadaan bebas. Semua proton-proton dalam satu molekul yang ada dalam lingkungan kimia yang serupa kadang-kadang menunujukkan pergeseran kimia yang sama. Setiap senyawa memberikan penaikan menjadi puncak absorpsi tunggal dalam spektrum NMR.