i SKRIPSI
Diajukan untuk Memenuhi Salah Satu Syarat Memperoleh Gelar Sarjana Farmasi (S. Farm.)
Program Studi Farmasi
Oleh:
Theresia Weliana Kosasih NIM: 078114093
FAKULTAS FARMASI UNIVERSITAS SANATA DHARMA
iv
PAPA
MAMA
KAKAK DAN ADIK
TEMAN-TEMANKU
DAN TERISTIMEWA
ALMAMATERKU, SANATA DHARMA
YOGYAKARTA
Janganlah takut, sebab Aku menyertai engkau, janganlah bimbang,
sebab Aku ini Allahmu; Aku akan meneguhkan, bahkan akan
vii
kuasa-Nya, sehingga skripsi berjudul “Optimasi Pemisahan Kurkumin dalam Kapsul Lunak Obat Herbal Terstandar (OHT) Rheumakur® dengan Metode Kromatografi Lapis Tipis Densitometri” dapat dikerjakan dengan sebaik-baiknya. Skripsi ini disusun untuk memenuhi salah satu persyaratan untuk memperoleh gelar Sarjana Strata Satu Program Studi Ilmu Farmasi (S. Farm).
Dalam menyelesaikan skripsi ini, penulis mengalami permasalahan dan kesulitan. Namun demikian dengan adanya bantuan dari berbagai pihak, penulis dapat menyelesaikan skripsi ini dengan baik. Oleh karena itu dengan segala hormat, penulis ingin mengucapkan terima kasih atas bantuan yang telah diberikan, kepada :
1. Ipang Djunarko, M.Sc, Apt. selaku dekan Fakultas Farmasi Universitas Sanata Dharma Yogyakarta
2. Christine Patramurti, M.Si., Apt. selaku dosen pembimbing yang telah membimbing penulis, memberikan masukan, dan dukungan selama penyusunan skripsi ini.
3. Yohanes Dwiatmaka, M.Si. selaku dosen penguji yang memberikan kritik dan saran untuk skripsi ini.
viii
senyawa baku kurkumin yang berguna dalam penelitian.
7. Dr. C. J. Soegihardjo, Apt. selaku Dosen Obat Tradisional yang telah meluangkan waktu untuk memberikan diskusi dan saran yang membangun. 8. Seluruh staf laboratorium di Fakultas Farmasi Universitas Sanata Dharma
Yogyakarta terutama Mas Bimo, Mas Wagiran, Pak Parlan, dan Mas Kunto yang telah membantu dan mendukung kelangsungan skripsi ini.
9. Teman-teman FST 2007 yang sangat kompak dan memberikan proses pembelajaran yang berharga.
10. Seno, Lilis, Eliz, Yunita, Veny, Katrin, Beny, Dian P., Katiti, Lala, Toro tim pelaksana pemisahan kurkumin.
11. Kakakku, Bayu Aryono yang memberikan semangat dan doa selama kelangsungan skripsi ini.
12. Teman-teman seperjuangan yang tidak dapat saya sebutkan satu persatu namanya.
Penulis menyadari bahwa dalam skripsi ini masih terdapat banyak kekurangan mengingat keterbatasan kemampuan dan pengetahuan penulis. Maka penulis mengharapkan saran dan kritik yang membangun dari semua pihak. Akhir kata, semoga skripsi ini berguna bagi kemajuan ilmu pengetahuan.
ix
HALAMAN PERSETUJUAN PEMBIMBING... HALAMAN PENGESAHAN... HALAMAN PERSEMBAHAN... PERNYATAAN KEASLIAN KARYA... LEMBAR PERNYATAAN PERSETUJUAN PUBLIKASI KARYA... PRAKATA... BAB II. PENELAAHAN PUSTAKA...
A. Kurkumin...
x
C. Obat Herbal Terstandar... D. Kapsul Obat Tradisional... E. Kromatografi Lapis Tipis Densitometri... 1. Kromatografi lapis tipis secara umum... 2. Jenis fase diam KLT... 3. Jenis fase gerak KLT... 4. Aplikasi penotolan sampel... 5. Pengembangan... 6. Penentuan kromatogram... 7. Kromatografi lapis tipis kuantitatif... F. Landasan Teori... BAB III. METODE PENELITIAN...
A. Jenis dan Rancangan Penelitian... B. Variabel... C. Definisi Operasional... D. Bahan Penelitian... E. Alat Penelitian... F. Tata Cara Penelitian... 1. Pembuatan metanolp.a.pH 4...
xi
5. Optimasi metode KLT densitometri... G. Analisis Hasil...
32 33 BAB IV. HASIL DAN PEMBAHASAN...
A. Jenis dan Komposisi Fase Gerak... B. Pembuatan Metanolp.a.pH 4... C. Pembuatan Larutan Baku... D. Preparasi Sampel... E. Penentuan Panjang Gelombang Maksimum Baku Kurkumin dengan KLT Densitometri... F. Optimasi Pemisahan Kurkumin dalam Kapsul Lunak OHT Rheumakur®dengan Metode KLT Densitometri... 1. Fase gerak kloroform p.a.:metanol p.a. dengan perbandingan 48:2 (komposisi I)... 2. Fase gerak kloroform p.a.:asam asetat glasial p.a. dengan
perbandingan 9,50:0,50 (komposisi II)... 3. Fase gerak heksan p.a.:kloroform p.a.:asam asetat glasial p.a.
dengan perbandingan 5:4,875:0,125 (komposisi III)... 4. Fase gerak heksan p.a.:kloroform p.a.:asam asetat glasial p.a.
dengan perbandingan 0,5:8,5:1,0 (komposisi IV)...
xii
LAMPIRAN... BIOGRAFI PENULIS...
xiii
Tabel II. Nilai indeks polaritas pelarut... 17 Tabel III. Jenis dan komposisi fase gerak... 33 Tabel IV. Nilai indeks polaritas dari jenis dan komposisi fase gerak... 35 Tabel V. Data pengukuran panjang gelombang serapan maksimum
kurkumin... 39 Tabel VI. Pemisahan pada berbagai jenis dan komposisi fase gerak... 43 Tabel VII. Parameter pemisahan dan nilai koefisien variansi (KV) dari
xiv
Gambar 2. Reaksi degradasi kurkumin dalam kondisi basa... 8
Gambar 3. Produk fotodegradasi kurkumin... 9
Gambar 4. Logo obat herbal terstandar... 11
Gambar 5. Ikatan hidrogen pada permukaan silika... 15
Gambar 6. Cara penentuan harga Rf... 19
Gambar 7. Keadaan simetris dan pelebaran puncak kromatogram... 21
Gambar 8. Ilustrasi 3 prinsip utama yang menggambarkan puncak... 21
Gambar 9. Isoterm sorpsi serta profil-profil puncak yang dihasilkan... 22
Gambar 10. Penentuanpeak asymmetry... 23
Gambar 11. Pemisahan dua senyawa... 24
Gambar 12. Gugus kromofor dan auksokrom pada struktur kurkumin... 39
Gambar 13. Kromatogram panjang gelombang maksimum baku kurkumin 100, 300, dan 500 ppm masing-masing direplikasi 3 kali... 40
Gambar 14. Gugus polar dan non polar kurkumin... 41
Gambar 15. Interaksi fase diam dengan kurkumin... 42
Gambar 16. Peak baku kurkumin konsentrasi 300 ppm dan peak pemisahan dari kurkumin dalam kapsul lunak OHT Rheumakur®dengan fase gerak kloroform:metanol (48:2)... 45 Gambar 17. Peak baku kurkumin konsentrasi 300 ppm dan peak
xv
pemisahan dari kurkumin dalam kapsul lunak OHT Rheumakur® dengan fase gerak heksan p.a.:kloroform p.a.:asam asetat glasialp.a.(5:4,875:0,125) ... 49 Gambar 19. Peak baku kurkumin konsentrasi 300 ppm dan peak
pemisahan dari kurkumin dalam kapsul lunak OHT Rheumakur® dengan fase gerak heksan p.a.:kloroform p.a.:asam asetat glasialp.a.(0,5:8,5:1,0) ... ... 50 Gambar 20. Tiga replikasi peak pemisahan dari kurkumin dalam kapsul
lunak OHT Rheumakur® dengan fase gerak heksan p.a.:kloroformp.a.:asam asetat glasialp.a.(0,5:8,5:1,0) ... 52 Gambar 21. Interaksi kurkumin dengan fase gerak heksan p.a.:kloroform
xvi
Lampiran 2. Hasil kromatogram scanning dengan panjang gelombang serapan maksimum kurkumin... ... 61 Lampiran 3. Sistem KLT-Densitometri yang digunakan... 62 Lampiran 4. Perhitungan kepolaran fase gerak... 66 Lampiran 5. Penimbangan baku dan sampel serta contoh perhitungan
kadar seri baku... ... 67 Lampiran 6. Kromatogram pada fase gerak kloroform : metanol (48:2)... 69 Lampiran 7. Kromatogram pada fase gerak kloroform : asam asetat
glasial (9,50:0,50) ... ... 71 Lampiran 8. Kromatogram pada fase gerak heksan : kloroform : asam
asetat glasial (5:4,875:0,125) ... 73 Lampiran 9. Kromatogram pada fase gerak heksan : kloroform : asam
asetat glasial (0,5:8,5:1,0)... 75 Lampiran 10. Kromatogram pada fase gerak heksan : kloroform : asam
asetat glasial (0,5:8,5:1,0) replikasi I... 77 Lampiran 11. Kromatogram pada fase gerak heksan : kloroform : asam
asetat glasial (0,5:8,5:1,0) replikasi II... 79 Lampiran 12. Kromatogram pada fase gerak heksan : kloroform : asam
xvii
tiga replikasi komposisi fase gerak V... 85 Lampiran 15. Nilai resolusi (Rs) kelima komposisi fase gerak dan tiga
replikasi komposisi fase gerak V serta contoh perhitungan nilai resolusi pemisahan kurkumin... 87 Lampiran 16. Nilai koefisien variansi (KV) dari nilai resolusi ketiga
xviii
hanya mengandung kurkumin tetapi juga mengandung senyawa-senyawa lain termasuk turunan lain dari kurkuminoid. Salah satu metode analisis yang dapat digunakan untuk dapat memisahkan kurkumin dalam kapsul lunak OHT Rheumakur® ialah kromatografi lapis tipis (KLT) densitometri. Tujuan dari penelitian ini untuk mengetahui jenis dan komposisi fase gerak yang optimum untuk memisahkan kurkumin dalam kapsul lunak OHT Rheumakur® dengan metode KLT densitometri.
Penelitian ini bersifat eksperimental dua tingkat. Sistem KLT merupakan fase normal dengan fase diam silika gel G60 dan fase gerak pada penelitian ini
ialah variasi komposisi dari kloroform:asam asetat glasial dan heksan:kloroform:asam asetat glasial. Scan dilakukan pada panjang gelombang 425 nm.
Dari hasil penelitian ini kondisi optimum ditunjukkan pada fase gerak heksan p.a.:kloroform p.a.:asam asetat glasial p.a (0,5:8,5:1). Kondisi ini memenuhi parameter pemisahan yang baik yaitu bentukpeakyang simetris (0,95-1,10), sempit, dan tajam; nilai faktor retardasi 0,2-0,8; nilai resolusi dari pemisahan peak yang terdapat dalam kapsul lunak OHT Rheumakur®≥ 1,5; dan reprodusibilitas nilai resolusi pemisahan peak yang terdapat dalam kapsul lunak OHT Rheumakur®ditunjukkan dengan nilai koefisien variasi≤2.
xix
another compound included other curcuminoid derivatif. One of analysis method that can be used to be able separate curcumin in SBHM Rheumakur®soft capsule is thin layer chromatography (TLC) densitometry. The aim of this research is to detect the kind and the composition of optimum mobile phase to separated curcumin in SBHM Rheumakur®soft capsule is TLC densitometry.
This research have two level experiment characteristic. TLC system is normal phase with G60 silica gel stationary phase and mobile phase in this
research is composition variation of cloroform:glacial acetic acid and hexane: cloroform:glacial acetic acid. Scanning is carried out at wavelenght 425 nm.
From this result of research, optimum condition is showed at hexane: cloroform:glacial acetic acid (0,5:8,5:1,0) mobile phase. This condition fill the good separating parameter that is simetric peak shape (0,95-1,10), narrow, and sharp; value of retardation factor 0,2-0,8; resolution value of peak separation in the SBHM Rheumakur®soft capsule≥1,5; and reprodusibility of resolution value of peak separation in the SBHM Rheumakur® soft capsule is showed with variation coefisien value≤2.
1
A. Latar Belakang
Beberapa waktu belakangan ini, semboyan back to nature kembali digunakan oleh banyak orang. Banyak produk obat tradisional yang beredar di pasaran mengandung ekstrak dari rimpang kunyit (Curcuma domestica). Kunyit mengandung senyawa kimia yang mempunyai keaktifan fisiologi, yaitu kurkuminoid. Kurkuminoid terdiri dari kurkumin, demetoksikurkumin dan bis-demetoksikurkumin. Kurkumin merupakan senyawa aktif dari kunyit dan memiliki khasiat sebagai anti inflamasi, anti oksidan, efek pencegah kanker dan menurunkan risiko serangan jantung (Sumiati, 2010). Kurkumin banyak digunakan dalam campuran obat tradisional, salah satunya dalam bentuk kapsul lunak obat herbal terstandar (OHT) Rheumakur®.
WHO merekomendasi penggunaan obat tradisional termasuk herbal dalampemeliharaan kesehatan masyarakat, pencegahan dan pengobatan penyakit, terutama untuk penyakit kronis, penyakit degeneratif dan kanker. WHO juga
mendukung upaya-upaya dalam peningkatan keamanan dan khasiat dari obat
tradisional (WHO, 2003). Peningkatan keamanan dan khasiat dalam sediaan jamu
aktif dan aktivitas farmakologi yang ditimbulkan. Begitu pula dengan penjaminan mutu kadar dari kurkumin dalam sampel kapsul lunak produk OHT Rheumakur®.
Produk OHT Rheumakur® tidak mengandung satu senyawa tunggal kurkuminoid dari Curcuma domesticatetapi juga mengandung senyawa-senyawa lain, yaitu minyak atsiri dari Curcuma xanthorizza dan Curcuma domestica. Pemakaian kurkumin sebagai campuran obat tradisional harus diberikan dengan dosis yang tepat berkaitan dengan efek farmakologi yang akan ditimbulkan. Oleh karenanya, diperlukan suatu metode analisis yang dapat digunakan untuk memisahkan kurkumin dari senyawa-senyawa lain sediaan kapsul lunak OHT Rheumakur® dan menetapkan kadar kurkumin dalam sediaan kapsul lunak OHT Rheumakur®. Metode analisis tersebut dapat memberikan jaminan kualitas dan mutu terhadap produk obat tradisional yang ditetapkan serta terhadap konsumen yang menggunakan produk obat tradisional tersebut.
Rohman, 2007). Reprodusibilitas dari nilai resolusi yang didapat ditunjukkan dengan nilai KV≤2 (Harmita, 2004).
Sebelum dilakukan penetapan kadar dengan metode KLT densitometri ini perlu dilakukan optimasi metode KLT densitometri. Optimasi ini bertujuan untuk mengetahui kondisi yang optimum untuk dapat memisahkan kurkumin dari senyawa-senyawa lain dalam sediaan kapsul lunak OHT Rheumakur®. Optimasi ini perlu dilakukan karena dalam penelitian ini metode KLT densitometri dengan sistem yang baru yaitu penggunaan jenis dan komposisi fase gerak yang belum pernah dilakukan sebelumnya. Selain itu OHT Rheumakur®belum pernah diteliti sebelumnya sehingga dibutuhkan suatu sistem yang baru untuk dapat memperoleh hasil pemisahan yang baik.
Optimasi yang dilakukan pada metode KLT densitometri ini ialah jenis dan komposisi fase gerak. Variasi jenis dan komposisi fase gerak akan berpengaruh terhadap pemisahan dari kurkumin dengan senyawa-senyawa lain dalam sediaan kapsul lunak OHT Rheumakur®. Penelitian ini bertujuan untuk mengetahui jenis dan komposisi fase gerak yang optimum untuk memisahkan kurkumin dalam kapsul lunak OHT Rheumakur® dengan metode KLT densitometri.
1. Permasalahan
nilai resolusi ≤ 2 untuk memisahkan kurkumin dalam kapsul lunak OHT Rheumakur®dengan metode KLT densitometri?
2. Keaslian penelitian
Sejauh pengetahuan peneliti, penelitian kurkumin dalam kapsul lunak OHT Rheumakur® menggunakan KLT densitometri ini belum pernah dilakukan. Penelitian yang pernah dilakukan terkait penelitian mengenai kurkumin menggunakan KLT densitometri yaitu Penentuan Kadar Kurkumin secara KLT Densitometri dengan fase gerak kloroform:etanol:air suling (25:0,96:0,04) dilakukan oleh Martono, 1996; Simultaneous determination of curcuminoids in curcuma samples using high performance thin layer chromatographydengan fase gerak kloroform:metanol (98:2 dan 95:5) dilakukan oleh Gupta, Gupta, Kumar, 1999, dan Occurrence of curcuminoids in curcuma longa: a quality standardization by HPTLC dengan fase gerak kloroform:metanol (48:2) pernah dilakukan oleh Paramasivam, Aktar, Poi, Banerjee, Bandyopahyay, 2008.
3. Manfaat penelitian
b. Manfaat praktis. Dari hasil penelitian ini untuk memberikan informasi bagi konsumen mengenai mutu, keamanan dan kemanfaatan kurkumin dalam kapsul lunak OHT Rheumakur®yang beredar di masyarakat.
B. Tujuan Penelitian
6
Kurkumin berupa serbuk kristal berbentuk batang atau prisma, berwarna kuning orange, larut dalam alkohol dan aseton, tidak larut dalam air dan eter (Robinson, 1995). Kurkumin memiliki sifat yaitu rasanya sedikit pahit. Kurkumin juga larut dalam asam asetat glasial dan alkali hidroksida (Majeed et al., 1995). Kurkumin (C21H20O6) memiliki titik lebur 184-185 °C, berat molekul 368,37
g/mol (Majeedet al., 1995).
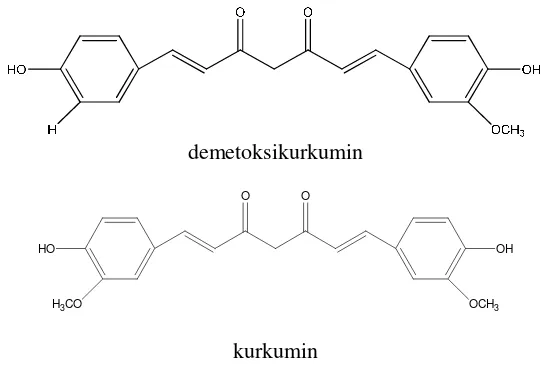
Kurkumin merupakan senyawa fenol alami berwarna kuning orange, terdapat bersama golongannya (dikenal dengan nama kurkuminoid). Kurkuminoid ada 3 macam yaitu kurkumin, demetoksikumin dan bis-demetoksikurkumin (Martono, 1996). Struktur kimia dari golongan kurkuminoid ditunjukan pada gambar berikut:
demetoksikurkumin
OH
OCH3
HO
H3CO
O O
OH
Gambar 1. Struktur kimia dari golongan kurkuminoid
Dari ketiga senyawa kurkuminoid tersebut, kurkumin merupakan komponen terbesar. Sering kadar total kurkuminoid dihitung sebagai % kurkumin, karena kandungan kurkumin paling besar dibanding komponen kurkuminoid lainnya. Karena alasan tersebut beberapa penelitian baik fitokimia maupun farmakologi lebih ditekankan pada kurkumin (Muhsin, 2009).
Kurkumin memiliki aktifitas sebagai antiinflamasi pada penyakit osteoarthritis. Osteoartritis adalah penyakit reumatik dengan prevalensi yang terus meningkat sesuai dengan pertambahan usia. Secara klinis osteoartritis ditandai oleh nyeri, deformitas, pembesaran sendi, hambatan gerak; disamping itu juga terjadi inflamasi tingkat ringan sampai berat (Kalim, 1996; Rahardjo, 1994).
Ekstrak rimpang kunyit dengan kadar kurkuminoid 3,66 ± 0,65 % b/b dan 25 mL minyak atsiri rimpang temulawak yang mengandung kamfora, kamfen, kurkumin, bergamoten germakren B, kurserenon, germakron dan antorizol mampu menurunkan angka leukosit di dalam cairan sinovial penderita osteoarthritis. Sehingga produksi sitokin yang menyebabkan inflamasi menjadi berkurang (Kertia, Sudarsono, Imono, Mufrod, Catur, Rahardjo, dkk, 2005).
strukturnya sehingga senyawa ini disebutkan berasal dari penguraian karotenoid (Robinson, 1995).
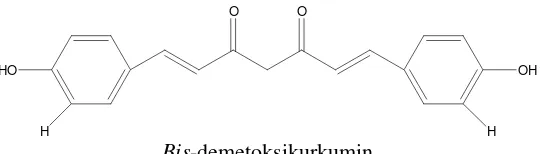
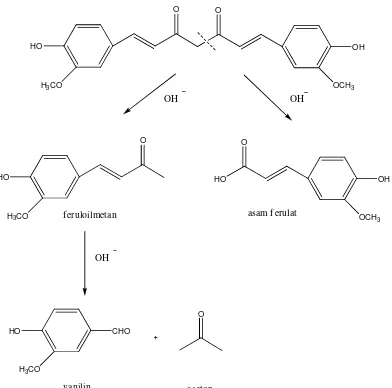
Kurkumin stabil pada pH dibawah 6,5; hal ini disebabkan adanya gugus metilen yang aktif. Produk degradasi kurkumin dalam lingkungan alkali (pH 7-10) akan menghasilkan asam ferulat dan feruloilmetan. Akibat degradasi ini, terjadi perubahan pada warna larutannya yaitu pada pH 7,5-9,1 larutan berwarna merah jingga (Tonnesen dan Karlsen, 1997). Reaksi degradasi kurkumin dalam kondisi basa ditunjukkan pada gambar berikut:
OH
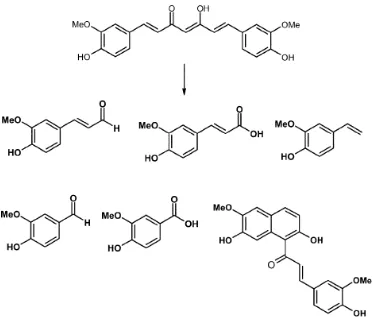
Selain itu, instabilitas kurkumin juga dipengaruhi oleh adanya cahaya yang menyebabkan terjadinya degradasi fotokimia. Prinsipnya, kurkumin tidak stabil terhadap cahaya, terutama dalam bentuk larutan. Setelah mengalami foto-iradiasi, akan terdeteksi produk siklisasi, sama halnya dengan produk dekomposisi asam vanilat, vanilin, dan asam ferulat (Sasakiet al., 1998). Produk fotodegradasi kurkumin ditunjukkan pada gambar berikut:
Gambar 3. Produk fotodegradasi kurkumin (Sasakiet al., 1998)
B. Kunyit
1. Kegunaan tanaman
Kunyit berkhasiat menyejukkan, membersihkan, mengeringkan, menghilangkan gatal dan menyembuhkan kesemutan. Bermanfaat sebagai antiinflamasi, antioksidan, antimikroba, pencegahan kanker, antitumor dan menurunkan kadar lemak darah dan kolesterol serta sebagai pembersih darah (Sumiati, 2010).
2. Kandungan kimia
Kunyit mengandung zat warna kuning yang disebut kurkuminoid sebanyak ≥ 33,9% (meliputi kurkumin 77%, demetoksikurkumin 17%, dan bidesmetoksikurkumin 3%), protein, fosfor, kalium, besi dan vitamin C (Anggarwal, 1995). Dari ketiga senyawa kurkuminoid tersebut, kurkumin merupakan komponen terbesar. Sering kadar total kurkuminoid dihitung sebagai % kurkumin, karena kandungan kurkumin paling besar dibanding komponen kurkuminoid lainnya Minyak atsiri (2-5%) terdiri dari seskuiterpen dan turunan fenil propan (turmeron, arilturmeron, ß-turmeron, kurkumol, atlantor, borneol, tumerol). Kunyit juga mengandung arabinosa, fruktosa, glukosa, pati, tannin, dammar, mineral, gom dan getah (Sumiati, 2010).
C. Obat Herbal Terstandar
Pasal 1 “obat herbal terstandar adalah sediaan obat bahan alam yang telah dibuktikan keamanan dan khasiatnya secara ilmiah dengan uji praklinik dan bahan bakunya telah di standarisasi. Logo untuk kelompok Obat Herbal Terstandar :”
Gambar 4. Logo obat herbal terstandar
Obat Herbal Terstandar (OHT) disajikan dari ekstrak atau penyarian bahan alam dapat berupa tanaman obat, binatang, maupun mineral. Obat Herbal Terstandar umumnya telah ditunjang dengan pembuktian ilmiah berupa penelitian-penelitian pra-klinik seperti standart pembuatan ekstrak tanaman obat, standart pembuatan obat tradisional yang higienis, dan uji toksisitas akut maupun kronis (PT. Phapros, 2005). Untuk menjaga kualitas bahan baku obat alam perlu dilakukan usaha budidaya dan standarisasi terhadap bahan baku tersebut, baik yang berupa simplisia maupun yang berbentuk ekstrak atau sediaan galenik (Badan Pengawas Obat dan Makanan Republik Indonesia, 2005).
D. Kapsul Obat Tradisional
Kapsul cangkang lunak umumnya terbuat dari gelatin. Cangkang gelatin lunak umumnya mengandung 6% hingga 13% air. Umumnya kapsul cangkang lunak diisi dengan cairan. Khususnya bahan aktif dilarutkan atau disuspensikan dalam bahan pembawa cair. Digunakan pula bahan pembawa minyak seperti minyak nabati. Keunggulan kapsul cangkang lunak adalah keseragaman kandungan dan disolusi obatnya lebih baik daripada kapsul berisi serbuk kering. Namun, kontak antara cangkang lunak atau keras dengan isi zat cair lebih besar dibandingkan dengan kapsul berisi serbuk kering (Departemen Kesehatan Republik Indonesia, 1995).
Pada industri kapsul lunak, ekstrak kering biasa dikombinasikan dengan minyak kedelai sebagai pembawa, beeswax sebagai agen pensuspensi dan pengental, dan lesitin sebagai lubrikan. Jumlah ekstrak dan bahan lain bergantung pada dosis ekstrak yang hendak diadministrasikan. Agen pensuspensi beRfungsi untuk mencegah pengendapan padatan dan menjaga homogenitas dalam kapsul. Agen pensuspensi yang banyak digunakan dengan basis minyak adalah wax, contohnya adalah beeswax, sedangkan polietilen glikol untuk basis tidak berminyak (Naguib, 2000).
E. Kromatografi Lapis Tipis Densitometri 1. Kromatografi Lapis Tipis secara umum
kedua fase (fase diam dan fase gerak). Dalam konteks kromatografi, nilai D didefinisikan sebagai perbandingan konsentrasi solut dalam fase diam (Cs) dan dalam fase gerak (Cm). Jadi semakin besar nilai D maka migrasi solut semakin lambat; dan semakin kecil nilai D maka migrasi solut semakin cepat. Solut akan terelusi menurut perbandingan distribusinya. Jika perbedaan perbandingan distribusi solut cukup besar maka campuran-campuran solut akan mudah dan cepat dipisahkan (Gandjar dan Rohman, 2007).
Kromatografi Lapis Tipis merupakan metode pemisahan komponen atas dasar perbedaan adsorbsi atau pelarut pengembang campur sangat dipengaruhi oleh macam dan polaritas zat-zat kimia yang dipisahkan (Mulja dan Suharman, 1995). Pemisahan dan pemurnian kandungan tumbuhan dapat dilakukan dengan menggunakan salah satu dari teknik kromatografi atau gabungan dari teknik kromatografi empat teknik kromatografi tersebut yakni kromatografi kertas, KLT, kromatografi gas cair dan kromatografi cair kinerja tinggi. Pemilihan teknik kromatografi sebagian besar tergantung pada sifat kelarutan dan keatsirian senyawa yang akan dipisahkan (Harborne, 1987).
Adsorpsi merupakan penyerapan pada permukaannya saja. Adsorpsi pada permukaan melibatkan interaksi-interaksi elektrostatik seperti ikatan hidrogen, penarikan dipol-dipol, dan penarikan yang diinduksi oleh dipol. Solut akan bersaing dengan fase gerak untuk berikatan dengan sisi-sisi polar pada permukaan adsorben. Adsorbsi solut oleh fase diam atau oleh adsorben sangat tergantung pada struktur kimia solute, ukuran partikel adsorben, dan kelarutan solut dalam fase gerak. Adanya gugus aktif tertentu yang berinteraksi dengan adsorben, ukuran partikel adsorben. Semakin kecil ukuran partikel adsorben, maka luas permukaannya semakin luas sehingga interaksinya dengan solut juga semakin luas. Solut yang semakin mudah larut dalam fase gerak akan semakin mudah lepas dari fase diam. Kedudukan gugus fungsional tertentu dalam suatu senyawa juga menentukan interaksinya. Sorpsi adsorpsi ini umumnya terjadi pada kromatografi padat cair sebagaimana dalam kromatografi lapis tipis dan pada kromatografi gas-padat (Gandjar dan Rohman, 2007).
2. Jenis fase diam KLT
Tabel.I
Tatanama lempeng KLT
Simbol/Singkatan Arti
“Sil” Suatu produk yang mengandung silika gel seperti Anasil dari pabrik Analabs
G Pengikat (lapisan halus) gipsum (CaSO4.½H2O) 60 Silika gel (dari E.Merck) yang mempunyai ukuran pori 60 A°
(10 A° = 1 nm)
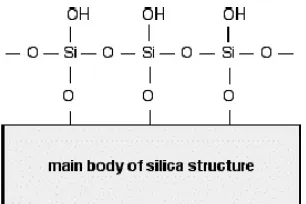
(Gandjar dan Rohman, 2007). Namun pada permukaan silika gel, atom silikon berlekatan pada gugus hidroksi. Jadi pada permukaan silika gel terdapat ikatan Si-O-H selain terdapat ikatan Si-O-Si. Permukaan silika gel sangat polar oleh karenanya gugus hidroksi dapat membentuk ikatan hidrogen dengan senyawa-senyawa yang sesuai disekitarnya, sebagaimana halnya gaya van der Waals dan atraksi dipol-dipol (Clark, 2007). Gambar ini menunjukkan bagian kecil dari permukaan silika:
Gambar 5. Ikatan hidrogen pada permukaan silika (Clark, 2007)
Semakin polar solut maka semakin tertahan kuat ke dalam adsorben silika gel ini. Solut-solut non polar tidak mempunyai afinitas atau mempunyai sedikit afinitas terhadap adsorben polar, sementara solut-solut yang terpolarisasi memiliki afinitas yang kecil terhadap adsorben polar disebabkan adanya interaksi dipol atau interaksi-interaksi yang diinduksi oleh dipol (Gandjar dan Rohman, 2007).
3. Jenis fase gerak KLT
Fase gerak dapat hampir segala macam pelarut atau campuran pelarut. Sistem campuran yang dipilih berdasarkan pustaka atau biasanya merupakan hasil uji coba dengan variasi tingkat kepolaran (Gritter, Bobbit and Scharting, 1991). Fase gerak dalam medium KLT merupakan medium angkut dan terdiri atas satu atau beberapa bahan pelarut yang bergerak dalam fase diam, karena gaya kapiler (Stahl, 1985). Campuran pelarut organik dipilih yang mempunyai polaritas serendah mungkin karena akan mengurangi serapan setiap komponen dari campuran pelarut. Jika komponen-komponen campuran mempunyai sifat polar tinggi akan mengubah sistem menjadi partisi (Sastrohamidjojo, 1985).
a. Kelarutan senyawa dalam pelarut. Bergantung pada besar atraksi antara molekul-molekul senyawa dengan pelarut.
b. Kemampuan senyawa melekat pada fase diam, misalnya gel silika. Tergantung pada bagaimana besar atraksi antara senyawa dengan gel silika (Clark, 2007).
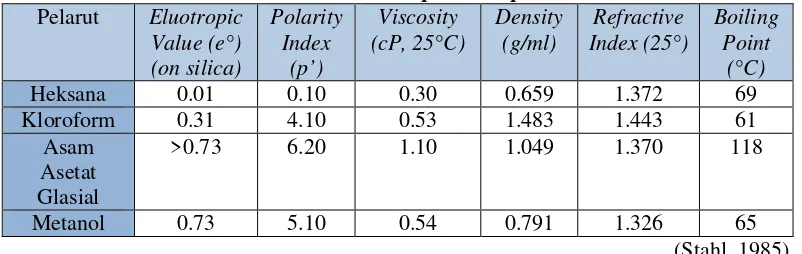
Tabel II. berikut ini menampilkan indeks polaritas beberapa pelarut yang sering digunakan:
Tabel II. Nilai indeks polaritas pelarut Pelarut Eluotropic
Heksana 0.01 0.10 0.30 0.659 1.372 69
Kloroform 0.31 4.10 0.53 1.483 1.443 61
Asam Asetat Glasial
>0.73 6.20 1.10 1.049 1.370 118
Metanol 0.73 5.10 0.54 0.791 1.326 65
(Stahl, 1985). 4. Aplikasi penotolan sampel
Pemisahan pada KLT yang optimal akan diperoleh jika menotolkan sampel dengan ukuran bercak sekecil dan sesempit mungkin. Sebagaimana dalam prosedur kromatografi yang lain, jika sampel yang digunakan terlalu banyak maka akan menurunkan resolusi. Reprodusibilitas diperoleh dengan volume sampel yang ditotolkan paling sedikit 0,5 µL. Jika volume sampel yang akan ditotolkan lebih besar dari 2-10 µL maka penotolan harus dilakukan secara bertahap dengan dilakukan pengeringan antar totolan (Gandjar dan Rohman, 2007).
5. Pengembangan
sebelumnya telah dijenuhi dengan uap fase gerak. Tepi bagian bawah lempeng lapis tipis yang telah ditotoli sampel dicelupkan ke dalam fase gerak kurang lebih 0,5-1 cm. Tinggi fase gerak dalam bejana harus dibawah lempeng yang telah berisi totolan sampel. Bejana kromatografi harus tertutup rapat dan sedapat mungkin volume fase gerak sedikit mungkin. Akan tetapi harus mampu mengelusi lempeng sampai ketinggian lempeng yang telah ditentukan. Penjenuhan fase gerak biasanya bejana dilapisi dengan kertas saring. Jika fase gerak telah mencapai ujung atas kertas saring, maka dapat dikatakan bahwa fase gerak telah jenuh. (Gandjar dan Rohman, 2007).
6. Penentuan kromatogram
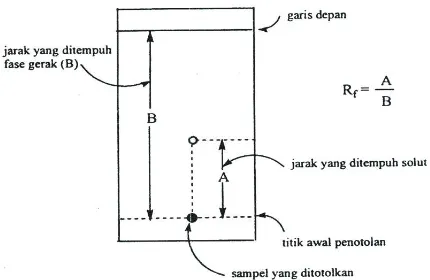
Data yang diperoleh dari KLT adalah nilai Rf yang berguna untuk identifikasi senyawa. Nilai Rf untuk senyawa murni dapat dibandingkan dengan nilai Rf dari senyawa standar. Nilai Rf dapat didefinisikan sebagai jarak yang ditempuh oleh senyawa dari titik asal dibagi dengan jarak yang ditempuh oleh pelarut dari titik asal (Clark, 2007).
Gambar 6. Ca Rf adalah 0 dan ini permukaan fase diam. 0,8 (Gandjar dan Rohm
Selama pemisa konsentrasi yang sim aliran fase gerak. Prof lahan akan melebar solut-solut melanjutka alasan bentuk puncak
Cara penentuan hargaRf(Gandjar dan Rohman
hitung dengan menggunakan perbandingan seba
ksimum Rf adalah 1 dan ini dicapai ketika sol ibusi (D) dan faktor retensi (k’) sama dengan
ngan kecepatan yang sama dengan fase gerak. ini teramati jika solut tertahan pada posisi m. Nilai Rfmemenuhi persyaratan bila berada ohman, 2007).
isahan kromatografi, solut individual akan me simetri atau dikenal juga dengan profil Gauss
rofil, dikenal juga dengan puncak atau pita, se r dan sering juga membentuk profil yang a utkan migrasinya ke fase diam. Prinsip yang me
ak dan pelebaran puncak dapat diringkas sebaga an, 2007)
sebagaimana dalam
(1) solut mempunyai an 0 yang berarti k. Nilai minimum posisi titik awal di da pada range
a. Sorpsi dan desorpsi solut yang terus menerus antara fase diam dan fase gerak, secara inheren akan menghasilkan profil konsentrasi Gaussian yang akan melebar karena solut bermigrasi lebih lanjut.
b. Perjalanan solut melalui partikel fase diam sedikit berbeda, sehingga menyebabkan profil konsentrasinya melebar secara simetris. Keadaan seperti ini disebut dengan pengaruh lintasan ganda (multiple-path effect).
c. Spesies solut menyebar ke segala arah dengan difusi ketika berada di dalam fase gerak. Difusi terjadi dengan arah yang sama dan berlawanan dengan aliran fase gerak (longitudinal or axial diffusion) karenanya akan berkontribusi terjadinya pelebaran pita secara simetris.
d. Sorpsi dan desorpsi, atau transfer massa antara fase diam dan fase gerak, bukanlah suatu proses yang instan dan terkadang proses tersebut terjadi secara lambat. Karena fase gerak berjalan secara terus-menerus, maka distribusi kesetimbangan solut yang sebenarnya tidak pernah terjadi . Profil konsentrasi dalam fase diam tertinggal sedikit dibanding profil konsentrasi dalam fase gerak yang akan mengakibatkan adanya pelebaran puncak lebih lanjut. Desorpsi yang lambat dapat juga menghasilkan puncak yang asimetris atau condong.
Gambar 7. Keadaan
Gambar 8. Ilustrasi 3 lintasan ganda (m Pengaru Profil konsent solut (D) konstan sel ditunjukkan oleh isote dalam fase diam (C Meskipun demikian, kur yakni membentuk pun
aan simetris dan pelebaran puncak kromatogram Rohman, 2007)
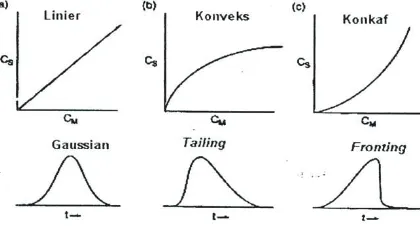
asi 3 prinsip utama yang menggambarkan puncak (multiple-path effect); (b). Pengaruh difusi longi aruh transfer massa (Gandjar dan Rohman, 2007) konsentrasi solut yang bermigrasi akan simetris jika
selama kisaran konsentrasi keseluruhan punca soterm sorpsi yang linier yang merupakan plot konse
(Cs) terhadap konsentrasi solut dalam fase n, kurva isoterm akan berubah menjadi 2 jenis punc
puncak yang berekor (tailing) dan adanya punc
(fronting) jika ada pe (Gandjar dan Rohman,
Gambar 9. Isoterm s linier (b). Puncaktai
Adanya pun pertama apabila ukura interaksi yang kuat ant terelusi sehingga da memiliki nilaiAssam 0,95-1,1 masih dikata (Gambar 10):
da perubahan rasio distribusi solut kearah ya an, 2007).
sorpsi serta profil-profil puncak yang dihasilkan tailingdan (c). Puncakfronting(Gandjar dan R puncak asimetri dapat disebabkan oleh beber ukuran sampel yang dianalisis terlalu besar. Yan
antara solut dengan fase diam dapat menyebabka dapat menyebabkan terbentuknya puncak y nya kontaminan dalam sampel yang dapat m menimbulkan puncak mendahului (fronting)
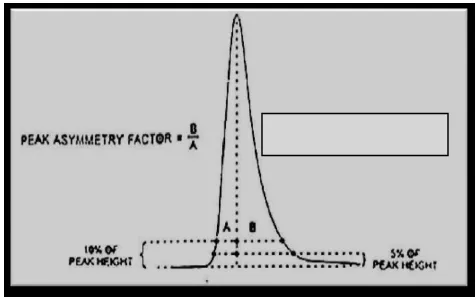
yang digunakan untuk menilai bentuk punc As), yang diukur pada 10% tinggi puncak. Pe sama dengan 1, sedangkan puncak dengan nilai katakan baik. Cara penentuan dapat diamati pada
Gambar 10. Penentuanpeak asymmetry(Snyder, Kirkland and Glajch, 1997) Resolusi didefinisikan sebagai perbedaan antara Z2 dan Z1 (Z1 sebagai
max Rf1 dan Z2 sebagai max Rf2) dibagi dengan rata-rata lebar puncak 0,5 (W1 +
W2). Nilai resolusi dapat dihitung dengan cara sebagai berikut:
Rs =
, ( ) (2)
Dari persamaan ini dapat diketahui bahwa yang sangat berpengaruh terhadap pemisahan suatu komponen adalah max Rfmasing-masing solut (max Rf1
dan max Rf2) serta lebar puncak masing-masing komponen yang dipisahkan (W1
dan W2). W1 dihitung dari selisih nilai end Rf1 dikurangi start Rf1. W2 dihitung
dari selisih nilai end Rf2 dikurangi start Rf2. Nilai Rs harus mendekati atau lebih
Gambar 11. Pemisahan dua senyawa (Sherma and Fried, 1996)
Nilai reprodusibilitas dapat dihitung dari nilai koefisien variansi (KV). Secara umum, nilai KV dikatakan reprodusibel apabila ≤ 2. Perhitungan niali koefisien variasi (KV) sebagai berikut:
% KV = × 100% (3)
7. Kromatografi lapis tipis kuantitatif
metode ini dilakukan dengan mengukur intensitas warna bercak dari senyawa standar adalah murni, inert dan stabil (Sastrohamidjojo, 1985).
Pemantulan ini akan bersifat selektif bila sinar yang digunakan adalah sinar monokromatis, biasanya dipilih sinar pada panjang gelombang yang sesuai dengan warna bercak yang diteliti. Alat densitometer ini mempunyai sumber sinar yang bergerak diatas bercak pemisahan pada lempeng kromatogram yang akan ditetapkan kadar komponennya. Bercak kecil menghasilkan puncak yang sempit dan tajam (Sudjadi, 1988).
Teknik pengukuran dapat didasarkan atas pengukuran intensitas sinar yang diserap (absorbansi), intensitas sinar yang dipantulkan (reflaktansi) atau intensitas sinar yang difluoresensikan (fluoresensi). Teknik pengukuran berdasarkan refleksi di mana sinar datang sebagian diserap dan sebagian lagi dipantulkan (Mintarsih, 1990).
Sifat pemantulan ini akan menjadi sensitif dan selektif bila sinar yang datang adalah monokromatis. Disini biasanya dipilih sinar pada panjang gelombang yang diserap atau dipantulkan paling banyak oleh noda yang diteliti. Banyaknya sinar yang direfleksikan akan ditangkap oleh suatu alat yang disebut reflection photomultiplier yang akan diteruskan ke pencatat atau rekorder untuk diubah menjadi suatu puncak atau kromatogram. Luas puncak atau tinggi puncak sesuai dengan konsentrasi senyawa pada noda yang diukur kerapatannya (Mintarsih, 1990).
penelusuran lurus, sinar yang mengenai bercak berjalan lurus dari kiri ke kanan, sedangkan pada penelusuranzig-zag, sinar yang mengenai bercak berjalanzig-zag dari kiri ke kanan. Besarnya jarak, naik turunnya sinar dapat diatur menurut kebutuhan, yang diperhitungkan dengan besar kecilnya bercak, yang dalam operasi alat dikenal sebagai lebar penelusuran (scan widht) (Mintarsih, 1990).
Penelusuran bercak akan mendapatkan hasil yang baik apabila dilakukan pada panjang gelombang maksimum, karena perubahan konsentrasi pada bercak sedikit saja sudah terdeteksi. Pengukuran dilakukan dengan menelusuri bercak yang akan ditetapkan kadarnya pada kisaran panjang gelombang zat tersebut (Mintarsih, 1990).
Pelat yang digunakan untuk KLT pada densitometri sebaiknya digunakan pelat buatan pabrik, karena pada pelat buatan sendiri fase diamnya kurang kompak sehingga akan mempengaruhi hasil penelusuran dengan densitometri, yaitu berupa puncak yang lebar dan kasar. Puncak yang lebar disebabkan kurang kompaknya fase diam, sedangkan puncak yang kasar disebabkan permukaan pelat yang kurang rata. Pada umumnya tebal lapisan tipis pada lempeng yang digunakan adalah 0,20-0,25 mm maksimum 0,33 mm, untuk mengurangi efek hamburan sinar yang disebabkan oleh fase diam terhadap linearitas hubungan serapan dan konsentrasi dari senyawa yang diteliti (Mintarsih, 1990).
F. Landasan Teori
demetoksikurkumin, dan bis-demetoksikurkumin. Kurkumin merupakan senyawa aktif yang terdapat dalam rimpang kunyit (Curcuma domestica). Produk-produk OHT yang beredar di pasaran mengandung kurkuminoid dari kunyit. OHT merupakan sediaan obat bahan alam yang telah dibuktikan keamanan dan khasiatnya secara ilmiah dengan uji praklinik dan bahan bakunya telah di standarisasi. Sediaan OHT dikemas dengan berbagai macam, salah satunya menggunakan kapsul lunak. Kapsul lunak ini memiliki keunggulan yakni dapat mempertahankan stabilitas dari zat aktif yang terdapat dalam sediaan. Produk OHT tidak hanya mengandung satu senyawa tunggal tetapi juga senyawa-senyawa yang lain.
Metode KLT densitometri dapat digunakan untuk analisis kualitatif dan
G. Hipotesis
29
Penelitian ini merupakan jenis rancangan penelitian eksperimental dua tingkat karena pada subjek uji diberikan dua perlakuan yaitu jenis dan komposisi fase gerak.
B. Variabel 1. Variabel bebas
Variabel bebas dalam penelitian ini ialah jenis dan perbandingan komposisi fase gerak yaitu kloroform p.a. : asam asetat glasial p.a. dan heksan p.a.: asam asetat glasialp.a.: kloroformp.a.
2. Variabel tergantung
Variabel tergantung pada penelitian ini ialah pemisahan peak kurkumin dalam kapsul lunak OHT Rheumakur®yang dilihat dari bentukpeak, nilaiRf, dan nilai resolusi.
3. Variabel pengacau terkendali
a. Kemurnian pelarut yang digunakan. Untuk mengatasinya digunakan pelarut yangpro analysisyang memiliki kemurnian tinggi.
c. Paparan cahaya terkait kurkumin yang fotosensitif. Untuk mengatasinya saat preparasi ditutup denganaluminium foil.
C. Definisi Operasional
1. Kurkumin merupakan senyawa aktif yang berada dalam sampel kapsul lunak OHT Rheumakur®.
2. Kromatografi Lapis Tipis dengan fase diam silika gel G60 dan fase gerak
kloroformp.a.:asam asetat glasial p.a.; heksanp.a.: kloroformp.a.:asam asetat glasialp.a.
3. Optimasi dilakukan dengan mengubah-ubah jenis dan komposisi fase gerak. 4. Parameter pemisahan komponen dengan KLT densitometri adalah bentukpeak,
nilai faktor retardasi, nilai resolusi.
D. Bahan Penelitian
Bahan yang digunakan dalam penelitian ini adalah baku kurkumin (hasil sintesis Prof. Dr. Sudibyo Martono, M.S., Apt yang telah dikonfirmasi strukturnya dengan metode spektroskopi 1H-NMR dan Mass Spectra, kurkumin hasil sintesis tersebut memiliki titik lebur 181,2-182,4 °C), metanol p.a. EMSURE®ACS, ISO, Reag. Ph Eur (E. Merck), kloroformp.a.EMSURE®ACS , ISO, Reag. Ph Eur (E. Merck), heksan p.a. EMSURE®ACS (E. Merck), asam asetat glasial p.a. EMPARTA®ACS (E. Merck), lempeng KLT silika gel G60 20 x 20 (E. Merck),
E. Alat Penelitian
Alat yang digunakan dalam penelitian ini meliputi neraca, neraca analitik (OHAUS Carat Series PAJ 1003, max 60/120 g, min 0,001 g, d=0,01/0,1 mg, e=1 mg), Densitometer (CAMAC TLC Scanner 3 CAT. No. 027.6485 SER. No.160602), maserasi mekanis (Hotplate Stirer Lab Tech Model: LMS-1003, V OHS = 220 V 50 Hz, Wats=500 W 3A, Serial No. 08210004), labu takar 5,00 mL, labu takar 25,00 mL, Erlenmeyer 10,00 mL, cawan arloji, pipet mikro volume 0,1-2 μL, pipet mikro volume 1-10 mL, corong, flakon, pipet tetes, beaker glass, sendok, pengaduk, magnetik stirer, bejana kromatografi.
F. Tata Cara Penelitian 1. Pembuatan pelarut (metanolp.a.pH 4)
Metanol p.a. ditambah dengan asam asetat glasial p.a. tetes demi tetes sampai pH 4. Cek dengan pH indikator.
2. Pembuatan larutan baku kurkumin
a. Pembuatan larutan stok. Menimbang kurang lebih seksama sebanyak 10 mg kurkumin. Masukkan dalam labu takar 10 ml dan tambahkan metanol pH 4 hingga batas tanda.
3. Preparasi sampel
Satu kapsul lunak OHT Rheumakur® dikeluarkan isinya dan ditimbang dengan seksama lebih kurang 0,05 gram. Masukkan ke dalam erlenmeyer dan dilarutkan ke dalam 5 mL metanol pH 4. Kemudian diaduk dengan magnetik stirer selama 15 menit dengan kecepatan 60 rpm menggunakan maserasi mekanis. Ekstrak disaring dan filtrat diencerkan dengan metanol pH 4 sampai 5,00 mL. Larutan ini siap untuk ditotolkan.
4. Penentuan panjang gelombang maksimum (λmaks)
Tiga seri larutan baku kurkumin (100 ppm, 300 ppm, dan 500 ppm) dengan replikasi tiga kali masing-masing konsentrasi baku ditotolkan sebanyak 1 L pada lempeng silika gel G60 berukuran 12 x 12 cm. Kemudian segera
dikembangkan dalam bejana kromatografi yang telah dijenuhi dengan fase gerak kloroform p.a.:metanol p.a. (48:2). Pengembangan dilakukan setinggi 10 cm. Segera keluarkan lempeng silika gel dan keringkan. Penentuan panjang gelombang maksimum dilakukan dengan merekam pola spektra pada daerah panjang gelombang 400-500 nm menggunakan KLT densitometer.
5. Optimasi metode KLT Densitometri
Tabel III. Jenis dan Komposisi Fase Gerak Fase gerak Heksan
p.a.
Kloroformp.a. Metanolp.a. Asam asetat glasialp.a.
Komposisi I - 48 2
-Komposisi II - 9,5 - 0,5
Komposisi III 5 4,875 - 0,125
Komposisi IV 0,5 8,5 - 1
b. Optimasi pemisahan kurkumin dari kapsul lunak OHT Rheumakur®. Tiga seri larutan baku kurkumin dan larutan kapsul lunak OHT Rheumakur® ditotolkan sebanyak 1 L pada lempeng silika gel G60 berukuran 5 x 12 cm.
Kemudian segera dikembangkan dalam bejana kromatografi yang telah dijenuhi oleh jenis dan komposisi fase gerak yang akan dioptimasi. Pengembangan dilakukan setinggi 10 cm. Segera keluarkan lempeng silika gel, dikeringkan dan secepatnya discanning dengan panjang gelombang maksimum dari hasil point 4 dengan KLT densitometer.
c. Reprodusibilitas dari fase gerak hasil optimasi. Pembuatan larutan seri baku kurkumin (100 ppm, 300 ppm, dan 500 ppm) maupun sampel kapsul lunak OHT Rheumakur® direplikasi sebanyak 3 kali. Ulangi langkah kerja point 3.b. dengan fase gerak hasil optimasi. Hitung nilai KV dari nilai resolusi pada kapsul lunak OHT Rheumakur®yang didapat dari 3 kali replikasi.
G.Analisis Hasil
1. Bentuk peak yang baik ialah simetris ditentukan dari nilai faktor asimetri (As) dapat dihitung dengan cara sebagai berikut:
dimana: As= faktor asimetris
B = lebar setelah puncakpeakpada ketinggian 10% dari bawah A = lebar sebelum puncakpeakpada ketinggian 10% dari bawah 2. Nilai Rfdapat dihitung dengan cara sebagai berikut:
Rf = (4)
dimana: Rf= faktor retardasi
a = jarak rambat bercak yang dihasilkan oleh fase gerak b = jarak rambat elusi fase gerak
3. Nilai resolusi dapat dihitung dengan cara sebagai berikut:
(5) dimana: Rs = nilai resolusi
Z1= max Rf1
Z2= max Rf2
W1= selisih nilai end Rf1dikurangi start Rf1
W2= selisih nilai end Rf2dikurangi start Rf2
4. Nilai % koefisien variansi dari resolusi dihitung dengan cara sebagai berikut: (6)
dimana: % KV = koefisien variansi SD = standard deviasi
35
Optimasi jenis dan komposisi fase gerak ini bertujuan untuk mendapatkan pemisahan kurkumin dari senyawa-senyawa lain dalam sediaan kapsul lunak OHT Rheumakur®. Jenis dan komposisi fase gerak yang akan dioptimasi dalam penelitian ini ada empat, seperti tertera pada tabel IV. Perbedaan jenis dan komposisi fase gerak ini bertujuan untuk mendapatkan pemisahan kurkumin dalam kapsul lunak obat herbal terstandar Rheumakur®yang optimum.
Tabel IV. Nilai Indeks Polaritas dari Jenis dan Komposisi Fase Gerak Fase gerak Heksan
Komposisi III 5 4,875 - 0,125 2,12
Komposisi IV 0,5 8,5 - 1 4,11
Pemilihan variasi jenis dan komposisi fase gerak ini didasarkan pada pada penelitian terdahulu yakni kloroform:metanol dengan perbandingan 48:2 (Paramasivam, dkk; 2008). Indeks polaritas pada komposisi I ini sebesar 4,14. Dalam fase gerak kloroform:metanol (48:2), kloroform menjadi senyawa yang non polar dengan indeks polaritas 4,1 dan metanol menjadi senyawa polar dengan indeks polaritas 5,1.
sebesar 6,2 lebih besar dari indeks polaritas metanol 5,1. Pengembangan lain dari fase gerak ini yaitu dengan penambahan heksan yang bertujuan untuk penambahan senyawa non polar. Heksan p.a. merupakan senyawa yang paling non polar (IP = 0,1) diantara kloroform (IP = 4,1) dan asam asetat glasialp.a.(IP = 6,2).
Perbedaan komposisi fase gerak untuk mendapatkan perbedaan nilai indeks polaritas dan profil kromatogram. Semakin besar nilai indeks polaritas dari jenis dan komposisi fase gerak menunjukkan campuran fase gerak tersebut semakin polar. Pada tabel 4, komposisi II memiliki indeks polaritas paling besar diantara komposisi fase gerak lain. Hal ini menunjukkan komposisi fase gerak II bersifat paling polar. Sedangkan komposisi III memiliki indeks polaritas paling kecil. Hal ini menunjukkan komposisi fase gerak III bersifat paling non polar diantara komposisi fase gerak lain.
B. Pembuatan Metanolp.a.pH 4
C. Pembuatan Larutan Baku
Optimasi fase gerak dengan metode kromatografi ini menggunakan larutan baku kurkumin yang bertujuan untuk mendeteksipeak yang terdapat pada sampel ialah peak kurkumin. Hal ini ditunjukkan dari faktor retardasi (Rf) yang terdapat pada baku kurkumin sama atau mendekati Rf yang terdapat pada sampel. Larutan baku kurkumin dibuat dengan pelarut metanol p.a. pH 4 yang memiliki kemurnian tinggi. Pada penelitian ini digunakan tiga level konsentrasi baku yaitu 100 ppm, 300 ppm, dan 500 ppm. Pembuatan tiga level konsentrasi baku kurkumin untuk mengetahui respon (AUC) pada tiga level konsentrasi baku kurkumin dan mengetahui AUC sampel berada pada konsentrasi baku rendah, sedang atau tinggi.
D. Preparasi Sampel
Pada preparasi sampel dilakukan penyaringan yang bertujuan agar senyawa-senyawa yang tidak larut metanol tertinggal pada kertas saring.
E. Penentuan Panjang Gelombang Maksimum(λmaks) Baku Kurkumin dengan KLT Densitometri
Penentuan panjang gelombang serapan maksimum bertujuan untuk memperoleh besar area di bawah kurva (AUC) kurkumin yang paling maksimum. Penentuan panjang gelombang maksimum dilakukan bersamaan ketika bercak di-scan dengan alat densitometer. Pengukuran pada panjang gelombang serapan maksimum akan memberikan respon yang lebih sensitif dan stabil. Panjang gelombang maksimum ini akan memberikan perubahan absorbansi untuk setiap satuan konsentrasi paling besar. Selain itu, pada panjang gelombang maksimum, kesalahan yang terjadi pada pengulangan pengukuran adalah yang paling kecil.
Gambar 12. Gugus kromofor dan auksokrom pada struktur kurkumin Pengukuran λmaks pada penelitian ini menggunakan konsentrasi 100ppm,
300ppm, dan 500ppm dengan replikasi 3 kali masing-masing konsentrasi. Penentuan λmaks ini dilakukan dengan menggunakan fase gerak yaitu
kloroform:metanol (48:2). Pengukuran λmaks menggunakan tiga level konsentrasi
baku dengan replikasi tiga kali masing-masing konsentrasi dengan tujuan dapat meyakinkan bahwa yang diperoleh benar-benar panjang gelombang dari senyawa kurkumin. Penentuan λmaksdengan merekam pola spektra larutan baku kurkumin
pada panjang gelombang 400-500 nm. Hasil pengukuran λmaks yang didapat
dengan replikasi 3 kali dari masing-masing konsentrasi sesuai dengan teori yaitu 425 nm (Paramasivam, dkk; 2008) dan tidak terjadi pergeseran.
Tabel V. Data pengukuran panjang gelombang serapan maksimum kurkumin Replikasi Baku 100 ppm Baku 300 ppm Baku 500 ppm
I 425 nm 425 nm 425 nm
II 425 nm 425 nm 425 nm
Keterangan: A= replikasi I, II, dan III baku kurkumin 100 ppm B= replikasi I, II, dan III baku kurkumin 300 ppm C= replikasi I, II, dan III baku kurkumin 500 ppm
Gambar 13. Kromatogram panjang gelombang maksimum baku kurkumin 100, 300 500ppm masing-masing direplikasi 3 kali
F. Optimasi Pemisahan Kurkumin dalam Kapsul Lunak OHT Rheumakur®dengan KLT Densitometri
Pemisahan kurkumin dalam kapsul lunak OHT Rheumakur® menggunakan sistem kromatografi adsorpsi fase normal. Prinsip kromatografi ini ialah sorpsi-adsorpsi. Sorpsi merupakan proses pemindahan solut dari fase gerak ke fase diam sedangkan proses sebaliknya dinamakan desorpsi. Kedua proses ini terjadi secara terus menerus selama pemisahan kromatografi dan diharapkan
C
B
terjadi kesetimbangan distribusi yang dinamis antara fase diam dan fase gerak. Adsorpsi merupakan penyerapan pada permukaannya saja. Adsorpsi pada permukaan melibatkan interaksi-interaksi elektrostatik seperti interaksi hidrogen, penarikan dipol-dipol, dan penarikan yang diinduksi oleh dipol. Fase normal yang dimaksudkan yaitu fase diam lebih polar daripada fase gerak. Gambar.15 menunjukkan gugus polar dan non polar dari kurkumin.
Kurkumin
Gambar 14. Gugus polar dan non polar kurkumin Keterangan: = gugus non polar
= gugus polar
Fase diam yang digunakan dalam penelitian ini ialah silika gel G60.Silika
H3CO
Gambar 15. Interaksi fase diam dengan kurkumin
Pada tahap optimasi fase gerak dielusi dengan jarak rambat yang sama sehingga apabila ada perbedaan pada hasil yang diperoleh maka perbedaan tersebut dapat disimpulkan karena perbedaan fase gerak yang digunakan. Jarak rambat yang digunakan untuk mengelusi yaitu 10 cm, hal ini bertujuan untuk mengoptimalkan pemisahan kurkumin dari senyawa-senyawa lain yang terdapat dalam sediaan kapsul lunak OHT Rheumakur®.
Tabel VI. Pemisahan pada berbagai jenis dan komposisi fase gerak No. Jenis dan Komposisi Fase
Gerak
Baku/sampel As Rf Rs Keterangan
1 Komposisi I,
kloroform:metanol (48:2)
Baku 100 ppm
0,90 0,38 - Bentukpeak tidak
0,85 0,66 - Bentukpeak tidak
0,96 0,09 - Bentukpeak simetris
sampel - 0,04 0,20
0,99 0,08
0,99 0,80 - Bentukpeak simetris
tiga peak. Kemungkinan peak selain kurkumin merupakan turunan lain dari kurkuminoid yaitu demetoksikurkumin dan bisdemetoksikurkumin. Turunan lain dari kurkuminoid ini memiliki kepolaran yang mirip dengan kurkumin sehingga ketika dilarutkan dengan metanol p.a. pH 4 turunan lain dari kurkuminoid ini larut.
1. Fase gerak kloroform p.a.:metanol p.a. dengan perbandingan 48:2 (komposisi I)
Komposisi fase gerak I merupakan komposisi fase gerak dari penelitian Paramasivam, dkk; 2008. Komposisi fase gerak ini memiliki indeks polaritas sebesar 4,14. Berikut gambar kromatogram peak baku kurkumin dan pemisahan kurkumin dari kapsul OHT Rheumakur®:
Gambar 16.Peakbaku kurkumin konsentrasi 300 ppm danpeakpemisahan dari kurkumin dalam kapsul lunak OHTRheumakur®dengan fase gerak kloroformp.a.:metanolp.a.
(48:2). Keterangan A. Baku kurkumin konsentrasi 300 ppm (konsentrasi sedang) B. Pemisahan dari kurkumin dalam kapsul lunak OHTRheumakur®
Pada komposisi fase gerak Ipeakkromatogram baik pada baku maupun sampel kapsul lunak OHT Rheumakur® tidak simetris, lebar, dan tumpul ditunjukkan pada gambar 17. Nilai As berada dibawah 0,95 ditunjukkan pada tabel VI. Pada gambar 17 terlihat bahwa peak kromatogram yang dihasilkan asimetri. Hal ini menunjukkan ikatan kurkumin dengan fase diam lebih besar daripada dengan fase gerak. Komposisi fase gerak ini belum memiliki kepolaran yang sesuai sehingga belum dapat memisahkan kurkumin dari senyawa lain yang terdapat dalam kapsul lunak OHT Rheumakur®secara sempurna.
Untuk mengetahui komposisi fase gerak yang optimum dilakukan dua cara yaitu meningkatkan dan menurunkan nilai indeks polaritas. Kedua cara ini dilakukan agar dapat melihat profil kromatogram baik baku maupun sampel kapsul lunak OHT Rheumakur®. Peningkatan nilai indeks polaritas dengan mengganti metanol dengan asam asetat glasial. Asam asetat glasial memiliki indeks polaritas yang lebih besar dibanding metanol. Asam asetat glasial memiliki
indeks polaritas sebesar 6,3 sedangkan metanol memiliki indeks polaritas sebesar 5,1. Asam asetat glasial memiliki kekuatan untuk mengelusi kurkumin yang terdapat dalam fase diam lebih besar dibandingkan metanol. Hal ini ditunjukkan dari nilai eluotropik asam asetat glasial 0,73 sedangkan nilai eluotropik metanol sebesar 0,73 (Stahl, 1995). Selain itu, asam asetat glasial berfungsi untuk menjaga stabilitas dari kurkumin.
Cara kedua dengan mengurangi kepolaran dari fase gerak pertama yaitu dengan menambahkan komposisi heksan. Heksan merupakan senyawa non polar dengan indeks polaritas sebesar 0,1. Indeks polaritas semakin kecil menunjukkan bahwa senyawa tersebut semakin non polar. Dengan penambahan senyawa ini diharapkan kurkumin dapat terelusi dan lebih berikatan dengan fase gerak.
2. Fase gerak kloroform p.a.:asam asetat glasial p.a. dengan perbandingan 9,50:0,50 (komposisi II)
Gambar 17.Peakbaku kurkumin konsentrasi 300 ppm danpeakpemisahan dari kurkumin dalam kapsul lunak OHT Rheumakur®dengan fase gerak kloroform p.a.:asam asetat glasialp.a.(9,50:0,50). Keterangan A. Baku kurkumin konsentrasi
300 ppm (konsentrasi sedang) B. Pemisahan dari kurkumin dalam kapsul lunak OHT Rheumakur®
Pada komposisi fase gerak ini peak kromatogram yang didapat tidak simetris ditunjukkan pada gambar 18. NilaiAspada tabel VI berada dibawah 0,95. Pada gambar 18 terlihat bahwa peak kromatogram yang dihasilkan asimetri. Hal ini menunjukkan ikatan kurkumin dengan fase diam masih lebih besar daripada dengan fase gerak. Namun, peak yang didapat lebih sempit dan tajam dibandingkan komposisi fase gerak I.
A
Penambahan komposisi fase gerak lebih polar belum dapat menghasilkan pemisahan yang sempurna terutama pada sampel kapsul lunak OHT Rheumakur®. Untuk memperbaiki komposisi fase gerak tersebut maka dilakukan penurunan kepolaran dengan penambahan heksan.
3. Fase gerak heksan p.a.:kloroform p.a.:asam asetat glasial p.a. dengan perbandingan 5:4,875:0,125 (komposisi III)
Komposisi fase gerak III memiliki indeks polaritas sebesar 2,13. Komposisi fase gerak ini memiliki indeks polaritas yang paling rendah dibandingkan dengan keempat komposisi fase gerak yang lain. Indeks polaritas rendah menunjukkan bahwa komposisi pada fase gerak tersebut semakin non polar. Berikut gambar kromatogram peak baku kurkumin dan pemisahan kurkumin dari kapsul OHT Rheumakur®:
Gambar 18.Peakbaku kurkumin konsentrasi 300 ppm danpeakpemisahan dari kurkumin dalam kapsul lunak OHT Rheumakur®dengan fase gerak heksan p.a.:kloroformp.a.:asam asetat glasialp.a.(5:4,875:0,125). Keterangan A. Baku kurkumin konsentrasi 300 ppm (konsentrasi sedang B. Pemisahan dari kurkumin
dalam kapsul lunak OHT Rheumakur®
Pada komposisi fase gerak III peak kromatogram yang didapat simetri, sempit, dan tajam ditunjukkan pada gambar 19. Nilai As pada tabel VI berada 0,95-1,10. Namun nilai Rf baik baku maupun sampel dibawah 0,2. Kemungkinan besar interaksi kurkumin dengan fase diam lebih kuat daripada kurkumin pada fase gerak. Kenonpolaran dari komposisi fase gerak ini tidak sesuai dengan kurkumin sehingga hanya sedikit yang mampu terabsorpsi.
Untuk memperbaiki komposisi fase gerak tersebut maka dilakukan pengurangan komposisi dari heksan dan menambah komposisi asam asetat glasial. Hal ini bertujuan agar komposisi fase gerak yang dihasilkan lebih polar dan dapat mencapai kesetimbangan distribusi yang dinamis antara fase diam dan fase gerak.
4. Fase gerak heksan p.a.:kloroform p.a.:asam asetat glasial p.a. dengan perbandingan 0,5:8,5:1,0 (komposisi IV)
Komposisi fase gerak IV memiliki indeks polaritas sebesar 4,11. Indeks polaritas pada komposisi ini lebih besar dibandingkan dengan komposisi fase gerak III. Berikut gambar kromatogram peak baku kurkumin dan pemisahan kurkumin dari kapsul OHT Rheumakur®:
Gambar 19.Peakbaku kurkumin konsentrasi 300 ppm danpeakpemisahan dari kurkumin dalam kapsul lunak OHT Rheumakur®” dengan fase gerak heksan
p.a.:kloroformp.a.:asam asetat glasialp.a.(0,5:8,5:1,0). Keterangan A. Baku kurkumin konsentrasi 300 ppm (konsentrasi sedang) B. Pemisahan dari kurkumin
dalam kapsul lunak OHT Rheumakur®
A
Pada komposisi fase gerak IV peak kromatogram yang didapat simetris, sempit dan tajam. Pada tabel VII ditunjukkan baik pada baku maupun sampel nilai As berada dalam range 0,95-1,10, nilai Rf berada dalam range 0,2-0,8, nilai resolusi yang didapat 2,45. Nilai resolusi telah memenuhi baseline resolution lebih dari 1,5. Dari kelima komposisi fase gerak, komposisi fase gerak IV memenuhi kriteria pemisahan yang paling baik.
Setelah mendapat jenis dan komposisi fase gerak yang optimum yaitu heksan:kloroform:asam asetat glasial (0,5:8,5:1) dilakukan replikasi baik pada baku kurkumin maupun sampel sebanyak tiga kali dan dikembangkan pada fase gerak yang optimum. Hal ini bertujuan untuk melihat reprodusibilitas dari pemisahan kurkumin dari kapsul lunak OHT Rheumakur®. Reprodusibilitas pemisahan kurkumin dari kapsul lunak OHT Rheumakur® dilihat dari nilai resolusi yang didapat. Ketiga replikasi pemisahan kurkumin dari kapsul lunak OHT Rheumakur® dengan fase gerak heksan:kloroform:asam asetat glasial (0,5:8,5:1) ditunjukkan pada gambar berikut:
Gambar 20. Tiga replikasipeakpemisahan dari kurkumin dalam kapsul lunak OHT Rheumakur®dengan fase gerak heksanp.a.:kloroformp.a.:asam asetat glasial
p.a.(0,5:8,5:1,0). Keterangan A=Replikasi 1, B=Replikasi 2, C= Replikasi 3 B
Tabel VII. Parameter pemisahan dan nilai koefisien variansi (KV) dari nilai resolusi ketiga replikasi dengan komposisi fase gerak IV, heksan:kloroform:asam asetat
glasial (0,5:8,5:1,0)
No. Replikasi Baku/sampel As Rf Rs KV Keterangan
1 I Baku 100
Adapun interaksi kurkumin dengan fase gerak pada komposisi IV ini ditunjukkan pada gambar berikut:
Gambar 21. Interaksi kurkumin dengan fase gerak heksanp.a.: kloroformp.a.: asam asetat glasial p.a (0,5:8,5:1,0)
55 A. Kesimpulan
Jenis dan komposisi fase gerak yang optimum yang dapat memberikan bentukpeakyang simetris, sempit, dan tajam; nilai Rfberada dalam range 0,2-0,8; nilai resolusi ≥1,5; dan nilai KV dari nilai resolusi ≤ 2 untuk memisahkan kurkumin dalam kapsul lunak OHT Rheumakur® dengan metode KLT densitometri ialah heksan p.a. :klorofom p.a. :asam asetat glasial p.a. dengan perbandingan 0,5:8,5:1.
B. Saran
1. Perlu dilakukan validasi metode penetapan kadar kurkumin kapsul lunak OHT Rheumakur® dengan metode KLT densitometri fase normal dalam kondisi optimal.
56
Badan Pengawas Obat dan Makanan Republik Indonesia, 2005, Standarisasi Ekstrak Tumbuhan Obat Indonesia Salah Satu Tahapan Penting dalam Pengembangan Obat Asli Indonesia,Info POM, 6 (4), 1-5.
Clark, J., 2007, Kromatografi Lapis Tipis, diakses dari http://www.chem-is-try.org/materi_kimia/instrumen_analisis/kromatografi1/kromatografi_lap is_tipis, diakses tanggal 1 November 2010.
Direktorat Jenderal Pengawasan Obat dan Makanan RI, 1995, Farmakope Indonesia, jilid IV, Departemen Kesehatan Republik Indonesia, Jakarta, 34, 150.
Gandjar I.G. dan Rohman A., 2007, Kimia Farmasi Analisis, 353, 356, 360-361, Pustaka Pelajar, Yogyakarta.
Gritter, J.R., Bobbit, J.M., and Scharting, A.E, 1991, Pengantar Kromatografi, diterjemahkan oleh Kosasih Pamawinata, Edisi II, 109-112, 140-147, Penerbit ITB, Bandung.
Gupta, A. P., Gupta, M. M., Kumar, S., 1999, Simultaneous determination of curcuminoids in curcuma samples using high performance thin layer chromatography,http://203.190.147.121/bitstream/123456789/80/1/J_Jou rnal_Liquid_Chromatography_Related_Technologies_22_1561.pdf, diakses tanggal 10 Februari 2010.
Harborne, J. B., 1987,Metode Fitokimia : Penuntun Cara Modern Menganalisis Tumbuhan, diterjemahkan oleh Kosasih Padmawinata, hal. 27, ITB, Bandung.
Harmita, 2004, Petunjuk Pelaksanaan Validasi Metode dan Cara Perhitungannya, Majalah Ilmu Kefarmasian, Vol.I, No.3, Desember 2004, 122.
dan pendaftaran obat tradisional, Departemen Kesehatan Republik Indonesia, Jakarta, 6.
Kementerian Kesehatan Republik Indonesia, 1994, Lampiran Kepmenkes Nomor 661/Menkes/SK/VII/1994 Tentang Persyaratan Obat Tradisional, Departemen Kesehatan RI, Jakarta, 9.
Kertia, N., Sudarsono, Imono, A.D., Mufrod, Catur., E., Rahardjo, P., dkk, 2005, Pengaruh pemberian kombinasi minyak atsiri temulawak dan ekstrak kunyit dibandingkan dengan piroksikam terhadap angka leukosit cairan sendi penderita dengan osteoarthritis lutut, Majalah Farmasi Indonesia 16 (3), 156-160.
Majeed, M., Vladimir Badmaev, M.D., Uma Shivakumar, and R. Rajendran, M.S., 1995, Curcuminoids antioxidantphytonutrient, Nutriscience Publisher, Inc., New Jersey : Piscataway, USA, pp. 24-27, 69-71.
Martono, 1996, Penentuan kadar kurkumin secara kromatografi lapis tipis-densitometri, Buletin ISFI Yogyakarta, Vol. 2, No. 4, April 1996, 11-21. Mintarsih, E. R. R., 1990,Penetapan Kadar Alkaloid Kinina dalam Akar, Batang,
dan Daun Chinchona Succirubra Pavon et Klotzch dari Daerah Kaliurang secara Spektrodensitometri (TLC-Scanner), Skripsi, Fakultas Farmasi, UGM, Yogyakarta.
Muhsin, B., 2009, Khasiat Kunyit, diakses dari
http://spesifikasihabbatussauda.blogspot.com/2009/09/khasiatkunyit.html , diakses tanggal 10 Oktober 2010.
Mulja, M. dan Suharman, 1995, Analisis Instrumental, Universitas Airlangga, Surabaya, hal.26.
Naguib, Y., 1998, Soft Gel Capsule: An Elegant & Versatile Dosage Form, diakses dari info@vitaminretailer.com, diakses tanggal 14 November 2010.
Paramasivam, M., Aktar, W., Poi, R., Banerjee, H., Bandyopahyay, A., 2008, Occurrence of curcuminoids in Curcuma longa:A quality standardization byHPTLC,diakses
darihttp://www.banglajol.info/index.php/BJP/article/viewFile/833/913, diakses tanggal 10 Februari 2010.
Phapros, 2005, Penggolongan Obat Tradisional, diakses dari http://www.ptphapros.co.id/article.php, diakses tanggal 10 Oktober 2010. Rahardjo, P., 1994, Masalah dan Penanganan Osteoartritis, Konggres Ahli
Robinson, T., 1995, Kandungan Organik Tumbuhan Tinggi, Edisi 6, terjemahan Kosasih Pandmawinata, hal. 164, ITB, Bandung.
Sasaki, S.S., Sat, K., Abe, M., Sugimoto, N., & Maitani, T, 1998, Components of turmeric oleoresin preparations and photo-stability of curcumin., Jpn. J. Food Chem., 5(1).
Sastrohamidjojo, H., 1985, Kromatografi, Edisi I, Liberty, Yogyakarta, 32.
Sherma, J. and Fried, B., 1996,Handbook of Thin Layer Chromatography, Marcel Dekker, Inc. New, pp. 56, 57.
Snyder, L.R., Kirkland, J.J., and Glajch, J.L., 1997, Practical HPLC Method Development, 2ndEdition, JohnWiley & Sons, Inc., New York, pp. 690. Stahl, E., 1985, Drug Analysis by Chromatography and Microscopy, Penerbit
ITB, Bandung, pp. 1-8.
Stankovic, 2004, Curcumin Chemical and Technical Assessment (CTA), JECFA 61st edition, FAO, ftp://ftp.fao.org/es/esn/jecfa/cta/CTA_61_Curcumin .pdf, diakses tanggal 2 Desember 2010.
Sudjadi, 1988,Metode Pemisahan, Fakultas Farmasi UGM, Yogyakarta, hal.175. Sumiati, T., 2010, Keunggulan dan Manfaat Kunyit diakses dari
http://id.shvoong.com/lifestyle/2005091-keunggulan-dan-manfaatkunyit/, diakses tanggal 29 Oktober 2010.
Tonnesen, H.H and Karlsen J., 1997, Recent Development In The Use of Curcumin As A Potential Drug, in Pramono S (ed): Recent development in curcumin pharmacochemistry: Procedding of The International Symposium of Curcumin Pharmacochemistry (ISCP), 27-38, Aditya Media, Yogyakarta.
WHO, 2003, Traditional medicine, diakses dari
Lampiran 3. Sistem KLT-Densitometri yang digunakan
Sistem KLT-Densito yang digunakan pada penelitian ini adalah sebagai berikut:
Stationary phase
Plate size (X x Y) 5,0 x 12,0 cm
Material TLC plates silica gel G
Manufacturer E. MERCK KGaA
Pre-washing Yes
Drying device Oven
Temperature 105ºC
Time 60 Minutes
Calibration parameters
Calibration mode Single level
Statistics mode CV
Avaluation mode Peakarea
Sample application-Nanomat / Manual device
Instrument Graduated Disposable Micropipettes First application position X 10,0 mm
Application position Y 15,0 mm Distance between tracks 10,0 mm Application volume 1,000μl Development – Glass tank
Chamber type Twin Trough Chamber 20x20 cm Mobile phase Cloroform : Methanol (48:2)
Cloroform : Acetic Acid Glacial (9,50:0,50) Heksane Cloroform : Acetic Acid Glacial (5:4,875:0,125)
Heksane Cloroform : Acetic Acid Glacial (0,5:8,5:1,0)
Solvent front position 100,0 mm
Volume 25,0 mL
Drying device Oven
Temperature 60ºC
Time 5 Minutes
Detection – CAMAG TLC Scanner 3
Instrument CAMAG TLC Scanner 3
“Scanner3_160602” S/N 160602 (1. 14.28) Scan start pos. Y 15,0 mm
Scan end pos. Y 115,0 mm
Slit dimensions 8,00 x 0,90 mm, Macro Optimize optical system Light
Scanning speed: 20 mm/s Data resolution 100μm/step Measurement Table
Lamp D2 & W Measurement Type Remission Measurement Mode Absorption Optical filter Second order
Detector mode Automatic
PM high voltage 312 V Detector properties
Y-position for 0 adjust 15,0 mm Track # for 0 adjust 0
Analog Offset 10%
Sensitivity Automatic (27)
Integration Properties
Data filtering Savitsky-Golay 7 Baseline correction Lowest Slope Peakthreshold min. slope 5
Peakthreshold min. height 10 AU Peakthreshold min. area 50 Peakthreshold max. height 700 AU
Display scaling 700
Lampiran 4. Perhitungan kepolaran fase gerak
Diketahui :
Kloroform dengan indeks polaritas = 4,1 Metanol dengan indeks polaritas = 5,1
Asam asetat glasial dengan indeks polaritas = 6,2 Heksan dengan indeks polaritas = 0,1
Fase gerak :
1. Kloroform : metanol = 48:2
2. Kloroform : asam asetat glasial = 9,50 : 0,50
3. Heksan : kloroform :asam asetat glasial = 5 : 4,875 : 0,125
Lampiran 5. Penimbangan baku dan sampel serta contoh perhitungan kadar seri baku
Penimbangan baku kurkumin
Berat Orientasi Replikasi I Replikasi II Replikasi III Berat Zat 0,0100 gram 0,0101 gram 0,0100 gram 0,0100 gram
Penimbangan sampel Berat zat 0,0500 gram 0,0501 gram 0,0500 gram 0,0500 gram
Contoh perhitungan larutan seri baku awal : Cstok = = 1000 ppm
Larutan seri baku baku awal a. Larutan seri baku 100 ppm
C1V1= C2V2
1000 ppm x 0,5 mL = C2x 5 mL
C2= 100 ppm
b. Larutan seri baku 300 ppm C1V1= C2V2
1000 ppm x 1,5 mL = C2x 5 mL
c. Larutan seri baku 500 ppm C1V1= C2V2
1000 ppm x 2,5 mL = C2x 5 mL
C2= 500 ppm
Lampiran 6. Kromatogram pada fase gerak kloroform : metanol (48:2) 1. Kromatogram baku kurkumin 100 ppm
2. Kromatogram baku kurkumin 300 ppm
Lampiran 7. Kromatogram pada fase gerak kloroform : asam asetat glasial (9,50:0,50)
1. Kromatogram baku kurkumin 100 ppm
2. Kromatogram baku kurkumin 300 ppm
Lampiran 8. Kromatogram pada fase gerak heksan : kloroform : asam asetat glasial (5:4,875:0,125)
1. Kromatogram baku kurkumin 100 ppm
2. Kromatogram baku kurkumin 300 ppm
Lampiran 9. Kromatogram pada fase gerak heksan : kloroform : asam asetat glasial (0,5:8,5:1,0)
1. Kromatogram baku kurkumin 100 ppm
2. Kromatogram baku kurkumin 300 ppm