SKRIPSI
Oleh : IWAN FERDIANA
NPM : 0333010054
PROGRAM STUDI TEKNOLOGI PANGAN FAKULTAS TEKNOLOGI INDUSTRI
UNIVERSITAS PEMBANGUNAN NASIONAL “VETERAN” JATIM SURABAYA
PEMBUATAN TAUWA KACANG HIJAU DENGAN
PENGGUMPAL GLUCONO DELTA LACTONE (GDL)
Proposal Penelitian
Diajukan Untuk Melengkapi Tugas – tugas dan Memenuhi Syarat – syarat Guna Mencapai
Gelar Sarjana Teknologi Pangan
Oleh : IWAN FERDIANA
NPM : 0333010054
PROGDI TEKNOLOGI PANGAN FAKULTAS TEKNOLOGI INDUSTRI
UNIVERSITAS PEMBANGUNAN NASIONAL “VETERAN” JAWA TIMUR
KATA PENGANTAR
Dengan mengucapkan rasa syukur Alhamdulillah kehadirat Allah SWT
yang telah memberikan rahmat dan karuniaNya, sehingga penyusun dapat menyelesaikan skripsi dengan judul “PEMBUATAN TAUWA KACANG HIJAU DENGAN PENGGUMPAL GLUCONO DELTA
LACTONE (GDL) ”.
Penyusunan skripsi ini dimaksudkan untuk memenuhi persyaratan dalam menyelesaikan perkuliahan pada Jurusan Teknologi Pangan di Fakultas Teknologi Industri, Universitas Pembangunan Nasional “Veteran” Jawa Timur, untuk meraih gelar Sarjana (S1) Teknologi Pangan.
Dalam penyusunan dan penulisan skripsi ini tentunya tidak terlepas dari bimbingan, dukungan serta motivasi dari berbagai pihak. Melalui kesempatan ini, dengan segala kerendahan hati dan rasa hormat penyusun mengucapkan terima kasih yang sebesar-besarnya kepada :
1. Bapak Ir. Sutiyono, MT. selaku Dekan Fakultas Teknologi Industri, Universitas Pembangunan Nasional “ Veteran “ Jawa Timur.
3. Dra. Jariyah MP, selaku dosen pembimbing I, yang telah meluangkan waktu untuk memberikan arahan dan bimbingan pada penyusun dalam penyusunan skripsi ini.
4. Ir. Titi Susilowati, MT, selaku dosen pembimbing II, yang telah meluangkan waktu untuk memberikan arahan dan bimbingan pada penyusun dalam penyusunan skripsi ini.
5. Ir. Sri Winarti, MP, , selaku dosen Penguji seminar proposal dan hasil, yang telah memberikan saran dan kritik pada penyusun
6. Rosida, STP, MP, selaku dosen wali.
7. Pak Samingan, mas Taufik, yang telah banyak membantu selama di laboratorium.
8. Bapak, Ibu, dan Adiku serta semua keluargaku yang telah membantu dalam segala hal, mendukung dan mendo’akan dalam kelancaran penyusunan skripsi. 9. Keluarga Besar Mahapala, teman-teman angkatan 2003 dan adik kelas, terima
kasih untuk suport dan bantuannya.
Penyusun menyadari bahwa dalam penyusunan skripsi ini masih jauh dari sempurna dan masih banyak kekurangan karena terbatasnya pengetahuan penyusun, untuk itu dengan segala kerendahan hati penyusun mengharapkan kritik dan saran yang membangun dari pembaca guna sempurnanya skripsi ini. Semoga skripsi ini bermanfaat untuk pembaca dan seluruh pihak yang membutuhkan.
Surabaya, Desember , 2009
DAFTAR ISI
Halaman
KATA PENGANTAR………... i
DAFTAR ISI………. iii
DAFTAR TABEL………. vi
DAFTAR GAMBAR……… vii
DAFTAR LAMPIRAN……… viii
INTISARI……….. ix
BAB I PENDAHULUAN A. Latar Belakang……… 1
B. Tujuan………. 3
C. Manfaat………... 3
BAB II TINJAUAN PUSTAKA A. Kacang Hijau……….………. 4
B. Protein...………... 6
C. Denaturasi Protein…..………. 7
D. pH Isoelektrik………...………. 8
E. GDL...……… 9
F. Tauwa... 10
G. Analisis Keputusan………. 13
I. Landasan Teori……… 17
J. Hipotesis……….. 21
BAB III METODE PENELITIAN A. Tempat dan Waktu Pelaksanaan………. 22
B. Bahan……….. 22
C. Alat………. 22
D. Rancangan Percobaan………. 23
E. Parameter……… 26
F. Prosedur Penelitian………. 27
BAB IV HASIL DAN PEMBAHASAN A. Analisa Bahan Baku ……… 30
B. Hasil pH awal susu Kacang hijau…..………. 30
C. Hasil Tauwa susu Kacang Hijau 1. pH Penggumpala susu Kacang Hijau……….. 31
2. Randemen………. 33
3. Sineresis...……… 35
4. Kadar Protein...………... 38
D. Hasil Uji Organoleptik 1. Rasa………... 39
2. Aroma……….... 41
3. Tekstur……… 42
E. Analisis Keputusan……….. 43
BAB V KESIMPULAN DAN SARAN
A. Kesimpulan………... 50 B. Saran………... 50 DAFTAR PUSTAKA
DAFTAR TABEL
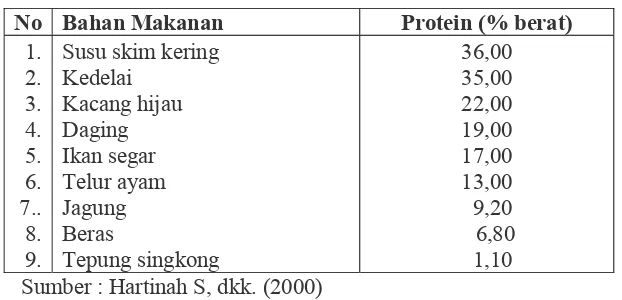
Halaman Tabel 1. Perbandingan Antara Kadar Protein Kacang Hijau
Dengan beberapa Bahan Makanan lain………...… 5 Tabel 2. Kandungan unsur gizi pada kacang hijau………..……… 6 Tabel 3. pH Susu kacang hijau………..…………...….. 30 Tabel 4. Rerata pH penggumpalan tauwa kacang hijau dari perlakuan
Penambahan air dan konsentrasi GDL ..…………..………….. 31 Tabel 5. Rerata nilai randeman tauwa kacang hijau penambahan air dan
konsentrasi GDL ……… 33 Tabel 6. Rerata nilai sineresis tauwa kacang hijau dari perlakuan
Penambahan air dan konsentrasi GDL...……….. 35 Tabel 7. Rerata kadar protein tauwa kacang hijau pengaruh perlakuan
penambahan air...……….……….. 38 Tabel 8. Rerata kadar protein tauwa kacang hijau pengaruh perlakuan
Konsentrasi GDL... ……….. 39 Tabel 9. Nilai rata-rata uji Rangking Rasa Tauwa Kacang Hijau
dengan perlakuan Penambahan air dan konsentrasi GDL...…. 40 Tabel 10. Nilai rata-rata uji Rangking Aroma Tauwa Kacang Hijau
dengan perlakuan Penambahan air dan konsentrasi GDL... 41 Tabel 11. Nilai rata-rata uji Skoring Tekstur Tauwa Kacang Hijau
dengan perlakuan Penambahan air dan konsentrasi GDL... 42 Tabel 11. Hasil analisis keseluruhan pada produk Tauwa Kacang
DAFTAR GAMBAR
Halaman
Gambar 1. Mekanisme pH isoelektris...……….... 9
Gambar 2. Pembentukan GDL...……….... 10
Gambar 3. Struktur Kimia Glucono Delta Lactone (GDL)……...……..…. 11
Gambar 4. Diagram Alir pembuatn Curd……...……..…. 13
Gambar 5. Skema pH asam amino...……...……..…. 19
Gambar 6. Reaksi kiamia pengaruh asam ...……...……..…. 20
Gambar 7. Diagram Alir pembutan larutan penggumpal...…....…. 27
Gambar 8. Diagram Alir pembutan Tauwa...……..…. 29
Gambar 9. Hubungan perlakuan penambahan air dan konsentrasi GDL terhadap pH tauwa kacang hijau …...…... 32
Gambar 10. Hubungan perlakuan penambahan air dan konsentrasi GDL terhadap randeman tauwa kacang hijau... 35
Gambar 11. Hubungan perlakuan penambahan air dan konsentrasi GDL terhadap sineresis tauwa kacang hijau... 36
DAFTAR LAMPIRAN
Halaman Lampiran 1. Prosedur analisis……… 51 Lampiran 2. Lembar kuisioner uji organoleptik……… 53 Lampiran 3. Data hasil pengamatan dan analisis pH
penggumpalan tauwa kacang hijau………...…… 54 Lampiran 4. Data hasil pengamatan dan randeman tauwa kacang
hijau………...…… 56 Lampiran 5. Data hasil pengamatan dan analisis sineresis tauwa
kacang hijau………...…… 58 Lampiran 6. Data hasil pengamatan dan analisis Kadar Protein
tauwa kacang hijau………...…... 60 Lampiran 7. Data hasil Uji Organolepti rasa (Metode Hedonik)
tauwa kacang hijau ………...…... 62 Lampiran 8. Data hasil Uji Organolepti aroma (Metode Hedonik)
tauwa kacang hijau………...…... 64 Lampiran 9. Data hasil Uji Organolepti Tekstur (Skoring)
tauwa kacang hijau ………...…... 66 Lampiran 11. Perhitungan Net Percen Value (NPV) dan
PEMBUATAN TAUWA KACANG HIJAU DENGAN
PENGGUMPAL
GLUCONO DELTA LACTONE
(GDL
IWAN FERDIANA NPM : 0333010054
INTISARI
Tauwa merupakan minuman yang dibuat dari susu kedelai dari proses penggumpalan protein kedelai. Penelitian ini merupkan pengembangan pembuatan tauwa yang menggunakan bahan baku kacang hijau dengan penggumpal Glucono Delta Lactone (GDL). Permasalahan yang dihadapi dalam pembuatan tauwa kacang hijau adalah ketepatan penambahan air dan konsentrasi GDL. Penelitian ini bertujuan mengetahui perbandingan kacang hijau : air dan konsentrasi GDL terhadap kualitas tauwa kacang hijau yang dihsilkan.
Metode penelitian menggunakan Rancangan Acak Lengkap (RAL) pola faktorial dengan dua faktor dan tiga kali ulangan. Faktor pertama : Penambahan air pembautan susu kacang hijau ( 300 ml; 450 ml; dan 600 ml) dan faktor kedua : konsentrsi GDL (2%b/bb, 3%b/bb dan 4%b/bb). Data yang diperoleh diuji dengan Anova dan apabila terdapat beda nyata antar perlakuan, maka dilajutkan dengan uji Duncan.
Hasil penelitian menunjukan perlakuan yang terbaik adalah perlakuan dengan perbandingan kacang hijau dengan air 600 ml dan konsentrasi GDL 3 %. Perlakuan tersebut menghasilkan tauwa kacang hijau dengan pH penggumpalan 4,65 rendemen 296,0818 % sineresis 0,2115 g/j kadar protein 6,1187% tingkat kesukaan rasa 144,5(sangat suka), aroma 142 (sangat suka) dan skor tekstur 82.
BAB I PENDAHULUAN
A. Latar Belakang
mengkonsumsi makanan dari kacang hijau kebutuhan gizi akan protein dapat terpenuhi. Dari hasil penelitian Santosa, (2003) telah dibuat tauwa dengan bahan baku kedelai dengan proporsi kacang hijau dan penambahan tapioka dengan menggunakan penggumpal CaSO4.
Penggunaan penggumpal CaSO4 akan meninggalkan residu sulfat yang dapat menbahayakan konsumen, yaitu dapat menyebabkan iritasi pada saluran pernapasan (Saputra,2009), sedangkan unsur Ca dapat menyebabkan ganggun batu ginajal pada saluran kencing (Djoko, 2003). Dari hal tersebut kami mengunnakan GDL sebagai bahan penggumpal. Menurut Jungbunzlaur (2008), GDL meurupakan bahan alami berupa glucono acid dalam bentuk kristal tidak menimbulkan efek terhadap kesehatan dapat digunakan sebagai penggumpalkan protein pada proses pembuatan tahu.
Berdasarkan uraian tersebut diatas, maka perlu adanya penelitian penggunaan GDL sebagai penggumpal dan konsentrasi susu kacang hijau terhadap mutu tauwa kacang hijau yang di hasilkan.
B. Tujuan Penelitian
1. Untuk mengetahui pengaruh penambahan air dan konsentrasi GDL terhadap kualitas tauwa.
2. Untuk mengetahui perlakuan terbaik kombinasi penambahan air dan konsentrasi GDL terhadap tauwa kacang hijau yang dihasilkan.
C. Manfaat
1. Hasil penelitian ini dapat memberikan informasi tentang pembuatan tauwa dari bahan baku kacang hijau dan penggumpal GDL
BAB II
TINJAUAN PUSTAKA
B. KACANG HIJAU
Kacang hijau (Mungbean) merupakan tanaman yang mempunyai potensi
pasar yang cukup menjanjikan karena masih dapat dikembangkan lebih lanjut.
Kacang hijau merupakan sumber protein, karbohidrat, vitamin dan mineral yang
penting bagi manusia serta mempunyai kandungan gizi yang cukup tinggi
(Andrianto,2004) .
Menurut Siswono (2004), protein kacang hijau kaya akan asam amino
leusin, arginin, isoleusin, valin dan lisin. Kualitas protein kacang hijau seperti
halnya kacang-kacangan yang lain dibatasi oleh kandungan asam amino bersulfur
seperti metionin dan sistein. Kendati demikian, dibandingkan jenis kacang
lainnya, kandungan metionin dan sistein pada kacang hijau masih relatif lebih
tinggi. Keseimbangan asam amino pada kacang hijau mirip dan sebanding dengan
kedelai. Kandungan lemak dalam kacang hijau relatif sedikit (1-1,2 persen).
Keadaan ini menguntungkan, sebab dengan kandungan lemak yang rendah,
kacang hijau dapat disimpan lebih lama dibandingkan kacang-kacangan lainnya.
Lemak kacang hijau sebagian besar tersusun atas asam lemak tidak jenuh oleat
(20,8 persen), linoleat (16,3 persen) dan linolenat (37,5 persen). Linoleat dan
linolenat merupakan asam lemak esensial yang sangat diperlukan bagi
Kacang hijau juga mengandung vitamin dan mineral yang penting untuk
tubuh manusia. Mineral seperti kalsium, fosfor, besi, natrium dan kalium banyak
terdapat pada kacang hijau. Kalsium banyak terdapat pada bagian kulit biji, diikuti
bagian lembaga dan paling sedikit pada bagian kotiledon. Sebaliknya fosfor
banyak terdapat pada bagian lembaga. Zat besi paling banyak terdapat pada
bagian embrio dan kulit biji. Vitamin yang paling banyak terkandung pada
kacang hijau adalah thiamin (B1), riboflavin (B2) dan niasin (B3). Protein kacang
hijau kaya akan asam amino lisin (Kosman, 2007). Perbandingan antara kadar
protein kacang hijau den beberapa bahan makanan lain dapat
dilihat pada Tabel 1
Tabel 1. Perbandingan antara kadar protein kacang hijau dengan beberapa bahan makanan lain
No Bahan Makanan Protein (% berat) Sumber : Hartinah S, dkk. (2000)
Vitamin yang menonjol pada kacang hijau adalah B1 . Pada 100 gr biji
kacang hijau mengandung 150 – 400 I.U. (Internasional Unit) . Menurut Seran
dan Masniah, (2005), kacang hijau mempunyai kandungan vitamin dan asam
aimino yang tinggi dalam bahan sangat dibutuhkan oleh tubuh. kandungan unsur
Tabel 2. Kandungan unsur gizi pada kacang hijau Sumber : Adrianto, 2005.
B. PROTEIN
Protein merupakan suatu zat makanan yang amat penting bagi tubuh,
dapat berfungsi sebagai bahan bakar dalam tubuh juga sebagai zat pembangun dan
pengatur. Asam amino penyusun protein sangat bervariasi, hal ini menyebabkan
protein sangat bervariasi. Protein yang banyak mengandung asam amino (yang
bersifat asam) seperti glutamat atau aspartat, protein tersebut mempunyai titik
isoelektrik rendah, sebaliknya jika mengandung asam amino yang bersifat basa
seperti garam netral misalnya magnesium atau kalsium titik isoelektriknya
berubah dari semula (Suhardi, 1988).
Menurut Suhardi (1988) dan Fennema (1985). Protein sering mengalami
perubahan sifat setelah mengalami perlakuan tertentu, meskipun sangat ringan dan
belum mengakibatkan pemecahan ikatan kovalen (peptida). Protein yang
mengalami denaturasi akan memberikan berbagai perubahan dalam beberapa hal
yaitu :
2. Penurunan kelarutan
3. Aktifitas biologis sebagai enzim turun atau hilang sama sekali
4. Kristalisasi tidak mungkin terjadi
5. Viskositas naik
6. Rotasi larutan protein meningkat.
a. Denaturasi Perotein
Denaturasi adalah perubahan struktur protein dimana pada keadaan
terdenaturasi penuh, hanya struktur primer protein saja yang tersisa, protein tidak
lagi memiliki struktur sekunder, tersier dan quarter (Sugiran, 2007)
.Menurut Suhardi (1988), denaturasi dapat disebabkan oleh berbagai faktor
yaitu bahan, pH, garam dan pengaruh permukaan. Proses denaturasi dapat
menyebabkan flokulasi protein tetapi dapat juga mengakibatkan terbentuknya gel.
Denaturasi dan koagulasi protein merupakan aspek kestabilan bahan yang dapat
berkaitan dengan susunan dan urutan asam amino dalam.
Pemanasan adalah penyebab terjadinya denaturasi secara umum,
keberhasilan denaturasi dengan pemasan dipengaruhi oleh berbagai faktor :
konsentrasi protein, pH, dan kekuatan ion (Fennema, 1985). Menurut Syamsir
(2009), Koagulan adalah bahan yang digunakan untuk mendenaturasi protein
didalam susu kedelai sehingga dihasilkan curd (gumpalan tahu). Jenis koagulan
yang digunakan antara lain kalsium/magnesium-klorida; kalsium sulfat;
glukano-D-laktone; dan koagulan asam (asam laktat, asam asetat).
Kalsium/magnesium-klorida akan menghasilkan tahu dengan flavor sangat baik; pembentukan curd
tekstur tahu cenderung kasar. Kalsium sulfat merupakan koagulan yang paling
umum digunakan. Koagulan ini kelarutannya didalam air lambat sehingga
pembentukan curd juga berlangsung lambat. Daya ikat airnya tinggi, sehingga
rendemen tahu yang dihasilkan akan lebih banyak daripada Ca/Mg-klorida dan
tekstur tahunya halus. Glucano-D-laktone merupakan koagulan asam, memiliki
daya ikat air yang tinggi, dan membentuk tahu dengan tekstur seperti gel dan
flavor sedikit asam. Koagulan ini biasa digunakan untuk membuat tahu sutra.
Sementara itu, koagulan asam (asam laktat, asam asetat) memberikan rendemen
yang rendah, dengan tekstur tahu yang rapuh (mudah hancur) dan flavor agak
asam.
b. pH Isoelektris
Titik isoelektrik adalah pH larutan asam amino (protein) dimana molekul
tidak menunjukkan tidak adanya perpindahan medan listrik. Pada keadaan
tersebut kelarutan asam amino paling rendah. Pada protein yang banyak
mengandung asam amino (yang bersifat asam) seperti glutamat atau aspartat,
protein mempunyai titik isoelektrik rendah sebaliknya jika mengandung asam
amino yang bersifat basa misalnya magnesium atau kalsium titik isoelektrik
tinggi (Suhardi,1989).
Secara kimia dapat dikatakan bahwa proses pembuatan tahu adalah
pengendapan protein yang terdapat dalam sari kedelai pada titik
Isoelektris.(SII,1990 dalam Mryam 2007). Menurut Suhardi, (1988). muatan
listrik mempengaruhi kelarutan protein, pada pH selain pada titik isoelektriknya
muatan antar molekul mengecil dan akhirnya sangat kecil, molekul-molekul
saling berdampingan, menbentuk agregat dan mengendap. Sifat kelarutan protein
dalam air dipengaruhi oleh ikatan hidrogen dalam air dangan protein, pH
lingkungan di luar pH isoelektrik.
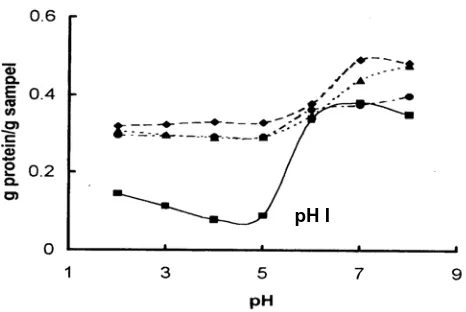
Protein akan mengalami kekeruhan terbesar pada saat mencapai pH
isoelektris yaitu pH dimana protein memiliki muatan positif dan negatif yang
sama, pada saat inilah protein mengalami denaturasi yang ditandai kekeruhan
meningkat dan timbulnya gumpalan. (Poejiadi,1994). Gambar 1. mekanisme pH
isoelektris
Gambar 1. Mekanisme pH isoelektris (Subagio,2002).
C. GDL (Glucano Delta Lactone)
Menurut Obatolu, (2006). Tahu adalah curd yang berasal dari susu kedelai
dengan penggumpal mengunakan suatu garam (CaCl2 atau CaSO4) atau suatu
asam (glucano delta lactone). Penggumpal dapat memproduksi gel protein susu
kedelai. dengan air terikat, lemak kedelai dan pendukung dalam susunan curd.
Glucono delta lactone adalah hasil kristalisasi dari glucano acid. Untuk
keperluan tertentu GDL digunakan untuk mengontrol pH. GDL merupakan
molekul yang tersusun atas C6H10O6 dengan berat melekul 178,15 g/mol. Tahu
sutera merupakan susu kedelai yang diproduksi dengan GDL. Menurut Sarwono,
(2004). GDL merupakan bahan penggumpal yang dapat dicampurkan ke dalam
sari kedelai dingin dengan jumlah sedikit, kemudian dapat dimasukan dalam
wadah dan ditutup rapat kemudian dicelupkan dalam air bersuhu 85o – 95oC selama 30 – 50 menit. Pengaruh panas akan mengaktifkan lactone sehingga
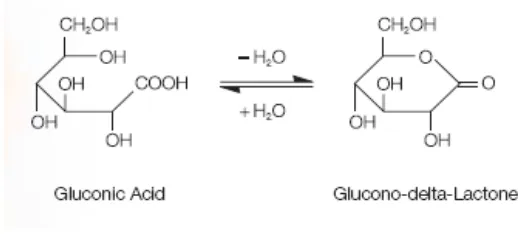
terbentuk tahu yang bagus tanpa harus memisahkan air tahu. Dibawah ini adalah
proses terbentuknya GDL pada gambar 1 dan struktur kimia GDL pada gambar 2.
Gambar 2. Pembentukan GDL, Jungbunzlauer, (2008).
Gambar 3. Struktur kimia Glucano delta lactone (GDL) , Jungbunzlauer, (2008). 1/2O2 -H2O
D. TAUWA
Tauwa (tahwa) merupakan minuman yang dibuat dari susu kedelai
(Novie, 2009). Tauwa terbentuk dari proses pengumpalan protein kedelai berupa
gel (puding) . Faktor yang mempengaruhi pembuatan tauwa adalah proses
penggumpalan ekstrak protein susu kacang hijau. Tauwa merupakan curd yang
terbentuk dari hasil pencampuran antara penggumpal dengan ekstrak susu kacang
hijau
Menurut Susilowati (1989). pada prinsipnya cara pembuatan tahu sutera
sama dengan pembuatan tahu biasa. Perbedaannya, pada pembuatan tahu sutera
bahan penggumpal yang digunakan adalah GDL dengan konsentrasi sangat rendah
yaitu 0,2 – 0,3 persen dari jumlah susu kedelai yang digunakan. Tahu sutera
merupakan hasil penggumpalan (curd) yang tidak mengalami pengepresan dan
pemisahan cairan.
Menurut Koswara (1992). proses pembuatan curd susu kedelai dari hasil
reaksi dengan penggumpal CaSO4
1. Timbang biji kedelai bersih. Rendam dalam air 8 - 12 jam , selama
perendaman air diganti-ganti
2. Atuskan biji kedelai, larutkan dengan 8-10 berat kedelai dalam blender
selama 5 menit dengan kecepatan tinggi
3. Bubur kedelai disaring dan filtratnya dimasak
4. Penggumpalan dilakukan dengan penambahan CaSO4
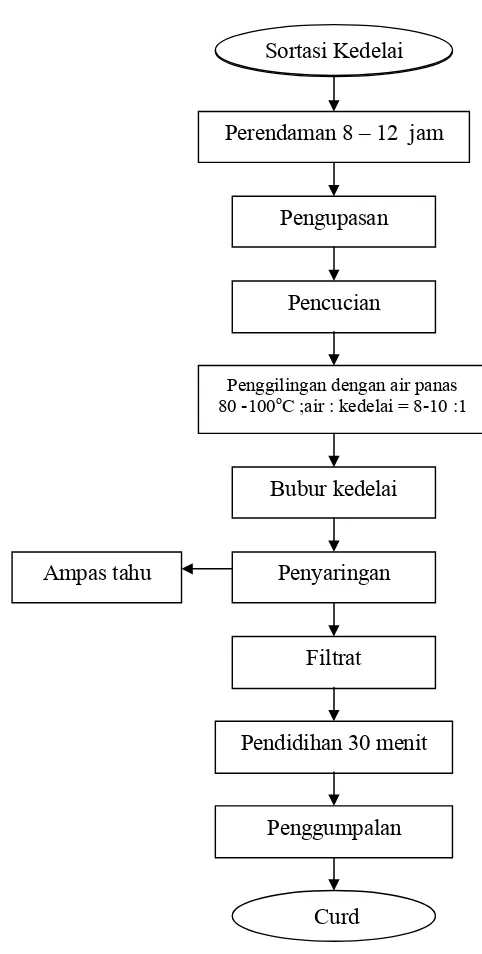
Pada penelitian ini yang akan digunakan sebagai acuan adalah penggunaan
CaSO4 pada produk tahu untuk memperoleh Curd pada Gambar 4. diagram alir
pembuatan curd.
Gambar 4. Diagram alir pembuatan Curd, (Koswara, 1992). Sortasi Kedelai
Perendaman 8 – 12 jam
Pencucian Pengupasan
Penggilingan dengan air panas 80 -100oC ;air : kedelai = 8-10 :1
Bubur kedelai
Penyaringan
Filtrat Sortasi Kedelai
Curd Ampas tahu
Pendidihan 30 menit
F. ANALISA KEPUTUSAN
Analisis keputusan pada dasarnya adalah satu prosedur yang logis dan
kuantitatif yang tidak hanya menerangkan mengenai pengambilan keputusan
tetapi juga merupakan suatu cara untuk membuat keputusan (Susanto dan saneto,
1994).
Analisis keputusan adalah untuk memilih alternatif terbaik yang dilakukan
antara aspek kualitas, aspek kuantitas dan aspek finansial dan produk tauwa yang
dihasilkan dari kombinasi setiap perlakuan.
G. ANALISA KELAYAKAN FINANSIAL
Data yang diperoleh dari analisis mutu kemudian diuji dengan
analisis sidik ragam untuk mengetahui pengaruh perlakuan-perlakuan terhadap
tauwa yang dihasilkan. Data sekunder berupa harga-harga baik bahan baku
maupun produk tauwa. Analisis finansial yang dilakukan meliputi :
analisis nilai uang dengan metode Break Event Point (BEP),
Net Present Value (NPV), Rate of Return dengan metode Internal Rate of Return
dan Payback Periode (PP)
(Susanto dan Saneto, 1994).
1. Break Event Point (BEP) (Pujawan, 2002)
Break Even Point (BEP) adalah suatu keadaan dimana pada tingkat
penjualan tertentu perusahaan tidak memperoleh keuntungan atau mengalami
FC
BEP = ……….….( 1 )
P - VC
Keterangan :
P : Produk pulang/pokok
FC : Biaya tetap
VC : Baya tidak tetap per satuan produk
Rumus untuk mencari titik impas adalah sebagai berikut Biaya titik impas
Biaya tetap
BEP = ……….( 2 )
1 – ( biaya tidak tetap / pendapatan)
Presentase
Titik Impas :
BEP (Rp)
BEP (%) = X 100 ...( 3) Pendapatan
Kapasitas titik Impas
Kapasitas titik impas adalah jumlah produksi yang harus dkilakukan untuk
mncapai impas. Rumus kapasitas adlah s ebagai berikut :
Kapasitas Tikik Impas = Pesrsen titik impas X Pendapatan
Net Persent Value (NPV) merupakan selisih antara nilai saat investasi
sekarang dengan nilai pemeriksaan kas bersih dimasa akan datang . Suatu proyek
dapat dipilih bila NPV > 0.
NPV =
n
t l i
Ct Bt
1 ( )'
... ( 4
)
Dimana :
Bt : Penerimaan pada tahun t
Ct : Biaya pada tahun t
N : Umur ekonomi proyek (untuk industri dianggap layak selama
10 tahun)
i : Suku bunga Bank
3. Internal Rate of Return (IRR)
Internal Rate of Return (IRR) merupakan tingkat suku bunga yang
menunjukkan persamaan antara nilai penerimaan bersih sekarang dengan jumlah
investasi (modal) awal dari suatu proyek yang sedang dikerjakan. Dengan kata
lain IRR adalah tingkat suku bunga yang akan menyebabkan NPV = 0. Bila nilai
IRR suatu proyek lebih besar dari suku bunga yang berlaku, maka proyek
dinyatakan layak untuk dilaksanakan (Susanto dan Saneto, 1994).
IRR = i’+ " '
i’ : Tingkat suku bunga sekarang
i” : Tingkat suku bunga yang akan datang
NPV’ : NPV positif hasil pecobaan nilai
NPV” : NPV negatif hasil percobaan nilai
4. Gros Benefit Cost Ratio (gros B/C Ratio)
Menerapkan perbandingan antara penerimaan kotor dengan biaya kotor
yang telah dipresent valuekan (dirupiahkan sekarang)
Gross B/C =
Kriteria ini menyatakan bahwa proyek yang akan dipilih akan dipilih apabila Gross B/C>1
5. Payback Period (PP) (Susanto dan Saneto, 1994)
Payback Periode (PP) merupakan perhitungan jangka waktu yang
dibutuhkan untuk pengembalian modal yang ditanam pada proyek, nilai tersebut
berupa persentase maupun waktu (baik tahun maupun bulan). Payback Periode
tersebut harus lebih kecil dari nilai ekonomis proyek. Kriteria ini memberikan
nilai bahwa proyek yang akan dipilih jika mempunyai waktu Payback Periode
I
PP = ...(7)
A/B
Dimana :
PP : Payback Period
I : Jumlah modal
AB : Penerimaan bersih pertahun
H. Landasan Teori
Tauwa merupakan minuman yang dibuat dari susu kedelai (Novie, 2009).
Menurut Andrianto, (2004). Kandungan protein kacang hijau cukup tinggi
mencapai 22,9 g tiap 100 g kacang hijau kering. Faktor utama pembuatan tauwa
kacang hijau adalah proses penggumpalan ekstrak ptotein susu kacang hijau
menjadi Curd
Pemanasan adalah penyebab terjadinya denaturasi secara umum,
keberhasilan denaturasi dengan pemasan dipengaruhi oleh berbagai faktor :
konsentrasi protein, pH, dan kekuatan ion (Fennema, 1985). GDL merupakan
hasil kristalisasi glucano acid yang secara umum digunakan sebagai penggumpal
pada pambuatan tahu sutera. Menurut Obatolu, (2006). Tahu merupakan curd
yang terbentuk dari ekstrak protein susu kedelai panas dengan penggumpal
menghasilkan gel protein, dengan air teriakat, lemak kedelai, dan faktor pendukng
dalam pembentukan curd.
Menurut Suhardi, (1988). Muatan listrik mempengaruhi kelarutan protein,
pada pH selain pada titik isoelektriknya protein mempunyai muatan dan saling
menolak, tetapi pada titik isoelektrik beda muatan antar molekul mengecil dan
akhirnya sangat kecil, molekul-molekul saling berdampingan, membentuk
agregat dan mengendap. Sifat kelarutan protein dalam air dipengaruhi oleh
ikatan hidrogen dalam air dengan protein dan pH lingkungan di luar pH
isoelektrik.
Menurut Winarno, (2004), Asam amino dalam kondisi netral (pH
isoelektris , pI) berada dalam bentuk ion dipolar atau disebut ion zwitter. Pada
asam amino dipolar , gugus amino mendapat tambahan sebuah proton dan gugus
karboksil terdisosiasi. Pada pH rendah misalnya pH 1,0 gugus karboksilnya tinggi
misalnya pada pH 11,0 , karboksilnya terdisosisi sedang gugus aminonya tidak,
seperti terlihat pada skema berikut ini. Gambar 5 di bawah ini menunjukan
terjadinya pH isoelektris
H+ H
-pH<pI pH=pI pH>pI
Gambar 5. Skema pH asam amino (Winarno, 2004)
Apabila asam amino larut dalam air, gugus karboksilat akan melepaskan
NH3+
H C COO
R
NH3
H C COOH
R
NH2
H C COO
ion H+, sedangkan gugus amina akan menerima ion H+, seperti yang tertera pada
Gambar 6. Reaksi kimia yang terjadi akibat pengaruh asam adalah sebagai
berikut :
Gambar 6. Reaksi kimia tang terjadi akibat pengaruh asam, (Poejiadi,1994)
Mekanisme denaturasi karena pengaruh pH isoelekris disebabkan adanya
gugus amino dan karboksil bebas pada ujung-ujung rantai molekul protein,
menyebabkan protein mempunyai banyak muatan dan dapat bereaksi dengan asam
maupun basa. Daya reaksi berbagai jenis protein terhadap asam dan basa tidak
sama, tergantung dari jumlah dan letak gugus amino dan karboksil dalam
molekul. Dalam lartan asam, gugus amino bereaksi dengan amino H+ , sehingga protein bermuatan positif. Bila pada kondisi ini dilakukan elektrolisis, molekul
protein akan bergerak ke arah katoda. Sebaliknya, dalam larutan basa (pH tinggi)
molekul protein akan bereaksi sebagai asam atau bermuatan negatif, sehingga
muatan protein akan baergerak menuju anoda. Pada pH tertentu yang disebut titik
isoelektrik (pI), muatan gugus amino dan karboksil bebas akan saling menetralkan
sehaingga molekul bermuatan nol. Pada titik isoelektrik pengendapan protein
BAB III
METODE PENELITIAN
A. Tempat dan Wkatu Penelitian
Penelitian dilakukan di Laboratorium Analisa Pangan, Laboratorium
Teknologi Pengolahan Pangan, Laboratorium Uji Inderawi Universeitas
Pembangunan Nasional “Veteran” Jawa Timur, dan Laboratorium Teknologi
Hasil Pertanian Univesitas Muhamadiyah Malang. Penelitian dilakukan pada
bulan Mei s/d November 2009.
B. Bahan Penelitian
Bahan yang digunakan dalam pembuatan Tauwa adalah kacang hijau dan
GDL (Glukono Delta Lactone)
Bahan untuk analisa H2SO4 (93 % - 98 % bebas N), HCL 0,02 NaOH 0,1
N Indikator M.M, dan M.B, Na2SO3, asam borat, Na2SO4.H6O larutan buffer, batu
didih, serbuk Zn, tablet kjeidhal.
C. Alat Penelitian
Alat-alat yang digunakan untuk proses meliputi, neraca analitik, pH meter,
kain saring, kompor gas, blender, baskom, dan termometer.
Alat yang digunkan untuk analisa antara lain: beaker glass, Gelas ukur,
Erlenmeyer, Pipet Volum, Buret, cawan Porselin, oven, Labu kjeidahl, Corong,
D. Metode Penelitian
Rancangan penelitian yang digunakan adalah Rancangan Acak lengkap
(RAL) denga dua fator yaitu proprsi kacan hijau dalam larutan dan konsentrasi
GDL. Masing-masing kombinasi perlakuan dilakukan 3 kali ulangan. Data yang
diperoleh dianalisa dengan mengunakan analisa ragam. Untuk mengetahui adanya
perbedaan diantara pelakuan digunakan uji Duncan.
Faktor I : Penambahan air pembautan susu kacang hijau 150 gr terdiri
dari 3 level (A1, A2, A3)
A1 : Penambahan air 300 ml
A2 : Penambahan air 450 ml
A3 : Penambahan air 600 ml
Faktor II: Konsentrasi GDL terdiri dari 3 level (K1, K2, K3)
K1 : Konsentrasi GDL 2 %
K2 : Konsentrasi GDL 3 %
K3 : Konsentrasi GDL 4 %
Dari kedua Faktor tersebut di atas didapat 9 perlakuan kombinasi sebagai
berikut :
Konsentrasi GDL Proprsi air proses
A1 A2 A3
K1 A1K1 A1K2 A1K3
K2 A2K1 A2K2 A2K3
A1K1 : Penambahan air 300 ml, dan konsentrasi GDL 2 %
A1K2 : Penambahan air 450 ml, dan konsentrasi GDL 3 %
A1K3 : Penambahan air 600 ml, dan konsentrasi GDL 4 %
A2K1 : Penambahan air 300 ml, dan konsentrasi GDL 2 %
A2K2 : Penambahan air 450 ml, dan konsentrasi GDL 3 %
A2K3 : Penambahan air 600 ml, dan konsentrasi GDL 4 %
A3K1 : Penambahan air 300 ml, dan konsentrasi GDL 2 %
A3K2 : Penambahan air 450 ml, dan konsentrasi GDL 3 %
A3K3 : Penambahan air 600 ml, dan konsentrasi GDL 4 %
Model matematik yang diguanakan adalah :
Yijk = μ + α1 +βj + ( αβ)ij + €ijk
Dimana :
Yijk : nilai pengamatan pada satuan percobaan ke-k yang memperoleh
kombinasi perlakuan ij ( taraf ke-I faktor A dan ke –J dari faktor
B)
μ : nilai tengah populasi (rata-rata tyang sesungguhnya)
α1 : pengaruh aditif taraf ke-1 dari faktor A
βj : [engaruh aditif taraf ke-j dari faktor B
( αβ)ij : pengaruh interaksi dari faktor A dan taraf ke-J dari faktor B
€ijk : pengaruh galat dari satuan percobaan ke-k yang memperoleh
Faktor yang digunakan :
1. Faktor Berubah :
a. Air untuk ektrak susu kacang hijau 150 g : 300 ml 450 ml, dan : 600 ml
b. Konsentrasi GDL : 2%, 3%, dan 4% (b/bb)
2. Faktor Tetap
a. Kacang hijau lokal
b. Berat bahan kering 150 gr
c. Waktu perendaman kacang hijau 8 jam
c. Suhu pengendapan pati (ksrbohidrat) 50o – 60oC d. Waktu pengendapan pati (ksrbohidrat) 10 menit
e. Suhu pemanasan 90o-100oC f. Suhu penggumpalan 90o-100oC
g. lama pemasakan susu kedelai 10 menit
h Tinggi penuangan susu kedelai ke larutan GDL 30-50 cm
i. Larutan untuk GDL 100 ml
E. Parameter
Parameter yang diamaati dalam penelitian ini adalah
1. Produk Akhir
- Kadar Protein metode kejdahl semi makro ( Sudarmaji, 1992)
- pH (pH meter)
- Randemen (Hartanti, 2003)
- Sineresis (Annonymous, 2004)
- Uji Organoleptik
- Rasa (Metode Hedonik, skala rangking)
- Aroma (Metode Hedonik, skala rangking)
- Tekstur ( Metode skoring, skala skoring)
F. Prosedur Penelitian
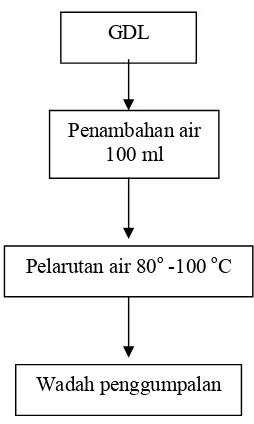
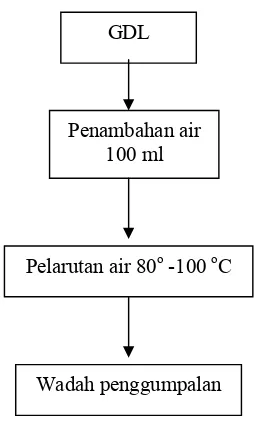
a. Pembutan larutan Pengumpal
1. Gdl ditimbang sesuai dengan persentase berat perlakuan 2%b/bb,
3%b/bb dan 4%b/bb
2. GDL dilarutkan dengan air panas 80o -100oC, kemudian diaduk sampai terlarut
3. Larutan GDL dituankan ke dalam wadah (panci) tauwa.
Adapun diagram alir pembuatan larutan penggumpal ditunjukan
Gambar : 7 . Pembauatan larutan penggumpal
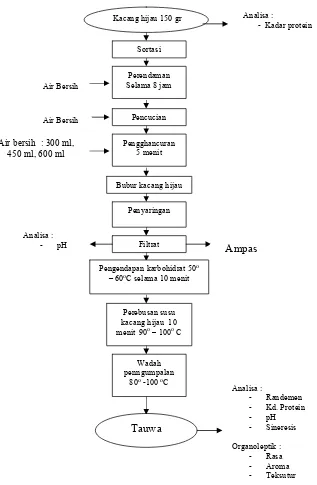
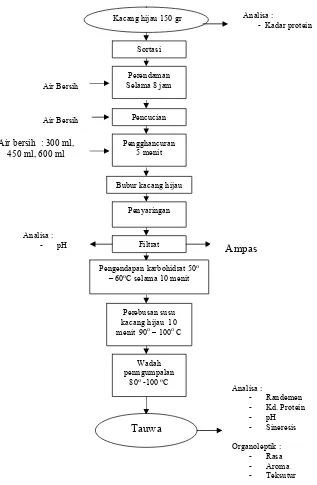
b. Pembuatan Tauwa
1. Kacang hijau disortasi dan dibersihkan sebanyak 150 gr untuk 1
perlakuan
2. Kacang hijau dicuci kemudian direndamdalam air selama ± 8 jam
dengan air 500 ml
3. Hancurkan kacang hijau menjadi bubur dengan perbandingan air
300 ml, 450 ml dan 500 ml untuk setiap proporsi.
4. Peras ekstrak kacang hijau sampai untuk memperoleeh sari kacang
hijau, dengan kain saring lapis 2
8. Sari kacang hijau direbus 10 menit dengan air 50 – 60 oC untuk mngendapakan karbohidrat kemudian dibiarkan sebentar, setelah
GDL
Penambahan air 100 ml
Pelarutan air 80o -100 oC
itu dipisahkan pelan-pelan dengan menuangkan ke tempat lain.
Endapan warna putih merupakan grannula pati
9. Rebus sari kacang hijau 90o – 100oC selama 10 menit rebus juga bersamaan di wadah berbeda untuk GDL suhu 80o – 100oC
10. Tuangkan larutan GLD panas dalam wadah yang telah disiapkan
sebagai wadah tauwa kemudian tuangkan sari kacang hijau ke
dalam wadah dengan ketinggian 30 – 50 Cm untuk pencampuran
supaya homogen
11. Tutup wadah utuk mempertahankan suhu penggumpalan dan
biarkan reaksi penggumpalan berlangsung 10 menit
Adapun diagram alir pembuatan tauwa kacang hijau ditunjukan pada
I. Hipotesa
Diduga penggunaan bahan GDL sebagai penggumpal dan konsentrasi susu
kacang hijau akan mempengaruhi pembentukan tauwa yang dihasilkan yang baik
BAB III
METODE PENELITIAN
A. Tempat dan Wkatu Penelitian
Penelitian dilakukan di Laboratorium Analisa Pangan, Laboratorium
Teknologi Pengolahan Pangan, Laboratorium Uji Inderawi Universeitas
Pembangunan Nasional “Veteran” Jawa Timur, dan Laboratorium Teknologi
Hasil Pertanian Univesitas Muhamadiyah Malang. Penelitian dilakukan pada
bulan Mei s/d November 2009.
B. Bahan Penelitian
Bahan yang digunakan dalam pembuatan Tauwa adalah kacang hijau dan
GDL (Glukono Delta Lactone)
Bahan untuk analisa H2SO4 (93 % - 98 % bebas N), HCL 0,02 NaOH 0,1
N Indikator M.M, dan M.B, Na2SO3, asam borat, Na2SO4.H6O larutan buffer, batu
didih, serbuk Zn, tablet kjeidhal.
C. Alat Penelitian
Alat-alat yang digunakan untuk proses meliputi, neraca analitik, pH meter,
kain saring, kompor gas, blender, baskom, dan termometer.
Alat yang digunkan untuk analisa antara lain: beaker glass, Gelas ukur,
Erlenmeyer, Pipet Volum, Buret, cawan Porselin, oven, Labu kjeidahl, Corong,
D. Metode Penelitian
Rancangan penelitian yang digunakan adalah Rancangan Acak lengkap
(RAL) denga dua fator yaitu proprsi kacan hijau dalam larutan dan konsentrasi
GDL. Masing-masing kombinasi perlakuan dilakukan 3 kali ulangan. Data yang
diperoleh dianalisa dengan mengunakan analisa ragam. Untuk mengetahui adanya
perbedaan diantara pelakuan digunakan uji Duncan.
Faktor I : Penambahan air pembautan susu kacang hijau 150 gr terdiri
dari 3 level (A1, A2, A3)
A1 : Penambahan air 300 ml
A2 : Penambahan air 450 ml
A3 : Penambahan air 600 ml
Faktor II: Konsentrasi GDL terdiri dari 3 level (K1, K2, K3)
K1 : Konsentrasi GDL 2 %
K2 : Konsentrasi GDL 3 %
K3 : Konsentrasi GDL 4 %
Dari kedua Faktor tersebut di atas didapat 9 perlakuan kombinasi sebagai
berikut :
Konsentrasi GDL Proprsi air proses
A1 A2 A3
K1 A1K1 A1K2 A1K3
K2 A2K1 A2K2 A2K3
A1K1 : Penambahan air 300 ml, dan konsentrasi GDL 2 %
A1K2 : Penambahan air 450 ml, dan konsentrasi GDL 3 %
A1K3 : Penambahan air 600 ml, dan konsentrasi GDL 4 %
A2K1 : Penambahan air 300 ml, dan konsentrasi GDL 2 %
A2K2 : Penambahan air 450 ml, dan konsentrasi GDL 3 %
A2K3 : Penambahan air 600 ml, dan konsentrasi GDL 4 %
A3K1 : Penambahan air 300 ml, dan konsentrasi GDL 2 %
A3K2 : Penambahan air 450 ml, dan konsentrasi GDL 3 %
A3K3 : Penambahan air 600 ml, dan konsentrasi GDL 4 %
Model matematik yang diguanakan adalah :
Yijk = μ + α1 +βj + ( αβ)ij + €ijk
Dimana :
Yijk : nilai pengamatan pada satuan percobaan ke-k yang memperoleh
kombinasi perlakuan ij ( taraf ke-I faktor A dan ke –J dari faktor
B)
μ : nilai tengah populasi (rata-rata tyang sesungguhnya)
α1 : pengaruh aditif taraf ke-1 dari faktor A
βj : [engaruh aditif taraf ke-j dari faktor B
( αβ)ij : pengaruh interaksi dari faktor A dan taraf ke-J dari faktor B
€ijk : pengaruh galat dari satuan percobaan ke-k yang memperoleh
Faktor yang digunakan :
1. Faktor Berubah :
a. Air untuk ektrak susu kacang hijau 150 g : 300 ml 450 ml, dan : 600 ml
b. Konsentrasi GDL : 2%, 3%, dan 4% (b/bb)
2. Faktor Tetap
a. Kacang hijau lokal
b. Berat bahan kering 150 gr
c. Waktu perendaman kacang hijau 8 jam
c. Suhu pengendapan pati (ksrbohidrat) 50o – 60oC d. Waktu pengendapan pati (ksrbohidrat) 10 menit
e. Suhu pemanasan 90o-100oC f. Suhu penggumpalan 90o-100oC
g. lama pemasakan susu kedelai 10 menit
h Tinggi penuangan susu kedelai ke larutan GDL 30-50 cm
i. Larutan untuk GDL 100 ml
E. Parameter
Parameter yang diamaati dalam penelitian ini adalah
2. Produk Akhir
- Kadar Protein metode kejdahl semi makro ( Sudarmaji, 1992)
- pH (pH meter)
- Randemen (Hartanti, 2003)
- Sineresis (Annonymous, 2004)
- Uji Organoleptik
- Rasa (Metode Hedonik, skala rangking)
- Aroma (Metode Hedonik, skala rangking)
- Tekstur ( Metode skoring, skala skoring)
F. Prosedur Penelitian
a. Pembutan larutan Pengumpal
1. Gdl ditimbang sesuai dengan persentase berat perlakuan 2%b/bb,
3%b/bb dan 4%b/bb
2. GDL dilarutkan dengan air panas 80o -100oC, kemudian diaduk sampai terlarut
3. Larutan GDL dituankan ke dalam wadah (panci) tauwa.
Adapun diagram alir pembuatan larutan penggumpal ditunjukan
Gambar : 7 . Pembauatan larutan penggumpal
b. Pembuatan Tauwa
1. Kacang hijau disortasi dan dibersihkan sebanyak 150 gr untuk 1
perlakuan
2. Kacang hijau dicuci kemudian direndamdalam air selama ± 8 jam
dengan air 500 ml
3. Hancurkan kacang hijau menjadi bubur dengan perbandingan air
300 ml, 450 ml dan 500 ml untuk setiap proporsi.
4. Peras ekstrak kacang hijau sampai untuk memperoleeh sari kacang
hijau, dengan kain saring lapis 2
8. Sari kacang hijau direbus 10 menit dengan air 50 – 60 oC untuk mngendapakan karbohidrat kemudian dibiarkan sebentar, setelah
GDL
Penambahan air 100 ml
Pelarutan air 80o -100 oC
itu dipisahkan pelan-pelan dengan menuangkan ke tempat lain.
Endapan warna putih merupakan grannula pati
9. Rebus sari kacang hijau 90o – 100oC selama 10 menit rebus juga bersamaan di wadah berbeda untuk GDL suhu 80o – 100oC
10. Tuangkan larutan GLD panas dalam wadah yang telah disiapkan
sebagai wadah tauwa kemudian tuangkan sari kacang hijau ke
dalam wadah dengan ketinggian 30 – 50 Cm untuk pencampuran
supaya homogen
11. Tutup wadah utuk mempertahankan suhu penggumpalan dan
biarkan reaksi penggumpalan berlangsung 10 menit
Adapun diagram alir pembuatan tauwa kacang hijau ditunjukan pada
BAB IV
HASIL DAN PEMBAHASAN
Analisa yang dilakukan pada penelitian ini dimulai dengan analisa pH susu
kacang hijau, analisa pH penggumpalan protein kacang hijau pada produk tauwa
yang dihasilkan (terdiri dari analisa fisikokimiawi dan organoleptik. Analisa
dilanjutkan denga analisa keputusan dan analisa finansial yang didasarkan pada
segi ekonomis apabila produk digunakan pada industi.
A. Analisa Bahan Baku
Pada penelitian pembuatan tauwa kacang hijau dilakukan analisa kadar
protein bahan awal pada kacang hijau. Hasil analisa kadar protein kacang hijau
adalah 23,22% bahan.
Hasil analisa bahan baku pada kacang hijau menunjukkan kadar protein
kacang hijau 23,22% cukup tinggi. Hal tersebut mendekati dengan pendapat
Andrianto (2004), menyatakan kadar protein kacang hijau 22,20%
B. Hasil pH susu kacang hijau
Pada penelitian pembuatan tauwa ini dilakukan analisa terhadap pH susu
kacang hijau Tabel 3. menunjukan pH susu kacang hijau pada pengenceran yang
berbeda
Tabel 3. pH susu kacang hijau pada pengenceran yang berbeda
Penambahan air (ml) pH
300 450 600
Berdasarkan hasil analisa pH susu kacang hijau dengan penambahan
(300ml, 450 ml dan 600 ml) diperoleh data rata-rata pH susu kacang hijau dengan
pH terendah dari perlakuan perbandingan kacan hijau 150 gr dengan air 300 ml
pH 6,00 dan pH susu kacang hijau tertinggi pada perlakuan perbandingan kacang
hijau 150 gr dengan air 600 ml dengan pH 6,20
C. Hasil Analisa pH penggunmpalan susu kacang hijau
Berdasarkan hasil analisa ragam (Lampiran 3). dapat diketahui bahwa
antara pelakuan penambahan air dan konsentrasi GDL berpengaruh nyata
( p≤ 0,05) terhadap pH penggumpalan susu kacang hijau. Nilai rata-rata pH
penggumpalan susu kacang hijau dengan perlakuan perlakuan konsentrasi GDL
dan penambahan volume air susu dapat dilihat pada Tabel 4.
Tabel 4. Rerata nili pH tauwa kacang hijau pengaruh perlakuan Penambahan air dan konsentrasi GDL
Perlakuan
air (ml) Konsentrasi GDL (%)
Keterangan : Nilai rerata yang diikuti huruf yang berbeda berbeda berarti berbeda nyata (p≤0,05)
Berdasarkan Tabel 4. menunjukkan bahwa perlakuan penambahan air 300
(4,15) dan penambahan air 600 ml dan konsentrasi GDL 3% rata-rata pH
penggumpalan tertinggi (5,3800) Hubungan antara perlakuan penambahan air dan
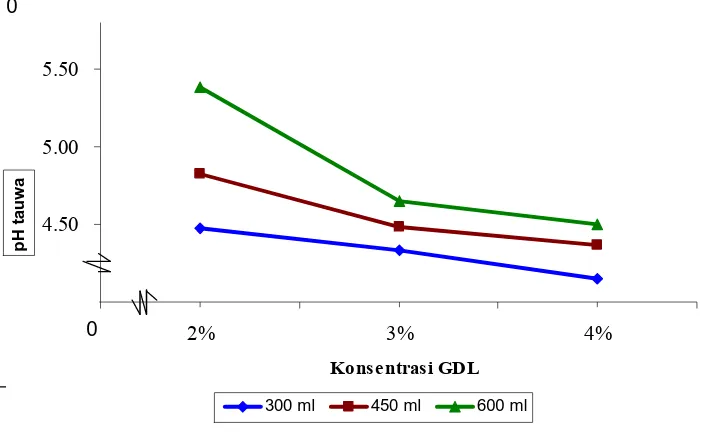
konsentrasi GDL terhadap pH tauwa kacang hijau ditunjukan pada Gambar 9:
4.00 4.50 5.00 5.50
2% 3% 4%
Konse ntrasi GDL
pH
t
a
uw
a
300 ml 450 ml 600 ml
0
0
Gambar 9. Hubungan perlakuan penambahan air dan konsentrasi GDL terhadap pH tauwa kacang hijau
Pada Gambar 9. menunjukan bahwa semakin tinggi konsentrasi GDL dan
semakin rendah penambahan air pH tauwa semakin turun. Hal ini disebabkan
GDL memiliki sifat asam sehingga dapat menurunkan pH, hal ini sesui dengan
pendapat Omry (2002), bahwa GDL merupakan asam organik yang dapat
menurunkan pH. Semakin tinggi penambahan air dapat menaikan pH karena air
bersifat nitral (pH + 7,00) hal ini sesui dengan pendapat Driscoll ( 1986), nilai pH
D. Randemen
Berdasarkan hasil analisis ragam ( Lampiran 4) dapat diketahui pelakuan
penambahan air dan konsentrasi GDL terdapat interaksi yang nyata (p≤0,05)
terhadap randemen tauwa kacang hijau yang dihasilkan. Rata-rata randemen
tauwa kacang hijau untuk tiap perlakuan perlakuan penambahan air konsentrasi
dan GDL dapat dilihat pada Tabel 5.
Tabel 5. Rerata nilai randeman tauwa kacang hijau dari penambahan air dan konsentrasi GDL Keterangan : Nilai rerata yang diikuti huruf yang berbeda berbeda berarti
berbeda nyata (p≤0,05)
Pada Tabel 5. terlihat bahwa pada perlakuan penambahan air 300 ml dan
konsentrasi GDL 4% memiliki randemen yang paling rendah (126,9554%) ,
sedangkan pada perlakuan penambahan air 600 ml dan konsentrasi GDL 4%
memiliki randemen yang paling tinggi (300,1553 %). Hubungan perlakuan
penambahan air dan konsentrasi GDL terhadap randemen yang dihasilkan
0 100 200 300
2% 3% 4%
Konse ntrasi GDL
R
a
nde
me
n (%)
300 ml 450 ml 600 ml
Gambar 9. Hubungan perlakuan penambahan air dan konsentrasi GDL terhadap randeman tauwa kacang hijau
Pada Gambar 10. menunjukan bahwa semakin tinggi konsentrasi GDL
dan semakin rendah penambahan air, maka randeman yang dihasilkan semakin
rendah. Hal ini disebabkan semakin tinggi konsentrasi GDL pH tauwa semakin
turun menyebabkan pH tauwa menjauhi pH isoelektris, sehingga curd yang
terbentuk semakin sedikit. Semakin kecil penambahan air randeman yang
terbentuk semakin rendah karena masa air yang terperangkap dalam curd semakin
sedikit sedangkan semakin banyak penambahan air randeman yang terbentuk
semakin tinggi karena protein semakin encer..
Hal tersebut sesuai dengan pendapat Fennema (1985), protein kedelai
memiliki titik pH Isoelektris pada pH 4,6. Randeman tauwa kacang hijau tertinggi
hijau mengalami pengendapan paling maksimal untuk menghasilkan randeman.
Hal ini sesuai dengan pendapat Winarno (2004), pada titik isoelektrik
pengendapan protein terjadi paling cepat. Suhardi, (1988), menambahakan
muatan listrik mempengaruhi kelarutan protein, pada pH selain pada titik
isoelektriknya protein mempunyai muatan dan saling menolak, tetapi pada titik
isoelektrik beda muatan antar molekul mengecil dan akhirnya sangat kecil,
molekul-molekul saling berdampingan, membentuk agregat dan mengendap
E. Sineresis
Berdasarkan hasil analisis ragam ( Lampiran 5) dapat diketahui perlakuan
penambahan air dan konsentrasi GDL pada tauwa kacang hijau terdapat interaksi
yang nyata (p≤0,05) terhadap sineresis tauwa yang dihasilkan. Demikian juga
antara masing-masing perlakuan terdapat perbedaan yang nyata. Rerata sineresis
tauwa kcang hijau dengan perlakuan konsentrasi GDL dan penambahan volume
air susu tiap perlakuan dapat dilihat pada Tabel 6
Keteranagan : Nilai rata-rata yang didampingi huruf berbeda berarti berbeda nyata (p≤0,05)
Pada Tabel 6. terlihat bahwa pada perlakuan penambahan air 300 ml dan
konsentrasi GDL 4% memiliki rerata sineresis tertinggi tauwa (0,4168 g/g/jam )
sedangkan pada perlakuan penambahan GDL 3% dan volume air 600 ml
sedangkan sinersis terendah (0,2115 g/g/jam)
Hubungan antara perlakuan penambahan air dan konsentrasi GDL
terhadap sineresis tauwa kacang hijau dapat dilihat pada Gambar 11.
0.20
Gambar 10. Hubungan perlakuan penambahan air dan konsentrasi GDL terhadap sineresis tauwa kacang hijau
Pada Gambar 11. menunjukan semakin tinggi konsentrasi GDL dan
semakin rendah penambahan air maka nilai sineresis semakin tinggi. Hal ini
disebabkan, semakin tinggi konsentrasi GDL pH tauwa semakin turun, menjauhi
pH isoelektris sehingga curd yang terbentuk semakin lembek menyebabkan air
sineresis yang dihasilkan semakin tinggi, hal ini disebabkan curd yang terbentuk
semakin lembek karena air yang menetes semakin banyak karena pH tauwa
menjauhi pH isoelektris.
Pada penambahan air 600 ml terjadi penyimpangan grafik yaitu pada
konsentrasi 2% pH tauwa 5,38 menunjukan bahwa pH tauwa menjauhi pH
isoelektris sehigga curd yang terbentuk lebih lembek menyebabkan air yang
keluar dari curd lebih banyak. Sedangkan pada perlakuan konsentrasi GDL 3 %
pH tauwa 4,65 dan pada perlakuan konsentrasi GDL 4% pH tauwa 4,49 pada
kondisi tersebut pH tauwa mendekati pH isoelektris 4,6 sehingga curd yang
terbentuk lebih kokoh karen air yang keluar lebih sedikit
Terbentukya sineresis yang dikehendaki adalah nilai seneresis yang kecil
karena ini menunjukan bahwa pada tauwa kacang hijau tersebut air yang terikat
dalam tauwa lebih kuat dan nampak kokoh, akan tetapi pada tauwa yang
memiliki nilai seneresis terbesar menujukan bahwa tauwa tersebut memiliki sifat
yang lembek. Hal tersebut sesuai dengan pendapat Harianto,(2005) bahwa
terdapat hubungan nilai konsistensi gel dengan nilai sineresis, dan terdapat
hubungan antara nilai konsistensi gel dengan tekstur dan ditambahkan pula oleh
Eryanti (2004), bahwa semakin tinggi tingkat sineresis maka semakin cepat lunak
tekstur produk pangan tersebut, dimana definisi sineresis menurut Winarno
(1992), adalah keluarnya air atau merembesnya cairan dari dalam bahan pangan
F. Kadar Protein
Berdasarkan hasil analisis ragam ( Lampiran 6) dapat diketahui perlakuan
penambahan air dan konsentrasi GDL air susu kacang hijau tidak terdapat
interaksi yang nyata (p≥0,05) terhadap kadar protein tauwa yang dihasilkan.
Sedangkan masing-masing perlakuan terdapat perbedaan beda nyata. Rerata
kadar protein curd tauwa tiap perlakuan dapat dilihat pada Tabel 7.
Tabel 7. Rerata pengaruh perlakuan penambahan air terhadap kadar protein tauwa kacang hijau
Keteranagan : Nilai rata-rata yang didampingi huruf berbeda berarti berbeda nyata (p≤0,05)
Pada Tabel 7. menujukan bahwa prlakuan penambahan air kacang hijau
300 ml memiliki kadar protein terendah (5,4503 %) kondisi curd lembek
sehingga kandungan air dalam curd tinggi sehingga menyebabkan kadar protein
rendah. dan perlakuan penambahan air 450 ml memiliki kadar protein tertinggi
(6,0311%), pada kondisi tersebut curd yang terbentuk memiki kecenderunngan
kokoh menyebabkan perbandingan air lebih rendah sehingga kadar protein
tinggi. Pada perlakuan penambahan air 600 ml curd yang terbentuk kurang kokoh
sehingga kandungan air lebih tinggi menyebabkan kadar protein lebih tinggi. Hal
tersebut sesuai dengan hasil pengamatan Obatolu (2008) bahwa tahu yang
memiliki tekstur yang keras memiliki kadar protein yang tinggi daripada tahu
Tabel 8. Rerata pengaruh perlakuan konsentrasi GDL terhadap kadar protein tauwa kacang hijau
Perlakuan
Keteranagan : Nilai rata-rata yang didampingi huruf berbeda berarti berbeda nyata (p≥0,05)
Pada Tabel 8. menujukan bahwa prlakuan penambahan konsentrasi
GDL 3 % memiliki kadar protein tertinggi (6,0096 %) kondisi curd yang
terbentuk lebih kokoh sehingga kandungan air rendah menyebabkan kandungan
protein tinggi, sedangkan pada perlakuan konsentrasi GDL 2 % kondisi curd
sedikit lembek sehingga kandungan air dalam curd tinggi menyebabkan kadar
protein lebih rendah. Pada perlakuan konsentrasi GDL 4% kandisi curd lebih
lembek sehingga kandungan air dalam curd tinggi sehingga kadar protein lebih
rendah. Tekstur tauwa yang kokoh dipngaruhi oleh pH pnggumpalan, pH
penggumpalan yang mendekati pH isoelektris memiliki sifat tekstur yang kokoh
sedangkan tekstur tauwa yang lembek nmenjauhi pH isoelektri Hal tersebut
sesuai dengan hasil pengamatan Obatolu (2008) bahwa tahu yang memiliki tekstur
yang keras memiliki kadar protein yang tinggi daripada tahu yang lunak.
E. Uji Organoleptik
1. Uji organoleptik rasa
Dari hasi uji orgnoleptik dengan metoe hedonik skala rangking dan
kacang hijau terhadap tingkat kesukaan rasa tauwa yang dihasilkan. Jumlah
rangking terhadap rasa tauwa dapat dilihat pada Tabel 9
Tabel 9. Rerata ranngking kesukaan rasa tauwa kacang hijau pengaruh perlakuan penambahan air dan konsentrasi GDL
. Keterangan : Semakin tinggi rangking, maka rasa semakin suka
Pada Tabel 9. Hasil uji organoleptik terhadap kesukaan rasa tauwa kacang
hijau diperoleh rata-rata 52 – 134,5. Perlakuan penambahan volume air 600 ml
dan GDL 3% kesukaan rasa dengan total rangking tertinggi (134,5), sedangkan
perlakuan penambahan air 300 ml dan GDL 4% merupakan perlakuan yang
memiliki total rangking kesukaan rasa terendah (54).
Hal ini disebabkan karena semakin tinggi GDL yang ditambahkan dan
semakin rendah volume air yang ditambahkan maka akan memberikan tinggkat
kesukaan rasa rendah, karena rasa tauwa kacang hijau yang dihasilkan menjadi
semakin asam. Rasa asam berasal dari GDL yang ditambahkan dengan
perbandingan konsentrasi air yang semain sedikit. Hal tersebut sesui dengan
pendapat Obatolu (2008). Semakin tinggi GDL yang ditambahkan pada
2. Uji organoleptik aroma
Dari hasi uji orgnoleptik dengan metoe hedonik skala scoring dan
dilanjutkan dengan uji friedman, menunjukan adanya pengaruh yang nyata (x2 hitung > x2 tabel) antara pelakuan penambahan air dan konsentrasi GDL terhadap tingkat kesukaan aroma tauwa yang dihasilkan. Jumlah rangking terhadap aroma
tauwa dapat dilihat pada Tabel 10.
Tabel 10. Rerata rangking kesukaan aroma tauwa kacang hijau pengaruh perlakuan penambahan air dan konsentrasi GDL
Perlakuan Keterangan : Semakin tinggi rangkin, maka aroma semakin suka
Pada Tabel 10 menunjukan haasil uji organoleptik terhadap kesukaan
aroma tauwa kacang hijau diperoleh rata-rata 49,5 – 144,5. Perlakuan
penambahan air 600 ml dan konsentrasi GDL 3 % merupakan perlakuana yang
memiliki kesukaan rasa dengan total rangking tertinggi (144,5), sedangkan
perlakuan penambahan air 300 ml dan konsentrasi GDL 4% merupakan perlakuan
Hal ini disebabkan karena semakin tinggi GDL yang ditambahkan dan
semakin rendah volume air yang ditambahkan maka akan memberikan tinggkat
kesukaan aroma rendah, karena aroma tauwa kacang hijau yang dihasilkan
menjadi semakin asam. Rasa asam berasal dari GDL yang ditambahkan dengan
perbandingan konsentrasi air yang semain sedikit. Hal tersebut sesui dengan
pendapat Obatolu (2008). Semakin tinggi GDL yang ditambahkan pada
pembautan tahu sutera dapat meningkatkan keasaman tahu sutra.
3. Uji skoring Tekstur
Dari hasi uji orgnoleptik dengan metoe skoring tekstur tauwa merupakan
salah satu parameter yang penting.. Berdasarkan hasil analisis ragam (Lampiran 9)
menunjukkan bahwa perlakuan penambahan air dan konsentrasi GDL tidak
berpengaruh nyata terhadap skor tekstur yang dihasilkan. Nilai rata-rata skor
tauwa kacan hijau pengaruh perlakua penambahan air dan konsentrasi GDL dapat
dilihat pada Tabel 12.
Tabel 12.Rerata ranngking kesukaan aroma tauwa kacang hijau pengaruh perlakuan penambahan air dan konsentrasi GDL
Pada Tabel 12. menunjukkan bahwa rata-rata skor tauwa kacang hijau (45 –
82). Nilai rata-rata skor tertinggi terdapat pada penambahan air 600 ml dan
konsentrasi GDL 3% (82), sedangkan nilai rata-rata skor terendah terdapat pada
perlakuan penambahan air 300 ml dan konsentrasi GDL 4% (45)
Tauwa kacang hijau yang dikehendaki konsumen merupakan tauwa yang
memiliki sifat yang kokoh dimana tauwa kacang hijau yang kokoh merupakan
tauwa yang memiliki pH mendekati pH isoelektris (4,6). Hal ini sesuai dengan
pendapat Suhardi (1988), pada titik isoelektrik beda muatan antar molekul
mengecil dan akhirnya sangat kecil, molekul-molekul saling berdampingan,
membentuk agregat dan mengendap
F. Analisa Keputusan
Pemilihan alternatif pada kualitas curd tauwa kacang hijau dilakukan
bedasarkan uji dengan mempertimbangkan fisikokiiawi dan organoleptik.
Berdasarkan hsil rata-rata uji fisikokimiawi dan organoleptik dari 9 kombinasi
perlakuan dari 20 panelis. Data-data hasil analisa secara kualitatif dan kuantitatif
ditentukan oleh sifat organoleptk pangan tersebut. Mutu orgaoleptik legih
menentukan karena konsumen menilai mutu secara langsung.
G. Analisis Finansial
Analisa finansial ditujukan untuk mengetahui tingkat kelayakan (secara
ekonomis) dari produksi tauwa kacang hijau. Pada penelitian ini delakukan
analisis finansial untuk keperluan yang telah memenuhi kriteria yang diharapkan
yaitu pada perlakuan penambahan air 600 ml dan GDL 4% merupakan produk
tauwa yang disukai konsumen.
Parameter yang dilakukan untuk mengukur tingkat kelayakan produksi
tauea meliputi BEP, NPV, Gros B/C, IRR dan PP hasil perhitungan analisis
finansial dapat dilihat pada Lampiran 10.
1. Kapasitas Produksi
Kapasitas produksi yang direncanakan pada perusahaan tauwa kacang
hijau adalah 4.618,88 kg/tahun atau sebanyak 153.962 mangkuk/tahun
Data kapasitas produksi lebih lengkap dapat dilihat pada Lampiran 10.
2. Biaya Produksi
Biaya produksi merupakan biaya yang harus dikeluarkan untuk
menjalankan suatu usaha. Biaya produksi terdiri dari biaya tetap dan biaya
produksi langsung (biaya tidak tetap). Biaya tetap adalah biaya-biaya yang
produksi. Biaya tetap bersifat konstan pada relevan range tertentu, sedangkan
biaya tidak tetap adalah biaya yang besarnya berubah sejalan dengan tingkat
produksi yang dihasilkan.
Secara singkat total produksi per tahun dari industri tauwa kacanng
hijau dapat dijelaskan sebagai berikut :
Total Biaya Produksi = Biaya Tetap + Biaya Tidak Tetap
= Rp. 54.539.851,04 + Rp 237.503.974. ,-
= Rp 292.043.825
Perincian total biaya produksi tiap tahun dapat dilihat pada Lampiran 10.
3. Harga Pokok Produksi
Berdasarkan kapasitas produksi tiap tahun dan biaya produksi tiap
tahun, maka dapat diketahui harga pokok tiap mangkuk tauwa kacang hijau :
Harga Pokok = Total biaya produksi Kapasitas produksi per tahun
= Rp. 292.043.825 153.961,6
= Rp. 1.896,86/mangkuk atau
4. Harga Jual Produksi
Harga jual diperoleh berdasarkan dari harga pokok produk, keuntungan
yang ingin dicapai ditambah pajak. Keuntungan yang ingin dicapai sebesar
30% dari harga pokok, dan pajak 10% dari harga pokok.
Harga Jual = harga pokok + keuntungan 60%
= Rp. 1.900+ Rp. 1.140
= Rp 3.040/mangkuk
5. Break Event Point (BEP)
Break Event Point (BEP) adalah suatu keadaan tingkat produksi
tertentu yang menyebabkan besarnya biaya produksi keseluruhan sama dengan
besarnya nilai atau hasil penjualan, jadi pada keadaan tersebut perusahaan
tidak mendapat keuntungan juga tidak mengalami kerugian.
Berdasarkan hasil perhitungan pada Lampiran 10 diperoleh BEP tauwa
kacang hiaju yaitu :
a. BEP = Rp 110.628.501,1
b. Persen Titik Impas = 23,63 %
c. Kapasitas titik impas = 35.657,59 mangkuk/tahun
Kapasitas tiitik impas adalah jumlah produksi yang harus dilakukan
untuk mencapai titik impas tersebut, jadi produksi tauwa kacang hijau per
tahun mencapai keadaan impas jika produksinya sebesar 35.657,59
produksinya diatas kapasitas titik impas. Grafik BEP dapat dilihat pada
Lampiran 12.
6. Net Present Value
Net Present Value merupakan selisih antara nilai investasi saat
sekarang dengan nilai penerimaan kas bersih dimasa yang akan datang. Suatu
proyek dapat dipilih apabila NPV > 0.
Berdasarkan perhitungan yang terdapat pada Lampiran 11 tentang
perhitungan NPV pada tauwa kacang hijau adalah sebesar Rp.
139.357.694,-. Hal ini berarti proyek dapat diterima139.357.694,-.
7. Payback Periode
Payback Periode adalah perhitungan jangka waktu yang dibutuhkan
untuk pengembalian modal yang ditanam pada proyek. Payback Periode
tersebut harus lebih kecil dari nilai ekonomis proyek. Kriteria ini memberikan
nilai bahwa proyek akan dipilih jika mempunyai waktu Payback Periode yang
paling cepat.
Berdasarkan perhitungan yang terdapat di Lampiran 10, diperoleh nilai
Payback Periode (PP) sebesar 3,43 tahun. Umur ekonomis proyek yang
direncanakan selama 5 tahun. Hal ini berarti investasi pada proyek ini dapat
diterima karena nilai Payback Periode (PP) lebih kecil daripada umur
ekonomis.
8. Gross Benefit Cost Ratio
Gross Benefit Cost Ratio (Gross B/C) adalah merupakan perbandingan
(dirupiahkan sekarang). Kriteria ini memberikan pedoman bahwa proyek akan
dipilih apabila Gross B/C > 1, bila proyek memiliki Gross B/C = 1 tidak akan
dipilih.
Berdasarkan Lampiran 11, diperoleh nilai Gross B/C sebesar 1,16. Hal
ini berarti proyek ini dapat diterima.
9. Internal Rate of Return (IRR)
Internal Rate of Return (IRR) merupakan tingkat suku bunga yang
menunjukkan persamaan antara nilai penerimaan bersih sekarang dengan
jumlah investasi (modal) awal dari suatu proyek yang sedang dikerjakan.
Dengan kata lain IRR adalah tingkat suku bunga yang akan menyebabkan
NPV = 0. Bila nilai IRR suatu proyek lebih besar dari suku bunga yang
berlaku maka proyek dinyatakan layak untuk dilaksanakan.
Berdasarkan Lampiran 13, diperoleh IRR sebesar 24,42 %. Hal ini
berarti proyek dapat diterima karena IRR lebih besar dari pada suku bunga
KESIMPULAN DAN SARAN
A. KESIMPULAN
1. Hasil penelitian menunjukkan terjadi interaksi yang nyata antara perlakuan
GDL dan Volume air susu kacang hijau terhadap pH penggumpalan
randemen, sineresis dan kesukaan rasa, aroma, Namun tidak berinteraksi
terhadap kadar protein
2. Perlakuan GDL 3% dan Volume air susu kacang hijau 600 ml menghasilkan
tauwa kacang hijau terbaik. Berdasarkan hasil uji organoleptik terhadap
kesukaan rasa, dan aroma. Perlakuan tersebut mempunyai pH penggumpalan
4,65, rendemen 296,0818 % sineresis 0,2115 g/jam kadar protein 6,117%
tingkat kesukaan rasa 144,5(sangat suka), aroma 142 (sangat suka)
3. Hasil analisis finansial diketahui bahwa nilai Break Event Point (BEP) dicapai
pada Rp.108.429.127,3 sebesar 26,13 % dan kapasitas titik impas 35.658
mangkuk/tahun, sedangkan Internal Rate of Return (IRR) mencapai 24,42%,
Payback Period (PP) dicapai selama 3,36 tahun, Net Present Value (NPV)
Pada penelitian lebih lanjut mengenai rasa dan tekstur tauwa kacang
sedemikian rupa sehingga didapatkan produk tauwa kacang hijau yang lebih
menarik dan berpeluang lebih besar untuk dibeli oleh konsumen, sehingga perlau
Andrianto, T.T. dan Nova Indarto, 2004. Kedelai Kacang Hijau Kacang Panjang, Absolut. Yogyakarta.
Cahyadi W. 2006. Bahan Tambahan Pangan. Bumi Aksara, Jakarta
Cahyadi W, 2006. Kedelai Khasiat dan Teknologi. Bumi Aksara, Jakarta
Cai R. 2002. Textural Property of Six Legume Curds in Relation to Their Protein Contituents. Deartement of Food Science and Human Nutrition and IMPACT. Washington State University, Washington. http://www.impact.wsu.edu
deMann J.M. 1997. Kimia Makanan. Jurusan Farmasi, ITB, Bandung.
Dewi, N.R. 2006. Pengaruh Suhu Koagulasi dan intensitas Penambahan “Whey” Sebagai Koagulan Terhadap Karateristik Fsikokimia dan Organoleptik tahu yang dihasilkan. THP, FTP, Unibraw, Malang.
Djoko, 2003. Kesehatan Tak ternilai Harganya.www.kimia.net Tangaal akses 9 Desembeer 2009.
Driscoll, 1986. Earth Sciences pH of the Water. www.water-resate.com. Tanggal akses 8 Desember 2009
Eryanti, 2004. Pemanfaatan Rumput Laut Sebagai Bahan Dodol. www.publikasi.umm.ac.id. Tanggal akases 11 Desember 2009
Kohir I, 2009. pH Air. PT. CIPTA MULIA SENTOSA. www.puretex.com
Fennema, O. R. 1996. Food Chemistry. Third Edition. Marcel Dekker, Inc. New York.
Irfahmi, 2009. Manfaat Kacang Hijau dan Kedelai. www.gizi.tnet. Tanggal akses 14 maret.2009
Harianto,2005. Nilai Gizi, Sifat Fisik dan Mutu Organoleptik "Jeli Liput"dari" Lidah Buaya (Aloe vera) dan Rumput Laut (Eucheuma cottonii). www.adln-lib-unair.ac.id. Tanggal akses 10 Desember 2009
Nakamura, Korosumi. A, and Mtui G, 2008. Manufacturing Method of okara containing Soybean curd Using Steam Exploration. Juranl Of Fod Technologi, Institute of Technologi and Science, University, Tokushima Po.Box 35179, from Des es Saloam Tanzania
Nuryati, 2006. Efektivitas Asam Sitrat Sebagai bahan penggumpal dan pengawet pada produk Tahu. Teknologi Pangan, FTI, Universitas Pembangunan Nasional “Veteran” Jawa Timur, Surabaya
Obatolu A.V, 2008. Efect of diferent coagulants of yield and quality of Tofu from Soymilk. Eur Food Reserch Technologi, www.springer.com
Poedjiadi A, 1994. Dasar-Dasar Biokimia. Penerbit UI-Press: Jakarta.
Rashidah, S., *Jinap, S., Nazamid, S. dan Jamilah, B. 2007. Characterisation of the Ability of Globulins from Legume Seeds to Produce Cocoa Specific Aroma. Faculty of Food Science and Technology, Universiti Putra Malaysia , Selangor, Malaysia.
http/:psasir.upm.edu.my. Diakses 9 Juli 2009
Sarwono, B. 2004. Membuat Aneka Tahu. Penebar Swadaya, Jakarta.
Saneto, B. Dan Susanto, T. 1994, Teknologi pengolahan dan Hasil Interpretasinya,. Gramedia Pustaka Utama, Jakarta.
Santosa E.B, 2003. Pengaruh proporsi Kacang Hijau dan Kedelai serta konsentrasi CaSO4 terhadap proses pembuatan Takoa. Teknologi Pangan, FTI, Universitas Pembangunan Nasional “Veteran” Jatim, Surabaya
Saputra, 2009. Dampak Pencemaran Udara oleh Beleran Oksida. www.chem-is-try.com Tanggal akases 9 Desember 2009.
Siswon,. 2004. Kaya karbohidrat dan Protein, tapi Rendah Lemak. Tabloid Senior. http//:www.gizi.net . Diakses 3 Agustus 2009
Subagio A, 2002. Kajian sifat Fisikokimia dan Organoleptik Hidrolisat Tempe hasil Hidolisis Protease. Jurnal FTP, Unjem. Jember