BAB II
TINJAUAN PUSTAKA
2.1 Uraian Tumbuhan
Uraian tumbuhan meliputi habitat, nama daerah, nama asing, morfologi tumbuhan, sistematika tumbuhan, kandungan kimia dan kegunaan dari tumbuhan. 2.1.1 Daerah Tumbuh
Kurmak mbelin adalah tumbuhan yang berasal dari wilayah Indo-China, yang tumbuh di daerah tropis di Asia dan Afrika. Tumbuhan ini umum ditemukan di Asia Tenggara dan beberapa negara di Asia Selatan (Kuri, et al., 2014).
Tumbuhan kurmak mbelin terdapat pada daerah yang beriklim subtropis dan tropis. Tumbuhan ini tumbuh di dataran tinggi dengan ketinggian 1800 m dari permukaan laut. Tumbuhan ini biasanya terdapat di selokan atau aliran sungai kecil, tepi kolam ikan, rawa dan sawah (Anonim, 2010).
2.1.2Nama Daerah
Nama daerah kurmak mbelin menurut Anonim (2010) adalah sebagai berikut:
Sumatera : Ambur
Jawa Barat : Kokoha, Godobos 2.1.3 Nama Asing
Nama asing kurmak mbelin menurut Ali, et., al (2013) dan Uddin (2013) adalah sebagai berikut:
Bangladesh : Helencha, Harhack, Hinchashak Filipina : Kangkong kelabaw
Indonesia : Kokoha, Godobos, Ambur Kamboja : Kanting ring
Inggris : Buffalo spinach, Water cress, Marsh herb Malaysia : Chengkeru, Kangkong kerbau
Thailand : Phakbum-ruang, Phakpaeng 2.1.4 Sistematika Tumbuhan
Sistematika tumbuhan kurmak mbelin menurut Ali, et al., (2013) adalah sebagai berikut:
Kingdom : Plantae
Divisi : Spermatophyta Sub divisi : Angiospermae Kelas : Dicotyledoneae Ordo : Asterales Famili : Asteraceae Genus : Enydra
Spesies : Enydra fluctuans Lour. 2.1.5Morfologi Tumbuhan
2.1.6 Kandungan kimia
Tumbuhan kurmak mbelin kaya akan protein dan merupakan penghasil β
-carotene yang baik (3,7 - 4,2 mg/100 g berat tumbuhan segar). Tumbuhan ini
mengandung saponin, tanin, steroid, glikosida, kaurol, giberelin A9 dan A13, seskiterpen laktonnya yaitu germakranolida, enhydrin, fluctuanin dan fluctuandin (Ali, et al., 2013).
2.1.7 Kegunaan
Semua bagian kurmak mbelin yang berwarna hijau terutama pucuk muda, digunakan sebagai sayur di Asia Tenggara, baik mentah maupun direbus. Di Kolkata, daun tumbuhan ini dibuat menjadi jus dan digunakan sebagai tonik yang diberikan pada penderita neuralgia dan penyakit saraf lainnya. Di Filipina, daunnya ditumbuk dan digunakan untuk mengobati kulit yang melepuh pada penderita penyakit herpes. Daunnya sedikit pahit, digunakan sebagai antiinflamasi, pencahar, pengobatan penyakit kulit dan cacar. Berdasarkan hasil penelitian, telah dilaporkan bahwa tumbuhan ini memiliki aktivitas antioksidan, antimikroba, antihelmintik dan hipotensif (Ali, et al., 2013; Kumar, et al., 2012).
2.2 Uraian Kandungan Kimia Tumbuhan 2.2.1 Alkaloida
Contoh:
Gambar 2.1 Koniina 2.2.2 Flavonoida
Golongan flavonoid dapat digambarkan sebagai deretan senyawa C6-C3-C6. Yang berarti, kerangka karbonnya terdiri atas dua gugus C6 (cincin benzena tersubstitusi) disambungkan oleh rantai alifatik tiga karbon (Robinson, 1995).
Flavonoid mencakup banyak pigmen yang paling umum dan terdapat pada seluruh dunia tumbuhan mulai dari fungi sampai angiospermae. Beberapa fungsi flavonoid untuk tumbuhan ialah sebagai pengatur tumbuh, pengatur fotosintesis, antimikroba dan antivirus (Robinson, 1995).
Contoh:
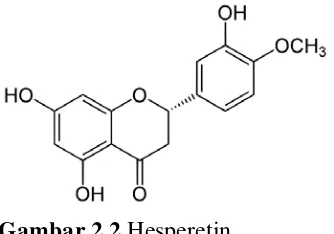
Gambar 2.2 Hesperetin 2.2.3 Saponin
sangat encer saponin sangat beracun untuk ikan, dan tumbuhan yang mengandung saponin telah digunakan sebagai racun ikan selama beratus-ratus tahun. Beberapa saponin bekerja sebagai antimikroba (Robinson, 1995).
Molekul saponin terdiri dari dua bagian yaitu, aglikon dan glikon. Bagian aglikon atau non-sakarida dari molekul molekul saponin disebut genin atau sapogenin. Berdasarkan aglikonnya, Hostettman dan Marston (1995) membagi saponin menjadi 3 kelas utama yaitu:
1. Glikosida triterpenoid 2. Glikosida steroid
3. Glikosida steroid alkaloid Contoh:
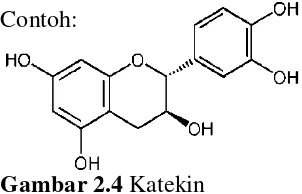
Gambar 2.3 Diosgenin 2.2.4 Tanin
Tanin terdapat luas dalam tumbuhan berpembuluh, dalam angiospermae terdapat khusus dalam jaringan kayu. Pada kenyataanya, sebagian besar tumbuhan yang banyak tanin dihindari oleh hewan pemakan tumbuhan karena rasanya yang sepat (Harborne, 1987).
Contoh:
2.2.5 Glikosida
Glikosida adalah suatu golongan senyawa bila dihidrolisis akan terurai menjadi gula (glikon) dan senyawa lain (aglikon atau genin). Umumnya glikosida mudah terhidrolisis oleh asam mineral atau enzim. Hidrolisis oleh asam memerlukan panas, sedangkan hidrolisis oleh enzim tidak memerlukan panas (Sirait, 2007).
Berdasarkan ikatan antara glikon dan aglikon, glikosida dapat dibedakan menjadi (Sirait, 2007):
a. Tipe O-glikosida, ikatan antara bagian glikon dengan aglikon melalui jembatan O.
Contoh:
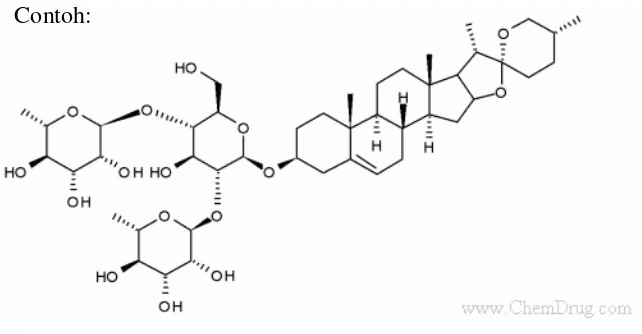
Gambar 2.5 Dioscin
b. Tipe S-glikosida, ikatan antara bagian glikon dengan aglikon melalui jembatan S.
Contoh:
c. Tipe N-glikosida, ikatan antara bagian dari glikon dengan aglikon melalui jembatan N.
Contoh:
Gambar 2.7 Nikleosidin
d. Tipe C-glikosida, ikatan antara bagian glikon dengan aglikon melalui jembatan C.
Contoh:
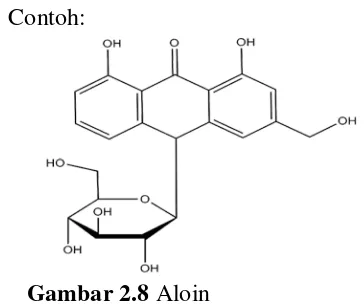
Gambar 2.8 Aloin 2.2.6 Glikosida antrakuinon
Golongan kuinon alam terbesar terdiri dari antrakuinon. Beberapa antrakuinon merupakan zat warna penting dan yang lainnya sebagai pencahar. Keluarga tumbuhan yang kaya akan senyawa jenis ini ialah Rubiaceae, Rhamnaceae, Polygonaceae (Robinson, 1995). Contoh: Aloin.
2.2.7 Steroid/triterpenoid
dari hidrokarbon C30 asiklik, yaitu skualena. Triterpenoid berupa senyawa tanpa warna, berbentuk kristal, sering kali bertitik leleh tinggi dan aktif optik. Uji yang banyak digunakan ialah reaksi Liebermann-Burchard yang dengan kebanyakan triterpena dan sterol memberikan warna hijau-biru (Harborne, 1987).
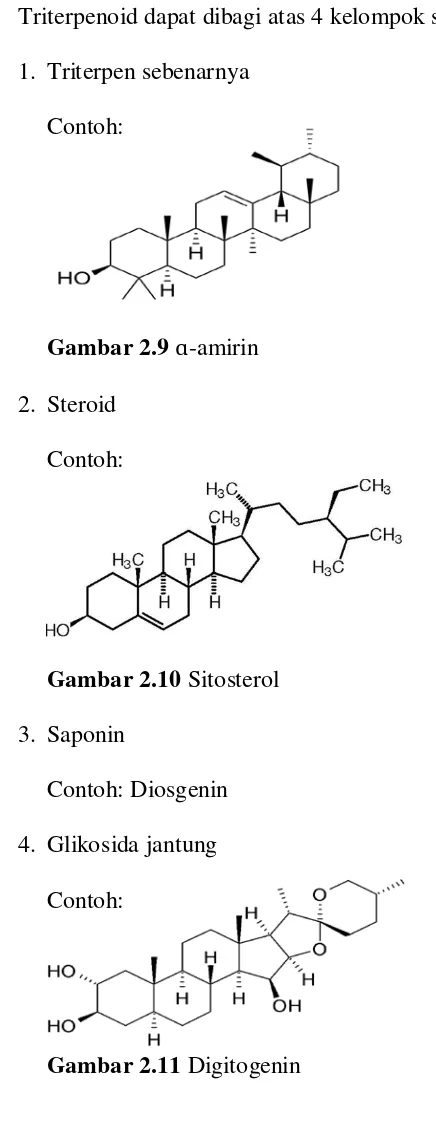
Triterpenoid dapat dibagi atas 4 kelompok senyawa yaitu: 1. Triterpen sebenarnya
Contoh:
Gambar 2.9 ɑ-amirin 2. Steroid
Contoh:
Gambar 2.10 Sitosterol 3. Saponin
Contoh: Diosgenin 4. Glikosida jantung
Contoh:
Senyawa triterpenoid merupakan komponen aktif dalam tumbuhan obat yang telah digunakan untuk penyakit termasuk diabetes, gangguan menstruasi, patukan ular, gangguan kulit, kerusakan hati, dan malaria (Harborne, 1987; Robinson, 1995).
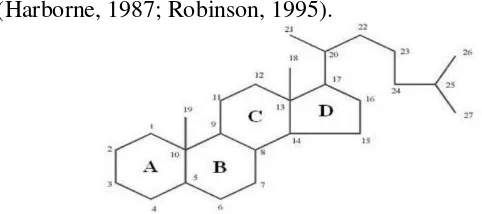
Sterol adalah triterpen yang kerangka dasarnya sistem cincin siklopentana perhidrofenantren. Dahulu steroid dianggap sebagai senyawa satwa (digunakan sebagai hormon kelamin, asam empedu) tetapi pada tahun-tahun terakhir ini makin banyak senyawa steroid yang ditemukan dalam jaringan tumbuhan (Harborne, 1987; Robinson, 1995).
Gambar 2.12 Struktur dasar steroida dan sistem penomorannya Menurut asalnya senyawa steroid dibagi atas:
a. Zoosterol, yaitu steroid yang berasal dari hewan. Contoh:
Gambar 2.13 Kolesterol
b. Fitosterol, yaitu steroid yang berasal dari tumbuhan. Contoh:
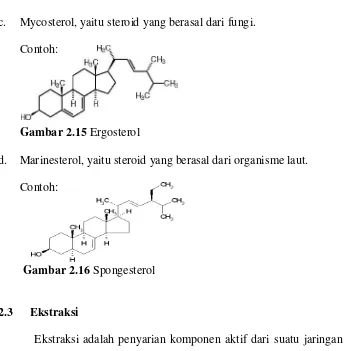
c. Mycosterol, yaitu steroid yang berasal dari fungi. Contoh:
Gambar 2.15 Ergosterol
d. Marinesterol, yaitu steroid yang berasal dari organisme laut. Contoh:
Gambar 2.16 Spongesterol
2.3 Ekstraksi
Ekstraksi adalah penyarian komponen aktif dari suatu jaringan tumbuhan atau hewan dengan menggunakan pelarut yang cocok (Handa, 2008).
Beberapa metode ekstraksi dengan menggunakan pelarut yaitu: A. Cara dingin
1. Maserasi
Maserasi adalah proses pengekstrakan simplisia dengan menggunakan pelarut dengan beberapa kali pengocokan atau pengadukan pada temperatur kamar. Maserasi kinetik berarti dilakukan pengadukan yang kontinu (terus – menerus). Remaserasi berarti dilakukan penyaringan maserat pertama, dan seterusnya (Depkes, 2000).
2. Perkolasi
Proses perkolasi terdiri dari tahap pengembangan bahan, tahap maserasi antara, tahap perkolasi sebenarnya (penetesan/penampungan ekstrak), terus menerus sampai diperoleh ekstrak (perkolat) yang jumlahnya 1 - 5 kali bahan (Depkes, 2000).
B. Cara panas 1. Refluks
Refluks adalah ekstraksi dengan menggunakan pelarut pada temperatur titik didihnya, selama waktu tertentu dan jumlah pelarut terbatas yang relatif konstan dengan adanya pendingin balik.
2. Digesti
Digesti adalah maserasi kinetik (dengan pengadukan kontinu) pada temperatur lebih tinggi dari temperatur ruangan (kamar), yaitu secara umum dilakukan pada temperatur 40 - 50oC.
3. Sokletasi
Sokletasi adalah proses penyarian dengan menggunakan pelarut yang selalu baru yang umumnya dilakukan dengan alat khusus sehingga terjadi ekstraksi kontinu dengan jumlah pelarut yang relatif konstan dengan adanya pendingin balik.
4. Infundasi
5. Dekoktasi
Dekoktasi adalah infus pada waktu yang lebih lama (≥30 menit) dan temperatur sampai titik didih air (Depkes, 2000).
2.4 Kromatografi
Kromatografi adalah suatu metode pemisahan berdasarkan perbedaan perpindahan dari komponen-komponen senyawa di antara dua fase yaitu fase diam (dapat berupa zat cair atau zat padat) dan fase gerak (dapat berupa gas atau zat cair). Jika fase diam berupa zat padat maka cara tersebut dikenal sebagai kromatografi serapan, jika zat cair dikenal sebagai kromatografi partisi (Depkes, 1995; Sastrohamidjojo, 1985).
Pemisahan dan pemurnian kandungan kimia tumbuhan terutama dilakukan dengan menggunakan salah satu dari lima teknik kromatografi atau gabungan teknik tersebut. Kelima teknik kromatografi itu adalah: kromatografi kolom (KK), kromatografi kertas (KKt), kromatografi lapis tipis (KLT), kromatografi gas cair (KGC), dan kromatografi cair kinerja tinggi (KCKT). Pemilihan teknik kromatografi sebagian bergantung pada sifat kelarutan dan keatsirian senyawa yang akan dipisah (Harborne, 1987).
2.4.1 Kromatografi lapis tipis
Kromatografi lapis tipis merupakan metode pemisahan campuran analit dengan mengelusi analit melalui suatu lempeng kromatografi lalu melihat komponen/analit yang terpisah dengan penyemprotan atau pewarnaan (Gandjar dan Abdul, 2012).
Campuran yang akan dipisah, berupa larutan ditotolkan berupa bercak ataupun pita, setelah plat atau lapisan dimasukkan ke dalam bejana tertutup rapat yang berisi larutan pengembang yang cocok (fase gerak), pemisahan terjadi selama pengembangan, selanjutnya senyawa yang tidak berwarna harus ditampakkan (Stahl, 1985).
Pendeteksian bercak hasil pemisahan dapat dilakukan dengan beberapa cara. Untuk senyawa tak berwarna cara yang paling sederhana adalah dilakukan pengamatan dengan sinar ultraviolet. Beberapa senyawa organik bersinar atau berfluorosensi jika disinari dengan sinar ultraviolet gelombang pendek (254 nm) atau gelombang panjang (366 nm), jika dengan cara itu senyawa tidak dapat dideteksi maka harus disemprot dengan pereaksi yang membuat bercak tersebut tampak yaitu pertama tanpa pemanasan, kemudian bila perlu dengan pemanasan (Gritter, et al., 1991; Stahl, 1985).
a. Fase diam (lapisan penyerap)
Fase diam berupa lapisan tipis yang terdiri atas bahan padat yang dilapiskan pada permukaan penyangga datar yang biasanya terbuat dari kaca, plastik atau logam. Lapisan fase diam melekat pada permukaan dengan bantuan bahan pengikat, biasanya kalsium sulfat atau amilum (Gritter, et al., 1991).
b. Fase gerak (pelarut pengembang)
Fase gerak ialah medium angkut yang terdiri atas satu atau campuran beberapa pelarut, jika diperlukan sistem pelarut multi komponen, harus berupa suatu campuran sesederhana mungkin yang terdiri atas maksimum tiga komponen (Stahl, 1985).
Pemisahan pada KLT dikendalikan oleh rasio distribusi komponen dalam sistem fase diam/penyerap dan fase gerak tertentu. Profil pemisahan pada KLT dapat dimodifikasi dengan mengubah rasio distribusi dengan mengubah komposisi fase gerak dengan memperhatikan polaritas (Gandjar dan Abdul, 2012). c. Harga Rf
Mengidentifikasi noda-noda dalam kromatogram KLT sangat lazim menggunakan harga Rf (Retardation Factor) yang didefinisikan sebagai:
Rf= Jarak titik pusat bercak dari titik awal Jarak garis depan pelarut dari titik awal
Faktor-faktor yang mempengaruhi harga Rf: a. struktur kimia dari senyawa yang sedang dipisahkan, b. Sifat penyerap, c. tebal dan kerataan lapisan penyerap, d. pelarut dan derajat kemurniannya, e. derajat kejenuhan uap pengembang dalam bejana, f. teknik percobaan, g. jumlah cuplikan yang digunakan, h. Suhu dan i. kesetimbangan (Sastrohamidjojo, 1985).
2.4.2 Kromatografi kolom
Kromatografi kolom biasanya dikembangkan dengan campuran pelarut yang terus-menerus berubah dengan cara landaian. Eluat yang keluar dari dasar kolom harus dipantau untuk mengetahui dimana linarut itu berada. Ini dapat dilakukan secara terus-menerus dengan memakai detektor yang cocok atau dengan membagi eluat menjadi sejumlah cuplikan yang berurutan dan menganalisisnya dengan KLT (Gritter, et al., 1991).
2.4.3 Kromatografi lapis tipis preparatif
Kromatografi lapis tipis (KLT) preparatif merupakan salah satu metode pemisahan yang memerlukan pembiayaan paling murah dan menggunakan peralatan sederhana. Ketebalan penyerap yang sering dipakai adalah 0,5 - 2 mm, ukuran plat kromatografi biasanya 20 x 20 cm. Pembatasan ketebalan lapisan dan ukuran plat sudah tentu mengurangi jumlah bahan yang dapat dipisahkan dengan KLT preparatif. Penyerap yang paling umum digunakan adalah silika gel (Hostettmann, et al., 1995).
Penotolan cuplikan dilakukan dengan melarutkan cuplikan dalam sedikit pelarut. Cuplikan ditotolkan berupa pita dengan lebar pita sesempit mungkin karena pemisahan tergantung pada lebar pita. Penotolan dapat dilakukan dengan pipet tetapi lebih baik dengan penotol otomatis. Pengembangan plat KLT preparatif dilakukan dalam bejana kaca yang dapat menampung beberapa plat. Bejana dijaga tetap jenuh dengan pelarut pengembang dengan bantuan kertas saring yang tercelup ke dalam pengembang (Hostettmann, et al., 1995).
yaitu dengan cara menutup plat dengan sepotong kaca lalu menyemprot kedua sisi dengan penyemprot (Hostettmann, et al., 1995).
2.4.4 Kromatografi lapis tipis dua arah (two-dimensional TLC)
KLT dua arah atau KLT dua dimensi ini bertujuan untuk meningkatkan resolusi sampel ketika komponen-komponen solut mempunyai karakteristik kimia yang hampir sama, karena nilai Rf juga hampir sama. Selain itu, dua sistem fase gerak yang sangat berbeda dapat digunakan secara berurutan pada suatu campuran tertentu sehingga memungkinkan untuk melakukan pemisahan analit yang mempunyai tingkat polaritas yang hampir sama. Dengan demikian maka KLT dua dimensi dapat dipakai untuk memeriksa kemurnian isolat (Rohman, 2009).
KLT dua dimensi dilakukan dengan melakukan penotolan sampel disalah satu sudut lapisan lempeng tipis dan mengembangkannya sebagaimana biasa dengan fase gerak pertama. Lempeng kromatografi selanjutnya dipindahkan dari chamber pengembang dan eluen dibiarkan menguap dari lempeng. Lempeng
dimasukkan ke dalam chamber yang menggunakan eluen kedua sehingga pengembangan dapat terjadi pada arah kedua yang tegak lurus dengan arah pengembangan yang pertama. Suksesnya pemisahan tergantung pada kemampuan untuk memodifikasi selektifitas eluen kedua dibandingkan dengan selektifitas eluen pertama (Rohman, 2009).
2.5 Spektrofotometri
2.5.1 Spektrofotometri sinar ultraviolet
nm. Serapan cahaya oleh molekul dalam daerah spektrum ultra violet tergantung pada struktur elektronik dari molekul yang bersangkutan (Sastrohamidjojo, 1985).
Suatu atom atau molekul menyerap sinar UV dan energi tersebut akan menyebabkan tereksitasinya elektron pada kulit terluar ke tingkat energi yang lebih tinggi. Tipe eksitasi tergantung panjang gelombang cahaya yang diserap. Gugus yang dapat mengabsorpsi cahaya disebut dengan gugus kromofor (Dachriyanus, 2004).
Pelarut yang banyak digunakan untuk spektrofotometri sinar UV adalah etanol 95% karena kebanyakan golongan senyawa larut dalam pelarut tersebut dan etanol tidak menyerap sinar UV. Alkohol mutlak niaga harus dihindari karena mengandung benzena yang dapat menyerap di daerah sinar UV pendek. Pelarut yang sering digunakan ialah air, etanol, metanol, n-heksana, eter minyak bumi dan eter. Konsentrasi dari analit di dalam larutan bisa ditentukan dengan mengukur absorban pada panjang gelombang tertentu dengan menggunakan hukum Lambert-Beer (Gandjar dan Rohman, 2007; Harborne, 1987).
2.5.2 Spektrofotometri sinar inframerah