BAB III
METODE PENELITIAN
3.1 Lokasi Penelitian
Penelitian dilakukan di Laboratorium Farmasi Fisik Fakultas Farmasi Universitas Sumatera Utara, Laboratorium Penelitian Fakultas Farmasi Universitas Sumatera Utara, dan Laboratorium Fitokimia Fakultas Farmasi Universitas Sumatera Utara.
3.2 Jenis Penelitian
Jenis penelitian yang dilakukan adalah penelitian eksperimental yang meliputi pembuatan beadsalginat yang mengandung ekstrak kunyit,evaluasi dan karakterisasi sediaan, uji in vitro dan uji in vivo.
3.3 Alat
Alat-alat yang digunakan adalah alat disolusi metode dayung (Erweka), beaker glass (Pyrex), cawan porselen, erlenmeyer (Pyrex), gelas arloji, gelas ukur
3.4 Bahan
Bahan-bahan yang digunakan adalah rimpang kunyit (Curcuma domesticaVal.), etanol 96%, Akua DM (Brataco), Kurkumin baku (Sigma
Aldrich), Tween 80 (Merck), Natrium alginat 80-120 cP dan 500-600 cP (Wako pure chemical industries, Ltd. Japan), dan bahan-bahan yang berkualitas pro analysis (Merck): kalsium klorida dan asam klorida. Akuades diperoleh dari laboratorium Farmasi Fisik, Fakultas Farmasi, USU.
3.5 Prosedur Penelitian
3.5.1 Penyiapan bahan tumbuhan
Penyiapan bahan tumbuhan meliputi pengambilan, identifikasi, dan pengolahan bahan.
3.5.1.1 Pengambilan bahan tumbuhan
Metode pengambilan bahan tumbuhan dilakukan secara purposif yaitu diambil dari satu daerah saja tanpa membandingkan dengan tumbuhan yang sama di daerah lain. Bahan tumbuhan diperoleh dari Pasar Sentral, Kota Medan, Provinsi Sumatera Utara.
3.5.1.2 Identifikasi bahan tumbuhan
Identifikasi bahan tumbuhan (rimpang) dilakukan di Herbarium Medanense (MEDA), Universitas Sumatera Utara, Medan.
3.5.1.3 Pengolahan bahan tumbuhan
ditimbang. Dikeringkan dalam lemari pengering sampai bahan tumbuhan rapuh (dapat dipatahkan) kemudian simplisia ditimbang.
3.5.2 Pemeriksaan karakteristik simplisia
Pemeriksaan karakteristik simplisia meliputi pemeriksaan makroskopik dan mikroskopik, penetapan kadar air, penetapan kadar sari larut air, penetapan kadar sari larut etanol, penetapan kadar abu total, dan penetapan kadar abu yang tidak larut asam (Depkes RI, 1989; WHO, 1992).
3.5.2.1 Pemeriksaan makroskopik
Pemeriksaan makroskopik dilakukan dengan mengamati bentuk, ukuran, warna, dan bau rimpang kunyit.
3.5.2.2 Pemeriksaan mikroskopik
Pemeriksaan mikroskopik dilakukan terhadap serbuk simplisia rimpang kunyit. Serbuk simplisia ditaburkan di atas kaca objek yang telah ditetesi dengan larutan kloralhidrat dan ditutup dengan kaca penutup, kemudian diamati dengan mikroskop. Untuk melihat bentuk butir pati ditetesi dengan akuades.
3.5.2.3 Penetapan kadar air
Penetapan kadar air dilakukan dengan metode Azeotropi, yang meliputi: a. Penjenuhan toluen
b. Penetapan kadar air simplisia
Sebanyak 5 g serbuk simplisia yang telah ditimbang seksama dimasukkan ke dalam labu yang berisi toluen yang telah dijenuhkan, dipanaskan secara hati-hati selama 15 menit. Kecepatan tetesan diatur 2 tetes per detik setelah toluen mendidih sampai sebagian besar air terdestilasi, kemudian kecepatan destilasi dinaikkan sampai 4 tetes per detik. Bagian dalam pendingin dibilas dengan toluen setelah semua air terdestilasi. Destilasi dilanjutkan selama 5 menit, tabung penerima dibiarkan mendingin pada suhu kamar. Volume air dibaca setelah air dan toluen memisah sempurna dengan ketelitian 0,05 ml. Selisih kedua volume air yang dibaca sesuai dengan kadar air yang terdapat dalam bahan yang diperiksa. Kadar air dihitung dalam persen (WHO, 1992).
3.5.2.4 Penetapan kadar sari larut air
Sebanyak 5 g serbuk dimaserasi selama 24 jam dalam 100 ml air - kloroform (2,5 ml kloroform dalam akuades sampai 1 liter) dengan menggunakan botol bersumbat warna coklat sambil sekali-kali dikocok selama 6 jam pertama, kemudian dibiarkan selama 18-24 jam dan disaring, sejumlah 20 ml filtrat pertama diuapkan hingga kering dalam cawan yang telah dipanaskan dan ditara. Residu dipanaskan dalam oven pada suhu 1050C sampai diperoleh bobot tetap. Kadar sari yang larut dalam air dihitung terhadap bahan yang telah dikeringkan diudara (Depkes RI, 1989).
3.5.2.5 Penetapan kadar sari larut etanol
disaring.Sejumlah 20 ml filtrat pertama diuapkan hingga kering dalam cawan yang telah dipanaskan dan ditara. Residu dipanaskan dalam oven pada suhu 1050C sampai diperoleh bobot tetap. Kadar sari larut dalam etanol dihitung terhadap bahan yang telah dikeringkan diudara (Depkes RI, 1989).
3.5.2.6 Penetapan kadar abu total
Lebih kurang 2 g zat yang telah digerus dan ditimbang seksama, dimasukkan kedalam krus porselin yang telah dipijar dan ditara, kemudian diratakan. Krus porselen bersama isinya dipijarkan perlahan–lahan hingga arang habis, didinginkan, ditimbang sampai diperoleh bobot yang tetap. Kadar abu dihitung terhadap bahan yang telah dikeringkan diudara (Depkes RI, 1989).
3.5.2.7 Penetapan kadar abu yang tidak larut asam
Abu yang diperoleh pada penetapan kadar abu total dididihkan dengan 25 ml asam klorida encer selama 5 menit, dikumpulkan bagian yang tidak larut dalam asam, disaring dengan kertas saring, lalu dicuci dengan air panas. Kemudian residu dan kertas saring dipijarkan sampai diperoleh bobot tetap, didinginkan dan ditimbang beratnya. Kadar abu yang tidak larut dalam asam dihitung terhadap bahan yang telah dikeringkan diudara (Depkes, 1989).
3.5.3Pembuatan pereaksi
3.5.3.1 Pembuatan larutan kalsium klorida 0,15 M
Kalsium klorida ditimbang 22,053 gram kemudian dilarutkan dengan akua bebas CO2 secukupnya sampai 1000 ml (Ditjen POM, 1995).
3.5.3.2 Pembuatan medium lambung buatan (medium pH 1,2)
3.5.4 Pembuatan kurva serapan dan kurva kalibrasi kurkumin
3.5.4.1 Pembuatan larutan induk baku kurkumin
Dilarutkan 10 mg kurkumin baku dengan etanol hingga larut sempurna di dalam labu 10 ml, kemudian dicukupkan HCl 0,1 N(LIB I= 1000 ppm). Kemudian dipipet 5 ml ke dalam labu 50 ml (LIB II= 100 ppm).
3.5.4.2 Pembuatankurva serapankurkumin dalam medium lambung pH 1,2
Dipipet 1 ml dari LIB II ke dalam labu 10 ml, dicukupkan dengan HCl 0,1 N. Diukur pada λ 400-800 nm.
3.5.4.3 Pembuatan kurva kalibrasi kurkumin dalammediumlambung pH 1,2
Dipipet 2,5, 5, 7, 10, 12,5 ml dari LIB II, dimasukkan ke dalam labu 50 ml, dicukupkan dengan HCl 0,1 N (konsentrasi 5, 10, 15, 20, 25 ppm). Diukur pada λmaksimum (λ= 428 nm).
3.5.5 Pembuatan ekstrak kunyit
Dihaluskan simplisia rimpang kunyit, kemudian ditimbang. Dimaserasi serbuk kunyit (750 gram) dengan etanol 96% (5 liter) selama 5 hari, kemudian di remaserasi selama 3 hari dengan etanol 96% (3 liter). Kemudian diuapkan dengan rotary evaporator hingga didapatkan ekstrak kental dan diuapkan dengan
waterbathhingga ekstrak bebas dari pelarut.
3.5.6 Pembuatan beadsalginat
R/ Ekstrak kunyit 5, 10, 15%
Tween 80 5%
Timbang seksamaNatrium Alginat, didispersikan ke sejumlah akua DM dan didiamkan selama 24 jam. Ekstrak kunyit digerus dengan etanol secukupnya hingga larut, kemudian ditambahkan Tween 80. Natrium alginat dimasukkan dan dihomogenkan. Kemudian diteteskan ke dalam larutan kalsium klorida (CaCl2)
0,15 M dengan curing time 4-5 menit. Beads dibilasdengan akua DM, dikumpulkan dan dikeringkan di suhu ruangan selama 2 hari.Beads disimpan dalam desikator hingga waktu pemakaian.
3.5.7 Karakterisasi beads
3.5.7.1 Penentuan berat beads
Dilakukan penimbangan 20 beads sebanyak 6 kali. 3.5.7.2 Penentuan ukuran beads
Dilakukan pengukuran sebanyak 6 beads dari 3 sisi diameter, dirata-ratakan diameter untuk memperolah diameter beads.
3.5.8 Penentuan PenjerapanBeads
Ditimbang ±50 mg beads, diekstrak dengan etanol 96% secukupnya sampai larutan tidak menghasilkan absorbansi pada spektrofotometer. Dimasukkan hasil ekstrak ke labu tentukur 50 ml, dicukupkan dengan medium lambung buatan pH 1,2. Dipipet 1 ml ke dalam labu 20 ml, kemudian dipipet kembali 1 ml ke dalam labu 10 ml. Diukur pada λ 428 nm.
3.5.9 Studi pelepasan in-vitro
Medium disolusi : medium lambung buatan (pH 1,2) Kecepatan Pengadukan : 50 rpm
Volume medium : 900 ml
Metode : dayung
Ditimbang beadsalginat dan dimasukkan ke apparatus disolusi tipe dayung berisi 900 ml medium lambung buatan, suhu 37±0,5oC dengan kecepatan 50 rpm. Sampel diambil pada interval waktu 5 menit, 10 menit, 15 menit, 30 menit, 45 menit, 60 menit, lalu sampel selanjutnya diambil pada interval 30 menit. Diambil aliquot sebanyak 5 ml dan dijaga volume nya tetap 900 ml. Pengambilan dilakukan pada tempat yang sama yaitu pertengahan antara permukaan medium disolusi dan bagian atas dari dayung tidak kurang dari 1 cm dari dinding wadah (Ditjen POM, 1995). Sampel dianalisis dengan Spektrofotometer pada λmaks untuk menentukan konsentrasi obat.
3.5.10 Uji bioadhesi
Dipilih formula dengan pelepasan paling bagus dan dilakukan uji bioadhesif in vitro. Mukosa lambung tikus dibersihkan, dan direndam dalam NaCl fisiologis. Mukosa lambung ditempelkan ke kaca objek dengan bagian muka menghadap ke atas. Dimiringkan kaca objek dengan sudut 450. Sebanyak 20 beads ditempelkan di atas mukosa lambung, kemudian ditetesi cairan lambung
buatan dan dibiarkan 1 menit. Mukosa dialiri dengan cairan lambung buatan suhu 37 ± 0,50C dengan kecepatan 22 ml/ menit. Dihitung jumlah beads yang tertinggal pada 5 menit dan 10 menit. Dihitung nomor adhesi dengan rumus:
Na =�
N No � � 100
3.5.11 Induksi luka lambung dengan larutan HCl 1 M dan penyembuhan lesi lambung menggunakan beads alginat dari ekstrak kunyit
Tikus yang dipakai berjenis kelamin jantan dengan berat 150-200 g. Semua tikus diaklimatisasi selama 1 minggu sebelum perlakuan. Tikus dipuasakan selama 36 jam, kemudian diinduksi dengan 1 ml larutan HCl 1 M untuk membuat luka lambung (Bangun, et al., 2016). Setelah 1 jam induksi, 3 tikus dikorbankan dengan dislokasi, kemudian lambung dibuka dan dicuci dengan larutan NaCl 0,9%, dan luka diamati secara makroskopik dan mikroskopik (histopatologi).
BAB IV
HASIL DAN PEMBAHASAN
4.1 Identifikasi Tumbuhan
Hasil identifikasi yang dilakukan oleh Herbarium Medanense (MEDA) terhadap tumbuhan yang diteliti adalah tumbuhan Curcuma domestica Val. suku Zingiberaceae. Hasil identifikasi tumbuhan dapat dilihat pada Lampiran 4.
4.2 Karakteristik Simplisia
Hasil karakterisasi simplisia rimpang kunyit dapat dilihat pada Tabel 4.1. Tabel 4.1 Hasil karakterisasi simplisia rimpang kunyit
No. Pemeriksaan karakteristik
simplisia A (%) B (%)
1 Kadar air 11,95 8-13,7
2 Kadar sari larut etanol 20,81 > 10
3 Kadar sari larut air 17,31 > 15
4 Kadar abu total 7,185 < 9
5 Kadar abu tidak larut asam 0,44 < 1,6 Keterangan:
A: kadar hasil penelitian B: kadar menurut MMI
reaksienzimatik tidak berlangsung lagi bila kadar air dalam simplisia memenuhi persyaratan MMI.
Penetapan kadar sari dilakukan terhadap 2 pelarut, yakni kadar sari larut etanol dan air. Penetapan kadar sari simplisia menyatakan jumlah zat yang dapat tersari dalam etanol dan dalam air. Kadar sari larut etanol yang didapat sebesar 20,81% dan kadar sari larut air yang didapat sebesar 17,31%.
Penetapan kadar abu dimaksudkan untuk mengetahui kandungan mineral yang terkandung dalam simplisa serta senyawa organik yang tersisa selama pembakaran. Kadar abu total yang didapatkan adalah sebesar 7,185%. Sedangkan kadar abu tidak larut asam yang diperoleh sebesar 0,44%.
4.3 Pemeriksaan Makroskopik dan Mikroskopik Rimpang Kunyit
4.3.1 Hasil pemeriksaan makroskopik
Hasil pemeriksaan makroskopik simplisia rimpang kunyit berupa irisan-irisan berbentuk bundar berwarna kuning kecoklatan, warna daging jingga, diameter kira-kira 2-3 cm dan memiliki bau khas.
4.3.2 Hasil pemeriksaan mikroskopik
Hasil pemeriksaan mikroskopik pada simplisia rimpang kunyit terdapat butir pati, rambut penutup dan jaringan parenkim, dapat dilihat pada Lampiran 3.
4.4 Pembuatan dan spesifikasi beads alginat
memilikimanfaat sebagai surfaktan yang membantu pelarutan kurkumin yang praktis tidak larut dalam air dan suasana asam. Campuran alginat kemudian diteteskan ke dalam larutan CaCl2 0,15 M menggunakan spuit dengan ukuran
syringe yang berbeda selama curing time 4-5 menit agar beads yang dihasilkan tidak begitu kompak sehingga dikhawatirkan mempersulit pelepasan bahan aktif dari beads.
(a)
(b)
(d)
(e)
(c) (f)
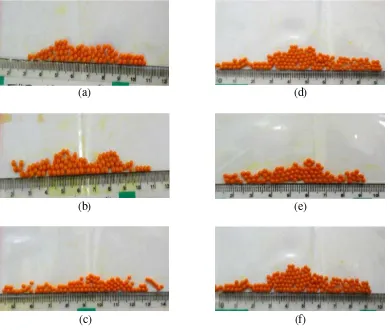
Gambar 4.1Beads alginat sebelum pengeringan. Beads dibuat menggunakan syringe dan alginat berdasarkan keterangan:
Hasil gelasi alginat ditunjukkan pada Gambar 4.1. Beads yang terbentuk memiliki ukuran ± 2 mm dan tidak terdapat perbedaan ukuran yang signifikan diantara masing-masing beads berdasarkan perbedaan viskositas dan ukuran syringe. Setelah itu, dilakukan pengeringan terhadap beads yang dihasilkan. Demikian pula beads setelah pengeringan yang ditunjukkan pada Gambar 4.2, tidak terdapat perbedaan signifikan terlihat dari segi penampakan beads.
(a)
(b)
(c)
(d)
(e)
(f)
Gambar 4.2Beadsalginat setelah pengeringan. Beads dibuat menggunakan syringe dan alginat berdasarkan keterangan:
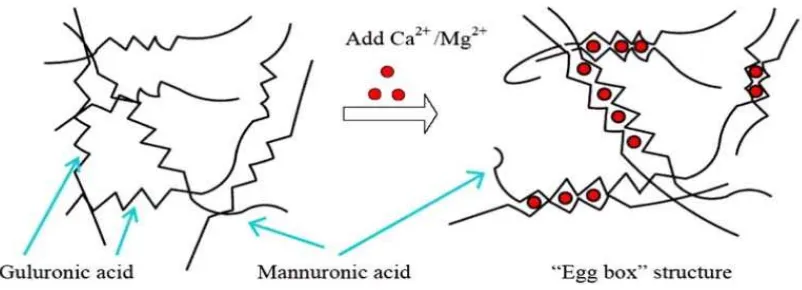
Alginat adalah polisakarida alami linear yang terdiri dari asam β
-D-mannuronat dan asam α-L-guluronat. Kation divalen, seperti ion kalsium
dapatmengikat residu guluronat membentuk struktur “kotak telur” dan menyebabkan gelasi (Grant, et al., 1973; Smidsrod, et al., 1990).
Gambar 4.3 Gelasi larutan alginat dengan penambahan ion kalsium dan pembentukan struktur “kotak telur” (Grant, et al., 1973; Smidsrod, et al., 1990).
4.4.1 Hasil pengukuran diameter beads alginat
Pengukuran diameter beads alginat mengambil rata – rata dari 3 sisi oleh karena bentuk beads yang sferis. Tabel 4.2 menunjukkan bahwa terdapat perbedaan ukuranbeads berdasarkan viskositas dan ukuran syringe. Beads dengan alginat viskositas 500-600 cP memiliki ukuran beads lebih besardibandingkan alginat viskositas80-120 cP.
Tabel 4.2 Perbandingan diameter beads berdasarkan ukuran diameter dalam syringe dan viskositas (n = 6)
Ukuran syringe Viskositas
Ukuran beads (mm) 21G
(ɸ = 0,514 mm)
23G
(ɸ = 0,337 mm)
25G
(ɸ = 0,260 mm)
Semakin kental viskositas alginat yang dipakai, semakin banyak jumlah blok G dalam strukturnya sehingga lebih mudah membentuk gel dengan adanya ion Ca2+ (Tipton, 2010). Alginat viskositas 500-600 cP lebih mudah membentukgel sehingga ukurannya lebih besar daripada viskositas 80-120 cP. Berdasarkan ukuran syringe, semakin kecil ukuran syringe, semakin kecil pula ukuran beads yang diperoleh.
4.4.2 Hasil penimbangan berat beads alginat
Penentuan berat dilakukan dengan menimbang sebanyak 20 beads alginat. Tabel 4.3 menunjukkan bahwa beads 500-600 cP lebih berat dibandingkan beads 80-120 cP. Hal ini sesuai dikarenakan alginat viskositas 500-600 cP yang lebih membentuk gel dengan Ca2+ sehingga menyebabkan beads alginat 500-600 cP lebih berat dibandingkan beads alginat 80-120 cP. Berdasarkan ukuran syringe, semakin besar ukuran syringe maka semakin besar ukuran beads sehingga semakin berat pula beads yang diperoleh.
Tabel 4.3 Perbandingan berat beads berdasarkan ukuran diameter dalam syringe dan viskositas (n = 6)
4.5 Uji pelepasan kurkumin dari beads alginat
4.5.1Hasil uji pelepasan berdasarkan perbedaan viskositas alginat dan ukuran syringe
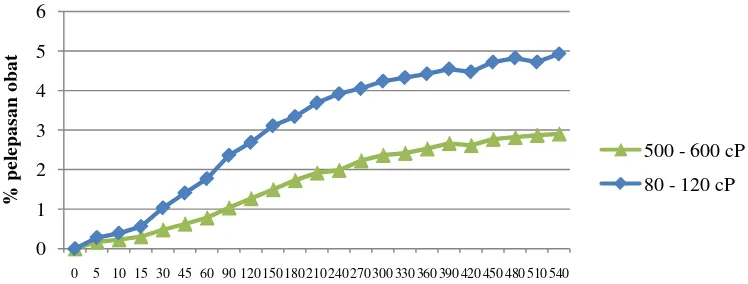
Berdasarkan uji statistikIndependent Sample T Test, pelepasan kurkumin dari beads alginat viskositas 80-120 cP berbeda signifikan dibandingkan viskositas 500-600 cP yang dapat dilihat pada Lampiran 34. Hal ini dikarenakan alginatviskositas 500-600 cP lebih kental sehingga menghasilkan beads yang lebih padat dibandingkan alginat viskositas 80-120 cP. Kepadatan yang tinggi menyulitkan pelepasan obat dari dalam beads.
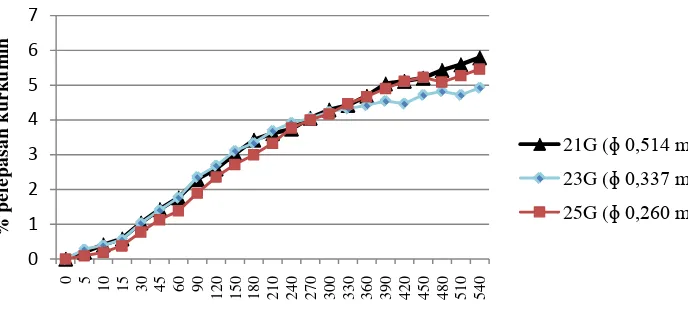
Gambar 4.4Grafik perbandinganpelepasan obatvs waktuberdasarkan
perbedaan viskositas alginatbeads alginat ukuran syringe 23G
(ɸ = 0,337 mm)
Berdasarkan ukuran syringe, ditunjukkan melalui grafik pada Gambar 4.5 bahwa tidak terdapat perbedaan pelepasan kurkumin antara beads dari tiap ukuran syringe. Berdasarkan uji statistik ANOVA, tidak terdapat pelepasan kurkumin
yang signifikan dari beads alginat berdasarkan perbedaan ukuran syringe. Hasil pengujian statistik dapat dilihat pada Lampiran 35. Hal ini dikarenakan ukuran diameter dalam syringe yang tidak berbeda jauh menghasilkan beads dengan ukuran yang tidak berbeda jauh pula sehingga pelepasan kurkumin relatif sama. 4.5.2Hasil Uji Pelepasan Berdasarkan Perbedaan Kadar Ekstrak
0
0 5 10 15 30 45 60 90 120150180210240270300330360390420450480510540
BerdasarkanGambar 4.6, dapat dilihat bahwa ada pengaruh kadar ekstrak terhadap rata-rata % kumulatif obat yang terlepas.Berdasarkan uji statistik ANOVA, tidak terdapat perbedaan AUC yang signifikan dari beads alginat berdasarkan perbedaan kadar ekstrak. Hasil pengujian statistik dapat dilihat pada Lampiran 36. Beads alginat dengan kadar ekstrak terendah yakni 5% menunjukkan pelepasan bahan aktif yang lebih tinggi dibandingkan kadar ekstrak 10% dan 15%. Ini dikarenakan semakin tinggi kadar ekstrak, semakin padat beads sehingga memperkecil pelepasan kurkumin dari beads. Selain itu, formula dengan ekstrak 5% memiliki perbandingan 1:1 terhadap surfaktan Tween 80, sehingga dibandingkan formula dengan ekstrak 10% dan ekstrak 15% (perbandingan ekstrak banding Tween 80 2:1 dan 3:1 berurutan) tidak efisien melepaskan bahan aktif.
Gambar 4.5Grafikperbandingan pelepasan obatvs waktuberdasarkan
Gambar 4.6Grafik pengaruh kadar ekstrak terhadap pelepasan kurkumin 4.6Hasil Kinetika Orde Pelepasan
Kinetika orde pelepasan dilakukan terhadap setiap beads dengan tiga model kinetika yaitu: orde nol, orde satu, dan model Higuchi. Penentuan kinetika pelepasan dilakukan untuk mengetahui berapa persen bahan aktif yang dilepaskan dari waktu ke waktu selama pengujian dengan memplotkan hasil uji pelepasan kurkumin dalam grafik waktu versus persen kumulatif, logaritma persen kumulatif versus waktu, dan persen kumulatif versus akar waktu maka dapat diperoleh nilai korelasi (R2). Kinetika pelepasan dari beads alginat dapat dilihat pada Tabel 4.4, 4.5, 4.6, dan 4.7. Kinetika orde pelepasan kurkumin dari semua beads alginat mengikuti kinetika pelepasan mengikuti kinetika pelepasan Orde Higuchi.
Tabel 4.4 Kinetika pelepasan obat dari beads alginat viskositas 500-600 dengan syringe 23G
Orde Kinetika Pelepasan Persamaan Regresi R2
Orde Nol y = 0,0052x + 0,4959 0,9371
Orde Satu y = 0,0019x - 0,3172 0,7459
Higuchi y = 0,1418x - 0,2334 0,9925
Model persamaan Higuchi adalah model teoritis untuk pelepasan obat yang larut dan sukar larut dalam air dari berbagai matriks, termasuk semipadat
dan padat. Obat yang terdispersi homogen di seluruh matriks dianggap melarut dalam matriks polimer dan berdifusi keluar dari permukaan matriks (Sinko, P. J., 2012).
Tabel 4.5 Kinetika pelepasan obat dari beads alginat viskositas 80-120 dengan syringe 21G
Orde Kinetika Pelepasan Persamaan Regresi R2
Orde Nol y = 0,0147x + 1,529 0,9412
Orde Satu y = 0,0019x + 0,1397 0,6798
Higuchi y = 0,398x - 0,52 0,9979
Tabel 4.6 Kinetika pelepasan obat dari beads alginat viskositas 80-120 dengan syringe 23G
Orde kinetika pelepasan Persamaan regresi R2
Orde Nol y = 0,0083x + 1,203 0,8678
Orde Satu y = 0,0017x - 0,0055 0,6491
Higuchi y = 0,2313x - 0,0426 0,9721
Tabel 4.7 Kinetika pelepasan obat dari beads alginat viskositas 80-120 dengan syringe 25G
Orde kinetika pelepasan Persamaan regresi R2
Orde Nol y = 0,0101x + 0,7747 0,9393
Orde Satu y = 0,0023x - 0,1964 0,6503
Higuchi y = 0,2721x - 0,6248 0,9948
4.7 Uji Bioadhesi
Tabel 4.8 Tabel hasil uji bioadhesi dari beads alginat
Mukoadhesi dan kekuatan interaksi beads alginat dapat dipengaruhi oleh struktur polimer dan gugus fungsional. Saat ini, polimer mukoadhesi yang umum digunakan tersusun atas gugus fungsi polar seperti gugus hidroksil (-OH), karboksil (-COOH), amida (-NH2), dan sulfat (-SO4) yang bisa berinteraksi
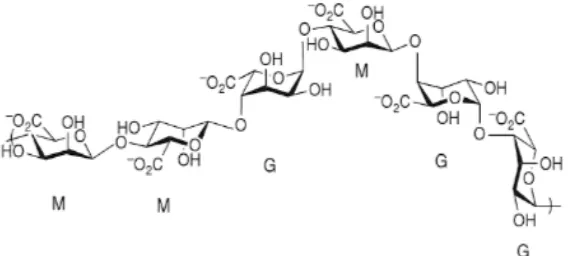
dengan glikoprotein musin (Yu, et al., 2014). Alginat, terlihat pada Gambar 4.7mengandung gugus –OH dan (-COOH) menyebabkan sifat alaminya yang mukoadhesif sehingga cocok sebagai pembawa sediaan farmasi yang gastroretentif melekat di mukosa lambung.
Gambar 4.7 Struktur Alginat. Residu mannuronat diberi label M dan residu guluronat diberi label G (Tipton, 2010)
Percobaan Jumlah beads
Menit 0 Menit 5 Menit 10
1 20 15 15
2 20 18 15
3 20 19 19
4.8 Hasil Uji In Vivo
4.8.1 Penginduksian Lesi Lambung dengan HCl 1 M
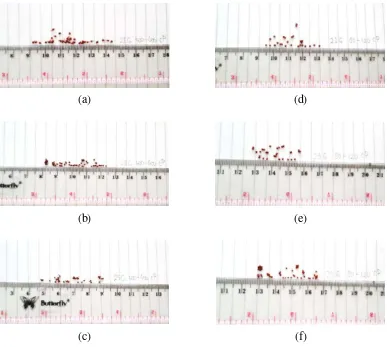
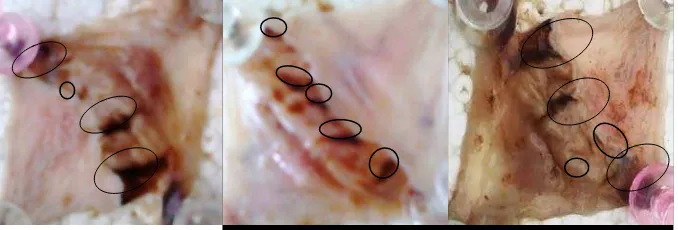
Pada semua tikus menunjukkan terjadinya lesi lambung setelah pemberian larutan HCl 1 M. Gambar 4.8 menunjukkan kerusakan pada mukosa lambung setelah pemberian HCl 1 M.
Gambar 4.8 Mukosa lambung setelah pemberian HCL 1 M
Pada Gambar 4.8 menunjukkan terdapat luka di mukosa lambung tikus yang diinduksi HCl 1 M satu jam sebelum pembedahan. Sekresi asam lambung ditetapkan sebagai salah satu faktor pembentuk tukak dalam menginduksipenyakit tukak lambung. Telah dilaporkan bahwa sekitar 50% pasien tukak lambung mensekresi pepsin dan asam lambung berlebihan (Szabo, et al., 1998; Aihara, et al., 2003; Sunil, et al., 2012).
4.8.2 Penyembuhan Lesi lambung
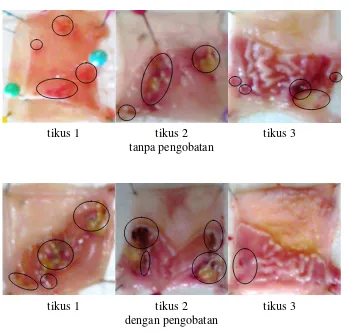
4.8.2.1 Pengamatan makroskopis lambung tikus
tikus 1 tikus 2 tikus 3
tanpa pengobatan
tikus 1 tikus 2 tikus 3
dengan pengobatan
Gambar 4.9 Gambar makroskopik lambung tikus hari ke-2
Pengamatan secara makroskopis lambung tikus dilakukan dengan menghitung jumlah ulkus dan luas ulkus, kemudian dihitung indeks ulkus dari kelompok tanpa pengobatan dan kelompok dengan pengobatan dan dibandingkan.
tikus 1 tikus 2 tikus 3 tanpa pengobatan
tikus 1 tikus 2 tikus 3
dengan pengobatan
Gambar 4.10 Gambar makroskopik lambung tikus hari ke-4
Kelompok tanpa pengobatan masih menunjukkan adanya ulkus hingga pada hari ke-8 pada 1 subjek sedangkan kelompok dengan pengobatan sudah bersih yang ditunjukkan pada Gambar 4.12.
tikus 1 tikus 2 tikus 3
tikus 1 tikus 2 tikus 3 dengan pengobatan
Gambar 4.11 Gambar makroskopik lambung tikus hari ke-6
tikus 1 tikus 2 tikus 3
tanpa pengobatan
tikus 1 tikus 2 tikus 3
dengan pengobatan
Gambar 4.12 Gambar makroskopik lambung tikus hari ke-8
Selain pengamatan makroskopis dengan menghitung jumlah ulkus, dilakukan juga perhitungan indeks ulkus pada masing-masing kelompok. Efek penyembuhan dari beads alginat dapat dilihat juga dari penurunan indeks ulkus pada pembedahan hari kedua sampai hari kedelapan. Hasil indeks ulkus rata-rata pada kedua kelompok dapat dilihat pada Tabel 4.10.
Tabel 4.9 Jumlah ulkus rata-rata pada masing-masing kelompok (n = 3) Hari Jumlah ulkus rata-rata tanpa
pengobatan
Beads Alginat ekstrak kunyit 100 mg /kgBB tikus pengobatan dan dengan pengobatan (n = 3).
Pada Tabel 4.9 dan Gambar 4.13 dapat disimpulkan bahwa beads alginat dengan ekstrak kunyit mampu menyembuhkan lesi lambung lebih cepat jika dibandingkan dengan tanpa pengobatan.
Hari Indeks ulkus rata-rata tanpa pengobatan
Beads Alginat ekstrak kunyit 100 mg/kgBB
Pada Tabel 4.10 dan Gambar 4.14, dilihat dari penurunan indeks ulkus dapat disimpulkan bahwa pemberian beads alginat dapat menyembuhkan ulkus lambung pada tikus, namun dibandingkan dengan kelompok tanpa pengobatan kurang signfikan, dilihat dengan adanya beberapa titik pada grafik dengan pengobatan yang masih bersinggungan dengan grafik tanpa pengobatan.
Grafik perbandingan indeks ulkus pada mukosa lambung masing – masing kelompok tampak pada Gambar 4.14.
Gambar 4.14 Perbandingan indeks ulkus antara kelompok tikus tanpa pengobatan dan yang diberi beads alginat (n = 3)
Sel-sel saluran pencernaan memiliki kecepatan pergantian tinggi yang membuat mukosa saluran pencernaan menjadi jaringan paling cepat berproliferasi dalam tubuh setelah jaringan kulit (Davenport, 1982). Pada kondisi normal, populasi sel dalam saluran pencernaan dipertahankan pada kondisi stabil dinamis
akibat kehilangan sel karena pengelupasan permukaan sel (sebab mukosa lambung sering terpapar senyawa-senyawa yang memiliki pH, osmolaritas, dan suhu dengan rentang luas) diseimbangkan dengan pembaharuan sel yang terus menerus (Lipkin, 1987). Keseimbangan antara sel yang hilang dan pembaharuan sel harus diatur dengan ketat, karena kehilangan sel yang berlebihan dapat menyebabkan atrofi atau pembentukan tukak, sedangkan kelebihan proliferasi atau perpanjangan waktu hidup sel dapat memicu hiperplasia (Johnson dan McCormack, 1994).
Kurkumin, komponen bioaktif dari kunyit, telah menunjukkan peran penting dalam pencegahan dan pengobatan berbagai penyakit kronik proinflamasi termasuk penyakit neurodegeneratif, kardiovaskular, paru-paru, metabolisme, autoimun, dan penyakit mematikan. Aktivitas kurkumin melawan penyakit kronik dihubungkan dengan penghambatan biomarker inflamasi. Banyak studi in vitro telah melaporkan bahwa kurkumin memiliki kemampuan menghambat faktor transkripsi proinflamasi (Krishnaswamy, 2009).
menunjukkan efek penghambatan pada aktivasi NF-kappa B dan juga IL oleh H. pylori (Munzeinmaier, et al., 1997). Ini menjelaskan efek anti H. pylori dari kunyit dan kemudian penyembuhan tukak lambungnya.
4.8.2.2 Pengamatan mikroskopis lambung tikus
Pengamatan mikroskopis dilakukan dengan uji histologi jaringan lambung tikus. Gambar 4.15 menunjukkan hasil mikroskopik dari lambung tikus normal.
Gambar 4.15 Hasil mikroskopik lambung normal perbesaran 40 (kiri) dan 100 (kanan)
Keterangan: 1. Lapisan mukosa
2. Lapisan muskularis mukosa 3. Lapisan submukosa
4. Lapisan tunika muskularis
Pada Gambar 4.16 menunjukkan tikus kelompok kontrol ulkus setelah 1 jam pemberian HCl. Erosi yang terbentuk ditunjukkan oleh gambar panah. Terjadi kerusakan dan erosi sel-sel epitel yang cukup dalam (ditunjukkan oleh anak panah) pada permukaan mukosa lambung karena bersentuhan langsung dengan HCl. Iritasi yang bersifat lokal menimbulkan kerusakan jaringan dan menyebabkan difusi kembali asam lambung ke mukosa (Sherwood, 2011).
1
2
3
Gambar 4.16 Hasil mikroskopik lambung setelah pemberian HCl perbesaran 40 (atas) dan 100 (bawah)
Keterangan: 1. Lapisan mukosa
2. Lapisan muskularis mukosa 3. Lapisan submukosa
4. Lapisan tunika muskularis
Gambar 4.17 Hasil mikroskopik lambung kelompok tanpa pengobatan hari ke-2 perbesaran 40 (atas) dan 100 (bawah)
Gambar 4.18 Hasil mikroskopik lambung kelompok dengan pengobatan hari ke-2 perbesaran 40 (kiri) dan 100 (kanan)
Gambar 4.19 Hasil mikroskopik lambung kelompok tanpa pengobatan hari ke-4 perbesaran 40 (atas) dan 100 (bawah)
Gambar 4.20 Hasil mikroskopik lambung kelompok dengan pengobatan hari ke-4 perbesaran 40 (atas) dan 100 (bawah)
Pengamatan mikroskopik hari ke-6 menujukkan bahwa kelompok tanpa pengobatan masih terdapat erosi dan kelompok dengan pemberian
1
1
1
2
2
2
3 3
3
4 4
1
1 1
2
2 2
3
3
3 4
4
obatmenunjukkan sel-sel epitel yang mendekati kondisi normal. Pengamatan mikroskopik hari ke -6 ditunjukkan pada Gambar 4.21 dan 4.22.
Pengamatan mikroskopik hari ke-8, menunjukkan kelompok tanpa pengobatan masih terdapat erosi sedangkan kelompok dengan pengobatan menunjukkan sel-sel epitel yang normal. Pengamatan mikroskopik hari ke-8 ditunjukkan pada Gambar 4.23 dan 4.24.
Hasil mikroskopik menunjukkan bahwa kelompok pengobatan mencapai tingkat kesembuhan pada hari ke-8 dibandingkan kelompok tanpa pengobatan.
Gambar 4.21 Hasil mikroskopik lambung kelompok tanpa pengobatan hari ke-6 perbesaran 40 (atas) dan 100 (bawah)
Penyembuhan tukak lambung membutuhkan penyusunan kembali struktur epitel dan jaringan penghubung yang menopang, termasuk lapisan pembuluh dan otot. Beberapa faktor pertumbuhan telah dilibatkan dalam proses ini, karena kemampuannnya dalam mengatur fungsi penting sel, seperti proliferasi sel, migrasi, diferensiasi, sekresi, dan degradasi matriks ekstraseluler, dimana semuanya penting selama penyembuhan jaringan (Milani dan Calabro, 2001).
1 1
1
2
2 2
3
3
3 4
4
Gambar 4.22 Hasil mikroskopik lambung kelompok dengan pengobatan hari ke-6 perbesaran 40 (atas) dan 100 (bawah)
Gambar 4.23 Hasil mikroskopik lambung kelompok tanpa pengobatan hari ke-8 perbesaran 40 (atas) dan 100 (bawah)
4
4 4
3
3 3
2 2
2 1
1
1
1
1 1
2 2
2
3
3 3
4
4
Gambar 4.24 Hasil mikroskopik lambung kelompok dengan pengobatan hari ke-8 perbesaran 40 (atas) dan 100 (bawah)
Penyembuhan luka merupakan proses yang melibatkan peptida faktor pertumbuhan dimana TGF-beta adalah salah satu yang paling penting. Nitric oxide juga merupakan faktor penting penyembuhan dan produksinya diatur oleh
inducible nitric oxide synthase (iNOS).Kurkumin secara signifikan mempercepat
penyembuhan luka oleh karena peningkatan ekspresi TGF-beta1 dan TGF-beta tIIrc dan peningkatan level iNOS (Mani, et al., 2002).
Gambar 4.25 Jalur infeksi pembentukan tukak lambung oleh H. pylori (Li, et al., 2015).
4
4 4
1
2
2 2
1 1
3
BAB V
KESIMPULAN DAN SARAN
5.1 Kesimpulan
Berdasarkan hasil penelitian yang telah dilakukan dapat disimpulkan bahwa:
1. Ada pengaruh viskositas alginatdan kadar ekstrak terhadap pelepasan kurkumin daribeads alginat, tetapi tidak ada pengaruh ukuran syringe terhadap pelepasan kurkumin.
2. Sediaan beads alginat yang mengandung ekstrak kunyit bersifat gastroretentif dengan nilai persen bioadhesi 87% pada menit ke-5 dan 82% pada menit ke-10.
3. Sediaan beads alginat dari ekstrak kunyit efektif menyembuhkan lesi lambung pada dosis 100mg/kgBB tikus pada hari ke-8.
5.2 Saran