BAB 2
TINJAUAN PUSTAKA
2.1 Karakteristik Kimia
Kadmium adalah unsur yang banyak tersebar secara alami dalam bentuk mineral dan digunakan secara komersial dalam bentuk bijih kadmium, yang dinamakan greenockite, yang biasanya ditemukan bersama bijih zink. Produksi komersial bijih kadmium bergantung pada tambang zink. Secara komersial kadmium tersedia dalam bentuk oksida, klorida atau sulfida. Logam kadmium (Cd2+) dimurnikan dari bentuk bijih menjadi logam berat yang berwarna putih keperakan dengan sedikit kebiruan cemerlang dan berbentuk padat pada suhu ruangan (ATSDR, 2008).
Kadmium merupakan unsur logam yang terletak dalam grup IIB pada tabel periodik dengan berat atom 112,40. Kadmium adalah unsur yang diklasifikasikan sebagai logam transisi, yang memiliki tekanan uap 1 mmHg pada suhu 394ºC dan tidak berwarna. Umumnya kadmium terdapat dalam jumlah yang sangat kecil yang terikat dengan logam lain, khususnya zink. Kadmium mencair pada suhu 320,9⁰C dan mendidih pada suhu 767⁰C. Kadmium dapat membentuk sejumlah garam seperti kadmium sulfat dan kadmium sufida (Hays et al. 2008).
dapat melarut dalam larutan asam nitrit, amonium nitrat dan asam sulfur panas. Dalam udara lembab, kadmium teroksidasi secara lambat. Bila dipanaskan kadmium akan berubah menjadi gas buangan dalam bentuk kadmium oksida. Kadmium dan senyawa kadmium tidak mudah terbakar namun dapat terurai bila dibakar dan melepaskan gas buangan yang bersifat korosif dan toksik. Logam kadmium panas bereaksi dengan halogen, pospor, selenium, sulfur, dan tellurium, dan uap kadmium bereaksi dengan oksigen, karbon dioksida, uap air, sulfur dioksida, dan hidrogen klorida (ATSDR 1999).
Secara komersial kadmium tersedia dengan kemurnian 99% sampai 99,999% dalam bentuk bubuk, alumunium foil, batang atau lempeng logam, dan kristal. Beberapa garam kadmium bersifat larut dalam air seperti kadmium klorida, kadmium sulfat dan kadmium nitrat. Garam-garam lain yang sulit larut dalam air dapat menjadi mudah larut air bila diinteraksikan dengan asam, cahaya atau oksigen (IARC 1993, Llewellyn 1994).
dalam atenol, aseton, air, dietil eter dan etil asetat dan juga tidak berwarna. Kadmium nitrat tersedia dengan kemurnian 99% atau lebih tinggi (IARC, 1993; HSDB, 2006)
Senyawa kadmium penting lainnya adalah kadmium oksida dan kadmium sulfida. Kadmium oksida berbentuk kristal coklat gelap atau bubuk amorf yang tidak berwarna, terlarut dalam larutan asam dan garam amonium. Kadmium oksida tidak larut dalam air dan larutan basa. Tingkat kemurnian kadmium oksida mencapai 99% sampai 99,999%. Di lain pihak, kadmium sulfida berbentuk kristal hexagonal berwarna kuning jingga atau kristal semitransparan dimorfik atau berbentuk bubuk kuning kecoklatan, namun dapat pula berwarna putih sampai jingga kemerahan. Kadmium sulfida terlarut dalam larutan asam mineral pekat, sedikit larut dalam amonium hidroksida dan tidak larut dalam air dan larutan basa. Kadmium sulfida tersedia dengan tingkat kemurnian 98% sampai 99,999%. Namun demikian, sebagian besar produk kadmium sulfida adalah campuran kompleks yang mengandung senyawa logam lainnya (HSDB, 2006).
2.2 Sumber Kadmium
dengan kandungan tertinggi di daerah pantai dan di dalam fosfat dan fosforit lautan. Sementara di sedimen dan air laut adalah sekitar 0.1 ppm (Morrow, 2001).
Kadmium terbentuk secara alami dari proses yang lambat dari erosi dan abrasi bebatuan dan tanah (Nikic et al., 2009). Emisi alami kadmium ke lingkungan dapat berasal dari letusan gunung berapi, kebakaran hutan, pembentukan aerosol garam laut dan fenomena alami lainnya (Shevchenko et al. 2003). Konsentrasi kadmium di atmosfer adalah sekitar 1-5 ng/m3 (ATSDR, 2008).
Konsentrasi kadmium yang cukup tinggi dapat terjadi akibat adanya aktifitas manusia. Sumber dari aktifitas manusia tersebut antara lain adalah adanya penggunaan pupuk fosfat, pembakaran bahan bakar fosil, produksi besi, baja, dan logam non besi, produksi semen dan pembakaran sampah. Sumber antropogenik berkontribusi terhadap pajanan pada manusia dalam jumlah yang cukup besar akibat produksi, pemakaian, dan pembuangan serta pembakaran produk-produk yang mengandung kadmium (Bull, 2010).
plastik dan sebagai absorben neutron pada fasilitas reaktor nuklir (Sahmoun et al. 2005).
Kadmium ditemukan pada tahun 1817, namun baru digunakan secara komersial pada akhir abad ke-19. Penggunaan kadmium yang pertama sekali adalah dalam bentuk sulfida pada pigmen cat. Pada awal tahun 1990an, digunakan dalam jumlah yang sedikit untuk amalgam gigi. Selama Perang Dunia I, kadmium digunakan sebagai bahan pengganti kaleng. Sejak Perang Dunia II, hampir seluruh kadmium dimanfaatkan untuk pembuatan baterai, pigmen, elektroplating, pelapis dan stabilisator plastik. Namun demikian, seluruh penggunaan kadmium dalam industri menunjukkan penurunan yang signifikan pada akhir abad ke-20 kecuali pada industri baterai (ATSDR, 1999).
Kadmium klorida digunakan untuk elektroplating, fotokopi, printer warna, pengering, cermin/kaca, kimia analitik, tabung vakum, cairan pelumas, dan sebagai bahan kimia perantara dalam produksi stabilisator dan pigmen yang mengandung kadmium (IARC 1993, HSDB 2006). Akan tetapi, penggunaannya menunjukkan penurunan. Kadmium klorida juga dipakai sebagai fungisida di lapangan golf dan halaman rumput di perumahan. Namun, pada akhir tahun 1980an pemanfaatannya telah dilarang oleh Dewan Perlindungan Lingkungan di negara Amerika Serikat (US EPA = Environmental Protection Agency) (ATSDR, 1999).
digunakan dalam baterai alkalin. Sedangkan, kadmium sulfida digunakan secara primer untuk pigmen dalam industri cat, gelas, plastik, tekstil, kertas, dan petasan. Kadmium juga dipakai untuk sel-sel solar, monitor fluoresen, alat deteksi radiasi, pendeteksi asap, laser elektron, transistor film tipis dan dioda, fosfor dan foto (ATSDR, 1999).
2.3 Kontaminasi Kadmium ke Lingkungan
Senyawa kadmium yang seukuran dengan partikel yang dapat terhisap ke saluran nafas, dapat terbawa ke daerah yang sangat jauh apabila dilepaskan dari sumbernya ke atmosfer. Kadmium kemudian akan turun ke tanah akibat hujan atau jatuh dari udara. Saat berada di tanah, kadmium dapat dengan mudah bergerak melalui lapisan-lapisan tanah dan masuk ke rantai makanan karena terserap oleh tumbuh-tumbuhan seperti sayuran, kacang-kacangan, dan biji-bijian (ATSDR, 2008).
Konsentrasi kadmium dalam sumber air minum biasanya kurang dari 1 μg/L atau 1 part per billion (ppb). Air tanah jarang mengandung kadmium dalam
2.4 Kadmium dalam Rantai Makanan
Tumbuh-tumbuhan tertentu seperti tembakau, padi, biji-bijian, kentang, dan sayuran lainnya menyerap kadmium dari tanah lebih banyak dibandingkan penyerapan logam berat lain seperti timbal dan merkuri (Satarug et al. 2003). Kadmium juga ditemukan dalam daging, khususnya hati dan ginjal. Di daerah-daerah tertentu, konsentrasi kadmium meningkat dalam kerang dan jamur (Jarup, 2002).
Kadmium masuk ke rantai makanan melalui air. Di Jepang, tambang zink mengkontaminasi sumber air lokal dengan kadmium. Petani lokal menggunakan air tersebut untuk irigasi sawah. Tanah menjadi terkontaminasi oleh kadmium yang mengakibatkan penyerapan kadmium ke tanaman padi (Jarup, 2002).
2.5 Jalur Pajanan Kadmium
Perokok pada umumnya terpapar kadmium melalui inhalasi. Dalam sebatang rokok terdapat 2 μg kadmium, dimana hampir sebanyak 2-10% nya
berubah menjadi asap rokok (Mannino et al. 2004). Perokok umumnya memiliki kandungan kadmium dalam darah dan kandungan dalam tubuh dua kali lebih tinggi dibandingkan dengan orang yang tidak merokok (Waalkes et al. 2003). Selain itu, perokok juga akan memiliki kandungan kadmium yang tinggi dalam urin (Mannino et al. 2004).
Asupan oral adalah jalur utama pajanan kadmium bagi populasi yang bukan perokok. Tetapi, kandungan kadmium dalam makanan, air, dan udara ambien bukan merupakan masalah kesehatan yang nyata bagi populasi di Amerika Utara. Asupan kadmium per harinya adalah sebesar 30-50 μg (Satarug, 2003; NTP, 2004) namun individu normal hanya menyerap sebagian kecil yaitu sekitar 1-10% dari dosis oral (Horiguchi et al. 2004).
Pajanan kadmium melalui kulit sangat sedikit sehingga dapat diabaikan. Pajanan ini tidak dianggap sebagai jalur utama pajanan (ATSDR, 2008).
2.6 Nilai Standar untuk Pajanan Kadmium
Nilai standar pajanan untuk melindungi masyarakat umum dari pajanan kadmium telah ditetapkan oleh beberapa institusi kesehatan. FDA dan ATSDR (1999) menetapkan bahwa kandungan maksimum kadmium dalam air minum dan air botol adalah 0,005 mg/l, sedangkan untuk kandungan kadmium yang masih dapat dikonsumsi secara kronik melalui oral tanpa adanya risiko gangguan kesehatan adalah 0,0002 mg/kg berat badan/hari.
WHO menentukan bahwa asupan kadmium yang masih dapat ditoleransi secara mingguan adalah 7μg/kg/berat badan/minggu. OSHA menetapkan pajanan kadmium yang aman di lingkungan kerja adalah 5 μg/m3
(sebagai gas buangan). The National Institute of Occupational Safety and Health (NIOSH) juga telah
menentukan kandungan yang dapat membahayakan kehidupan dan kesehatan adalah 9 mg/m3 (NIOSH, 2006; NTP, 2004).
Minum dan menetapkan kadar maksimum kadmium dalam air minum adalah 0,003 mg/l.
2.7 Kinetika Kadmium dalam Tubuh
Absorbsi kadmium tergantung dari beberapa faktor, di antaranya : usia, jenis kelamin, kebiasaan merokok, dan status gizi. Kadmium merupakan salah satu toksin yang dapat terakumulasi, akan mengakibatkan kandungannya dalam tubuh akan bertambah sesuai dengan usia. Kandungan kadmium dalam darah perempuan lebih tinggi dibandingkan laki-laki. Perempuan dengan kadar besi yang rendah, diyakini berisiko terhadap absorbsi kadmium yang cukup besar setelah terpapar secara oral (Olsson et al. 2002).
Sebanyak 10% sampai 50% dari kadmium yang terhirup akan diabsorbsi, tergantung pada ukuran partikel, kelarutan senyawa kadmium yang terinhalasi, dan lama pajanan (Jarup, 2002). Absorbsi sangat sedikit pada partikel kadmium yang berukuran besar (lebih dari 10 μm) dan tidak larut air, sebaliknya bila ukuran partikel kurang dari 0.1 μm dan mudah larut air, absorbsi akan lebih besar.
Absorbsi kadmium dari asap rokok sangat tinggi karena partikel kadmium yang terdapat dalam asap rokok berukuran sangat kecil (ATSDR, 1999).
kromium dan zink pada konsentrasi yang tinggi dalam makanan dapat menurunkan uptake kadmium.
Absorpsi kadmium melalui kulit bukan merupakan jalur pajanan yang signifikan, hanya sekitar 0,5% kadmium yang diabsorpsi melewati kulit (ATSDR 2008).
Kadmium dalam tubuh dibuang melalui urin. Kecepatan ekskresi kadmium rendah, disebabkan kadmium masih terikat erat dengan metallothionein yang direabsorpsi hampir seluruhnya dalam tubulus ginjal. Akumulasi kadmium dalam tubuh dapat bermakna, karena ekskresinya yang rendah. Konsentrasi kadmium dalam darah merefleksikan pajanan yang baru terjadi, sedangkan kadmium urin lebih menunjukkan kandungan total kadmium dalam tubuh. Namun demikian, saat terjadi kerusakan ginjal akibat pajanan kadmium, kecepatan ekskresi akan meningkat secara tajam, dan konsentrasi kadmium tidak lagi merefleksikan kandungan kadmium dalam tubuh (ATSDR, 2008).
Kandungan kadmium dalam tubuh saat lahir tidak terdeteksi (CDC, 2005). Konsentrasi kadmium secara bertahap akan meningkat sejalan dengan pertambahan usia dari 9,5 mg sampai 50 mg (ATSDR, 1999). Ginjal dan hati dapat mengandung 50% kadmium yang terakukmulasi dalam tubuh (HSDB, 2006).
adalah 7 (tujuh) sampai 16 tahun. Waktu paruh yang panjang menunjukkan bahwa manusia tidak mempunyai jalur ekskresi yang efektif untuk membuang kadmium. Kadmium dikenal tidak memiliki fungsi biologis pada manusia. Akumulasi kadmium yang berlebihan dalam tubuh dianggap berpotensi toksik.
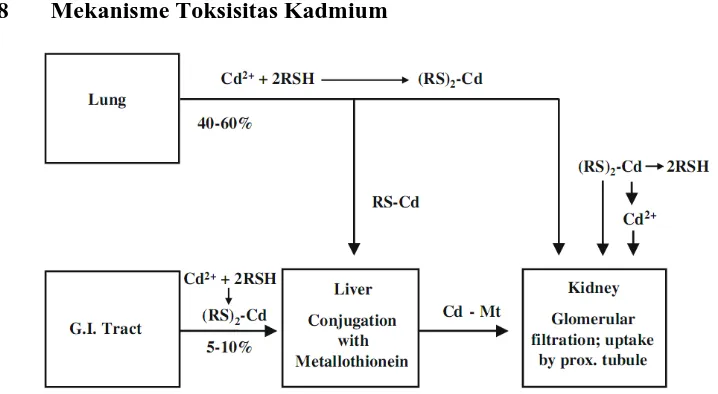
2.8 Mekanisme Toksisitas Kadmium
Gambar 2.1 Skema Absorbsi dan Distribusi Kadmium dalam Tubuh (Sumber Prozialeck et al, 2010)
secara sistemik dan berlanjut dengan terjadinya kerusakan organ (Prozialec et al, 2010).
Kadmium yang diabsorbsi ke dalam pembuluh darah, baik yang berasal dari paru-paru atau saluran cerna, akan terkonsentrasi di dalam sel darah (terutama eritrosit, tapi juga leukosit), hanya sekitar 10% yang tertinggal di plasma darah. Oleh sebab itu, pemantauan sampel darah untuk tingkat pajanan kadmium akan mengikutsertakan analisis darah lengkap. Selain itu, penting juga untuk diketahui bahwa pada dasarnya seluruh kadmium yang berada di plasma darah terikat pada protein dan molekul lain (Barbier et al., 2005; Bridges et al., 2005). Kadmium di plasma dapat juga terikat pada protein spesifik yang mengikat logam yaitu metallothionein atau dapat beredar bebas dan bergabung dengan molekul-molekul seperti albumin, asam amino, senyawa sulfhidril, glutation atau sistein. Daya afinitas kadmium terhadap metallothionein yang sangat kuat menyebabkan kadmium tidak dapat diambil oleh kebanyakan jaringan, namun kompleks kadmium-metallothionein dapat diambil oleh epitel tubulus proksimal (Klaassen et al., 2009).
akibat kerusakan kadmium maka komplek kadmium-metallothionein akan terlepas ke dalam pembulah darah (Klaassen et al., 2009). Meskipun komplek kadmium-metallothionein tidak menyebabkan efek toksik bagi sebagian besar organ, komplek ini akan difiltrasi di glomerulus dan diambil kembali oleh sel epitel tubulus proksimal, efekya adalah kadmium-metallothionein memiliki efek paradox yang mempermudah mengantarkan kadmium dari hati ke ginjal (Bridges dan Zalups, 2005).
Organ utama yang dirusak oleh kadmium akibat pajanan kronis adalah ginjal dan tulang. Paru-paru merupakan organ target pada pajanan akut dosis tinggi melalui saluran pernafasan. Kadmium dikenal dapat meningkatkan stres oksidatif melalui keberadaan katalis dalam pembentukan spesis oksigen reaktif, meningkatkan peroksidasi lemak, dan menurunkan glutathione dan grup sulfhydryl yang terikat protein. Kadmium juga dapat menstimulasi produksi sitokin inflamasi dan menurunkan fugsi protektif dari pembentukan nitrit oksida (Navas-Acien et al. 2004).
Kadmium mengekspresikan aktifitas genotoksik in vitro dalam sel dan in vivo pada hewan. Bukti epidemiologi untuk genotoksisitas pada manusia secara in vivo masih sangat terbatas. Penelitian okupasional menunjukkan peningkatan
jumlah penyimpangan kromosom dalam limfosit pada pekerja yang terpajan kadmium (NTP, 2004). Kadmium telah ditemukan menyebabkan kerusakan kromosom dalam studi eksperimen pada hewan yang diberikan secara subkutan (ATSDR, 1999). Kadmium mengakibatkan mutasi, putusnya rantai DNA, kerusakan kromosom, transformasi sel dan gangguan perbaikan DNA dalam kultur sel DNA (NTP, 2004). Kadmium diketahui dapat mengubah ekspresi gen dan sinyal transduksi (Waisberg et al. 2003).
2.9 Dampak Kadmium tehadap Ginjal
Ginjal adalah target organ utama akibat pajanan kronik kadmium. Kerusakan ginjal dapat terjadi akibat inhalasi atau ingesti. Dari hasil penelitian pada manusia menunjukkan bahwa pajanan kadmium selama lebih kurang sekitar 10 tahun dapat mengakibatkan kerusakan ginjal, tergantung intensitas pajanan. Pajanan kadmium yang kronik dihubungkan dengan disfungsi tubulus ginjal yang progresif. Tanda awal abnormalitas ginjal adalah ditemukannya proteinuria tubulus pada konsentrasi 2 - 4 μg/g kreatinin yaitu B2MG dan ά1-mikroglobulin yang merupakan biomarker kerusakan ginjal akibat pajanan kadmium. Enzimes N-acetyl-B-glucosaminidase (NAG) akan meningkat dalam urin dan tanda-tanda kerusakan glomerulus ginjal seperti peningkatan albumin dalam urin dan penurunan laju filtrasi glomerulus juga terlihat. Pada tingkat akhir kerusakan ginjal adalah adanya glycosuria, sisa kalsium dan fosfat dan gangguan metabolisme kalsium dengan efek sekunder pada tulang yaitu osteoporosis dan osteomalasia (Roels et al. 1999; Jarup et al. 2000).
Beberapa ahli percaya bahwa mikroproteinuria berkaitan dengan pajanan kadmium tidak selalu progresif meskipun setelah penghentian pajanan terjadi pada kandungan kadmium urin > 4 μg/g kreatinin atau pada kondisi konsentrasi B2MG
Nefropati kadmium adalah penentu kematian yang penting pada pekerja kadmium. Efek toksik di ginjal berkaitan dengan dosis kadmium (Mueller et al. 1992). Bagi para pekerja, risiko nefropati klinis meningkat secara signifikan dengan total pajanan udara lebih besar dari 300 mg/m3, konsentrasi kadmium urin lebih dari 10 µg/g creatinine, dan konsentrasi kortek ginjal di atas 200 ppm (Roels et al. 1999).
Tanda-tanda dini kerusakan ginjal yang telah dilaporkan dari populasi umum adalah konsentrasi kadmium urin antara 2-4 nmol/mmol kreatinin. Sejumlah penelitian telah melihat efek kadmium pada ginjal akibat pajanan lingkungan yaitu Cadmibel (Buchet et al. 1990), Jepang (Ikeda et al. 2003, 2005; Kobayashi et al. 2006), OSCAR (Jarup et al. 2000), Swedia, dan US (Noonan et al. 2002).
Penelitian-penelitian ini telah membuktikan bahwa meskipun terpajan kadmium dalam konsentrasi yang sangat rendah kadmium masih mengakibatkan efek yang merusak ginjal. WHO telah menetapkan bahwa konsentrasi kadmium 200 μg/g berat basah ginjal menyebabkan efek yang merusak ginjal pada 10%
populasi (Satoh et al. 2002).
peningkatan ά-1 mikroglobulin (Jarup et al. 2000). Noonan et al. (2002)
melaporkan bahwa belum diketahui jika perubahan subklinis dini pada biomarker ginjal berhubungan dengan pajanan kadmium pada konsentrasi yang rendah memiliki hubungan dengan penurunan fungsi ginjal. Pajanan konsentrasi yang biasa diterima di lingkungan kerja dapat meningkatkan ekskresi protein berat molekul tinggi seperti albumin dan transferin yang merupakan tanda dini dari kerusakan glomerulus akibat pajanan kadmium.
Bila telah terjadi kerusakan pada glomerulus maka akan irreversible dan tingkat kerusakan akan tergantung pada dosis (Jarup, 2002). Laju Filtrasi Glomerulus (LFG) menurun dengan lambat berlangsung progresif, membuktikan bahwa kadmium mempercepat penurunan fungsi ginjal. Uremia jarang terjadi, namun kapasitas cadangan filtrasi menurun dapat ditunjukkan pada pekerja-pekerja yang terpajan kadmium dengan LFG dan kreatinin serum yang normal. Pajanan kadmium juga mempermudah perkembangan glomerulopati pada populasi diabetik (Buchet et al. 1990). Pajanan kadmium yang mencukupi dapat juga mengarah pada penurunan LFG dan gagal ginjal kronik yang ditandai oleh : aminoasiduria, glukosuria, hiperkalsiuria, hiperfosfaturia, dan poliuria (Jarup 2002).
hiperfosfaturia. Faktor lain yang juga ikut berkontribusi adalah asam urat urin, penurunan sitrat urin dan asidosis tubulus renal.
2.10 Biomarker Akibat Pajanan Kadmium
2.10.1 Kadmium Urin
Pada pajanan rendah dan sedang, kadmium urin merefleksikan pajanan yang terpadu dari berbagai jalur pajanan dan kandungan kadmium dalam tubuh secara total. Kandungan kadmium dalam urin tidak meningkat secara signifikan setelah pajanan akut dan tidak berguna untuk pemeriksaan akibat pajanan akut. Di lingkungan kerja, kandungan kadmium urin memberikan sedikit atau bahkan tidak adanya informasi yang bermanfaat selama pajanan pada tahun pertama. Menurut data dari NHANES, orang-orang muda yang sehat yang bukan perokok dan tidak terpapar kadmium di tempat kerja memiliki kandungan kadmium yang sangat rendah (kandungan rata-rata 0,08 μg/g kreatinin) (Jarup 2002).
Umumnya, pada orang-orang yang bukan perokok konsentrasi kadmium urin berada pada kisaran 0,02 – 0,7 µg/g kreatinin dan konsentrasinya akan perlahan meningkat sesuai dengan pertambahan usia dan sebanding dengan akumulasi konsentrasinya di ginjal. Perokok pada umumnya memiliki kandungan kadmium urin lebih tinggi dibandingkan bukan perokok (Mannino et al. 2004).
Selama terpajan dalam jangka waktu yang lama di tempat kerja konsentrasi kadmium urin meningkat perlahan dan sebanding dengan jumlah akumulasinya di dalam tubuh. Berdasarkan laporan nasional ke-3 mengenai pajanan bahan-bahan kimia dari lingkungan menunjukkan bahwa konsentrasi kadmium urin pada usia ≥ 20 tahun adalah 0,210 μg/g kreatinin selama tahun 2001-2002 (CDC, 2005).
Bila seluruh tempat pengikatan kadmium di ginjal telah jenuh setelah terpajan secara kronik pada konsentrasi yang tinggi, disfungsi ginjal dan konsentrasi kadmium urin meningkat secara dramatis. Pada kondisi ini, konsentrasi urin lebih merefleksikan pajanan yang baru terjadi bukan kandungan total kadmium dalam tubuh. Disfungsi renal dianggap belum terjadi bila konsentrasi kadmium urin kurang dari 10 µg/g kreatinin (Roels et al. 1999).
2.10.2 Kadmium Darah
kadmium di tempat kerja konsentrasi kadmium cukup tinggi yaitu sekitar 1 – 4 µg/l (Jarup et al. 1998).
Pada populasi umum, kadmium darah juga sangat dipengaruhi oleh kandungan kadmium dalam tubuh. Dalam satu studi yang bertujuan untuk melihat pengaruh konsentrasi kadmium darah dari berbagai sumber diet menunjukkan bahwa tidak ditemukan hubungan yang signifikan antara konsentrasi kadmium darah dan diet. Namun, konsentrasi kadmium urin (menggambarkan kandungan kadmium dalam tubuh) dan ferritin serum (ukuran cadangan besi dalam tubuh) merupakan faktor yang menetukan konsentrasi kadmium darah (Berglund et al. 1994).
Pengaruh akumulasi kadmium pada konsentrasi kadmium darah menyebabkan peningkatan kadmium darah sesuai dengan peningkatan usia (Berglund et al. 1994). Orang yang berusia lanjut memiliki kandungan kadmium darah lebih tinggi dibandingkan pada dewasa muda. Pada sebuah penelitian mengenai konsentrasi kadmium darah pada orang dewasa dan orang tua, peningkatan kadar kadmium darah sesuai dengan usia diamati terjadi pada lelaki yang bukan perokok, namun tidak terjadi pada wanita yang tidak merokok, hal ini dimungkinkan terjadi akibat absorbsi intestinal yang lebih tinggi karena kandungan besi yang tidak adekuat pada saat sebelum dan sesudah menopause (Baecklund et al. 1996).
(0,3 µg/l). Perbedaan ini mungkin berhubungan dengan diet kadmium pada wanita dengan kondisi besi yang rendah sebelum menopause.
Pada wanita hamil juga menunjukkan kecendrungan kadar kadmium darah yang lebih tinggi dibanding wanita yang tidak hamil. Alasan yang menyebabkan peningkatan kadmium darah selama hamil adalah terjadinya peningkatan absorbsi kadmium karena penurunan cadangan besi dalam tubuh yang biasanya terjadi pada trimester ketiga kehamilan (Chan et al. 1993). Pada wanita yang tidak hamil penurunan cadangan besi dalam tubuh berkaitan dengan meningkatnya konsentrasi kadmium darah (Berglund et al. 1994).
Kandungan kadmium darah untuk populasi sehat yang tidak terpajan kadmium di US dengan batas kepercayaan 95% adalah 0,4 μg/L. Populasi yang terpajan kadmium di tempat kerja memiliki kandungan kadmium darah yang lebih tinggi dibandingkan populasi umum (CDC, 2005).
2.10.3 Kadmium di Ginjal
Kadmium terakumulasi terutama di hati dan ginjal dan konsentrasi tertinggi ditemukan pada korteks ginjal. Konsentrasi kadmium di ginjal akan meningkat sampai usia 50 – 60 tahun dan setelah itu akan menurun. Namun demikian, terdapat variasi yang sangat besar di antara masyarakat di tempat dan group yang sama (Elinder et al. 1988).
sinar-X atau analisis aktivasi neutron. Metode in vivo memberikan sejumlah keuntungan dibandingkan dengan analisis sampel dari otopsi yaitu pemilihan popolasi studi dan kemungkinan untuk melakukan follow up orang berdasarkan waktu. Pilihan untuk melakukan otopsi biasanya pada korban-korban yang mengalami kematian mendadak atau kematian akibat kecelakaan. Pemeriksaan otopsi ini tidak mewakili populasi umum (Jarup et al., 1998).
2.10.4 Metallothionein Urin
Metallothionein adalah protein lainnya dengan berat molekul rendah yang disintesis akibat respon dari pajanan kadmium dan logam lain. Kandungan metallothionein urin berkorelasi kuat dengan kandungan kadmium urin dan dapat merefleksikan kandungan kadmium total dalam tubuh. Tapi, konsentrasi dalam urin akan meningkat secara signifikan bila gangguan ginjal telah terjadi (Bernard, 1997).
berbeda jauh dengan konsentrasi kadmium anorganik bila tanpa metallothionein yaitu 130-200 µg/g. Pengamatan ini sesuai dengan dugaan bahwa kadmium yang terikat ke metallothionein lebih diutamakan disaring melalui glomerulus lalu diabsorbsi dan disimpan di tubulus atau masuk ke tubulus ginjal langsung dari kapiler peritubular. Zink-metallothionein, senyawa yang berbeda dengan kadmium-metallothionein, merupakan agen nontoksik ketika diberikan dalam dosis yang sebanding menunjukkan efek proteksi terhadap terjadinya kerusakan ginjal (Dorian dan Klaassen, 1995).
Sato dan Kondoh (2002) mempublikasikan hasil review terhadap peran metallothionein pada toksisitas kadmium. Sintesis metallothionein diinduksi oleh berbagai macam stimulus seperti kadmium, merkuri, zink, stress oksidatif, glukokortikoid, dan agen anti kanker. Dari sebuah studi yang menggunakan tikus-tikus yang telah dihilangkan metallothionein-nya menunjukkan bahwa metallothionein mempunyai kemampuan untuk memberikan perlindungan terhadap kerusakan ginjal, hati dan tulang akibat diinduksi oleh kadmium ( Liu et al. 2000)
ginjal, sejalan dengan peningkatan 150 kali konsentrasi metallothionein ginjal, yang mencapai 800 µg metallothionein per gram ginjal. Pada kelompok tikus yang telah dihilangkan kandungan metallothionein-nya, konsentrasi kadmium ginjal jauh lebih rendah dan metallothionein ginjal tidak ditemukan. Tikus-tikus yang tidak memiliki metallothionein lebih mudah terkena kerusakan ginjal dibandingkan kelompok kontrol, yang dibuktikan oleh terjadinya peningkatan ekskresi protein urin, glukosa urin, gamma glutamyl transferase, dan NAG urin serta peningkatan kadar nitrogen urea darah. Ginjal pada tikus-tikus yang diberikan kadmium melebar dan secara histopatologi menunjukkan bentuk-bentuk lesi yang bervariasi termasuk degenerasi tubulus proksimal, apoptosis, atrofi, inflamasi intersisiel, dan pembengkakan glomerulus. Kelainan ini tampak lebih berat pada tikus-tikus yang tidak memiliki metallothionein dibanding kelompok tikus kontrol. (Liu et al. 2000). Oleh sebab itu, kerusakan ginjal yang diinduksi oleh kadmium tidak sepenuhnya diperantarai melalui kompleks kadmium-metallothionein, meskipun metallothionein tampak sebagai protein intraseluler yang penting dalam perlindungan terhadap terjadinya kerusakan ginjal (Gonick, 2008).
2.10.5 Kadmium di Rambut
yang baik untuk indikator pajanan kadmium di tempat kerja, karena besarnya peluang kontaminasi dari lingkungan. Kadmium yang terakumulasi di rambut menggambarkan konsentrasi logam ini dalam darah selama fase pertumbuhan rambut. (Lauwerys et al. 1994).
2.10.6 β
2-mikroglobulin (B2MG) Urin
Salah satu tanda kerusakan tubulus ginjal adalah peningkatan ekskresi protein dengan berat molekul rendah yaitu B2MG urin. B2MG diisolasi pada tahun 1968 oleh beggard dan Bearn dari urin penderita penyakit Wilson dan keracunan kadmium kronik, kedua kondisi tersebut ditandai secara primer dengan kerusakan tubulus proksimal ginjal. B2MG adalah protein berat molekul rendah dengan berat 11.800 daltonn yang terdiri dari 100 asam amino dengan satu jembatan disulfida. Sekitar 95% B2MG difiltrasi melalui glomerulus dan direabsorbsi hampir seluruhnya dan dikatabolisassi oleh sel-sel di tubulus proksimal ginjal. Ginjal yang sehat mampu mengabsorbsi sekitar 99,9% B2MG yang difiltrasi, artinya maksmial 370 µg/24 jam akan diekskresikan ke dalam urin. Adanya kerusakan tubulus proksimal dengan laju filtrasi glomerulus yang normal akan berkaitan dengan penurunan reabsorbsi tubulus dan meningkatkan ekskresi B2MG urin (Schardijn dan Eps, 1987).
Pada orang yang sehat dan tidak terpajan kadmium, konsentrasi B2MG adalah sekitar 200 µg/g kreatinin. Ekskresi akan meningkat sesuai dengan pertambahan usia dan pajanan kadmium. Pada pekerja-pekerja yang terpajan kadmium, konsentrasi urin dapat lebih besar dari 300 µg/g kreatinine yang mengindikasikan kemungkinan terjadinya penyakit ginjal awal, dan pekerja-pekerja yang demikian seharusnya mendapat pemeriksaan lanjutan (ATSDR, 2010).
Tabel berikut menampilkan nilai konsentrasi B2MG yang berkaitan dengan kondisi ginjal (ATSDR, 1997).
Tabel 2.1 Kadar B2MG Urin Yang Berhubungan dengan Fungsi Ginjal
Konsentrasi Beta 2 Mikroglobulin Kondisi
< 300 µg/g kreatinin Nilai normal
300 – 1.000 µg/g kreatinin Ancaman kerusakan tubulus (kemungkinan masih reversibel bila dihentikan pajanan dari kadmium). Tidak ada perubahan pada laju fitrasi glomerulus (LFG)
1.000 – 10.000 µg/g kreatinin Proteinuria tubulus yang irreversible yang dapat berlanjut pada penurunan LFG. LFG dapat normal atau sedikit mengalami perubahan
> 10.000 µg/g kreatinin Nefropati kadmium yang biasanya diikuti oleh penurunan LFG
2.10.7 Retinol Binding Protein (RBP) Urin
sebab itu, RBP hanya digunakan sebagai pemeriksaan konfirmasi dalam kasus tersangka pajanan kadmium (ATSDR, 2010).
2.11 Albuminuria
Albuminuria adalah ekskresi albumin urin dengan konsentrasi antara 30 sampai 300 mg/hari jika diukur dengan pengumpulan urin selama 24 jam, atau antara 30 sampai 300 mg/g jika diukur dengan menggunakan rasio kreatinin albumin urin dengan pengumpulan urin sewaktu. Makroalbuminuria atau
proteinuria klinik menunjukkan bahwa setiap ekskresi albumin atau protein telah melebihi konsentrasi ini. Skrining albuminuria direkomendasikan untuk pasien-pasien yang mengalami hipertensi, diabetes, dan penyakit ginjal kronik dini, namun karena skrining mudah dan berbiaya murah maka juga direkomendasikan untuk populasi umum (Bakris, 2007; Duka, 2008).
Pengukuran albuminuria dapat dilakukan dengan beberapa cara, yaitu dengan mengukur konsentrasi albumin atau rasio kreatinin albumin dalam spesimen urin sewaktu acak. Selain itu juga dapat dilakukan dengan mengukur konsentrasi albumin dan secara simultan mengukur bersihan kreatinin dalam pengumpulan urin selama 24 jam. Cara yang lain adalah dengan melakukan
2004). Pada 80% penderita diabetes tipe 1 dan sekitar 20-40% penderita diabetes tipe 2 dengan albuminuria (<300 mg/dl) akan berlanjut menjadi makroalbuminuria bila tanpa pengobatan. Kondisi hipertensi akan berkembang menjadi proteinuria dan insufisiensi ginjal (ADA, 2008).
2.12 Kadmium dan Albuminuria
Albuminuria merupakan biomarker yang jarang digunakan untuk menganalisis terjadinya kerusakan ginjal pada populasi yang terpajan kadmium. Terjadinya albuminuria pada populasi yang terpajan kadmium, bervariasi (Gonick, 2008). Pada suatu studi yang dilakukan di Australia (Haswell et al. 2008) ditemukan hubungan yang signifikan antara pajanan kadmium dengan konsentrasi yang rendah dari lingkungan dengan albumin dalam urin. Namun, sebaliknya tidak diperoleh hubungan yang bermakna pada studi di 2 wilayah di China (Chen, 2006) dan Amerika (Noonan, 2002). Acien et al. (2009) menemukan hubungan yang signifikan antara konsentrasi kadmium dalam darah dengan terjadinya albuminuria pada poluasi umum di US.
2.13 Faktor-Faktor yang Meningkatkan Risiko Terjadinya Gangguan Fungsi Tubuh Akibat Pajanan Kadmium
2.13.1 Usia
antara tahun 1998 – 2008 menemukan bahwa kadar kadmium darah pada responden pada kelompok usia di atas 20 tahun berada pada konsentrasi tertinggi yaitu pada kisaran 1.5 sampai 1.8 µg/l. Sebaliknya pada kelompok usia kurang dari 20 tahun, kisaran kadmium dalam darah hanya 0.3 – 1.1 µg/l (CDC, 2009). Sementara itu, Adnan et al. (2012) membuktikan bahwa terdapat korelasi yang positif antara usia dengan kandungan kadmium dalam urin. Konsentrasi kadmium dalam darah dan urin yang meningkat sesuai dengan pertambahan usia disebabkan karena kadmiium memiliki waktu parah yang lama dalam tubuh (10-30 tahun). 2.13.2 Jenis Kelamin
2.13.3 Kandungan dan Durasi Pajanan
Kandungan kadmium dalam tubuh meningkat menurut usia karena eliminasi yang sedikit dari tubuh (hanya 0.001% kadmium yang diekskresikan per hari) dan terus berlanjut selama 38 tahun. Pajanan dalam jumlah yang besar dapat terjadi melalui pekerjaan (ATSDR, 2010).
2.13.4 Pekerjaan
Pada tahun 1990an sekitar 297.000 pekerja di Amerika Serikat diperkirakan berisiko tinggi terhadap pajanan kadmium. Tipe-tipe pekerja yang berpotensi terpapar adalah: pekerja di industri logam campur, solder alumunium, amunisi, baterai, pelapisan kadmium, kawat dan kabel troli, keramik dan tembikar, pelapisan elektronik, tambang, tekstil, pestisida, cat, gelas, farmasi, plastik. Selain itu untuk profesi sebagai seniman pahat dan pembuat amalgam gigi juga berisiko untuk terpajan kadmium (NIOSH, 1990).
2.13.5 Jumlah Asupan Air
berat molekul rendah dilaporkan terjadi pada penduduk di sekitar area pemukiman di Jepang yang sangat terkontaminasi dengan kadmium pada konsentrasi yang sangat tinggi (WHO, 2004).
2.13.6 Tinggi Badan, Berat Badan dan Status Gizi
Selama tahun 2001 sampai 2006, dilakukan pemeriksaan biomonitoring pada penduduk di Flanders, Belgia, untuk mengkaji dampak kesehatan akibat pajanan lingkungan. Dalam studi ini, peneliti menganalisis ada tidaknya pengaruh polutan tertentu terhadap tinggi dan indeks massa tubuh pada remaja dan dewasa. Sampel darah dan urin diambil dari 1679 remaja, 775 lelaki dewasa dan 808 perempuan dewasa ikut ambil bagian dalam skirining untuk pajanan polutan. Peneliti juga mencatat tinggi dan berat badan responden, termasuk kuesioner mengenai status kesehatan, gaya hidup, dan pola makan. Dari hasil penelitian ini menunjukkan bahwa konsentrasi kadmium yang tinggi dalam urin berhubungan dengan indeks massa tubuh yang rendah. Konsentrasi kadmium urin secara negatif mempengaruhi hormone seks pada remaja, oleh sebab itu sangat dimungkinkan bahwa tinggi badan pada remaja laki-laki dapat dipengaruhi oleh perubahan kadar hormone seks. Selain itu, kadmium diketahui juga berpengaruh pada hormon pertumbuhan (Dhooge, 2010).
2.13.7 Kebiasaan Merokok
Sebatang rokok mengandung sekitar 2.0 μg kadmium, 2-10% dari
paru-paru menuju sirkulasi sistemik (Satarug 2003; Jarup 2002). Kadmium yang terkandung dalam darah perokok dua kali lebih banyak bila dibanding dengan orang-orang yang bukan perokok (Waalkes 2003). Perokok juga akan memiliki kandungan kadmium yang lebih tinggi di dalam urin dibanding mereka yang tidak perokok (Mannino et al. 2004).
2.13.8 Pajanan Lingkungan
Kandungan kadmium dalam makanan, air, dan udara ambien secara alami yang belum terkontaminasi oleh aktifitas industri dan bahan buangan produk industri tidak begitu tinggi dan tidak menyebabkan gangguan kesehatan. Asupan diet umumnya sekitar 30 μg/hari (Satarug et al. 2003) dan pada individu yang
normal mengabsorbsi hanya dalam jumlah yang kecil dari jalur oral (1-10%) (Horiguchi et al. 2004).
2.13.9 Pajanan dari Makanan
Di pinggiran sungai Jinzu di Jepang, kontaminasi kadmium ke lingkungan dari aktifitas manusia menyebabkan uptake (penyerapan) logam ini ke tanaman padi. Konsumsi padi yang mengandung kadmium dalam jumlah berlebihan memicu terjadinya penyakit “itai-itai” pada perempuan lansia pasca menopause di daerah itu. Asupan padi terhitung 40% dari pajanan kadmium oleh orang-orang yang terkena. Wanita paruh baya menelan sekitar 37.5 μg kadmium per hari
2.13.10 Hipertensi
Hipertensi adalah salah satu faktor yang ditemukan berhubungan dengan tingginya kandungan kadmium dalam urin (Eum et al, 2008). Satarug et al. (2005) juga menemukan hubungan yang signifikan antara hipertensi dan kandungan kadmium dalam urin.
2.14 Analisis Risiko Kesehatan Lingkungan (ARKL)
2.14.1 Konsep dan Definisi
2.14.2 Model ARKL
Louvar (1998) dan Kolluru (1996) menggambarkan analisis risiko kesehatan terdiri dari empat langkah yaitu Identifikasi Bahaya, Analisis Pemajanan, Analisis Dosis Respon, dan Karakteristik Risiko.
Identifikasi Bahaya
Identifikasi bahaya adalah tahap awal ARKL untuk mengenali sumber risiko. Informasinya bisa ditelusuri dari sumber dan penggunaan risk agent memakai pendekatan orientasi terhadap agen, bisa juga dilakukan dengan mengamati gejala dan penyakit yang berhubungan dengan toksisitas agen risiko di masyarakat yang telah terkumpul dalam studi-studi sebelumnya, baik di wilayah kajian atau di tempat-tempat lain. Pendekatan seperti ini dikenal sebagai pendekatan orientasi penyakit (Rahman, 2005).
masalah. Jadi, keberadaan agen risiko dapat disimpulkan dari gangguan kesehatan yang teramati, tingkat pencemaran datau keduanya (Rahman, 2005).
Analisis Pemajanan
Analisis pemajanan disebut juga dengan penilaian kontak bertujuan untuk mengenali jalur-jalur pajanan agen risiko agar jumlah asupan yang diterima individu dalam populasi yang berisiko bisa dihitung. Pemajanan adalah proses yang menyebabkan organisme kontak dengan bahaya. Pemajanan dapat terjadi karena agen risiko terhirup dalam udara, tertelan bersama air atau makanan, terserap melalui kulit atau kontak langsung dalam kasus radiasi (Kolluru, 1996). Analisis Dosis Respon
Analisis dosis respon menetapkan nilai-nilai kuantitatif toksisitas agen risiko untuk setiap bentuk spesi kimianya. Toksisitas dinyatakan sebagai dosis referensi untuk efek-efek nonkarsinogenik dan Cancer Slope Factor (CSF) untuk efek-efek karsinogenik. Analisis dosis respon merupakan tahapan yang paling menentukan untuk agen risiko yang sudah memiliki dosis respon (Kolluru, 1996).
Reference Dose (RfD) adalah toksisitas kuantitatif nonkarsinogenik,
Hubungan dosis respon yang berbeda dapat diamati pada bahan yang sama, karena efek toksikang dipengaruhi oleh jumlah asupan bahan kimia atau dosis yang diabsorbsi, frekuensi pajanan dan waktu. Pada analisis risiko kesehatan manusia risiko yang dikaji hanya terpusat pada manusia. Oleh karena itu ketidakpastian dalam analisis risiko manusia hanya terbatas pada variasi jalur pajanan dan perbedaan sensitifitas setiap individu, sehingga konsep risiko mengandung pengertian probabilitas yang disebut dengan RfD. RfD bukan dosis yang dapat diterima melainkan hanya untuk acuan saja, jika dosis yang diterima manusia melebihi RfD maka probabilitas mendapatkan risiko juga bertambah (Rahman, 2005).
Karakterisasi Risiko
Karakterisasi risiko adalah penghubungan antara analisis risiko dengan manajemen risiko. Rasio asupan pada manusia dengan nilai RfD dikenal dengan bilangan risiko (Risk Quotient), disingkat RQ. Dalam ARKL, RQ menyatakan kemungkinan risiko yang potensial terjadi. Semakin besar nilai RQ di atas 1, semakin besar kemungkinan risiko itu terjadi. Dan sebaliknya jika nilai RQ kurang dari 1, maka semakin kecil kemungkinan risiko kesehatan itu terjadi (Kolluru, 1996).
Manajemen Risiko
zat toksik. Hasil dari karakterisasi risiko kemudian digunakan untuk memutuskan upaya-upaya pengendalian dengan memperhatikan faktor-faktor lain seperti ketersediaan teknologi, perangkat hukum dan perundangan, sosial, ekonomi, dan informasi politik.
Formula untuk manajemen risiko adalah membuat berbagai macam scenario sedemikian rupa sehingga asupan suatu agen risiko sama dengan nilai RfD-nya. Caranya adalah dengan mengurangi masa pajanan atau waktu kontak atau dengan menurunkan konsentrasinya (Rahman, 2005).
2.15 Teori Simpul
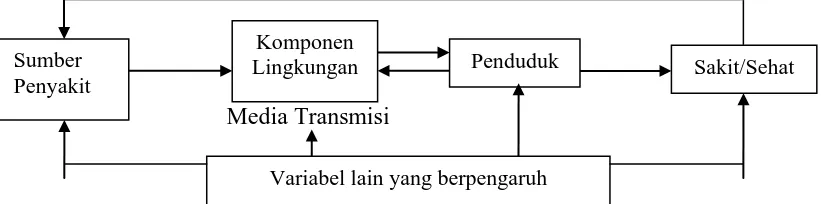
Ahmadi (2005) menjelaskan proses terjadinya penyakit dalam prespektif lingkungan dalam suatu teori yang disebut sebagai teori Simpul pada gambar 2.2 sebagai berikut:
Media Transmisi
Gambar 2.2 Diagram Skematik Patogenesis Penyakit (diadaptasi dari Ahmadi, 2005)
Berdasarkan skematik patogenesis penyakit (gambar 2.2) maka proses/patogenesis penyakit diuraikan dalam empat simpul, yakni simpul 1, yang disebut sebagai sumber penyakit; simpul 2, komponen lingkungan yang
Sakit/Sehat Penduduk
Komponen Lingkungan Sumber
Penyakit
merupakan media transmisi penyakit; simpul 3, penduduk dengan berbagai variabel kependudukan seperti pendidikan, perilaku, kepadatan, jender, sedangkan simpul 4, penduduk yang dalam keadaan sehat atau sakit setelah mengalami interaksi atau pajanan dengan komponen lingkungan yang mengandung bibit atau agen penyakit.
Titik simpul akan menjadi tuntunan dalam manajemen pencegahan penyakit tertentu. Dengan mengendalikan sumber penyakit maka proses kejadian di simpul 3 dan 4 dapat dicegah. Gambaran skematik yang tertera pada gambar 2.2 dapat memberikan petunjuk yakni titik - titik simpul tempat mendapatkan informasi. Informasi kesehatan yang diperoleh dengan kegiatan surveilans secara paripurna dapat diperoleh dari titik simpul 1, 2, 3 atau 4. Dengan demikian manajemen penyakit berdasarkan informasi yang terpercaya atau bukti dapat digambarkan dengan teori Simpul (Ahmadi, 2005).
Simpul 1: Sumber Penyakit
Sumber penyakit adalah titik yang secara konstan mengeluarkan agen penyakit. Agen penyakit adalah komponen lingkungan yang dapat menimbulkan gangguan penyakit melalui kontak secara langsung atau melalui media perantara. Umumnya, melalui produk beracun yang dihasilkannya ketika berada dalam tubuh, atau secara langsung dapat mencederai sebagian atau keseluruhan bagian tubuh manusia sehingga menimbulkan gangguan fungsi maupun morfologi tubuh.
kekuatan radiasi, energy, kebisingan, kekuatan cahaya; kelompok bahan kimia toksik, seperti pestisida, logam berat, gas polutan udara dan lain-lain (Ahmadi, 2005).
Simpul 2: Media Transmisi Penyakit
Komponen lingkungan yang dapat memindahkan agen penyakit yang dikenal sebagai media transmisi penyakit diantaranya adalah: udara, air, tanah/pangan, binatang/serangga dan manusia. Media transimisi tidak akan memiliki potensi penyakit bila di dalamnya tidak terdapat agen penyakit.
Air dapat memiliki potensi menimbulkan penyakit bila terdapat bakteri Salmonella typhi, bakteri Vibrio cholerae atau air tersebut mengandung bahan beracun seperti pestisida, logam berat dan lainnya. Demikian pula, udara dikatakan berbahaya bila mengandung polutan toksik atau jamur.
Penyakit tidak menular juga dapat dipindahkan melalui perantaraan media tertentu seperti udara, air atau pangan. Agen penyakit tidak menular seperti bahan kimia toksik juga berasal dari sebuah sumber, misalnya knalpot mobil, cerobong asap industri, titik buangan limbah, atau secara alamiah disemburkan oleh kawah gunung berapi.
Simpul 3: Perilaku Pemajanan
padi di sawah, mengonsumsi sejumlah air minum yang mengandung kadmium, atau ukuran man bite hour untuk mengukur gigitan nyamuk, dan sebagainya. Jadi jumlah kontak pada setiap orang berbeda satu sama lain. Ada yang mengonsumsi air yang tercemar logam berat dalam jumlah besar, ada juga dalam jumlah kecil. Semua ditentukan oleh perilaku masing-masing orang yang dipengaruhi pendidikan, pengetahuan dan lain-lain (Ahmadi, 2005).
Simpul 3 dapat diukur dengan melakukan pemeriksaan biomarker atau tanda biologi. Misalnya, pengukuran kandungan merkuri dalam darah atau dalam urin, kandungan plasmodium malaria dalam darah, atau kandungan Pb dalam darah. Selain itu juga dapat diukur kandungan agen penyakit yang bersangkutan atau metabolitnya. Secara tidak langsung juga bisa diukur derajat perlawanan antibody seseorang terhadap agen penyakit yang bersangkutan.
Simpul 4: Penyakit
Penyakit merupakan outcome hubngan interaktif antara penduduk dengan lingkungan yang memiliki potensi bahaya gangguan kesehatan. Seseorang dikatakan sakit bila terdapat kelainan bentuk, fungsi akibat hasil interaksi dengan lingkungan, baik lingkungan fisik maupun sosial.
2.16 Landasan Teori
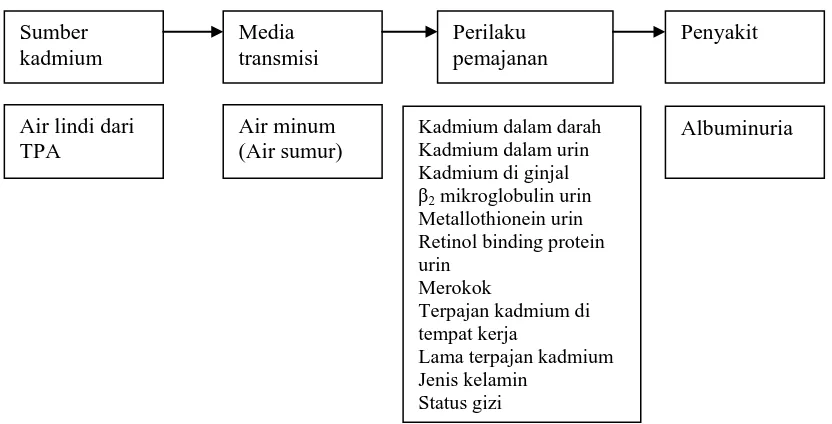
Berdasarkan tinjauan kepustakaan yang telah diuraikan mengenai karakteristik kadmium yang meliputi sifat fisikokimiawi, sumber dan penggunaan kadmium, kinetika kadmium dalam tubuh, efek kadmium bagi tubuh, maka disusun suatu landasan teori yang mengadopsi teori Simpul yang dikemukakan oleh Ahmadi (2005) yang dapat digambarkan sebagai berikut:
Gambar 2.3 Kerangka Teori
Kadmium yang ditemukan dalam air sumur milik masyarakat dapat berasal dari leachate (air lindi) yang mengandung kadmium dari hasil penguraian limbah padat seperti plastik, alat-alat elektronik, logam-logam, baterai atau dari sisa pupuk di tempat penampungan akhir sampah, yang mengalir dalam air tanah dan akhirnya mengkontaminasi air sumur. Air lindi yang berasal dari tempat
Sumber
β2 mikroglobulin urin
penampungan akhir sampah adalah sumber pencemaran kadmium yang merupakan simpul satu dalam teori simpul.
Air sumur milik masyarakat yang dijadikan sebagai sumber air minum berdasarkan studi yang dilakukan oleh Nainggolan (2010), Ashar dan Santi (2011) membuktikan bahwa air sumur memiliki kandungan kadmium yang telah melebihi baku mutu air bersih. Keberadaan kadmium yang merupakan agen kimia yang bersifat toksik menjadikan air sumur sebagai simpul dua atau media transmisi penyakit.
Jumlah kadmium yang masuk ke dalam tubuh masyarakat yang mengkonsumsi air minum yang berasal dari air sumur yang mengandung kadmium dapat berjumlah banyak atau sedikit tergantung dari perilaku pemajanan seperti lama terpajan (mengkonsumsi air), frekuensi pajanan, banyaknya asupan, jenis kelamin, usia, status gizi dan berat badan populasi. Tambahan kandungan kadmium dalam tubuh dapat terjadi akibat kebiasan merokok dan bekerja di lingkungan industri yang menggunakan kadmium dalam proses produksi. Biomarker keberadaan kadmium dalam tubuh dapat diketahui melalui pemeriksaan kadmium dalam darah, urin, ginjal, kadar B2MGurin, metallothionein urin dan retinol binding protein urin. Faktor-faktor yang berhubungan dengan tinggi rendahnya agen toksik (kadmium) dalam tubuh masyarakat adalah simpul tiga dalam teori simpul.
ginjal yang ditandai dengan terjadinya proteinuria yaitu B2MG urin dan albuminuria. Penyebab lain timbulnya albuminuria selain akibat pajanan kadmium melalui oral yang paling sering adalah hipertensi dan penyakit diabetes mellitus (Bakris, 2007; Duka, 2008).
2.17 Kerangka Konsep Penelitian
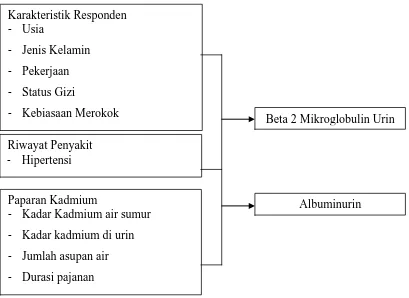
Berdasarkan tinjauan pustaka, kerangka teori, dan tujuan penelitian maka disusun kerangka konsep penelitian sebagai berikut:
Gambar 2.4 Kerangka Konsep Penelitian Riwayat Penyakit
- Hipertensi
Karakteristik Responden - Usia
- Jenis Kelamin - Pekerjaan - Status Gizi
- Kebiasaan Merokok
Paparan Kadmium
- Kadar Kadmium air sumur - Kadar kadmium di urin - Jumlah asupan air - Durasi pajanan
Beta 2 Mikroglobulin Urin