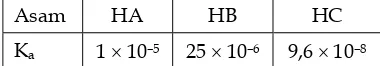Da la m U N be rla k u Pe t unjuk U m um se pe rt i ini :
M a t a Pe la ja ra n : K im ia
SM A / M A I PA
La t iha n Soa l U jia n N a siona l 2 0 1 0
Se k ola h M e ne nga h At a s / M a dra sa h Aliya h I PA
1. Isikan identitas Anda ke dalam Lembar Jawaban Ujian Nasional (LJUN) yang
tersedia dengan menggunakan pensil 2B sesuai petunjuk di LJUN.
2. Hitamkan bulatan di depan nama mata ujian pada LJUN.
3. Tersedia waktu 120 menit untuk mengerjakan paket tes tersebut.
4. Jumlah soal sebanyak 40 butir, pada setiap soal terdapat 5 (lima) pilihan
jawaban.
5. Periksa dan bacalah soal-soal sebelum Anda menjawabnya.
6. Laporkan kepada pengawas ujian apabila terdapat lembar soal yang kurang
jelas, rusak, atau tidak lengkap.
7. Tidak diizinkan menggunakan kalkulator, HP, tabel matematika atau alat
bantu hitung lainnya.
8. Periksalah pekerjaan Anda sebelum diserahkan kepada pengawas ujian.
9. Lembar soal boleh dicoret-coret untuk mengerjakan perhitungan.
Petunjuk A: dipergunakan dalam menjawab soal nomor 1 sampai ke nomor 40.
1. Diketahui unsur–unsur perioda ketiga sebagai berikut:
Na, Mg, Al, Si, P, S, Cl, dan Ar
Unsur-unsur yang terdapat pada titik puncak utama dan titik terendah dalam hal energi ionisasi berturut-turut adalah ....
(A) Ne dan Ar (B) Li dan Na (C) Li dan Ne (D) Na dan Ar (E) Ne dan Na
2. Diketahui konfigurasi elektron unsur-unsur sebagai berikut:
P : 1s2 2s2
Q : 1s2 2s2 2p6 3s1
R : 1s2 2s2 2p6 3s2 3p4
S : 1s2 2s2 2p6 3s2 3p5
T : 1s2 2s2 2p6 3s2 3p6 3d3 4s2
U : 1s2 2s2 2p6 3s2 3p6 3d10 4s1
Pasangan unsur yang dapat membentuk senyawa ion adalah ....
(A) P dengan Q (B) P dengan R (C) Q dengan S (D) T dengan U (E) R dengan S
3. Pada pembakaran sempurna 5 liter gas propana (C3H8) menurut reaksi berikut (belum
setara):
C3H8(g) + O2(g)→ CO2(g) + H2O(l)
diperlukan udara (mengandung 20% volume oksigen) yang diukur pada P dan T yang sama sebanyak ....
(A) 1 liter (B) 5 liter (C) 25 liter (D) 50 liter (E) 125 liter
4. Suatu reaksi kimia berlangsung dengan persamaan reaksi sebagai berikut:
aCu(s) + bHNO3(l)→cCu(NO3)2(aq) + dNO2(g) + eH2O(l)
Koefisien untuk a, b, c, d, dan e adalah .... (A) 1, 4, 1, 2, dan 2
(B) 1, 4, 2, 2, dan 2 (C) 1, 4, 1, 1, dan 2 (D) 1, 4, 2, 2, dan 1 (E) 2, 4, 1, 2, dan 2
5. x gram logam aluminium (Ar = 27) direaksikan dengan larutan asam klorida encer berlebih
dengan persamaan reaksi sebagai berikut (belum setara):
Al(s) + HCl(aq)→ AlCl3(aq) + H2(g)
Jika volume gas hidrogen yang dihasilkan 6,72 liter (STP), maka nilai x adalah .... (A) 1,35 gram
(B) 2,7 gram (C) 5,4 gram (D) 8,1 gram (E) 10,8 gram
6. Di antara larutan di bawah ini yang mempunyai jumlah partikel paling banyak adalah ....
(A) NaCl 0,5 M
(B) CO(NH2)2 0,4 M
(C) CuSO4 0,4 M
(D) CaCl2 0,3 M
(E) C6H12O6 0,6 M
7. Tabel harga Ka dari beberapa senyawa asam adalah sebagai berikut:
Asam HA HB HC
Ka 1 × 10–5 25 × 10–6 9,6 × 10–8
Berdasarkan tabel di atas dapat ditarik kesimpulan bahwa urutan kekuatan asam adalah ....
(A) HA > HB > HC (B) HC > HA > HB (C) HB > HC > HA (D) HC > HB > HA (E) HB > HA > HC
8. Dalam suatu percobaan, 100 mL larutan NH3 0,3 M (Kb = 2,0 × 10–5) dicampurkan dengan
100 mL larutan HCl 0,1 M. pH larutan yang terjadi adalah ....
(A) 5 – 2 log 2 (B) 5 – log 2 (C) 5 (D) 9
(E) 9 + 2 log 2
9. Diketahui data:
Ka CH3COOH = 10–5
Kb NH3(aq) = 10–5
Kw = 10–14
Larutan di bawah ini yang mempunyai pH = 5 adalah ....
(A) 5 mL CH3COONa 0,1 M
(B) 10 mL NH4Cl 0,1 M
(C) 10 mL NH3 0,2 M + 10 mL NH4Cl 0,1 M
(D) 10 mL NH3 0,1 M + 10 mL NH4Cl 0,1M
(E) 10 mL CH3COOH 0,2 M + 10 mL CH3COONa 0,1 M
10. Berikut ini data percobaan:
Percobaan 200 mL HCl endapan AgCl
1 0,1 M 1 gram
2 0,2 M 1 gram
3 0,3 M 1 gram
4 0,4 M 1 gram
5 0,5 M 1 gram
Bila Ksp AgCl =1,0 × 10–10, maka kelarutan AgCl paling besar terdapat pada percobaan
nomor ....
12. Sol Fe(OH)3 dapat dibuat di laboratoriumdengan cara memasukkan larutan FeCl3 jenuh ke
dalam air yang mendidih. Reaksi yang terjadi pada pembuatan sol Fe(OH)3 di atas adalah
....
13. Pada pembakaran sempurna suatu senyawa hidrokarbon diperoleh gas CO2 dan uap H2O
dengan jumlah mol yang sama. Senyawa hidrokarbon yang dimaksud adalah ....
(A) C6H14
(B) C5H12
(C) C4H8
(D) C3H8
(E) C2H2
14. Untuk menaikkan bilangan oktan pada bahan bakar bensin, salah satu faktornya adalah dengan menambahkan senyawa MTBE untuk mengurangi terjadinya knocking. MTBE adalah singkatan dari ....
(A) metil tersier butil ester (B) metil tersier butil eter (C) metil tri butil eter (D) metoksi tri butil ester (E) metoksi tri butil etana
15. Diketahui beberapa senyawa:
1. CH3 – CH2 – CH2 – CH2 – COOH
2. CH3 – CH2 – CH2 – CH2 – CH2 – OH
3. CH3 – CH2 – CH2 – CH(OH) – CH3
4. CH3 – CH2 – CO – CH2 – CH3
5. CH3 – O – CH2 – CH2 – CH2 – CH3
Pasangan senyawa yang memiliki isomer fungsi adalah ....
(A) 1 dan 4 (B) 2 dan 3 (C) 4 dan 5 (D) 2 dan 5 (E) 1 dan 3
16. Perhatikan reaksi senyawa karbon berikut:
1. CH3OH + CH3OH → CH3 – O – CH3 + H2O
2. CH2 = CH2 + HCl → CH3 – CH2Cl
3. C2H5OH → CH2 = CH2 + H2O
Jenis reaksi di atas berturut-turut adalah ....
(A) substitusi, eliminasi, dan adisi (B) adisi, substitusi, dan eliminasi (C) eliminasi, adisi, dan substitusi (D) adisi, eliminasi, dan substitusi (E) substitusi, adisi, dan eliminasi
17. Perhatikan rumus struktur senyawa karbon berikut:
Nama yang tepat untuk senyawa karbon tersebut adalah .... C
O
O CH3
CH3 CH2
(A) metil propanoat (B) metil pentanoat (C) etil propanoat (D) etil etanoat (E) metil butanoat
18. Dalam sebuah percobaan, jika larutan NaOH dicampurkan dengan larutan HCl akan terjadi kenaikan suhu dalam campuran. Hal ini berarti bahwa ....
(A) entalpi pereaksi dan hasil reaksi tidak berbeda (B) entalpi pereaksi dan hasil reaksi bertambah (C) entalpi pereaksi dan hasil reaksi berkurang (D) entalpi pereaksi lebih besar dari hasil reaksi (E) entalpi pereaksi lebih kecil dari hasil reaksi
19. Perhatikan diagram tingkat energi dari reaksi karbon dengan oksigen membentuk CO2:
C + ½O2
0 kJ
WWW.SM A8 .COM
CO + ½O2– 110,5 kJ
CO2
– 393,5 kJ
Perubahan entalpi untuk reaksi:
CO (g) + ½O2(g)→ CO2(g)
adalah ....
(A) – 566 kJ (B) – 504 kJ (C) – 283 kJ (D) + 283 kJ (E) + 504 kJ
20. Perhatikan data energi ikatan rata-rata berikut ini:
C ≡ C : 833 kJ C – C : 343 kJ C – H : 415 kJ Cl – Cl : 238 kJ C – Cl : 335 kJ
Perubahan entalpi reaksi yang dihasilkan dari reaksi antara gas asetilena dengan gas klor menurut reaksi:
C2H2 + 2Cl2→ C2H2Cl4
adalah ....
(A) – 748 kJ (B) – 374 kJ (C) + 374 kJ (D) + 1683 kJ (E) + 2992 kJ
21. Di bawah ini adalah data hasil ekperimen laju reaksi untuk reaksi:
2A(g) + B(g)→ 2AB(g)
1 0,1 M 0,1 M 6
2 0,1 M 0,2 M 12
3 0,1 M 0,3 M 18
4 0,2 M 0,1 M 24
5 0,3 M 0,1 M 54
Dari data tersebut dapat disimpulkan bahwa persamaan laju reaksi adalah ....
(A) V = k [A]2
(B) V = k [B] (C) V = k [A] [B] (D) V = k [A]2 [B]
(E) V = k [A] [B]2
22. Setiap kenaikan suhu 20°C suatu reaksi kimia berlangsung 3 kali lebih cepat. Jika pada suhu 25°C reaksi berlangsung selama 6 menit, maka pada suhu 65°C reaksi berlangsung selama ....
hingga mencapai kesetimbangan dengan persamaan reaksi:
2HI(g)⇔ H2(g) + I2(g)
Jika derajat disosiasi (α) HI = 40%, maka harga tetapan kesetimbangan Kc pada suhu yang
sama adalah ....
24. Pada industri amonia yang dikenal dengan proses Haber-Bosch, amonia dibuat berdasarkan reaksi:
N2(g) + 3H2(g)⇔ 2NH3(g) ΔH = – 92 kJ
Untuk mendapatkan gas NH3 sebanyak mungkin maka langkah-langkah yang harus
dilakukan adalah ....
(A) menambah katalis (B) suhu dinaikkan
(C) tekanan diturunkan (D) [N2] dan [H2]ditambah
(E) volume diperbesar
25. Bila larutan natrium tiosulfat (Na2S2O3) direaksikan dengan larutan asam klorida (HCl)
akan terjadi reaksi:
2Na2S2O3 + 4HCl → 4NaCl + 2S + 2SO2 + 2H2O
Bilangan oksidasi belerang berubah dari ....
(A) +8 menjadi 0 dan +4 (B) +6 menjadi 0 dan +8 (C) +6 menjadi 0 dan +4 (D) +4 menjadi 0 dan +8 (E) +2 menjadi 0 dan +4
26. Diketahui data potensial reduksi standar sebagai berikut:
Ag++ e → Ag E° = + 0,80 volt
Cu+2 + 2e → Cu E° = + 0,34 volt
Fe+2 + 2e → Fe E° = – 0,44 volt
Cr+3 + 3e → Cr E° = – 0,74 volt
Zn+2 + 2e → Zn Eo = – 0,76 volt
Mg+2 + 2e → Mg Eo = – 2,37 volt
Al+3 + 3e → Al Eo = – 1,66 volt
Reaksi yang dapat berlangsung terjadi pada sel ....
(A)
Ag Cu
(B)
(C)
Fe Cr
Zn Mg
(D)
Al Ag
(E)
WWW.SM A8 .COM
27. Elektrolisis larutan dengan menggunakan elektrode inert di bawah ini yang dapat menghasilkan gas pada katode dan anodenya pada suhu kamar adalah ....
Cu Fe
(A) ZnSO4
(B) AgNO3
(C) CuSO4
(D) KBr (E) NaCl
28. Proteksi katodik dilakukan untuk mencegah perkaratan pada logam besi, terutama yang digunakan untuk pipa-pipa air dalam tanah dan bahan bangunan.
Diketahui data potensial reduksi standar sebagai berikut:
Fe+2 + 2e → Fe Eo = – 0,44 volt
Cu+2 + 2e → Cu Eo = +0,34 volt
Cr+3 + 3e → Cr Eo = – 0,74 volt
Zn+2 + 2e → Zn Eo = – 0,76 volt
Mg+2 + 2e → Mg Eo = – 2,37 volt
Al+3 + 3e → Al Eo = – 1,66 volt
Berdasarkan data di atas, logam yang tidak dapat digunakan untuk mencegah terjadinya perkaratan pada besi adalah ....
(A) tembaga (B) krom (C) seng (D) magnesium (E) aluminium
29. Perhatikan reaksi nyala beberapa senyawa logam berikut ini:
Warna nyala untuk senyawa yang mengandung unsur kalium dan natrium berturut-turut adalah ....
(A) jingga dan ungu (B) ungu dan kuning (C) kuning dan merah (D) merah dan hijau (E) kuning dan ungu
30. Pengolahan logam aluminium secara industri yang dikenal dengan nama proses Hall, dilakukan dengan cara elektrolisis lelehan Al2O3 dalam kriolit cair dan menggunakan
elektrode grafit (karbon). Reaksi yang terjadi pada katode adalah ....
(A) 2H2O + 2e → 2OH– + H2
(B) 2H2O → 4H+ + O2 + 4e
(C) Al → Al+3 + 3e
(D) Al+3 + 3e → Al
(E) Al2O3 + H2O → Al(OH)3
31. Proses pengolahan besi dari bijihnya dilakukan dalam tanur tinggi, sebagai bijih besi yaitu hematit (Fe2O3). Bahan yang ditambahkan pada proses tersebut adalah kapur (CaCO3), pasir
(SiO2) dan kokas (C). Bahan bakar yang digunakan dan sekaligus juga bertindak sebagai
reduktor adalah ....
(A) kokas (B) batu kapur (C) hematit
(D) gas karbobmonoksida (E) gas karbondioksida
32. Ion kompleks yang mempunyai bilangan koordinasi empat adalah ....
(A) [Ag(NH3)2]+
(B) [Fe(CN)6]3–
(C) [Au(H2O)2(S2O3)4]5–
(D) [Cu(H2O)2(NH3)2]2+
(E) [Cr(NH3)4Cl2]+
33. Diketahui sifat fisika unsur halogen sebagai berikut:
Unsur Titik didih Titik leleh
F2 –188 °C – 233 °C
Cl2 – 34,6 °C – 103 °C
Br2 58 °C – 7,2 °C
I2 184 °C 113,5 °C
Di antara unsur-unsur di atas yang pada suhu kamar berwujud cair adalah ....
(A) F2
(B) F2 dan Cl2
(C) Br2
(D) I2
(E) Br2 dan I2
34. Sebanyak 50 gram batuan belerang direaksikan dengan oksigen menghasilkan 32 gram gas belerang dioksida. Reaksi yang terjadi:
S (s) + O2(g)→ SO2(g)
Jika Ar S = 32 dan O = 16, maka kemurnian belerang dalam batuan adalah ....
(A) 16% (B) 25% (C) 32% (D) 50% (E) 90%
35. Pernyataan berikut yang sesuai dengan gas nitrogen (nomor atom N = 7) adalah ....
(A) di udara terdapat sebanyak 21% volume (B) gas tersebut bersifat sangat elektropositif
(C) mempunyai ikatan rangkap tiga yang sangat kuat (D) mudah bereaksi dengan unsur logam dan non-logam (E) mempunyai sifat berwarna dan berbau tajam
36. Dari turunan benzena di bawah ini yang bersifat asam dan sebagai antiseptik (pembunuh kuman) adalah ....
(A) CHO
(B) NH2
(C) OH
(D) NO2
(E) CH3
37. Dalam kehidupan sehari-hari banyak digunakan bahan kimia seperti:
1. kaporit, Ca(OCl)2
2. iodoform, CHI3
3. halotan, CF3−CHClBr
4. kapur klor, CaOCl2
Berdasarkan data di atas, pasangan senyawa yang tergolong haloalkana adalah ....
(A) 1 dan 2 (B) 2 dan 3 (C) 3 dan 4 (D) 1 dan 4 (E) 2 dan 4
38. Disakarida yang dihidrolisis menghasilkan glukosa dan fruktosa adalah ....
(A) sukrosa (B) maltosa (C) laktosa (D) amilum (E) selulosa
39. Adanya ikatan antar asam amino dalam protein dapat diidentifikasi dengan menggunakan pereaksi Biuret menghasilkan warna ungu. Struktur ikatan tersebut adalah ....
(A)
40. Persamaan lemak dan minyak adalah ....
(A) sama-sama padat (B) sama-sama cair (C) bersifat asam (D) bersifat amfoter (E) ester trigliserida