TOPIK 1
PENGENALAN LABORATORIUM DAN ALAT – ALAT
KULTUR JARINGAN TANAMAN
PENDAHULUAN
Latar Belakang
Kultur jaringan adalah salah satu metode yang digunakan dalam pengembangan Bioteknologi Tumbuhan. Metode ini merupakan prosedur pemeliharaan dan pertumbuhan jaringan tanaman (sel, kalus, protoplas) serta organ (batang, akar, embrio) pada kultur aseptis (in vitro). Metode kultur jaringan diantaranya digunakan untuk perbanyakan tanaman, modifikasi genotip (plant breeding), produksi metabolit sekunder, pemeliharaan plasma nutfah, penyelamatan embrio (embryo rescue) (Hartmann dkk 1997). Menurut Pierik (1977), ada beberapa kelebihan metode kultur jaringan dibandingkan metode yang lain yaitu 1). Metode perbanyakan lebih cepat dibandingkan metode yang lain; 2). Metode ini digunakan untuk perbanyakan tanaman yang sulit diperbanyak dengan metode konvensional; 3). Tanaman hasil kultur jaringan mempunyai jaringan yang lebih kuat dibandingkan metode yang lain ;4). Dapat digunakan untuk memperoleh tanaman yang bebas penyakit dan tidak terbatas oleh musim dalam pelaksanaanya.
Laboratorium Kultur Jaringan Tumbuhan terdiri dari ruangan-ruangan yang dipisahkan berdasarkan fungsinya, yaitu ruang persiapan (preparation area), ruang penanaman (transfer area), ruang pertumbuhan (growing area). Seberapapun luasnya laboratorium, ketiga ruang tersebut harus ada. Ketiga ruang di atas juga harus terpisah dari kebun bibit dan green house untuk menghindari masuknya kontaminasi ke dalam ruang kultur. Kebersihan lantai, meja dan kursi harus terus dijaga secara intensif (Hartman dkk, 1997).
(wastafel), lemari untuk alat dan bahan kimia, sentrifuse, fumehood, destilator dan kereta dorong, ruang transfer yang di dalamnya terdapat laminar air flow, dissecting, mikroskop, alat diseksi, lemari tempat penyimpanan alat-alat steril dan timbangan kecil, ruang kultur yang dilengkapi dengan rak kultur dan lampu fluorescent, timer untuk mengatur lama penyinaran, AC untuk mengontrol temperatur, mikroskop binokuler dan shaker (Barahima 2011).
Tujuan
BAHAN DAN METODE
Alat dan Bahan
Pengenalan laboratorium dan alat-alat kultur jaringan tanaman semua praktikan memakai jas laboratorium dan membawa alat tulis seperti buku dan pulpen untuk menulis penjelasan dari dosen dan asisten praktikum saat menjelaskan.
Metodologi
Prosedur kerja pada praktikum ini yaitu sebagai berikut :
a. Mempersilahkan praktikan masuk ke dalam area laboratorium dengan terlebih dahulu memakai baju atau jas laboratorium.
b. Memberikan respon kepada praktikan dan sedikit pengarahan serta pengenalan tentang kegiatan yang akan di lakukan praktikan.
c. Mempersilahkan praktikan masuk ke dalam ruangan kultur jaringan.
d. Memperkenalkan alat dan bahan di masing-masing ruangan tempat praktikum.
HASIL DAN PEMBAHASAN
Hasil
Alat-alat yang digunakan di dalam laboratorium untuk praktikum kultur jaringan tanaman seperti tabel dibawah ini.
Tabel 1. Beberapa alat dalam praktikum kultur jaringan
No Gambar Alat Nama Alat
1 Timbangan Analitik
2 Autoclave
3 Laminar Air Flow
4 Hotplate stirrer
6 Gelas ukur
7 Bola hisab
8 Shaker inkubator
9 Botol spiritus
10 Beaker glass
11 Pipet
13 Gelas pengaduk
14 Gelas kultur
15 Labu ukur
16 Microwave
18 Pipet ukur
19 Rak kultur
20 Spatula
21 Gunting
Pembahasan
Alat dan bahan yang digunakan dalam kegiatan di laboratorium memerlukan perlakuan khusus sesuai sifat dan karakteristik masing-masing. Perlakuan yang salah dalam membawa, menggunakan dan menyimpan alat dan bahan di laboratorium dapat menyebabkan kerusakan alat dan bahan, terjadinya kecelakaan kerja serta dapat menimbulkan penyakit. Cara memperlakukan alat dan bahan di laboratorium secara tepat dapat menentukan keberhasilan dan kelancaran kegiatan. Adapun perlakuan terhadap alat-alat di laboratorium seperti membawa alat sesuai petunjuk penggunaan, menggunakan alat sesuai petunjuk penggunaan, menjaga kebersihan alat dan menyimpan alat (Yuwono triwibowo, 2008).
Berdasarkan tabel hasil diatas ada beberapa alat yaitu Timbangan Analitik, Autoclave, Laminar Air Flow, Hotplate stirrer, Oven, Gelas ukur, Bola hisab, Shaker, Botol spiritus, Beaker glass, Pipet, Botol semprot, Gelas pengaduk, Gelas kultur, Labu ukur, Microwave, pH meter, Pipet ukur, Rak kultur, Spatula, Gunting, dan Pisau lanset. Kegunaan dari timbangan analitik yaitu untuk menimbang bahan percobaan. Autoclave berfungsi untuk mensterilkanbahan, alat, danmedia yang akandigunakan dalampembiakan kultur jaringan.
Laminar Air Flow yaitu tempat pengerjaan kultur jaringan dalam kondisi steril yang dengan kaca sebagai penutup ruangannya dan dilengkapi dengan lampu serta lampu ultraviolet (UV) juga digunakan untuk mensterilkan ruang, sebelum LAF digunakan. Pemotongan eksplan juga dilakukan di dalam LAF yang kemudian dilanjutkan dengan beberapa tahapan sterilisasi sebelum ditanam pada media kultur. Hot plate stirrer digunakan untuk pemanas larutan dan menghomogenkan larutan. Oven berfungsi untuk memanaskan bahan. Gelas ukur berfungsi untuk mengukur volume larutan. Bola hisab digunakan untuk menyedot larutan yang dipasang pada pipet ukur dan untuk membuang gas.
dan bakteri yang menempel pada alat tersebut mati. Beaker glass berfungsi untuk menampung bahan kimia atau larutan dalam jumlah yang banyak. Pipet tetes berfungsi untuk memindahkan beberapa tetes zat cair. Botol semprot berfungsi untuk menyimpan aquadest dan digunakan untuk mencuci atau membilas alat-alat dan bahan. Gelas pengaduk berfungsi untuk mengaduk larutan tanpa alat pengaduk tambahan hanya menggoyangkan gelas saja.
Gelas kultur berfungsi sebagai tempat untuk mengkultukan atau menanam eksplan yang siap untuk ditanam. Labu ukur berfungsi menampung dan mencampur larutan kimia. Microwave hampir sama dengan oven yaitu berfungsi untuk menghangatkan atau mencairkan serta menaikkan suhu. pH meter adalah alat untuk mengukur tingkat keasaman dan kebasaan suatu larutan atau bahan percobaan. Pipet ukur digunakan untuk mengambil larutan dengan volume tertentu sesuai dengan label yang tertera pada bagian pada bagian yang menggembung. Rak kultur berfungsi untuk menyimpan botol-botol kultur yang telah di sterilkan. Spatula berfungsi untuk memindahkan bahan-bahan kimia. Gunting, pisau dan lanset digunakan sebagai alat untuk memotong bahan tanaman, memindahkan bahan tanaman agar tidak menggunakan kontak langsung dengan tangan.
PENUTUP
Simpulan
Saran
Praktikan sebaiknya berhati-hati dalam penggunaan alat laboratorium agar tidak terjadi kerusakan.
DAFTAR PUSTAKA
Barahima Abbas. 2011. Prinsip dasar teknik kultur jaringan. Alfabeta. Bandung.
Hartmann, H.T., D.E. Kester, F.T. Davies Jr., and R.L. Geneve. 1997. Plant Propagation: Principle And Practices. Sixth Ed.
TOPIK 2
PEMBUATAN MEDIA KULTUR JARINGAN TANAMAN
Oleh : Zeisa Bintan Tsalitsan
(A24130036)
PENDAHULUAN
Latar Belakang
Bahan-bahan yang diperlukan dan biasa digunakan dalam metode kultur jaringan adalah media MS (Murashige and Skoog), yang terdiri dari makronutrien, mikronutrien, vitamin, iron, zat pengatur tumbuh (ZPT), myoinositol, sukrosa dan agar. Bahan-bahan seperti makronutrien, mikronutrien, vitamin, zpt, dan iron biasanya dibuat dalam bentuk larutan stok (media yang lebih pekat), sehingga pada saat akan membuat media, cukup mengambil larutan stok yang sudah dibuat. Zat pengatur tumbuh sangat penting digunakan untuk mengontrol organogenesis dan morfogenesis dalam pembentukan dan perkembangan tunas dan akar, serta pembentukan kalus. Penggunaan ZPT tergantung pada arah pertumbuhan jaringan tanaman yang diinginkan. Jenis dan konsentrasi ZPT untuk setiap tanaman berbeda tergantung pada genotip 2 dan kondisi fisiologi jaringan tanaman (Endang G. Lestari, 2011)
Pembuatan stok bertujuan untuk mempermudah dibandingkan setiap kali membuat media harus menimbang (Edhi Sandra, 2013). Pada pembuatan stok media, pemberian label pada botol larutan stok juga jangan sampai lupa dan harus benar agar mempermudah pada saat akan membuat media kultur. Selain media kultur jaringan, ada beberapa bahan yang digunakan untuk sterilisasi eksplan, diantaranya adalah detergen, alkohol, clorox, aquadest steril, dan spiritus yang dapat digunakan untuk sterilisasi permukaan LAF atau untuk cairan dalam bunsen.
Tujuan
Tujuan dari pratikum ini agar dapat mengetahui dan berlatih proses pembuatan media kultur jaringan tanaman komposisi MS yang baik dan benar.
BAHAN DAN METODE
Alat dan Bahan
Alat yang diperlukan dalam pembuatan media yaitu labu takar, botol kultur, pipet, panci, kompor gas, karet gelang, dan plastik penutup.
Bahan yang digunakan yaitu larutan stok seperti tercantum dalam Tabel lampiran 1, gula, agar-agar, akuades, HCL 1N atau KOH 1N
Metodologi
2. Larutkan gula dengan menambahkan akuades sebanyak 50 ml dan campurkan dengan larutan stok yang telah dipipet.
3. Tambahkan ke dalam larutan tadi akuades sampai mencapai mendekati 500 ml.
4. Tera pH media dengan menambahkan HCL 1N atau KOH 1N sampai mencapai 5.9.
5. Masukkan media ke dalam panci dan tambahkan agar sebanyak 7-8 g lalu masak hingga mendidih.
6. Masukkan media ke dalam botol kultur sebanyak 25 ml dan tutup botol dengan plastik lalu diikat dengan karet gelang. Beri kode pada plastik dan kode kelompok dengan huruf yang kecil. Sterilkan media dengan autoclave selama 20 menit. Media yang steril disimpan di ruang kultur pada suhu 200C.
Skema Pembuatan Media dengan Media Dasar MS (1 Liter) menggunakan setengah dari kebutuhan stok
Larutkan 30 gram gula ke dalam aquades ↓
Masukkan ke dalam labu takar 1 liter ↓
Tambahkan 10 ml masing-masing larutan stok A dan B ↓
Tambahkan 2.5 ml masing-masing larutan stok C, D dan E ↓
Tambahkan 10 ml masing-masing stok F, Myo dan VIT ↓
Tambahkan media kevdalam tempat yang volumenya 2 liter, lalu tambahkan 7-8 gram agar-agar
↓
Panaskan media sampai agar-agar larut (sambil diaduk) ↓
Sterilisasi media selama 15-20 menit pada suhu 1210C tekanan 17.5 psi
HASIL DAN PEMBAHASAN
Hasil
Media kultur yang baik dan dapat digunakan sebagai bahan tanaman yaitu media yang steril dari kontaminasi. Berikut ini tabel hasil pengamatan kontaminasi pada media kultur jaringan tanaman.
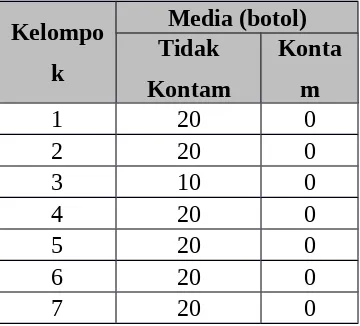
Tabel pengamatan kontaminasi pada media kultur jaringan
Kelompo k
Media (botol) Tidak
Kontam
Konta m
1 20 0
2 20 0
3 10 0
4 20 0
5 20 0
6 20 0
8 12 0
Media yang digunakan dalam praktikum kultur jaringan yaitu media padat dengan jenis media Murashige and Skoog (MS). Medium padat umumnya digunakan untuk menghasilkan kalus yang selanjutnya diinduksi membentuk tanaman yang lengkap (planlet). Media tumbuh dapat mengandung lima komponen utama, yaitu senyawa anorganik (unsur makro dan unsur mikro), zat pengatur tumbuh, sumber karbon, vitamin dan suplemen organik. Media kultur jaringan juga memerlukan bahan tambahan seperti agar, gula (digunakan sebagai sumber energi), dan lain-lain.
Media ini berbentuk padat karena tambahan dari agar-agar yang diberikan sebanyak 7-8 gram. Agar adalah campuran polisakarida yang diperoleh dari beberapa spesies algae dan digunakan sebagai bahan pemadat media. Gula digunakan sebagai sumber energi dalam media kultur, karena umumnya bagian tanaman atau eksplan yang dikulturkan tidak autotrof dan mempunyai laju fotosintesis yang rendah. Pemilihan jenis media kultur yang tepat akan menghasilkan pertumbuhan dan perkembangan eksplan sesuai yang diinginkan. Penambahan HCL 1N atau KOH 1N sampai mencapai 5.9 karena pH media biasanya sedikit masam. Media biasanya diatur pada kisaran 5.6-5.8 tapi tanaman yang berbeda mungkin memerlukan pH yang berbeda untuk pertumbuhan optimum. Jika pH lebih tinggi dari 6.0, media mungkin menjadi terlalu keras dan jika pH kurang dari 5.2, agar tidak dapat memadat (Arianto 2006).
mengeras dan tidak terjadi kontaminasi sebelum dilakukan penanaman eksplan. Setelah didiamkan selama satu minggu, media pun tidak terjadi kontaminasi. Media yang bagus dan steril dari kontaminasi dapat digunakan sebagai media kultur jaringan tanaman. Proses sterilisasi, baik yang dilakukan terhadap peralatan pembuatan media maupun terhadap media itu sendiri dilakukan dengan menggunakan Autoklaf. Di dalam autoklaf tersebut peralatan dan media dipanaskan pada suhu 1210C dan diberi tekanan sebesar 17.5 psi dalam beberapa waktu tertentu. Perlakuan tersebut mengakibatkan berbagai mikroorganisme seperti bakteri ataupun cendawan dan kemudian akhirnya tidak tahan dan mati. Peralatan media pun menjadi steril. terkontaminasi maka semakin baik tingkat keberhasilan kita. Penggunaan autoklaf juga sangat berpengaruh dalam pembuatan media yang steril dari kontaminasi. Penggunaan autoklaf yang benar dapat menghasilkan media yang steril dari kontaminasi karena autoklaf dapat dipakai untuk membunuh mikroorganisme seperti bakteri dan cendawan, sehingga media yang kita buat dapat steril dari mikroorganisme-mikroorganisme tersebut.
Saran
DAFTAR PUSTAKA
Arianto, N, Heru Sugito 2006. Pedoman Pelaksanaan Teknik Kultur Jaringan. Penerbit :Penebar Swadaya. Jakarta.
Edhi Sandra .2013. Cara Mudah Memahami dan Menguasai Kultur Jaringan. IPB Press.
Endang G. Lestari. 2011. Peranan Zat Pengatur Tumbuh dalam Perbanyakan Tanaman melalui Kultur Jaringan. Jurnal Biogen 7 (1):63-68
LAMPIRAN
Tabel 1. Komposisi Media Murashige – Skoog (1962)
FeSO4.7H2O 2.780 27.8 Vit Thiamine
Niacin Pyrodoxine
Glycin
0.010 0.050 0.050 0.200
10 0.1
0.5 0.5 2.0
Myo Myo inositol 10 10 100