AKTIVITAS ANTIBAKTERI EKSTRAK ETANOL KULIT BUAH
DURIAN (
Durio zibethinus
Murr.) TERHADAP
Klebsiella pneumoniae
dan
Streptococcus pyogenes
SERTA BIOAUTOGRAFINYA
NASKAH PUBLIKASI
Oleh :
LU’LU’ HANIF FAIZAH
K100110065
FAKULTAS FARMASI
UNIVERSITAS MUHAMMADIYAH SURAKARTA
SURAKARTA
AKTIVITAS ANTIBAKTERI EKSTRAK ETANOL KULIT BUAH DURIAN (Durio
zibethinus Murr.) TERHADAP Klebsiella pneumoniae DAN Streptococcus pyogenes SERTA BIOAUTOGRAFINYA
ANTIBACTERIAL ACTIVITY OF ETHANOLIC EXTRACT OF DURIAN FRUIT RINDS (Durio zibethinus Murr.) AGAINST Klebsiella pneumoniae AND Streptococcus
pyogenes
Lu’lu’ Hanif Faizah, Haryoto, Ratna Yuliani
Fakultas Farmasi Universitas Muhammadiyah Surakarta Jl. A. Yani Tromol Pos 1 Pabelan, Kartasura, Surakarta 57102
Email : Lulughanif@yahoo.com
ABSTRAK
Limbah kulit durian diketahui mempunyai antibakteri yang baik dalam menghambat pertumbuhan bakteri. Senyawa kimia yang terdapat dalam kulit durian diantaranya flavonoid, saponin, dan minyak atsiri yang berfungsi sebagai antibakteri. Penelitian ini bertujuan untuk menentukan aktivitas ekstrak etanol kulit buah durian terhadap Klebsiella pneumoniae dan Streptococcus pyogenes. Metode penelitian terdiri dari proses maserasi, kulit buah durian direndam dengan dengan etanol 96% selama semalam. Kemudian disaring dan diuapkan diatas waterbath sampai didapat ekstrak kental. Uji aktivitas antibakteri dilakukan dengan metode difusi disk pada media Mueller Hinton. Uji KLT menggunakan fase gerak kloroform:etanol (19:1) dan fase gerak silica gel GF254. Uji bioautografi dilakukan dengan metode bioautografi kontak pada media Mueller Hinton. Rentang konsentrasi yang digunakan dalam penelitian ini 3125 µg/disk, 6250 µg/disk, 1250 µg/disk, 2500µg/disk. Hasil uji aktivitas antibakteri menunjukkan bahwa ekstrak kulit buah durian memiliki aktivitas antibakteri terhadap Klebsiella pneumoniae dengan zona hambat sebesar 8,3±2,08 mm, 9,17±0,29 mm, 9,6±0,28 mm, 10,6±0,57 mm, dan Streptococcus pyogenes sebesar 10±1 mm, 8±1 mm, 8,3±0,57 mm, 8.6±1,15 mm. Hasil analisis KLT menunjukkan bahwa ekstrak etanol kulit buah durian mengandung senyawa flavonoid, saponin, dan minyak atsiri. Berdasarkan uji bioautografi, senyawa kimia yang terkandung dalam kulit buah durian yang berfungsi sebagai antibakteri belum diketahui.
Kata kunci :Antibakteri, Durio zibethinus Murr., Klebsiella pneumoniae, Streptococcus pyogenes
ABSTRACT
Durian rind has been known as good antibacterial agent due to its potential for inhibiting growth of bacteria. Durian rind contain chemical compounds such as flavonoid, saponin, and also essential oil that has antibacterial activity. This research aimed to determine the activity of ethanolic extract of Durian rind against
Klebsiella pneumoniae and Streptococcus pyogenes. Durian rind was soaked in 96% ethanol overnight. Antibacterial activity test performed by disc diffusion on Mueller Hinton medium. Thin layer chromatography method used chloroform:ethanol (19:1) as mobile phase and silica gel GF254 as stationary phase. Bioautography test was conducted using contact bioautography on Mueller Hinton medium. The range of concentrations used in this study were 3125 µg/disc, 6250 µg/disc, 1250 µg/disc, 2500µg/disc. The result of this study showed that ethanol extract of Durian rind has antibacterial activity against Klebsiella pneumoniae with inhibition zones8,3±2,08 mm, 9,17±0,29 mm, 9,6±0,28 mm, 10,6±0,57 mm and Streptococcus pyogenes
respectively 10±1 mm, 8±1 mm, 8,3±0,57 mm, 8.6±1,15 mm. The result of thin layer chromatography showed that the ethanolic extract of durian rind contains flavonoid, saponin, and essential oil. Based on bioautography test, the chemical compounds in the durian rind extract that serves as an antibacterial have not been known.
Key word :Antibacterial, Durio zibethinus Murr., Klebsiella pneumoniae, Streptococcus pyogenes
PENDAHULUAN
Infeksi bakteri merupakan kondisi patogenis akibat dari berkembangnya
mikroorganisme dalam inang (Subandi, 2010). Di negara maju, penyakit yang disebabkan
oleh infeksi masih menjadi masalah yang cukup tinggi (Noer, 2012). Penyakit tersebut
diantaranya disebabkan oleh bakteri Klebsiella pneumoniae dan Streptococcus pyogenes.
Klebsiella pneumoniae merupakan bakteri patogen Gram negatif yang sering dapat
menyebabkan infeksi nokosomial (Susilo et al., 2004). Klebsiella pneumoniae
menyebabkan penyakit infeksi pernafasan seperti pneumonia, rhinoscleroma serta sinusitis
(Sikarwar & Harsh., 2011). Streptococcus pyogenes merupakan bakteri patogen
ekstraseluler Gram positif yang sering menginfeksi manusia. Bakteri tersebut sering
menyebabkan infeksi tenggorokan diantaranya faringitis, impetigo, serta demam scarlet
(Cunningham, 2000).
Infeksi bakteri tersebut dapat diatasi dengan menggunakan antibiotik yang memiliki
mekanisme aksi menghambat pertumbuhan bakteri. Penggunaan antibakteri secara terus
menerus dapat menyebabkan kerusakan organ tubuh apabila digunakan dalam dosis yang
tidak tepat. Hal ini dapat diatasi salah satunya dengan cara menemukan senyawa antibakteri
baru yang berasal dari bagian tanaman tertentu (Karadi et al., 2011).
Indonesia merupakan negara yang mempunyai iklim tropis dengan kondisi tanah yang
subur. Beraneka ragam tanaman dapat ditemukan di Indonesia, diantaranya banyak tanaman
yang memiliki khasiat sebagai obat. Dalam beberapa tahun terakhir, pemanfaatan tanaman
sebagai obat herbal di Indonesia maupun luar negeri mengalami peningkatan. Obat herbal
lebih dipilih karena memiliki tingkat keamanan yang baik atau tidak memiliki efek samping
yang berbahaya. Salah satu pemanfaatan obat herbal tersebut adalah sebagai antibakteri
(Poelungan et al., 2007). Buah durian dapat digunakan sebagai antibakteri, antiinflamasi,
antioksidan dan antikarsinogenik (Ashraf et al., 2010). Ekstrak etanol kulit buah durian
(Durio zibethinus Murr.) memiliki aktivitas antibakteri yang baik terhadap Pseudomonas
aeruginosa dengan kadar hambat minimum sebesar 4% dan kadar bunuh minimum sebesar
6% (Noorhamdani et al., 2009). Gel polisakarida dari kulit durian juga memiliki manfaat
sebagai antibakteri (Lipipun et al., 2002). Senyawa kimia yang terdapat di dalam kulit buah
durian adalah flavonoid, minyak atsiri, dan saponin (Noorhamdani et al., 2009).
Penelitian ini dilakukan untuk menguji aktivitas antibakteri ekstrak etanol kulit buah
serta profil bioautografinya. Hasil dari penelitian ini diharapkan dapat membuktikan secara
ilmiah khasiat dari kulit buah durian sebagai antibakteri.
METODE PENELITIAN
A. Alat dan Bahan
1. Alat
Alat yang digunakan dalam penelitian ini yaitu waterbath WNB-14 (Memmert®), rotary
evaporator (Heidolph®), neraca analitik (Ohaus®), autoklaf (MA 672®), oven (Memmert®),
Laminar Air Flow (Astari Niagara®), vortex (Thermolyne), dan alat-alat gelas lain.
2. Bahan
Bahan yang digunakan antara lain, kulit buah durian yang diambil dari Omah Duren
Klaten, Klebsiella pneumoniae, Streptococcus pyogenes, DMSO 96%, akuades, media
Mueller Hinton (MH), media Brain Heart infution (BHI), disk antibiotic, lempeng Silika
GF254, sitroborat, reagen Liebermann-Buchard dan anisaldehid H2SO4.
B. Jalannya Penelitian
1. Pembuatan Simplisia
Pembuatan simplisia dilakukan dengan memilih kulit durian yang segar kemudian
dibersihkan dengan air yang mengalir. Selanjutnya kulit durian dipotong menjadi bagian
kecil-kecil dan dikeringkan dengan cara dijemur. Kemudian dilakukan sortasi kering, dan
simplisia dihaluskan menjadi serbuk halus.
2. Ekstraksi Kulit Buah Durian
Serbuk kulit buah durian sebanyak 1 kg direndam dalam 10 L etanol 96% selama
semalam sambil diaduk beberapa kali. Dilakukan penyaringan maserat dengan corong
Buchner. Ampas yang didapat dilakukan remaserasi sebanyak 2x, maserat dievaporasi dengan
rotary evaporator, kemudian diuapkan di atas waterbath sampai didapat ekstrak yang kental.
3. Sterilisasi alat
Alat gelas seperti cawan petri, labu takar, tabung reaksi serta alat gelas yang lain dicuci
sampai bersih dan kemudian dikeringkan, setelah itu dibungkus dengan kertas, disterilkan
dengan oven pada suhu 1700C selama 1 jam. Alat-alat lain seperti yellow tips, blue tips, serta
media disterilkan dengan metode panas basah pada suhu 1210C selama 20 menit. Setelah
semua disterilkan, alat sudah bisa digunakan atau disimpan dengan tutup rapat.
4. Pembuatan Media
Media MH ditimbang sebanyak 9,5 gram dilarutkan dalam 250 ml akuades.
sebanyak 8 gram dan media LIA sebanyak 8,25 gram masing-masing dilarutkan dalam 250
ml akuades. Media dilarutkan dan disterilisasi menggunakan sterilisasi uap basah 1210C
selama 20 menit. Media disimpan di dalam kulkas sebagai stok media.
5. Pembuatan Stok Bakteri
Klebsiella pneumoniae dan Streptococcus pyogenes diambil sebanyak satu mata ose
digoreskan secara streak plate pada media Mueller Hinton. Kultur diinkubasi pada suhu 370C
selama 24 jam. Setelah bakteri tumbuh, disimpan pada suhu 40C.
6. Pembuatan Suspensi Bakteri
Pembuatan suspensi bakteri dilakukan dengan cara sebanyak 3-5 koloni bakteri diambil
dari stok bakteri 24 jam, disuspensikan ke dalam media BHI steril dan diinkubasi selama 2-6
jam dengan suhu 37oC. Mc. Farland 1.5x108 CFU/mL digunakan sebagai standar untuk
menentukan kekeruhan suspensi bakteri. Suspensi yang lebih keruh ditambah dengan larutan
salin untuk uji dengan metode difusi disk.
7. Pengecatan Gram
Suspensi bakteri diambil 1 mata ose, digoreskan pada obyek gelas yang telah
dibebaslemakkan. Goresan bakteri ditetesi formalin 1% dan dibiarkan 5 menit, dikeringkan
lagi, dan preparat siap digunakan. Preparat yang sudah siap dicat digenangi cat gram A
selama 1-3 menit, kemudian digenangi cat gram B selama 0,5-1 menit, setelah itu cat dibuang
dan dicuci menggunakan air. Selanjutnya preparat ditetesi dengan gram C sampai warna cat
luntur, kemudian preparat digenangi gram D 1-2 menit, dicuci dan dikeringkan pada suhu
kamar. Preparat diamati di bawah mikroskop dengan pembesaran 1000x.
8. Uji Biokimiawi
Uji biokimiawi bakteri Klebsiella pneumoniae dilakukan dengan cara diambil satu mata
ose digoreskan dalam media KIA, LIA, dan MIO. Ketiga media yang telah ditanami tersebut
diinkubasi pada suhu 37oC selama 18-24 jam. Uji biokimiawi bakteri Streptococcus pyogenes
dilakukan dengan cara uji katalase dengan meletakkan bakteri pada kaca objek dan diteteskan
H2O2 3% di atas kaca objek sebanyak satu tetes dan langsung diamati terjadinya pengurangan
hidroksi peroksida. Uji katalase dilakukan untuk mengetahui kemampuan bakteri memecah
H2O2. Analisis hasil dilakukan berdasarkan karakteristik kedua bakteri tersebut.
9. Pembuatan Seri Konsentrasi
Seri konsentrasi ekstrak etanol kulit buah durian masing-masing dibuat 25%, 12,5%,
6,25%, dan 3,125%. Konsentrasi 25% dibuat dengan cara ekstrak etanol kulit buah durian
diambil sebanyak 250 mg dan larutkan dengan DMSO sampai 1 mL. Konsentrasi 12,5%
sampai 1 mL. Untuk konsentrasi 6,25% dibuat dengan cara diambil 500 µl dari konsentrasi
12,5% dan dilarutkan dengan 1 mL DMSO. Konsentrasi 3,125% dibuat dengan cara diambil
500 µL dari konsentrasi 6,25% kemudian dilarutkan dengan 1 mL DMSO. Masing-masing
seri konsentrasi diambil 10 µL dan diteteskan pada disk dan dibiarkan sampai mengering.
10. Uji Aktivitas Antibakteri
Sebanyak 20 mL media MH dimasukkan dalam cawan petri yang steril, didiamkan 30
menit ditunggu sampai mengeras. Sebanyak 200 µL suspensi bakteri diambil, dimasukkan
dalam media MH, diratakan dengan spreader glass steril pada permukaan MH, didiamkan
3-5 menit sebelum penanaman disk. Media diinkubasi pada suhu 370C selama 18-24 jam di
dalam inkubator. Diameter zona hambat masing-masing konsentrasi dihitung dan
dibandingkan terhadap kontrol. Kontrol positif yang digunakan adalah streptomisin untuk
Klebsiella pneumoniae sedangkan untuk Streptococcus pyogenes adalah tetrasiklin. Kontrol
negatif yang digunakan adalah DMSO 100%. Aktivitas antimikroba dapat ditentukan dengan
mengukur diameter zona hambat yang dinyatakan dalam satuan mm.
11. Uji Kromatografi Lapis Tipis
Uji kromatografi lapis tipis dilakukan dengan menggunakan fase diam silica gel GF254
yang telah diaktifkan dengan cara dipanaskan pada suhu 1050-1100C selama 1 jam.
Konsentrasi ekstrak yang digunakan sebesar 10%, sebanyak 6 µL larutan ditotolkan pada fase
diam, ditunggu sampai kering, kemudian akan dielusi dengan fase gerak. Plat diangkat dan
dikeringkan hingga pelarut menguap. Penampakan bercak dilihat dibawah sinar tampak, UV
254 dan 366 nm. Deteksi flavonoid dilakukan dengan reagen sitroborat. Bercak terlihat
semakin tinggi intensitas warnanya di bawah UV 366 nm. Deteksi saponin dilakukan dengan
reagen Liebermann-Burchard dan diamati bercak dibawah sinar tampak UV 366 nm. Bercak
yang muncul berwarna biru, hijau, merah muda, oranye. Deteksi minyak atsiri dilakukan
dengan pereaksi semprot anisaldehid-H2SO4 kemudian dipanaskan pada suhu 1100C selama
10 menit dan bercak yang muncul berwarna biru, hijau, merah dan coklat pada UV 366 nm.
Bercak yang muncul kemudian dianalisis dengan menentukan nilai Rf untuk masing-masing
uji.
12. Uji Tabung
Deteksi senyawa saponin menggunakan uji busa dilakukan dengan cara ekstrak kulit
buah durian ditambahkan 1 ml air panas ke dalam tabung, dibiarkan dingin, dikocok selama 1
menit, diamati terbentuknya busa. Busa yang terbentuk ditambahkan HCl 1%, jika busa stabil
13. Uji Bioautografi
Bioautografi dilakukan dengan cara meletakkan plat hasil KLT pada permukaan media
MH di dalam petri yang telah diinokulasi dengan Klebsiella pneumoniae dan Streptococcus
pyogenes dengan konsentrasi 1,5x108 CFU/mL sebanyak 200 µL selama 25 menit. Plat KLT
diambil, kemudian petri diinkubasi selama 24 jam, dengan suhu 370C. Jika bercak pada hasil
elusi memiliki aktivitas antibakteri, maka akan terbentuk area jernih yang merupakan hasil
zona hambatan.
HASIL DAN PEMBAHASAN
A. Ekstraksi
Proses ekstraksi merupakan proses pemisahan suatu zat dengan pelarut yang sesuai.
Ekstraksi dapat dilakukan dengan berbagai metode, diantaranya metode maserasi.maserasi
merupakan teknik ekstraksi yang sederhana dibanding metode ekstraksi yang lain. Proses
maserasi menggunakan pelarut yang banyak, semakin banyak pelarut yang digunakan maka
hasil ekstraksi akan semakin banyak (Voight, 1995). Sebanyak 1000 gram serbuk kulit durian
yang direndam dalam etanol 96% menghasilkan ekstrak kental sebesar 135,567 gram. Proses
remaserasi dilakukan sebanyak 2 kali dan dihasilkan rendemen sebesar 13,56%.
B. Identifikasi Bakteri
Proses identifikasi bakteri dilakukan dengan 2 cara, yaitu dengan metode pengecatan
Gram dan uji biokimiawi. Uji ini dilakukan untuk menggolongkan bakteri ke dalam Gram
positif atau Gram negatif dan mengetahui sifat asli dari bakteri.
1. Metode Pengecatan Gram
Berdasarkan hasil yang diperoleh pada pengecatan bakteri saat diamati di bawah
mikroskop setelah pengecatan Gram, Klebsiella pneumonia memiliki bentuk batang, memiliki
susuna sel yang bergerombol, dan berwarna merah. Hasil pengecatan Gram yang dilakukan
terhadap Streptococcus pyogenes memiliki bentuk bulat, susunan sel berbentuk rantai, dan
berwarna ungu. Bakteri Gram negatif mempunyai lapisan peptidoglikan yang tipis, sedangkan
bakteri Gram positif memiliki lapisan peptidoglikan yang banyak (Pratiwi, 2008).
2. Uji Biokimiawi
Uji biokimiawi dilakukan untuk mengetahui sifat kimia suatu bakteri. Klebsiella
pneumoniae diidentifikasi dengan menggunakan media Kligler Iron Agar (KIA), Lysine Iron
Agar (LIA), dan Motility Indole Ornithine (MIO). Streptococcus pyogenes diidentifikasi
Hasil uji biokimia pada bakteri Klebsiella pneumoniae menggunakan media KIA terlihat
adanya perubahan warna media dari merah menjadi kuning pada bagian tegak dan bagian
miring, ini mendandakan bahwa Klebsiella pneumoniae mampu menghasilkan asam serta
dapat memfermentasi laktosa dan glukosa. Pada bagian bawah media tidak terdapat
gelembung gas dan tidak terdapat warna hitam pada media, hal ini menunjukkan bahwa
Klebsiella pneumoniae tidak dapat memproduksi gas dan serta tidak membentuk H2S. Hasil
identifikasi dengan menggunakan media LIA pada Klebsiella pneumoniae terlihat warna
ungu pada bagian tegak dan miring pada media, ini menandakan bahwa Klebsiella
pneumoniae memiliki sifat basa dan dapat mendekarboksilasi lisin. Klebsiella pneumoniae
tidak dapat membentuk H2S ditandai dengan tidak adanya warna hitam pada bagian miring
media. Hasil uji biokimia Klebsiella pneumoniae terhadap media MIO terlihat warna ungu
pada bagian atas media serta warna kuning pada bagian bawah media, dan tidak terbentuk
cincin merah setelah penambahan reagen Kovac, serta tidak ada kekeruhan pada media.
Pertumbuhan bakteri hanya terdapat pada daerah hasil tusukan. Hal ini menunjukkan bahwa
Klebsiella pneumoniae tidak mendekarboksilasi ornithin, tidak menghasilkan indol, serta
tidak menunjukkan pergerakan bakteri.
Hasil identifikasi yang dilakukan terhadap Streptococcus pyogenes dengan uji hemolisis
mengunakan agar darah menunjukkan adanya daerah jernih di sekitar koloni bakteri atau
sering disebut dengan hemolisis beta. Hasil uji katalase menunjukkan hasil negatif ditandai
dengan tidak terbentuknya gelembung gas.
C. Uji Aktivitas Antibakteri
Uji aktivitas antibakteri dilakukan dengan tujuan mengetahui aktivitas antibakteri ekstrak
kulit buah durian (Durio zibethinus Murr.) terhadap Klebsiella pneumoniae dan
Streptococcus pyogenes. Metode yang digunakan dalam pengujian aktivitas antibakteri ini
adalah metode difusi disk (Kirby Bauer) dengan menggunakan media Mueller Hinton.
Metode difusi disk tergolong metode yang sederhana serta dapat digunakan untuk melihat
terbentuknya zona hambat. Area jernih di sekitar disk menunjukkan adanya penghambatan
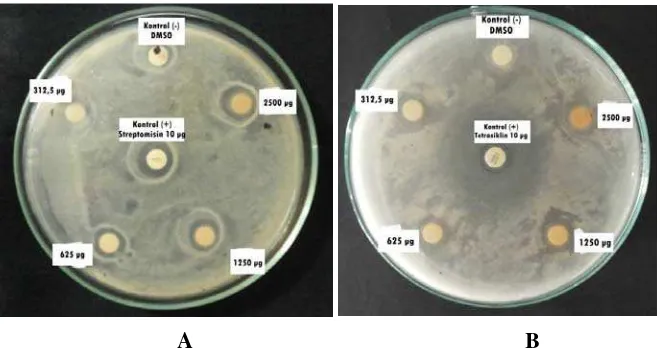
A B
Gambar 4. Hasil uji aktivitas antibakteri ekstrak etanol kulit buah durian terhadap Klebsiella pneumoniae (A) dan Streptococcus pyogenes (B)
Pada pengujian ekstrak kulit buah durian terhadap Klebsiella pneumoniae dengan
konsentrasi 312,5 µg/disk, 625 µg/disk, 1250 µg/disk, dan 2500 µg/disk masing-masing
menghasilkan zona hambat sebesar 8,3 mm; 9,17 mm; 9,6 mm; 10,6 mm. Berdasarkan
pengujian yang dilakukan terhadap Klebsiella pneumoniae diameter zona hambat yang
terbentuk semakin bertambah besar seiring dengan peningkatan konsentrasi ekstrak yang
dimasukkan ke dalam disk. Semua sampel yang diujikan terhadap Klebsiella pneumoniae
menghasilkan zona hambat yang radikal. Terbentuknya diameter zona hambat kemungkinan
dipengaruhi oleh proses difusi yang merata dari disk ke permukaan media yang telah
diinokulasi dengan bakteri.
Pengujian terhadap Streptococcus pyogenes dengan konsentrasi 312,5 µg/disk, 625
µg/disk, 1250 µg/disk, dan 2500 µg/disk, menghasilkan zona hambat yang irradikal sebesar
10 mm, 8 mm, 8,3 mm, 8,6 mm. Zona hambat yang terbentuk semakin besar seiring dengan
peningkatan konsentrasi. Tetapi zona hambat yang terbentuk pada konsentrasi terkecil yaitu
312,5 µg/disk menunjukkan hasil yang paling besar. Hal ini kemungkinan terjadi karena
proses difusi yang terjadi antara ekstrak yang terdapat di dalam disk dengan media tidak
tidak merata.
Kontrol positif yang digunakan untuk Klebsiella pneumoniae (streptomisin)
menghasilkan zona hambat sebesar 13,8 mm, sedangkan kontrol positif yang digunakan untuk
Streptococcus pyogenes (tetrasiklin) menghasilkan zona hambat sebesar 30,6 mm. Kontrol
negatif (DMSO) yang digunakan untuk kedua bakteri Klebsiella pneumoniae dan
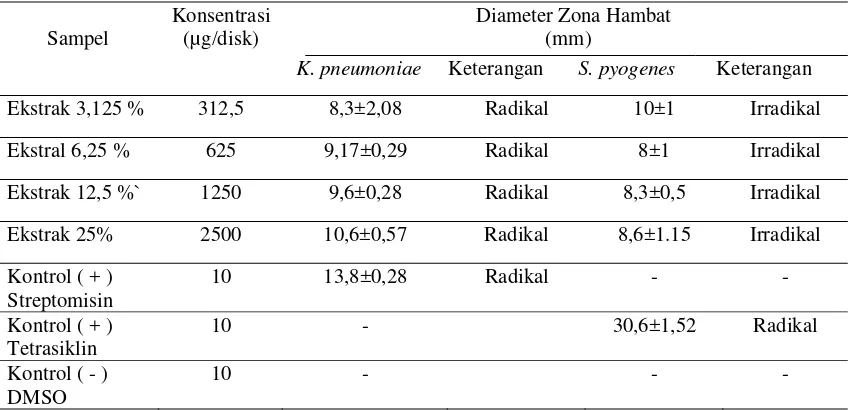
Tabel 1. Hasil uji aktivitas antibakteri ekstrak etanol kulit buah durian terhadap bakteri Klebsiella pneumoniae dan Streptococcus pyogenes
Uji Kromatografi Lapis Tipis
Kromatografi merupakan teknik yang digunakan untuk memisahkan suatu campuran
senyawa dalam suatu sampel. Uji kromatografi lapis tipis ini diharapkan dapat mengetahui
suatu golongan senyawa flavonoid, saponin, dan minyak atsiri yang terkandung di dalam
ekstrak kulit buah durian.
Fase gerak yang digunakan dalam uji KLT yaitu kloroform:etanol (19:1) v/v dengan fase
diam silica GF254 serta konsentrasi sampel yang digunakan adalah 10% sebanyak 6 µl dengan
jarak pengembangan 5 cm. Pereaksi semprot yang digunakan silica GF254 serta konsentrasi
sampel yang digunakan adalah 10% sebanyak 6 µl dengan jarak pengembangan 5 cm.
Deteksi bercak dilihat secara visual, UV 254 nm, UV 366 nm dan dengan beberapa
pereaksi semprot. Pereaksi semprot yang digunakan untuk deteksi saponin adalah Liebermann
Buchard dan uji buih dengan metode tabung (Hajnos, et al., 2008). Deteksi flavonoid
digunakan pereaksi semprot sitroborat, sedangkan deteksi minyak atsiri digunakan
anisaldehid-H2SO4. Senyawa saponin dideteksi dengan pereaksi semprot Liebermann
Buchard di bawah sinar UV 366 nm menghasilkan warna biru, hijau, merah muda, oranye
yang menandakan adanya senyawa saponin. Senyawa flavonoid digunakan pereaksi semprot
sitroborat di bawah sinar UV 254 nm terjadi pemadaman dan pada UV366 nm menghasilkan
warna hijau, biru, serta kuning, dan oranye (Alam et al., 2012). Deteksi minyak atsiri
digunakan pereaksi semprot anisaldehid-H2SO4 pada sinar tampak menghasilkan warna biru,
hijau, merah serta coklat (Wagner dan Bladt, 1996).
Sampel
Konsentrasi (µg/disk)
Diameter Zona Hambat (mm)
K. pneumoniae Keterangan S. pyogenes Keterangan
Ekstrak 3,125 % 312,5 8,3±2,08 Radikal 10±1 Irradikal
Ekstral 6,25 % 625 9,17±0,29 Radikal 8±1 Irradikal
Ekstrak 12,5 %` 1250 9,6±0,28 Radikal 8,3±0,5 Irradikal
Ekstrak 25% 2500 10,6±0,57 Radikal 8,6±1.15 Irradikal
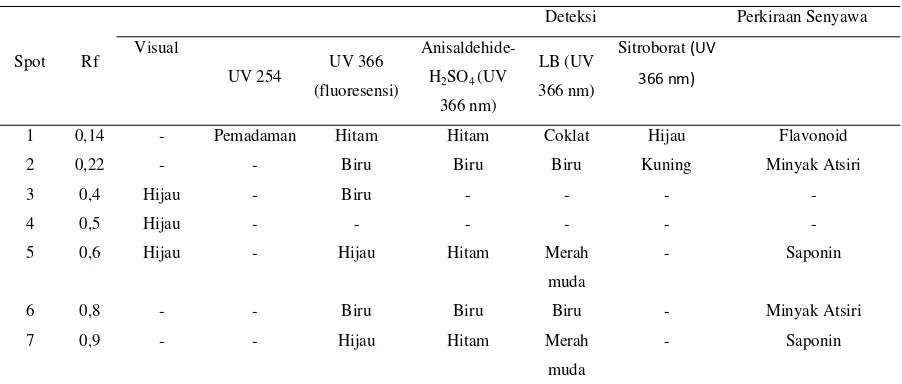
Tabel 2. Hasil KLT ekstrak etanol kulit buah durian (Durio zibethinus Murr.)
Berdasarkan hasil KLT ekstrak etanol kulit buah durian (Tabel 2) menunjukkan bahwa
ekstrak etanol kulit buah durian mengandung saponin yang terdeteksi dengan pereaksi
semprot Liebermann Buchard ditandai dengan warna merah ketika dilihat di bawah UV366.
Minyak atsiri terdeteksi dengan pereaksi semprot anisaldehide-H2SO4 ditandai dengan adanya
warna biru ketika dilihat di bawah UV366. Hasil uji flavonoid ketika sebelum disemprot
dengan sitroborat dan dilihat di bawah UV 254 menunjukkan adanya pemadaman, sebelum
disemprot plat dilihat di bawah UV366 menghasilkan warna biru, hijau kekuningan, setelah
disemprot dilihat di bawah UV366 nm warna biru dan hijau terihat semakin intensif, ini berarti
ekstrak kulit buah durian mengandung flavonoid.
Berdasarkan hasil KLT, ekstrak etanol kulit buah durian (Durio zibethinus Murr.)
menunjukkan adanya senyawa golongan flavoniod, saponin dan minyak atsiri. Uji buih
menunjukkan hasil positif saponin ditandai dengan buih yang tetap terbentuk (konstan)
setelah ditetesi dengan HCl.
D. Uji Bioautografi
Uji bioautografi dilakukan untuk mengetahui senyawa kimia yang terkandung di dalam
ekstrak kulit buah durian yang mampu menghambat pertumbuhan Klebsiella pneumoniae dan
Streptococcus pyogenes. Metode bioautografi merupakan metode yang spesifik untuk
membandingkan bercak kromatogram hasil kromatografi lapis tipis (KLT) dengan zona jernih
yang ada di dalam petri yang telah diinokulasi dengan bakteri. Aktivitas antibakteri
ditunjukkan dengan adanya zona jernih di bekas totolan bercak pada media MH yang telah
Berdasar hasil bioautografi yang telah dilakukan dengan konsentrasi sampel 10% dan
digunakan volume sebanyak 6 µl tidak terlihat zona jernih pada daerah totolan. Penambahan
konsentrasi telah dilakukan, namun tetap tidak memperlihatkan adanya hasil zona jernih di
bekas totolan bercak. Hal ini menunjukkan bahwa senyawa yang bertanggungjawab sebagai
antibakteri yang terdapat di dalam kulit buah durian belum dapat diketahui.
KESIMPULAN DAN SARAN
Kesimpulan
Berdasarkan hasil penelitian, maka dapat ditarik kesimpulan sebagai berikut :
1. Ekstrak etanol kulit buah durian (Durio zibethinus Murr.) mempunyai aktivitas
antibakteri terhadap Klebsiella pneumoniae dan Streptococcus pyogenes.
2. Senyawa kimia yang terdapat di dalam kulit buah durian yang bertanggungjawab
sebagai antibakteri terhadap Klebsiella pneumoniae dan Streptococcus pyogenes belum
dapat diketahui.
Saran
1. Perlu dilakukan penelitian lebih lanjut dengan metode yang lain, misalnya dilusi cair
untuk membandingkan aktivitas antibakteri dengan metode yang berbeda.
2. Perlu dilakukan bioautografi dengan metode selain metode kontak, misal bioautografi
imersi atau bioautografi langsung.
UCAPAN TERIMAKASIH
Dalam pelaksanaannya penulis tidak luput dari bantuan dan doa banyak pihak. Penulis
mengucapkan banyak terimakasih, khususnya kepada :
1. Bapak Azis Saifudin Ph.D, Apt., selaku Dekan Fakultas Farmasi Universitas
Muhammadiyah Surakarta.
2. Bapak Dr. Muhammad Da’i, M.Sc., Apt., selaku pembimbing akademik.
3. Bapak Dr. Haryoto, M.Sc., selaku pembimbing I dan Ibu Ratna Yuliani, M.Biotech
St., selaku Pembimbing II.
4. Ibu Rima Munawaroh, M.Sc, Apt., dan Bapak Dedi Hanwar, M.Sc, Apt., selaku
penguji I dan penguji II.
5. Keluarga penulis, kedua orangtuaku, Ibu Isna Rokhmawati, S.Pd., M.Pd.I dan Alm.
Bp. Ifyanto serta adikku Zuha Rahma Salsabila.
DAFTAR PUSTAKA
Alam, G., Mufidah., Nasrum, M., Felix, K., Abdul, R., & Usmar., 2012, Skrining Komponen Kimia dan Uji Aktivitas Mukolitik Ekstak Rimpang Bengle (Zingiber purpureum Roxb.) Terhadap Mukosa Usus Sapi Secara In Vitro, Majalah Farmasi dan Farmakologi, 16 (3), 123-126.
Ansel, H. C., Pengantar Bentuk Sediaan Farmasi, 2008 diterjemahkan oleh Ibrahim, F., Edisi keempat, UI Press, Jakarta.
Ashraf, M., Jamil, M., Yusoff. & Ismail, 2010, Esthimation of Antioxidant Phytochemicals in Four Different Varities of Durian Fruit, Journal of Scientific Research, 6 (5), 465-466.
Acumedia, 2014, Lysine Iron Agar, http://www.neogen.com (diakses tanggal 13 Desember 2014).
Biokar, 2014, Kliger Iron Agar, http://www.biokar‐diagnostics.com (diakses tanggal 13 Desember 2014).
Cunningham, M., 2000, Pathogenesis of Group A Streptococcal Infection, Clinical Microbiol, 13 (3), 470-511.
Departemen Kehutanan, 2014, Sim Penghijauan Durian, http://sim‐
rlps.dephut.go.id/simpenghijauan (diakses tanggal 14 April 2014).
Fransworth, Norman., 1996, Biological and Phytocemical Screening of Plants, Journal of Pharmaceutical Science, 55 (3).
Hardy Diagnostic, 2013, MIO (Motility Indole Ornithine) Medium
https://catalog.hardydiagnostics.com (diakses tanggal 13 Desember 2014).
Hart, T. & Paul, S., 1997, Atlas Berwarna Mikrobiologi Kedokteran, diterjemahkan oleh Ferdian, E. P. & Poppy, K., Jakarta, Penerbit Hipokrates.
Jawetz, E., Melnick, J.L.,dan Adelberg, E. 2005, Medical Microbiology, Twenty Second Ed, diterjemahkan oleh Nugroho, E., Edisi XX, Jakarta, Penerbit Buku Kedokteran EGC.
Karadi, R., Arpan, S., Pranav, P. & Parvez, A., 2011, Antimicrobial Activities of Musa paradisiacal and Cocos nucifera, International Journal of Research in Pharmaceutical and Biomedical Sciences, 2 (1), 264-265.
Kusumaningtyas, E., Astuti, E., dan Darmono., 2008, Sensitivitas Metode Bioautografi Kontak dan Agar Overlay dalam Penentuan Senyawa Anti Kapang, Jurnal Ilmu Kefarmasian Indonesia, 6 (2).
Lipipun, F., Nantawan, N. & Sunanta, P., 2002, Antimicrobial Activity (in vitro) of Polysaccharide Gel From Durian Fruit-hulls, J. Sci. Technol, 24 (1), 31-38.
NCBI, 2014, Klebsiella pneumoniae dan Streptococcus pyogenes,
Noer, S., 2012, Pola Bakteri dan Resistensinya Terhadap Antibiotik yang Ditemukan Pada Air dan Udara Ruang Instalasi Rawat Khusus RSUP Dr. Wahidin Sudirohusodo Makassar, Majalah Farmasi dan Farmakologi, 16 (2).
Noorhamdani, Samodriyanti, & Pranitia, K., 2009, Uji Ekstrak Kulit Durian Sebagai Antimikroba Terhadap Pseudomonas aeruginosa Secara In Vitro, Skripsi, Fakultas Kedokteran, Universitas Brawijaya Malang.
Noorhamdani, A., Setyohadi, R. & Fawzi, A., 2010, Uji Efektifitas Ekstrak Daun Binahong Sebagai Antimikroba Terhadap Bakteri Klebsiella pneumoniae Secara In vitro,
Skripsi, Fakultas Kedokteran, Universitas Brawijaya Malang.
Nurliani, Anni., 2007, Penelusuran Potensi Antifertilitas Kulit Kayu Durian (Durio zibethinus Murr.) Melalui Skrining Fitokimia, Sains dan Terapan, 2, 53-54.
Oesman, F., Murniana., Khairunnas, M., & Saidi, N., 2011, Antifungal Activity of Alkaloid From Bark of Cerbera odollam, Jurnal Natural,10, 2, 2.
Poelungan, M., Andriani., Susan, M., Komala, I. & Hasnita., M., 2007, UjiDaya Antibakteri Ekstrak Etanol Kulit Batang Bungur Terhadap Staphylococcus aureus dan
Escherichia coli Secara In vitro, Seminar Nasional Teknologi Peternakan dan Veternier.
Pratiwi, S. T., 2008, Mikrobiologi Farmasi, 188, 191, Penerbit Erlangga, Jakarta.
Rosenthal, V., Hu, B., Maki., Dennis, G., Yatin, M., Anucha, A., et al., 2009, International Nocosomial Infection Control Consortium (INCC) Report, Data Summary of 36 Countries, for 2004-2009, INICC Report, 1-34.
Sikarwar, A. & Harsh, V., 2011, Challenge to healthcare : Multidrug resistance in Klebsiella pneumoniae, International Conference on Food Engineering and Biotechnology, 9, 130-134.
Subandi, 2010, Mikrobiologi Perkembangan, Kajian, dan Pengamatan dalam Perspektif Islam, Bandung, PT. Remaja Rosdakarya.
Susilo, J., Teguh, R. & Sunarno., 2004, Deteksi Bakteri Klebsiella pneumoniae Pada Sputum dengan Metode Imunositokimia Menggunakan Anti Outer Membrane Protein Berat Molekul 40 KDA Klebsiella pneumoniae Sebagai Antibodi, Jurnal Kedokteran Brawijaya, 20 (1), 12-18.
Untung, O., 2005, Durian Untuk Komersial dan Hobi, 1, 2, Jakarta, Penebar Swadaya.
Utami, D., 2013, Aktivitas Antibakteri Ekstrak Buah Kapulaga (Amomum compactum
Soland. Ex Maton) Terhadap Escherichia coli dan Streptococcus pyogenes, Skripsi, Fakultas Teknobiologi, Universitas Sanata Dharma Yogyakarta.
Wagner, H., dan Bladt, S., 1996, Plant Drug Analisys- A Thin Layer Chromatography Atlas, 6, Springer, Germany.
Wijaya, S & Nopriansyah, S., 2011, Uji Invitro Efek Antibakteri Ekstrak Daging Muda Buah Mahkotadewa (Phaleria macrocarpa) Terhadap Klebsiella pneumoniae, Skripsi, Fakultas Kedokteran, Universitas Sriwijaya.