LAMPIRAN 1:
PENENTUAN KADAR ALKOHOL SECARA KUALITATIF DAN KUANTITATIF DARI HASIL FERMENTASI
Fermentasi adalah perubahan kimia dalam bahan pangan yang disebabkan enzim. Enzim yang berperan dapat dihasilkan oleh mikroorganisme atau telah ada dalam bahan pangan.
Prinsip Pelaksanaan
Berdasarkan uji kualitatif dari alkohol yang mengalami reaksi oksidasi reduksi dimana alkohol dioksidasi menjadi aldehid dan dengan pemanasan terbentuk asam karboksilat, dimana K2Cr2O7 sebagai oksidator mengalami reduksi dari Cr6+ menjadi Cr3+ yang ditandai dengan terjadinya perubahan warna dari bening menjadi kuning kehijauan dan dengan pemanasan terbentuk larutan biru.
Bahan yang akan di Destilasi
1. Nira aren asli manis
2. Nira ditambah Raru rasa manis
3. Tuak Asli adalah nira ditambah raru kemudian dibuat sedikit di gelas lalu digantung dipohon kemudian nira aren asli menetes-netes ketempat penampungan dan menjadi tuak asli
Prosedur Kerja Destilasi
1. Nira asli dimasukkan kedalam labu alas 500 ml.
2. Kemudian dipanaskan 70 s.d 100°C sampai mendidih dengan rentang waktu 30' (pemanasan).
3. Setelah mendidih didinginkan sampai gelembung-gelembung air hilang ± 5' kemudian dipanaskan kembali 10' (yang kedua) mendidih dan didinginkan selama ± 5', demikian seterusnya.
4. Setelah sampel selesai didestilasi kemudian diambil sebanyak 5 ml ditambah 3 tetes K2CrO7 dan dipanaskan sampai berubah warna, ternyata tidak ada perubahan warna dan kesimpulan sementara: tidak ada etanol pada nira asli pada proses destilasi (kualitas).
Prosedur Kerja dan Alat-alat I. Alat-alat terdiri dari:
Labu alas 500 ml, bunsen (lampu yang bahan bakarnya dari alkohol), kondensor, penjepit tabung, tabung reaksi, termometer 360oC, Elmayer, pipet tetes, elektro mantel, plastik dan karet, statif dan klem, selang, cok sambung, ember plastik, teflon, dlukol, labu ukur, buret, statik pen klem, tabung reaksi, aquadest, galass ukur , beaker glass 500 ml, dan gabus karet.
III. Prosedur Kerja secara kualitas
1. Masukkan nira 500 ml ke dalam labu alas 2. Dirangkai alat destilasi
3. Didestilasi pada suhu 78°C
4. Destilasinya di bagi ke dalam 2 tabung reaksi:
Tabung I Tabung II
- Ditambahkan 3 tetes K2CrO7 - Diamati perubahan yang terjadi
- Ditambahkan 3 tetes K2CrO7 - Dipanaskan
- Diamati perubahan yang terjadi
IV. Prosedur Kerja Secara kuantitas A. Tuak Asli
1. Ambil 5 ml tuak asli lalu masukkan ke dalam tabung reaksi. 2. Encerkan dengan aquadest ke labu ukur sampai 100 ml.
3. Setelah diencerkan diambil 1 ml masukkan ke tabung reaksi ditambah 5 ml K2CrO7 dipanaskan sampai suhu 80°C selama 15' kemudian didinginkan sampai dingin.
4. Masukkan sampel ke dalam tabung Elmeyer ditambah Ferosin 3 tetes sebagai indikator.
B. Nira Campur Raru
1. Ambil 5 ml tuak asli lalu masukkan ke dalam tabung reaksi. 2. Encerkan dengan aquadest ke labu ukur sampai 100 ml.
3. Setelah diencerkan diambil 1 ml masukkan ke tabung reaksi ditambah 5 ml K2CrO7 dipanaskan sampai suhu 80°C selama 15' kemudian didinginkan sampai dingin.
4. Masukkan sampel ke dalam tabung Elmeyer ditambah Ferosin 3 tetes sebagai indikator.
5. Masukkan Aluminium Ferosulfat sebanyak 7,5 ml ke dalam tabung Buret sampai setinggi pandangan mata, sampai berubah warna.
C. Nira Asli
1. Ambil 5 ml tuak asli lalu masukkan ke dalam tabung reaksi. 2. Encerkan dengan aquadest ke labu ukur sampai 100 ml.
3. Setelah diencerkan diambil 1 ml masukkan ke tabung reaksi ditambah 5 ml K2CrO7 dipanaskan sampai suhu 80°C selama 15' kemudian didinginkan sampai dingin.
4. Masukkan sampel ke dalam tabung Elmeyer ditambah Ferosin 3 tetes sebagai indikator.
V. Tuak yang dipasarkan di masyarakat
1. Ambil 5 ml tuak asli lalu masukkan ke dalam tabung reaksi. 2. Encerkan dengan aquadest ke labu ukur sampai 100 ml.
3. Setelah diencerkan diambil 1 ml masukkan ke tabung reaksi ditambah 5 ml K2CrO7 dipanaskan sampai suhu 80°C selama 15' kemudian didinginkan sampai dingin.
4. Masukkan sampel ke dalam tabung Elmeyer ditambah Ferosin 3 tetes sebagai indikator.
5. Masukkan Aluminium Ferosulfat sebanyak 3,7 ml ke dalam tabung Buret sampai setinggi pandangan mata, sampai berubah warna.
Demikianlah hal ini dilakukan selama 3 hari berturut-turut untuk mengetahui konsentrasi etanol di dalam nira aren asli, nira ditambah raru, tuak asli dan tuak yang dipasarkan di masyarakat.
Data : Volume Titrasi Larutan (NH4)2 Fe (SO4) 0,393 N
No. Sampel Hari I Hari II Hari III
1. Tuak Asli 2,3 ml 3,1 ml 3,9 ml 2. Nira ditambah Raru 7,5 ml 7,7 ml 8,0 ml 3. Nira Asli 2,4 ml 3,5 ml 4,5 ml 4. Tuak di Pasarkan 3,7 ml 4,5 ml 4,9 ml
Data : Kadar Etanol Persen (%)
No. Sampel Hari I Hari II Hari III
1. Tuak Asli 12,07% 16,97% 21,88%
2. Nira ditambah Raru 43,97% 45,20% 47,04%
3. Nira Asli 12,68% 19,43% 25,56%
4. Tuak di Pasarkan 20,66% 25,56% 28,02%
Keterangan : Kadar etanol yang dikandung masing-masing sampel tuak setelah diamati sampai beberapa hari.
LAMPIRAN 2:
1. BOBOT GINJAL MENCIT.
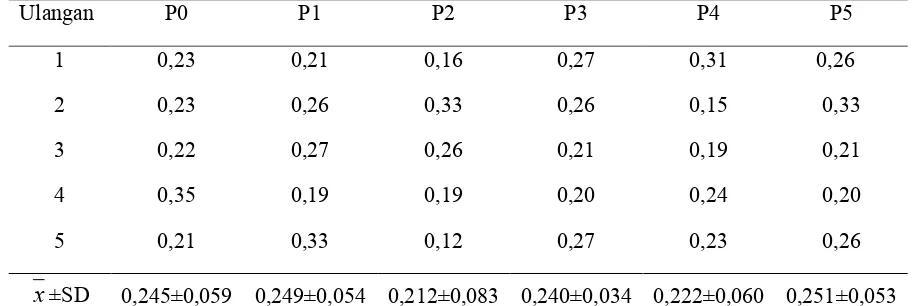
Tabel 1.: Hasil Pengukuran Bobot Ginjal Mencit Jantan Dewasa (g)
Ulangan P0 P1 P2 P3 P4 P5
x±SD 0,245±0,059 0,249±0,054 0,212±0,083 0,240±0,034 0,222±0,060 0,251±0,053
Tests of Normality
Berat_ginjal Statistic df Sig. Statistic df Sig.
Kolmogorov-Smirnova Shapiro-Wilk
This is a lower bound of the true significance. *.
Lilliefors Significance Correction a.
Test of Homogeneity of Variance
.792 5 24 .566
.491 5 24 .780
.491 5 19.531 .779
.763 5 24 .586
Based on Mean Based on Median Based on Median and with adjusted df
Based on trimmed mean Berat_ginjal
Levene
Statistic df1 df2 Sig.
NPar Tests
Bobot-Ginjal
Kruskal-Wallis Test
Berat_ginjal N Mean Rank
Test Statistics a,b
2. PENILAIAN PERUBAHAN TUBULUS PROKSIMAL (SEL GINJAL YANG MENGALAMI NEKROTIK).
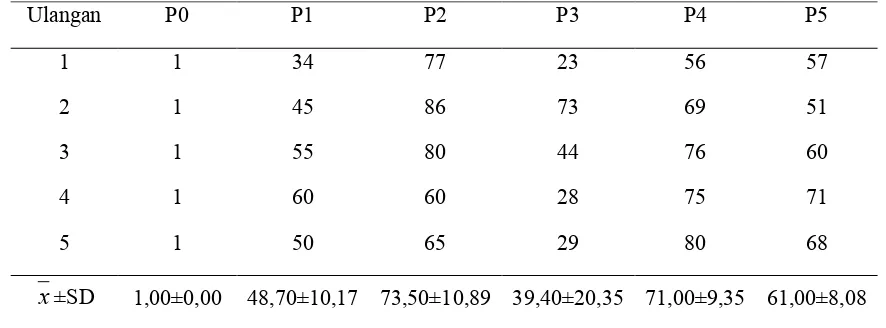
Tabel 2.: Hasil pengamatan sel ginjal yang mengalami nekrosis (%)
Ulangan P0 P1 P2 P3 P4 P5
x±SD 1,00±0,00 48,70±10,17 73,50±10,89 39,40±20,35 71,00±9,35 61,00±8,08
Tests of Normalityb
Nekrosis Statistic df Sig. Statistic df Sig.
Kolmogorov-Smirnova Shapiro-Wilk
This is a lower bound of the true significance. *.
Lilliefors Significance Correction a.
Nekrosis is constant when Kelompok = P0. It has been omitted. b.
Test of Homogeneity of Variancea
1.547 4 20 .227 Based on Median and with adjusted df
Based on trimmed mean Nekrosis
Levene
Statistic df1 df2 Sig.
Nekrosis is constant when Kelompok = P0. It has been omitted. a.
Oneway
ANOVA
Nekrosis
18238.167 5 3647.633 27.905 .000
3137.200 24 130.717
Post Hoc Tests
Multiple Comparisons Dependent Variable: Nekrosis
Bonferroni
-47.800* 7.231 .000 -71.36 -24.24
-72.600* 7.231 .000 -96.16 -49.04
-38.400* 7.231 .000 -61.96 -14.84
-70.200* 7.231 .000 -93.76 -46.64
-60.400* 7.231 .000 -83.96 -36.84
47.800* 7.231 .000 24.24 71.36
-24.800* 7.231 .033 -48.36 -1.24
9.400 7.231 1.000 -14.16 32.96
-22.400 7.231 .074 -45.96 1.16
-12.600 7.231 1.000 -36.16 10.96
72.600* 7.231 .000 49.04 96.16
24.800* 7.231 .033 1.24 48.36
34.200* 7.231 .001 10.64 57.76
2.400 7.231 1.000 -21.16 25.96
12.200 7.231 1.000 -11.36 35.76
38.400* 7.231 .000 14.84 61.96
-9.400 7.231 1.000 -32.96 14.16
-34.200* 7.231 .001 -57.76 -10.64
-31.800* 7.231 .003 -55.36 -8.24
-22.000 7.231 .084 -45.56 1.56
70.200* 7.231 .000 46.64 93.76
22.400 7.231 .074 -1.16 45.96
-2.400 7.231 1.000 -25.96 21.16
31.800* 7.231 .003 8.24 55.36
9.800 7.231 1.000 -13.76 33.36
60.400* 7.231 .000 36.84 83.96
12.600 7.231 1.000 -10.96 36.16
-12.200 7.231 1.000 -35.76 11.36
22.000 7.231 .084 -1.56 45.56
-9.800 7.231 1.000 -33.36 13.76
(J) Kelompok
(I-J) Std. Error Sig. Lower Bound95% Confidence IntervalUpper Bound
LAMPIRAN 5: SINGKATAN.
BAC : Blood Alcohol Concentration
Ca++ : Kalsium
Cl- : Klorida
Cu,Zn-SOD : Copper, Zinc-Superoxide Dismutase
DDW : Double Distsch Webster
DL : Resemik
DNA : Deoxi Nucleic Acid
Fe(NH4)2 : Aluminium Ferosulfat
FMIPA : Fakultas Matematika Ilmu Pengetahuan Alam PUFAs : Poly-unsaturated fatty acid s
GFR : Glomerular Filtration Rate
GSH-PX : Glutation Peroksida
GSH-R : Glutation Reduktase
HCO3- : Bikarbonat
H-E : Hematoksilin- Eosin
HOCl : Asam Hipoklorus
HPO4= : Fosfat
H2O2 : Hidrogen Peroksida
KBM : Kimia Bahan Makanan
K+ : Kalium
LDL : Low Density Lipoprotein
LO- : Radikal Alkoxyl
LO-2 : Radikal Peroksil
Mg++ : Magnesium
NaOH : Natrium Hidroxide
Na+ : Natrium
NAPQI : N-Acetyl-P-Benzoquinone Imine
NO- : Nitrit Oksida
NTA (ATN) : Nekrosis Tubular Akut
ONOO- : Peroksinitrit
O2- : Anion Superoksida
RAL : Rancangan Acak Lengkap
RBF : Renal Blood Flow
RPF : Rernal Plasma Flow
ROS : Reactive Oxygen Species
R-S : Radikal Thiyl
SOD : Superdioksida Dismutase
USU : Universitas Sumatera Utara
3O2 : Triplet
LAMPIRAN 6: GAMBAR-GAMBAR.
1. Gambar Pohon Aren.
Gambar 6.1.1. Pohon Aren yang menghasilkan Air Nira.
Gambar 6.1.4. Bunga Pohon Aren yang menjadi Bakal Penghasil Air Nira.
2. Gambar-gambar Pada Saat Penelitian dan Pembuatan Preparat.
Gambar 6.2.1. Pemberian Perlakuan Kepada Mencit.
Gambar 6.2.3. Pelaksanaan Dislokasi Leher dan Pembedahan Mencit
Gambar 6.2.6. Isolasi Ginjal Kelompok 1 (P0).
Gambar 6.2.7. Isolasi Ginjal Kelompok 2 (P1).
Gambar 6.2.8. Isolasi Ginjal Kelompok 3 (P2).
Gambar 6.2.10. Isolasi Ginjal Kelompok 5 (P4).
Gambar 6.2.13. Lemari Pengatur Suhu Tempat Pemanasan parafin.
Gambar 6.2.14. Penanaman Ginjal pada Blok Parafin.
Gambar 6.2.16. Pengirisan Blok Parafin pada Mikritom.
Gambar 6.2.19. Preparat Kelompok 2 (P1).
Gambar 6.2.20. Preparat Kelompok 3 (P2).
Gambar 6.2.22. Preparat Kelompok 5 (P4).